固体在平衡常数中为什么是1?该是一个常数吧,
 yaoyao领先2022-10-04 11:39:543条回答
yaoyao领先2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 edisonbubu 共回答了16个问题
edisonbubu 共回答了16个问题 |采纳率87.5%- 理论上讲固体和纯液体都应该有自己的物质的量浓度的,只不过每个都是定值(通常不是1),在平衡常数运算中因为浓度可以视为没有改变,所以通常不必要考虑.例如纯水的物质的量浓度是可以计算的一样
C(H2O)=〔1000g/18(g/mol)〕/1L - 1年前
 惊哲 共回答了560个问题
惊哲 共回答了560个问题 |采纳率- 楼主的理解正确。物质是通过浓度来影响平衡的,只能说固体的“浓度”基本不变,而不能当作1.
- 1年前
 lixiaojie226 共回答了41个问题
lixiaojie226 共回答了41个问题 |采纳率- 你可以这样想,固体单位体积内的物质的量是一定的,如果1体积中有1摩尔的物质,则物质的量浓度就是1,反应了0.5摩尔,体积就变成了0.5体积,物质的量浓度没变,所以化学平衡常数无法计算
- 1年前
相关推荐
- 晶体都是固体吗 NH3 F2 NF3 之中有没有分子晶体
 ssg46481年前1
ssg46481年前1 -
 挺华盟主 共回答了17个问题
挺华盟主 共回答了17个问题 |采纳率100%晶体都是固体吗
当然.
NH3 F2 NF3 之中有没有分子晶体?
如果深冷冷冻到结晶,他们都是分子晶体.1年前查看全部
- 向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
A. CO32-
B. Cl-
C. OH-
D. Cu2+ 望太白1年前1
望太白1年前1 -
 hgz1314 共回答了17个问题
hgz1314 共回答了17个问题 |采纳率88.2%解题思路:分别加入烧碱固体,溶液中OH-的浓度增大,与OH-反应的离子不能大量共存,以此解答该题.分别加入烧碱固体,溶液中OH-的浓度增大,因Cu2+与OH-反应,它的浓度减小,而A、B中离子浓度不变,故选D.
点评:
本题考点: 离子反应发生的条件.
考点点评: 本题考查离子的性质,侧重于元素化合物知识的综合考查,难度不大,注意把握常见与OH-反应的离子的性质以及反应类型的判断.1年前查看全部
- 1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为
1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为C和D的混合溶液,则A、B、C、D的化学式分别是:
2. 将一定质量的镁铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaoH溶液的体
积关系如图:
求A点为多少?具体的方程式和式子)
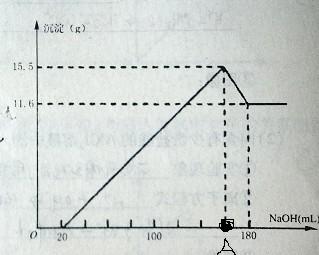
图上有个地方错了。A点的地方,沉淀是19.4... 5513600011年前1
5513600011年前1 -
 alexissui 共回答了19个问题
alexissui 共回答了19个问题 |采纳率94.7%赤铁矿被还原生成铁单质,A是Fe.Fe在纯氧中燃烧生成四氧化三铁B为Fe3O4.Fe3O4可视为FeO·Fe2O3所以C和D分别为FeSO4和Fe2(SO4)3.就是这个分析,真的没有计算方法.
2.当加入体积为20ml的时候把盐酸完全的中和了,在A点的时候生成Mg(OH)2和Al(OH)3,在180的时候Al(OH)3反应生成AlO2^-
Al(OH)3 + OH- = AlO2^- + 2H2O.得到Al(OH)3的质量为15.5 - 11.6 = 3.9g 氢氧化铝的物质的量为3.9/78 = 0.05mol,消耗氢氧根为0.05mol
11.6为氢氧化镁的质量Mg(OH)2,物质的量为11.6/58 = 0.2mol,则消耗氢氧根的量为0.4mol
共消耗氢氧化钠0.45mol.体积为0.45/5 x 1000 = 90ml
加上一开始中和盐酸的20ml,则在A点的体积为90+20 = 110ml
不够详细,很多都是文字,请见谅.
有问题欢迎追问.
希望我的回答能够对你有所帮助1年前查看全部
- 我一直搞不清楚吸水的是NaOH固体还是溶液还是均可 能与CO2反应的是NaOH固体还是溶液还是均可?
我一直搞不清楚吸水的是NaOH固体还是溶液还是均可 能与CO2反应的是NaOH固体还是溶液还是均可?
还有做吸水剂的是NaOH溶液还是固体 hdadqyp1年前2
hdadqyp1年前2 -
 余小宝的老娘 共回答了19个问题
余小宝的老娘 共回答了19个问题 |采纳率78.9%只有氢氧化钠固体才吸水.
只有氢氧化钠溶液才能与二氧化碳反应.1年前查看全部
- 请问用NaOH固体吸水后会风化吗?
请问用NaOH固体吸水后会风化吗?
如果会那吸水不是不完全了吗?
NaOH形成结晶体之后的确最后会形成Na2CO3,但是在NaOH形成结晶体期间,会不会有一部分H2O重新回到空气中?所以我要问的是,如果会,那么吸水就不完全了。 272班回帖1年前2
272班回帖1年前2 -
 andypjl 共回答了21个问题
andypjl 共回答了21个问题 |采纳率85.7%因为水不是以结晶的方式存在的,水是和NaOH形成溶液,只可以蒸发不能叫做风化,风化是指结晶水的失去,比如NaSO4.10H2O可以风化.1年前查看全部
- 为了加快固体溶解速率,常用热水溶解CuSO4,但会产生浑浊,原因是什么?如何得到澄清的CuSO4溶液?
 剑啸梅雪1年前2
剑啸梅雪1年前2 -
 lanytian 共回答了16个问题
lanytian 共回答了16个问题 |采纳率93.8%Cu离子在水中存在水解平衡,Cu离子+水=氢氧化铜+H离子,反应吸热.热水会导致平衡右移,促进水解,产生氢氧化铜沉淀,向溶液中添加H离子则可抑制水解,为了不引入杂质,应该加入稀硫酸1年前查看全部
- H2与O2混合气体26克充分反应所得再与NA2O2反应,是固体增加2克
H2与O2混合气体26克充分反应所得再与NA2O2反应,是固体增加2克
求原混合气体中H2与O2的质量 秋水封尘1年前2
秋水封尘1年前2 -
 九天冰海1 共回答了20个问题
九天冰海1 共回答了20个问题 |采纳率85%方程式:
2 Na2O2+2 H2O =4 NaOH +O2
用差量法算
设Na2O2物质的量是X,80*X-78*X=2
X=1
则水为1MOL
1:H2 10, O2 16
2:H2 2, O2 241年前查看全部
- 把26g含有SiO3的CaCO3固体在高温下加热至质量不在改变
把26g含有SiO3的CaCO3固体在高温下加热至质量不在改变
冷却后称重为17.2g.
(1)写出有关的化学反应方程式?
(2)求生成CO2的体积(标准状况)?
(3)求原混合物中所含SiO2的质量?
我的题目那里的SiO3打错了,应该是SiO2
不过1楼的高手没有被误导
可是SiO2在高温条件下不是可以跟CaCO3反应吗? 999hazt1年前1
999hazt1年前1 -
 Lin_HH 共回答了29个问题
Lin_HH 共回答了29个问题 |采纳率96.6%CaCO3=CaO+CO2 质量减少
100 44
X 26-17.2
(26-17.2)/1.97=4.47L
原混合物中碳酸钙x=20g
二氧化硅的质量26-20=6g
生成物CaO11.2g
sio2 6g1年前查看全部
- D是我们已经学过的四种常见物质,其中A是红色固体,D用于玻璃、造纸、纺织、洗涤剂的生产,A、B、C、D不是酸和碱,它们与
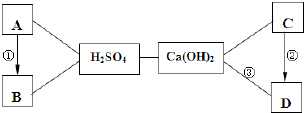
D是我们已经学过的四种常见物质,其中A是红色固体,D用于玻璃、造纸、纺织、洗涤剂的生产,A、B、C、D不是酸和碱,它们与稀H2SO4、Ca(OH)2之间的相互关系如图所示(“→”表示物质间的转化关系,“--”表示物质间可以相互反应),请回答下列问题:
(1)H2SO4与 Ca(OH)2反应的基本类型是.
(2)写出下列物质的化学式:B,C.
(3)写出下列反应的化学方程式:②,③.
(4)若①是一个置换反应,则反应的化学方程式是.
 yellowpage1年前1
yellowpage1年前1 -
 Loochoo 共回答了19个问题
Loochoo 共回答了19个问题 |采纳率94.7%(1)离子反应
(2)B:Fe C:CO2
(3)2. Na2O+CO2=Na2O3 3. Ca(OH)2+Na2CO3=2NaOH+CaCO3(沉淀)
(4)2Fe2O3+3C=4Fe+3CO21年前查看全部
- 2.某兴趣小组用氯酸钾和二氧化锰的化合物加热制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适
2.某兴趣小组用氯酸钾和二氧化锰的化合物加热制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.

(1)共制得氧气 g.
(2)计算生成氯化钾的质量. 在镜中飞翔1年前1
在镜中飞翔1年前1 -
 晓曦cc 共回答了13个问题
晓曦cc 共回答了13个问题 |采纳率100%1) 28.0-18.4=9.6g
2KClO3 = 2KCl + 3O2
149 96
x 9.6
x=14.9g1年前查看全部
- 有人猜想:浸没在液体中的固体所受的浮力可能跟固体的形状有关.请你为检验这个猜想设计一个实验.说出实验所需的器材和实验步骤
有人猜想:浸没在液体中的固体所受的浮力可能跟固体的形状有关.请你为检验这个猜想设计一个实验.说出实验所需的器材和实验步骤.(提示:借助图说明也可以)
(1)实验器材:
(2)实验步骤: lvhenghai2002321年前1
lvhenghai2002321年前1 -
 clx4 共回答了16个问题
clx4 共回答了16个问题 |采纳率81.3%解题思路:探究浸没在液体中的固态所受浮力是否与固体形状有关,应控制液体密度与固体体积不变而改变物体的形状进行实验.答:(1)实验器材:烧杯、弹簧测力计、橡皮泥、细线、水.
(2)实验步骤:
a、用细线拴上橡皮泥,悬挂在弹簧测力计下端,使橡皮泥缓慢地完全浸没在水中,读出弹簧测力计示数F1;
b、改变橡皮泥的形状,重复上述步骤,测出弹簧测力计示数F2;
c、比较F1与F2的大小,如果F1=F2,说明浮力大小与物体形状无关,如果F1≠F2,说明浮力大小与形状有关.点评:
本题考点: 探究浮力大小的实验.
考点点评: 根据实验目的、应用控制变量法设计实验即可正确解题.1年前查看全部
- 固体材料存在哪些结构转变类型?受哪些因素的影响?举例说明.
 feichangww1年前1
feichangww1年前1 -
 如果爱我就别走 共回答了28个问题
如果爱我就别走 共回答了28个问题 |采纳率92.9%主要是受温度的影响比较大,热胀冷缩.比如:桥梁,受冬夏温度差别的影响,要留有一定的伸缩逢.1年前查看全部
- 将21.8g氯酸钾和二氧化锰的混合物,装入大试管加热到不再有气体产生.剩余固体质量为12.2g.
将21.8g氯酸钾和二氧化锰的混合物,装入大试管加热到不再有气体产生.剩余固体质量为12.2g.
1.生成氧气多少克?2.氯化钾多少克?3.二氧化锰多少克? rieu1年前3
rieu1年前3 -
 hhb127 共回答了18个问题
hhb127 共回答了18个问题 |采纳率88.9%根据题意可知生成氧气的质量为:21.8g-12.2g=9.6g
设生成氯化钾质量为x
2KClO3==MnO2==2KCl+3O2↑
149 96
x 9.6g
149/x=96/9.6g
x=14.9g
说明你的数据有问题,因为生成氯化钾的质量比反应后混合物的总质量都多,1年前查看全部
- 某化验员分析可知,Cu (NO 3)2,Fe (NO 3)3,Fe (NO 3)2的固体混合物中金属元素的质量分数的总和
某化验员分析可知,Cu (NO 3)2,Fe (NO 3)3,Fe (NO 3)2的固体混合物中金属元素的质量分数的总和为百分之69,则混合物中氮元素的质量分数为多少?
 冒充一回老大1年前1
冒充一回老大1年前1 -
 月夜枯禅 共回答了13个问题
月夜枯禅 共回答了13个问题 |采纳率69.2%金属元素质量分数69%
则硝酸根质量分数31%
硝酸根中N元素的质量分数为(14/62)
所以混合物中氮元素的质量分数为31%*(14/62)=7%1年前查看全部
- 请问材料或者是固体在经过化学反应以后,对于材料或者是固体本身的力学性质发生怎样的变化?
请问材料或者是固体在经过化学反应以后,对于材料或者是固体本身的力学性质发生怎样的变化?
就是说化学反应对于力学性质的改变
应该看哪方面的参考文献呢?
请问是高分子化学的哪一章呢? pingzy1年前2
pingzy1年前2 -
 rergregf 共回答了18个问题
rergregf 共回答了18个问题 |采纳率83.3%我化学本科毕业,
你应该看高分子化学,里边有一章介绍这方面的内容.
还有材料化学、分子内部结构、物理化学等这方面的书1年前查看全部
- 化学题下列操作的后果 把大块固体垂直投入试管 给烧杯直接加热 同一支试管取不同药液 用天平
化学题下列操作的后果 把大块固体垂直投入试管 给烧杯直接加热 同一支试管取不同药液 用天平
化学题下列操作的后果
把大块固体垂直投入试管
给烧杯直接加热
同一支试管取不同药液
用天平称物时右物左码
用力洗刷试管
实验剩余的药物放回原瓶
滴管使用后平放货或倒放 eeig1年前2
eeig1年前2 -
 chengdanming 共回答了23个问题
chengdanming 共回答了23个问题 |采纳率91.3%把大块固体垂直投入试管:会造成试管底部破裂
给烧杯直接加热:使烧杯受热不均,造成破裂
同一支试管取不同药液:会造成试液污染
用天平称物时右物左码:称量重量比真实值低
用力洗刷试管:会将试管底部戳破
实验剩余的药物放回原瓶:造成原瓶药品污染
滴管使用后平放货或倒放:可能造成滴管内药液倒流,腐蚀胶头1年前查看全部
- 固体硫酸亚铁铵结成块状失效了吗如何确认放置久了的固体硫酸亚铁铵的成分没有发生变化!
 黑客新手1年前3
黑客新手1年前3 -
 zh8445 共回答了18个问题
zh8445 共回答了18个问题 |采纳率100%硫酸亚铁铵较FeSO4晶体不易被空气中的O2氧化.应该只是吸水结块.
可以取少量固体溶解到水中,观察颜色即可.Fe2+是浅绿色的,相对Fe3+不易被观察.如果溶液有明显的黄色则说明已经有些被氧化成Fe3+了.1年前查看全部
- 将质量为m 克的二氧化碳与过量过氧化钠固体充分反应,试分析固体质量的变化(谢谢大家)
 pretencer1年前3
pretencer1年前3 -
 楠喃 共回答了16个问题
楠喃 共回答了16个问题 |采纳率87.5%(1)差量法
2Na2O2+2CO2=2Na2CO3+O2 固体的分子量增大了(212-156=56)
88 56
m x
x=56m/88=7m/11 固体质量增加7m/11
(2)一般的设xy来解
2Na2O2+2CO2=2Na2CO3+O2
156 88 212
x m y x=156m/88 y=212m/88
固体质量增加=212m/88-156m/88=7m/111年前查看全部
- 向等质量双氧水溶液中分别加入绿豆大小的氯化铁和硫酸铜固体,比较二者的催化能力,正确吗?
向等质量双氧水溶液中分别加入绿豆大小的氯化铁和硫酸铜固体,比较二者的催化能力,正确吗?
如果错了,错在哪里呢? lords52661年前1
lords52661年前1 -
 太平洋小宝 共回答了11个问题
太平洋小宝 共回答了11个问题 |采纳率100%错,影响反应速率的条件有反应物浓度,温度,压强,接触面大小等.控制变量法除变量外,其它条件必须相同,这里的变量是催化剂种类,所以必须保证双氧水的浓度相同,而不是质量相同.1年前查看全部
- 将Cu与CuO固体混合物粉末放入烧杯中,当加入100克稀硫酸时,CuO与H2SO4好完全反应,过滤后所得溶液的质量为10
将Cu与CuO固体混合物粉末放入烧杯中,当加入100克稀硫酸时,CuO与H2SO4好完全反应,过滤后所得溶液的质量为108克,(不考虑过滤过程中溶液质量的损失).请分析并计算
(1)反应后溶液增加的质量为参加反应▁▁▁的质量.
(2)稀硫酸中含H2SO4的质量分数. 逍遥灵子1年前1
逍遥灵子1年前1 -
 aiya3602 共回答了19个问题
aiya3602 共回答了19个问题 |采纳率89.5%(1)cuo
(2)9.8%
因为反应后的物质没有气体等会溢出的东西,故增加的即为cuo质量
因为刚好完全反应,故列出反应式即可求得h2so4有9.8g1年前查看全部
- 氢氧化钠固体变质方程式
 钱掉了你1年前1
钱掉了你1年前1 -
 dmin 共回答了10个问题
dmin 共回答了10个问题 |采纳率100%2NAOH+CO2=NA2CO3+H2O1年前查看全部
- 放置培养基斜面有没有特殊工具也就是用来放置试管,使液态培养基变成斜面固体培养基的工具.
 suiyuewusheng1年前4
suiyuewusheng1年前4 -
 勇往直前狼 共回答了19个问题
勇往直前狼 共回答了19个问题 |采纳率78.9%不需要,只要找到一个长的木板放在台面上,或者找一个台面,能靠东西的,把你灭了菌的试管摆靠上去,液体培养基能倾斜就ok了,它凝固后就可以用了1年前查看全部
- 弱酸HA,电离方程HA=H++a-,向溶液中加入适量NAA固体,平衡将?怎样移动?c(A-)和c(OH-)的变化?
 ltm36939131年前1
ltm36939131年前1 -
 手拉着手 共回答了20个问题
手拉着手 共回答了20个问题 |采纳率95%因为有电离平衡存在: HA =H+ + A-
加入NaA固体,NaA = Na+ + A- (完全电离) 增大了A-的浓度,平衡向左移动.根据勒夏特里原理,平衡移动只能减弱A-的增大,但不能改变A-增大的趋势,最终A-浓度变大.
而上述平衡左移结果造成H+的浓度减小, 而在水溶液中,C(H+) * C(OH-) =K(常数),因此,C(OH-)=K / C(H+)是增大的.1年前查看全部
- 用氢气还原8gCuO,将反应后的气体全部通入足量的浓硫酸,浓硫酸的质量增加了0.9g,则剩余的固体是什么?
用氢气还原8gCuO,将反应后的气体全部通入足量的浓硫酸,浓硫酸的质量增加了0.9g,则剩余的固体是什么?
额........只有Cu Raincho1年前1
Raincho1年前1 -
 吃了八分饱 共回答了25个问题
吃了八分饱 共回答了25个问题 |采纳率96%根据题目可得:浓硫酸增加的质量应该为H2还原CuO生成的水的质量,所以n(H2O)=0.9/18=0.05mol.因为n(CuO)=8/80=0.1mol,得n(CuO)>n(H2O),所以固体中含有Cu和CuO,且均为0.05mol1年前查看全部
- 有NaOH、NaHCO3和与其他物质都不反应、受热也不分解的杂志组成固体混合物17.11克
有NaOH、NaHCO3和与其他物质都不反应、受热也不分解的杂志组成固体混合物17.11克
有NaOH、NaHCO3和与其他物质都不反应、受热也不分解的杂质组成固体混合物17.11克,密闭加热至250度,充分反应
将产生气体通入过量澄清石灰水,的沉淀2.5克
冷却后全溶于水制成50毫升溶液
取出10毫升,与含HCl 1.825克的盐酸溶液25毫升 恰好中和
求原混合物中含杂质的质量分数? win2131年前1
win2131年前1 -
 ly_liuyou 共回答了14个问题
ly_liuyou 共回答了14个问题 |采纳率92.9%m(CaCO3)=2.5g
n(CaCO3)=2.5/100=0.025mol
由:Ca(OH)2+CO2=CaCO3+H2O
则:n(CO2)=0.025mol
由:2NaHCO3=Na2CO3+H2O+CO2
则:原有NaHCO3 0.05mol,为4.2g
加热后固体中含Na2CO3 0.025mol,为2.65g
m(HCl)=1.825g,n(HCl)=0.05mol
由:NaOH+HCl=NaCl+H2O;Na2CO3+2HCl=2NaCl+H2O+CO2,取出了原有的1/5,恰好中和
则:Na2CO3消耗的HCl为0.025/5*2=0.01mol,NaOH消耗的HCl为0.05-0.01=0.04mol
则:混合物中含有NaOH 0.04*5=0.2mol,为8g
所以:共有NaOH 8g,NaHCO3 4.2g 总计12.2g
含杂质:17.11-12.2=4.91g 杂质质量分数:4.91/17.11=28.697%1年前查看全部
- 氯化铵与氢氧化钠混合固体受热
 上来丢个图1年前1
上来丢个图1年前1 -
 懒人MM 共回答了30个问题
懒人MM 共回答了30个问题 |采纳率90%NH4Cl +NaOH ===加热==NaCl +H2O+NH3气体1年前查看全部
- 一定量的铁和氧化铁混合物投入250mL2mol/L的硝酸溶液中,反应完全后,无固体剩余,生成1.12LNO气体
一定量的铁和氧化铁混合物投入250mL2mol/L的硝酸溶液中,反应完全后,无固体剩余,生成1.12LNO气体
一定量的Fe和Fe2O3混合物投入250ml2mol/L的HNO3溶液中,反应完全后,无固体剩余,生成1.12LNO气体(标况),再向反应后溶液中加入1mol/L的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是?400ml
错了,答案是450ml怎么算的? ssx05461年前2
ssx05461年前2 -
 Doffy 共回答了13个问题
Doffy 共回答了13个问题 |采纳率84.6%生成1.12LNO气体(标况)——需要硝酸1.12/22.4=0.05摩尔,这是被还原的硝酸的物质的量;250ml2mol/L的HNO3溶液中含有硝酸=2*0.25=0.5摩尔,这是硝酸总的物质的量.
那么总的物质的量—被还原的物质的量=0.5-0.05=0.45摩尔,0.45摩尔消耗1mol/L的NaOH溶液体积=0.45/1=0.45升=450毫升.1年前查看全部
- 关于固体物理的 求达人为什么爱因斯坦与德拜比热理论在高温下都能给出与经典理论相同的结果,而在低温下则与经典结果不同?
 blanch1年前2
blanch1年前2 -
 小色一条 共回答了19个问题
小色一条 共回答了19个问题 |采纳率89.5%爱因斯坦理论采用恒定频率ω0,德拜模型使用色散关系ω=vk,其都是建立在波色-爱因斯坦分布的基础上,而经典理论是建立在玻尔兹曼分布的基础上的.
低温时,爱因斯坦理论的热熔计算值与温度成指数关系衰减;德拜模型的热熔与温度成三次方关系,两者与经典理论结果都不一样.高温时,爱因斯坦与德拜理论都趋近与玻尔兹曼分布,符合经典理论模型.1年前查看全部
- 1、做溶解固体药品实验时,需要用到的主要仪器是( )
1、做溶解固体药品实验时,需要用到的主要仪器是( )
A、量筒、烧杯 B、烧杯、玻璃棒 C、漏斗、滴管 D、量筒、试管
就一道题目,希望大家能够回答! hyouruisu91年前3
hyouruisu91年前3 -
 生還者 共回答了19个问题
生還者 共回答了19个问题 |采纳率89.5%B ,因为溶解固体药品的时候,是不需要测量液体的体积的,所以用不到量筒,漏斗与试管自然就更没用了,只有需要用烧杯来盛液体,玻璃棒来搅拌1年前查看全部
- 检验铁脱氧剂使用后固体中含有+3价铁元素的化学方法?
 760456901年前1
760456901年前1 -
 思顽 共回答了20个问题
思顽 共回答了20个问题 |采纳率80%溶解,加KSCN,变红,说明有三价铁离子1年前查看全部
- 铜有两种常见氧化物铜有两种常见的氧化物:CuO和Cu2O.某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成
铜有两种常见氧化物
铜有两种常见的氧化物:CuO和Cu2O.某学习小组取0.98gCu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示.另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示.则下列分析正确的是
[ ]
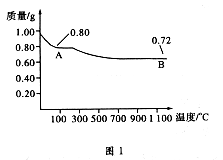

A.图1中产物A、B的化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26g水
C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是C
D.图1中,A到B过程中有0.01mol电子发生了转移
D liulei1237891年前1
liulei1237891年前1 -
 2006开往春天 共回答了16个问题
2006开往春天 共回答了16个问题 |采纳率93.8%0.80和0.72分别对应了CuO和Cu2O的分子量——80和144(一半,因为1摩尔俩铜),A对
加热时H全部以H2O形式离开,起始H共0.2mol,则水有0.1mol即0.18g,B错
CuO中,Cu与CuO质量比为4:5,趋近B线,C错
A至B被还原者仅为Cu,其还原量为0.005mol,每mol转移1mol电子(因为是1价Cu)故转移0.005mol电子,D错
综上选A
希望能帮助你1年前查看全部
- 气体固体液体三者的溶点沸点分别是指什么?
气体固体液体三者的溶点沸点分别是指什么?
甲烷的沸点为-10.熔点为-180.是指什么? 晶莹的心1年前5
晶莹的心1年前5 -
 lt1979 共回答了24个问题
lt1979 共回答了24个问题 |采纳率87.5%首先,气体固体液体的状态不一样,气体的温度是在它的沸点之上的,液体的温度是在它的熔点之上沸点之下的,固体的温度是在它的熔点之下的,所以当一个物体的温度在不同的范围内是有不同的状态的,而熔点沸点只不过是这个范围的界限罢了.(非晶体不存在溶点沸点)1年前查看全部
- 化学实验室中常用的白色固体是什么
化学实验室中常用的白色固体是什么
急
那和一种黑色粉末混合后产生一种白色固体
白色是什么
黑色是什么
白色固体又是什么 wennee1年前2
wennee1年前2 -
 胆小的剪子 共回答了17个问题
胆小的剪子 共回答了17个问题 |采纳率88.2%碳酸钙、氧化钙、氢氧化钙.1年前查看全部
- 溶液浓度的配置 有固体物质(CuSO4),可称量.要配置100ml浓度为0.2mol/L的硫酸铜溶液,怎样计算和配置?要
溶液浓度的配置
有固体物质(CuSO4),可称量.要配置100ml浓度为0.2mol/L的硫酸铜溶液,怎样计算和配置?要配置浓度为20%的硫酸铜溶液呢?
3.2g的计算公式是?20%浓度硫酸铜溶液 怎么配置?谁能再解释的清楚点? 快乐小喜12151年前4
快乐小喜12151年前4 -
 yang1219 共回答了24个问题
yang1219 共回答了24个问题 |采纳率87.5%先计算CuSO4的质量
0.1*0.2*160=3.2g
用天平称放在烧杯中,加适量水,用玻璃棒引流导入100ml容量瓶中
再用水清洗烧杯及玻璃棒,将清洗的液体也导入容量瓶中,在距刻度线1-2cm处,改用胶头滴管滴,直至凹液面一刻度线相平,盖住塞子,摇,贴标签.
20%的同理
打字真累.1年前查看全部
- 将含有杂质的固体氯化铜13.5g溶于水,加入足量的硝酸银,的28g沉淀,杂志是什么 A cacl2 B Alcl3 CK
将含有杂质的固体氯化铜13.5g溶于水,加入足量的硝酸银,的28g沉淀,杂志是什么 A cacl2 B Alcl3 CKcl D Fecl
 clxgz1231年前1
clxgz1231年前1 -
 怪怪笨笨 共回答了16个问题
怪怪笨笨 共回答了16个问题 |采纳率93.8%13.5g氯化铜与足量的硝酸银反应可以生成28.7克氯化银沉淀,
现在28g沉淀,小于13.5g
说明杂质中含氯的质量分数小于氯化铜,
所以选择氯化钾.
选择:C1年前查看全部
- 固体可以无限量在水中溶解吗在初三的物理书中出现一句话,“大多数固体物质都不能在水中无限量溶解”。这就是说明会有某种可以
 pwj0071年前5
pwj0071年前5 -
 巍巍蓝 共回答了24个问题
巍巍蓝 共回答了24个问题 |采纳率83.3%不可以,当溶解到一定程度达到饱和.1年前查看全部
- 由CaO和CaCO3组成的混合物mg在高温下充分煅烧,所得固体质量是原混合物质量的67%,则原混合物中CaO与CaCO3
由CaO和CaCO3组成的混合物mg在高温下充分煅烧,所得固体质量是原混合物质量的67%,则原混合物中CaO与CaCO3的质量比为多少?
 幸福貝宝1年前3
幸福貝宝1年前3 -
 飞翼hj 共回答了19个问题
飞翼hj 共回答了19个问题 |采纳率94.7%解题思路:根据题干提供的数据结合反应的化学方程式进行分析解答即可.高温煅烧碳酸钙和氧化钙的混合物,会生成二氧化碳,故减少的质量为二氧化碳,其数值为:mg×(1-67%)=0.33mg,
设碳酸钙的质量为x
CaCO3
高温
.
CaO+CO2↑
100 44
x 0.33mg
[100/x=
44
0.33mg] x=0.75mg
故氧化钙的质量为:mg-0.75mg=0.25mg
氧化钙与碳酸钙的质量比为:0.25mg:0.75mg=1:3
答:原混合物中氧化钙与碳酸钙的质量比为1:3.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题考查了根据化学方程式的计算,完成此题,可以依据题干提供的数据结合反应的化学方程式进行.1年前查看全部
- 碱金属的相关问题1.NaHCO3变成NA2CO3时需固体加热,但为什么需加NAOH?2.焰色反应“为什么铂丝每次检验前都
碱金属的相关问题
1.NaHCO3变成NA2CO3时需固体加热,但为什么需加NAOH?
2.焰色反应“为什么铂丝每次检验前都蘸盐酸?
过氧化钠的强氧化性:与H2S,NA2SO3,品红,反应时是不是因为生成了H2O2才表现的强氧化性?不是则是因为什么? 金鑫旺1年前4
金鑫旺1年前4 -
 oneshoe 共回答了16个问题
oneshoe 共回答了16个问题 |采纳率100%(1)NaHCO3是酸式盐,Na2CO3是正盐,使酸式盐变为正盐加碱加快反应(HCO3-=H^+ +CO3^2-;H^+ +OH^-=H2O)(2)盐酸易挥发还可以洗杂质(3)过氧化合物是有于氧显-1价才具有强氧化性1年前查看全部
- 用三种不同的方法鉴别蒸馏水和饱和食盐水.例:操作方法 取少量液体蒸干 结论 能留下固体颗粒的是饱和食盐
 将mm香烟1年前1
将mm香烟1年前1 -
 xinwen0412 共回答了17个问题
xinwen0412 共回答了17个问题 |采纳率100%1.滴加AgNo3,出现沉淀的是饱和盐溶液.2.降低温度到10摄氏度,出现固体的是饱和盐溶液.3.加盐搅拌,若能溶解则是水,不能则是饱和盐溶液.1年前查看全部
- 有关混合物中求质量分数有二氧化碳和一氧化碳的混合物共70g,通入足量的灼热氧化铜,充分反应后,固体质量减少32g,二氧化
有关混合物中求质量分数
有二氧化碳和一氧化碳的混合物共70g,通入足量的灼热氧化铜,充分反应后,固体质量减少32g,二氧化碳的质量分数为多少?
(不求最快,只求最好的) chenxin1281年前1
chenxin1281年前1 -
 hlw3607353017 共回答了15个问题
hlw3607353017 共回答了15个问题 |采纳率93.3%CuO+CO=Cu+CO2
减少的32克都是CuO中的氧,也就是32/16=2mol
根据反应式与CuO反应的CO也是2mol,所以CO的质量为28*2=56g
CO2含量为70-56=14g
质量分数为14/70=20%1年前查看全部
- 1:氯化铵固体加热再通过氢氧化钙出去氯化氢制氨气 为什么不可以?
1:氯化铵固体加热再通过氢氧化钙出去氯化氢制氨气 为什么不可以?
2:干燥氨气不用浓硫酸无水氯化钙硫酸铜 为什么?
3:收集氨气为防止倒吸,加入四氯化碳 为什么? 虎儿乖1年前0
虎儿乖1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 化学判断题中的白色固体和白色沉淀有区别吗?
 枫叶的形状1年前1
枫叶的形状1年前1 -
 huagen 共回答了12个问题
huagen 共回答了12个问题 |采纳率100%简单的说,白色固体包括了白色沉淀,白色沉淀是难溶于水的白色固体!1年前查看全部
- 现有25%的氯化钠溶液 5%的氯化钠溶液 氯化钠固体和水.请用上述四种中的两种配制10%的氯化钠溶液,将用量的质量最简整
现有25%的氯化钠溶液 5%的氯化钠溶液 氯化钠固体和水.请用上述四种中的两种配制10%的氯化钠溶液,将用量的质量最简整数比填入下表相应的位置.
25%氯化钠溶液 5%氯化钠溶液 氯化钠固体 水
示例 1 3
方案1
方案2
方案3 kenow1年前3
kenow1年前3 -
 mmlanmei 共回答了19个问题
mmlanmei 共回答了19个问题 |采纳率84.2%25%氯化钠溶液 5%氯化钠溶液 氯化钠固体 水
示例 1 3
方案1 1 9
方案2 10 10 1 19
方案3 4 1 151年前查看全部
- 常温下,固体分为晶体和非晶体.那么晶体与非晶体的最主要区别在哪里?
 hover1511年前5
hover1511年前5 -
 xx才 共回答了17个问题
xx才 共回答了17个问题 |采纳率94.1%晶体:具有固定熔沸点
非晶体:没有固定熔沸点1年前查看全部
- 为什么结构紧密的固体Si3N4不再受H2O和O2的侵浊?
 失意尽欢1年前2
失意尽欢1年前2 -
 追梦阳光 共回答了22个问题
追梦阳光 共回答了22个问题 |采纳率100%解析:SiCl4与NH3反应生成Si3N4的同时应该有HCl生成.由Si—N键的键能小于Si—O键的键能,Si3N4与H2O反应时,Si—N键向Si—O键转化,生成SiO2,同时应该有NH3生成.同样,Si3N4与O2反应时,产物应有SiO2生成,同时生成稳定的N2;而与MgO在一定条件下反应,生成结构紧密的SiO2覆盖在Si3N4固体表面,阻止了Si3N4继续受空气中的H2O和O2的侵蚀.1年前查看全部
- 下图是用绿色粉末A制取红色金属H的两种流程,其中白色固体Fe(Cao)是一种常见的建筑材料,固体乙是目前用途最广,产量最
下图是用绿色粉末A制取红色金属H的两种流程,其中白色固体Fe(Cao)是一种常见的建筑材料,固体乙是目前用途最广,产量最高的金属.
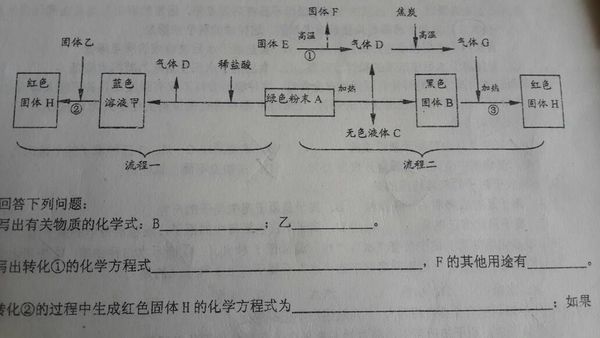
 想长翅膀的猪1年前2
想长翅膀的猪1年前2 -
 tttjuan 共回答了19个问题
tttjuan 共回答了19个问题 |采纳率100%1、固体乙是目前用途最广,产量最高的金属.可判断乙=Fe.
2、由绿色粉末A及红色固体H,可判断是碱式碳酸铜:A=Cu2(OH)2CO3
3、Cu2(OH)2CO3+盐酸可知:分解出二氧化碳气体,故知道D=CO2,蓝色液体是CuCl2
4、CuCl2+乙(Fe)置换出来纯铜Cu,故知道H=Cu.
5、白色固体(Cao)是一种常见的建筑材料可知,固体E=CaCO3,碳酸钙.
6、碳酸钙加热生成氧化钙和二氧化碳,故知道固体F=CaO、气体D=CO2.
7、CO2+焦炭=CO一氧化碳,煤气反应,故知道气体G=CO.
8、绿色粉末A碱式碳酸铜加热,生成CuO+H2O+气体D(CO2):Cu2(OH)2CO3CO+CuO+H2O+CO2,知道黑色固体B=CuO.1年前查看全部
- 举例说明溶液中进行的化学反应比固体之间发生的化学反应速率快
举例说明溶液中进行的化学反应比固体之间发生的化学反应速率快
要固体间反应的实物例子 VCD555DCV1年前1
VCD555DCV1年前1 -
 yantra 共回答了18个问题
yantra 共回答了18个问题 |采纳率77.8%例如:硫酸铜溶液跟氯化钡溶液反应就比它们固体之间反应速率快!1年前查看全部
- 晶体(包括离子,原子,分子,金属)发生物理变化(比如固体液化)是不是只克服分子间作用力?
 liaops-1021年前1
liaops-1021年前1 -
 guoting501 共回答了13个问题
guoting501 共回答了13个问题 |采纳率100%只有共价晶体分子才要克服分子间作用力
其他不存在分子结构,离子晶体克服离子键,金属克服金属键,原子晶体克服共价键1年前查看全部
- 某固体仅有一种元素组成,其密度为5g/cm3.该固体结构为:在棱长为1*10^-7cm的立方体中有20个原子,则此元素的
某固体仅有一种元素组成,其密度为5g/cm3.该固体结构为:在棱长为1*10^-7cm的立方体中有20个原子,则此元素的相对原子质量约为_____?
 xingfu3331年前2
xingfu3331年前2 -
 假名士2008 共回答了17个问题
假名士2008 共回答了17个问题 |采纳率88.2%首先你要求出cm3有多少原子数 1/1*10^-7cm 再乘以20 城出来在除以阿伏伽德罗常数 是摩尔数 再用5除以摩尔数就可以 估计不用考虑原子公共的问题 我没计算器 不算了1年前查看全部
大家在问
- 1You family is smaller than mine.(同义句)
- 2英语翻译1;christmas unbearable proves storeroom managed ballon2;
- 3根据提示,用often, always, sometimes, seldom, usually, never 填空。 N
- 4如果要制作一个地球仪,赤道半径定为15厘米,那么请算一算,极半径的长度应为多少?怎么做啊?
- 5已知a^2+2b+b^2-4b+5=0求2a^2+4b-3的值
- 6此处的that要么?
- 7a=20cm,b=11cm,B=30°
- 8这只鸟非常恨大海,就决定吧大海填满.的英文翻译
- 9我很想你 英语怎么说
- 1025乘13分之7.简便方法
- 112011年用水和家庭用水总和为5.8亿立方米家庭用水比用水的3倍还多0.6亿立方米用水和家庭用水各多少亿立方米
- 128 If he___to college,he __a lot more.
- 1316.进入初中,学习的科目增多了,难度加大了,老师讲课的方法也变了,学校、家长对同学的要求也高了,有的同学不适应这种变化
- 142012年10月25日23时33分,中国在西昌卫星发射中心用“长征三号丙”运载火箭,成功将第16颗北斗导航卫星发射升空并
- 15Sam saw me to go out (改错)
