滤液蒸发什么时候停止加热粗盐精制中,滤液蒸发时,当( )时,停止加热,利用余热将剩余水分蒸发.
 rynu491e_z0_b852022-10-04 11:39:541条回答
rynu491e_z0_b852022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 fotolo的爷爷 共回答了22个问题
fotolo的爷爷 共回答了22个问题 |采纳率90.9%- 有大量晶体析出时
- 1年前
相关推荐
- 下列实验操作不正确的是( ) A.用pH试纸(即广泛pH试纸)测得某盐酸的pH为1.2 B.过滤一次后滤液仍然浑浊,要
下列实验操作不正确的是( ) A.用pH试纸(即广泛pH试纸)测得某盐酸的pH为1.2 B.过滤一次后滤液仍然浑浊,要再次过滤1、2次 C.称量时,氢氧化钠固体必须要放在玻璃器皿或烧杯中称量 D.用量筒量取液体时,视线要与凹液面的最低处保持水平读数  sundaeyiyi1年前1
sundaeyiyi1年前1 -
 草莓男孩 共回答了20个问题
草莓男孩 共回答了20个问题 |采纳率75%A、广泛pH试纸测定的pH值为整数,1.2是小数,故A不正确;
B、过滤后,发现滤液仍有浑浊,应再次过滤,故B正确;
C、氢氧化钠具有强烈的腐蚀性,将氢氧化钠的固体必须要放在玻璃器皿或烧杯中称量,故C正确;
D、用量筒量取液体时,视线与量筒内液体凹液面的最低处保持水平,俯视或仰视都会使读数不准确,故D正确.
故选项为:A.1年前查看全部
- 将足量的铁粉投入硫酸铜和硫酸的混合溶液中,反应完毕后过滤,在滤液里含有的物质是( )
将足量的铁粉投入硫酸铜和硫酸的混合溶液中,反应完毕后过滤,在滤液里含有的物质是( )
A. Fe2(SO4)3
B. CuSO4
C. FeSO4
D. H2SO4 ananvox1年前8
ananvox1年前8 -
 boomen 共回答了23个问题
boomen 共回答了23个问题 |采纳率95.7%解题思路:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.A、铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,不能生成硫酸铁,故A错误;
B、铁粉足量,能与硫酸铜完全反应,故不会含有硫酸铜,故B错误;
C、铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,故C正确;
D、铁粉足量,能与硫酸完全反应,故不会含有硫酸,故D错误.
故选C.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,要充分考虑参加反应的物质的量对反应程度的影响.1年前查看全部
- 同问 将铁粉 碳粉 和少量氯化钠加入一定量的硫酸铜溶液中,充分反映后过滤,滤液中的溶质一定有---
 跳舞的琴键1年前1
跳舞的琴键1年前1 -
 ww3r 共回答了16个问题
ww3r 共回答了16个问题 |采纳率75%氯化钠、硫酸亚铁一定有.
只有一个反应 Fe+CuSO4==FeSO4+Cu
一定生成FeSO4,不知道CuSO4剩没剩,碳不溶,所以溶液一定有氯化钠、硫酸亚铁1年前查看全部
- 把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余.将溶液过滤,滤液中含有的溶质是( )
把含有少量氧化铜的铁粉加入稀盐酸中,加热充分反应后,发现铁粉有剩余.将溶液过滤,滤液中含有的溶质是( )
A. 稀盐酸
B. 氯化亚铁
C. 氯化铁
D. 氯化铜 wqx0231年前2
wqx0231年前2 -
 hlyyy1 共回答了11个问题
hlyyy1 共回答了11个问题 |采纳率100%解题思路:由于铁能与稀盐酸、氯化铜均能发生反应,所以当铁有剩余时,氧化铜与稀盐酸反应生成的氯化铜及稀盐酸均被完全反应.氧化铜可与稀盐酸反应生成氯化铜和水,根据金属的活动性顺序铁>氢>铜,可知铁与稀盐酸及氯化铜均能发生反应,因此,当铁有剩余时,溶液中的稀盐酸及氯化铜被完全反应,溶液中只含有氯化亚铁.所以过滤后的滤液中含有的溶质只有氯化亚铁;
故选B.点评:
本题考点: 金属的化学性质;酸的化学性质.
考点点评: 利用金属的活动性分析溶液中所发生的反应,在解答时要注意到铁在与酸或盐发生置换反应时,只能生成氯化亚铁.1年前查看全部
- 氯化铜与氧化镁的混合溶液中加入一定质量的铁粉,充分反应后过滤.在滤渣中加入稀硫酸有气泡产生,则滤液中一定含有的阳离子是什
氯化铜与氧化镁的混合溶液中加入一定质量的铁粉,充分反应后过滤.在滤渣中加入稀硫酸有气泡产生,则滤液中一定含有的阳离子是什么?
滤渣中一定含有的物质是什么? 让自己快乐些1年前4
让自己快乐些1年前4 -
 7221178 共回答了16个问题
7221178 共回答了16个问题 |采纳率93.8%因为加稀硫酸有气泡产生,所以铁粉一定过量,即铜全部被置换出来了
滤液中一定含有的阳离子有Mg2+,Fe2+
滤渣中一定含有Fe,Cu1年前查看全部
- 在Cu(NO3)2和AgNO3的混合溶液中加入一少量的铁粉,充分反应后过滤,在滤液中加入稀盐酸
在Cu(NO3)2和AgNO3的混合溶液中加入一少量的铁粉,充分反应后过滤,在滤液中加入稀盐酸
有不溶于稀硝酸的白色沉淀产生,则过滤后滤纸上有_______,产生白色沉淀的化学方程式为_____________________. jxdx661年前2
jxdx661年前2 -
 aprilandroy 共回答了17个问题
aprilandroy 共回答了17个问题 |采纳率82.4%Ag
AgNO3+HCl=HNO3+AgCl(沉淀)1年前查看全部
- 在用明矾净化水的过程中,发现过滤速度太慢,原因可能是?过滤后发现滤液仍浑浊,可能原因是?
 铁嘴铜牙金不换1年前4
铁嘴铜牙金不换1年前4 -
 没智商还谈智慧 共回答了11个问题
没智商还谈智慧 共回答了11个问题 |采纳率81.8%发现过滤速度太慢:(1)沉淀附着太多,需要更换滤纸
(2)明矾形成的絮状物没有完全沉淀
过滤后发现滤液仍浑浊 (1)滤纸破裂
(2)液面高于滤纸边缘
(3)仪器不干净1年前查看全部
- 做回收率时的对照品在什么位置加处理方法是:取供试品10g,精密称定,加稀乙醇加热回流30分钟,滤过,滤液用乙酸乙酯卒取2
做回收率时的对照品在什么位置加
处理方法是:取供试品10g,精密称定,加稀乙醇加热回流30分钟,滤过,滤液用乙酸乙酯卒取2次,每次20ml,收集乙酸乙酯液,水浴蒸干,残渣用乙酸乙酯溶解并转移置10ml量瓶中,稀释至刻度.请问,做回收率时的对照品应该在“加稀乙醇加热回流”时加入,还是应该在“转移置10ml量瓶中”加入, 红07011年前1
红07011年前1 -
 萧雨022 共回答了24个问题
萧雨022 共回答了24个问题 |采纳率83.3%回收率是反应待测物在样品分析过程中的损失的程度,所以要看是哪个反应了, 如果是测制乙酸乙酯那么就应该在加稀乙醇加热回流(因为这个时候反应完)1年前查看全部
- 绿叶中色素的提取和分离1、什么叫研钵?2、将研磨液迅速倒入玻璃漏斗(漏斗基部放一块单层尼龙布)中进行过滤.将滤液收集到试
绿叶中色素的提取和分离
1、什么叫研钵?
2、将研磨液迅速倒入玻璃漏斗(漏斗基部放一块单层尼龙布)中进行过滤.将滤液收集到试管中,及时用棉塞将试管口塞严.请问这一步的目的是什么?为什么要放一块单层尼龙布,而且还要及时用棉塞将试管口塞严?
3、制备滤纸条
将干燥的定性滤纸条剪成长与宽略小于试管长与宽的滤纸条,将滤纸条的一端剪去两角,放在试管下端,并在距这一端1厘米处用铅笔画一条细的横线.每一步的原因是什么?
4、画滤线细线
用毛笔吸管吸取少量滤液,沿铅笔线均匀地画出一条细线.待滤液干后,再画一两次.每一步的原因是什么? 02ironbird1年前1
02ironbird1年前1 -
 andywangjunkai 共回答了8个问题
andywangjunkai 共回答了8个问题 |采纳率100%我们高中是老师做好的,给我们看,然后到了大学才自己做的!
1、呵呵……真可爱!研钵就是用来研磨叶片的啊~还要加碳酸钙和二氧化硅研磨充分!你可以去百度上看看它长啥样的.
2、研磨液迅速倒入以及用棉塞是因为研磨要加入丙酮,丙酮很容易挥发,丙酮是用来溶解提取叶绿体中的色素,因为叶绿素能溶解在丙酮里.单层尼龙布是为了过滤充分吧,因为叶片的研磨有残渣.
3、“将干燥的定性滤纸条剪成长与宽略小于试管长与宽的滤纸条”是因为,你还要放到试管中,让它跑开,在后面的步骤里.滤纸条一端剪去两个角使之呈梯形,是为了防止滤液就沿两边往上跑,这样就分不开了.就象毛细管一样的那个原理.距离1cm是因为等下要放在分离液中跑,又不能让叶绿素浸到分离液中啊.用铅笔可以划得整齐,这样让每一种色素都有共同的起点,才分得开!
4、画得越细越多次,就越浓,越好跑,分得开,越清楚.
还有不懂的就看下原理:
分离要用的主要试剂是层析液.层析液是一种脂溶性很强的有机溶剂.叶绿体中的色素在层析液中的溶解度不同:溶解度高的随层析液在滤纸上扩散得快;溶解度低的随层析液在滤纸上扩散得慢.
层析分离叶绿体中的色素:将纸条画有滤液细线的一端置于烧杯中的层析液中,注意千万不要将滤液细线浸没在层析液中,否则会使色素溶解而导致试验失败.层析液是挥发性较强的有机溶剂,并且具有一定的毒性,所以在操作中要尽量用培养皿盖住烧杯口.
观察实验结果:最后滤纸条上将分离出四条色素带,颜色从上往下分别是橙黄色、黄色、蓝绿色和黄绿色,四种色素分别是胡萝卜素、叶黄素、叶绿素a和叶绿素b.1年前查看全部
- (2007•攀枝花)在Cu0和铁粉的混合物中加入一定量的稀H2S04,反应完全后滤出不溶物,再向滤液中加入一薄铁片,足够
(2007•攀枝花)在Cu0和铁粉的混合物中加入一定量的稀H2S04,反应完全后滤出不溶物,再向滤液中加入一薄铁片,足够时间后,铁片上无任何变化.据此,你认为下列结论不正确的是( )
A.滤出的不溶物中有铜,也可能有铁
B.如果滤出的不溶物中有铁,则一定有铜
C.滤出的不溶物中一定有铜,但不可能有铁
D.滤液中一定含有FeS04,不可能含有CuS04和H2S04 天香641年前1
天香641年前1 -
 kivifruit 共回答了16个问题
kivifruit 共回答了16个问题 |采纳率87.5%解题思路:在金属活动性顺序中,氢前的金属能与酸发生置换反应生成氢气,位置在前的金属能把位于其后的金属从其盐溶液中置换出来.氧化铜能与硫酸反应生成硫酸铜和水,铁可以与硫酸反应生成硫酸亚铁,能与硫酸铜反应生成硫酸亚铁和铜,向滤液中加入一薄铁片,铁片上无任何变化,说明滤液中无硫酸和硫酸铜,则滤出的固体中一定有铜,可能有铁,滤液中一定含有硫酸亚铁,观察选项,只有C不正确.
故选C.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.1年前查看全部
- ksp(BaSO4)=1*10^-10 将浓度均为0.1mol/L的BaCl2溶液与Na2SO4溶液等体积混合,滤液中钡
ksp(BaSO4)=1*10^-10 将浓度均为0.1mol/L的BaCl2溶液与Na2SO4溶液等体积混合,滤液中钡离子浓度是多少
为什么不用Ksp除以硫酸根离子浓度计算? 鱼鱼2151年前1
鱼鱼2151年前1 -
 燕_然 共回答了20个问题
燕_然 共回答了20个问题 |采纳率95%ksp(BaSO4)=c(Ba2+)c(SO42-)=[c(Ba2+)]2=1*10^-10
c(Ba2+)=1*10^-5mol/L1年前查看全部
- 经过明矾净化的水过滤后的滤液再加入新制漂白粉会有什么现象?
经过明矾净化的水过滤后的滤液再加入新制漂白粉会有什么现象?
在九年级物理课本的小实验里出现
请帮忙具体分析一下里面会是水解反应吗?该是什么现象? 鹰天下1年前2
鹰天下1年前2 -
 九点的馒头 共回答了23个问题
九点的馒头 共回答了23个问题 |采纳率91.3%不对...
明矾是十二水合硫酸钾铝KAl(SO4)2·12H2O
净水是铝离子在水中生成沉淀
因此溶液中剩余钾离子和硫酸根离子
漂白粉是次氯酸钙Ca(ClO)2
加入原溶液后
钙离子和硫酸根离子生成硫酸钙(微溶)
因此应生成白色沉淀1年前查看全部
- 重结晶提纯硫酸铜,蒸发滤液时,问什么加热不可过猛
 火元素师1年前1
火元素师1年前1 -
 爱原来是孤独 共回答了23个问题
爱原来是孤独 共回答了23个问题 |采纳率87%防止液体溅出,防止滤液蒸干1年前查看全部
- 取下某番茄叶片,经过研磨、过滤后,得到滤液,然后用纸层析法将其色素分离,得到如图所示的结果.对造成此结果原因的叙述,不正
取下某番茄叶片,经过研磨、过滤后,得到滤液,然后用纸层析法将其色素分离,得到如图所示的结果.对造成此结果原因的叙述,不正确的是( )
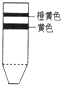 A. 此番茄可能是在长期缺镁的培养液中进行培养的
A. 此番茄可能是在长期缺镁的培养液中进行培养的
B. 此番茄在生长过程中可能受到了低温的影响
C. 研磨此叶片时可能忘记加入碳酸钙
D. 培养此番茄时可能严重缺水 LIA391年前3
LIA391年前3 -
 永恒龙渊 共回答了15个问题
永恒龙渊 共回答了15个问题 |采纳率93.3%解题思路:(1)分离色素的原理是根据色素在层析液中的溶解度不同,溶解度高的在滤纸条上扩散速度最快,滤纸条从上到下依次是:胡萝卜素(橙黄色)、叶黄素(黄色)、叶绿素a(蓝绿色)、叶绿素b(黄绿色).
(2)分析图形:得到两条色素带,从上到下依次是橙黄色的是胡萝卜素、黄色的是叶黄素,缺少叶绿素a和叶绿素b.A、缺镁元素会影响叶绿素的合成,导致缺乏叶绿素a(蓝绿色)、叶绿素b(黄绿色)两条色素带,A正确;
B、叶绿素和类胡萝卜素相比,稳定性更低,在低温下容易分解,B正确;
C、碳酸钙的作用是中和液泡中的有机酸,保护色素的作用,由于叶绿素不稳定,最容易遭到破坏,C正确;
D、缺水会影响各种色素,D错误.
故选:D.点评:
本题考点: 叶绿体色素的提取和分离实验.
考点点评: 本题结合题图,考查绿叶中色素的提取和分离实验,对于此类试题,需要考生注意的细节较多,如实验原理、实验材料的选取、实验试剂的选用、实验结果的分析、实验结论等,需要考生在平时的学习过程中注意积累.1年前查看全部
- 为什么水玻璃和阳离子交换树脂进行离子交换后滤液还是呈现碱性?原因出在哪?
 黑金岁月1年前1
黑金岁月1年前1 -
 ubin56749 共回答了22个问题
ubin56749 共回答了22个问题 |采纳率86.4%控制ph值,保持在PH=2~31年前查看全部
- 向硫酸铜 、硝酸银混合溶液中加入铁粉,充分反应后,滤渣是?滤液中含有的阳离子有?、、
 nnmhr1年前2
nnmhr1年前2 -
 你kk沉默 共回答了16个问题
你kk沉默 共回答了16个问题 |采纳率75%滤渣是置换出的铜和银;
滤液中的阳离子有二价铁离子、三价铁离子1年前查看全部
- 含杂质(杂质不溶于水)的硫酸钠15.5克与35.8克水配制成溶液.过滤后去滤液10克,加入20%的氯化钡溶液20.8克
含杂质(杂质不溶于水)的硫酸钠15.5克与35.8克水配制成溶液.过滤后去滤液10克,加入20%的氯化钡溶液20.8克
含杂质(杂质不溶于水)的硫酸钠15.5克与35.8克水配制成溶液.过滤后去滤液10克,加入20%的氯化钡溶液20.8克恰好完全反应.计算:(1)滤液的质量分数.(2)硫酸钠的纯度.
不要用摩尔,用初三水平做 夜叶1年前1
夜叶1年前1 -
 sleeplesser 共回答了15个问题
sleeplesser 共回答了15个问题 |采纳率100%Na2SO4+BaCl2===BaSO4↓+2NaCl
142 208
x 20.8g*20%
142/x=208/4.16g
x=2.84g
(1)滤液的质量分数2.84g/10g*100%=28.4%.
(2)硫酸钠的纯度.
15.5克样品中硫酸钠的质量为 35.8g*2.84g/(10g-2.84g)=14.2g
纯度 14.2g/15.5g*100%=91.6%1年前查看全部
- 不知mal是什么单位?示例:用干燥滤纸过滤,准确吸取25ml滤液于100ml锥形瓶中,用移液管加入5malc(1/2 H
不知mal是什么单位?
示例:
用干燥滤纸过滤,准确吸取25ml滤液于100ml锥形瓶中,用移液管加入5malc(1/2 H2SO4)=10mol/L硫酸酸化.准确吸取20ml酸化后的乳清于半微量定氮蒸馏器的内管中.调节蒸汽通入量,使每分钟蒸馏出3~5ml液体,直至馏出液达100ml为止.将馏出... 找工作的猫1年前9
找工作的猫1年前9 -
 利令猪昏 共回答了12个问题
利令猪昏 共回答了12个问题 |采纳率83.3%都错了..
是LZ你自己看错好嘛..印的不是mal 而是 mol...中文说法是摩尔..是物质的量 的单位1年前查看全部
- 有一硫酸和硝酸的混合溶液,从中取出10ml.加入足量氯化钡溶液,过滤、洗涤、干燥后得9.32g沉淀.滤液跟4mol/L的
有一硫酸和硝酸的混合溶液,从中取出10ml.加入足量氯化钡溶液,过滤、洗涤、干燥后得9.32g沉淀.滤液跟4mol/L的NaOH反映,用去35ml恰好中和
1.求混合溶液中硫酸和硝酸的物质的量浓度
2.另取10ml原溶液,加入3.2g铜共热,在STP下生成多少毫升气体? zhegea1年前3
zhegea1年前3 -
 起个名真难哪 共回答了16个问题
起个名真难哪 共回答了16个问题 |采纳率93.8%1.
H2SO4------BaSO4
1 233
x 9.32
解得 x=0.04mol
溶液中H+物质的量为 4*0.035 = 0.14mol
所以 HNO3的物质的量为 0.14-2*0.04 = 0.06mol
其物质的量浓度为 0.06/0.01 = 6mol/L
2.3Cu + 8H+ + 2NO3- === 3Cu2+ + 4H2O + 2NO↑
3*64g 8mol 2
3.2g 0.14 0.06
看出 Cu最少 按Cu计算
3Cu + 8H+ + 2NO3- === 3Cu2+ + 4H2O + 2NO↑
3*64g 2*22.4L
3.2g y
解得 y=746.6ml
如果还有疑问 百度HI找我 详谈1年前查看全部
- 氯化钠浓溶液中滴加硝酸银浓溶液,过滤后在滤液中滴加硝酸银溶液,如滤液中出现白色沉淀……
氯化钠浓溶液中滴加硝酸银浓溶液,过滤后在滤液中滴加硝酸银溶液,如滤液中出现白色沉淀……
说明氯化银在水中存在溶解平衡.
这个实验可以达到目的吗? 1eyn5o1年前1
1eyn5o1年前1 -
 season1 共回答了27个问题
season1 共回答了27个问题 |采纳率88.9%应该可以吧,好久没看化学了,但我刚试着在草稿纸上简要分析了一下,是可以达到目的的,再其他细节情况不影响的前提下.
首先原滴入硝酸银的氯化钠溶液,会产生一定量的氯化银.如果存在一定的溶解度(此处为假设),则会有一小部分溶解在溶液里,而另一大部分(如果真的存在溶液平衡,溶解的也为一小部分)的氯化银因为溶液度已经达到,会出现沉淀现象,即大规模氯化银沉淀,即是基本上接近于以氯化银沉淀的形势存在.
这时过滤,可以滤去的只是沉淀,则大部分氯化银沉淀被滤去.而如果剩下少部分的氯化银溶在溶液里的将会保留下来.此时过滤后的溶液里的溶质有硝酸钠,可能有氯化钠(因量的多少,反映是否充分完全而决定)以及剩余一小部分的氯化银.
当继续滴加硝酸银的时候,溶液中Ag离子的浓度会慢慢趋向于饱和.而AgNO3可溶,则饱和后多余的银离子就会以氯化银的形式析出,析出的白色沉淀则是因为溶液饱和,析出来的,而开始溶解进去的氯化银.(此时验证了假设)便证明了结论.
补充说明的是:这个只是关于质变的粗略的分析,如果涉及到量的变化是很复杂的,也就是说“氯化钠浓溶液中滴加硝酸银浓溶液,过滤后在滤液中滴加硝酸银溶液,如滤液中出现白色沉淀…说明氯化银在水中存在溶解平衡.”这样说还是不够严密的.会存在很多量问题影响验证结果的准确性.看问题的复杂程度要不要考虑到这个程度了.
也就是说,作为题目这么叙述的试验过程问你是否可以达到目的,你就可以做肯定回答了,如果是题目提出目的,让你设计试验,你却这么叙述试验过程,那就是不严密的了.1年前查看全部
- 高二化学选择题向某水溶液加过量稀盐酸后有白色沉淀生成,过滤后在滤液中通入足量H2S气体又有淡黄色沉淀生成,过滤后,向滤液
高二化学选择题
向某水溶液加过量稀盐酸后有白色沉淀生成,过滤后在滤液中通入足量H2S气体又有淡黄色沉淀生成,过滤后,向滤液中加入足量碳酸钠溶液又生成白色沉淀.则此溶液中含有( )
A.Ag +,Cu2+,Mg2+
B.Ag +,Fe3+,Ba2+
C.Ag +,Al3+,Mg2+
D.Ag +,Fe2+,Ca2+
写一下理由可以么?谢谢~~~好的会追加 静夜柔云1年前5
静夜柔云1年前5 -
 骑和尚的黑马 共回答了13个问题
骑和尚的黑马 共回答了13个问题 |采纳率92.3%加过量稀盐酸,仍有白色沉淀,高中阶段只有Ag+符合要求.
加H2S生成浅黄色沉淀,所以有硫单质生成,于是需要一种氧化性的金属离子,题中的Fe3+符合要求(Cu2+和H2S生成黑色硫化铜溶淀).
所以选择B1年前查看全部
- 滤纸边缘高于漏斗边缘,会不会影响滤液清澈度?原因?
滤纸边缘高于漏斗边缘,会不会影响滤液清澈度?原因?
RT
求速解 oyqyang1年前4
oyqyang1年前4 -
 Yvettechung 共回答了22个问题
Yvettechung 共回答了22个问题 |采纳率90.9%不会影响滤液清澈度,因为滤液低于滤纸边缘,只要经过滤纸而不是直接漏下去就没有影响,但是这属于错误操作1年前查看全部
- (2006•雅安)把一定量的铁粉放入硝酸银和硝酸铜的混合液中,充分反应后有少量金属析出,过滤后在滤液中滴加盐酸,无明显变
(2006•雅安)把一定量的铁粉放入硝酸银和硝酸铜的混合液中,充分反应后有少量金属析出,过滤后在滤液中滴加盐酸,无明显变化,则下列有关说法中肯定正确的是( )
A.析出的少量金属中一定有铜
B.析出的少量金属中一定有银
C.滤液中一定含有硝酸铜
D.滤液中可能含有硝酸银 果汁点点1年前1
果汁点点1年前1 -
 WEIB__ren_ren 共回答了13个问题
WEIB__ren_ren 共回答了13个问题 |采纳率92.3%解题思路:根据金属活动性顺序,上面金属的活动性:铁>铜>银:因为“把一定量的铁粉放入硝酸银和硝酸铜的混合液中”,所以铁会与硝酸银和硝酸铜分别反应生成银和铜;而硝酸银足够多的话,则铜消失,而银一定存在;又因为“在滤液中滴加盐酸,无明显变化”,则铁一定反应完,也一定无硝酸银,因为氯离子与银离子会形成沉淀;A、硝酸银足够多的话,铜与硝酸银反应,则铜消失,故A错误;
B、根据金属活动性顺序,银的金属活动性最差,所以析出的少量金属中一定有银,故B正确;
C、如果铁足量,滤液中不会含有硝酸铜,故C错误;
D、因为盐酸与硝酸银反应生成白色沉淀,而“在滤液中滴加盐酸,无明显变化”,则一定无硝酸银,故D错误.
故选B.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 利用金属活动性顺序,可知金属的活动性;学会利用它们处理和解释问题.1年前查看全部
- 向AgNO3溶液中加人一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液.关于该滤渣和滤
向AgNO3溶液中加人一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液.关于该滤渣和滤
①向滤渣中加入稀盐酸,一定有气泡产生.②向滤液中加入稀盐酸,一定有沉淀产生.③滤渣中一定含有Ag.④滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3.以上说法正确的个数为( )
A.0个B.l个C.2个D.3个
写详细过程 谢谢 化学真的晕si了 特别是这章! khang92601年前1
khang92601年前1 -
 麦悉 共回答了13个问题
麦悉 共回答了13个问题 |采纳率100%由题目得到滤渣和浅绿色的滤液,可以知道滤液中含有Fe2+,而向AgNO3溶液中加人一定质量的Al和Fe的混合粉末,发生的是置换反应,金属活泼性是Al>Fe,因此Al先和Ag发生置换反应,Al消耗完了,再是Fe和Ag发生置换反应,因为滤液呈绿色,所以,Al全部消耗,Fe可能是部分消耗,也可能是全部消耗变成Fe2+,
1,错,可能Fe粉已经没有了,滤渣都是Ag,可能不产生气泡
2、向滤液中加入盐酸,因为溶液里本来就有NO3-,所以他们形成硝酸将Fe2+变成Fe3+,但是不会产生沉淀.
3正确
4错误,因为一定是先有Al(NO3)3再有Fe(NO3)2,所以一定有Al(NO3)3
正确的答案选择B只有一个正确,1年前查看全部
- 海带提碘步骤中,为什么要在滤液中滴加稀硫酸?
 52三毛1年前3
52三毛1年前3 -
 平凡一世 共回答了11个问题
平凡一世 共回答了11个问题 |采纳率90.9%创造酸性环境.因为加稀硫酸时还要加过氧化氢,过氧化氢的作用是氧化碘离子,从而得到碘单质,而只有在酸性条件下这个反应才能发生.
H2O2 + 2I- + 2H+===I2 + H2O
两个碘后面的是离子符号,两个氢后面也是离子符号,百度不好写离子方程式,请原谅.1年前查看全部
- 将铜和氧化铜的固体混合物粉末11.2g放入烧杯中,当加入100g稀硫酸时,氧化铜和稀硫酸恰好完全反应,过滤得到滤液的质量
将铜和氧化铜的固体混合物粉末11.2g放入烧杯中,当加入100g稀硫酸时,氧化铜和稀硫酸恰好完全反应,过滤得到滤液的质量108g(不考虑过程中溶液的质量损失),则原混合物中铜元素的质量分数( )
A.95.6% B85.7% C80% D40%
 走在世界边缘1年前1
走在世界边缘1年前1 -
 -denny 共回答了14个问题
-denny 共回答了14个问题 |采纳率85.7%选B
根据配平的反应方程式
Cuo+H2SO4==CuSO4+ H2O
而铜不参见化学反应
则根据反应前后质量守恒可知,滤液增加的重量就是原来氧化铜的质量,就可以知道氧化铜的质量是8g,铜的质量就是3.2g,于是就可以算出来,原固体粉末质量分数就可以算出来.
这个在高中化学中应该不是什么特别棘手的问题,冒昧的问一句,你是不是化学上稍微有点问题啊?有时间的话可以多问问我.
望采纳.1年前查看全部
- 硫酸铜和硫酸铁中加入锌,充分反应.为什么滤液中一定有硫酸锌?
 xx11年前3
xx11年前3 -
 本方球门里 共回答了16个问题
本方球门里 共回答了16个问题 |采纳率100%由物质活泼性表可知 锌比铁活泼 可置换出铁 得到硫酸锌
硫酸又可以与 锌反应 生成硫酸锌
所以 一定有硫酸锌1年前查看全部
- 几道有关金属的题(化学)1.向硫酸铜,硫酸锌,硫酸混合溶液中加铁,则滤液中一定有什么?2.向氧化铜和铁中加入硫酸,充分反
几道有关金属的题(化学)
1.向硫酸铜,硫酸锌,硫酸混合溶液中加铁,则滤液中一定有什么?
2.向氧化铜和铁中加入硫酸,充分反应,过滤,向滤液中加铁,无变化,则滤液中一定有什么?
3.铁中含有少量氧化铜,加硫酸充分反应,氧化铜没有剩余,则滤液( )
A.一定有铜离子和亚铁离子
B.一定有铜离子,可能有亚铁离子
C.一定有亚铁离子,没有铜离子
D.一定有亚铁离子,没有铜离子
4.一定量铁中加入硝酸银和硝酸铜,则滤液中一定有什么? 天蓝093371年前2
天蓝093371年前2 -
 金鬼童 共回答了14个问题
金鬼童 共回答了14个问题 |采纳率85.7%1.ZnSO4、FeSO4.
ZnSO4不反应,Fe和硫酸或硫酸铜都生成FeSO4.
2.FeSO4.
滤液没反应说明CuO没参加反应.因此只有Fe+H2SO4=FeSO4+H2↑.
3.A
铁先反应,氧化铜后反应.已知氧化铜无剩余.则有Fe2+和Cu2+
4.Fe(NO3)2
因为铁置换出铜,同置换出银.无论反应进行到哪一步,肯定都有Fe(NO3)21年前查看全部
- 一道化学推断题把铁片和铜片同时放入盛有硝酸银溶液的试管中,充分反应后过滤,在滤纸上留下少量金属,并得到滤液.(1)在滤液
一道化学推断题
把铁片和铜片同时放入盛有硝酸银溶液的试管中,充分反应后过滤,在滤纸上留下少量金属,并得到滤液.
(1)在滤液里滴加盐酸:
①若有白色沉淀产生,则滤纸上一定含有的金属是( ),滤液中一定含有的金属离子是( )
②若无白色沉淀产生,则滤纸上一定含有的金属是( ),可能含有的金属是( );滤液中一定含有的金属离子是( ),可能含有的金属离子是( ).
(2)向从滤纸上得到的金属中滴加稀盐酸:
①若有气体产生,则滤纸上一定含有的金属是( ),滤液中一定含有的金属离子是( ).
②若无气体产生,则滤纸上一定含有的金属是( ),可能含有的金属是( );滤液中一定含有的金属离子是( ),可能含有的金属离子是( ). 天狼Lin1年前2
天狼Lin1年前2 -
 btgxd 共回答了16个问题
btgxd 共回答了16个问题 |采纳率87.5%(1)一定有银,因为有沉淀,所以有银离子,说明铜、铁的量不足以置换出全部的银,所以只有一部分置换出来的银成为了滤渣中一定有的金属!
溶液中一定有银离子,因为有白色沉淀,一定有铁、铜离子因为,铁、铜置换了银.
若无沉淀,说明银离子全部置换出来,一定有银.可能有铜和铁,因为铜和铁可能都过量.也可能恰好完全反应!溶液中一定有铁离子,因为铁的活动性比铜强,所以铁和溶液先反应,如果铁不够用,铜才会开始反应.所以不管怎么说,铁离子一定有.可能有铜离子啦.因为铁可能真的不够用.一定没银离子,因为没沉淀.
(2)一定有铁、铜、银,因为有气体,而铜、银活动性在氢后,所以一定有铁.上一问以说明了铁有剩余,铜一定等于没反应,银全部置换出的原因,所以,也一定有铜和银.
一定有银,因为铜铁可能恰好完全反应,或铜铁不足,可能有铜,因为可能铜过量.一定有的离子是铁,理由同第一问.可能有铜、银两种离子,因为铜银不足时,就会有银离子未被置换出来.1年前查看全部
- (1999•台州)1824年,法国青年学生巴拉尔德在把氯气通入海藻灰的浸出液提取碘的实验过程中,意外地发现在提取后的滤液
(1999•台州)1824年,法国青年学生巴拉尔德在把氯气通入海藻灰的浸出液提取碘的实验过程中,意外地发现在提取后的滤液中总沉着一层极少量深棕色液体,这引起了他的极大重视.进而深入研究证明这种深棕色液体就是单质(Br2).就这样,一种新的元素被发现了.已知海藻灰的主要成分为碘化钠(Nal),还含有少量的溴化钠(NaBr).根据上述材料及所学过的有关置换反应及金属活动性顺序知识推断:
(1)氯气与溴化钠溶液的反应的化学方程式______;
(2)非金属活动性强弱:氯______溴(填“>”、“=”或“<”) runescape1年前1
runescape1年前1 -
 可爱的你 共回答了14个问题
可爱的你 共回答了14个问题 |采纳率92.9%解题思路:根据题中信息结合学过的有关置换置换反应及金属活动性顺序知识进行分析.(1)根据题中信息可知,氯气与溴化钠溶液反应生成了溴单质和氯化钠,反应的化学方程式是Cl2 +2NaBr=2NaCl+Br2,故填:Cl2 +2NaBr=2NaCl+Br2.
(2)根据反应的化学方程式Cl2 +2NaBr=2NaCl+Br2可知,氯气置换出溴化钠中的溴,因此氯的活动性比溴强,故填:>.点评:
本题考点: 金属活动性顺序及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题难度不大,根据题中信息结合学过的化学知识是顺利解答此题的关键.1年前查看全部
- 45.把氧化铜和铁粉的混合物加到一定量的盐酸中,搅拌让他们充分反应后,过滤.取滤液
45.把氧化铜和铁粉的混合物加到一定量的盐酸中,搅拌让他们充分反应后,过滤.取滤液
加入少量铁粉,无任何现象.则下列判断正确的是……() (( )
A.滤渣中不含铜 B.滤液中含FeCl2和CuCl2
C.滤渣可能是铜和铁的混合物 D.滤液中含FeCl2和HCl
铁比铜活动性强,优先反应铁.Fe+2HCl=FeCl2+H2↑
还可能有 CuO+2HCl=H2O+CuCl2 Fe+CuCl2=FeCl2+Cu
加少量铁粉,无现象 没有HCl,CuCl2
所以 HCl用完,CuO还没反应,不含铜,选A
有什么错呢? davidwu3361年前4
davidwu3361年前4 -
 北狼008 共回答了19个问题
北狼008 共回答了19个问题 |采纳率94.7%铁比铜活动性强,优先反应铁.这句话错了,这题里面是氧化铜,不是铜,氧化铜比铁跟容易与盐酸反应.先有CuO+2HCl=H2O+CuCl2 ,由题意(滤液加入少量铁粉,无任何现象)盐酸反应完全了,则滤液中没有CuCl2和HCl,由于有滤渣则不可能是盐酸和两种物质同时反应完,铁就会有剩余的,会发生这个反应Fe+CuCl2=FeCl2+Cu,A就是错的,因此只能选C .1年前查看全部
- 在氯化铜、氯化铝溶液中加入过量的铁粉,充分反应后过滤,滤液里的溶质是( )
在氯化铜、氯化铝溶液中加入过量的铁粉,充分反应后过滤,滤液里的溶质是( )
A.氯化铜
B.氯化铝
C.氯化铁
D.氯化亚铁和氯化铝 cey001年前1
cey001年前1 -
 水果月亮 共回答了15个问题
水果月亮 共回答了15个问题 |采纳率100%解题思路:铜不如铁活泼,因此铁和氯化铜反应生成氯化亚铁和铜;
铝比铁活泼,铁不能和氯化铝反应.氯化铝不能和铁反应;
铁和氯化铜反应生成氯化亚铁和铜,因此在氯化铜、氯化铝溶液中加入过量的铁粉,充分反应后过滤,滤液里的溶质是氯化亚铁和氯化铝.
故选:D.点评:
本题考点: 金属的化学性质.
考点点评: 金属活动性顺序中,排在前面的金属,能够把排在后面的金属从它的盐溶液中置换出来,这里要注意是从它的盐溶液中置换出来,如果排在后面的金属形成的盐不溶于水,则不能发生置换反应,要注意理解.1年前查看全部
- (2012•峨眉山市二模)有一杯KNO3溶液,测得温度为80℃,将其置于冷水中冷却,有晶体析出,滤出晶体,测得滤液温度为
(2012•峨眉山市二模)有一杯KNO3溶液,测得温度为80℃,将其置于冷水中冷却,有晶体析出,滤出晶体,测得滤液温度为20℃.下列有关该叙述中,错误的是( )
A. 80℃时KNO3溶液,一定为饱和溶液
B. 20℃时的滤液,一定为饱和溶液
C. KNO3的溶解度随温度的降低而降低
D. 降温结晶过程中,溶剂质量不变,溶液质量、溶质质量、溶液质量分数减小 lzsdel1年前1
lzsdel1年前1 -
 hooly 共回答了15个问题
hooly 共回答了15个问题 |采纳率93.3%解题思路:温度为80℃时的KNO3溶液,将其置于冷水中冷却,有晶体析出,说明溶解度随温度降低而减小,有晶体析出的溶液一定是饱和溶液,降温结晶过程中,溶质质量减小,而溶剂质量不变.A、温度为80℃时的KNO3溶液,将其置于冷水中冷却,有晶体析出,并不能说明80℃时KNO3溶液,一定为饱和溶液,也可能是不饱和溶液,降温到高于20℃时达到饱和,然后再降温也会析出晶体.故A错误;
B、20℃时的溶液中有晶体析出,因此一定为饱和溶液,故说法正确;
C、温度为80℃时的KNO3溶液,将其置于冷水中冷却,有晶体析出,说明硝酸钾的溶解度随温度降低而降低.故说法正确;
D、降温结晶过程中,溶剂质量不变,而溶质质量减少,所以溶液质量、溶液中溶质质量分数也减小,故D说法正确;
故选A点评:
本题考点: 晶体和结晶的概念与现象;饱和溶液和不饱和溶液;固体溶解度的影响因素.
考点点评: 硝酸钾饱和溶液降温一定析出晶体,不饱和溶液降温也可能析出晶体.1年前查看全部
- 将提取的叶绿素色素滤液装入试管中,让一束白光穿过该滤液后经三棱镜对光进行色散,哪条光谱的颜色最明显
将提取的叶绿素色素滤液装入试管中,让一束白光穿过该滤液后经三棱镜对光进行色散,哪条光谱的颜色最明显
A. 绿光
B. 黄光
C. 红橙光、蓝紫光
D. 红光
 blueicehit1年前1
blueicehit1年前1 -
 魔术卡 共回答了20个问题
魔术卡 共回答了20个问题 |采纳率80%答案A
色素主要吸收的光呈暗带,吸收最少的光呈亮带,色素对绿光几乎不吸收,所以最明显是A选项.1年前查看全部
- 关于硫酸铜与氢氧化钠的化学反应向一定量的硫酸铜溶液中加入一定量的氢氧化钠溶液反应后充分过滤,填写下列问题:1.你认为滤液
关于硫酸铜与氢氧化钠的化学反应
向一定量的硫酸铜溶液中加入一定量的氢氧化钠溶液反应后充分过滤,填写下列问题:
1.你认为滤液中的溶质组成最多有几种组成情况
2.把你认为可能的组成情况用化学式写出来(有几种写几种) xin_yang1年前2
xin_yang1年前2 -
 云过青山1 共回答了25个问题
云过青山1 共回答了25个问题 |采纳率84%1.CuSO4 (NaOH少量)
2.Na2SO4 (恰好完全反应)
3.Na2SO4 NaOH (NaOH过量)
CuSO4+2NaOH=Cu(OH)2↓+Na2SO41年前查看全部
- (2013•昆都仑区一模)向含有硫酸镁、硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,完全反应后过滤,滤渣为A,滤液为B.将
(2013•昆都仑区一模)向含有硫酸镁、硫酸亚铁、硫酸铜的混合溶液中加入一些锌粉,完全反应后过滤,滤渣为A,滤液为B.将A放入稀硫酸中没有气泡冒出.则下列说法不正确的是( )
A.A中一定有铜、可能有铁
B.A中只有铜
C.B中一定有硫酸镁、硫酸锌、硫酸亚铁
D.B中可能有硫酸铜 绝望的重生1年前1
绝望的重生1年前1 -
 鼠你唯一 共回答了16个问题
鼠你唯一 共回答了16个问题 |采纳率93.8%解题思路:根据金属活动性顺序.在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;据此结合题意进行分析判断.根据金属活动顺序表可知,锌比铁活泼,铁比铜活泼,锌的活动性比镁弱,所以加入一定量的锌粉,锌不能与硫酸镁溶液反应;首先锌粉和硫酸铜溶液反应,置换出单质铜,如果锌粉足量可以继续与硫酸亚铁反应置换出铁.由题意可知,向滤出的固体A中滴加稀硫酸,没有气泡产生,说明固体中不含和稀硫酸反应的金属,金属不可能是铁和锌;
A、向滤出的固体A中滴加稀硫酸,没有气泡产生,说明固体中不含和稀硫酸反应的金属,金属A不可能是铁和锌,A中一定有铜,故选项说法错误;
B、向滤出的固体A中滴加稀硫酸,没有气泡产生,说明固体中不含和稀硫酸反应的金属,A中一定有铜,金属A不可能是铁和锌,故选项说法正确;
C、滤液B中一定有硫酸镁、生成的硫酸锌、硫酸亚铁,故选项说法正确;
D、由于滤渣A中只含有金属铜,当加入的锌量极少时,硫酸铜可能有剩余,B中可能有硫酸铜,故选项说法正确.
故选:A.点评:
本题考点: 金属的化学性质.
考点点评: 本题有一定难度,主要考查了学生对金属活动顺序表的运用,在解题时要注意对定量(如一定量、过量、少量等)概念的理解和掌握.1年前查看全部
- 将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,
将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,求
(1)产生O 2 的质量;
(2)原混合物中MnO 2 的质量. 余山雨夜1年前1
余山雨夜1年前1 -
 流浪乡下 共回答了20个问题
流浪乡下 共回答了20个问题 |采纳率90%设生成氧气的质量为x.
2KClO 3
Mn O 2
.
△ 2KCl+3O 2 ↑
149 96
100g×7.45% x
(1)
149
96 =
100g×7.45%
x ,x=4.8g
(2)MnO 2 的质量为:15.5g-(100g×7.45%+4.8g)=3.25g
答:(1)产生4.8g氧气;(2)二氧化锰的质量为3.25g.1年前查看全部
- 某溶液中加入过量盐酸产生沉淀,滤液中再通入硫化氢又产生沉淀,不符合此现象的组是:
某溶液中加入过量盐酸产生沉淀,滤液中再通入硫化氢又产生沉淀,不符合此现象的组是:
A.Hg2+、Al3+、Ba2+、Na+ B.Ag+、Fe3+、Mg2+、Cs+
C.Ag+、Cu2+、Rb+、NH4+ D.Fe2+、Ca2+、Li+、K+.
谁能说明一下为什么 jackie1211年前1
jackie1211年前1 -
 oyeqeoei 共回答了13个问题
oyeqeoei 共回答了13个问题 |采纳率100%加入过量盐酸产生沉淀
根据四个选项排除D
因为D中没有可以与氯离子产生沉淀的
在滤液中通入硫化氢产生沉淀
排除A
因为A中可与S离子产生沉淀的是Hg离子
而前面加入过量盐酸
说明Hg离子已经没有了
故答案为AD1年前查看全部
- 往某BaCL2溶液中加入密度为1.28/mL硫酸溶液,恰好完全反应后,过滤,测得滤液的质量与对BaCL2溶液的质量相等.
往某BaCL2溶液中加入密度为1.28/mL硫酸溶液,恰好完全反应后,过滤,测得滤液的质量与对BaCL2溶液的质量相等.则所加硫酸溶液的物质的量浓度是多少?
 丑小鸭工作室1年前1
丑小鸭工作室1年前1 -
 静以养心 共回答了20个问题
静以养心 共回答了20个问题 |采纳率85%BaCL2+H2SO4---baso4+hcl
陪平 用书上的例题就可解答
为什么要问?1年前查看全部
- .33.2g KClO3和MnO2的混合物,加热一段时间后,质量变为28.4g.冷却后加水搅拌,溶解完全后过滤,在滤液中
.33.2g KClO3和MnO2的混合物,加热一段时间后,质量变为28.4g.冷却后加水搅拌,溶解完全后过滤,在滤液中加硝酸银.滤纸上的不溶物与足量的浓盐酸反应,可生成0.1molCl2,求:
(1)KClO3的分解百分率.
(2)可生成AgCl沉淀的质量. zhutianren1年前1
zhutianren1年前1 -
 gujienanhai88 共回答了14个问题
gujienanhai88 共回答了14个问题 |采纳率78.6%(2) 氯酸钾分2KClO3=(Δ/MnO2)=2KCl+3O2↑
Δm=m(O2)=33.2-28.4=4.8g 则n(O2)=0.15mol 推得n(KCl)=0.15×2/3=0.1mol
加水后,滤液中溶解有生成的KCl,则生成AgCl沉淀物质的量与KCl相同.
n(AgCl)=0.1mol m(AgCl)=14.35g
(1) 2步骤中先加水滤出的沉淀是MnO2,方程式:MnO2+4HCl(浓)=(加热)=MnCl2+Cl2↑+2H2O
生成n(Cl2)=0.1mol,则n(MnO2)=0.1mol 推得m(MnO2)=8.7g
原混合物质量为33.2g,分解后剩余28.4g,
则总m(KClO3)=33.2-8.7g=24.5g,
分解的m(KClO3)=0.1×122.5=12.25g
则分解率(用质量算)=12.25/24.5=50%1年前查看全部
- 为什么粗盐提纯蒸发步骤中,不能用酒精灯加热至滤液蒸干,再停止加热.而是待蒸发皿中有较多晶体就停止...
为什么粗盐提纯蒸发步骤中,不能用酒精灯加热至滤液蒸干,再停止加热.而是待蒸发皿中有较多晶体就停止...
为什么粗盐提纯蒸发步骤中,不能用酒精灯加热至滤液蒸干,再停止加热.而是待蒸发皿中有较多晶体就停止加热?还有:醋酸和甲醇的化学式怎么写? 雨baby1年前1
雨baby1年前1 -
 千禧成狼d 共回答了20个问题
千禧成狼d 共回答了20个问题 |采纳率95%当彻底加热至滤液蒸干时,蒸发皿还是热的这样会容易破碎,如果加热至晶体出现时,再用蒸发皿的余热就可以是其中的水分蒸干.1年前查看全部
- 取12.5g含杂质的石灰石,加到100g稀盐酸中恰好完全反应,过滤得滤液105.6g,则该石灰石的纯度为
 天下第一5211年前2
天下第一5211年前2 -
 ze123456 共回答了14个问题
ze123456 共回答了14个问题 |采纳率100%百分之八十
溶液中增加的质量其实是CaO的质量 因为碳酸钙和盐酸反应 二氧化碳挥发 真正留下来的是氧化钙
105.6-100=5.6 也就是说氧化钙5.6g 也就是0.1mol
所以碳酸钙有0.1mol 也就是10g
10/12.5=80%1年前查看全部
- 将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,
将KClO 3 和MnO 2 的混合物15.5克,加热完全反应后,剩余固体加水溶解,过滤,洗涤不溶物,洗涤液与滤液合并,得100克溶质质量分数为7.45%的溶液,
求:
(1)产生O 2 的质量;
(2)原混合物中MnO 2 的质量。 swq5021年前0
swq5021年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有____
向铁粉和氧化铜的混合物中加入一定量的稀硫酸,微热,充分反应后过滤,向滤液中插入铁片,有气泡产生,则滤渣中一定含有______;氧化铜与稀硫酸反应的化学反应方程式为______.实验室用浓硫酸配制一定量的稀硫酸,正确操作是将______,并不断搅拌.  rosemarying1年前1
rosemarying1年前1 -
 baoyuhai 共回答了19个问题
baoyuhai 共回答了19个问题 |采纳率84.2%根据氧化铜与硫酸反应生成硫酸铜和水;铁与硫酸反应生成硫酸亚铁和氢气;由题目给出的信息可知:向滤液中插入薄铁片,有气泡产生,说明滤液中一定含有硫酸,没有硫酸铜;也说明铁把硫酸铜中的铜置换出来,因此固体中一定有铜,其中氧化铜和硫酸反应的方程式为CuO+H 2 SO 4 =CuSO 4 +H 2 O;浓硫酸溶于水会释放大量的热,可能会溅出伤人,所以用浓硫酸配制一定量的稀硫酸时,要把浓硫酸沿容器壁慢慢注入水中,并不断搅拌.
故答案为:铜;CuO+H 2 SO 4 =CuSO 4 +H 2 O;要把浓硫酸沿容器壁慢慢注入水中;1年前查看全部
- 在学习碳酸钠知识时,张老师在做完碳酸钠溶液和澄清石灰水反应演示实验后,对浑浊液过滤,得到澄清的滤液.对于滤液的组成,课堂
在学习碳酸钠知识时,张老师在做完碳酸钠溶液和澄清石灰水反应演示实验后,对浑浊液过滤,得到澄清的滤液.对于滤液的组成,课堂上老师的提问和同学们的回答如下表:
(1)假设你是丁同学,请你也提出一个与甲、乙、丙同学不同的猜想,把猜想写在上面表格中.并对你自己的猜想设计一个简单的实验加以证明.人 员 对话 老 师 问:滤液里可能含有哪些溶质呢? 甲同学 答:可能是NaOH、Na2C03 乙同学 答:可能是NaOH、Na2C03、Ca(OH)2 丙同学 答:可能是NaOH 丁同学 答:可能是______
(2)你认为甲、乙、丙同学的猜想都合理吗?如有不合理的请说明理由.______.实验步骤 实验现象 实验结论 取样于试管中,______ ______ 自己的猜想成立
(3)甲同学针对自己的猜想进行了如下实验:
你认为甲同学的实验设计是否正确?请说明理由是______.实验步骤 实验现象 实验结论 取样于试管中,滴入足量稀盐酸 没有气体产生 甲的猜想不成立
(4)为了进一步证明甲同学的猜想,丁同学又进行了又下实验探究:
写出碳酸钠溶液与氯化钙溶液反应的化学方程式______.实验步骤 实验现象 实验结论 取样于试管中,再滴入氯化钙溶液 生成______ 甲的猜想成立  wondercom1年前1
wondercom1年前1 -
 dengjiege 共回答了14个问题
dengjiege 共回答了14个问题 |采纳率92.9%解题思路:物质之间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,然后结合其他同学的猜想及碳酸钠和澄清石灰水反应一定生成氢氧化钠进行回答;
(1)根据氢氧化钙的化学性质分析;
(2)根据碳酸钠和氢氧化钙可发生反应,剩余物中两种反应物不会同时剩余进行解答;
(3)根据碳酸盐的检验是采用加酸观察是否有气体产生的方法进行分析;
(4)根据碳酸钠的化学性质分析,碳酸钠会与氯化钙反应生成白色沉淀碳酸钙和氯化钠;由碳酸钠和氢氧化钙反应的方程式可知:反应后滤液中一定会有氢氧化钠存在,若碳酸钠过量,则含有碳酸钠,即甲同学的猜想,若氢氧化钙过量,则含有氢氧化钙,故丁同学的猜想:可能含有NaOH和Ca(OH)2;
(1)因为碳酸钠和氢氧化钙反应一定生成氢氧化钠,所以只需证明溶液中是否有氢氧化钙就可以了,氢氧化钙与二氧化碳和可溶性的碳酸盐反应会生成沉淀,所以可以根据氢氧化钙的这些性质设计实验进行证明;
(2)物质之间发生化学反应时存在一定量的关系,如果某种反应物过量,会有剩余,但是两种反应物不会同时剩余,因为二者可反应,所以乙同学的猜想不合理;
(3)要证明碳酸钠的存在,涉及到的就是碳酸盐的检验,所以可以采用加酸的方法,由于滤液中含有氢氧化钠,因此需要加入足量的盐酸,始终没有CO2气体放出,说明没有碳酸钠,甲的猜想不成立;
(4)取样于试管中,再滴入氯化钙溶液,如果该滤液中含有碳酸钠,则碳酸钠会与氯化钙反应生成白色沉淀碳酸钙,从而证明甲的猜想正确;碳酸钠溶液与氯化钙溶液反应生成碳酸钙和氯化钠,反应的化学方程式是Na2CO3+CaCl2=CaCO3↓+2NaCl.
故答案是:NaOH和Ca(OH)2
(1)滴加碳酸钠溶液;溶液变浑浊;
(2)乙同学的猜想不合理,因为氢氧化钙与碳酸钠在溶液中不能共存,二者能相互反应;
(3)正确,因为盐酸的量足量,始终没有CO2气体放出,说明没有碳酸钠;
(4)白色沉淀;Na2CO3+CaCl2=CaCO3↓+2NaCl.点评:
本题考点: 实验探究物质的组成成分以及含量;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 物质之间发生化学反应时会完全进行,存在量的关系,所以不会出现反应物同时剩余的情况.另外在设计实验方案时,为保证实验结果准确,需要控制加入的药品的用量.1年前查看全部
- 把氧化铜和铁粉的混合物放在一定量的稀硫酸中,反应停止后过滤除去不溶物,向滤液中加入一块薄铁片,观察不到
把氧化铜和铁粉的混合物放在一定量的稀硫酸中,反应停止后过滤除去不溶物,向滤液中加入一块薄铁片,观察不到
A.滤出的不溶物中只有铜,不可能含铁
B.滤出的不溶物中只有铁,不可能含铜
C.滤出的不溶物中一定含有铜,也可能含有铁
D.滤液中一定含有FeSO4,不可能有CuSO4和H2SO4
为什么答案上说C也是对的呢?哪有Cu? zhangyying1年前1
zhangyying1年前1 -
 若渝 共回答了22个问题
若渝 共回答了22个问题 |采纳率90.9%稀硫酸先和氧化铜反应生成CuSO4,因为稀硫酸是一定量的所以还有铁粉剩下,剩下的铁粉再和CuSO4发生反应,所以有Cu.1年前查看全部
- 在进行叶绿体中色素的提取和分离的试验时,不能让层析液没及滤液细线的原因是
 tianya海角1年前1
tianya海角1年前1 -
 爱上飞鸟的鱼 共回答了13个问题
爱上飞鸟的鱼 共回答了13个问题 |采纳率69.2%分离色素时,一定不要让滤纸条上的滤液细线没及到层析液,这是因为色素易溶解于层析液中,导致色素带不清晰,影响实验效果.1年前查看全部
- 在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温
在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温度下无水硫酸铜的溶解度为40g,则此包无水硫酸铜的质量是多少?
 默儿爱李强1年前3
默儿爱李强1年前3 -
 光看不回帖 共回答了20个问题
光看不回帖 共回答了20个问题 |采纳率90%解题思路:根据饱和溶液中质量分数不变和溶解度计算出剩余饱和溶液中溶质和溶剂的质量,根据硫酸铜晶体组成计算晶体中溶质的质量,两者之和为此包无水硫酸铜的质量.把无水硫酸铜粉末加入150g蒸馏水中,得到一定量的蓝色晶体CuSO4•5H20,剩余溶液仍然是饱和溶液,设剩余溶液中的溶质为xg,
则[40g/100g+40g]=[xg/84g]得:x=24
结晶水的质量=150g-(84g-24g)=90g,设结晶中硫酸铜的质量为yg
CuSO4~5H20
160 90
yg90g
[160/90]=[yg/90g]
y=160,此包无水硫酸铜的质量为=160g+24g=184g.
答:此包无水硫酸铜的质量是184g.点评:
本题考点: 溶液中溶质的质量分数及相关计算.
考点点评: 本题考查质量守恒定律,质量分数的计算,解题时注意守恒思想的运用.1年前查看全部
- 关于化学推断题类型的几道题1.白色的粉末A,加入B后变成蓝色溶液.向期中加入试剂C,生成白色沉淀硫酸钡,过滤后滤液中加入
关于化学推断题类型的几道题
1.白色的粉末A,加入B后变成蓝色溶液.向期中加入试剂C,生成白色沉淀硫酸钡,过滤后滤液中加入试剂D,得到蓝色沉淀E.再次过滤,滤液是氯化钠溶液.根据以上现象判断A__ B__ C__ D__E__
2.A、B、C、D、E都是无色气体,F是无色液体,他们之间有如下反应关系:
(1)A+B→点燃→F
(2)A+Cl2→点燃→C;将C通入F,能使石蕊试剂变红
(3)B+D→点燃→E;将E通入澄清石灰水,能使石灰水变浑浊
试判断(化学式表示)
A___ B___ C___ D__ E___ F___ ddf6201年前3
ddf6201年前3 -
 jinxb 共回答了22个问题
jinxb 共回答了22个问题 |采纳率86.4%1.白色的粉末A,加入B后变成蓝色溶液.向期中加入试剂C,生成白色沉淀硫酸钡,过滤后滤液中加入试剂D,得到蓝色沉淀E.再次过滤,滤液是氯化钠溶液.根据以上现象判断
A__ CuSO4
B__ H2O
C__ BaCl2
D__NaOH
E__Cu(OH)2
2.A、B、C、D、E都是无色气体,F是无色液体,他们之间有如下反应关系:
(1)A+B→点燃→F
(2)A+Cl2→点燃→C;将C通入F,能使石蕊试剂变红
(3)B+D→点燃→E;将E通入澄清石灰水,能使石灰水变浑浊
试判断(化学式表示)
A___ H2
B___O2
C___ HCl
D__ CO
E___ CO2
F___H2O1年前查看全部
大家在问
- 1英语翻译把:我叫李华,是个十八岁的男孩,正在上高中,擅长英语,爱好体育,乐于助人,善于交往 翻译成英语,要连成一段话,适
- 2加、乘原理红、黄、蓝、白四种颜色不同的小旗,各有2、2、3、3面,任意取出三面按顺序排成一行,表示一种信号,问:共可以表
- 3各有各的姿态换成成语
- 4将一堆沙子分成3堆,第一队和第二堆沙子的质量占总质量的2/5,第二队和第三堆沙子的质量占总质量的5/8,第
- 5翻译下列句子 看新年晚会
- 6直线l与椭圆x22+y2=1交于不同的两点P1、P2,线段P1P2的中点为P,设直线l的斜率为k1(k1≠0),直线OP
- 7小刚想测量家中酱油的密度,但家里没有量筒,只有天平、砝码、小空瓶、 水。他按照自己设计的实验方案进行了测量。
- 81 l spend a lot time p___English every morning
- 9串联电路电源电压不变,电路中串联有定值电阻R,为使电流表的示数略有增加,则需给R---
- 10《制冷与低温技术原理》第266页中是否有错误?
- 11用一句话概括下面的新闻内容,最准确的一项是( )
- 121个三角形变成4个,4个三角形变成13个,下一次应该变成多少个
- 13L/C在国际贸易中式什么意思
- 14课文题为“大自然的启示”,我们从这两篇文章中各得到了什么启示呢?
- 15充满活力,富有朝气的词语
