4个碳酸分子和3个硫酸分子具有相同的( )
 fanjihua_20002022-10-04 11:39:543条回答
fanjihua_20002022-10-04 11:39:543条回答A氢原子数 B原子种类
C原子总数 D氧原子数
我知道答案选D.就是为什么啊.

已提交,审核后显示!提交回复
共3条回复
 林狗剩 共回答了12个问题
林狗剩 共回答了12个问题 |采纳率100%- 4H2CO3 3H2SO4
A氢原子数 8 6
B原子种类 H、C、O H、S、O
C原子总数 24 21
D氧原子数 12 12 - 1年前
 yl444444 共回答了617个问题
yl444444 共回答了617个问题 |采纳率- 4H2CO3 3H2SO4
4H2CO3中有:8H,4C,12O
3H2SO4中有:6H,3S,12O
故答案为D。 - 1年前
 yhydsj 共回答了302个问题
yhydsj 共回答了302个问题 |采纳率- 一个碳酸分子中有三个氧原子,一个硫酸分子中含有四个氧原子,4个碳酸分子和3个硫酸分子具有相同的氧原子数相等
- 1年前
相关推荐
- 用氢氧化钙和碳酸纳制氢氧化钠,怎样提高氢氧化钠的纯度?
用氢氧化钙和碳酸纳制氢氧化钠,怎样提高氢氧化钠的纯度?
氢氧化钙——建筑用的“精灰”
碳酸钠——食用纯碱 yunxiao001年前2
yunxiao001年前2 -
 寒江821 共回答了16个问题
寒江821 共回答了16个问题 |采纳率100%首先,要提高氢氧化钙溶液和碳酸钠溶液的质量分数,建议在低温下反应,但要增加反应时间.反应后过虑,将剩下的溶液 加热蒸发.补充:建议楼主增大反应剂量,有利于后期的蒸发提纯.蒸发时可用容积较大的容器进行蒸发,此时可用煤气灶代替酒精灯.还有,反应物中应增大碳酸钠的剂量,宁可过量也不能让氢氧化钙过量(钙的化合物多不融于水,会对后期使用造成影响) 重点:反应物溶液的质量分数(低温反应),反应剂量增大,碳酸钠过量.1年前查看全部
- 某地1,000Kg化肥的市场价格如下:CO(NH2)2 1,780元、NH4NO3 1,360元、NH4HCO3(碳酸氢
某地1,000Kg化肥的市场价格如下:CO(NH2)2 1,780元、NH4NO3 1,360元、NH4HCO3(碳酸氢铵)560元.分别用10,000元采购上述化肥,则购得化肥中含氮元素最高的是哪一种?
 mistletoe_831年前2
mistletoe_831年前2 -
 爱猫的老鼠913 共回答了14个问题
爱猫的老鼠913 共回答了14个问题 |采纳率100%解题思路:通过计算四种化肥中的性价比,可以得出本题的答案.首先计算10000元采购各种化肥的质量,然后用化肥的质量乘以各化肥中N元素的质量分数,既可得出购得化肥中N元素的质量,比较大小.10000元钱能买CO(NH2)2的质量为:[10000元/1.78元/kg]≈5618.0kg
5618.0kgCO(NH2)2中氮元素的质量为:5618.0kg×[14×2
12+16+(14+1×2)×2×100%≈2621.7kg;
10000元钱能买NH4N03的质量为:
10000元/1.36元/kg]≈7352.9kg
7352.9kgNH4N03中氮元素的质量为:7352.9kg×[14×2/14+1×4+14+16×3 ]×100%≈2573.5kg;
10000元钱能买NH4HC03的质量为:[10000元/0.56元/kg]≈17857.1kg
17857.1kgNH4HC03中氮元素的质量为:17857.1kg×[14/14+1×4+1+12+16×3]×100%≈3164.6kg;
三者相比较 3164.6kg>2621.7kg>2573.5kg
故碳酸氢铵含氮量最高
答:含氮元素最高的是碳酸氢铵点评:
本题考点: 化合物中某元素的质量计算.
考点点评: 本题主要考查有关化学式的计算中元素质量分数的计算和元素质量的计算.1年前查看全部
- 氯化铁中加硫氢化氨,再加碳酸氨的现象及解释
 yishix1年前1
yishix1年前1 -
 flight1982 共回答了14个问题
flight1982 共回答了14个问题 |采纳率92.9%第一步会看到红褐色沉淀,闻到臭鸡蛋气味,原因是铁离子和硫离子双水解产生氢氧化铁和硫化氢.第二步无现象1年前查看全部
- 将a克聚苯乙烯树脂溶于b升苯中,然后通入c摩尔乙炔气体,所混合物中的碳酸氢两种元素的质量比是多少?
 miniqun1年前1
miniqun1年前1 -
 A20010571 共回答了16个问题
A20010571 共回答了16个问题 |采纳率93.8%聚苯乙烯可以看为nC8H8 苯C6H6 乙炔C2H2
注意到聚苯乙烯树脂最简试是CH,苯CH,乙炔CH
则C:H个数比始终1:1
所以质量比C:H=12:11年前查看全部
- 为什么碳酸钠溶液中氢离子浓度大于碳酸分子浓度?
 wang26591年前1
wang26591年前1 -
 myzpc 共回答了14个问题
myzpc 共回答了14个问题 |采纳率92.9%c(NA+)〉c(CO32-)〉c(OH-)〉c(HCO3-)〉c(H+)
A.Na2CO3 = 2Na+ + CO3(2-) 完全电离,则c(NA+)〉2c(CO32-);
B.CO3(2-) + H2O == HCO3- + OH-; Kb1= Kw/Ka2 约等于10^(-4),说明水解程度小,主要以CO3(2-)形式存在.
Kb1=〔HCO3-〕〔OH-〕/〔CO3(2-)〕
所以c(CO32-)〉c(OH-)
C.HCO3- + H2O == H2CO3 + OH-; Kb2 = Kw/Ka1
D.H2O == H+ + OH-
c(OH-)=c(HCO3-)+c(H2CO3)+ c(H+)
所以c(OH-)〉c(HCO3-),但是二者相差不大:C和D相比B而言,很小;所以c(HCO3-)〉c(H+) .
c(H+) =Kw/c(OH-)1年前查看全部
- (2008•杭州)某化工厂排出的废水中含有硝酸银,硝酸钡,为了不污染环境并充分利用资源,需要从废水中回收金属银并制得碳酸
(2008•杭州)某化工厂排出的废水中含有硝酸银,硝酸钡,为了不污染环境并充分利用资源,需要从废水中回收金属银并制得碳酸钡,操作步骤和实验结果如下表,请填出表中未完成部分(写化学式)
操作步骤 实验结果 (1)向废水中加入适量______后过滤 分离出滤液A和滤出物______ (2)向滤液A中加入______溶液后过滤 滤出物是蓝色沉淀,滤液B中只含一种溶质 (3)向滤液B中加入______溶液后过滤 得到碳酸钡晶体  xiaonn8208211年前1
xiaonn8208211年前1 -
 oo是Id 共回答了12个问题
oo是Id 共回答了12个问题 |采纳率83.3%解题思路:根据题意:要从废水中回收金属银,可向废水中加入适量的排在银前的金属,由(2)滤出物是蓝色沉淀,说明该沉淀是氢氧化铜,可知(1)中加入的金属是铜,与硝酸银反应生成硝酸铜和银;(2)向滤液A中加入溶液过滤得到氢氧化铜沉淀,说明加入的是一种碱,又滤液B中只含一种溶质,说明该碱溶液与硝酸铜反应生成氢氧化铜和硝酸钡,据复分解反应原理可知加入的是氢氧化钡溶液;硝酸钡溶液可与碳酸钠、碳酸钾溶液反应生成碳酸钡沉淀.要从废水中回收金属银,可向废水中加入适量的排在银前的金属,由(2)滤出物是蓝色沉淀,说明该沉淀是氢氧化铜,由此说明(1)中加入的金属是铜,与硝酸银反应生成硝酸铜和银;(2)向滤液A中加入溶液过滤得到氢氧化...
点评:
本题考点: 金属的化学性质;盐的化学性质.
考点点评: 了解顺序表中前面的金属可将后面的金属从其盐溶液中置换出来,氢氧化铜是蓝色沉淀,及复分解反应的原理,才能结合题意正确分析解答,本题能很好考查学生依据所学分析、解决问题的能力.1年前查看全部
- (7分)类比法是化学研究物质的重要方法之一。草酸(C 2 H 2 0 4 )的化学性质与碳酸相似,草酸受热会分解得到三种
(7分)类比法是化学研究物质的重要方法之一。草酸(C 2 H 2 0 4 )的化学性质与碳酸相似,草酸受热会分解得到三种氧化物,某兴趣小组对草酸的有关性质进行了探究,按要求回答相关的问题:
[提出猜想](1)草酸能够使紫色石蕊试液变为 色。
(2)三种氧化物可能是 ,该猜想的依据是 。
[查阅资料]
1.无水硫酸铜是一种白色粉末物质,遇水变成蓝色的硫酸铜晶体。
2.向氯化钯溶液中通入CO,产生黑色沉淀。
[实验探究]兴趣小组为验证猜想,将草酸受热后得到的气体,依次通过了装置A、B、C: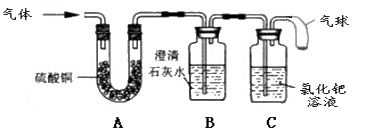
[实验结论](3)当装置A、B、C实验现象是 ,证明猜想是正确的。
[实验反思](4)①实验装置中气球所起的作用是 。
②是否可以将装置A和B对调,其理由是 。 gshengyi1年前1
gshengyi1年前1 -
 阿其郎 共回答了15个问题
阿其郎 共回答了15个问题 |采纳率86.7%[提出猜想](1)红 (2)CO 2 H 2 O CO;元素守恒
[实验结论](3) A种白色固体变为蓝色,B中澄清石灰水变浑浊,C中出现黑色沉淀(2分)
[实验反思](4)①调节C装置容积和收集气体(防CO扩散)
②不可以对调,其理由是气体若先通入B,会将溶液中的水带出,干扰水的检验。
1年前查看全部
- 向氢氧化钡溶液中滴加硫酸氨溶液和向碳酸氢氨溶液中滴加氢氧化钠溶液的化学方程式及离子方程式
 killy06211年前1
killy06211年前1 -
 red_2005 共回答了18个问题
red_2005 共回答了18个问题 |采纳率94.4%(1)向氢氧化钡溶液中滴加硫酸铵溶液,不管怎么加,反应只有一种情况
Ba(OH)2+(NH4)2SO4=BaSO4↓+2NH3·H2O
(2)向碳酸氢铵溶液中滴加氢氧化钠溶液,有2种情况
刚开始,由于滴加的NaoH量少.反应2NH4HCO3+2NaOH=(NH4)2CO3+Na2CO3+2H2O
离子方程式:HCO3- +OH-=CO32+H2O
再继续滴加NaOH,后续反应:(NH4)2CO3+2NaOH=Na2CO3+2NH3·H2O
离子方程式:NH4+ +OH-=NH3·H2O
如果一下子加入大量的NaOH:NH4HCO3+2NaOH=Na2CO3+NH3·H2O+H2O
离子方程式:
NH4+ +HCO3-+2OH- =CO32- +NH3·H2O+H2O1年前查看全部
- 请问碳酸(H2CO3)和氢氧化钙(Ca(OH)2)能不能发生反应?如果能,请给出化学方程式
请问碳酸(H2CO3)和氢氧化钙(Ca(OH)2)能不能发生反应?如果能,请给出化学方程式
一定要给出完整的,
最好配平一下,西西,我懒的配平了 Norleber1年前4
Norleber1年前4 -
 灵魂痛笑 共回答了18个问题
灵魂痛笑 共回答了18个问题 |采纳率83.3%肯定能生成反映,H2CO3 + Ca( OH )2 = CaCO3 + H2O1年前查看全部
- 碳酸氢铝 Al(HCO3)3 是否是易溶于水
 quliang11031年前2
quliang11031年前2 -
 guo子狸 共回答了10个问题
guo子狸 共回答了10个问题 |采纳率90%在水中双水解,形成氢氧化铝胶体和二氧化碳气体
讨论溶解度没有什么意义1年前查看全部
- 水能区分出硫酸与碳酸吗?是硫酸与碳酸!
 馨冰露1年前3
馨冰露1年前3 -
 电脑玩 共回答了21个问题
电脑玩 共回答了21个问题 |采纳率100%浓硫酸加水时会放出大量的热,现象很明显
碳酸则没什么现象,所以应该可以区分
不过考试时不会出这个的,碳酸一般就是二氧化碳溶于水产生的1年前查看全部
- 碳酸溶液可促进土壤中的钙离子、镁离子被植物吸收.为什么?
 kikikids1年前2
kikikids1年前2 -
 也许wugou 共回答了23个问题
也许wugou 共回答了23个问题 |采纳率73.9%可溶性盐可以被植物很好利用
因为土壤中的钙,镁离子基本上是以碳酸盐的形式存在,加二氧化碳可以使其成为可溶性的碳酸氢盐 ,促进吸收啦!1年前查看全部
- 有下列化学物质:钠、铁、铜、氨气、一水合氨、二氧化碳、碳酸、水、氧化铝、稀盐酸、氯化氢、稀硫酸、硫酸、氢氧化钠固体、氢氧
有下列化学物质:
钠、铁、铜、氨气、一水合氨、二氧化碳、碳酸、水、氧化铝、稀盐酸、氯化氢、稀硫酸、硫酸、氢氧化钠固体、氢氧化钠溶液、澄清石灰水、氢氧化钙、氯化钠、硫酸钠、乙醇、碳酸钙、硫酸钡、氧化钠、硝酸钾、硫酸铵、氯酸钾、四氯化碳、石墨.
1.属于电解质的是:
2.属于非电解质的是:
3.水溶液中能导电的是:
4.固体能导电的是:
5.熔融状态能导电的是:
6.属于强电解质的是:
7.属于弱电解质的是:
麻烦大家了,这道题真的很麻烦 , 银色触角1年前1
银色触角1年前1 -
 草莓气息 共回答了14个问题
草莓气息 共回答了14个问题 |采纳率100%1.属于电解质的是:一水合氨.碳酸,水,氧化铝,稀盐酸,氯化氢,稀硫酸、硫酸、氢氧化钠固体、氢氧化钠溶液、澄清石灰水、氢氧化钙、氯化钠、硫酸钠、碳酸钙、硫酸钡、氧化钠、硝酸钾、硫酸铵、氯酸钾
2.属于非电解质的是:钠、铁、铜、二氧化碳、氨气、乙醇.四氯化碳、石墨.
3.水溶液中能导电的是:钠、 氨气、二氧化碳、氯化氢、氢氧化钠固体、氢氧化钙、氯化钠、硫酸钠、碳酸钙、硫酸钡、氧化钠、硝酸钾、硫酸铵、氯酸钾
4.固体能导电的是:钠、铁、铜、石墨.
5.熔融状态能导电的是:氢氧化钠固体、氢氧化钙、氯化钠、硫酸钠、碳酸钙、硫酸钡、氧化钠、硝酸钾、硫酸铵、氯酸钾、石墨.氯化氢、稀硫酸、硫酸、氢氧化钠固体、氢氧化钠溶液、氢氧化钙、氯化钠、硫酸钠、6.属于强电解质的是:稀盐酸、碳酸钙、硫酸钡、氧化钠、硝酸钾、硫酸铵、氯酸钾、
7.属于弱电解质的是:一水合氨、
碳酸、水、1年前查看全部
- 碳酸氢铝溶解度碳酸氢铝存在吗
 nsx19951年前1
nsx19951年前1 -
 Andrewpengpeng 共回答了24个问题
Andrewpengpeng 共回答了24个问题 |采纳率87.5%不存在
互相促进水解,很大幅度
于是Al3+ + 3HCO3- = Al(OH)3 沉淀 + 3CO2 气体
目前不知如何制备固体碳酸氢铝.知道了也没用,没有实际应用价值1年前查看全部
- (1)用化学符号表示:①2个氢原子______;②3个氧分子______;③碳酸______; ④标出氧化镁中镁
(1)用化学符号表示:
①2个氢原子______;
②3个氧分子______;
③碳酸______;
④标出氧化镁中镁元素的化合价
O+2 Mg .
O+2 Mg
(2)现有下列各种仪器,请根据它们的用途,选择相应的仪器,将它们的序号字母填在相应位置.
A.试管 B.烧杯 C.坩埚钳 D.漏斗 E.胶头滴管
①在做镁条燃烧实验时,用于夹持镁条的仪器是______;
②可以直接在酒精灯火焰上加热的玻璃仪器是______;
③溶解较多量的固体用到的容器是______;
④取用少量液体药品的仪器是______. 448598581年前1
448598581年前1 -
 早根 共回答了15个问题
早根 共回答了15个问题 |采纳率93.3%解题思路:(1)元素符号可以表示一种元素,也可以表示该元素的1个原子,有时还可以表示一种物质;
每个氧分子由2个氧原子构成;
每个碳酸分子由2个氢原子、1个碳原子和3个氧原子构成;
元素的化合价应该标在元素符号的正上方.
(2)在做镁条燃烧实验时,用于夹持镁条的仪器是坩埚钳;
试管、蒸发皿、燃烧匙等可以直接加热,烧杯、烧瓶等不能直接加热;
烧杯可以用于溶解较多量的固体;胶头滴管可以用来取用少量液体药品.(1)①2个氢原子可以表示为2H;
②3个氧分子可以表示为3O2;
③碳酸可以表示为H2CO3;
④氧化镁中,氧元素的化合价是-2,镁元素的化合价是+2,氧化镁中镁元素的化合价可以表示为
+2
MgO.
故填:2H;3O2;H2CO3;
+2
MgO.
(2)①在做镁条燃烧实验时,用于夹持镁条的仪器是坩埚钳C;
②可以直接在酒精灯火焰上加热的玻璃仪器是试管A;
③溶解较多量的固体用到的容器是烧杯B;
④取用少量液体药品的仪器是胶头滴管E.
故填:C;A;B;E.点评:
本题考点: 化学符号及其周围数字的意义;常用仪器的名称和选用.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.1年前查看全部
- 人体胃液中用于帮助消化食物的酸是( ) 1、盐酸 2、硫酸 3、碳酸 4、
人体胃液中用于帮助消化食物的酸是( ) 1、盐酸 2、硫酸 3、碳酸 4、
人体胃液中用于帮助消化食物的酸是( )
1、盐酸 2、硫酸 3、碳酸 4、硝酸 阿弥陀佛546051年前1
阿弥陀佛546051年前1 -
 anitallt 共回答了13个问题
anitallt 共回答了13个问题 |采纳率84.6%明显11年前查看全部
- 为什么碳酸在空气中容易分解?都是做鸡蛋和醋有关实验的问题,还有鸡蛋放在醋中表面上起的一层皮是什么?
 wangzhenfei1年前1
wangzhenfei1年前1 -
 87eeee 共回答了22个问题
87eeee 共回答了22个问题 |采纳率90.9%鸡蛋壳中的碳酸钙与醋酸作用,生成醋酸钙和碳酸,碳酸不稳定分解成二氧化碳和水(不一定非在空气中),醋酸钙易溶于水,不应该形成膜,鸡蛋在醋酸中浸泡时间短时,外面的膜是一些不溶的无机盐,如磷酸钙,或某些有机物,浸泡时间长后,碳酸钙都溶解了,那层软膜就是蛋壳的内膜,人称凤凰衣,该是蛋白质组成.1年前查看全部
- 碳酸氢铵和碳酸铵,碳酸氢钠和碳酸钠 这两对中有什么区别,也就是碳酸氢与碳酸之间的区别
 泰拳1年前3
泰拳1年前3 -
 xianzizh 共回答了29个问题
xianzizh 共回答了29个问题 |采纳率96.6%从盐的角度看,一种是酸式盐,另一种是正盐,两组中的物质都不一样.
碳酸氢铵与氨水反应可以得到碳酸铵;碳酸铵溶液中通入二氧化碳可以得到碳酸氢铵.
碳酸氢钠俗称"小苏打",加热能分解,生成碳酸钠和二氧化碳与水.热稳定性差;碳酸钠俗称"食碱",不易分解,且与二氧化碳和水反应能生成碳酸氢钠.两者都能与酸反应生成二氧化碳,碳酸氢钠可以继续与氢氧化钠反应生成碳酸钠.1年前查看全部
- 碳酸钙可以生成碳酸吗?
 彩芸追刖1年前1
彩芸追刖1年前1 -
 wmj13 共回答了11个问题
wmj13 共回答了11个问题 |采纳率81.8%加入酸就可以了,但是生成的 碳酸 不稳定会分解成 水+二氧化碳 .
例如:碳酸钙+盐酸=氯化钙+水+二氧化碳1年前查看全部
- 碳酸氢铵与氢氧化钠在不足量和过量前提下分别反应生成什么?碳酸氢铝呢?碳酸氢镁呢?
 柚子的寒香1年前1
柚子的寒香1年前1 -
 安静得像只鱼 共回答了18个问题
安静得像只鱼 共回答了18个问题 |采纳率83.3%氢氧化钠在不足量时,生成的水和碳酸根.
氢氧化钠在足量时,生成的一水合氨、水和碳酸根.
在此类反应中书写离子方程式的时候注意先是酸碱中和反应,剩下的再反应.1年前查看全部
- 弱酸酸性大小排列?苯酚、醋酸、碳酸、磷酸、氢硫酸、氢氟酸、氢碘酸、溴化氢......越多越好
 11mm1年前3
11mm1年前3 -
 tornado930 共回答了19个问题
tornado930 共回答了19个问题 |采纳率100%由强到弱依次为:高氯酸,氢碘酸,硫酸,氢溴酸,盐酸,硝酸,碘酸(以上为强酸,了解即可,大学涉及强弱排序),草酸(乙二酸),亚硫酸,磷酸,丙酮酸,亚硝酸(以上五种为中强酸),柠檬酸,氢氟酸,苹果酸,葡萄糖酸,甲酸,乳酸,苯甲酸,丙烯酸,乙酸,丙酸,硬脂酸,碳酸,氢硫酸,次氯酸,硼酸,硅酸,苯酚(其余为弱酸或极弱酸)!已经很全了,绝对够你用的了!不够的话,发留言我再给你补充!1年前查看全部
- 某钙片主要成分碳酸钙,其碳酸含量为80%,现需要补充钙元素4g需要吃钙片多少?
 polybear1年前4
polybear1年前4 -
 piaoer5757 共回答了20个问题
piaoer5757 共回答了20个问题 |采纳率95%CaCO3------Ca
100 40
x*80% 4g
100/40=x*80%/4g
x=12.5g1年前查看全部
- 碳酸易分解吗?(就是存在那个可逆反应吗?在水溶液中生成氢离子和碳酸根离子)
 daniao_8861年前5
daniao_8861年前5 -
 3020722320 共回答了11个问题
3020722320 共回答了11个问题 |采纳率90.9%碳酸在汽水中有,当然不稳定了,要不它往外流啊
水溶液中不叫分解,那叫在水中电解1年前查看全部
- 酸和盐生成酸和盐的化学方程式.不是生成碳酸!
 loverstears1年前5
loverstears1年前5 -
 木头33 共回答了15个问题
木头33 共回答了15个问题 |采纳率86.7%你就本着强酸制弱酸和复分解反应原理构造就行~~初中化学的话,一般就是硫酸与钡盐生成硫酸钡和一种酸,盐酸跟银盐生成氯化钡和一种酸~1年前查看全部
- 二氧化碳溶于水产生碳酸,溶液中存在的阳离子是什么
 cxuhua1年前4
cxuhua1年前4 -
 水她她 共回答了21个问题
水她她 共回答了21个问题 |采纳率100%二氧化碳溶于水产生碳酸,碳酸是弱酸,会电离出部分氢离子(即溶液中存在的阳离子)1年前查看全部
- 下列叙述正确的是A只有含有钙离子,镁离子的水都属于硬水 B软水中不含和含较少的钙离子和镁离子 C水垢的成分是碳酸钙和碳酸
下列叙述正确的是
A只有含有钙离子,镁离子的水都属于硬水
B软水中不含和含较少的钙离子和镁离子
C水垢的成分是碳酸钙和碳酸镁
D用明矾净化后的水一定是软水 隐子小雪1年前1
隐子小雪1年前1 -
 气候暗暗 共回答了17个问题
气候暗暗 共回答了17个问题 |采纳率94.1%A还有别的离子;
B对;
C水垢的主要成分是碳酸钙和碳酸镁
D用明矾净化后的水一定是硬水1年前查看全部
- 下列各组溶液,相互不能发生反应的是( ) A.氯化铁和氢氧化钠 B.硝酸银和盐酸 C.氢氧化钡和硝酸 D.硫酸钠和碳酸
下列各组溶液,相互不能发生反应的是( ) A.氯化铁和氢氧化钠 B.硝酸银和盐酸 C.氢氧化钡和硝酸 D.硫酸钠和碳酸钾  sgping1231年前1
sgping1231年前1 -
 emily_xu 共回答了20个问题
emily_xu 共回答了20个问题 |采纳率95%A、因氯化铁和氢氧化钠相互交换成分能生成氢氧化铁沉淀,则能发生化学反应,故A错误;
B、因硝酸银和盐酸相互交换成分能生成氯化银沉淀,则能发生化学反应,故B错误;
C、因氢氧化钡和硝酸相互交换成分能生成水,则能发生化学反应,故C错误;
D、因硫酸钠和碳酸钾之间相互交换成分不能生成水、气体、沉淀,则不能反应,故D正确;
故选D.1年前查看全部
- 碱式碳酸铜和碳酸氢纳的化学式化学式看清楚 不要一大堆东西
 爱就让你幸福1年前1
爱就让你幸福1年前1 -
 C风雨飘摇 共回答了17个问题
C风雨飘摇 共回答了17个问题 |采纳率88.2%cu(oh)2co3
nahco31年前查看全部
- 欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如图所示.已知:碳酸不能溶解Al(OH)
欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如图所示.已知:碳酸不能溶解Al(OH)3沉淀.
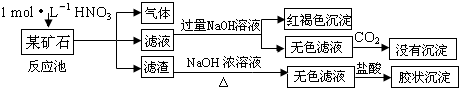
(1)Si在周期表中的位置是______.
(2)下列说法正确的是______.
a.酸性:H2CO3>H2SiO3b.原子半径:O<C<Si<Al
c.稳定性:H2O>CH4>SiH4d.离子半径:O2-<Al3+
(3)该矿石的组成是______,滤渣和NaOH溶液反应的离子方程式是______.
(4)该矿石和1mol L-1HNO3反应的离子方程式______.
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,目的是______;若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1mol L-1 HNO3的体积为______L. 劫啊劫1年前1
劫啊劫1年前1 -
 心中的海豚 共回答了17个问题
心中的海豚 共回答了17个问题 |采纳率100%解题思路:(1)根据硅的原子核外电子排布确定在周期表中的位置;
(2)a.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
b.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断;
c.元素的非金属性越强,对应的氢化物越稳定;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小;
(3)矿石加硝酸生成气体,可说明含有FeCO3,加入过量NaoH溶液后通入过量二氧化碳没有沉淀生成,说明没有Al2O3,滤渣溶解后加入盐酸生成胶状沉淀,说明含有SiO2;
(4)矿石含有FeCO3,可与HNO3反应;
(5)处理该矿石,逸出的气体为NO,可与氧气反应生成硝酸,可循环利用,结合反应的方程式计算.(1)硅的原子核外有3个电子层,最外层电子数为4,则应位于周期表第三周期、ⅣA族,
故答案为:第三周期、ⅣA族;
(2)a.非金属性:C>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故a正确;
b.同周期元素从左到右原子半径逐渐减小,O<C、Si<Al,同主族元素从上到下原子半径逐渐增大,则C<Si,故b正确;
c.非金属性O>C>Si,元素的非金属性越强,对应的氢化物越稳定,故c正确;
d.两种离子核外电子排布相同,核电荷数越大,离子半径越小,则O2->Al3+,故d错误;
故答案为:abc;
(3)矿石加硝酸生成气体,可说明含有FeCO3,加入过量NaoH溶液后通入过量二氧化碳没有沉淀生成,说明没有Al2O3,滤渣溶解后加入盐酸生成胶状沉淀,说明含有SiO2,
滤渣和NaOH溶液反应的离子方程式是SiO2+2OH-=SiO32-+H2O,
故答案为:FeCO3和SiO2;SiO2+2OH-=SiO32-+H2O;
(4)矿石含有FeCO3,可与HNO3反应,离子方程式为3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O,
故答案为:3FeCO3+10H++NO3-=3Fe3++3CO2↑+NO↑+5H2O;
(5)由于NO是有毒气体,不能随意排放,所以这样做的目的是NO循环使用能减少环境污染,且NO跟H2O、O2反应后又得到硝酸提高原料利用率.根据以上分析可知,该矿石中含有碳酸亚铁和二氧化硅,其中碳酸亚铁的质量是2.36×103 kg-1.2×103 kg=1.16×103kg,物质的量是10000mol,则根据(4)中的方程式可知,消耗硝酸的物质的量是
105
3mol,所以理论上至少需要1molL-1 HNO3的体积为3.0×104L.
故答案为:NO循环使用能减少环境污染,NO跟H2O、O2反应后又得到硝酸提高原料利用率;3×104.点评:
本题考点: 探究物质的组成或测量物质的含量;元素周期律的作用;物质分离和提纯的方法和基本操作综合应用.
考点点评: 该题综合考查粗硅的制备、元素周期律的应用、物质的检验、氧化还原反应方程式的书写、尾气处理和原料的使用以及有关计算,是高考中的常见题型,难度较大,试题综合性强,侧重对学生能力的培养和解题方法的指导,有助于培养学生逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.该试题还通过鼓励学生去大胆的猜想及拓展探究实验,考查学生的基本科学素养.该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论.1年前查看全部
- 写出下列反应的离子方程式:①向氢氧化钠溶液中加入氯化铜溶液:______②稀硫酸与氢氧化钡溶液反应:______③向碳酸
写出下列反应的离子方程式:
①向氢氧化钠溶液中加入氯化铜溶液:______
②稀硫酸与氢氧化钡溶液反应:______
③向碳酸氢钠溶液中加入稀盐酸:______
④过量二氧化碳通入澄清石灰水:______. 亩亩不1年前1
亩亩不1年前1 -
 jian520174 共回答了22个问题
jian520174 共回答了22个问题 |采纳率90.9%解题思路:①反应生成氢氧化铜沉淀和氯化钠;②反应生成硫酸钡沉淀和水;③反应生成氯化钠和是、二氧化碳;④反应生成碳酸氢钙.①向氢氧化钠溶液中加入氯化铜溶液反应生成氢氧化铜沉淀和氯化钠,该离子反应为Cu2++2OH-=Cu(OH)2↓,故答案为:Cu2++2OH-=Cu(OH)2↓;
②稀硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,该离子反应为2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
③向碳酸氢钠溶液中加入稀盐酸反应生成氯化钠和是、二氧化碳,该离子反应为HCO3-+H+=C02↑+H2O,故答案为:HCO3-+H+=C02↑+H2O;
④过量二氧化碳通入澄清石灰水中反应生成碳酸氢钙,该离子反应为CO2+OH-=HCO3-,故答案为:CO2+OH-=HCO3-.点评:
本题考点: 离子方程式的书写.
考点点评: 本题考查离子反应方程式的书写,明确发生的化学反应是解答本题的关键,注意离子反应的书写方法即可解答,题目难度不大.1年前查看全部
- 高一化学中学的酸都有哪些?如题,除了盐酸 硫酸 硝酸 碳酸 硅酸 醋酸 还有哪些能把化学式写出来吗?形如H3XO4和HX
高一化学中学的酸都有哪些?
如题,除了盐酸 硫酸 硝酸 碳酸 硅酸 醋酸 还有哪些能把化学式写出来吗?形如H3XO4和HXO4的什么酸啊. d1503721年前3
d1503721年前3 -
 虫子521 共回答了25个问题
虫子521 共回答了25个问题 |采纳率100%卤族元素加H都是算
HF氢氟酸
HBr氢溴酸
HI氢碘酸
HClO4高氯酸(最强的酸)
H3PO4磷酸
HClO次氯酸
H2SO3亚硫酸
HNO2亚硝酸
还有有机的酸
草酸 苯酚1年前查看全部
- 对大棚农作物施用汽水(碳酸溶液),为什么可促进土壤中的钙、镁离子被植物吸收
 ma_xuexiao1年前2
ma_xuexiao1年前2 -
 ee没有蓝天白云 共回答了23个问题
ee没有蓝天白云 共回答了23个问题 |采纳率82.6%因为土壤中的钙,镁离子基本上是以碳酸盐的形式存在,加碳酸可以使其成为可溶性的碳酸氢盐 ,1年前查看全部
- 敞口酒精会挥发出的是( )分子,碳酸饮料中的碳酸易分解,分解产生的物质是什么?
敞口酒精会挥发出的是( )分子,碳酸饮料中的碳酸易分解,分解产生的物质是什么?
结合这两个例子对挥发和分解的认识是什么? 念飞云1年前4
念飞云1年前4 -
 橘庆太君 共回答了19个问题
橘庆太君 共回答了19个问题 |采纳率78.9%敞口酒精会挥发出的是( 乙醇)分子,碳酸饮料中的碳酸易分解,分解产生的物质是水和二氧化碳.
其中:挥发是分子运动,间距变化,分子本身不变,是物理属性;
分解是物质分子分为原子再重新组合成分子,是化学变化.1年前查看全部
- (2008•佛山一模)过氧化氢是一种很弱的酸,酸性比碳酸还要弱,为了验证其酸性,请选择一种最合适的盐溶液与其反应( )
(2008•佛山一模)过氧化氢是一种很弱的酸,酸性比碳酸还要弱,为了验证其酸性,请选择一种最合适的盐溶液与其反应( )
A.碳酸钠溶液
B.碳酸氢钠溶液
C.偏铝酸钠溶液
D.硫化钠溶液 桃红色的鸵鸟1年前1
桃红色的鸵鸟1年前1 -
 变脸姬 共回答了14个问题
变脸姬 共回答了14个问题 |采纳率100%解题思路:过氧化氢是一种很弱的酸,酸性比碳酸还要弱,根据强酸制取弱酸来分析,过氧化氢能和弱于双氧水的弱酸盐发生复分解反应.A.双氧水的酸性小于碳酸,所以和碳酸钠溶液不反应,故A错误;
B.双氧水的酸性小于碳酸,和碳酸氢钠溶液也不反应,故B错误;
C.双氧水的酸性大于偏铝酸,能和偏铝酸钠反应生成白色沉淀,故C正确;
D.双氧水的酸性小于氢硫酸,且双氧水具有强氧化性,能把硫离子氧化生成硫单质,所以双氧水体现了氧化性而不是酸性,故D错误.
故选C.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查了双氧水性质的判断,根据强酸制取弱酸来方向性解答,易错选项是D,不能忘记双氧水还有强氧化性,为易错点.1年前查看全部
- 欲探究某矿石可能是由FeCO 3 、SiO 2 、Al 2 O 3 中的一种或几种组成,探究过程如下图所示。(已知:碳酸
欲探究某矿石可能是由FeCO 3 、SiO 2 、Al 2 O 3 中的一种或几种组成,探究过程如下图所示。(已知:碳酸不能溶解Al(OH) 3 沉淀)
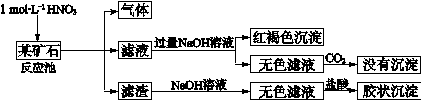
(1)用滤渣制备粗硅的化学反应方程式为
(2)下列说法正确的是
a.酸性:H 2 CO 3 >H 2 SiO 3 b.结合质子的能力:CO> AlO 2 - >HCO 3 -
c.稳定性:H 2 O>CH 4 >SiH 4 d.离子半径:O 2 - <Al 3+
(3)滤渣和NaOH溶液反应的离子方程式是
通过 现象说明此矿山中不含Al 2 O 3
(4)该矿石和稀HNO 3 发生氧化还原反应的离子方程式为
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O 2 混合循环通入反应池中,主要两个目的是 , ;
若处理该矿石2.36×10 3 kg,得到滤渣1.2×10 3 kg ,理论上至少需要1 mol L - 1 HNO 3 的体积为 L。 1314-Crystal1年前1
1314-Crystal1年前1 -
 marym2 共回答了18个问题
marym2 共回答了18个问题 |采纳率83.3%1年前查看全部
- 甲醛和氢氧化铜反应被氧化为甲酸还是碳酸,为什么和氢氧化铜产生5水1c02
 hjj19871年前3
hjj19871年前3 -
 3kgytrj3 共回答了15个问题
3kgytrj3 共回答了15个问题 |采纳率93.3%因为形成的甲酸里面也相当于有醛基,也要和氢氧化铜反应的.先是甲醛和氢氧化铜以1:2反应 HCHO+2Cu(OH)2== HCOOH+Cu2O(沉淀) +2H2O再接下来HCOOH中的醛基又要和氢氧化铜反应HCOOH+2Cu(OH)2==H2CO3+Cu2O(沉淀) +2H2O两个方程式相加就是HCHO + 4Cu(OH)2 →2Cu2O + CO2 + 5H20两个方程式都是正确的1年前查看全部
- “碳酸”和“硅酸”哪个更容易挥发?
“碳酸”和“硅酸”哪个更容易挥发?
有一个化学方程式是“二氧化硅和碳酸钠在高温下反应生成硅酸钠和二氧化碳”,那么通过这个方程式怎么解释“难挥发性酸制挥发性酸”呢?
谢谢大家~
 gxlinxiang1年前1
gxlinxiang1年前1 -
 sxs3 共回答了16个问题
sxs3 共回答了16个问题 |采纳率87.5%硅酸是固体酸.硅酸(H2SiO3)可以写成SiO2.H2O(注意:H2O不是结晶水).这样就可以解释了.1年前查看全部
- 比较一下醋酸,苯酚,氰氢酸碳酸,碳酸氢根,ALO2-的酸性强弱,我只要这几种酸的强弱
 liesbeth1年前1
liesbeth1年前1 -
 等你oo 共回答了22个问题
等你oo 共回答了22个问题 |采纳率86.4%从强到弱:醋酸,碳酸,氢氰酸,苯酚,碳酸氢根,AlO2-
弱酸酸性由强到弱为:草酸,亚硫酸,磷酸,亚硝酸,氢氟酸,甲酸,乳酸,苯甲酸,乙酸,丙酸,硬脂酸,碳酸,氢硫酸,次氯酸,硼酸,硅酸1年前查看全部
- 下列说法不正确的是( )A.四碳酸、五碳糖、六碳糖等都是多糖B.蔗糖、麦芽糖是植物体内含有的重要二糖C.糖原、淀粉分别
下列说法不正确的是( )
A.四碳酸、五碳糖、六碳糖等都是多糖
B.蔗糖、麦芽糖是植物体内含有的重要二糖
C.糖原、淀粉分别是动植物内含有的贮存能量的多糖
D.纤维素是植物体内的多糖 lsynqj1年前1
lsynqj1年前1 -
 linguwu 共回答了19个问题
linguwu 共回答了19个问题 |采纳率84.2%解题思路:糖类可以分为单糖、二糖和多糖,单糖包括葡萄糖、果糖、半乳糖、核糖和脱氧核糖,其中葡萄糖是生命活动所需的主要能源物质,核糖与脱氧核糖是构成核酸的成分,多糖主要包括淀粉、纤维素和糖原,淀粉是植物体内的主要储能物质,纤维素是构成细胞壁的主要成分,糖原是动物细胞内的储能物质,分为肝糖原和肌糖原.据此分析解答.A、多糖是由多个单糖聚合而成的糖,而不是看碳原子的数量,葡萄糖是六碳糖,但是葡萄糖属于单糖,A错误;
B、蔗糖和麦芽糖是植物细胞中的二糖,B正确;
C、糖原、淀粉分别是动植物内含有的贮存能量的多糖,C正确;
D、纤维素是植物体内的多糖,主要作用是用来形成植物细胞壁,D正确.
故选:A.点评:
本题考点: 糖类的种类及其分布和功能.
考点点评: 此题主要考查糖类的种类以及分布和功能等知识,意在考查学生对基础知识的理解掌握,难度适中.1年前查看全部
- SiO2对应水化合物酸性比碳酸强吗?
 神秘的地球1年前3
神秘的地球1年前3 -
 我家在哪 共回答了20个问题
我家在哪 共回答了20个问题 |采纳率95%比碳酸弱.从这个方程式就能看出:NaSiO3+CO2+H2O=Na2CO3+H2SiO31年前查看全部
- 用化学方程式证明次氯酸酸性比碳酸弱
 hfwyf1年前1
hfwyf1年前1 -
 gzliheng 共回答了18个问题
gzliheng 共回答了18个问题 |采纳率72.2%2NaClO + H2CO3 == Na2CO3 + 2HClO1年前查看全部
- 甲烷、氨气、溴化氢、碘化氢、硝酸、碳酸、磷酸、亚硫酸的化学式是什么?
 断刀流水11151年前1
断刀流水11151年前1 -
 烁远 共回答了17个问题
烁远 共回答了17个问题 |采纳率100%CH4,NH3,BrH,IH,HNO3,H2CO3,H3PO4,H2SO31年前查看全部
- 同一浓度的乙酸和碳酸,哪一个的PH值大?为什么?
 niefers1年前2
niefers1年前2 -
 zhuxiaosheng 共回答了21个问题
zhuxiaosheng 共回答了21个问题 |采纳率81%碳酸的大;因为碳酸根离子的酸性小于醋酸根离子,所以水解程度小,pH大.1年前查看全部
- 为什么二氧化碳通入NaALO2溶液中,过量时是生成碳酸氢更离子,碳酸的电离,对产物有什么影响?
 轻风雨1年前1
轻风雨1年前1 -
 kxiaokk 共回答了24个问题
kxiaokk 共回答了24个问题 |采纳率87.5%二氧化碳能与碳酸根离子、水反应生成碳酸氢根离子.(注意“过量”)
碳酸钠的碱性强于碳酸氢钠,二氧化碳通入水显酸性,
所以生成的是碱性小的产物,即碳酸氢钠
不管是不是偏铝酸钠,过量二氧化碳都是生成碳酸氢根离子.
促进反应的进行啊,这是离子反应,电离程度越高越好啊!1年前查看全部
- 醋酸亚铜与碳酸钠反应生成的黄色物质是碳酸亚铜吗?2CH3COOCu+Na2CO3=Cu2CO3
醋酸亚铜与碳酸钠反应生成的黄色物质是碳酸亚铜吗?2CH3COOCu+Na2CO3=Cu2CO3
2CH3COONa 10007121年前1
10007121年前1 -
 临渊之石 共回答了15个问题
临渊之石 共回答了15个问题 |采纳率86.7%应该是氧化亚铜吧!你可以过滤出来,加完全看看是不是冒气泡1年前查看全部
- 下列物质中属于有机酸的酸是?A.碳酸B.足球烯C.醋酸D.酒精为什么是不是碳酸
 葵花公公1年前3
葵花公公1年前3 -
 云滔天 共回答了22个问题
云滔天 共回答了22个问题 |采纳率95.5%所谓有机物通常指含碳元素的化合物,或碳氢化合物及其衍生物总称为有机物.因此醋酸算作有机酸.而无机物是无机化合物的简称,通常指不含碳元素的化合物.少数含碳的化合物,如一氧化碳、二氧化碳、碳酸盐、氰化物等也属于无机物.无机物大致可分为氧化物、酸、碱、盐等.由于碳酸是由二氧化碳溶于水形成的,因此碳酸算作无机酸.1年前查看全部
- 比较下列物质的酸性次氯酸 氢硫酸 碳酸 硅酸 乙酸 氢碘酸 氢溴酸
 swinfo1年前3
swinfo1年前3 -
 gigilau 共回答了26个问题
gigilau 共回答了26个问题 |采纳率92.3%氢碘酸 氢溴酸 乙酸 碳酸 氢硫酸 次氯酸 硅酸 (强到弱)
高氯酸,氢碘酸,硫酸,氢溴酸,盐酸,硝酸,碘酸(以上为强酸,了解即可,大学涉及强弱排序),草酸(乙二酸),亚硫酸,磷酸,丙酮酸,亚硝酸(以上五种为中强酸),柠檬酸,氢氟酸,苹果酸,葡萄糖酸,甲酸,乳酸,苯甲酸,丙烯酸,乙酸,丙酸,硬脂酸,碳酸,氢硫酸,次氯酸,硼酸,硅酸,苯酚
以上强到弱,有时间看看、背背.1年前查看全部
- 植物栽培在适宜的条件下,如果将环境中CO2含量突然降至极低水平,此时叶肉细胞内的三碳酸,五碳糖和ATP含量的变化情况依次
植物栽培在适宜的条件下,如果将环境中CO2含量突然降至极低水平,此时叶肉细胞内的三碳酸,五碳糖和ATP含量的变化情况依次是 A.上升;下降;上升 B.上升;下降;下降 C.下降;上升;上升 D.下降;上升;下降
ATP不是应该下降吗?ADP增多呀 shawn811年前4
shawn811年前4 -
 destroymee 共回答了19个问题
destroymee 共回答了19个问题 |采纳率78.9%三碳糖下降,五碳糖上升,ATP上升.
因此选C
因为五碳糖结合二氧化碳生成三碳糖,产生三碳糖后需要消耗ATP.因此,二氧化碳减少后,五碳糖没有结合的物质了,因此上升,三碳糖不再产生而减少,ATP由于缺少三碳糖,因此消耗量减少,总量上升.1年前查看全部
大家在问
- 1用英文表达2008年九月是 Sept.2008 还是 Sept,2008
- 2今天风和日丽用英语怎么说
- 31,已知f(x)=(3a-1)x+4a,x=1是(-∞,+∞)上的减函数,那么a的取值范围?
- 4一块长60宽24高5公分轻体砖的重量是多少
- 5如图,将两张等宽的长方形纸条交叉叠放重叠部分是一个四边形ABCD,若AD=2cm,∠ABC=45º,则四边形A
- 6温度计夹多长时间最标准十分钟还是五分钟测量的最准,体温计
- 7英语翻译explain in more details about density2.include what meas
- 8occur,happen,take place,hold的区别
- 9THREE+THREE+FOUR=ELEVEN
- 10一个重量为10N的物体,在15N的水平拉力的作用下,一次在光滑水平面上移动0.5m,另一次在粗糙水平面上移动相同的距离,
- 11窗户朝南的那个房间是我的 翻译成英语怎么翻译 The room ___window faces to _____ ___
- 12Someone___all the cakes.I will go to buy some more. will eat
- 13明明家里来了两位小客人,妈妈冲了800ML果汁.如果用右图中的玻璃杯喝果汁,明明和客人每人一杯够吗?
- 14y=sinarccos2/∏(pai)这个式子怎么化解?
- 1526.Imagine that you are a angel..