卤水炒糖色是每次卤之前都要炒,还是炒一次可以用很久?
 人生无意义啊2022-10-04 11:39:541条回答
人生无意义啊2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 zhuyaol841026 共回答了16个问题
zhuyaol841026 共回答了16个问题 |采纳率81.3%- 炒一次可以用很久,卤水嘛,越老越好.
- 1年前
相关推荐
- 晒盐后的卤水中加生石灰反应方程式
 long880078201年前2
long880078201年前2 -
 吃一钱长一智 共回答了20个问题
吃一钱长一智 共回答了20个问题 |采纳率85%有两个
CaO + H2O == Ca(OH)2
Ca(OH)2 + MgCl2 == Mg(OH)2↓ + CaCl2
最好不要合并起来写1年前查看全部
- 在含溴卤水中吹入空气可将的溴,这是利用了溴的什么性质
 pengxixi_19801年前1
pengxixi_19801年前1 -
 wwse 共回答了27个问题
wwse 共回答了27个问题 |采纳率85.2%利用溴的易挥发性1年前查看全部
- 海洋资源开发前景广阔.海水晒盐能够得到粗盐和卤水,卤水中含有MgCl 2 、KCl和MgSO 4 等物质,如图是它们的溶
海洋资源开发前景广阔.海水晒盐能够得到粗盐和卤水,卤水中含有MgCl 2 、KCl和MgSO 4 等物质,如图是它们的溶解度曲线.下列说法不正确的是( )

A.t 1 ℃时,三种物质的饱和溶液中,溶质质量分数最大的是MgCl 2 B.t 1 ℃时,分别在100g水中溶解了等质量的MgCl 2 、KCl,两溶液都可达到饱和 C.t 2 ℃时,KCl和MgSO 4 两种物质的溶解度相同 D.将t 2 ℃时的三种物质的饱和溶液降低到t 1 ℃时,均能析出晶体  任林1年前1
任林1年前1 -
 jianxuewaner 共回答了17个问题
jianxuewaner 共回答了17个问题 |采纳率94.1%B
1年前查看全部
- 用海水制盐,分离出食盐后的卤水主要有什么物质
 雌狗1年前2
雌狗1年前2 -
 飞刀td7ewqj大侠 共回答了20个问题
飞刀td7ewqj大侠 共回答了20个问题 |采纳率95%盐类含量大于5%的液态矿产.聚集于地表的称表卤水或湖卤水.聚集于地面以下者称地下卤水.与石油聚集一起的称石油卤水.
按地下卤水赋存条件有孔隙卤水、晶间卤水、裂隙卤水.按卤水的水力性质分潜卤水、承压卤水.
卤水中,常含有K+、Na+、Ca2+、Mg2+、Cl-、SO2-、CO2-、HCO3-、B、Li、Br、I、Sr、Rb、Cs等离子.
按卤水的水化学性质,分为氯化物型卤水、硫酸盐型卤水、碳酸盐型卤水.
评价卤水矿床时,应详细研究卤水的赋存状态、水力学性质,划分其水化学类型.1年前查看全部
- 英语翻译最近在写桂林菜的介绍,谁知道桂林米粉的卤水 用英语怎么说呀
 scorpio91年前1
scorpio91年前1 -
 sandy_520 共回答了18个问题
sandy_520 共回答了18个问题 |采纳率88.9%1 .bittern 气象学专业词汇 英语 翻译...刺骨寒风 biting wind 卤汁 bittern 双波状云 bi-undulatus ...www.***.com/vocabulary/ pages2/235_66_10 ...- 搜索相关网页 - 基于5个网页 2 .soppings 【食品词典】S9 ...sophorose槐二糖;α-葡糖-β-葡糖苷 soppings 浇汁; 卤汁 sopressata 用猪结肠为肠衣的香肠;意大利式大香肠 ...www.***.cn/html/spcyzywzd/ 130950166.html - 搜索相关网页 - 基于6个网页 3 .Master stock 中文:滷水; 卤汁 英语:Master stock en.wikipedia.org/wiki/Master stock - 搜索相关网页 - 基于21个网页 卤汁缸 :gravy bowl 浸卤汁 :marinate 卤汁饭 :mulled rice 腊肉西芹卤汁面 :Noodles with Preserved Pork and Celery | Noodles with Preserved Ham and Celery 鱼酱析出的卤汁 :patis (意式)卤汁面条 :lasagna 鱼酱析出的卤汁〔缅甸 :ngam-pya-ye 把...浸泡在卤汁中 :marinate1年前查看全部
- (6分)海洋中有丰富的水生生物和化学资源。海水晒盐后,以其母液(卤水)和贝壳为原料,还可生产具有特殊用途的材料——纳米氧
(6分)海洋中有丰富的水生生物和化学资源。海水晒盐后,以其母液(卤水)和贝壳为原料,还可生产具有特殊用途的材料——纳米氧化镁,其简要流程如下:

(1)海水晒盐是_____________(填“物理”或“化学”)变化,包含蒸发、_________等过程。(2)写出食盐的一种用途:____________。(3)A步骤反应的化学方程式是_____________。(4)实验室进行a操作时,需要的玻璃仪器有烧杯、漏斗、_______________。 荫下跃跃1年前1
荫下跃跃1年前1 -
 恋芝风雪 共回答了23个问题
恋芝风雪 共回答了23个问题 |采纳率78.3%(1)物理,结晶(2)做调味品(3)CaCO 3 CaO+CO 2 ↑(4)玻璃棒 根据流程结合已有的知识进行分析,海水晒盐没有生成新的物质,属于物理变化,该过程包含水的蒸发和食盐的结晶;食盐具有咸味,能用...1年前查看全部
- (2011•广州)从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl2、NaCl、KCl的混合液)转化为氯化镁晶体.
(2011•广州)从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl2、NaCl、KCl的混合液)转化为氯化镁晶体.实验室中模拟该转化的过程如下,回答有关问题a
(1)制备氢氧化镁:向卤水中加入适量生石灰(CaO),充分反应后过滤.
①该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)______
②过滤操作需用到的玻璃仪器除烧杯外,还有______.
(2)制备氯化镁溶液:用盐酸溶解Mg(OH)2.为了便于后续操作.盐酸不宜过量.
①反应的化学方程式是______.
②通过计算,可准确知道所需盐酸的量.理论上溶解5.8gMg(OH)2需要36.5%HCl溶液______g
③由于准确称量Mg(OH)2的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到到控制盐酸用量的目的.操作是:将Mg(OH)2加入烧杯中,______直到Mg(OH)2完全溶解为止.
(3)制备氯化镁晶体:蒸发浓缩MgCl2溶液,冷却结晶. fzhcg8881年前1
fzhcg8881年前1 -
 蓝锋 共回答了13个问题
蓝锋 共回答了13个问题 |采纳率84.6%解题思路:(1)氧化钙能和水反应生成氢氧化钙,同时放出大量的热;过滤操作需用到的玻璃仪器有烧杯、玻璃棒、漏斗;
(2)盐酸和氢氧化镁反应能生成氯化镁和水;根据化学方程式可以进行相关方面的计算;可以控制稀盐酸的用量,从而达到恰好完全反应的目的.(1)①氧化钙和水反应能够放出大量的热,反应的化学方程式为:CaO+H2O=Ca(OH)2.
②过滤操作需用到的玻璃仪器除烧杯外,还有漏斗、玻璃棒.故填:漏斗、玻璃棒.
(2)①盐酸和氢氧化镁反应的化学方程式是:Mg(OH)2+2HCl=MgCl2+2H2O.
②解设溶解5.8gMg(OH)2需要氯化氢的质量为X.
Mg(OH)2+2HCl=MgCl2+2H2O
58 73
5.8g X
[58/73=
5.8g
X]
X=7.3g
需要36.5%HCl溶液的质量为:7.3g÷36.5%=20g.
答:需要36.5%HCl溶液的质量为20g.
③操作是:将Mg(OH)2加入烧杯中,用胶头滴管逐滴加入稀盐酸溶液直到Mg(OH)2完全溶解为止.故填:用胶头滴管逐滴加入稀盐酸溶液.点评:
本题考点: 对海洋资源的合理开发与利用;过滤的原理、方法及其应用;生石灰的性质与用途;酸的化学性质;碱的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法,理解过滤操作,能够根据化学方程式进行相关方面的计算.1年前查看全部
- 英语翻译冷冻法快速通过新立西风井第四纪砾砂富含卤水层的工程实践 (山东黄金集团三山岛金矿;山东莱州三山岛街道办事处261
英语翻译
冷冻法快速通过新立西风井第四纪砾砂富含卤水层的工程实践
(山东黄金集团三山岛金矿;山东莱州三山岛街道办事处261442)
摘要:在三山岛金矿新立矿区西风井的施工中.通过多开盐水泵,增加盐水循环速度;通过增加冻结孔个数,降低冷冻孔间距;通过增加盐水浓度,把盐水温度降低到凝固临界点等措施,顺利的通过了都第四纪砾砂富含卤水层.它为工程地质和水文地质条件类似的工程,提供了宝贵的经验,并值得条件类似的矿山借鉴. brainyo1181年前1
brainyo1181年前1 -
 是我蓝色雨 共回答了26个问题
是我蓝色雨 共回答了26个问题 |采纳率100%Rapid frozen through the legislation of the new wells west Quaternary gravel layer of sand-rich brine engineering practice
Shandong Gold Group Sanshandao Gold; Sanshandao streets of the Office of Laizhou in Shandong 261442) Abstract:Sanshandao gold mine west of the new legislation in the construction of wells.Through the open salt water,saline to increase the speed of the cycle; by increasing the number of holes to freeze,reduce the frozen-hole pitch;By increasing the concentration of salt water,salt solidification temperature down to a critical point,and other measures to smooth the passage of both the Quaternary sand gravel-rich brine layer.It works for the geological and hydro-geological conditions similar projects provided valuable experience and should be similar to the conditions of the mine from.1年前查看全部
- 快!怎样确定卤水中的氧化镁已经全部转化为沉淀?
 jack-ww1年前1
jack-ww1年前1 -
 ivoire 共回答了21个问题
ivoire 共回答了21个问题 |采纳率95.2%往上层清水中加入NaOH,不见沉淀1年前查看全部
- 一道化学题(3)晒盐后得到的母液(又称卤水)中含有氯化镁(MgCl2)、硫酸镁(MgSO4)和氯化钾(KCl)等物质。参
一道化学题
(3)晒盐后得到的母液(又称卤水)中含有氯化镁(MgCl2)、硫酸镁(MgSO4)和氯化钾(KCl)等物质。参照右图各物质的溶解度曲线。从卤水中提取氯化钾晶体采用下列方法:
①将卤水加热到60℃以上蒸发水分就会逐渐析出_________(填名称)晶体,理由是_________。
②将①中的晶体过滤后,得到滤液,把滤液降温到30℃以下,又析出氯化钾晶体和氯化镁晶体,然后用少量的______(填热水,冷水)洗涤两晶体的混合物,就可以得到较纯的氯化钾晶体。
告诉我答案 并说明为啥 谢谢啦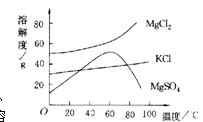
 kcwjq1年前4
kcwjq1年前4 -
 jamesyy 共回答了23个问题
jamesyy 共回答了23个问题 |采纳率87%①硫酸镁
理由:温度高于60℃时,硫酸镁溶解度较小
②冷水
理由:低于30℃时,氯化镁的溶解度大于氯化钾的溶解度1年前查看全部
- 英语翻译毛角豆、叫头、毛条牛肉、五香麻辣鸡、卤水耳片、蒜泥荷兰豆、葱油西兰花、南溪(地名)豆腐干、山塔菌炖乳鸽、法式鹅肝
英语翻译
毛角豆、叫头、毛条牛肉、五香麻辣鸡、卤水耳片、蒜泥荷兰豆、葱油西兰花、南溪(地名)豆腐干、山塔菌炖乳鸽、法式鹅肝扒芦笋、蜀南葫芦竹荪、明珠大河江团、培根鲜菜卷、芦笋炒鲜舌、五粮液烧白、宝尖烧鸡、蔬菜豆花、箱箱豆腐、特制松茸刺参捞饭、宜宾燃面、珍珠鸭儿耙、南瓜绿豆汤、珍珠醪糟、风味豆腐脑、水果拼盘. ggtf1年前2
ggtf1年前2 -
 beanbeanfish 共回答了14个问题
beanbeanfish 共回答了14个问题 |采纳率92.9%Mao Jiadou,is called,the wooltop beef,the five spices hot chicken,west the bittern ear piece,the crushed garlic peas,the onion oil the orchid,Nanxi (geographic name) the dried beancurd,Shan Tajun to cook the young pigeon,the Buddhist ritual procedures foie gras digs up south the bamboo shoots,Suchuan the bottle gourd dictyophora phalloidea,pearl river Jiang Tuan,the Bacon fresh vegetables volume,the bamboo shoots fries the fresh tongue,Wuliangye burns,the valuable sharp roast chicken,the vegetables legume flower,the box box bean curd,the specially made pine mushroom trepang white fishes the food,Ipin burns the surface,the pearl duck rake,the pumpkin mung bean soup,the pearl glutinous rice wine,the flavor bean curd brain,the fruit hors d'oeuvre.1年前查看全部
- 从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl 2 、NaCl、KCl的混合液)转化为氯化镁晶体。实验室中模拟该
从海水中可以提取镁,其中的一个步骤是将卤水(含MgCl 2 、NaCl、KCl的混合液)转化为氯化镁晶体。实验室中模拟该转化的过程如下,回答有关问题:
(1)制备氢氧化镁:向卤水中加入适量生石灰(CaO),充分反应后过滤。
①该过程中发生了多个反应,其中会大量放热的反应是(填化学方程式)_________________。
②过滤操作需用到的玻璃仪器除烧杯外,还有_____________。
(2)制各氯化镁溶液:用盐酸溶解Mg(OH) 2 。为了便于后续操作,盐酸不宜过量。
①反应的化学方程式是____________________。
②通过计算,可准确知道所需盐酸的量。理论上溶解5.8gMg(OH) 2 需要36.5%HCl溶液______g。
③由于准确称量Mg(OH) 2 的步骤繁琐,实验中并不常用,而是通过一定操作方法来达到到控制盐酸用量的目的。操作是:将Mg(OH) 2 加入烧杯中,_____________________直到Mg(OH) 2 完全溶解为止。
(3)制各氯化镁晶体:蒸发浓缩MgCl 2 溶液,冷却结晶。 灰人-风1年前1
灰人-风1年前1 -
 老格粉丝 共回答了16个问题
老格粉丝 共回答了16个问题 |采纳率93.8%⑴①CaO+H 2 O==Ca(OH) 2
②漏斗、玻璃棒
⑵①2HCl+Mg(OH) 2 ==MgCl 2 +2H 2 O
②20
③用胶头滴管逐滴加入稀盐酸溶液1年前查看全部
- 9.用酸性氢氧燃料电池电解苦卤水(含Cl—、Br—、Na+、Mg2+)的装置如图所示(a、b为 石墨电极)下列说法
9.用酸性氢氧燃料电池电解苦卤水(含Cl—、Br—、Na+、Mg2+)的装置如图所示(a、b为 石墨电极)下列说法
正确的是x05x05x05( )
x05A.电池工作时,正极反应式为:O2+2H2O+4e—=4OH—
x05B.电解时,a电极周围首先放电的是Cl—而不是OH—,说明当其它条件相同时前者的还
原型强于后者
x05C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
x05D.忽略能量耗损,当电池中消耗0.02gH2时,b极周围会产生0.02gH2
错的选项错在哪里了(此题是单选)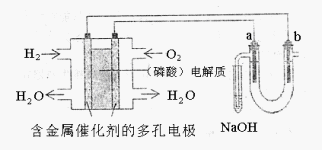
 Yuva1年前1
Yuva1年前1 -
 hao3626 共回答了16个问题
hao3626 共回答了16个问题 |采纳率87.5%选C
A项:完全错误.原电池负极失电子,且因为电解液为酸性电解液,故反应应为:
正极:H2-2e^-=2H^+
负极:O2+4e^-+4H^+=2H2O
B项:因为电池左为负极右为正极,故相应的a为阴极b为阳极.又因为电解池阳极失电子,故Cl^-应在b放电.
D项:数据显然错.1年前查看全部
- 卤水和石膏可以使带何种电荷的胶体粒子聚沉?
卤水和石膏可以使带何种电荷的胶体粒子聚沉?
有一种胶体,加入卤水或石膏会聚沉,加入氯化钠或硫酸钠不聚沉,此胶体带什么电荷?
可以给出理由吗? fwm88661年前1
fwm88661年前1 -
 anemia 共回答了20个问题
anemia 共回答了20个问题 |采纳率80%负电荷
因为两次加的都含有氯离子和硫酸根,但结果不一样.所以是阳离子的影响.
即钠离子聚沉性能没有钠离子等强1年前查看全部
- 下列关于海水提取镁盐来制取镁的过程中,叙述正确的是( ) A.直接蒸发海水得到氯化镁 B.将石灰乳加入海水或卤水中沉淀
下列关于海水提取镁盐来制取镁的过程中,叙述正确的是( ) A.直接蒸发海水得到氯化镁 B.将石灰乳加入海水或卤水中沉淀出氢氧化镁 C.电解氯化镁溶液 D.利用钠将氯化镁中的镁置换出来  ijustwannatry1年前1
ijustwannatry1年前1 -
 no2xt 共回答了30个问题
no2xt 共回答了30个问题 |采纳率90%A、因为海水中主要是NaCl,而MgCl 2 的含量较少,若直接蒸馏海水得到的主要是NaCl,而不是MgCl 2 ,故A错误;
B、将石灰乳加入海水或卤水中,石灰乳即Ca(OH) 2 与MgCl 2 反应生成Mg(OH) 2 沉淀,故B正确;
C、电解氯化镁溶液不会得到镁,电解熔融的氯化镁才会得到镁,故C错误;
D、虽然在金属活动顺序表中,钠在镁的前边,但钠不会从氯化镁溶液中把镁置换出来,故D错误.
故选B1年前查看全部
- 海水 结晶顺序 海水经过光晒蒸发后最先有NaCl结晶析出 然后剩下的卤水经过蒸发后形成卤块也叫卤粉 但不知道后来形成的卤
海水 结晶顺序
海水经过光晒蒸发后最先有NaCl结晶析出 然后剩下的卤水经过蒸发后形成卤块也叫卤粉 但不知道后来形成的卤粉的化学成分 谁知道说一下 bill_yang1年前2
bill_yang1年前2 -
 qqhbz 共回答了19个问题
qqhbz 共回答了19个问题 |采纳率84.2%主要成分为氯化镁,除此之外含有少量氯化钠、氯化钾、硫酸钠、碳酸钠、硫酸镁等杂质!1年前查看全部
- 海水晒盐能够得到粗盐和卤水。卤水中含有MgCl 2 、KCl和MgSO 4 等物质,如图是它们的溶解度曲线,完成下列填空
海水晒盐能够得到粗盐和卤水。卤水中含有MgCl 2 、KCl和MgSO 4 等物质,如图是它们的溶解度曲线,完成下列填空。

(1)在t 1 ℃时,向100g水中加入150g MgCl 2 ,形成 (填“饱和”或“不饱和”)溶液,将其温度升高到t 2 ℃时,此时溶液中溶质的质量分数为 。
(2)t 1 ℃时,MgCl 2 、KCl和MgSO 4 三种物质的饱和溶液中,溶质质量分数最大的是 。将t 2 ℃时MgCl 2 、KCl和MgSO 4 三种物质的饱和溶液降温至t 1 ℃时,可能会析出的晶体有 (填字母序号)。
A.MgCl 2 和KCl B.只有MgSO 4 C.MgCl 2 、KCl和MgSO 4 peggylau1年前1
peggylau1年前1 -
 心空了 共回答了18个问题
心空了 共回答了18个问题 |采纳率88.9%(1)饱和;50%;(2)MgCl 2 ;C
1年前查看全部
- 管道阻力损失离心泵流量是245立方米每小时,扬程67m,安装高度3米,输送密度1.21的卤水,管道上有9个弯头,请问不算
管道阻力损失
离心泵流量是245立方米每小时,扬程67m,安装高度3米,输送密度1.21的卤水,管道上有9个弯头,请问不算管道阻力,只计算弯头压力损失是多少?进口压力和出口压力损失了多少? wdmm1年前1
wdmm1年前1 -
 Fzhe2001 共回答了25个问题
Fzhe2001 共回答了25个问题 |采纳率92%你给的数据不全 ,按照我的步骤去自己算下吧:
1.由流量Q=VA,A是界面姐,V是水流速度计算出速度.
2.看看你的弯头是什么的,45°?90°弯头?然后查出弯头局部损失系数f,百度下就可以出来.
3.按照公式h=f*V^2/2g,g是重力加速度,得到压损高度h.
4.P=pgh,p是密度,就可以直道压力损失了.1年前查看全部
- (2014•黄浦区三模)海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
 (2014•黄浦区三模)海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
(2014•黄浦区三模)海洋是地球上最大的储水库,蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.
①卤水中含有MgCl2、KCl和MgSO4等物质,如图是三种物质的溶解度曲线.t2℃时,三种物质的饱和溶液中,溶质质量分数最小的是______.
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,仍然为饱和溶液的是______.
③将饱和氯化镁溶液由t3℃冷却至t1℃,下列四种叙述中,正确的是______(填序号).
Ⅰ.溶液的质量不变Ⅱ.氯化镁的溶解度变小
Ⅲ.溶液中溶质质量不变Ⅳ.溶液中溶质质量分数变小
④在t3℃时,60克KCl的饱和溶液与60克MgCl2的饱和溶液中,溶质MgCl2与KCl的质量比为3:1,则t3℃时MgCl2的溶解度为______. 骆世琼1年前1
骆世琼1年前1 -
 erinjiji 共回答了19个问题
erinjiji 共回答了19个问题 |采纳率94.7%①据图可以看出,t2℃时,氯化钾的溶解度最小,三种物质的饱和溶液中,溶质质量分数最小的是氯化钾,故填:KCl;
②将t2℃时三种物质的饱和溶液加热到t3℃以上时,温度高于t3℃,硫酸镁的溶解度减小,故仍然为饱和溶液的是硫酸镁,故填:MgSO4;
③Ⅰ.氯化镁的溶解度随温度而增大,故降温会析出晶体,溶液的质量减小,错误;
Ⅱ.氯化镁的溶解度随温度而增大,故降温氯化镁的溶解度变小,正确;
Ⅲ.氯化镁的溶解度随温度而增大,故降温会析出晶体,溶液中溶质质量减小,错误;
Ⅳ.氯化镁的溶解度随温度而增大,故降温会析出晶体,溶剂质量不变,溶液中溶质质量分数变小,正确;
故填:II、IV;
④在t3℃时,氯化钾的溶解度为20g,故60克KCl的饱和溶液中含有氯化钾的质量为:
20g
120g×60g=10g,60克KCl的饱和溶液与60克MgCl2的饱和溶液中,溶质MgCl2与KCl的质量比为3:1,t3℃时60g氯化镁饱和溶液中含有MgCl2的质量为3×10g=30g,t3℃时MgCl2的溶解度为
30g
30g×100g=100g,故填:100g.1年前查看全部
- 卤水点豆腐是不是蛋白质的盐析?卤水是什么物质呢?
 oydqifgp1年前1
oydqifgp1年前1 -
 王小88 共回答了18个问题
王小88 共回答了18个问题 |采纳率88.9%不是盐析.
盐析是“加入无机盐使某些溶质析出的过程”.如制肥皂过程中的盐析和蛋白质的盐析.而卤水点豆腐是蛋白质的凝聚,反应过程中溶质并没有析出,而是跟溶剂结合在一起形成了凝胶.1年前查看全部
- (2011•山东)实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和B
(2011•山东)实验室以含有Ca2+、Mg2+、Cl-、SO42-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如下:
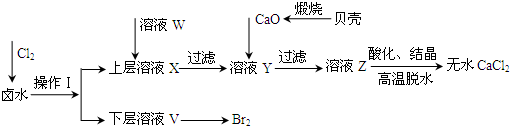
(1)操作Ⅰ使用的试剂是______,所用的主要仪器名称是______.
(2)加入溶液W的目的是______.用CaO调节溶液Y的pH,可以除去Mg2+.由表中数据可知,理论上可选择的pH最大范围是______.酸化溶液Z时,使用的试剂为______.
(3)实验室用贝壳与稀盐酸反应制备并收集气体,下列装置中合理的是______.开始沉淀时的pH 沉淀完全时的pH Mg2+ 9.6 11.0 Ca2+ 12.2 c(OH-)=1.8mol•L-1 
(4)常温下,H2SO3的电离常数Ka1=1.2×10-2,Ka2=6.3×10-8;H2CO3的电离常数Ka1=4.5×10-7,Ka2=4.7×10-11.某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3.该实验设计不正确,错误在于______.
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论).______.
仪器自选.
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸. 一天一笑1年前1
一天一笑1年前1 -
 anywayway 共回答了25个问题
anywayway 共回答了25个问题 |采纳率80%解题思路:实验室以含有Ca2+、Mg2+、Cl-、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,应将混合物中的Mg2+、SO42-、Br-等离子除去,根据流程可以看出分别加入氯气将溶液中的Br-氧化溴单质,加入氯化钡除去SO42-,用CaO调节溶液Y的pH,可以除去Mg2+.
(1)单质溴极易溶于有机溶剂,所以可以采用萃取的方法,萃取的主要仪器是分液漏斗;
(2)分析表中数据可知pH大于11时Mg2+沉淀完全,pH大于12.2时,Ca2+开始沉淀,所以理论上可选择pH最大范围是11.0≤pH<12.2;除杂时不能引入新的杂质;
(3)CO2的密度大于空气中的,所以采用向上排空气发收集CO2气体.若采用长颈漏斗时,长颈漏斗的下端必需插入到溶液中,以防止CO2气体从长颈漏斗中挥发出来;
(4)H2SO3和H2CO3均属于二元酸,要想通过比较二者的pH来验证二者的酸性强弱,必需使二者的浓度相同,但是SO2和CO2气体溶于水后的饱和溶液其浓度显然不相等(因为二者的溶解度不同),所以该实验设计不正确;要检验酸性强弱,可以采用多种方法,例如利用水解原理(酸越弱相应的强碱盐就越易水解),也可以利用较强的酸制取较弱的酸来检验.(1)氯气具有强氧化性,通入氯气后可以将溶液中的Br-氧化溴单质,因为单质溴极易溶于有机溶剂,所以可以采用萃取的方法,萃取的主要仪器是分液漏斗.由流程图可知单质溴在下层,因此该有机溶剂的密度要比水的大且不溶于水,所以该试剂是CCl4,故答案为:四氯化碳;分液漏斗;
(2)由于SO42-会与Ca2+结合形成微溶性的硫酸钙而影响氯化钙的制备,因此必需除去;由表中数据可知pH大于11时Mg2+沉淀完全,pH大于12.2时,Ca2+开始沉淀,所以理论上可选择pH最大范围是11.0≤pH<12.2;因为不能引入新的杂质,所以酸化溶液Z时,使用的试剂应该为盐酸,故答案为:除去溶液中的SO42-;11.0≤pH<12.2;盐酸;
(3)实验室制取CO2的特点是固体和液体反应且不需要加热,由于盐酸易挥发,因此在收集之前需要出去挥发出HCl气体,因为CO2的密度大于空气中的,所以采用向上排空气发收集CO2气体.若采用长颈漏斗时,长颈漏斗的下端必须插入到溶液中,以防止CO2气体从长颈漏斗中挥发出来,因此选项b、d正确,故答案为:b、d;
(4)H2SO3和H2CO3均属于二元酸,要想通过比较二者的pH来验证二者的酸性强弱,必需使二者的浓度相同,但是SO2和CO2气体溶于水后的饱和溶液其浓度显然不相等(因为二者的溶解度不同),所以该实验设计不正确;要检验酸性强弱,可以采用多种方法,例如利用水解原理(酸越弱相应的强碱盐就越易水解),也可以利用较强的酸制取较弱的酸来检验.由于SO2和CO2气体均可以使饱和石灰水变混浊,所以CO2气体在通入饱和石灰水之前必需除去CO2气体中混有的SO2气体,故答案为:
三种参考方案如下:
方案一:配制相同物质的量浓度的NaHSO3和NaHCO3溶液,用酸度计(或pH试纸)测两溶液的pH.前者的pH小于后者,证明H2SO3酸性强于H2CO3.
方案二:将SO2气体依次通过NaHCO3(Na2CO3)溶液、酸性KMnO4溶液、品红溶液、澄清石灰水.品红溶液不褪色、且澄清石灰水变混浊,证明H2SO3酸性强于H2CO3.
方案三:将CO2气体依次通过NaHSO3(Na2SO3)溶液、品红溶液.品红溶液不褪色,证明H2SO3酸性强于H2CO3.点评:
本题考点: 制备实验方案的设计;物质的分离、提纯和除杂;气体发生装置;气体的收集;比较弱酸的相对强弱的实验.
考点点评: 本题主要考查常见的基本实验操作、仪器的使用、离子的除杂和实验方案设计,综合性强.1年前查看全部
- 卤水是从海水中提取食盐后的母液,常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品.现按下
 卤水是从海水中提取食盐后的母液,常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品.现按下列步骤对卤水进行处理,试根据有关物质的溶解度曲线(如图所示)回答下列问题:
卤水是从海水中提取食盐后的母液,常含有MgCl2、NaCl、MgSO4、KCl等,可进一步加工制得一些重要的产品.现按下列步骤对卤水进行处理,试根据有关物质的溶解度曲线(如图所示)回答下列问题:
(1)将卤水加热升温到160℃以上,随着水分的蒸发,会逐渐析出晶体.这时得到的晶体的主要成分是______.
(2)过滤出上述晶体后,将滤液降温到30℃以下,还会逐渐析出晶体.这时得到的晶体的主要成分是______.
(3)将第(2)步操作得到的晶体用一定量的冷水洗涤,最后可以得到比较纯净的______晶体. longmiao1年前1
longmiao1年前1 -
 小黑SAM 共回答了17个问题
小黑SAM 共回答了17个问题 |采纳率94.1%解题思路:(1)加热时析出晶体,说明该晶体溶解度随温度的生高而降低.
(2)降温时析出晶体,说明该晶体溶解度随温度的降低而降低.
(3)比较温度较低时两种物质的溶解度大小,溶解度小的物质就会析出.(1)观察溶解度图象,当温度大于60℃,随着温度的升高,MgSO4的溶解度反而下降,NaCl的溶解度一直比较低.所以这两种物质就会结晶析出,故答案为:NaCl和MgSO4;
(2)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,MgCl2和KCl随着温度的降低而下降,故答案为:MgCl2和KCl;
(3)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,在温度较低时,MgCl2的溶解度大于KCl的溶解度;所以冷水洗涤时较纯的KCl固体就会析出.低于30℃时,MgCl2的溶解度大于KCl的溶解度,所以,用少量冷水淋洗析出的晶体,就得到较纯的KCl晶体.故答案为:KCl.点评:
本题考点: 固体溶解度曲线及其作用;结晶的原理、方法及其应用;晶体和结晶的概念与现象.
考点点评: 学会分析溶解度图象的方法,并且理解升温或者降温时结晶析出的条件.1年前查看全部
- 氯化镁(卤水)加入氧化镁(轻钙粉)“加入什么”?再加双氧水就可以膨胀?
氯化镁(卤水)加入氧化镁(轻钙粉)“加入什么”?再加双氧水就可以膨胀?
我是做防火门芯填空材料的,现在有个难题想请教大家:
氯化镁(卤水)加入氧化镁(轻钙粉)“加入什么”?再加双氧水就可以发(膨胀起来了)?
而且膨胀起来会比较稠粘呢? 做人没意思1年前3
做人没意思1年前3 -
 大话梅 共回答了21个问题
大话梅 共回答了21个问题 |采纳率95.2%应该是轻烧粉
主要有一下几过程:
1 氧化镁和水反应生成氢氧化镁
2 双氧水分解生成水和氧气(膨胀的主要原因)
3 随着体系中水分不断减少,卤水中的氯化镁开始析出结晶
4 水分继续减少,最终整个体系凝固,形成具有一定强度的固体.
实际上不需要加什么东西,如果膨胀不好,把原料温度提高一些就可以了.你的主要问题应该是卤水的浓度或者是卤水与氧化镁的配比有问题或者是双氧水加少了.
可以查一下镁质胶凝材料和膨胀混凝土方面的资料.1年前查看全部
- 卤水(提取食盐后的母液)含有MgCl2、NaCl、MgSO4、KCl.从卤水中提取KCl固体,采用下列方法:
 卤水(提取食盐后的母液)含有MgCl2、NaCl、MgSO4、KCl.从卤水中提取KCl固体,采用下列方法:
卤水(提取食盐后的母液)含有MgCl2、NaCl、MgSO4、KCl.从卤水中提取KCl固体,采用下列方法:
(1)将卤水加热到60℃以上蒸发水分就逐渐析出晶体A,滤出晶体得到母液R,根据下图所示溶解度曲线,晶体A中主要含有______和______,理由是______.
(2)将母液R降温(降到30℃以下)析出晶体B,则晶体B主要含有______和______,理由是______.
(3)将析出的晶体B,用一定量的冷水洗涤,就可以得到较纯的KCl固体,理由是______. 牧川牧川1年前1
牧川牧川1年前1 -
 表现不俗的 共回答了20个问题
表现不俗的 共回答了20个问题 |采纳率90%解题思路:(1)加热时析出晶体,说明该晶体溶解度随温度的生高而降低.
(2)降温时析出晶体,说明该晶体溶解度随温度的降低而降低.
(3)比较温度较低时两种物质的溶解度大小,溶解度小的物质就会析出.(1)观察溶解度图象,当温度大于60℃,随着温度的升高,MgSO4的溶解度反而下降,NaCl的溶解度一直比较低.所以这两种物质就会结晶析出,故答案为:NaCl,MgSO4;温度高于60℃时这两种物质的溶解度较小.
(2)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,MgCl2和KCl随着温度的降低而下降,故答案为:MgCl2,KCl;由于温度下降,这两种物质溶解度也随之下降.
(3)降温时析出晶体,说明该晶体溶解度随温度的降低而降低;从图象可以看出,在温度较低时,MgCl2的溶解度大于KCl的溶解度;所以冷水洗涤时较纯的KCl固体就会析出.故答案为:低于30℃时,MgCl2的溶解度大于KCl的溶解度,所以,用少量冷水淋洗析出的晶体,就得到较纯的KCl晶体.点评:
本题考点: 固体溶解度曲线及其作用;混合物的分离方法.
考点点评: 学会分析溶解度图象的方法,并且理解升温或者降温时结晶析出的条件.1年前查看全部
- 卤水中的主要成分为食盐(假设其所含杂质仅为NaBr),为了充分利用资源,有研究人员开发了以晒盐卤水和化肥碳酸氢铵为原料制
卤水中的主要成分为食盐(假设其所含杂质仅为NaBr),为了充分利用资源,有研究人员开发了以晒盐卤水和化肥碳酸氢铵为原料制取纯碱的工艺,其生产流程如下图。


(1)写出卤水和碳酸氢铵反应的化学方程式_______________;
(2)操作I是_________(填操作名称),试剂X为________,残液除NH 4 Cl外,还含有_________;
(3)若滤渣中含有NH 4 Cl杂质,则可能导致纯碱中混有杂质,写出煅烧时产生杂质的副反应的化学方程式__________________;
(4)实验室检测滤渣中是否含有NH 4 Cl的操作是_________________;
(5)碳酸氢铵与氯化钠的配料比是影响纯碱质量的因素之一,右图是(摩尔比)对NaHCO 3 产率的影响。实际生产中选择=1.2。
①下列相关说法正确的是___________。
a.碳酸氢铵过量是为了充分利用卤水
b.碳酸氢铵过量是为了减少纯碱中的NaCl
c.碳酸氢铵过量太多将会导致生产成本过高
②不考虑生产过程中的损耗,生产1mol纯碱,需消耗碳酸氢铵________mol。 kaka11141年前1
kaka11141年前1 -
 明月轻寒 共回答了16个问题
明月轻寒 共回答了16个问题 |采纳率93.8%(1)NaCl +NH 4 HCO 3 → NaHCO 3 ↓ + NH 4 Cl(2分)
∆
(2)过滤、洗涤(2分)盐酸(1分) NH 4 Br(或NaBr)(1分) (3)NaHCO 3 + NH 4 Cl→ NaCl +NH 3 ↑+H 2 O + CO 2 ↑(2分)
(4)取洗涤液,加入足量硝酸至溶液呈酸性,再滴加硝酸银溶液,无沉淀说明纯净(答案合理即可,1分)
(5)① bc(2分) ② 2.4mol(1分)
略1年前查看全部
- 分析下列试样选用什么类型的光谱仪 矿石的定性,定量分析 卤水中的微量铷和铯 高纯Y2o3中的稀土杂质元素
 微笑的鹿1年前3
微笑的鹿1年前3 -
 楚之剑 共回答了21个问题
楚之剑 共回答了21个问题 |采纳率104.8%楼主您的问题,太专业了,我帮您在网上搜集的了资料.1年前查看全部
- 从海水中提取镁的过程:通常将______加入到海水或卤水中,沉淀出______,然后再由______和盐酸反应生成氯化镁
从海水中提取镁的过程:通常将______加入到海水或卤水中,沉淀出______,然后再由______和盐酸反应生成氯化镁,电解熔融状态下的氯化镁,就能得到镁.  gillian381年前1
gillian381年前1 -
 多来米发索拉 共回答了17个问题
多来米发索拉 共回答了17个问题 |采纳率94.1%从海水中提取镁的方法:把石灰乳即氢氧化钙加入到海水中,生成氢氧化镁沉淀,再向氢氧化镁中加入稀盐酸得到氯化镁,最后通过电解熔融状态下的氯化镁,就能得到单质镁.
故答案为:石灰乳,氢氧化镁,氢氧化镁.1年前查看全部
- 化学卤水是什么的颜色?卤水在化学上是指海水晒盐时候产生的液体. 主要成分是氯化镁. (ps做豆腐时候用的卤水也是这个东西
化学卤水是什么的颜色?
卤水在化学上是指海水晒盐时候产生的液体.
主要成分是氯化镁.
(ps做豆腐时候用的卤水也是这个东西.)
卤水和海水的共同点是都含有氯化镁,区别是卤水中的氯化镁含量较高,海水中氯化钠的含量教高
 jackyduan1231年前2
jackyduan1231年前2 -
 shallcat 共回答了21个问题
shallcat 共回答了21个问题 |采纳率90.5%是卤素溶于水后的颜色,有很多种色1年前查看全部
- 卤水的主成分是什么?
 挑语病1年前1
挑语病1年前1 -
 流水条件 共回答了14个问题
流水条件 共回答了14个问题 |采纳率85.7%卤水中,常含有K+、Na+、Ca2+、Mg2+、Cl-、SO2-、CO2-、HCO3-、B、Li、Br、I、Sr、Rb、Cs等离子.
主要成分:水1年前查看全部
- 氧化镁在卤水中起什么化学反映
 huabeidiqu1年前1
huabeidiqu1年前1 -
 rt1127 共回答了21个问题
rt1127 共回答了21个问题 |采纳率85.7%MgO 放到卤水(酸性!)所以生成卤化镁或者卤酸镁!(Mg0不会成Mg(OH)2,就像Fe2O3放到 NaOH里,是不反映的!本来就是沉淀!1年前查看全部
- 广泛用于导弹、飞机制造业的金属镁就是从海水中提取镁盐制取的,通常将 _________ 加入海水中或卤水中,沉淀出 __
广泛用于导弹、飞机制造业的金属镁就是从海水中提取镁盐制取的,通常将 _________ 加入海水中或卤水中,沉淀出 _________ ,该沉淀再与盐酸反应生成 _________ ,电解 _________ 态的氯化镁就可制造金属镁,请写出上述反应的化学方程式 _________ ; _________ ; _________ .  13的粉丝1年前0
13的粉丝1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 高中化学 请讲一下此图片的流程在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下面的工艺流程生产单质碘
 tudou873021年前1
tudou873021年前1 -
 真没问题 共回答了24个问题
真没问题 共回答了24个问题 |采纳率91.7%富碘卤水中的碘与硝酸银反应生成碘化银沉淀,碘化银与铁粉和水反应生成单质银(甲中还混有过量的铁粉,用硫酸洗后铁粉变成硫酸亚铁溶液,银单质加入硝酸制成硝酸银循环使用)和碘化亚铁(乙),碘化亚铁与氯气反应,生成氯化铁和碘单质,经过萃取,分离出碘单质.
满意请采纳,不懂可追问,谢谢1年前查看全部
- 熟食用乙基麦芽酚的具体用法到底是直接加卤水里,还是做成溶液涂上呢?我直接加卤水里感觉吃起来没那么香.请内行回答,我是厨师
熟食用乙基麦芽酚的具体用法
到底是直接加卤水里,还是做成溶液涂上呢?我直接加卤水里感觉吃起来没那么香.请内行回答,我是厨师希望能交您这个朋友345983489
 冷鋒寒1年前1
冷鋒寒1年前1 -
 twowei40 共回答了16个问题
twowei40 共回答了16个问题 |采纳率87.5%你有用“星湖”牌乙基麦芽酚吗?确认是正品吗?用量正确吗?
正确的用法应该是用水溶化然后加到卤水里的!这样能去腥臭和膻味,还能赋予肉制品一种美妙的焦糖香!
我也是经常用的,一桶30KG重的卤水得放两汤匙的!要不等于没放!1年前查看全部
- 我熬制的卤水为什么会发苦我的卤水方;.1八角3两·2·姜02两·3·桂皮1两·4·草果5棵·5·丁香1两·6·桂枝5钱·
我熬制的卤水为什么会发苦
我的卤水方;.1八角3两·2·姜02两·3·桂皮1两·4·草果5棵·5·丁香1两·6·桂枝5钱·7·千里香8钱·8·母丁香1两·9·小茴香1两·10·槟榔片6钱·11·芝盐4钱·12·玉果6棵·13·长香果5棵·14·良姜7钱·15·甘草1两·16·土沙仁5钱·17·一品香7钱·18·白扣1钱·19·筚拨8钱·20·花椒8钱·21·白芷5钱·22·陈皮5钱·23·香叶1两·24·甘松4钱·25·三黄皮7钱·26·草寇8棵·27·罗汉果2个猪大骨5斤.鸡架2斤.水50斤...请师傅们指教谢谢. nysxf1年前1
nysxf1年前1 -
 hanxue0425 共回答了17个问题
hanxue0425 共回答了17个问题 |采纳率82.4%丁香多了会苦,丁香粒放20颗左右即可,还有往锅里加的糖不能太多,建议你所有卤料都减量,要不鸟那么多的 ,!多了味道一重当然苦了!1年前查看全部
- 浩瀚的海洋蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.将粗盐提纯可以得到纯净的NaCl.欲用纯净的NaCl配制10
浩瀚的海洋蕴含着丰富的化学资源.海水晒盐能够得到粗盐和卤水.将粗盐提纯可以得到纯净的NaCl.欲用纯净的NaCl配制100g0.9%的生理盐水,配制该溶液时需要的玻璃仪器有______.如果配制的溶液的溶质质量分数低于0.9%,你认为可能的原因是______(任写一个).
 kingner09131年前1
kingner09131年前1 -
 orthopedics 共回答了18个问题
orthopedics 共回答了18个问题 |采纳率94.4%解题思路:配制一定质量分数的溶液需要的玻璃仪器有:烧杯、量筒、玻璃棒、胶头滴管.
主要从溶剂的量多了或溶质的量少了等方面进行分析.烧杯用来溶解固体配制溶液,量筒用来量取水的体积,玻璃棒可以搅拌加速溶解,胶头滴管在量筒量取水的条件时用来校准体积,故答案为:烧杯、量筒、玻璃棒、胶头滴管.质量分数偏小,可能是溶剂多了,也可能是固体取少...
点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 本题主要考查了配制一定质量分数的溶液需要的玻璃仪器及配制的溶液的溶质质量分数偏低的原因,基础性强,难度不大.1年前查看全部
- 臭豆腐的卤水怎么做的?
 xdc1161年前1
xdc1161年前1 -
 哥特式幻想 共回答了12个问题
哥特式幻想 共回答了12个问题 |采纳率91.7%臭豆腐卤水制作
冷水15公斤 豆豉3公斤 烧开后煮30分钟左右,然后将豆豉汁滤出,冷却后加纯碱100克(2两),青矾20克(4钱),香菇200克(4两),冬笋4000克(4公斤),盐750克(1.5公斤),茅台酒3两(150克),豆腐脑3公斤(1500克)
浸泡15天左右(每天搅动一次),发酵后即成卤水.
卤水切勿沾油,注意清洁卫生,防杂物混入,根据四季不同气温灵活掌握,使之时刻处于发酵状态.连续使用隔3个月加入一次主料,做法和份量同上(不要加青矾和纯碱)用时要注意经常留老卤水(越久越好).
检验卤水的正常的标准是发酵.如果不发酵,气味不正常时,其办法是将净火砖烧红放在事水内促使发酵,同时,还按上述配方适当加一点佐料进,使其发酵后平致变味.(每次浸泡的豆腐取出后,卤水内加入适量的盐,以保持咸淡正常)
主料:精制白豆腐30块(1.5厘米厚,5X5厘米)
调料:植物油2公斤(2000克,实耗100克(2两)),红油1两(50克),酱油1两(50克),香油0.5两(25克),味精2.5克,鸡汤2两(100克)
制作:
1,青矾3克入桷内,到入沸水用棍子搅动,放入豆腐春秋浸泡时间为2--5小时,夏季1--2小时,冬季6--10小时,胚子硬多泡,软少泡,卤好后取出,用冷开水洗一下,装入筛子内沥干水份(洗后的水留着),洗到水浓时倒入卤水内)
2,用红油,酱油,香油,味精和少许汤兑成汁
3,将油烧沸后,豆腐逐块下锅炸5分钟(火大时,用小火,炸焦透为准)成外焦内嫩捞出,入盘用筷子在每块豆腐中间捅一个洞,将兑汁倒入眼内即可.
特点:闻起来臭,吃起来香,外焦内嫩,香辣味美,别有风味.1年前查看全部
- 在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下列工艺流程生产单质碘。完成下列问题:
在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用下列工艺流程生产单质碘。完成下列问题:
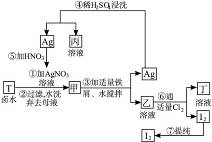
(1)写出乙、丁中溶质的化学式:乙___________,丁___________。
(2)第④步操作中用稀硫酸浸洗的目的是___________。
a.除去未反应的
b.除去未反应的I -
c.除去未反应的Fe
d.除去碱性物质
(3)第⑦步操作可供提纯I 2 的两种方法是___________和___________(不要求写具体步骤)。
(4)实验室检验I 2 的方法是_________________________________。
(5)甲物质见光易变黑,其原因是(用化学方程式表示):______________________。
(提示:3Ag+4HNO 3 ====3AgNO 3 +NO↑+2H 2 O)
(6)按上述实验过程填空:
写出①②③反应的化学方程式。
①____________________________________________________________________;
②____________________________________________________________________;
③____________________________________________________________________。 ujswamsvmj1年前1
ujswamsvmj1年前1 -
 雪原游龙 共回答了13个问题
雪原游龙 共回答了13个问题 |采纳率92.3%(1)FeI 2 FeCl 3
(2)C (3)升华 萃取
(4)将I 2 加在淀粉溶液中,溶液显蓝色
(5)2Ag====I2Ag+I 2
(6)c.蓝 d.紫
①2FeBr 2 +3Cl 2 ====2FeCl 3 +2Br 2
②2FeCl 3 +2KI====2FeCl 2 +I 2 +2KCl
③2KI+Br 2 2====KBr+I 2
由物质的转化图分析讨论,可得乙物质是由铁和碘化银反应生成的,由于铁在该反应中只能被氧化为+2价,故乙是FeI 2 ,而不是FeI 3 ,而Cl 2 将FeI 2 氧化为I 2 和FeCl 3 ,3Cl 2 +2FeI 2 ====2I 2 +2FeCl 3 ;在第④步操作中用稀硫酸浸洗银时,是除去银里的少量铁。I 2 单质易升华,易溶于有机溶剂(如酒精、四氯化碳等),提纯I 2 可用升华和萃取的方法。单质I 2 遇淀粉的水溶液显蓝色,这是检验单质I 2 的常用方法(也是检验淀粉的常用方法)。AgI的稳定性较差,见光受热易分解生成单质银和碘。1年前查看全部
- 广泛用于导弹、飞机制造业的金属镁就是从海水中提取镁盐制取的,通常将 _________ 加入海水中或卤水中,沉淀出 __
广泛用于导弹、飞机制造业的金属镁就是从海水中提取镁盐制取的,通常将 _________ 加入海水中或卤水中,沉淀出 _________ ,该沉淀再与盐酸反应生成 _________ ,电解 _________ 态的氯化镁就可制造金属镁,请写出上述反应的化学方程式 _________ ; _________ ; _________ .  我是哈密瓜1年前1
我是哈密瓜1年前1 -
 xu100202508 共回答了21个问题
xu100202508 共回答了21个问题 |采纳率95.2%1年前查看全部
- 从海水中提取镁、盐,通常将______加入海水或卤水中,沉淀出______,与盐酸反应生成______,______熔融
从海水中提取镁、盐,通常将______加入海水或卤水中,沉淀出______,与盐酸反应生成______,______熔融状态下的氯化镁,就能得到镁.转化过程中发生的化学方程式有______;______;MgCl
Mg+Cl2↑通电 .MgCl.
Mg+Cl2↑通电 . 河边草青青1年前1
河边草青青1年前1 -
 忍无可忍hnu2007 共回答了19个问题
忍无可忍hnu2007 共回答了19个问题 |采纳率94.7%解题思路:根据从海水中提取镁的流程及原理分析此题,根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式.从海水中提取镁盐,通常将熟石灰加入海水中或卤水中,沉淀出氢氧化镁,氢氧化镁与盐酸反应生成氯化镁,电解熔融状态的氯化镁,就能制的金属镁;转化过程中发生的化学反应主要有:Ca(OH)2+MgSO4═Mg(OH)2↓+CaSO4,Mg(OH)2+2HCl═MgCl2+2H2O,MgCl
通电
.
Mg+Cl2↑.
故答案为:熟石灰;氢氧化镁;氢氧化镁;氯化镁;电解;
Ca(OH)2+MgSO4═Mg(OH)2↓+CaSO4,Mg(OH)2+2HCl═MgCl2+2H2O,MgCl
通电
.
Mg+Cl2↑.点评:
本题考点: 对海洋资源的合理开发与利用;酸的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要掌握化学方程式的书写方法和从海水中提取金属镁的过程,只有这样才能对相关方面的问题做出正确的判断.1年前查看全部
- (2012•安徽)海洋中有丰富的水生生物和化学资源.海水晒盐后,以其母液(卤水)和贝壳为原料,还可生产具有特殊用途的材料
(2012•安徽)海洋中有丰富的水生生物和化学资源.海水晒盐后,以其母液(卤水)和贝壳为原料,还可生产具有特殊用途的材料--纳米氧化镁,其简要流程如图:

(1)海水晒盐是______(填“物理”或“化学”)变化,包含蒸发、______等过程.
(2)写出食盐的一种用途:______.
(3)A步骤反应的化学方程式是CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
(4)实验室进行a操作时,需要的玻璃仪器有烧杯、漏斗、______. single3141年前1
single3141年前1 -
 nonozht 共回答了14个问题
nonozht 共回答了14个问题 |采纳率92.9%解题思路:根据流程结合已有的知识进行分析,海水晒盐没有生成新的物质,属于物理变化,该过程包含水的蒸发和食盐的结晶;食盐具有咸味,能用作调味品;碳酸钙高温能分解生成氧化钙和二氧化碳;过滤操作中用到的玻璃仪器有烧杯、漏斗和玻璃棒等.(1)海水晒盐没有生成新的物质,属于物理变化,该过程包含水的蒸发和食盐的结晶,故填:物理,结晶;
(2)食盐具有咸味,能用作调味品,故填:做调味品;
(3)碳酸钙高温能够分解生成氧化钙和二氧化碳,故填:CaCO3
高温
.
CaO+CO2↑;
(4)过滤操作中用到的玻璃仪器有烧杯、漏斗和玻璃棒等,故填:玻璃棒.点评:
本题考点: 对海洋资源的合理开发与利用;过滤的原理、方法及其应用;碳酸钙、生石灰、熟石灰之间的转化;氯化钠与粗盐提纯;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了海洋资源的利用,完成此题,可以依据已有的知识进行,要求同学们加强对基础知识的储备,以便灵活应用.1年前查看全部
- 用热空气把溴从卤水中吹出的原因主要是_____和______
用热空气把溴从卤水中吹出的原因主要是_____和______
a溴容易溶解于水
b溴容易挥发
c溴的密度大
d温度升高,溴的溶解度减小 zhtceo1年前1
zhtceo1年前1 -
 re0lwe 共回答了13个问题
re0lwe 共回答了13个问题 |采纳率84.6%溴容易挥发
d温度升高,溴的溶解度减小1年前查看全部
- 从海水中制取溴的过程中是把氯气通入加热到90度,ph=3.5的卤水中,将溴离子化为溴气,用空气吹成的溴气,被碳酸钠溶液吸
从海水中制取溴的过程中是把氯气通入加热到90度,ph=3.5的卤水中,将溴离子化为溴气,用空气吹成的溴气,被碳酸钠溶液吸收得到NaBr和NaBr3混合液,再用酸化混合液,即可得到溴气
写出有关的离子方程式
1.碳酸钠溶液吸收溴气:
2.用酸化混合液制取溴气:
3.所得的液溴中混有少量的氯,可以选用NaBr固体做除杂试剂,其化学方程式为: notaryann1年前1
notaryann1年前1 -
 带刺的蜜蜂 共回答了27个问题
带刺的蜜蜂 共回答了27个问题 |采纳率92.6%1、3Br2 + 6CO3^2- + 3H2O = 5Br- + BrO3^- + 6HCO3^-
2、5Br- + BrO3^- + 6H^+ = 3Br2 + 3H2O
3、Cl2 + 2NaBr = 2NaCl + Br21年前查看全部
- 写出用氯气氧化卤水中溴离子的化学方程式
写出用氯气氧化卤水中溴离子的化学方程式
详细的问题说明,有助于回答者给出准确的答案 我就KAO这件事情1年前4
我就KAO这件事情1年前4 -
 zpfanta 共回答了23个问题
zpfanta 共回答了23个问题 |采纳率82.6%Cl2+2Br-====Br2+2Cl-
这没什么好说明的了,就是氯气的氧化性比溴强
可以将溶液中的溴离子氧化1年前查看全部
- 海水提镁 卤水化学讲卤水是晒盐后产生的水,但晒盐后水都蒸发掉了哪还有水?假设是水还未蒸发完时剩的水,为什么氯化镁较多?为
海水提镁 卤水
化学讲卤水是晒盐后产生的水,但晒盐后水都蒸发掉了哪还有水?假设是水还未蒸发完时剩的水,为什么氯化镁较多?
为什么氯化钠就结晶出来了而氯化镁没有? litiren1年前3
litiren1年前3 -
 糊糊2005 共回答了19个问题
糊糊2005 共回答了19个问题 |采纳率94.7%晒盐的过程:蒸发,使稀溶液转变为浓溶液直至为氯化钠的饱和溶液;再继续蒸发,就会有氯化钠晶体析出,当有大量晶体析出时,即可将底部析出的晶体从溶液中捞出来,就得到粗盐,剩余的少量液体就会人们说的卤水.
蒸发时,不能将水全部蒸干,那样就会使粗盐中含有更多的杂质如:氯化镁、氯化钙等.
在蒸发的过程中,同时对氯化镁也是一个浓缩的过程.
因为氯化镁在水中的溶解度很大,0℃时100克水能溶解59.5克氯化镁,20℃时能溶74g;而且氯化镁在海水的含量比氯化钠少,溶解度比氯化钠的大,但它也会有析出,只不过量很少,粗盐中也含有氯化镁这样的杂质.1年前查看全部
- 氧化镁活性降低,卤水浓度是不应该降低?
 microsim1年前1
microsim1年前1 -
 无所畏惧我怕谁 共回答了24个问题
无所畏惧我怕谁 共回答了24个问题 |采纳率75%我来给你回答:答案是应该降低,理由是卤水浓度会随着活性物质的扩散而其成分归一,瞬间聚合的可沉淀物质聚合沉淀,卤水中溶解性的盐类物质(卤化物)减少,水量不变,因而卤水浓度当然降低;氧化镁的扩散性较强,其活性状况呈抛物线状态,建议氧化镁放置时间不宜过长.1年前查看全部
- 乙烯是否能与所有卤素发生加成反应?一定要在卤水中进行吗?
乙烯是否能与所有卤素发生加成反应?一定要在卤水中进行吗?
如题
需要的具体条件是什么?一定要在卤素的溶液中才能进行吗? hpingchan1年前3
hpingchan1年前3 -
 超时空精灵 共回答了21个问题
超时空精灵 共回答了21个问题 |采纳率90.5%氟气除外,氟太活泼了,会氧化乙烯得到CF4和HF
碘的反应太慢,而且碘在水中溶解度也很小,不是很常用,但能反应
像卤的CCl4溶液也可以,但水比较常见,而且水无毒,所以常用卤水
因为加成反应是离子间的反应,纯的卤单质不能解离出离子1年前查看全部
- )为什么在晒盐时,食盐晶体析出,而氯化镁和氯化钙却大部分留在卤水中?
 ghkir1年前2
ghkir1年前2 -
 cqydxy 共回答了20个问题
cqydxy 共回答了20个问题 |采纳率90%在晒盐时,随着水分的蒸发,食盐首先达到饱和,食盐以晶体形式析出.而氯化镁和氯化钙则没有达到饱和,就会大部分留在卤水中.这卤水称为苦卤,可以再进一步提制所含化工物质.1年前查看全部
- 喝卤水(氯化镁)真能致死吗?《白毛女》中的杨白劳是喝卤水自杀的.不过那是文艺作品,不能算数.世上真有被氯化镁毒死的人吗?
喝卤水(氯化镁)真能致死吗?
《白毛女》中的杨白劳是喝卤水自杀的.
不过那是文艺作品,不能算数.
世上真有被氯化镁毒死的人吗?
我估计不过是使人腹泻而已.氯化镁的作用跟硫酸镁应该差不多,分量大了就是泻药.
我有根据:
我们吃下钙镁片,其中的镁,在胃里就要先转化为氯化镁,然后才能吸收.如果氯化镁有毒,那么钙镁片就有毒,甚至我们吃的大多数食物有毒,因为含镁,在胃里要变成氯化镁.
另外一个根据是:
我的观点是:氯化镁少量的吃,是补品,吃过量了就是泻药,不可能毒死人 xiaohao8210161年前1
xiaohao8210161年前1 -
 于凌 共回答了20个问题
于凌 共回答了20个问题 |采纳率100%氯化镁本身无毒 少量服用可以导致轻微腹泻 所以有时被用于防治便秘 很多防胃酸胃药中都有镁的成分(多为碱式碳酸盐)服用后会与胃酸反应生成氯化镁的.
但是高浓度的氯化镁会导致蛋白质发生盐析凝固 .
高浓度的氯化镁会通过细胞的渗透作用进入血管,使得血液中的蛋白质发生盐析作用,从而导致血液凝固,导致死亡.
同时盐卤对皮肤、粘膜有很强的刺激作用,对中枢神经系统有抑制作用,误服本品后对口腔、食道、胃粘膜产生强烈腐蚀作用,患者恶心呕吐、口干、胃痛、烧灼感,腹胀、腹泻,头晕,头痛,出皮疹等.严重者呼吸停止,出现休克,甚至造成死亡.
蛋白质盐析作用:
向某些蛋白质溶液中加入某些无机盐溶液后,可以降低蛋白质的溶解度,使蛋白质凝聚而从溶液中析出,这种作用叫作盐析,是物理变化,可复原.向某些蛋白质溶液中加入某些重金属盐,可以使蛋白质性质发生改变而凝聚,进而从溶液中析出,这种作用叫作变性,性质改变,是化学反应,无法复原.
利用高浓度中性盐使蛋白质发生沉淀;蛋白质的溶解度(S)不同,用于沉淀的盐浓度不同.1年前查看全部
- 如果在卤水会中加入氢氧化钙后溶液,氢氧化钙处于饱和状态,则卤水中镁离子的浓度可降到多少
如果在卤水会中加入氢氧化钙后溶液,氢氧化钙处于饱和状态,则卤水中镁离子的浓度可降到多少
已知Ksp氢氧化钙=1.08x10^-7.Ksp氢氧化镁=5.7x10^-12 缺qq1年前1
缺qq1年前1 -
 blueheart26 共回答了18个问题
blueheart26 共回答了18个问题 |采纳率88.9%先求氢氧根的浓度,KsP氢氧化钙=C钙离子*(C氢氧根)^2=1.08*10^-7.所以C氢氧根=1.08*10^-7开三次根号=0.00476
KsP氢氧化镁=C镁离子*(C氢氧根)^2=5.7x10^-12,得出C镁离子=Ksp氢氧化镁/(C氢氧根)^2=2.511x10^-7.1年前查看全部
大家在问
- 1若随机变量X服从两点分布,且成功概率为0.7;随机变量Y服从二项分布,且Y~B(10,0.8),则E(X),D(X),E
- 2有哪些物质可以加快铁的生锈速度?时间需要多长?
- 3若关于x的代数式x²+2mx+4m-4是一个完全平方式,求实数m的值
- 4以“漫”字开头的四字词语
- 5阅读理解 语文高手进喝墨水的笑话 我国古代的墨水都是用粮食做的,喝一点对身体没有什么害处。因此,教书先生常常用罚喝墨水来
- 6一个喷泉直径12米高0.4米宽0.3米。喷池的战地面积是多少?
- 7为什么?九为极数?
- 8Mr and Mrs Read have no d( ).They have only two
- 9什么是平行线,我们是平行线,还是相交线
- 10如图,以O为圆心的两个同心圆…………
- 11圣诞节的时候看见圣诞老人穿着酷酷的衬衫短裤,滑着冲浪板向沙滩上迎面奔来,这种装扮的圣诞老人会出现在(
- 12《论语》十则 子曰:“学而时习之,不亦说乎?有朋自远方来,不亦乐乎?人不知而不愠,不亦君子乎?”
- 13证明:2的N次方大于N的平方2的N次方大于N的平方证明一下朋友问得,偶给忘了.她还米学归纳法/我想的也是归纳法.
- 14AB//CD,EF交AB于G,交CD于F,FH平分∠EFD,交AB于H,∠AGE=50°,求BHF
- 15一种元素只能有一种质量数吗?

