将0.56克氧化钙投入含1.46克氯化氢的盐酸中,反应完全后,滴入石蕊试剂变成什么颜色
 鲤鱼跃龙门2022-10-04 11:39:544条回答
鲤鱼跃龙门2022-10-04 11:39:544条回答
已提交,审核后显示!提交回复
共4条回复
 浪花一朵朵 共回答了18个问题
浪花一朵朵 共回答了18个问题 |采纳率100%- cao+H2o=ca(oh)2
56 74
0.56 0.74
ca(oh)2 +2hcl =cacl2+h2o
74 73
0.74 0.73
0.73<1.46
所以HCL过量
所以显红色
呢个 计算的数可能是错的 但是思路绝对没错! - 1年前
 lead22 共回答了1个问题
lead22 共回答了1个问题 |采纳率- 红
HCL还多了
反应了以后生成CaCl2+h2o和Hcl。 - 1年前
 亚文_斯达克 共回答了6个问题
亚文_斯达克 共回答了6个问题 |采纳率- 红 溶液呈酸性
HCL还多了
反应了以后生成CaCl2+h2o和Hcl - 1年前
 qhjlove0305 共回答了18个问题
qhjlove0305 共回答了18个问题 |采纳率- 红色,溶液呈酸性
- 1年前
相关推荐
- 将 0.56克铁加到50毫升浓度为1mol/L的盐酸中 准状况下产生多少体积的氢气?
将 0.56克铁加到50毫升浓度为1mol/L的盐酸中 准状况下产生多少体积的氢气?
若反应后,溶液的体积为50ml,这时溶液中的Fe2+,和氢离子的浓度个为多少 vivian1181年前1
vivian1181年前1 -
 sbalcy 共回答了14个问题
sbalcy 共回答了14个问题 |采纳率92.9%产生0.224L氢气,亚铁离子浓度为0.2mol/L,氢离子浓度为0.6mol/L.1年前查看全部
- 标准状况下,0.56克某气体的体积为448毫升,则该气体的相对分子质量是多少
 森林憩狼1年前3
森林憩狼1年前3 -
 le嘟嘟 共回答了11个问题
le嘟嘟 共回答了11个问题 |采纳率100%448 ml
则气体物质的量为 0.448/22.4==0.02 mol
则摩尔质量==质量/物质的量==0.56/0.02==28 g/mol
则 分子量为 281年前查看全部
- 0.56克CaO正好和20毫升盐酸完全反应,这种盐酸的物质的量浓度为多少摩尔/升?A.0.10
0.56克CaO正好和20毫升盐酸完全反应,这种盐酸的物质的量浓度为多少摩尔/升?A.0.10
0.56克CaO正好和20毫升盐酸完全反应,这种盐酸的物质的量浓度为多少摩尔/升?
A.0.10 B.0.20 C.0.50 D.1.00 superlianglei1年前5
superlianglei1年前5 -
 黄诗玲 共回答了11个问题
黄诗玲 共回答了11个问题 |采纳率72.7%CaO+2HCl=CaCl2+H2O
56 2
0.56 X
X=0.02摩尔.
盐酸的物质的量浓度=0.02/0.02=1摩尔/升,选D1年前查看全部
- 0.56克的氧化钙正好与20ML盐酸完全反应,这种盐酸的物质的量的浓度为?
 中都宰1年前2
中都宰1年前2 -
 王天日 共回答了16个问题
王天日 共回答了16个问题 |采纳率87.5%CaO+2HCl===CaCl2+H2O
56-----2
0.56----0.02x
x=1MOL/L1年前查看全部
- 将0.56克KOH和1.38克K 2 CO 3 混合并配成溶液,向溶液中滴加0.1mol•L -1 稀盐酸.下列图象能正
将0.56克KOH和1.38克K 2 CO 3 混合并配成溶液,向溶液中滴加0.1mol•L -1 稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO 2 的物质的量的关系的是( ) A. 
B. 
C. 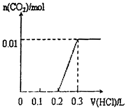
D. 
 卷-钢1年前1
卷-钢1年前1 -
 zhoulixing19 共回答了23个问题
zhoulixing19 共回答了23个问题 |采纳率95.7%0.56克KOH的物质的量为
0.56g
56g/mol =0.01mol,1.38克K 2 CO 3 的物质的量为
1.38g
138g/mol =0.01mol,KOH和K 2 CO 3 混合配成的溶液,当滴加盐酸时,先发生氢氧化钾与盐酸的中和反应,再发生碳酸钾与盐酸的反应生成碳酸氢钾和氯化钾,最后发生碳酸氢钾与盐酸反应才有二氧化碳气体生成,
A、加入0.1L盐酸,n(HCl)=0.1L×0.1mol/L=0.01mol,0.01mol盐酸与氢氧化钾反应没有气体生成,再加入0.01molHCl,与0.01mol碳酸钾恰好反应生成碳酸氢钾,也没有气体生成,则图象与实际不符,故A错误;
B、先发生氢氧化钾与盐酸的中和反应,图象中开始反应即有气体生成,与反应不符,故B错误;
C、向KOH和K 2 CO 3 混合溶液中滴加盐酸时,首先和KOH反应生成水和氯化钾,当滴入0.1L时,两者恰好反应完全;继续滴加时,盐酸和K 2 CO 3 开始反应,首先发生HCl+K 2 CO 3 =KHCO 3 +KCl,不放出气体,当再加入0.1L时,此步反应进行完全;继续滴加时,发生反应:KHCO 3 +HCl=KCl+H 2 O+CO 2 ↑,此时开始放出气体,再消耗0.1L盐酸,生成二氧化碳达最大,图象与实际相符合,故C正确;
D、因碳酸钾与盐酸的反应分步完成,则碳酸钾与盐酸先反应生成碳酸氢钾和氯化钾,此时没有气体生成,则图象与反应不符,故D错误;
故选C.1年前查看全部
大家在问
- 1把红、黄、蓝、白4种颜色的球各8个放到一个袋子里,至少要取( )个球,才可以保证取到3个颜色相同的球
- 2如图,直线AB、CD相交于点O,∠AOC=30°,半径为1cm的⊙P的圆心P在射线OA上,且与点O的距离为4cm,如果⊙
- 3两个边长为2的小正方形剪拼成一个大正方形,大正方形的边长x是一个无理数.你能估计x的保留两位小数的近似
- 4请问大家砌一平方24墙需要多少沙子和水泥?水泥用什么型号的?
- 5地球上的水能留下来.地球上的水孕育了生命.(用关联词把两句话和成一句话)
- 6如果把长,宽,高分别为5.28cm,9.65cm,12.68cm的长方体,熔化制成一个正方体,求这个正方体的棱长是多少?
- 7紧急英语问题For years,it's been assumed that the inside environmen
- 8设有0—9十个数,若在此十个数中抽取5个数(抽后放回)每次抽1个,求抽出的5个数字都不同的概率
- 9x+y+z=w是什么意思?
- 10(亻) 括号里的自读音是什么?
- 11英语翻译1.老师让我们将难懂的单词画线并查字典.(underline)2.他说像统计数据这样的细节就不必包括在内了.(s
- 12被减数,减数和差三个数的和为600,减数与差的比是5比7,那么减数是多少
- 13可用的空间我们都已经用上了用英语怎么说?
- 14五年级下册数学所说的长方体与正方体都是实心的吗
- 15若已定义:int a[]={0,1,2,3,4,5,6,7,8,9},*p=a,i; 其中 0≤i≤9,则对a数组元素正
