用黄铁矿制取硫酸,再用硫酸制取化肥硫酸铵,燃烧含FeS2为80%的黄铁矿75吨,生产出79.2吨硫酸铵.若在制取硫酸铵时
 夜之火焰2022-10-04 11:39:541条回答
夜之火焰2022-10-04 11:39:541条回答FeS2-------2H2SO4------2(NH4)2SO4
120---------------------------------------------------264
75t*80%*(1-X)----------------------------------------79.2t 90%
x=33.3%
是硫酸的90%用来至硫酸铵!不应是硫酸X顿,
x*90%*100000098*M(硫酸铵)=79200000吗

已提交,审核后显示!提交回复
共1条回复
 继续前行 共回答了20个问题
继续前行 共回答了20个问题 |采纳率90%- 那上边不是说 90%的利用率吗 除以90%就是硫酸铵的质量 大概如此了吧
从头说一遍不按照那上边的方程说 一步步的讲吧
79.2是实际出来的 除以90%是理论的应该出来的硫酸铵
题不是想要求FeS2的 损失率吗
那就是看 理论中应该产生的硫酸铵应该是多少纯的FeS2所能产生的 用 79.2/90%带回方程求出的FeS2是 理论中需要多少FeS2
在和75T*80% 做比 就是 FeS2的利用率
在用1 减去就是损失率了 - 1年前
相关推荐
- 用黄铁矿制硫酸的流程为什么?
 梁超伟1年前3
梁超伟1年前3 -
 反反46 共回答了14个问题
反反46 共回答了14个问题 |采纳率78.6%黄铁矿化学成分是FeS2.
在空气中煅烧即可得到SO2,SO2在催化剂作用下与氧气反应生成SO3.
SO3继续如水反应就得到硫酸H2SO4.
总的流程图为:
FeS2+O2——SO2+Fe2O3,
SO2+O2——SO3,
SO3+H2O——H2SO4.1年前查看全部
- 下列事实不能用勒夏特列原理解释的是( ) A.往氢硫酸溶液中加入碱,有利于S 2- 增多 B.经粉碎的黄铁矿燃烧得较快
下列事实不能用勒夏特列原理解释的是( ) A.往氢硫酸溶液中加入碱,有利于S 2- 增多 B.经粉碎的黄铁矿燃烧得较快、较完全 C.实验室用排饱和食盐水的方法收集氯气 D.合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率  zxhxy1年前0
zxhxy1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•北海)煅烧黄铁矿(主要成分是FeS2)的化学方程式是:4FeS2+11O2 高温 .
(2012•北海)煅烧黄铁矿(主要成分是FeS2)的化学方程式是:4FeS2+11O2
2M+8SO2.请判断M的化学式是( )高温 .
A.FeSO4
B.Fe2O3
C.Fe3O4
D.Fe2(SO4)3 luolanzxc1年前1
luolanzxc1年前1 -
 flash543 共回答了18个问题
flash543 共回答了18个问题 |采纳率94.4%解题思路:质量守恒定律定律的微观解释是原子的三不变,即化学反应前后原子的种类不变、原子的数目不变、原子的质量不变,据此分析解答即可.在反应前原子的种类和数目分别为:Fe→4个,O→22个,S→8个,反应后不包括物质M中,原子的种类和数目分别为:S→8个,O→16个,所以根据化学反应前后原子的种类和数目不变可得:2M中含有个4个Fe和6个O,所以M中含有2个Fe和3个O,化学式为Fe203.
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 此题考查的是质量守恒定律,根据其微观解释原子的三不变来做题,此题属于比较简单的题,但关键是要数清各原子的个数,另外要注意M前面有计量数2,很多学生往往忽略这一点,导致结果错误.1年前查看全部
- 工业上以黄铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2等对环境有较大影响的有害气体.能用于测定硫酸尾气
工业上以黄铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2等对环境有较大影响的有害气体.能用于测定硫酸尾气中SO2含量的是( )
A.NaOH溶液、酚酞试液
B.石灰水、石蕊试液
C.碘水、淀粉溶液
D.氨水、酚酞试液 chrishan1年前1
chrishan1年前1 -
 草根飘香 共回答了9个问题
草根飘香 共回答了9个问题 |采纳率100%解题思路:测定SO2含量必须要能跟SO2反应,而且可以用颜色变化来准确确定反应终点,A项和D项虽然能反应,但A在完全生成Na2SO3时溶液还是碱性,没变色,而D在SO2还没与氨水完全反应时就开始变色了.B项石灰水中所含溶质较少,且石蕊试液的颜色变化不明显,以此解答.A.在完全生成Na2SO3时溶液还是碱性,没变色,不能用于测定,故A错误;
B.石灰水中所含溶质较少,且石蕊试液的颜色变化不明显,故B错误;
C.碘水和二氧化硫发生氧化还原反应,终点时溶液褪色,可检测,故C正确;
D.氨水碱性较弱,在SO2还没与氨水完全反应时就开始变色了,不能测定,故D错误.
故选C.点评:
本题考点: 探究物质的组成或测量物质的含量;二氧化硫的化学性质.
考点点评: 本题考查物质的含量的测定实验方案的评价,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及溶液酸碱性的判断,难度不大.1年前查看全部
- 已知4FeS2+11O2=2Fe2O3+8SO2,使用1吨含杂质为20%的黄铁矿(FeS2)石,制得98%的浓硫酸约多少
已知4FeS2+11O2=2Fe2O3+8SO2,使用1吨含杂质为20%的黄铁矿(FeS2)石,制得98%的浓硫酸约多少吨?保留一位小
 向往变成神经病1年前1
向往变成神经病1年前1 -
 近几年 共回答了15个问题
近几年 共回答了15个问题 |采纳率86.7%4FeS2+11O2=2Fe2O3+8SO2
2SO2+ O2 ==催化==2SO3
SO3+H2O ==H2SO4
由上反应式得
1FeS2 2SO2 2SO3 2H2SO4
120 196
1*(1-20%) X*98%
X=1.31年前查看全部
- 某种含铁的矿石——黄铁矿种含有FeS2的质量分数为90%,10吨这种黄铁矿种含铁多少吨
 巨大小猫1年前1
巨大小猫1年前1 -
 zlf0056 共回答了18个问题
zlf0056 共回答了18个问题 |采纳率94.4%FeS2的质量:
M(FeS2)=10TX90%=9T
Fe的质量分数是56,S的是32,那么
M(Fe)=【56/(56+32X 2)】X9T=4.2T1年前查看全部
- 将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4,离子方程式怎么写
将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4,离子方程式怎么写
要分两步的 小偷cc1年前2
小偷cc1年前2 -
 懒人伤疤 共回答了22个问题
懒人伤疤 共回答了22个问题 |采纳率81.8%Fe3O4 + 8H+ ==2Fe3+ + Fe2+ +4H2O
2Fe3+ +Fe ==3Fe2+1年前查看全部
- 设某化工厂以黄铁矿(主要成分为Fes2)为原料产生硫酸.空气中的氧气的体积分数0,2,
设某化工厂以黄铁矿(主要成分为Fes2)为原料产生硫酸.空气中的氧气的体积分数0,2,
如果该厂生产98%的 浓硫酸100t.不考虑其他各生产阶段的物料损失.
1.需要含FeS260%的矿石质量为多少t?
2.最少需要消耗空气的体积(标状)为多少m³?
尽快回答, flowers41年前1
flowers41年前1 -
 5227720 共回答了15个问题
5227720 共回答了15个问题 |采纳率93.3%有关化学方程式为:1. 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 2. 8SO2 + 4O2 = 8SO3 3. 8SO3 + 8H2O = 8H2SO4 可以看出,题目中的已知物与待求物的关系为:
4FeS2 ~ 15O2 ~ 8H2SO4
4×120 t 15Mmol 8×98t
60% x y 100×98% t
解之 x= 100t y=1875Kmol
1.需要含FeS260%的矿石质量为100t.
2.最少需要消耗空气的体积(标状)为1875÷0.2×22.4=210000m³1年前查看全部
- 在沸腾炉中煅烧黄铁矿 化学方程式怎么写
 downsman1年前5
downsman1年前5 -
 老葱的星期天 共回答了16个问题
老葱的星期天 共回答了16个问题 |采纳率87.5%4FeS2+11O2==(煅烧)8SO2+2Fe2O31年前查看全部
- 以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:
以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:

(1)写出流程图中一种氧化物的名称______.
(2)将黄铁矿粉碎,目的是______.
(3)流程中SO2转化为SO3的化学方程式为2SO2+O2
2SO3催化剂 .△ 2SO2+O2.
2SO3催化剂 .△
(4)实验室稀释浓硫酸应注意什么?______.
(5)炉渣(Fe2O3)在工业上可用来______写出工业上以Fe2O3 为原料生产铁的化学方程式3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3.
2Fe+3CO2高温 . 861016520ppp1年前1
861016520ppp1年前1 -
 庚宝呵呵 共回答了24个问题
庚宝呵呵 共回答了24个问题 |采纳率91.7%解题思路:(1)氧化物是由两种元素组成,一种元素是氧元素的化合物;
(2)黄铁矿粉碎会增大反应物的接触面积加快反应速度;
(3)根据化学方程式的书写考虑;
(4)根据浓硫酸的稀释方法考虑;
(5)根据氧化铁可以用来炼铁考虑.(1)二氧化硫或三氧化硫或三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物;
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;
(3)反应物是二氧化硫和氧气,生成物是三氧化硫,用观察法配平,反应条件是催化剂和加热,所以方程式是:2SO2+O2
催化剂
.
△2SO3;
(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌;
(5)炉渣(Fe2O3)可以用来炼铁,一氧化碳与氧化铁反应生成铁和二氧化碳,所以可以用做冶铁原料,反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,根据得失氧进行配平,反应条件是高温,所以方程式是:3CO+Fe2O3
高温
.
2Fe+3CO2.
故答案为:(1)二氧化硫(或三氧化硫或三氧化二铁);(2)增大反应物的接触面积;(3)2SO2+O2
催化剂
.
△2SO3;(4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中;(5)炼铁;3CO+Fe2O3
高温
.
2Fe+3CO2.点评:
本题考点: 物质的相互转化和制备;浓硫酸的性质及浓硫酸的稀释;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题的关键是要知道氧化物的特点,知道反应物接触面积越大,反应越剧烈,熟悉方程式的书写注意事项,知道浓硫酸的稀释方法.1年前查看全部
- 将黄铁矿煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4.溶解过程中需保持溶液足够酸性,其原因是?
 舞台上的孤独1年前1
舞台上的孤独1年前1 -
 weilan37 共回答了19个问题
weilan37 共回答了19个问题 |采纳率94.7%因为铁离子和亚铁离子
在弱酸性,中性,碱性条件下会水解
使得制取的硫酸亚铁会转化为氢氧化铁
所以保持溶液足够酸性,使得不让铁离子和亚铁离子水解1年前查看全部
- (2011•江山市模拟)以黄铁矿为原料生产硫酸的主要设备是沸腾炉、(炉气精制)、接触室和吸收塔等.
(2011•江山市模拟)以黄铁矿为原料生产硫酸的主要设备是沸腾炉、(炉气精制)、接触室和吸收塔等.
(1)请写出炉气制造即沸腾炉中黄铁矿燃烧的化学方程式4FeS2+11O2
2Fe2O3+4SO2高温 .4FeS2+11O2.
2Fe2O3+4SO2高温 . (2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
(2)炉气精制的作用是将含SO2进行除法和水洗.而精制炉气即SO2的催化氧化,在接触室中进行.
A、精制炉气(含SO2体积分数为7%、O2为11%、N2为82%)中SO2平衡转化率与温度及压强关系如图1所示.在实际生产中,SO2催化氧化反应的条件选择常压、450℃左右(对应图中A点),而没有选择SO2转化率更高的B或C点对应的反应条件,其原因分别是______、______.
B、接触室中2SO2(g)+O2(g)
2SO3(g),反应过程的能量变化如图2所示.催化剂 .△
已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.请回答下列问题: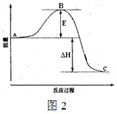
①图中C点表示______,E的大小对该反应的反应热______(填“有”或“无”) 影响.该反应通常用V2O5作催化剂,加V2O5会使图中B点______(填“升高”或“降低”).
②反应达到平衡时,平衡常数表达式K=c2(SO3) c2(SO2)c(O2) ,升高温度,K值______(填“增大”、“减小”或“不变”);图中△H=______kJ•mol-1.c2(SO3) c2(SO2)c(O2)
(3)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO3和NH4HSO3的混合物.取不同质量的铵盐,分别加入x mol/L的50.00mL NaOH溶液中,经沸水浴(此温度下铵盐自身不分解)加热使氨气全部逸出,干燥后用浓硫酸完全吸收.实验数据如下:
①该铵盐中(NH4)2SO3和NH4HSO3的物质的量之比为______.实验次数 铵盐质量(g) 浓硫酸增加的质量(g) 第一次 1.570 0.340 第二次 3.140 0.680 第三次 4.710 0.510 第四次 6.280 0
②x的值为______. XUANXUAN1001年前1
XUANXUAN1001年前1 -
 xingnvhai 共回答了17个问题
xingnvhai 共回答了17个问题 |采纳率88.2%解题思路:(1)结合工业制硫酸的原理书写化学方程式;
(2)A、根据图中所示,结合实际生成和需要,在常压下二氧化硫的转化率已经很高了,再加压需要对设备更新投入,且提高的余地很小,无经济效益;温度过低,反应速率低生产周期长影响生成效益;
B、根据图形分析结合能量高低进行判断,催化剂只改变反应的活化能不改变平衡,反应的焓变只与起始和终了物质的能量有关,与反应过程无关,运用化学平衡的理论,改变条件,依据平衡移动的方向来分析判断,K值只随温度的变化而变化;
(3)本反应历程是:OH-首先是和NH4HSO3中的H+反应,随后有多的OH-再和NH4+反应放出氨气,所以随着铵盐的量的增大,NH4HSO3的量也增大,放出的氨气的量会为0.浓硫酸增加的质量就是氨气的质量.第一次和第二次放出的氨气的量是一样的,所以说第一次肯定是OH-的量过量.利用第二次的量计算(因为是OH-不足).(1)根据反应原料写出化学方程式4FeS2+11O2
高温
.
2Fe2O3+4SO2,故答案为4FeS2+11O2
高温
.
2Fe2O3+4SO2
(2)①E为活化能,不影响化学反应能量,加入催化剂可改变反应历程并降低活化能.
②K只与温度相关的函数,升高温度,由于本反应为放热反应,平衡向逆移动,故K减小;图中表示的是反应2SO2(g)+O2(g)
催化剂
.
△2SO3(g),表示2mol二氧化硫反应放出的热量,已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1,所以图中的焓变为99kJ•mol-1×2=198KJ•mol-1,
故答案为:①生成物能量,无,降低.②,减小,-198.
(3)本反应历程是:OH-首先是和NH4HSO3中的H+反应,随后有多的OH-再和NH4+反应放出氨气,所以随着铵盐的量的增大,NH4HSO3的量也增大,放出的氨气的量会为0.浓硫酸增加的质量就是氨气的质量.第一次和第二次放出的氨气的量是一样的,所以说第一次肯定是OH-的量过量.利用第二次的量计算(因为是OH-不足).
设:(NH4)2SO3的物质的量为a,NH4HSO3的物质的量为b
116a+99b=3.140(质量守恒)…①
17(2a+b)=0.680(元素守恒)…②
解得a=0.010mol,b=0.020mol,即(NH4)2SO3和NH4HSO3的物质的量之比为1:2.
再根据(NH4)2SO3~2NaOH,NH4HSO3~NaOH,可算出x=1.2mol/L.
故答案为:①1:2.②1.2.点评:
本题考点: 工业制取硫酸;化学反应中能量转化的原因;化学平衡常数的含义.
考点点评: 本题考查了影响化学平衡的因素,利用平衡进行工业生产的条件选择,反应焓变的计算和影响因素,平衡常数的书写与判断,元素守恒、质量守恒的计算应用等知识.1年前查看全部
- 以黄铁矿(主要成分为二硫化亚铁,FeS2)为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、
以黄铁矿(主要成分为二硫化亚铁,FeS2)为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、
以黄铁矿(主要成分为二硫化亚铁,FeS2)为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、CaO、MgO等。现以硫酸渣制备铁红(Fe2O3)的过程 红铁的主要成分 lidaoxiang1001年前2
lidaoxiang1001年前2 -
 zdaceng 共回答了15个问题
zdaceng 共回答了15个问题 |采纳率93.3%Fe2O3加硫酸溶解,溶液成黄色
SiO2加氢氧化钠溶解,溶液呈粘稠的液体1年前查看全部
- (2014•闸北区二模)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40
(2014•闸北区二模)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2(约45%)、Fe2O3(约40%)、Al2O3(约10%)和MgO(约5%).
下表列出了相关金属离子生成氢氧化物沉淀的pH:
某同学设计了如下方案,分离样品中各种金属元素,请回答下列问题.金属离子 开始沉淀的pH 沉淀完全的pH Fe3+ 2.2 3.2 Al3+ 3.7 4.7 Mg2+ 9.6 11.1 
(1)试剂A的化学式:______;固体C的化学式:______;操作I的名称:______;
(2)请你按上述框图形式进一步完成由“溶液D”到“Al2O3”的流程(注明试剂、条件和操作);为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O
(3)若用铁粉还原Fe3+,测得的铁元素的含量______(填“偏大”或“偏小”或“不变”);如何确定Fe3+已全部被还原:______;
(4)判断到达滴定终点的现象是______;
(5)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100mL溶液,移取25.00mL,试样溶液,用1.000×10-2mol/L KMnO4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00mL,则硫酸渣中铁元素的质量分数是______. 海洋小舟1年前1
海洋小舟1年前1 -
 jetrocky 共回答了19个问题
jetrocky 共回答了19个问题 |采纳率94.7%解题思路:流程依据废渣溶于过量盐酸得到溶液B中含有溶质为:MgCl2、AlCl3、FeCl3和过量HCl;B溶液中加入氢氧化钠溶液,调节溶液PH=3.2后,生成氢氧化铁沉淀;和滤液MgCl2、AlCl3和过量HCl;在加入过量氢氧化钠溶液,过滤得到滤液中为NaCl,NaAlO2;通入二氧化碳气体生成氢氧化铝沉淀,过滤得到氢氧化铝沉淀,灼烧得到Al2O3;
(1)根据废渣主要化学成分中SiO2、Fe2O3、Al2O3和MgO的性质判断应加入过量盐酸或稀硫酸,Fe2O3碱性氧化物,Al2O3两性氧化物、MgO碱性氧化物都溶于过量的酸,只有二氧化硅不溶,经过滤后可分离;根据表中数据可知调节溶液PH=3.2后,生成氢氧化铁沉淀;
(2)依据流程图画出;
(3)若用铁粉还原Fe3+,会引入更多的铁元素,使测得的铁元素的含量偏大;可根据Fe3+的性质确定Fe3+是否已全部被还原;
(4)根据KMnO4标准溶液本身就是一种指示剂;
(5)利用关系式法计算和质量分数的概念来分析.依据废渣溶于过量盐酸得到溶液B中含有溶质为:MgCl2、AlCl3、FeCl3和过量HCl;B溶液中加入氢氧化钠溶液,调节溶液PH=3.2后,生成氢氧化铁沉淀;和滤液MgCl2、AlCl3和过量HCl;在加入过量氢氧化钠溶液,过滤得到滤液...
点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查了设计流程分离物质,试剂选择和反应现象,反应特征的应用,滴定实验的终点判断,滴定过程的计算应用,题目难度中等.1年前查看全部
- 工业上黄铁矿原料制H2SO4,请回答下列问题:
工业上黄铁矿原料制H2SO4,请回答下列问题:
(1)燃烧黄铁矿是在______(填设备名称)中进行的.
(2)在接触室中生成SO3反应条件的选择,可以完全用勒夏特列原理解释的是(填标号)______.
A.温度为400℃-500℃B.常压C.O2过量D.用V2O5作催化剂
(3)硫酸工业的尾气中,除含有N2、O2外,还含有SO2、微量SO3和酸雾,为保护环境和提高综合经济效益,应尽可能将尾气中的SO2转化为有用的副产品.处理方法可采用过量氨水吸收,主反应的化学方程式为______,同时还能发生多个反应,写出其中可能发生的两个氧化还原反应的反应式(或离子方程式):
______.
(4)SO2尾气可用饱和Na2SO3溶液吸收而得重要化工原料,反应的离子方程式为______.
(5)黄铁矿的煅烧产物Fe2O3(或Fe3O4等)溶于H2SO4后,加入铁粉,可制备FeSO4.酸溶过程中需保持溶液足够酸性,其原因是______. 夜月悄悄1年前1
夜月悄悄1年前1 -
 longzhu8888 共回答了15个问题
longzhu8888 共回答了15个问题 |采纳率86.7%解题思路:(1)根据工艺流程分析;
(2)能够使平衡发生移动,则可以用勒夏特列原理解释;
(3)根据溶液中的成分和物质的性质分析;
(4)SO2能与饱和Na2SO3溶液反应;
(5)Fe3+与Fe2+易水解,Fe2+易被氧化成Fe3+.(1)燃烧黄铁矿是在沸腾炉中与氧气反应,故答案为:沸腾炉;
(2)能够使平衡向正方向移动的条件,有利于三氧化硫的生成,则可以用勒夏特列原理解释:
A.二氧化硫与氧气反应是放热反应,温度为400℃-500℃,平衡逆移,不利于三氧化硫的生成,故A错误;
B.高温有利于三氧化硫的生成,但是高压对转化率改变不大,而且提高了生产成本,所以采用常压,故B错误;
C.O2过量,能促使平衡正移,提高二氧化硫的转化率,故C正确;
D.用V2O5作催化剂,能加快反应速率,但是平衡不移动,故D错误;
故答案为:C;
(3)氨水中的NH3•H2O能与二氧化硫反应,其反应方程式为:SO2+NH3•H2O=(NH4)2SO3,亚硫酸和亚硫酸根离子中的硫元素易被氧气氧化,其反应方程为2H2SO3+O2=2H2SO4 2SO32-+O2=2SO42-,
故答案为:SO2+NH3•H2O=(NH4)2SO3;2H2SO3+O2=2H2SO4 2SO32-+O2=2SO42-;
(4)SO2能与饱和Na2SO3溶液反应生成NaHSO3,其反应方程式为SO2+H2O+SO32-=2HSO3-,故答案为:SO2+H2O+SO32-=2HSO3-;
(5)Fe2O3(或Fe3O4等)溶于H2SO4后,生成的Fe3+与Fe2+易水解,Fe2+易被氧化成Fe3+,所以要加入Fe粉和酸,抑制Fe3+与Fe2+的水解,并防止Fe2+被氧化成Fe3+,
故答案为:抑制Fe3+与Fe2+的水解,并防止Fe2+被氧化成Fe3+.点评:
本题考点: 工业制取硫酸.
考点点评: 本题考查了元素及化合物的性质,涉及平衡的移动,化学方程式和离子方程式的书写等,考查的知识点较多,难度中等.1年前查看全部
- 含FeS2百分之80的黄铁矿在煅烧是有百分之5的硫损失,二氧化硫生成三氧化硫的转化率为百分之80,
含FeS2百分之80的黄铁矿在煅烧是有百分之5的硫损失,二氧化硫生成三氧化硫的转化率为百分之80,
要生产百分之98的硫酸1吨,需要这样的硫铁矿多少吨
希望在2天内回答出来
 粉红心情1年前1
粉红心情1年前1 -
 诗人的眼泪_ss 共回答了14个问题
诗人的眼泪_ss 共回答了14个问题 |采纳率85.7%设硫酸中硫的质量为X千克,需要这样的硫铁矿Y吨
S……H2SO4
32 98
X 1000*98%=980
X/32=980/98
X=320千克
由于二氧化硫生成三氧化硫的转化率为百分之80,因此二氧化硫含硫320/80%=400千克
硫铁矿在煅烧是有百分之5的硫损失,因此硫铁矿中应含硫400/(1-5%)=421.1千克
FeS2…………2S
120 64
Y*80%*1000 421.1
800Y/120=421.1/64
Y=0.987吨1年前查看全部
- 某硫酸厂用750吨黄铁矿(含FeS2 80%)为原料(所含杂质不参加反应),计算能生产98%的浓硫酸多少吨
 0vibg1年前1
0vibg1年前1 -
 muyunshe 共回答了19个问题
muyunshe 共回答了19个问题 |采纳率84.2%750t*80%=600t
FeS2----2S----2H2SO4
120 196
600t x*98%
120/600t=196/(x*98%)
x=1000t1年前查看全部
- 某化工厂生产硫酸,使用一种含有SiO2杂质的黄铁矿样品.
某化工厂生产硫酸,使用一种含有SiO2杂质的黄铁矿样品.
经过测试该矿石,发现1g矿石样品在氧气中充分燃烧,残余固体是0.76g.若取1t该矿石,可值得98%的浓硫酸多少吨 苏格格1年前1
苏格格1年前1 -
 哦哦18 共回答了17个问题
哦哦18 共回答了17个问题 |采纳率94.1%黄铁矿和空气反应的化学方程式:4FeS2+11O2=2Fe2O3+8SO2残余固体是0.76g,残余的就是二氧化硅和杂质还有三氧化二铁,根据差量设FeS2为Mg4FeS2(480)+11O2=2Fe2O3(320)+8SO2(512) △m(160)△m=0.24g 所以列式可...1年前查看全部
- :将0.5080g黄铁矿(FeS2)试样分解后,得1.561gBaSO4.若溶液中的铁沉淀为Fe(OH)3,灼烧可得Fe
:将0.5080g黄铁矿(FeS2)试样分解后,得1.561gBaSO4.若溶液中的铁沉淀为Fe(OH)3,灼烧可得Fe2O3多少克?
 babyqiu20051年前1
babyqiu20051年前1 -
 wabt_002 共回答了19个问题
wabt_002 共回答了19个问题 |采纳率89.5%根据硫元素守恒,可得
FeS2 2 BaSO4
根据铁元素守恒,可得
FeS2 1/2 Fe2O3
所以2 BaSO4 1/2 Fe2O3
· 2*233.37 0.5*159.7
· 1.561 g m
2*233.37/(159.7*0.5) = 1.561 g / m
所以m = 0.267 g
灼烧可得Fe2O3 0.267 g1年前查看全部
- 以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:
以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如图:

(1)写出流程图中一种氧化物的名称______.
(2)将黄铁矿粉碎,目的是______.
(3)流程中SO2转化为SO3的化学方程式为2SO2+O2
2SO3催化剂 .△ 2SO2+O2.
2SO3催化剂 .△
(4)实验室稀释浓硫酸应注意什么?______. 江边小筑1年前1
江边小筑1年前1 -
 东侃侃西侃侃 共回答了17个问题
东侃侃西侃侃 共回答了17个问题 |采纳率100%解题思路:(1)氧化物是由两种元素组成,一种元素是氧元素的化合物;(2)黄铁矿粉碎会增大反应物的接触面积加快反应速度;(3)根据化学方程式的书写考虑;(4)根据浓硫酸的稀释方法考虑.(1)二氧化硫、三氧化硫、三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物;
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度;
(3)反应物是二氧化硫和氧气,生成物是三氧化硫,用观察法配平,反应条件是催化剂和加热,所以方程式是:2SO2+O2
催化剂
.
△2SO3;
(4)浓硫酸的稀释方法是:将浓硫酸沿着容器壁慢慢倒入水中,并用玻璃棒不断搅拌;
故答案为:(1)二氧化硫(或三氧化硫或三氧化二铁);
(2)增大反应物的接触面积;
(3)2SO2+O2
催化剂
.
△2SO3;
(4)将浓硫酸沿器壁慢慢倒入水中,边倒边搅拌,且不可将水倒入浓硫酸中.点评:
本题考点: 物质的相互转化和制备;浓硫酸的性质及浓硫酸的稀释;从组成上识别氧化物;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题的关键是要知道氧化物的特点,知道反应物接触面积越大,反应越剧烈,熟悉方程式的书写注意事项,知道浓硫酸的稀释方法.1年前查看全部
- (2011•海门市二模)工业制硫酸主要分造气、氧化反应和吸收三个阶段.硫酸的生产流程如下(其中黄铁矿的主要成分为FeS2
(2011•海门市二模)工业制硫酸主要分造气、氧化反应和吸收三个阶段.硫酸的生产流程如下(其中黄铁矿的主要成分为FeS2):

请结合硫酸的生产流程回答:
(1)流程中含Fe2O3炉渣的用途是:______;在反应室中要不断排出热气,才能维持反应室的温度恒定.说明反应室中的化学反应是______(填“放热”或“吸热”)反应.含有SO2的废气造成空气的危害是:______.
(2)实验室通过稀释98%的浓硫酸配制20%稀硫酸98g,则需要加水的质量为______.
(3)用含硫元素32%的黄铁矿在反应流程中有2%的硫受到损失而混入炉渣和废气中(假设在SO2、吸收中没有损失).则这种黄铁矿石10t可以制得98%的硫酸多少t? hhm1111年前1
hhm1111年前1 -
 jefferyhsu 共回答了22个问题
jefferyhsu 共回答了22个问题 |采纳率90.9%解题思路:(1)充分理解节能环保的重要性.煅烧黄铁矿时生成的固体是三氧化二铁,所以炉渣是三氧化二铁,三氧化二铁用来炼铁.二氧化硫能形成亚硫酸,形成酸雨;
(2)根据稀释前后溶质质量不变;
(3)根据反应前后元素质量不变故反应前和反应后硫元素质量相等.(1)炉渣的主要成分是三氧化二铁;二氧化硫易形成酸雨;故答案为:用来炼铁.放热、造成酸雨.
(2)根据稀释前后溶质质量不变设需98%的浓硫酸的质量为x
x×98%═98g×20%
x=20g
需要加水的质量为:98g-20g═78g
答:需要加水的质量为78g
故答案为:78g
(3)根据反应前后元素质量不变故反应前和反应后硫元素质量相等;可列等式.
设98%的硫酸的质量为y
10t×32%×(1-2%)=y×98%×[32/98]
y═9.8t
答:98%的硫酸的质量为9.8t点评:
本题考点: 物质的相互转化和制备;用水稀释改变浓度的方法;酸雨的产生、危害及防治;物质组成的综合计算;物质发生化学变化时的能量变化.
考点点评: 解答本题的关键是要掌握稀释前后溶质质量不变,反应前后元素质量不变的判断方法,只有这样才能对问题做出正确的判断.1年前查看全部
- 硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~900℃时,硫铁矿在纯净的氧气中煅烧,可能发生下列反
硫铁矿又称黄铁矿,是生产硫酸的原料,其主要成分为FeS2.850℃~900℃时,硫铁矿在纯净的氧气中煅烧,可能发生下列反应:
① 3FeS2+8O2→Fe3O4+6SO2 ② 4FeS2+11O2→2Fe2O3+8SO2
⑵480 g纯净的FeS2在氧气中完全反应,若所得固体中,Fe和O的物质的量之比
n(Fe)∶n(O)=4∶a,此时消耗氧气b mol.
② b的最小值为_______▲ ____. tt深圳010101年前1
tt深圳010101年前1 -
 平安成都 共回答了12个问题
平安成都 共回答了12个问题 |采纳率100%从题目给出的反应方程式可以看出,FeS2中S元素消耗O2不管按照哪个反应进行都是一样多的(因为都是生成SO2),耗氧量多少关键是看Fe元素最后转化成什么.
如果转化为含O较少的Fe3O4,消耗氧就少;反之转化成含O较多的Fe2O3,则消耗O2就多.
480gFeS2物质的量为480g÷120g/mol=4mol,其中的含8molS原子和4molFe原子,S转化为SO2消耗8molO2,则Fe消耗的O2就是(b-8)mol,根据题意可知n(Fe) : n(O) = 4 : a = 4 : 2(b-8),解得:2b = a+16.
当FeS2全部生成含氧的质量分数较大的Fe2O3时,消耗氧最多,Fe2O3中n(Fe) : n(O) = 4 : a = 2 : 3,也就是a = 6,此时2b = a+16 = 22,b = 11.
当FeS2全部生成含氧的质量分数较小的Fe3O4时,消耗氧最少,Fe2O3中n(Fe) : n(O) = 4 : a = 3 : 4,也就是a = 16/3,此时2b = a+16 = 64/3,b = 32/3.
这是因为要解释a与b的关系才这样算的,如果只是要求出耗氧量的最小值,完全可以根据反应方程式计算得出.
3FeS2+8O2→Fe3O4+6SO2
3 8
4 x
x = 32/3
4FeS2+11O2→2Fe2O3+8SO2
4 11
4 y
y = 111年前查看全部
- 工业上制备100吨98%的浓硫酸 需含80% FeS2的黄铁矿多少吨
 D四代1年前1
D四代1年前1 -
 lyd827 共回答了11个问题
lyd827 共回答了11个问题 |采纳率72.7%FeS2 ~ 2*H2SO4
120 2*98
X*80% 100*98%
按上述方程算得:X=75,即要80%黄铁矿75吨.1年前查看全部
- 赤铁矿石和黄铁矿石哪个更适合炼铁
赤铁矿石和黄铁矿石哪个更适合炼铁
理由是什么 dyw123s1年前3
dyw123s1年前3 -
 suiyi332004 共回答了17个问题
suiyi332004 共回答了17个问题 |采纳率88.2%赤铁矿石适合 因为黄铁矿石中有硫酸根 燃烧后会生成二氧化硫 污染空气1年前查看全部
- 【化学与技术】以黄铁矿为原料(主要成分是FeS 2 )为原料,生产硫酸的简要流程图如下: (1)写出流程图中一种氧化物的
【化学与技术】
以黄铁矿为原料(主要成分是FeS 2 )为原料,生产硫酸的简要流程图如下: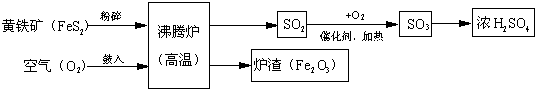
(1)写出流程图中一种氧化物的名称 。
(2)将黄铁矿粉碎,目的是 。
(3)流程中SO 2 转化为SO 3 的化学方程式为 。
(4)炉渣(Fe 2 O 3 )在工业上可用来 。 mickeymim1年前1
mickeymim1年前1 -
 城市猎人BG 共回答了22个问题
城市猎人BG 共回答了22个问题 |采纳率81.8%1年前查看全部
- 黄铁矿主要成分是FeS2,其中硫负价只有-2,那么铁是几价?血求.
 黑色紫色1年前5
黑色紫色1年前5 -
 BBT晓英 共回答了13个问题
BBT晓英 共回答了13个问题 |采纳率84.6%硫的化合价也是可变的,不只是-2价,在黄铁矿中铁是+2价,硫是-1价.1年前查看全部
- 1.某化工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品.已知黄铁矿与与氧气反映的化学方程式为4FeS2+11O2=2F
1.某化工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品.已知黄铁矿与与氧气反映的化学方程式为4FeS2+11O2=2Fe2O3+8SO2若取一吨该矿石,可制的98%的浓硫酸多少吨.
2.若往电炉里加入二氧化硅和适量的混合物通电失他们发生反应如下.SiO2+2C=Si+2CO↑
①求生成物的质量各式多少?生成一氧化碳再标准状况下体积是多少?②写出工业提纯硅的有关反应化学方程式. 天天331281年前1
天天331281年前1 -
 重阳子 共回答了19个问题
重阳子 共回答了19个问题 |采纳率94.7%第一问抓住质量守恒定律.S的总质量不变.第二问什么都没告诉怎么算啊...1年前查看全部
- 黄铁矿和王水反应方程式
 超越第三者1年前1
超越第三者1年前1 -
 bobbie221 共回答了17个问题
bobbie221 共回答了17个问题 |采纳率94.1%FeS2+5HNO3+3HCl=FeCl3+2H2SO4+5NO↑+2H2O1年前查看全部
- 胆矾(CuSO4.5H2O)当它溶于水渗入地下,遇到黄铁矿(FeS2),铜将以辉铜矿(Cu2S)的形式沉积,反应得到的铁
胆矾(CuSO4.5H2O)当它溶于水渗入地下,遇到黄铁矿(FeS2),铜将以辉铜矿(Cu2S)的形式沉积,反应得到的铁和硫的混合物进入水溶液,该溶液无臭味,透明不浑浊,绿色,呈强酸性,试用一个方程式来表示.
 yeyi1281年前1
yeyi1281年前1 -
 从青岛到上海 共回答了14个问题
从青岛到上海 共回答了14个问题 |采纳率92.9%反应物有CuSO4、FeS2,生成物中有Cu2S.
溶液显绿色 说明Fe2+存在
溶液无臭味,透明,不浑浊,呈强酸性 ,可能存在(SO4)2-
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO41年前查看全部
- 把一克含SiO2的黄铁矿样品在氧气流中灼烧,反应后完全得到0.88g残渣
把一克含SiO2的黄铁矿样品在氧气流中灼烧,反应后完全得到0.88g残渣
已知SiO2不与氧气反应,则铁矿的纯度A33%B36%C78%D88% 娃哈哈1121年前1
娃哈哈1121年前1 -
 vvwwvv 共回答了18个问题
vvwwvv 共回答了18个问题 |采纳率83.3%用质量差量法计算
设纯度x
4FeS2 + 11O2 =高温= 2Fe2O3 + 8SO2----固体质量减少
4*120----------------2*160--------------------------160
1g*x------------------------------------------------(1-0.88)g
x=36%
即B1年前查看全部
- 把1g含脉石(SiO2)的硫铁矿样品在氧气中灼烧,反应完全后得残渣0.78g,则此黄铁矿的纯度是 A,33% B,66%
把1g含脉石(SiO2)的硫铁矿样品在氧气中灼烧,反应完全后得残渣0.78g,则此黄铁矿的纯度是 A,33% B,66% C,78%
把1g含脉石(SiO2)的硫铁矿样品在氧气中灼烧,反应完全后得残渣0.78g,则此黄铁矿的纯度是
A,33% B,66% C,78% D,88%
为什么此题中生成的是正三价的 铁,而在别的题目中,铁在氧气中生成四氧化三铁,在空气中点燃生成三氧化二铁 qihuoyj1年前3
qihuoyj1年前3 -
 ljzhang 共回答了16个问题
ljzhang 共回答了16个问题 |采纳率81.3%4FeS2+11O2==2Fe2O3+8SO2 质量减小
480 320 160
x 1-0.78
x=0.66
黄铁矿的纯度是0.66/1*100%=66%
是B.
注意:Fe在纯O2中点燃,得到Fe3O4.
铁在空气中不能燃烧,只能加热缓慢氧化,得到铁锈(Fe2O3)
在空气中灼烧含铁物质得到的是Fe2O31年前查看全部
- 当胆矾渗入地下,遇到黄铁矿(FeS2)时可生成辉铜矿(Cu2S),同时还升成FeSO4和H2SO4,反应中Cu离子与Fe
当胆矾渗入地下,遇到黄铁矿(FeS2)时可生成辉铜矿(Cu2S),同时还升成FeSO4和H2SO4,反应中Cu离子与FeS2的物质的量比是?
 hchott1年前2
hchott1年前2 -
 倦倚西风夜已昏 共回答了18个问题
倦倚西风夜已昏 共回答了18个问题 |采纳率94.4%反应中Cu2+与FeS2的物质的量之比是14∶5
14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4
由题给的信息可知:反应物有CuSO4?5H2O、FeS2、还有可能有H2O.生成物有中Cu2S,硫和铁的价态运用直接法可确定:排除了硫以-2,0,+4等价态进入水溶液的可能,只能以SO42-存在.1年前查看全部
- 把1g含脉石(SiO2)的硫铁矿样品在氧气中灼烧,反应完全后得残渣0.78g,则此黄铁矿的纯度是
把1g含脉石(SiO2)的硫铁矿样品在氧气中灼烧,反应完全后得残渣0.78g,则此黄铁矿的纯度是
A,33% B,66% C,78% D,88%
我需要详细的解法 hexinoo1年前1
hexinoo1年前1 -
 pzw4850 共回答了16个问题
pzw4850 共回答了16个问题 |采纳率93.8%4FeS2+11O2==2Fe2O3+8SO2 质量减小
480 320 160
x 1-0.78
x=0.66
黄铁矿的纯度是0.66/1*100%=66%
正确答案是B.1年前查看全部
- 现有磁铁矿 黄铁矿 赤铁矿 .请从多种角度分析三种矿石中哪种不适合同来炼铁---,原因是?
 mixib1年前2
mixib1年前2 -
 lechang531 共回答了25个问题
lechang531 共回答了25个问题 |采纳率92%黄铁矿是铁与硫的化合物,工业上用来制取硫酸,焙烧后的炉渣含有大量的铁,在拿来炼铁,赤铁矿与磁铁矿都是工业上炼铁的主要原料,黄铁矿因为含大量的硫,在焙烧前是绝对不能炼铁的,因为黄铁矿较易燃烧,只有经过焙烧,将其中的硫取代为氧后才能用来炼铁1年前查看全部
- 燃烧含FeS2 80%的黄铁矿制硫酸的利用率为90%,用75吨该黄铁矿制得硫酸铵79.2吨,则用黄铁矿制硫酸铵的损失率是
燃烧含FeS2 80%的黄铁矿制硫酸的利用率为90%,用75吨该黄铁矿制得硫酸铵79.2吨,则用黄铁矿制硫酸铵的损失率是多少,
 tianping_03081年前1
tianping_03081年前1 -
 raupe 共回答了20个问题
raupe 共回答了20个问题 |采纳率85%4FeS2 + 11O2 =△= 2Fe2O3 + 8SO2
m(FeS2)=75000000*0.8=60000000 g
n(FeS2)=60000000/120=500000 mol
n(SO2)=500000*2=1000000 mol
n(SO3理论上)=1000000 mol
n(H2SO4理论上)=1000000 mol
n(硫酸铵理论上)=1000000 mol
m(硫酸铵理论上)=1000000*132/1000000=132 t
损失硫酸铵质量=132-79.2=52.8 t
损失率=52.8/132=40%1年前查看全部
- FeS2是黄铁矿的主要成分,但FeS2中铁元素和硫元素各几价?
 adfsdsfadsfdasfa1年前2
adfsdsfadsfdasfa1年前2 -
 顺谁自然 共回答了16个问题
顺谁自然 共回答了16个问题 |采纳率75%铁是正二价的.
FeS2中硫是-1价1年前查看全部
- 用硫酸钡沉淀法测定黄铁矿中硫酸的含量时,称取试样0.2436g最后得到硫酸钡沉淀0.
用硫酸钡沉淀法测定黄铁矿中硫酸的含量时,称取试样0.2436g最后得到硫酸钡沉淀0.
128g计算试样中硫的质量分数. happyhxf1年前1
happyhxf1年前1 -
 kevinzhangfengls 共回答了20个问题
kevinzhangfengls 共回答了20个问题 |采纳率90%你确定题目没有表达错误?黄铁矿中硫酸的含量?!1年前查看全部
- 为什么黄铁矿在氧气中灼烧生成氧化铁而不是四氧化三铁
 提前还贷1年前1
提前还贷1年前1 -
 l82916 共回答了19个问题
l82916 共回答了19个问题 |采纳率78.9%因为是完全燃烧,将二价铁完全氧化成三价铁了.
而Fe3O4是Fe2O3·FeO.1年前查看全部
- ①盐酸②碳酸钠溶液③水银④黄铁矿⑤硫磺⑥碘酒 如何区分 分类标准;(1) ,共包括三种物质(2)
 踢风浪仔1年前2
踢风浪仔1年前2 -
 wanghuiaijjj 共回答了14个问题
wanghuiaijjj 共回答了14个问题 |采纳率78.6%溶液 ①盐酸②碳酸钠溶液⑥碘酒1年前查看全部
- ①盐酸②碳酸钠溶液③水银④黄铁矿⑤硫磺⑥碘酒 如何区分 分类标准;(1) ,共包括三种物质(2)
 dorissong1131年前3
dorissong1131年前3 -
 magnifico 共回答了15个问题
magnifico 共回答了15个问题 |采纳率86.7%(1)溶液
(2)①盐酸②碳酸钠溶液⑥碘酒1年前查看全部
- 化学中h2o2在黄铁矿的作用
 清风之翼1年前1
清风之翼1年前1 -
 sz12 共回答了15个问题
sz12 共回答了15个问题 |采纳率86.7%黄铁矿中FeS2.双氧水用于氧化硫生成硫的氧化物后溶于酸,有助于黄铁矿的溶解.1年前查看全部
- 某工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品.知黄铁矿与氧气反应的化学方程式为FeS2+11O2=Fe2O3+8S
某工厂生产硫酸,使用一种含杂质为25%的黄铁矿样品.知黄铁矿与氧气反应的化学方程式为FeS2+11O2=Fe2O3+8So2.
若取一吨矿石,可制得98%的浓硫酸多少吨,假如生产过程硫的损失不记,求详解,若假设生产过程中硫损失2%呢?求详解 遗失的青春1年前1
遗失的青春1年前1 -
 朴洙秀 共回答了21个问题
朴洙秀 共回答了21个问题 |采纳率100%1吨该矿石含杂质为25%,则含75%的黄铁矿.1吨中有750kg黄铁矿.
4FeS2+11O22Fe2O3+8SO2
480 512
750kg x
列出式子,算得x=800kg
2SO2+O2+2H2O=2H2SO4
128 196
800 y
算得y=1225kg
1225÷98%=1250kg1年前查看全部
- 黄铁矿制二氧化硫反应是吸热还是放热
 西湖鱼鱼1年前1
西湖鱼鱼1年前1 -
 zy乐在其中 共回答了19个问题
zy乐在其中 共回答了19个问题 |采纳率84.2%可以利用热力学数据计算
4FeS2(s) + 11O2(g) = 2Fe2O3(s) + 8SO2(g)
△fHm,FeS2(g) = -177.9 kJ/mol
△fHm,O2(g) = 0
△fHm,Fe2O3(s) = -822.2 kJ/mol
△fHm,SO2(g) = -296.9 kJ/mol
反应的焓变△rHm = 8△fHm,SO2(g) + 2△fHm,Fe2O3(s) - 11△fHm,O2(g) - 4△fHm,FeS2(g)
= -3308.0 kJ/mol
△rHm < 0,说明反应放热,每摩尔FeS2参加反应时,放出的热量为3308.0/4 = 827.0 kJ.1年前查看全部
- 硫酸工业上大多用接触法制硫酸(设空气中氧气的体积分数为20%),为使黄铁矿煅烧充分,常通入过量40%的空气,将上述炉气经
硫酸工业上大多用接触法制硫酸(设空气中氧气的体积分数为20%),为使黄铁矿煅烧充分,常通入过量40%的空气,将上述炉气经净化除尘后直接送入接触室,气体体积减少了5%(同温同压下测定),试计算SO2的转化率
 端木秋1年前1
端木秋1年前1 -
 testing33333 共回答了18个问题
testing33333 共回答了18个问题 |采纳率94.4%解析:
相关反应方程式:
4FeS2 + 11O2 ―(高温煅烧)→ 2Fe2O3 + 8SO2
2SO2 + O2 =(400℃~500℃,V2O5)= 2SO3 (=表示可逆符号)
通入过量40%的空气,那么氧气也同样过量40%,
则氧气初始计量 = 11 * 1.4 = 15.4,反应掉11体积的O2,剩余4.4体积O2
反应前空气总量 = 15.4 / 0.2 = 77 体积
第一步反应:消耗11体积O2,生成8体积SO2,反应后气体总量 = 77 - 11 + 8 = 74体积
第二步反应:气体体积减少了5%
设反应掉的SO2 体积 为 x,反应掉的O2 体积 为 y,生成的SO3体积 为 z,则有:
2SO2 + O2 =(400℃~500℃,V2O5)= 2SO3 (=表示可逆符号)………… △V
2 1 2 (2+1-2)
x y z 5%
解得:x = 10%,y = 5%,z = 10%
则SO2转化率 = (74*10%)*100% / 8 = 92.5 %1年前查看全部
- 关于硫酸的制法的一些问题..1黄铁矿焙烧前要粉碎,解释是黄铁矿不能燃烧..为什么错?2沸腾炉出来的炉气必须净化,因为杂质
关于硫酸的制法的一些问题..
1黄铁矿焙烧前要粉碎,解释是黄铁矿不能燃烧..为什么错?
2沸腾炉出来的炉气必须净化,因为杂质会和SO2反应..为什么错?
3SO2氧化成SO3时需要使用催化剂,因为要提高SO2的转化率...为什么错? wwxtu241年前1
wwxtu241年前1 -
 heqing1980 共回答了17个问题
heqing1980 共回答了17个问题 |采纳率70.6%黄铁矿可以燃烧,粉碎是为了彻底完全燃烧;
杂质气体会使催化剂钝化;
催化剂不能提高转化率.1年前查看全部
- (2011•淄博二模)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为SiO2:约45%,Fe2O3:约40%,
(2011•淄博二模)硫酸渣是用黄铁矿制造硫酸过程中排出的废渣,主要化学成分为sio2:约45%,fe2o3:约40%,al2o3:约10%,mgo:约5%.目前***已经在技术上取得突破--用硫酸渣炼铁.
i.某学生探究性学习小组的同学设计了不同的方案,用化学基本知识进行金属元素的提取实验(已知25℃氢氧化镁ksp=5.6×10-12;氢氧化铁ksp=3.5×10-38;一水合氨电离常数k=1.8×10-5,其饱和溶液中c(oh-)约为1×10-3mol•l-1).
方案一: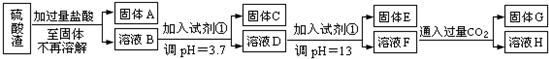
请回答:
(1)写出固体e的化学式:______.
(2)试剂①是______
a.氢氧化钠b.氧化铝c.氨水d.水
(3)若要准确测定溶液的ph是否达到3.7,下列物品中可供使用的是______
a.石蕊试液b.广泛ph试纸c.精密ph试纸d.ph计
(4)溶液h中溶质的化学式:______
(5)要将固体c、固体e和固体g都转化为相应的稳定的氧化物,需进行的实验操作为______.
(6)若不考虑溶液体积的变化,请计算溶液h中c(mg2+)=______.
方案二: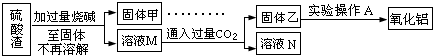
请回答:
(7)此方案的主要问题有:______
(8)写出由溶液m→固体乙这个过程中,最主要化学反应的离子方程式:______
ii.为了分析某硫酸渣中铁元素的含量,先将硫酸渣预处理,把铁元素还原成fe2+,再用kmno4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5fe2++mno4-+8h+=5fe3++mn2++4h2o.
(1)判断到达滴定终点的现象是______.
(2)某同学称取2.000g硫酸渣,预处理后在容量瓶中配制成100ml溶液,移取25.00ml,试样溶液,用1.000×10-2mol•l-1kmno4标准溶液滴定.达到滴定终点时,消耗标准溶液10.00ml,则残留物中铁元素的质量分数是______. vscrash1年前1
vscrash1年前1 -
 sntge123 共回答了18个问题
sntge123 共回答了18个问题 |采纳率77.8%解题思路:I.根据硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量盐酸时,二氧化硅和盐酸不反应,所以固体A是二氧化硅,氧化铁、氧化铝、氧化镁和盐酸反应,所以溶液B的溶质是氯化镁、氯化铁、氯化铝、盐酸(过量);向溶液B中加试剂①并调节溶液的pH值为3.7,结合题意溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,固体C是氢氧化铁;向溶液D中加入试剂①并调节溶液的pH值为13,溶液呈强碱性溶液,铝元素在溶液中以偏铝酸根离子存在,镁离子和氢氧根离子生成氢氧化镁沉淀,所以固体E是氢氧化镁;溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,所以G是氢氧化铝,
(1)固体E是氢氧化镁;
(2)试剂①是强碱溶液;
(3)根据pH值精确到小数点后一位;
(4)溶液F的溶质含有偏铝酸钠和氯化钠;
(5)根据难溶性碱加热分解;
(6)根据氢氧化镁Ksp=5.6×10-12来计算;
根据硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量氢氧化钠时,Fe2O3、MgO和氢氧化钠不反应,所以固体甲是Fe2O3、MgO,SiO2、Al2O3和氢氧化钠反应,所以溶液M的溶质是硅酸钠、偏铝酸钠、氢氧化钠(过量);向溶液M中通入过量二氧化碳气体,硅酸钠、偏铝酸钠、氢氧化钠都与二氧化碳反应,所以固体乙是硅酸、氢氧化铝,进行加热得到二氧化硅和氧化铝.
(7)根据产物和消耗的原料来分析;
(8)溶液主要含有硅酸钠;
II.(1)根据KMnO4标准溶液本身就是一种指示剂;
(2)利用关系式法计算和质量百分数的概念来分析.I.根据硫酸渣的成分为SiO2、Fe2O3、Al2O3、MgO,当向硫酸渣中加过量盐酸时,二氧化硅和盐酸不反应,所以固体A是二氧化硅,氧化铁、氧化铝、氧化镁和盐酸反应,所以溶液B的溶质是氯化镁、氯化铁、氯化铝、盐酸(过量);向溶液B中加试剂①并调节溶液的pH值为3.7,结合题意溶液pH=3.7时Fe3+已经沉淀完全知,试剂①是能和氯化铁反应生成沉淀的物质且和铝离子反应没有沉淀生成,所以试剂①只能是强碱溶液,固体C是氢氧化铁;向溶液D中加入试剂①并调节溶液的pH值为13,溶液呈强碱性溶液,铝元素在溶液中以偏铝酸根离子存在,镁离子和氢氧根离子生成氢氧化镁沉淀,所以固体E是氢氧化镁;溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,所以G是氢氧化铝,
(1)固体E是氢氧化镁,故答案为:Mg(OH)2;
(2)试剂①是强碱溶液,故选:A;
(3)因PH值精确到小数点后一位,而石蕊试液测得的PH值在一个范围内,广泛pH试纸测得的PH值是一个整数,精密pH试纸、pH计均可准确到小数点后一位,故选:CD;
(4)溶液F的溶质含有偏铝酸钠和氯化钠,向F溶液中通入过量二氧化碳气体,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀和碳酸氢钠,故答案为:NaCl、NaHCO3;
(5)固体C是氢氧化铁,固体E是氢氧化镁,固体G是氢氧化铝,加热均可分解得到对应的氧化物,故答案为:灼烧;
(6)因溶液的PH值为13,C(OH-)=10-1mol•L-1,Ksp=C(Mg2+)×C2(OH-)=C(Mg2+)×10-2=5.6×10-12,所以C(Mg2+)=5.6×10-10 mol•L-1,故答案为:5.6×10-10 mol•L-1;
(7)①产品不纯,最后产物中大多数是二氧化硅;②步骤多试剂消耗题量大,故答案为:①产品不纯,最后产物中大多数是二氧化硅;②步骤多试剂消耗题量大;
(8)溶液主要含有硅酸钠,硅酸钠和二氧化碳反应生成硅酸沉淀和碳酸氢钠,方程式为:Na2SiO3+2CO2+2H2O=H2SiO3↓+2NaHCO3,故答案为:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO32-;
II.(1)因KMnO4标准溶液本身就是一种指示剂,故答案为:与滴下最后一滴KMnO4标准溶液时,溶液颜色变为紫红色,且在半分钟内不褪色;
(2)利用关系式法计算:
5Fe2+~MnO4-
2×10-3mol 1.000×10-2mol•L-1×0.01L×4
铁元素的质量为:2×10-3mol×56g/mol=1.12×10-1g,铁元素的质量分数为
1.12×10 −1g
2.000g×100%=5.6%,故答案为:5.6%.点评:
本题考点: 物质的分离、提纯的基本方法选择与应用;难溶电解质的溶解平衡及沉淀转化的本质;铁的氧化物和氢氧化物;中和滴定.
考点点评: 本题考查了物质的分离、提纯的方法选择及应用,实验方案设计和评价,题目难度较大,明确各物质的性质是解本题的关键,本题注意关系式法的利用.1年前查看全部
- 以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
以黄铁矿为原料(主要成分是FeS2)为原料,生产硫酸的简要流程图如下:
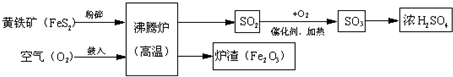
(1)写出流程图中一种氧化物的名称______.
(2)将黄铁矿粉碎,目的是______.
(3)流程中SO2转化为SO3的化学方程式为2SO2+O2
2SO3催化剂 .△ 2SO2+O2.
2SO3催化剂 .△  无及天使1年前1
无及天使1年前1 -
 yayayaya 共回答了16个问题
yayayaya 共回答了16个问题 |采纳率81.3%解题思路:(1)根据氧化物是由两种元素组成,一种元素是氧元素的化合物进行分析;
(2)根据黄铁矿粉碎会增大反应物的接触面积加快反应速度进行分析;
(3)根据题中的叙述找出反应物、生成物以及反应条件,然后依据质量守恒定律书写化学方程式.(1)通过分析反应流程中的物质可知,二氧化硫或三氧化硫或三氧化二铁都是由两种元素组成,一种元素是氧元素,属于氧化物;
(2)反应物接触面积越大,反应越剧烈,黄铁矿粉碎会增大反应物的接触面积,加快反应速度,所以将黄铁矿粉碎,目的是:增大反应物的接触面积;
(3)二氧化硫和氧气在催化剂的作用下加热生成三氧化硫,化学方程式为:2SO2+O2
催化剂
.
△2SO3.
故答案为:(1)二氧化硫;
(2)增大反应物的接触面积;
(3)2SO2+O2
催化剂
.
△2SO3.点评:
本题考点: 物质的相互转化和制备;从组成上识别氧化物;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答此类题的关键是要知道氧化物的定义,知道反应物接触面积越大,反应越剧烈,了解书写化学方程式的注意事项.1年前查看全部
- 用含FeS2 72%的黄铁矿制硫酸,煅烧时有1.5%的硫烧到损失混入炉渣.二氧化硫转化为三氧化硫的转化率97%,求一吨黄
用含FeS2 72%的黄铁矿制硫酸,煅烧时有1.5%的硫烧到损失混入炉渣.二氧化硫转化为三氧化硫的转化率97%,求一吨黄铁矿可产生98%硫酸多少吨?
 心跳乱了节奏1年前4
心跳乱了节奏1年前4 -
 skchenglong 共回答了20个问题
skchenglong 共回答了20个问题 |采纳率95%就是计算最后进入硫酸的硫的重量,进而换算成硫酸就可以了,因为硫元素是守恒的.
1t FeS2含有FeS2 720kg,FeS2中硫元素的质量分数是64/(64+56)=0.5333,所以S元素的质量就是384kg ,损失1.5%那么还剩下384×0.985=378.24kg,在转换三氧化硫的时候转化率是97%,所以这时候能转化成SO3的S的重量就是378.24×0.97=367kg,好了,现在知道变成硫酸的硫元素的质量,进而计算三氧化硫转化的纯硫酸质量:(367/32)×98=1123kg,因为硫酸是98%,所以再除以0.98,得到硫酸重量是1146.54kg
实际上运用守恒是很简单的,我写得很复杂,因为要介绍思想,如果你很熟悉,可以一步写齐所有算式,这样其中数字运算的约分等等能让计算更加简单,元素守恒、质量守恒、电荷守恒、能量守恒等等的应用有时候会让人视野更加开阔,看问题更宏观全面,简化思考和计算过程,十分有用.无论是做题还是研究,这都是很重要的思想和思考方法.1年前查看全部
大家在问
- 1一个英语故事 汉译英 是四副图画; 上星期天发生在宁波雅戈尔动物园里的一个故事我给你描述描述,1.我和爸爸妈妈在草地上吃
- 2谁会这道题:你能把两个算式合成一
- 3英语翻译我的生日即将来临,我迫不及待地想知道妈妈送我什么礼物.(can't wait to do)
- 4yourself 和 your self的区别
- 5ug中能不能根据算寸算出重量要怎么算出重量.有多少种方法
- 6在一个除法算式中,商是7,余数是3,被除数,除数,商,余数的和是229,被除数是多少?
- 7有些大数值问题可以通过用字母代替数,转化成整式问题来解决,请先阅读下面的解题过程,再解答后面的问题.
- 8(2010•郴州)下列符号中既表示一种元素,又表示该元素的一个原子,还表示一种单质的是( )
- 9要提高LC振荡电路辐射电磁波的本领,应该采取的措施是( )
- 10简述中水的概念以及其作用
- 11我国疆域辽阔,不同地区地理环境差异很大,根据各地的地理位置、自然和人文地理特点的不同,分为北方地区、南方地区、西北地区和
- 12选出关联词使用无误的一项( )。 A.虽然我们的工作取得了很大的成绩,但是不能骄傲,
- 13计数器因射线照射,内部气体电离,在时间t内有n个二价正离子到达阴极,有2n个电子到达阳极,则计数器中的电流为多少?
- 14(2014•安庆模拟)如图所示,空间有垂直向里的磁场B=1T,光滑绝缘的水平面上静止一质量为M=0.6kg、带电量为q=
- 15如何证明a/sinA=b/sinB=c/sinC=(a+b)/(sinA+sinB)

