A牌消毒剂,用药液和水按照1:99配制而成.如果现在要配置120千克的个消毒剂,需要药液( )千克,需要水( )千克
 李昱洁2022-10-04 11:39:541条回答
李昱洁2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 灏灏123 共回答了23个问题
灏灏123 共回答了23个问题 |采纳率95.7%- A牌消毒剂,用药液和水按照1:99配制而成.如果现在要配置120千克的个消毒剂,需要药液(1.2 )千克,需要水( 118.8)千克
方法:按比例分配
100份中有药1份 水99份 - 1年前
相关推荐
- 在一种消毒剂中由氢氧两种元素组成,且每个分子中含1个Cl原子,2个O原子,问该原子的化合式
 枫魂1年前3
枫魂1年前3 -
 蓝づ小小 共回答了20个问题
蓝づ小小 共回答了20个问题 |采纳率90%HClO21年前查看全部
- 化学问题,高手请进过氧乙酸(CH3COOOH)是被广泛应用的高效消毒剂.它不稳定易分解放出一种常见的气体单质,并生成醋酸
化学问题,高手请进
过氧乙酸(CH3COOOH)是被广泛应用的高效消毒剂.它不稳定易分解放出一种常见的气体单质,并生成醋酸(CH3COOH),该反应的化学方程式是( )
;若一瓶久置的过氧乙酸溶液已完全分解,所得溶液中醋酸的质量分数为12%,则原溶液中过氧乙酸的质量分数为( )%(结果保留一位小数).
请说明计算过程及思路,谢谢.
 rayzl20081年前1
rayzl20081年前1 -
 woshiwo___2004 共回答了21个问题
woshiwo___2004 共回答了21个问题 |采纳率85.7%方程式是
2CH3COOOH——2CH3COOH + O2(氧气)
上式已经配平
第二问,因为过氧乙酸已经完全分解,所以由上式,计算相对分子质量:
2CH3COOOH——2CH3COOH + O2
152 120 32
所以为了计算简便,可以设最后溶液为100g,那么易得其中醋酸为12g,根据上式,可知氧气为3.2g,过氧乙酸为15.2g,故原溶液的总质量为100+3.2=103.2g,过氧乙酸的质量分数为15.2/103.2=14.7%.解完.1年前查看全部
- 细菌与其他微生物能合成一些与____有关的酶类,能直接破坏___、___,这些微生物或细菌即为___,故消毒剂应注
 wandy1211年前1
wandy1211年前1 -
 wangyigu 共回答了16个问题
wangyigu 共回答了16个问题 |采纳率87.5%细菌与其他微生物能合成一些与消毒剂或抗生素代谢有关的酶,能直接破坏消毒剂或抗生素的结构或抑制其功能,这些微生物或细菌即为抗性微生物.1年前查看全部
- 被称为“绿色氧化剂”的过氧化氢(H 2 O 2 )俗称双氧水,是一种无色液体,常用做氧化剂、消毒剂和漂白剂.过氧化氢溶液
被称为“绿色氧化剂”的过氧化氢(H 2 O 2 )俗称双氧水,是一种无色液体,常用做氧化剂、消毒剂和漂白剂.过氧化氢溶液在二氧化锰做催化剂的条件下能迅速分解,生成氧气;分液漏斗可以通过调节活塞控制液体的滴加速度.回答下列问题: 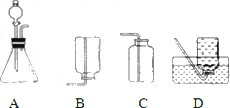
(1)分液漏斗中应加入的物质是 _________ ;锥形瓶中应放入的物质是 _________ .
(2)写出利用该方法制取氧气的反应的文字表达式: _________ ;要想收集一瓶纯净的氧气,最好选择装置 _________ (填字母).
(3)某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气,过了一段时间后,将带火星的木条伸入瓶口、瓶中和瓶底,都未见木条复燃.其原因可能是 _________ .
(4)如果在实验室中用此方法代替加热高锰酸钾制取氧气,请简述其优点有哪些.(至少写出两点) _________ ; _________ .
(5)小路同学用过氧化氢制取并收集了两瓶氧气,准备做硫粉燃烧和铁丝燃烧的实验,他在瓶底都加了少量水.请你来想一想,加水的目的分别是什么? _________ ; _________ . LunaMaldini1年前1
LunaMaldini1年前1 -
 蓝色小米330 共回答了18个问题
蓝色小米330 共回答了18个问题 |采纳率94.4%1年前查看全部
- 用二氧化氯作为生活用水消毒剂时,水中能否测出余氯?
用二氧化氯作为生活用水消毒剂时,水中能否测出余氯?
我用了能测出余氯,但有人说不应该能测出余氯, 汽车人之爵士1年前4
汽车人之爵士1年前4 -
 bzkybzky 共回答了17个问题
bzkybzky 共回答了17个问题 |采纳率94.1%应该不能检出.
二氧化氯用于消毒生活用水的浓度很低,一般不会高于1ppm.1年前查看全部
- 二氧化碳是一种新型的自来水消毒剂,该物质的化学公式是,该物质的相对分子质量
二氧化碳是一种新型的自来水消毒剂,该物质的化学公式是,该物质的相对分子质量
二氧化碳是一种新型的自来水消毒剂,该物质的化学公式是_____,该物质的相对分子质量______ djccargo1年前1
djccargo1年前1 -
 八百公尺的河 共回答了22个问题
八百公尺的河 共回答了22个问题 |采纳率95.5%二氧化氯吧?
ClO2 67.51年前查看全部
- 求 二氧化氯消毒剂+水反映的化学方程式 及消毒剂的化学式,貌似反映后会释放 热量 和二氧化氯气体
 价格便宜量又足1年前2
价格便宜量又足1年前2 -
 yoyo116697 共回答了22个问题
yoyo116697 共回答了22个问题 |采纳率90.9%二氧化氯和水反应主要歧化生成亚氯酸和氯酸,极少量的会和水发生反应生成氧气和氯气
消毒剂主要成分就是二氧化氯1年前查看全部
- 化学法二氧化氯消毒剂发生器和化学法二氧化氯复合消毒剂发生器的区别是什么
化学法二氧化氯消毒剂发生器和化学法二氧化氯复合消毒剂发生器的区别是什么
化学法二氧化氯消毒剂发生器和化学法二氧化氯复合消毒剂发生器的概念是什么?他们是怎么区分,谢谢解答
“复合”两字存在,到底是如何意思!他们两个有什么区别 dounimasi1年前4
dounimasi1年前4 -
 123明明 共回答了20个问题
123明明 共回答了20个问题 |采纳率80%纯的二氧化氯 / 复合的消毒剂发生器 ---制出的是二氧化氯和氯气的混合物
每克纯二氧化氯的消毒能力约是复合的有效氯的3倍1年前查看全部
- (2004•泰州)高锰酸钾俗称灰锰氧,其水溶液是常用的消毒剂.高锰酸钾的物质类别属于( )
(2004•泰州)高锰酸钾俗称灰锰氧,其水溶液是常用的消毒剂.高锰酸钾的物质类别属于( )
A.酸
B.碱
C.盐
D.氧化物 桑格花在漫天飞1年前1
桑格花在漫天飞1年前1 -
 heidi_wei 共回答了23个问题
heidi_wei 共回答了23个问题 |采纳率95.7%解题思路:氧化物是由两种元素组成并且一种元素是氧元素的化合物.
电离时生成的阳离子都是氢离子的化合物是酸,电离时生成的阴离子都是氢氧根离子的化合物是碱,由金属离子和酸根离子组成的化合物是盐.高锰酸钾是由钾离子和高锰酸根离子组成的化合物,属于盐.
故选C.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别.
考点点评: 解答本题要掌握物质的分类方法,只有这样才能对各种物质进行正确的分类.1年前查看全部
- (1)自来水生产过程中先用方法除去水中不溶性杂质,再进行消毒.X是一种常见的自来水消毒剂,工业上制取X的化学方程式为:C
(1)自来水生产过程中先用方法除去水中不溶性杂质,再进行消毒.X是一种常见的自来水消毒剂,工业上制取X的化学方程式为:Cl2+2NaClO2=2NaCl+2X,则X的化学式是______.
(2)地下水硬度过大会影响生产和生活,应软化后使用.
a.检验硬水常用的是物质是______
b.如果某地地下水钙、镁离子含量过高(假设主要以CaCl2、MgCl2形式存在),可先加入适量的熟石灰,反应的化学方程式为______,再加入适量的纯碱后生成沉淀,即可将水软化. amin3151年前1
amin3151年前1 -
 riverun 共回答了10个问题
riverun 共回答了10个问题 |采纳率90%解题思路:(1)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(2)利用肥皂水可以检验硬水和软水;
(3)氢氧化钙能和氯化镁反应生成氢氧化镁白色沉淀和氯化钙.(1)由Cl2+2NaClO2=2NaCl+2X可知,反应前氯原子是4个,反应后应该是4个,其中2个包含在2X中;
反应前钠原子是2个,反应后是2个;
反应前氧原子是4个,反应后应该是4个,包含在2X中;
由分析可知,每个X中含有1个氯原子和2个氧原子,化学式是ClO2.
故填:ClO2.
(2)a、向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生的泡沫很少或不产生泡沫,是硬水.
故填:肥皂水.
b、氢氧化钙和氯化镁反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
故填:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.点评:
本题考点: 质量守恒定律及其应用;硬水与软水;碱的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.1年前查看全部
- (2010•惠州模拟)ClO2是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):KClO3+H2C2O4
(2010•惠州模拟)ClO2是一种常用的预防“禽流感”的消毒剂,可通过以下反应制得(未配平):KClO3+H2C2O4+H2SO4→ClO2↑+K2SO4+CO2↑+H2O
下列说法正确的是( )
A.H2SO4做氧化剂
B.ClO2是氧化产物
C.H2C2O4被氧化
D.每消耗lmolKClO3就有2mol电子转移 我是cc我怕你1年前1
我是cc我怕你1年前1 -
 leaf2413 共回答了22个问题
leaf2413 共回答了22个问题 |采纳率90.9%解题思路:反应2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O 中,Cl元素的化合价由+5降低为+4价,C元素的化合价由+3升高到+4价,以此来解答.A、因反应中,H2SO4中元素化合价均未变,所以硫酸既不是氧化剂又不是还原剂,故A错误;
B、Cl元素的化合价降低,被还原,对应的产物为还原产物,即ClO2是还原产物,故B错误;
C、因C元素的化合价由+3升高到+4价,则H2C2O4在反应中作还原剂,被氧化,故C正确;
D、Cl元素的化合价由+5降低为+4价,1molKClO3参加反应转移的电子为1mol×(5-4)=1mol,故D错误;
故选C.点评:
本题考点: 氧化还原反应;氧化还原反应的电子转移数目计算.
考点点评: 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注意H2C2O4中C元素化合价的判断是学生的易错点.1年前查看全部
- 阅读有关消毒剂的资料并回答相关问题:
阅读有关消毒剂的资料并回答相关问题:
(1)“84消毒液”是由次氯酸钠和表面活性剂混合配制的消毒剂,是一种无色或淡黄色液体,广泛用于公共场所和家庭卫生消毒,由于“84消毒液”有一定腐蚀性,将其稀释成0.2%~0.5%,浸泡时间为10到30分钟.
①次氯酸钠化学式为NaClO,其中氯元素的化合价为______;
②使用“84消毒液”清洗衣服后要漂洗干净,其原因是______.
(2)阅读下表,回答其它消毒剂相关问题:
对生活中不慎产生的外伤伤口进行消毒时,选用的合适消毒剂是______,原因是______.消毒剂 化学式 性质和用途 注意事项 过氧乙酸溶液 CH3COOOH 过氧乙酸易挥发、易分解,其分解产物为醋酸和氧气.过氧乙酸具有很强的消毒杀菌能力,可以迅速杀灭各种微生物,包括病菌、细菌等 对皮肤有
腐蚀作用双氧水 H2O2 过氧化氢溶液俗称为双氧水,是一种无色液体,容易分解,其分解产物为水和氧气.双氧水具有较强的消毒杀菌能力. 需低温
避光保存
(3)水是生命之源.为了保障我市居民饮用水的安全,自来水必需进行消毒处理.
①自来水厂处理水的过程中一般可先加入______,吸附水中悬浮的颗粒而沉降;
②目前自来水厂常用二氧化氯进行消毒杀菌,二氧化氯的化学式为______;
③在一些偏远农村一般用漂白粉作为水源消毒剂,漂白粉的有效成分为次氯酸钙,化学式是Ca(ClO)2.次氯酸钙很不稳定,能和空气中的某些成分反应生成CaCO3和次氯酸(HClO),后者见光分解生成盐酸并放出氧气,因而具有消毒杀菌作用.请写出次氯酸分解反应的化学方程式2HClO
2HCl+O2↑光 ..2HClO.
2HCl+O2↑光 .. 我是小不及鸟1年前1
我是小不及鸟1年前1 -
 紫玫瑰香水 共回答了20个问题
紫玫瑰香水 共回答了20个问题 |采纳率75%解题思路:(1)在化合物中元素化合价代数和为零;
(2)双氧水对人体没有腐蚀性,能够杀菌消毒;
(3)明矾能够吸附水中的悬浮物,可以用来净化水;用元素符号和数字可以表示物质的化学式;次氯酸的光稳定性差.(1)①次氯酸钠化学式为NaClO,其中钠元素的化合价是+1价,氧元素的化合价是-2价,可以求出氯元素的化合价为+1价.故填:+1.
②使用“84消毒液”清洗衣服后要漂洗干净,其原因是84消毒液有腐蚀性.故填:84消毒液有腐蚀性.
(2)对生活中不慎产生的外伤伤口进行消毒时,选用的合适消毒剂是过氧化氢,原因是双氧水具有较强的消毒杀菌能力,对人体没有腐蚀性.故填:H2O2;双氧水具有较强的消毒杀菌能力,对人体没有腐蚀性.
(3)①自来水厂处理水的过程中一般可先加入明矾,吸附水中悬浮的颗粒而沉降;故填:明矾.
②目前自来水厂常用二氧化氯进行消毒杀菌,二氧化氯的化学式为ClO2;故填:ClO2;
③次氯酸分解反应的化学方程式为:2HClO
光
.
2HCl+O2↑.点评:
本题考点: 化学性质与物理性质的差别及应用;水的净化;化学式的书写及意义;有关元素化合价的计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查物质的性质和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- 高锰酸钾是常用的消毒剂吗?
 临窗听雪落1年前2
临窗听雪落1年前2 -
 犹豫什么 共回答了21个问题
犹豫什么 共回答了21个问题 |采纳率90.5%高锰酸钾
药物作用:本品用作消毒剂、除臭剂、水质净化剂.高锰酸钾为强氧化剂,遇有机物即放出新生态氧而且杀灭细菌作用,杀菌力极强,但极易为有机物所减弱,故作用表浅而不持久.高锰酸钾在发生氧化作用的同时,还原生成二氧化锰,后者与蛋白质结合而形成蛋白盐类复合物,此复合物和高锰离子都具有收敛作用.某些金属离子的分析中也用作氧化剂.也用它作漂白剂、毒气吸收剂、二氧化碳精制剂等.
工业应用:本品主要用做氧化剂.实验室中用来制取氧气.1年前查看全部
- (2010•青岛)过氧乙酸是一种常用的消毒剂.现有一种过氧乙酸溶液,其溶质质量分数为15%.请填空:
(2010•青岛)过氧乙酸是一种常用的消毒剂.现有一种过氧乙酸溶液,其溶质质量分数为15%.请填空:
(1)100g该溶液中含溶质______g.
(2)向100g该溶液中加入200g水,所得溶液的溶质质量分数为______.
(3)将100g该溶液与100g5%的过氧乙酸溶液混合,所得溶液的溶质质量分数为______. 戴警帽狂追足球1年前1
戴警帽狂追足球1年前1 -
 2491023 共回答了26个问题
2491023 共回答了26个问题 |采纳率76.9%解题思路:(1)利用一定量溶液中溶质的质量=溶液质量×溶液中溶质的质量分数,由溶液质量100g和溶液的溶质质量分数15%,计算溶液中溶质的质量;
(2)加入水后溶液质量增大而溶质质量不变,利用溶液中溶质的质量分数的计算公式,计算加水后所得溶液的溶质质量分数;
(3)与100g5%的过氧乙酸溶液混合后,所得溶液的质量为两溶液的质量和、溶液中溶质的质量为两溶液中溶质质量之和,利用溶液中溶质的质量分数的计算公式,计算所得溶液的溶质质量分数.(1)100g溶质质量分数为15%过氧乙酸溶液中含溶质的质量=100g×15%=15g;
故答案为:15;
(2)向100g该溶液中加入200g水,所得溶液的溶质质量分数=[15g/100g+200g]×100%=5%;
故答案为:5%;
(3)将100g该溶液与100g5%的过氧乙酸溶液混合,所得溶液的溶质质量分数=[15g+100g×5%/100g+100g]×100%=10%;
故答案为:10%.点评:
本题考点: 有关溶质质量分数的简单计算;用水稀释改变浓度的方法.
考点点评: 根据溶液中溶质的质量分数=[溶质的质量/溶液的质量]×100%,若已知等式中任意两个量可计算第三个量.1年前查看全部
- 下列关于常用消毒剂的叙述中,正确的是( ) A.高锰酸钾(KMnO 4 )是氧化物 B.H 2 O 2 中氢元素的质量
下列关于常用消毒剂的叙述中,正确的是( ) A.高锰酸钾(KMnO 4 )是氧化物 B.H 2 O 2 中氢元素的质量分数为11.1% C.次氯酸钠(NaClO)中氯元素的化合价为-1价 D.过氧乙酸的化学式为C 2 H 4 O 3 ,其碳、氢、氧三种元素的质量比为6:1:12  xiaoguier_781年前1
xiaoguier_781年前1 -
 yanghw64 共回答了19个问题
yanghw64 共回答了19个问题 |采纳率89.5%A、氧化物是由两种元素组成且含有氧元素的化合物,高锰酸钾KMnO 4 由K、Mn、O三种元素,不属于氧化物;故A不正确;
B、H 2 O 2 中氢元素的质量分数=
1×2
34 ×100%≈5.9%≠11.1%;故B不正确;
C、设化合物NaClO中氯元素化合价为x,依据化合物中各元素化合价代数和为0,则(+1)+x+(-2)=0,解得x=+1;故C不正确;
D、过氧乙酸C 2 H 4 O 3 中碳、氢、氧三种元素的质量比=(12×2):(1×4):(16×3)=6:1:12;故D正确;
故选D.1年前查看全部
- 二氧化氯(ClO2)是一种新型的自来水消毒剂,下列对它的描述错误的是( )
二氧化氯(ClO2)是一种新型的自来水消毒剂,下列对它的描述错误的是( )
A.这是一种化合物,且是一种氧化物
B.它是由一个氯原子和一个氧分子构成的
C.它的相对分子质量为67.5
D.其中氧元素的化合价为-2 lx32311年前1
lx32311年前1 -
 zome-2000 共回答了13个问题
zome-2000 共回答了13个问题 |采纳率76.9%解题思路:A、由不同种元素组成的纯净物是化合物,在由两种元素组成的化合物中,其中一种是氧元素的是氧化物.
B、根据二氧化氯的微观构成进行分析判断.
C、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
D、根据常见元素的化合价进行分析判断.A、二氧化氯(ClO2)是由不同种元素组成的纯净物,属于化合物;且是由两种元素组成且有一种是氧元素,属于氧化物;故选项说法正确.
B、二氧化氯是由二氧化氯分子构成的,1个二氧化氯分子是由一个氯原子和两个氧原子构成的,故选项说法错误.
C、它的相对分子质量为35.5+16×2=67.5,故选项说法正确.
D、氧元素在化合物中通常显-2价,故选项说法正确.
故选B.点评:
本题考点: 化学式的书写及意义;从组成上识别氧化物;单质和化合物的判别;有关元素化合价的计算;相对分子质量的概念及其计算.
考点点评: 本题难度不大,考查同学们结合新信息、灵活运用化合物与氧化物的概念、化学式的含义与有关计算等进行分析问题、解决问题的能力.1年前查看全部
- 漂白粉是防疫消毒剂中的一种,它是次氯酸钙和氯化钙的混合物,是用氯气与熟石灰反应制得的,
漂白粉是防疫消毒剂中的一种,它是次氯酸钙和氯化钙的混合物,是用氯气与熟石灰反应制得的,
,化学方程式是-----;1mol氯气可制得漂白粉------g,其中次氯酸钙含有氯原子个数为---- lucky6601年前1
lucky6601年前1 -
 cet462 共回答了21个问题
cet462 共回答了21个问题 |采纳率85.7%其实这是一个两步反应
1.Cl2+2H2O=2HClO+H2
2.2HClO+Ca(OH)2=Ca(ClO)2+2H2O
把两个方程式加和就是Ca(OH)2+Cl2=Ca(ClO)2+H2
1mol氯气对应1molCa(ClO)2=40+(35.5+16)*2=143G
含有2molCl原子~个数忘了1mol是多少个了.2*6.23*10的23次方?1年前查看全部
- 漂白粉是常用的消毒剂之一,它的主要成分是氯化钙和次氯酸钙【(ca(clo)2的混合物.氯气与石灰反应可制的漂
 星城里手1年前1
星城里手1年前1 -
 songlli 共回答了29个问题
songlli 共回答了29个问题 |采纳率82.8%漂白粉是氢氧化钙、氯化钙和次氯酸钙的混合物,其主要成分是次氯酸钙[Ca(ClO)2 ],有效氯含量为30%-38%.漂白粉为白色或灰白色粉末或颗粒,有显著的氯臭味,很不稳定,吸湿性强,易受光、热、水和乙醇等作用而分解.1年前查看全部
- 水净化过程常用到以下消毒剂,其中属于氧化物的是 A.氯气(Cl 2 ) B.臭氧(O 3 ) C.次氯酸钙[Ca(C
水净化过程常用到以下消毒剂,其中属于氧化物的是
A.氯气(Cl 2 ) B.臭氧(O 3 ) C.次氯酸钙[Ca(ClO) 2 ] D.二氧化氯(ClO 2 )  wzg7111171年前1
wzg7111171年前1 -
 寻找幸福的生活 共回答了22个问题
寻找幸福的生活 共回答了22个问题 |采纳率90.9%D
1年前查看全部
- 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是______(填序号).
A.只有还原性B.还原性和酸性C.只有氧化性D.氧化性和酸性
②若上述反应中产生0.1mol ClO2,则转移电子的物质的量为______mol.
(2)目前已开发出用电解法制取ClO2的新工艺.
①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2.写出阳极产生ClO2的电极反应式:______.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为______mol;用平衡移动原理解释阴极区pH增大的原因______.
(3)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN- a mg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为______;处理100m3这种污水,至少需要ClO2[50a/13][50a/13]mol. kakaup1年前1
kakaup1年前1 -
 ajiu555 共回答了13个问题
ajiu555 共回答了13个问题 |采纳率92.3%解题思路:(1)①HCl中的氯元素在产物存在于Cl2,氯元素的化合价升高,氯元素被氧化,存在NaCl中氯元素的化合价未变化,据此解答;
②ClO2是还原产物,氯元素的化合价由+5价降低为+4价,转移电子物质的量等于ClO2的物质的量;
(2)①由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子;
②在阴极发生2H++2e-=H2↑,通过阳离子交换膜的阳离子为+1价离子,根据n=
计算氢气的物质的量,根据电子转移守恒计算阳离子的物质的量,电解中H+浓度减小,使得H2O⇌OH-+H+的平衡向右移动;V Vm
(3)ClO2将CN-氧化,只生成两种气体,应生成氮气与二氧化碳,同时生成氯离子;
根据方程式计算需要ClO2的物质的量.(1)①HCl中的氯元素在产物存在于Cl2,氯元素的化合价升高,氯元素被氧化,HCl起还原剂注意,同时存在NaCl中氯元素的化合价未变化,故HCl还起酸的作用,故答案为:B;
②ClO2是还原产物,氯元素的化合价由+5价降低为+4价,转移电子物质的量为0.1mol×(5-4)=0.1mol,
故答案为:0.1mol;
(2)①由题意可知,氯离子放电生成ClO2,由元素守恒可知,有水参加反应,同时生成氢离子,电极反应式为:Cl--5e-+2H2O=ClO2↑+4H+,
故答案为:Cl--5e-+2H2O=ClO2↑+4H+;
②在阴极发生2H++2e-=H2↑,氢气的物质的量为[0.112L/22.4L/mol]=0.005mol,通过阳离子交换膜的阳离子为+1价离子,故交换膜的阳离子的物质的量为0.005mol×2=0.01mol,电解中阴极H+浓度减小,使得H2O⇌OH-+H+的平衡向右移动,溶液的pH增大,
故答案为:0.01;在阴极发生2H++2e-=H2↑,H+浓度减小,使得H2O⇌OH-+H+的平衡向右移动,OH-浓度增大,pH增大;
(3)ClO2将CN-氧化,只生成两种气体,应生成氮气与二氧化碳,同时生成氯离子,反应离子方程式为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-,
100m3废水中CN-质量=100m3×ag/m3=100ag,CN-的物质的量为[100ag/26g/mol]=[50a/13]mol,由方程式可知,至少需要ClO2的物质的量=[50a/13]mol,
故答案为:2ClO2+2CN-=N2↑+2CO2↑+2Cl-;[50a/13]mol.点评:
本题考点: 电解原理;氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查氧化还原反应、常用化学用语、电解原理、化学计算等,题目难度中等,电解反应是难点、易错点,是对学生综合能力的考查,需要学生具有扎实的基础与分析解决问题的能力.1年前查看全部
- 世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用.
世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用.下列说法中正确的是( )
A.ClO2是强氧化剂
B.ClO2是强还原剂
C.ClO2是离子化合物
D.ClO2中氯元素为-1价 chuyou991年前1
chuyou991年前1 -
 qjxjack 共回答了17个问题
qjxjack 共回答了17个问题 |采纳率88.2%解题思路:A、依据二氧化氯中氯的化合价为+4价,化合价为该元素的高价态分析判断;
B、依据氯的化合价情况分析判断;
C、依据离子化合物一般的特点分析判断;
D、依据化合物中各元素化合价代数和为零分析判断;A、二氧化氯中氯的化合价为+4价,化合价为该元素的高价态,所以该物质有较强的氧化性;
B、由A知ClO2是强氧化剂不是强还原剂;
C、离子化合物一般由金属离子与酸根离子构成,二氧化氯不具备该特点,所以ClO2不是离子化合物;
D、因为化合物中各元素化合价代数和为零,所以ClO2中氧元素为-2价,故氯元素为+4价;
故选A.点评:
本题考点: 氧化反应;有关元素化合价的计算.
考点点评: 此题是对氧化还原知识的考查,解题的关键是掌握氧化剂还原剂的组成元素化合价的特点.1年前查看全部
- (2013•嘉兴)臭氧(O3)、二氧化碳(CO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质中都含有(
(2013•嘉兴)臭氧(O3)、二氧化碳(CO2)、双氧水(H2O2)等都是生产、生活中常用的消毒剂,三种物质中都含有( )
A.氧分子
B.氧离子
C.氧气
D.氧元素 天秤女生1年前1
天秤女生1年前1 -
 贴心123 共回答了13个问题
贴心123 共回答了13个问题 |采纳率92.3%解题思路:根据臭氧(O3)、二氧化碳(CO2)、双氧水(H2O2)这三种物质的组成和构成进行分析解答即可.A、由三种物质的组成,三种物质中都不含有氧分子,只有氧气中才含有氧分子,故A错误.
B、三种物质中都不含有氧离子,含有氧原子,故B错误.
C、臭氧(O3)、二氧化碳(CO2)、双氧水(H2O2)都是纯净物,都不含有氧气,故C错误.
D、根据三种物质的化学式可知,三种物质中都含有氧元素,故D正确.
故选D.点评:
本题考点: 分子、原子、离子、元素与物质之间的关系.
考点点评: 本题难度不大,考查学生对物质组成和构成的认识,掌握物质组成的知识即可正确解答本题.1年前查看全部
- 发酵粉可用作消毒剂和漂白剂,是因为氯气与水反应生成的次氯酸具有强氧化性,还是生成游离态的氧气强氧化性?
 sntuu1年前1
sntuu1年前1 -
 chuiliu 共回答了16个问题
chuiliu 共回答了16个问题 |采纳率81.3%应该是漂白粉(有效成分:次氯酸钙)而不是发酵粉.
是次氯酸的氧化性导致了细菌的死亡.
因为次氯酸在常温下光不强时,其分解并不是很快的,产生的原子氧并不多.所以主要还是依靠了次氯酸的氧化作用.1年前查看全部
- 季铵盐在弱酸条件下杀菌性能有印象季铵盐呈碱性,在碱性条件下有较强杀菌性.商品新吉尔灭(十二烷基二甲基苄基溴化铵 )消毒剂
季铵盐在弱酸条件下杀菌性能
有印象季铵盐呈碱性,在碱性条件下有较强杀菌性.
商品新吉尔灭(十二烷基二甲基苄基溴化铵 )消毒剂溶液pH6,现配CTAB(十六烷基三甲基溴化铵)溶液,pH也是6,问:季铵盐在弱酸条件下也有较强杀菌性能?还是在碱性条件比较强? ty6881年前1
ty6881年前1 -
 gong0202 共回答了20个问题
gong0202 共回答了20个问题 |采纳率90%季铵盐类阳离子表面活性剂:杀菌机理是改变细胞膜透性,使细胞质外漏,妨碍呼吸或是蛋白质变性.特点是能杀死细菌繁殖体,但对芽孢、真菌、病毒、结核杆菌作用差.一般都是碱性下杀菌性能比较强,但是只要不是pH很低,PH的影响不大.氮原子与烷基相连形成带正电荷的阳离子基团,是杀菌的有效部分,pH很低的话会消弱阳离子基团带的正电荷1年前查看全部
- 世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,ClO2是一种消毒杀菌效率高、二次污染小的水处
世界卫生组织(WHO)将二氧化氯(ClO2)列为A级高效、安全灭菌消毒剂,ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,它在食品保鲜、饮用水消毒等方面有着广泛的应用.
(1)实验室制备ClO2的方法之一为:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价)则下列说法正确的是______.△ .
A.KClO3在反应中得到电子
B.ClO2是氧化产物
C.H2C2O4在反应中被氧化
D.1mol KClO3参加反应有2mol电子转移
(2)KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯.其变化可表示为2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O
①浓盐酸在反应中表现出来的性质是______;
②已知每产生0.1mol Cl2,则发生转移的电子的物质的量为0.2mol.ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的______倍. 娟老大1年前1
娟老大1年前1 -
 silver0rr 共回答了18个问题
silver0rr 共回答了18个问题 |采纳率83.3%解题思路:(1)2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价由+5价降低为+4价,C元素的化合价由+3价升高为+4价;△ .
(2)①反应中Cl元素的化合价升高表现还原性,反应生成盐,表现酸性;
②作消毒剂,其消毒后的还原产物是氯离子,利用化合价的变化计算消毒效率.(1)2KClO3+H2C2O4+H2SO4
△
.
2ClO2↑+K2SO4+2CO2↑+2H2O中,Cl元素的化合价由+5价降低为+4价,C元素的化合价由+3价升高为+4价,
A.KClO3在反应中Cl元素的化合价降低,得到电子,故A正确;
B.ClO2是还原产物,故B错误
C.H2C2O4在反应中,C元素的化合价升高,则被氧化,故C正确;
D.1molKClO3参加反应,Cl元素的化合价由+5价降低为+4价,有1mol电子转移,故D错误;
故答案为:AC;
(2)①KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯.其变化可表示为2KClO3+4HCl(浓)═2KCl+2ClO2↑+Cl2↑+2H2O,反应中Cl元素的化合价升高表现还原性,反应生成盐KCl,表现酸性;
故答案为:还原性和酸性;
②作消毒剂,其消毒后的还原产物是氯离子,则消毒效率为
m
67.5×5
m
71×2×1=2.63,故答案为:2.63.点评:
本题考点: 氧化还原反应.
考点点评: 本题以氯及其化合物考查氧化还原反应,侧重氧化还原反应的考查,明确反应中元素的化合价变化是解答的关键,注重知识的迁移应用,题目难度不大.1年前查看全部
- 氯化钠可以做食品防腐剂,高锰酸钾可以作为家庭常用消毒剂,什么是重金属?有什么特征吗?哪些是典型的重金属?
 贝贝的舞鞋1年前4
贝贝的舞鞋1年前4 -
 yuyangwei123 共回答了23个问题
yuyangwei123 共回答了23个问题 |采纳率87%1.高浓度的氯化钠溶液可以使细菌因失水而死亡.
2.高锰酸钾具有强氧化性,可以杀死细菌.一般,强氧化性的物质都能杀菌,如H2O2(双氧水),HClO(次氯酸),CH3COOOH(过氧乙酸)等
3.密度大于4.5g/cm^3的为重金属.重金属大多数有毒,摄入后很难排出,但也有少数是人体必需的微量元素.有毒的如Ba、Pb、Ag、Au、Hg、Cd等.如Cu则是人体所需的微量元素1年前查看全部
- 自来水厂净水过程示意图为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水
自来水厂净水过程示意图为:天然水→加絮凝剂→沉降→过滤→吸附→加消毒剂→自来水
其中常用的絮凝剂是 1.氯气 2.活性炭 3.明矾 4.漂白粉 解释,谢谢 _十戈1年前2
_十戈1年前2 -
 king7620 共回答了16个问题
king7620 共回答了16个问题 |采纳率81.3%首先要说的是氯气与漂白粉是消毒剂.
活性炭是吸附剂.
明矾不是絮凝剂,属于混凝剂,只是沾边.
混合和絮凝称为混凝.
大颗粒悬浮物在重力作用下易于沉淀,而颗粒微小的悬浮物及胶体杂质,却能在水中长期保持分散悬浮状态,使水呈浑浊现象.
混凝的作用就是让这些微小的颗粒变成大颗粒也易于沉淀.
混凝剂:硫酸铝、三氯化铁、硫酸亚铁.
助凝剂:氯气、石灰、重碳酸钠.
混凝后生成的相对较大易于沉定的颗粒(矾花),借助重力的作用在水中沉淀下来.
滤料层主要通过隔滤、吸附作用去除水中的悬浮杂质.
普通快滤池、虹吸滤池.
石英砂(砂滤池)
活性炭(碳滤池)
加氯消毒:杀灭水中病原菌和有害微生物.1年前查看全部
- 常用的消毒剂有氯气、二氧化氯、漂白粉等,这三种物质都含()理由是?
常用的消毒剂有氯气、二氧化氯、漂白粉等,这三种物质都含()理由是?
A.原子团 B.氯分子 C.氯离子 D.氯元素 毛毛与卡尔1年前3
毛毛与卡尔1年前3 -
 碳酸小子 共回答了16个问题
碳酸小子 共回答了16个问题 |采纳率93.8%D
氯气:Cl2
二氧化氯;ClO2
漂白粉:Ca(ClO)2(都由氯元素组成)
因为氯气为单质,不是由离子构成,更不是原子团
二氧化氯是由二氧化氯分子构成
所以选D1年前查看全部
- 谁除了用液氧和漂白粉消毒外还可以用哪些化学试剂作消毒剂
 梅青青1年前4
梅青青1年前4 -
 枫叶235 共回答了18个问题
枫叶235 共回答了18个问题 |采纳率88.9%高锰酸钾.
双氧水.臭氧.酒精也可以1年前查看全部
- 12、漂白粉属于( )A.酚类消毒剂 B.醇类消毒剂 C.氧化剂消毒剂 D.表面活性剂
 Haro11年前1
Haro11年前1 -
 热情我围绕台 共回答了19个问题
热情我围绕台 共回答了19个问题 |采纳率78.9%C.氧化剂消毒剂.1年前查看全部
- 化合物M是铁元素的+6价含氧酸钾盐,常用作净水剂与消毒剂.由铁元素的稳定氢氧化物与次氯酸钾、
化合物M是铁元素的+6价含氧酸钾盐,常用作净水剂与消毒剂.由铁元素的稳定氢氧化物与次氯酸钾、
氢氧化钾溶液反应制取化合物M,则制备M的离子方程式怎么写啊 ylcey1年前1
ylcey1年前1 -
 我的dd在杭州 共回答了21个问题
我的dd在杭州 共回答了21个问题 |采纳率95.2%离子方程式 2 Fe(OH)3 + 3 ClO- + 4 OH- = 2 FeO42- + 3 CI- + 5 H2O
化学方程式 2 Fe(OH)3 + 3 KClO + 4 KOH = 2 K2FeO4 + 3 KCI + 5 H2O
铁元素的稳定氢氧化物是Fe(OH)3,根据·化合价可知M是K2FeO4
剩下的就是配平了1年前查看全部
- 抗震救灾,众志成城.用于汶川震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分为三氯异氰尿酸(C 3 O 3 N 3 C
抗震救灾,众志成城.用于汶川震后防疫的众多消毒剂中,有一种高效消毒剂的主要成分为三氯异氰尿酸(C 3 O 3 N 3 C 13 ),又称高氯精.下列有关高氯精的说法正确的是( )
A、 该消毒剂由4种元素组成
B、 高氯精中有12个原子
C、 高氯精中C、N两种元素的质量比为1:1
D、 高氯精中元素的质量分数最大的是氯元素 不想再去爱1年前1
不想再去爱1年前1 -
 丹猪就是一只猪 共回答了19个问题
丹猪就是一只猪 共回答了19个问题 |采纳率84.2%D
利用化学式体现的宏观与微观的意义解决A、B两选项;利用元素的质量比等于元素原子量和的比解决C、D选项,质量分数最大即原子量和最大的元素.
此题是对化学式意义及简单计算进行的考查,涉及到化学式的意义的利用,元素的质量分数的计算,抓住化学式是解题的关键.
A、因为有一种高效消毒剂的主要成分为三氯异氰尿酸(C 3 O 3 N 3 C 13 ),所以不能判断该消毒剂只有高氯精,因此该物质含有4种元素说法错误,故此选项错误.
B、高氯精中有四种元素,一个分子中含有12个原子,故此选项错误.
C、元素的质量比等于元素原子量和的比,则有高氯精中C、N两种元素的质量比为:(12×3):(14×3)=12:14,故此选项错误.
D、质量分数最大即原子量和最大的元素,分析知氯元素质量分数最大,故此选项正确.
故选D1年前查看全部
- 高铁酸钠(Na2FeO4)是一种绿色环保高效的饮水消毒剂.高铁酸钠中铁元素的化合价为
 scyber1年前1
scyber1年前1 -
 rainxing 共回答了18个问题
rainxing 共回答了18个问题 |采纳率88.9%+61年前查看全部
- 下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是( )
下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是( )
A. 氯气(Cl2)
B. 臭氧(O3)
C. 漂白精[主要成分Ca(ClO)2]
D. 二氧化氯(ClO2) qiqig9111年前1
qiqig9111年前1 -
 merymaid 共回答了11个问题
merymaid 共回答了11个问题 |采纳率90.9%解题思路:氧化物是指由两种元素组成并且其中一种元素是氧元素的化合物.氧化物的特点是由两种元素组成的化合物,其中一种元素是氧元素.A、氯气是由氯元素组成的纯净物,属于单质,不属于氧化物.故错误;
B、臭氧是由氧元素组成的纯净物,属于单质,不属于氧化物.故错误;
C、次氯酸钙是由钙元素、氯元素和氧元素组成的,不属于氧化物.故错误;
D、二氧化氯是由氧元素和氯元素组成的化合物,属于氧化物.故正确.
故选:D.点评:
本题考点: 从组成上识别氧化物.
考点点评: 解答本题要正确的分析物质是由几种元素组成的,如果由氧元素和另外一种元素组成并且属于化合物就属于氧化物.1年前查看全部
- (2007•泉州)(泉州市)二氧化氯(Cl02)是一种新型自来水消毒剂.下列有关二氧化氯说法错误的是( )
(2007•泉州)(泉州市)二氧化氯(Cl02)是一种新型自来水消毒剂.下列有关二氧化氯说法错误的是( )
A.由氯元素和氧元素组成
B.相对分子质量是67.5
C.是一种氧化物
D.氯氧两元素的质量比是1:2 avaforget1年前1
avaforget1年前1 -
 weiminabc 共回答了17个问题
weiminabc 共回答了17个问题 |采纳率76.5%解题思路:A、由二氧化氯(Cl02)可知该物质的元素的组成;
B、相对分子质量,即各种元素的相对原子质量和的总和;
C、氧化物由两种元素组成,其中一种为氧元素;
D、元素的质量比为各种元素的相对原子质量和的比.由二氧化氯(Cl02)具体分析如下:
A、可知由氯元素和氧元素组成,故A正确;
B、相对分子质量=35.5+16×2=67.5,故B正确;
C、是一种氧化物,它由氯元素和氧元素组成,故C正确;
D、氯氧两元素的质量比=35.5:(16×2)=35.5:32,而1:2为原子个数比,故D错误.
故选D.点评:
本题考点: 化学式的书写及意义;从组成上识别氧化物;有关化学式的计算和推断.
考点点评: 了解化学式的书写及其意义,从组成上识别氧化物;了解有关化学式的计算和推断方法及其技巧.1年前查看全部
- 氯化铜晶体(CuCl2•xH2O)是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含
氯化铜晶体(CuCl2•xH2O)是重要的化工原料,可用作催化剂、消毒剂等.用孔雀石[主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物]制备氯化铜晶体,方案如下:

已知:有关金属离子从开始沉淀到沉淀完全时溶液的pH:
(1)若溶液A含有的金属离子有Cu2+、Fe2+、Fe3+,则试剂①选用______(填字母).Fe3+ Cu2+ Fe2+ 开始沉淀的pH 2.7 5.4 8.1 沉淀完全的pH 3.7 6.9 9.6
A.CuB.Cl2C.NH3•H2OD.NaOH
(2)加入试剂②的目的是调节pH至a,a的范围是______.由溶液C获得CuCl2•xH2O,包含4个基本实验操作,这4个基本实验操作依次是______、______过滤和无水乙醇洗涤等操作,使用无水乙醇代替水进行洗涤的主要原因是______.
(3)为了测定制得的氯化铜晶体(CuCl2•xH2O)中x值,有同学设计了如下两种实验方案:
①称取一定质量的晶体加热使其失去结晶水,称量所得无水CuCl2的质量.该方案存在的问题是______.
②称取a g晶体、加入足量氢氧化钠溶液,过滤、洗涤、加热沉淀至质量不再减轻为止,称量所得固体的质量为b g.则x=[80a−135b/18b][80a−135b/18b](用含a、b的代数式表示). 香如玉1年前1
香如玉1年前1 -
 vcactor 共回答了19个问题
vcactor 共回答了19个问题 |采纳率100%解题思路:(1)由工艺流程转化关系可知,实现由溶液A至溶液B转化,目的是将Fe2+氧化为Fe3+,试剂①应为氧化剂,且不能引入新的杂质.
(2)由工艺流程转化关系可知,试剂②应为调节溶液pH值,使Fe3+转化为Fe(OH)3,除去Fe3+,不能沉淀Cu2+,结合金属离子从开始沉淀到沉淀完全时溶液的pH选择pH的范围.
由溶液到晶体需要蒸发浓缩、冷却结晶、过滤、洗涤等.使用无水乙醇代替水进行洗涤,防止CuCl2•xH2O晶体溶解损失.
(3)①CuCl2•xH2O晶体加热时会发生水解.
②加热沉淀至质量不再减轻为止,b g为CuO质量,根据铜元素守恒可知,n(CuO)=n(CuCl2•xH2O),再结合m=nM计算x的值.(1)由工艺流程转化关系可知,实现由溶液A至溶液B转化,目的是将Fe2+氧化为Fe3+,试剂①应为氧化剂,且不能引入新的杂质.
A.Cu不能与Fe2+反应,故A错误;
B.Cl2可以将Fe2+氧化为Fe3+,且不引入新杂质,故B正确;
C.NH3•H2O可以沉淀Cu2+、Fe2+、Fe3+,引入铵根离子,故C错误;
D.NaOH可以沉淀Cu2+、Fe2+、Fe3+,引入钠离子,故D错误.
故选:B.
(2)由工艺流程转化关系可知,试剂②应为调节溶液pH值,使Fe3+转化为Fe(OH)3,除去Fe3+,不能沉淀Cu2+,由金属离子从开始沉淀到沉淀完全时溶液的pH可知,Fe3+从pH=2.7开始沉淀,在pH=3.7沉淀完全,Cu2+从pH=5.4开始沉淀,所以应该可知pH范围为3.7~5.4.
由溶液获得CuCl2•xH2O晶体需要蒸发浓缩、冷却结晶、过滤、洗涤等.
氯化铜易溶于水,使用无水乙醇代替水进行洗涤,防止CuCl2•xH2O晶体溶解损失.
故答案为:3.7~5.4;蒸发浓缩、冷却结晶;防止CuCl2•xH2O晶体溶解损失.
(3)①CuCl2•xH2O晶体加热时会发生水解CuCl2+2H2O⇌Cu(OH)2+2HCl,有HCl气体放出,CuCl2质量偏小,测得x值偏大.
故答案为:CuCl2•xH2O晶体加热时会发生水解.
②b g为CuO质量为[bg/80g/mol]=[b/80]mol,根据铜元素守恒可知,n(CuO)=n(CuCl2•xH2O),所以ag=[b/80]mol×(135+18x)g/mol,解得,x=[80a−135b/18b].
故答案为:[80a−135b/18b].点评:
本题考点: 制备实验方案的设计;化学方程式的有关计算;常见阳离子的检验;探究物质的组成或测量物质的含量.
考点点评: 考查阅读获取信息能力、对工艺流程理解与实验条件控制、实验方案的评价、化学计算、物质分离提纯除杂等有关实验操作以及在新情境下综合运用知识解决问题的能力.题目难度中等,要求学生要有扎实的实验基础知识和灵活应用信息解决问题的能力,注意基础知识的全面掌握.1年前查看全部
- 过氧化氢(俗名双氧水,化学式H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双
过氧化氢(俗名双氧水,化学式H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O 2 .其瓶上标签的部分文字如图所示,试解答下列问题:
(1)这瓶溶液可稀释为溶质质量分数为6%的溶液约______克.据标签上的说明文字推测双氧水具有的性质有:______.
(2)根据化学方程式计算:这瓶溶液稀释后理论上可制得多少克氧气?
 何梓欣1年前1
何梓欣1年前1 -
 dumle 共回答了26个问题
dumle 共回答了26个问题 |采纳率92.3%(1)设 这瓶溶液可稀释为溶质质量分数为6%的溶液约 mg,
m×6%=500g×10%,
解答m=833.3g;
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质为:见光、受热易分解;
故答案为:833.3; 见光、受热易分解;
(2)设生成的氧气质量为x,据题意得
2H 2 O 2
Mn O 2
.
2H 2 O+O 2 ↑
68 32
500×10%克 x克
∴
68
500×10%克 =
32
x克
解之得:x=23.5克
答:这瓶溶液稀释后理论上可制得23.5克氧气.1年前查看全部
- 化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )A.明矾常作为消毒剂B.发酵粉中主要
化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )A.明矾常作为消毒剂B.发酵粉中主要
化学知识在生产和生活中有着重要的应用.下列说法中正确的是( )
A.明矾常作为消毒剂
B.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔;而碳酸钠可作医疗上治疗胃酸过多的一种药剂
C.高纯度的硅单质广泛用于制作光导纤维
D.氧化铝可用来制造耐火砖和坩埚等
 jzny9991年前1
jzny9991年前1 -
 aiwuzhixin 共回答了23个问题
aiwuzhixin 共回答了23个问题 |采纳率82.6%A、明矾不具有氧化性,不能作常用作消毒剂,铝离子水解生成的氢氧化铝具有净水作用,所以明矾可以做净水剂,故A错误;
B、碳酸钠的碱性太强,不能用来中和胃酸,中和胃酸可以用碳酸氢钠,故B错误;
C、二氧化硅广泛用于制作光导纤维,单质硅用作半导体材料,故C错误;
D、氧化铝的熔点较高,可用来制造耐火砖和坩埚等,故D正确.
故选D.1年前查看全部
- “非典”肆虐时期,过氧乙酸(C2H4O3)是被人们广泛使用的消毒剂,它无色且有刺激性气味,具有强氧化性,温度稍高即分解放
“非典”肆虐时期,过氧乙酸(C2H4O3)是被人们广泛使用的消毒剂,它无色且有刺激性气味,具有强氧化性,温度稍高即分解放出氧气并生成醋酸(CH3COOH),请写出过氧乙酸分解的化学方程式______.
 hn12801年前4
hn12801年前4 -
 胡宽 共回答了16个问题
胡宽 共回答了16个问题 |采纳率81.3%解题思路:根据题意:过氧乙酸温度稍高即分解放出氧气并生成醋酸(CH3COOH),然后根据方程式的书写步骤“写配注等”进行书写.过氧乙酸温度稍高即分解放出氧气并生成醋酸,方程式是2C2H4O3=2CH3COOH+O2↑;
故答案为:2C2H4O3=2CH3COOH+O2↑.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了学生根据题目信息书写方程式的能力,难度不大.1年前查看全部
- 双氧水(H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
双氧水(H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为______克,溶剂为______克.
(2)小明倒出了300g双氧水溶液进行消毒,则剩下的溶液中溶质的质量分数为______. 上只角小开1年前1
上只角小开1年前1 -
 小言不分 共回答了28个问题
小言不分 共回答了28个问题 |采纳率82.1%(1)溶质=溶液的质量×溶液中溶质的质量分数=600g×5%=30g;溶剂=溶液-溶质=600g-30g=570g
(2)溶液具有均一性,所以剩下的溶液中的溶质质量分数不变.
故答案:(1)30;570;(2)5%1年前查看全部
- 用化学用语填空:(1)1个氧分子______,2个氢原子______,氧化铝______(2)某新型消毒剂由Cl、O两种
用化学用语填空:
(1)1个氧分子______,2个氢原子______,氧化铝______
(2)某新型消毒剂由Cl、O两种元素组成,且每个分子中含有1个Cl原子,2个O原子,该消毒剂的化学式是______. 风-情1年前1
风-情1年前1 -
 zjaklove 共回答了19个问题
zjaklove 共回答了19个问题 |采纳率73.7%(1)根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此1个氧分子 表示为:O 2 ;
根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.因此2个氢原子表示为:2H;
根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,氧元素的化合价为-2,铝元素的化合价为+3,因此氧化铝的化学式为:Al 2 O 3 ;
(2)根据题意:每个分子中含有1个Cl原子,2个O原子,因此该消毒剂的化学式为:ClO 2 ;
故答案为:
(1)O 2 ,2H,Al 2 O 3 ;
(2)ClO 2 .1年前查看全部
- (2008•海南)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2是新一代饮用水的消毒剂,我
(2008•海南)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观过程图如图:
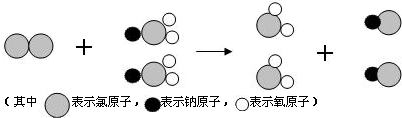
试回答:
(1)ClO2叫做______,其中氯元素的化合价为______;
(2)根据反应的微观过程图写出反应的化学方程式______. zhongwelfp1年前1
zhongwelfp1年前1 -
 7oo了 共回答了16个问题
7oo了 共回答了16个问题 |采纳率87.5%解题思路:(1)物质化学式的读法,由两种元素物质,一般从右向左依次读出各元素的名称,并在两种元素间加上“化”字,当原子个数不是一个时一般要读出原子个数;利用物质的化学式,根据化合物中元素化合价代数和为零,可计算其中氯元素的化合价;
(2)根据反应微观图中各物质的分子构成模型图,判断分子的构成,利用分子构成写出物质的化学式,然后完成反应的化学方程式.(1)化学式ClO2中有氯、氧两种元素,且每个分子中含有两个氯原子和一个氧原子,因此,物质的化学式读为二氧化氯;
其中O为-2价,设Cl元素化合价为x,则x+(-2)×2=0,解得x=+4;
故答案为:二氧化氯;+4;
(2)该反应的反应物分子为:由两个氯原子构成的一个氯气Cl2分子,由一个钠原子、一个氯原子、两个氧原子构成的NaClO2分子;生成物的分子为:由一个氯原子、两个氧原子构成的ClO2分子,一个钠原子、一个氯原子构成的NaCl分子;因此,该反应的化学方程式可写为Cl2+2NaClO2=2ClO2+2NaCl;
故答案为:Cl2+2NaClO2═2ClO2+2NaCl.点评:
本题考点: 微粒观点及模型图的应用;化学式的书写及意义;有关元素化合价的计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 根据构成物质的分子的微观模型图,可判断分子的构成,由分子的构成可确定物质的组成及物质的化学式.1年前查看全部
- 请求指点迷津……过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可由冰醋酸和过氧化氢在一定条件
请求指点迷津……
过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,它可由冰醋酸和过氧化氢在一定条件下制得;他可以迅速杀灭多种微生物,包括多种病毒、细菌、真菌及芽孢.有关过氧乙酸的叙述正确的是
A.过氧乙酸不能是品红褪色
B.过氧乙酸可与苯酚混合使用
C.过氧乙酸分子中只含有极性键
D.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体 沛丫头1年前4
沛丫头1年前4 -
 cndy24 共回答了19个问题
cndy24 共回答了19个问题 |采纳率78.9%D
具有氧化性,所以可使品红褪色
会氧化苯酚
含有氧氧非极性键1年前查看全部
- (2014•齐齐哈尔)84消毒液是一种消毒剂,主要成分为次氯酸钠(化学式是NaClO).它的消毒原理是:2NaClO+C
(2014•齐齐哈尔)84消毒液是一种消毒剂,主要成分为次氯酸钠(化学式是NaClO).它的消毒原理是:2NaClO+CO2+H2O═X+2HClO则X的化学式为( )
A.NaCl
B.NaOH
C.Na2CO3
D.Cl2 s366s3661年前1
s366s3661年前1 -
 伊荻鸶 共回答了25个问题
伊荻鸶 共回答了25个问题 |采纳率88%解题思路:化学反应前后,元素的种类不变,原子的种类、总个数不变.由2NaClO+CO2+H2O═X+2HClO可知,
反应前钠原子的相对个数是2个,反应后应该是2个,包含在X中;
反应前氯原子的相对个数是2个,反应后是2个;
反应前氧原子的相对个数是5个,反应后应该是5个,其中3个包含在X中;
反应前碳原子的相对个数是1个,反应后1个,包含在X中;
反应前氢原子的相对个数是2个,反应后是2个;
由分析可知,X是碳酸钠,化学式是Na2CO3.
故选C.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.1年前查看全部
- (2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图(表示氯原子,表示钠原子,○表示氧
 (2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图(
(2012•永州)ClO2是新型的饮用水消毒剂.如图是制取ClO2的化学反应微观过程图( 表示氯原子,
表示氯原子, 表示钠原子,○表示氧原子),你认为下列从中获取的信息错误的是( )
表示钠原子,○表示氧原子),你认为下列从中获取的信息错误的是( )
A.分子在化学变化中可以再分
B.氧原子的数目在反应前后不变
C.反应中只有一种物质是单质
D.可推出 的化学式为H2O
的化学式为H2O  Baby_Lily1年前1
Baby_Lily1年前1 -
 狂奔乱舞 共回答了14个问题
狂奔乱舞 共回答了14个问题 |采纳率78.6%解题思路:根据微观示意图可知反应的方程式为:Cl2+2NaClO2=2ClO2+2NaCl,分析微粒的变化:分子的种类发生了改变,原子的种类和个数都不变,Cl2属于单质等.A、由微观示意图可知:Cl2经过变化变成了新的分子ClO2;故说法正确;
B、由微观示意图可知:氧原子在反应前后的个数都是4个;故说法正确;
C、Cl2、NaClO2、ClO2、NaCl四种物质中只有Cl2是由一种元素组成的纯净物,属于单质,故说法正确;
D、根据 表示氯原子,○表示氧原子,因此
表示氯原子,○表示氧原子,因此 表示ClO2;故说法错误;
表示ClO2;故说法错误;
故选项为:D.点评:
本题考点: 微粒观点及模型图的应用;单质和化合物的判别.
考点点评: 本题主要考查了在化学变化中分子和原子的关系及其物质的分类方面的知识,可以依据质量守恒定律、分子和原子的区别及物质的微观结构结合图示进行分析.1年前查看全部
- 下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是 ( )
下列物质是自来水厂对水净化过程常用的消毒剂,其中属于氧化物的是( )
A.Cl2
B.O3
C.ClO2
D.Ca(ClO)2 koine1年前1
koine1年前1 -
 hj1019 共回答了19个问题
hj1019 共回答了19个问题 |采纳率94.7%解题思路:氧化物是指由两种元素组成并且其中一种元素是氧元素的化合物.氧化物的特点是由两种元素组成的化合物,其中一种元素是氧元素.A、氯气是由氯元素组成的纯净物,属于单质,不属于氧化物.故不正确;
B、臭氧是由氧元素组成的纯净物,属于单质,不属于氧化物.故不正确;
C、二氧化氯是由氧元素和氯元素组成的化合物,属于氧化物.故正确;
D、次氯酸钙是由钙元素、氯元素和氧元素组成的,不属于氧化物.故不正确.
故选:C.点评:
本题考点: 从组成上识别氧化物.
考点点评: 解答本题要正确的分析物质是由几种元素组成的,如果由氧元素和另外一种元素组成并且属于化合物就属于氧化物.1年前查看全部
- 11.世界卫生组织(WHO)将二氧化氯ClO2列为A级高效安全灭菌消毒剂,ClO2是一种消毒杀菌效率高,二次污染小的水处
11.世界卫生组织(WHO)将二氧化氯ClO2列为A级高效安全灭菌消毒剂,ClO2是一种消毒杀菌效率高,二次污染小的水处理剂,它在食品保鲜,饮用水消毒等方面有着广泛的应用.
(1)实验室制备ClO2的方法之一为:
2KClO3+H2C2O4+H2SO4 2ClO2↑+K2SO4+2CO2↑+2H2O(H2C2O4俗称草酸,其中H为+1价,O为-2价),则下列说法正确的是( )AC
A.KClO3在反应中得到电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.1 molKClO3参加反应有2mol电子转移
(2)下列关于ClO2的说法中正确的是( )AC
A.二氧化氯是强氧化剂
B.二氧化氯是强还原剂
C.1个二氧化氯分子由2个O原子和1个Cl原子组成
D.二氧化氯分子中氯为负1价
(3)KClO3和浓盐酸在一定温度下反应也会生成绿黄色的二氧化氯.其变化可表示为
2KClO3+4HCl=2KCl+2ClO2↑+Cl2↑+2H2O
①浓盐酸在反应中显示出来的性质是___________;
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②已知每产生0.1molCl2,则发生转移的电子的物质的量为0.2mol.ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒后的还原产物是氯离子,则其消毒的效率(以单位质量得到的电子数表示)是Cl2的 倍.
综合应用
最后一问的答案是2.63倍,不知道怎么算出来的
 冰与火的故事1年前1
冰与火的故事1年前1 -
 32520z12 共回答了17个问题
32520z12 共回答了17个问题 |采纳率88.2%1molCl2,则发生转移的电子的物质的量为2mol,消毒效率(以单位质量得到的电子数表示)=2/71,而1molClO2,发生转移的电子的物质的量为5mol,所以消毒效率(以单位质量得到的电子数表示)=5/67.5,5/67.5:2/71=2.63,所以ClO2消毒效率是Cl2的2.63倍.1年前查看全部
- (2014•徐汇区一模)有一种高效安全的灭菌消毒剂,其化学式为RO2,实验测得该氧化物中R与O的质量比为71:64,则R
(2014•徐汇区一模)有一种高效安全的灭菌消毒剂,其化学式为RO2,实验测得该氧化物中R与O的质量比为71:64,则R02是( )
A.ClO2
B.NO2
C.SO2
D.CaO gl99991年前1
gl99991年前1 -
 yuanye188 共回答了18个问题
yuanye188 共回答了18个问题 |采纳率94.4%解题思路:根据根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,可计算出R的相对原子质量,从而确定R的元素种类,写出其氧化物的化学式即可.设R的相对原子质量是x,则
x:(16×2)=71:64 解得x=35.5
因为氯原子的相对原子质量是35.5,所以RO2的化学式为ClO2.
故选:A.点评:
本题考点: 元素质量比的计算.
考点点评: 本题难度不大,考查同学们灵活运用化学式的有关计算进行推断化学式的能力.1年前查看全部
- 丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
丁子香酚可做香味剂,萨罗可做消毒剂,二者的结构简式如图所示,下列说法不正确的是( )
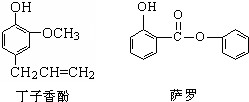
A.萨罗的分子式为C13H10O3
B.丁子香酚与浓溴水只发生取代反应
C.萨罗和丁子香酚均能发生氧化反应
D.丁子香酚和萨罗均能与氯化铁溶液发生显色反应 ggss1年前1
ggss1年前1 -
 warmdella 共回答了9个问题
warmdella 共回答了9个问题 |采纳率88.9%解题思路:A、根据结构简式书写分子式;
B、碳碳双键可以与溴水加成;
C、酚羟基易被氧化;
D、酚羟基遇到氯化铁溶液发生显色反应.A、根据结构简式得出分子式为:C13H10O3,故A正确;
B、丁子香酚中含有碳碳双键,可以与溴水加成,故B错误;
C、萨罗和丁子香酚中均含有酚羟基,易被氧化,故C正确;
D、丁子香酚和萨罗中均含有酚羟基,遇到氯化铁溶液会发生显色反应,故D正确.
故选B.点评:
本题考点: 有机物分子中的官能团及其结构.
考点点评: 本题是一道有关有机物基础知识点考查的题目,可以根据所学知识来回答,难度不大.1年前查看全部
大家在问
- 1动物园里饲养了一群丹顶鹤和一群乌龟,一共有46只眼睛,42只脚,丹顶鹤和乌龟各有多少只?
- 2If we give enough if we learn to trust,But only love can say
- 3社戏 句子理解回望戏台在等火光中,却又如初来乍到的时候一般,又飘渺得像一座仙山楼阁,满被红霞罩着了.“回望”表现了“我”
- 4马师傅要用一块圆形铁板尽量不浪费材料的情况下裁剪出一个等边三角形,他是这样做的:在圆o中画出直径a
- 5如何除去下列物质中的杂质,(写出除杂步骤和化学方程式)
- 6诗词欣赏 千山鸟飞绝,万径人踪灭.
- 7如图,手拉着小车静止在倾角为30°的光滑斜坡上,已知小车的质量为2.6kg,求:
- 8如图(20),在直三棱柱ABC-A1B1C1中,AB=4,AC=BC=3,D为AB的中点.
- 9把1,2,3,4,5,6,7,8,八个数字填入下面的方格中,使下图中所有的不等号都成立
- 10定积分里 旋转体积的问题如果旋转体不绕坐标轴转的话 那个体积公式应该怎么样的啊比如说 绕x=1 在原先的公式上该怎么改动
- 11翻译:随着科技发展,因特网被广泛的运用
- 127777=7加什么运算符号算式才成立
- 13若不等式x^2+ax+9>=0对x属于[0,4]恒成立 求a的取值范围
- 14解方程:0.3分之1.2y-1-0.6分之1-y
- 15关于电场力和洛伦兹力,下列说法中正确的是( )

