(2013•宝鸡一模)请根据化学反应的有关原理回答下列问题.
 Hamani2022-10-04 11:39:541条回答
Hamani2022-10-04 11:39:541条回答(1)现代工业采用甲烷部分氧化法制H2,其反应式为:
CH4(g)+[1/2]O2(g)=CO(g)+2H2(g)△H1=-35.6kJ/mol…①
试判断常温下,上述反应能否自发进行?______.(选填“能”或“否”).
有研究认为甲烷部分氧化的机理为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H2=-890.3kJ/mol…②
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H3=+247.3kJ/mol…③
试结合反应①确定下面热化学反应方程式中的△H:
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=______kJ/mol
(2)在恒温条件下,将N2与H2按一定比例混合的气体充入一个2L固定容积的密闭容器中,10分钟后反应达平衡时,n(N2)=1.2mol,n(H2)=1.2mol,n(NH3)=0.8mol,则反应速率
v(N2)=______mol/(L•min),H2的转化率=______,平衡常数K=______.若保持容器的温度和容积不变,将上述平衡体系中的混合气体均增加0.8mol,则平衡会向______移动(选填“正反应方向”、“逆反应方向”或“不”).
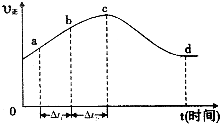
(3)O3氧化脱除燃煤烟气中NO的反应为NO(g)+O3(g)⇌NO2(g)+O2(g).在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应,正反应速率时间变化的关系如图所示.由图可得出的正确说法是______
A.该反应为放热反应
B.反应物浓度:b点小于c点
C.反应在c点恰好达到平衡状态
D.△t1=△t2时,NO的转化量:a~b段小于b~c段
(4)已知当溶液中某种离子浓度小于10-5mol/L时即可看作完全沉淀.现向浓度均
为0.022mol/L的CuSO4、Fe2(SO4)3的混合溶液中加入NaOH溶液,当溶液的pH=______时,Fe3+才能完全沉淀,此时Cu2+是否开始沉淀?______(选填“是”或“否”).[已知常温下Cu(OH)2的KSP=2.2×10-20,Fe(OH)3的KSP=1.25×10-36,lg2=0.3]
若要除去上述混合溶液中的Fe3+,可采取的方法是:先向溶液中加入下列物质中的______,然后过滤.
A.NaOH B.CuO C.Cu(OH)2 D.NH3•H2O.

已提交,审核后显示!提交回复
共1条回复
 gdzhwqs 共回答了20个问题
gdzhwqs 共回答了20个问题 |采纳率85%- 解题思路:(1)反应的自发性是由熵变和焓变共同决定,若△H<0,△S>0,则一定能自发进行,若△H>0,△S<0,则一定不能自发进行,若△H<0,△S<0或△H>0,△S>0,则可以自发进行,是否自发和温度有关.用盖斯定定律进行反应热的计算,如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的.
(2)化学反应速率、转化率和平衡移动有关知识的考查,涉及到三行式的应用.其中在保持容器的温度和容积不变,将上述平衡体系中的混合气体均增加0.8mol,相当于给原平衡体系加压,接下来考虑外界因素对平衡移动的影响.
(3)化学平衡图象题,根据图象开始阶段反应速率逐渐增大,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,所以该反应是放热反应,随着反应的进行,反应物的浓度逐渐减小,c点反应速率还再变化,而不是固定不变,只有不再随时间的变化而变化,才是平衡状态,△t1=△t2时,NO的转化量,看a~b段和b~c段斜率大小.
(4)通过溶度积的表达式,求溶液的PH;离子积和溶度积的相对大小来判断沉定是否形成.除杂是铁离子水解平衡的考查,除杂的同时不能新杂质.(1)在CH4(g)+[1/2]O2(g)=CO(g)+2H2(g)△H1=-35.6kJ/mol中,在化学反应中若△H<0,△S>0,则一定能自发进行,若△H>0,△S<0,则一定不能自发进行,若△H<0,△S<0或△H>0,△S>0,则可以自发进行,是否自发和温度有关.而该反应的△S>0,△H<0所以反应一定能自发.故答案为:能
用盖斯定定律进行反应热的计算,如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热是相同的.通过分析,
目标反应的△H=(4△H1-△H2-△H3)÷2=[-35.6kJ/mol×4-(-890.3kJ/mol)-247.3kJ/mol]÷2=+250.3kJ/mol,故答案为:+250.3kJ/mol.
(2)设起始时n(N2)为xmol,n(H2)为ymol,N2的转化量为amol由方程式可知:
N2 +3H2 ⇌2NH3
起始量(mol)xy0
变化量(mol)a3a2a
平衡量(mol)x-a3a 2a
由题意可知:x-a=1.2,y-3a=1.2,2a=0.8,
即:x=1.6mol,y=2.4mol,a=0.4mol,所以反应速率v(N2)=
0.4mol
2L
10min=0.02mol/(L•min),
H2的转化率为:[3×0.4mol/2.4mol]×100%=50%,平衡常数K为
(0.4mol/L)2
0.6mol/L×(0.6mol/L)3=1.23,
其中在保持容器的温度和容积不变,将上述平衡体系中的混合气体均增加0.8mol,相当于给原平衡体系加压,增加压强平衡向正反应方向.
故答案为:0.02mol/(L•min);50%;1.23;平衡向正反应方向;
(3)A.开始阶段反应速率逐渐增大,说明反应刚开始时温度升高对正反应速率的影响大于浓度减小对正反应速率的影响,所以该反应是放热反应,故A正确;
B.随着反应的进行,反应物的浓度逐渐减小,所以b点反应物的浓度大于c点,故B错误;
C.根据图象可知c点反应速率还再变化,因此不是平衡状态,故C错误;
D.根据曲线的斜率可知b~c段反应速率快,反应物的转化率大,故D正确.
故答案为:AD;
(4)当Fe3+完全沉淀时,C(OH-)=
3
Ksp
CFe3+
=
3
1.25×10−36
10−5
=5×10-11,则PH=-lg
10−14
5×10−11=3.7,
QC=0.022×(5×10-11)2=5.5×10-23<2.2×10-20=Ksp,所以没有Cu2+沉淀.Fe3++3H2O⇌Fe(OH)3+3H+ 加入这种物质必须促进其水解,而且不能引进新杂质,ABCD都促进水解,水解平衡正向移动,但AD引入新的杂质.
故答案为:3.7;否;BC.点评:
本题考点: 用盖斯定律进行有关反应热的计算;化学平衡的影响因素;化学平衡的计算;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题综合性较大,涉及盖斯定律的计算、化学平衡常数、图象分析,平衡移动、盐类水解,难溶电解质的考查等,难度中等,是对学生综合能力的考查,(4)为易错点,判断两者的相对大小是关键. - 1年前
相关推荐
- (2014•宝鸡二模)函数y=2sin(2x+[π/3])的最小正周期为( )
(2014•宝鸡二模)函数y=2sin(2x+[π/3])的最小正周期为( )
A.4π
B.π
C.2π
D.[π/2] rich2b1年前1
rich2b1年前1 -
 步惊云一号 共回答了14个问题
步惊云一号 共回答了14个问题 |采纳率92.9%解题思路:根据y=Asin(ωx+φ)的周期等于 T=[2π/ω],得出结论.函数y=2sin(2x+[π/3])的最小正周期为T=[2π/2]=π,
故选:B.点评:
本题考点: 三角函数的周期性及其求法.
考点点评: 本题主要考查三角函数的周期性及其求法,利用了y=Asin(ωx+φ)的周期等于 T=[2π/ω],属于基础题.1年前查看全部
- (2010•宝鸡三模)下列叙述中正确的是( )
(2010•宝鸡三模)下列叙述中正确的是( )
A.脂肪、淀粉、纤维素和蛋白质均属于天然高分子化合物
B.正丁烷、异丁烷分别与氯气反应生成的一氯代物都有两种同分异构体
C.乙烯、苯、乙烷三种分子中,所有的原子都在同一平面上
D.聚乙烯的结构简式为
 angelchen1年前1
angelchen1年前1 -
 风信孑 共回答了16个问题
风信孑 共回答了16个问题 |采纳率100%解题思路:A、脂肪不是高分子化合物.
B、根据等效H原子判断,有几种H原子,一氯代产物有几种同分异构体.
C、乙烷中含有甲基,具有甲烷的四面体结构.
D、聚乙烯中不含碳碳双键.A、淀粉、纤维素和蛋白质均属于天然高分子化合物,脂肪是饱和高级脂肪酸与甘油形成的酯,相对分子质量较小,不属于高分子化合物,故A错误;
B、正丁烷分子中有2种H原子,一氯代物有两种同分异构体;异丁烷中有2种H原子,一氯代物有两种同分异构体,故B正确;
C、乙烯、苯都是平面结构,所有原子处于同一平面,乙烷中含有甲基,具有甲烷的四面体结构,所有原子不可能处于同一平面,故C错误;
D、聚乙烯中不含碳碳双键,聚乙烯结构简式为 ,故D错误.
,故D错误.
故选:B.点评:
本题考点: 同分异构现象和同分异构体;结构简式;常见有机化合物的结构;有机高分子化合物的结构和性质.
考点点评: 考查同分异构体、分子构型、有机高分子化合物概念、结构简式等,难度不大,注意B选项中根据等效H原子判断同分异构体数目.分子中等效氢原子一般有如下情况:
①、分子中同一甲基上连接的氢原子等效,同一碳原子所连的氢原子是等效的;
②、同一碳原子所连甲基上的氢原子等效;
③、处于镜面对称位置(相当于平面成像时,物与像的关系)上的氢原子等效.1年前查看全部
- (2010•宝鸡三模)下列实验装置进行的实验中,不能达到相应实验目的是( )
(2010•宝鸡三模)下列实验装置进行的实验中,不能达到相应实验目的是( )
A.
分离沸点不同且互溶的液体混合物
B.
实验室制取乙酸乙酯
C.
验证NH3的溶解性
D.
b口进气可用排水法收集NO2、CO等气体 蛋黄酱超人1年前1
蛋黄酱超人1年前1 -
 落魄书生5 共回答了18个问题
落魄书生5 共回答了18个问题 |采纳率94.4%解题思路:A.分离沸点不同的液体混合物可用蒸馏的方法;
B.乙酸和乙醇在浓硫酸作用下加热可生成乙酸乙酯,用饱和碳酸钠溶液吸收并除杂;
C.根据氨气极易溶于水后压强的变化分析;
D.CO不能用排空法收集.A.沸点不同的液体混合物可用蒸馏的方法分离,装置正确,故A正确;
B.乙酸和乙醇在浓硫酸作用下加热可生成乙酸乙酯,乙酸乙酯不溶于饱和碳酸钠溶液,并且饱和碳酸钠溶液可除去杂质,导管不能插入到液面以下,防止倒吸,故B正确;
C.氨气极易溶于水,烧瓶内压强减小,气球体积变大,可证明,故C正确;
D.CO密度和空气接近,不能用排空法收集,故D错误.
故选D.点评:
本题考点: 化学实验方案的评价;物质的分离、提纯的基本方法选择与应用;气体的收集;氨的制取和性质;乙酸乙酯的制取.
考点点评: 本题考查实验方案的评价,题目难度中等,易错点为D,注意根据气体的性质选择收集方法.1年前查看全部
- (2013•宝鸡三模)NA表示阿伏加德罗常数,下列与含氯化合物有关的说法正确的是( )
(2013•宝鸡三模)NA表示阿伏加德罗常数,下列与含氯化合物有关的说法正确的是( )
A.HClO是弱酸,所以NaClO是弱电解质
B.向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C.HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物
D.电解NaCl溶液得到22.4LH2(标准状况),理论上需要转移NA个电子 zyu55001年前1
zyu55001年前1 -
 绿帽子真好看 共回答了15个问题
绿帽子真好看 共回答了15个问题 |采纳率93.3%解题思路:A、次氯酸是弱酸,次氯酸钠是盐属于强电解质;
B、依据氢氧化铁胶体的实验室制备方法分析判断;
C、离子化合物是离子构成的化合物,氯化氢是共价化合物水溶液中电离成离子;
D、依据电解氯化钠反应的化学方程式计算电子转移;A、次氯酸是弱酸,次氯酸钠是盐属于强电解质,故A错误;
B、向沸水中逐滴加入少量饱和FeCl3溶液,加热可制得Fe(OH)3胶体,故B正确;
C、离子化合物是离子构成的化合物,氯化氢是共价化合物水溶液中电离成离子,氯化钠是离子化合物,故C错误;
D、电解NaCl溶液得到22.4LH2(标准状况)物质的量为1mol,反应为:2NaCl+2H2O
通电
.
2NaOH+Cl2↑+H2↑,理论上需要转移2NA个电子,故D错误;
故选B.点评:
本题考点: 阿伏加德罗常数;氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查了强弱电解质的概念应用,氢氧化铁胶体的实验室制备方法,离子化合物的分析判断,电解反应的电子转移数目计算.1年前查看全部
- 有两张陕西省交通地图比例尺为1:1000000和1:600000,西安到宝鸡的距离差为12cm,求实际西安到宝鸡的距
 一念无望1年前1
一念无望1年前1 -
 e-sailing 共回答了29个问题
e-sailing 共回答了29个问题 |采纳率89.7%假设在比例尺是1:1000000的地图上图上距离为a,则在比例尺为1:60000的地图上图上距离就是a+12,实际距离不变,列方程1000000a=(a+12)600000,400000a=7200000,则a=18,所以实际距离=18×1000000=18000000厘米=180千米.1年前查看全部
- (2009•宝鸡)下列对日常生活中某些做法的认识没有科学依据的是( )
(2009•宝鸡)下列对日常生活中某些做法的认识没有科学依据的是( )
A.菜刀擦干后放在干燥的地方不易生锈
B.从某种意义上来说,垃圾也是资源,应分类回收处理
C.通常情况下,用硬水洗衣服比用软水洗衣服效果好
D.失火时,要冷静地根据具体情况,采取相应的措施自救 LOVE滢1年前1
LOVE滢1年前1 -
 clare001 共回答了19个问题
clare001 共回答了19个问题 |采纳率73.7%解题思路:A、根据铁生锈的实质和防止铁生锈的措施判断.
B、根据垃圾回收的意义判断.
C、根据硬水的危害判断.
D、根据火灾逃生的措施判断.A、铁生锈实际上是铁与空气中的氧气和水反应,要防止铁生锈就要隔绝氧气和水,所以正确.
B、垃圾回收再利用,不单可减少环境污染,还能节约资源,故从某种意义上说,垃圾也是资源,应分类回收处理,所以正确.
C、硬水洗衣浪费洗涤剂,且洗出的衣服较硬,所以错误.
D、失火时,要冷静地根据具体情况,采取相应的措施自救,如火势可控,则自行灭火,如不可控则求救或逃生,所以正确.
故选C点评:
本题考点: 金属锈蚀的条件及其防护;常见的意外事故的处理方法;硬水与软水;常见污染物的来源、危害及治理.
考点点评: 本题考查利用课本知识解决新问题能力,能加深学生对课本知识的理解,训练学生的思维能力.1年前查看全部
- (2012•宝鸡二模)如图所示,虚线A、B、C为某电场中的三条等势线,其电势分别为3V、5V、7V,实线为带电粒子在电场
 (2012•宝鸡二模)如图所示,虚线A、B、C为某电场中的三条等势线,其电势分别为3V、5V、7V,实线为带电粒子在电场中运动时的轨迹,P、Q为轨迹与等势线A、C的交点,带电粒子只受电场力,则下列说法正确的是( )
(2012•宝鸡二模)如图所示,虚线A、B、C为某电场中的三条等势线,其电势分别为3V、5V、7V,实线为带电粒子在电场中运动时的轨迹,P、Q为轨迹与等势线A、C的交点,带电粒子只受电场力,则下列说法正确的是( )
A.粒子可能带负电
B.粒子在P点的动能大于Q点动能
C.粒子在P点电势能大于粒子在Q点电势能
D.粒子在P点受到电场力大于Q点受到的电场力 听风男人1年前1
听风男人1年前1 -
 ww无间 共回答了22个问题
ww无间 共回答了22个问题 |采纳率86.4%解题思路:由电场线与等势面的关系可得出电场线的方向,根据曲线的弯曲方向可知粒子的受力方向及粒子的电性;由等势面的疏密可知电场强度的大小,由F=Eq可知电场力的大小关系;由电势及电势能的关系可知两点的电势能大小关系;由动能定理可知P、Q两点的间的动能的变化.A、因电场线与等势面相互垂直,且由高电势指向低电势,故电场线如图所示,由粒子运动的轨迹弯曲的方向可知粒子受力沿电场线的方向,故粒子带正电;故A错误;
B、若粒子从P到Q,则电场力做负功,粒子动能减小,故P点动能大于Q点动能;若粒子从Q到P,电场力做正功,动能增大,P点动能大于Q点动能,故粒子在P点动能一定大于Q点的动能,故B正确;
C、因P点电势小于Q点电势,粒子带正电,由E=φq可知P点的电势能小于Q点的电势能,故C错误;
D、因Q点处的等势面密集,故Q点的电场强度大,故电荷在Q点受到的电场力大于P点受到的电场力,故D错误;
故选:B.
点评:
本题考点: 电场线;电势能.
考点点评: 本题中解题的关键在于曲线的弯曲方向的判断,应掌握根据弯曲方向判断受力方向的方法;本题中告诉的是等势面,很多同学由于思维定势当成了电场线从而出现错判.1年前查看全部
- (2010•宝鸡模拟)为分析甲、乙两人数学学习状况,学校分别从他两的若干次数学模拟考试中,随机抽取6次的成绩,记录如下:
(2010•宝鸡模拟)为分析甲、乙两人数学学习状况,学校分别从他两的若干次数学模拟考试中,随机抽取6次的成绩,记录如下:

(I)用茎叶图表示这两组数据;
(II)现从统计学的角度考虑,你估计哪位学生下次数学考试成绩较高?请说明理由.
(III)若将频率视为概率,对甲同学在今后的3次数学考试成绩进行预测,求这3次成绩有2次高于80分的概率. 2347891年前0
2347891年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•宝鸡模拟)某班50名学生在一次百米测试中,成绩全部都介于13秒到18秒之间,将测试结果按如下方式分成五组,第
 (2012•宝鸡模拟)某班50名学生在一次百米测试中,成绩全部都介于13秒到18秒之间,将测试结果按如下方式分成五组,第一组[13,14),第二组[14,15)…第五组[17,18]如图是按上述分组方法得到的频率分布直方图.
(2012•宝鸡模拟)某班50名学生在一次百米测试中,成绩全部都介于13秒到18秒之间,将测试结果按如下方式分成五组,第一组[13,14),第二组[14,15)…第五组[17,18]如图是按上述分组方法得到的频率分布直方图.
(1)若成绩大于等于14秒且小于16秒规定为良好,求该班在这次百米测试中成绩为良好的人数.
(2)设m,n表示该班两个学生的百米测试成绩,已知m,n∈[13,14)∪[17,18]求事件“|m-n|>2”的概率. loca雨桐1年前1
loca雨桐1年前1 -
 823里的大哥 共回答了22个问题
823里的大哥 共回答了22个问题 |采纳率90.9%解题思路:(Ⅰ)根据直方图矩形的面积表示频率,可知成绩在[14,16)内的人数;
(Ⅱ)成绩在[13,14)的人数有2人,设为a,b.成绩在[17,18]的人数有3人,设为A,B,C;基本事件总数为10,事件“|m-n|>2”由6个基本事件组成.根据古典概型公式可求出所求.(Ⅰ)根据直方图可知成绩在[14,16)内的人数为:50×0.18+50×0.38=28人;(5分)
(Ⅱ)成绩在[13,14)的人数有:50×0.04=2人,设为a,b.
成绩在[17,18]的人数有:50×0.06=3人,
设为A,B,C.m,n∈[13,14)时有ab一种情况.
m,n∈[17,18]时有AB,AC,BC三种情况.
m,n分别在[13,14)和[17,18]时有aA,aB,aC,bA,bB,bC六种情况.
基本事件总数为10,事件“|m-n|>2”由6个基本事件组成.
所以P(|m-n|>2)=[6/10=
3
5](13分)点评:
本题考点: 频率分布直方图;用样本的数字特征估计总体的数字特征.
考点点评: 本题主要考查了频率分布直方图,以及古典概型的概率问题、用样本的数字特征估计总体的数字特征等有关知识,属于中档题.1年前查看全部
- (2012•宝鸡三模)A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素、原子半径A
(2012•宝鸡三模)A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素、原子半径A、B、E、D、C依次增大,C、D核外电子数之和与B、E核外电子数之和相等,B元素的原子核外L层电子数是K层电子数的3倍.下列叙述中正确的是( )
A.C、D、E的最高价氧化物对应的水化物两两间均能反应
B.A与E形成的化合物一定为离子化合物
C.B与C形成的化合物只含离子键
D.A.B.E三元素中两两形成的化合物最多有4种 水牛04021年前1
水牛04021年前1 -
 我是飘雪 共回答了13个问题
我是飘雪 共回答了13个问题 |采纳率92.3%解题思路:A、B、C、D、E五种短周期主族元素原子序数逐渐增大.B元素的原子核外L层电子数是K层电子数的3倍,则L层电子数为6,故B为O元素;B与E为同族元素,则E为S元素;C、D的核外电子数之和与B、E核外电子数之和相等,即C、D核外电子数之和为8+16=24,且C、D原子半径最大,应为金属元素,可知C为Na元素,D为Al元素,A与C同主族,且原子半径最小,应为H元素,根据元素所在周期表中的位置结合元素周期律的递变规律解答该题.A、B、C、D、E五种短周期主族元素原子序数逐渐增大.B元素的原子核外L层电子数是K层电子数的3倍,则L层电子数为6,故B为O元素;B与E为同族元素,则E为S元素;C、D的核外电子数之和与B、E核外电子数之和相等,即C、D核外电子数之和为8+16=24,且C、D原子半径最大,应为金属元素,可知C为Na元素,D为Al元素,A与C同主族,且原子半径最小,应为H元素,
A.C、D、E最高价氧化物的水化物分别为NaOH、Al(OH)3、H2SO4,Al(OH)3是两性氧化物与强碱、强酸反应,氢氧化钠与硫酸反应生成硫酸钠与水,三者可以两两反应,故A正确;
B.H元素与S元素形成的化合物为H2S,属于共价化合物,故B错误;
C.O元素与Na元素形成的化合物Na2O2,既含有离子键又含有共价键,故C错误;
D.H、O、S三元素中两两形成的化合物有:H2O、H2O2、H2S、SO2、SO3,故D错误,
故选A.点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题考查位置结构性质的关系及应用,难度中等,根据元素所在周期表中的位置结合元素周期律知识解答,推断元素是解题的关键.1年前查看全部
- (2014•宝鸡一模)函数f(x)=(sinx+cosx)2的最小正周期为( )
(2014•宝鸡一模)函数f(x)=(sinx+cosx)2的最小正周期为( )
A.2π
B.π
C.[π/2]
D.[π/4] maggie1181年前1
maggie1181年前1 -
 Mandy2008 共回答了14个问题
Mandy2008 共回答了14个问题 |采纳率92.9%解题思路:将f(x)=(sinx+cosx)2展开,可得f(x)=1+sin2x,从而可求得其最小正周期.∵f(x)=(sinx+cosx)2
=1+2sinxcosx
=1+sin2x,
∴f(x)的最小正周期为T=[2π/2]=π.
故选:B.点评:
本题考点: 三角函数的周期性及其求法.
考点点评: 本题考查三角恒等变换,考查三角函数的周期性及其求法,属于基础题.1年前查看全部
- (2014•宝鸡三模)设函数f(x)=x2+bln(x+1),其中b≠0.
(2014•宝鸡三模)设函数f(x)=x2+bln(x+1),其中b≠0.
(1)若b=-12,求f(x)在[1,3]的最小值;
(2)如果f(x)在定义域内既有极大值又有极小值,求实数b的取值范围;
(3)是否存在最小的正整数N,使得当n≥N时,不等式ln
>n+1 n
恒成立.n−1 n3  wwwtalent1年前0
wwwtalent1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•宝鸡一模)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料二次电池,则下列说法正
(2013•宝鸡一模)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料二次电池,则下列说法正确的是( )

A.图1若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则铅笔芯C点反应为O2+2H2O+4e-═4OH-
B.图2放电过程中,Na+从正极区向负极区迁移
C.图2充电时阳极区反应为BH-4-8e-+8OH-═BO-2+6H2O
D.图1若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,若铅笔芯C点处出现蓝色,则b接的是A电极 zfwms1年前1
zfwms1年前1 -
 楼主什么玩意 共回答了22个问题
楼主什么玩意 共回答了22个问题 |采纳率90.9%解题思路:A、原电池发生吸氧腐蚀,正极是氧气得电子生成大量的氢氧化钠,能使酚酞变红色;
B、在电池中阳离子向正极移动;
C、充电时阳极区反应为2OH--2e-═H2O2;
D、电解碘化钾溶液时,阳极放电的是碘离子,碘单质遇到淀粉显蓝色.A、若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,构成原电池,则锌电极为负极,锌失电子,铅笔芯为正极,氧气得电子,在该极生成大量的氢氧化钠,能使酚酞变红色,故A正确;
B、在电池中阳离子向正极移动,所以Na+从负极区向正极区迁移,故B错误;
C、充电时阳极区为阴离子失电子,发生氧化反应,其电极反应为2OH--2e-═H2O2,故C错误;
D、若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,A极是负极,B极是正极,阳极放电的是碘离子,碘单质遇到淀粉显蓝色,而铅笔芯C点处出现蓝色,所以C点放电的是碘离子,b为正极,b接的是B电极,故D错误.
故选:A.点评:
本题考点: 化学电源新型电池.
考点点评: 本题是一道有关原电池和电解池的工作原理的综合题目,要求学生熟悉教材基本知识,具备分析和解决问题的能力.1年前查看全部
- (2013•宝鸡三模)对健康的实验小鼠依次进行如下实验操作:先静脉注射放射性碘,待小鼠平静后再静脉注射适量的促甲状腺素.
(2013•宝鸡三模)对健康的实验小鼠依次进行如下实验操作:先静脉注射放射性碘,待小鼠平静后再静脉注射适量的促甲状腺素.随后定时测定甲状腺中的放射性强度.则下列各图能反映其变化规律的是( )
A.
B.
C.
D.
 赶不上我1年前1
赶不上我1年前1 -
 锦瑟横床 共回答了18个问题
锦瑟横床 共回答了18个问题 |采纳率72.2%解题思路:碘是合成甲状腺激素的原料,随着甲状腺利用碘元素合成甲状腺激素和甲状腺激素不断分泌的过程中会导致甲状腺中放射性强度的改变.碘是合成甲状腺激素的原料,促甲状腺激素能促进甲状腺激素的合成与分泌,所以甲状腺细胞利用含有放射性的碘合成甲状腺激素,会导致细胞中的放射性强度不断增加;随着甲状腺激素不断分泌到内环境中,细胞中的放射性强度又不断下降.
故选:C.点评:
本题考点: 动物激素的调节.
考点点评: 本题主要考查甲状腺激素的分级调节内容,意在考查考生理解所学知识的要点,把握知识间的内在联系的能力.1年前查看全部
- (2012•宝鸡模拟)如图所示,以下关于近代物理学的说法中正确的是( )
 (2012•宝鸡模拟)如图所示,以下关于近代物理学的说法中正确的是( )
(2012•宝鸡模拟)如图所示,以下关于近代物理学的说法中正确的是( )
A.光电效应现象中,光电子的最大初动能与照射光的频率成正比
B.氢原子的能级是不连续的,辐射光的能量也是不连续的
C.光的干涉现象中,干涉亮条纹部分是光子到达几率大的地方
D.宏观物体的物质波波长非常小,极易观察到它的波动性 pikaq361年前1
pikaq361年前1 -
 newbee416 共回答了22个问题
newbee416 共回答了22个问题 |采纳率100%解题思路:解答本题抓住:
1、根据光电效应方程EKm=hγ-W0,光电子的最大初动能随照射光的频率的增大而增大;
2、根据玻耳理论分析可知:氢原子的能级是不连续的,辐射光的能量也是不连续的;
3、光是概率波,光的干涉现象中,干涉亮条纹部分是光子到达几率大的地方;
4、宏观物体的物质波波长非常小,不容易观察到它的波动性.A、根据爱因斯坦光电效应方程EKm=hγ-W0,得知:光电子的最大初动能随照射光的频率的增大而增大,但不是正比;故A错误.
B、由玻耳理论可知:氢原子的能级是量子化的,即能级是不连续的,辐射光的能量也是不连续的;故B正确.
C、光是概率波,光的干涉现象中,干涉亮条纹部分是光子到达几率大的地方;故C正确.
D、波长越长,波动性越强,而宏观物体的物质波波长非常小,则不容易观察到它的波动性.故D错误.
故选BC点评:
本题考点: 光的干涉.
考点点评: 解决本题的关键要掌握光电效应方程EKm=hγ-W0、玻耳理论、光是概率波等等基础知识.1年前查看全部
- (2009•宝鸡)某些食品包装袋内有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂
(2009•宝鸡)某些食品包装袋内有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂”的是( )
A.铁粉
B.炭粉
C.氯化钙
D.生石灰 yy781年前1
yy781年前1 -
 我的小媳妇捏 共回答了9个问题
我的小媳妇捏 共回答了9个问题 |采纳率66.7%铁能和水、氧气反应生成铁锈,可以用作“双吸剂”;氯化钙和氧化钙只能吸收水,不能和氧气反应,不能用作“双吸剂”.
故选:A.1年前查看全部
- (2013•宝鸡三模)用化学反应原理相关知识同答
(2013•宝鸡三模)用化学反应原理相关知识同答
Ⅰ.根据下表所示化学反应与数据关系回答下列问题:
(1)反应①是______(填“吸热“或“放热”)反应.化学反应 平衡常数 温度 973K 1173K ①Fe(s)+CO2(g)⇌FeO(s)+CO(g) K1 1.47 2.15 ②Fe(s)+H2O(g)⇌FeO(s)+H2(g) K2 2.38 1.67 ③CO(g)+H2O(g)⇌CO2(g)+H2(g) K3 ? ?
(2)根据反应①与②可推导出同温下K1、K2与K3之间的关系,则K3=K2 K1 (用K1、K2表示).K2 K1
(3)若反应③的逆反应速率与时间的关系如图所示:
①反应在t1、t3、t7时都达到了平衡,若t2时只改变了一种外界条件j试判断:改变的条件可能是______.
②若t4时降压,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线.
Ⅱ.请根据醋酸的电离平衡回答下列问题:
(1)常温下,0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,则溶液的pH=______.
(2)将上述溶液加蒸馏水稀释,在稀释过程中,下列各项中增大的是______(填字母编号).
A.c(H+) B.
C.c(H+)•c(OH-) D.c(H+) c(CH3COOH) c(OH−) c(H+)
(3)25℃时,CH3COOH的电离平衡常数为1.75×10-5,现将一定量的CH3COOH与NaOH溶液混合,若测得混合液pH=5.6,则混合液中各离子浓度由大到小的顺序是______. 海浪琴声1年前1
海浪琴声1年前1 -
 等着月亮来载我 共回答了16个问题
等着月亮来载我 共回答了16个问题 |采纳率81.3%解题思路:Ⅰ、(1)①Fe(s)+CO2(g)⇌FeO(s)+CO(g)分析平衡常数随温度变化,升温平衡常数增大,平衡正向进行,正反应是吸热反应;
(2)依据反应①②③平衡常数表达式计算得到K3;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,根据外界条件对化学反应速率的影响来分析解答;
②t4时降压,逆反应速率减小,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡浓度;
Ⅱ、(1)0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,溶液中氢离子浓度为0.1mol/L×1%=0.001mol/L,依据溶液PH计算;
(2)弱电解质溶液中操作电离平衡,加水稀释促进电离,水溶液中操作离子积常数和电离平衡常数分析;
(3)CH3COOH与CH3COONa的混合溶液呈酸性,以CH3COOH的电离为主.Ⅰ、(1)①Fe(s)+CO2(g)⇌FeO(s)+CO(g)分析平衡常数随温度变化,升温平衡常数增大,平衡正向进行,正反应是吸热反应;
故答案为:吸热;
(2)①Fe(s)+CO2(g)⇌FeO(s)+CO(g) K1=
c(CO)
c(CO2)
②Fe(s)+H2O(g)⇌FeO(s)+H2(g) K2=
c(H2)
c(H2O)
③CO(g)+H2O(g)⇌CO2(g)+H2(g) K3=
c(H2)c(CO2)
c(CO)c(H2O)
K3=
c(H2)c(CO2)
c(CO)c(H2O)=
K2
K1;
故答案为:
K2
K1;
(3)①该反应是一个反应前后气体体积不变的且是正反应是放热的化学反应,t2时逆反应速率增大,且平衡时反应速率大于t2时反应速率,平衡向逆反应方向移动,改变的条件为增大生成物浓度或升高温度;
故答案为:升高温度或增大二氧化碳浓度或增大氢气浓度;
②t4时降压,逆反应速率减小,小于原平衡速率,但平衡不移动,t6时增大反应物的浓度,t6点逆反应速率不变,平衡向正反应方向移动,随着反应的进行,逆反应速率增大,大于原平衡速率,所以其图象为: ;
;
故答案为: ;
;
Ⅱ、(1)0.1mol/L 的CH3COOH溶液中有l%的CH3COOH分子发生电离,溶液中氢离子浓度为0.1mol/L×1%=0.001mol/L,则溶液PH=3;
故答案为:3;
(2)CH3COOH⇌CH3COO-+H+,溶液加蒸馏水稀释,在稀释过程中,电离程度增大,下列各项中增大的是;
A、电离平衡加入水稀释,c(H+)减小,故A错误;
B、电离平衡加入水稀释促进电离,溶液中氢离子物质的量增大,醋酸分子物质的量减小,所以
c(H+)
c(CH3COOH)比值增大,故B正确;
C、温度一定,加入水 促进电离,溶液中c(H+)•c(OH-)为常数不变,故C错误;
D、电离平衡加入水稀释促进电离,氢离子浓度减小,依据离子积常数氢氧根离子浓度增大,
c(OH−)
c(H+)比值增大,故D正确;
故选BD.
(3)CH3COOH与CH3COONa的混合溶液呈酸性,以CH3COOH的电离程度大于CH3COONa的水解程度所以c(CH3COO-)>c(Na+),溶液显酸性,c(H+)>c(OH-),因此c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故答案为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-).点评:
本题考点: 化学平衡常数的含义;化学反应速率与化学平衡图象的综合应用;弱电解质在水溶液中的电离平衡.
考点点评: 本题考查了弱电解质的电离和盐类的水解,及离子浓度大小比较,化学平衡常数的确定、外界条件对反应速率的影响等知识点,注意平衡常数的计算应用和推断分析,题目难度中等.1年前查看全部
- 宝鸡的天开始冷了,你那里呢?翻译成英语
 微凉洳荷1年前1
微凉洳荷1年前1 -
 绯雪千夜 共回答了17个问题
绯雪千夜 共回答了17个问题 |采纳率88.2%The weather is becoming colder in Baoji.Where are you?1年前查看全部
- 宝鸡当时公私合营工商业的情况,写出其中三家的名称 先到先采纳
 shenhuayumin1年前1
shenhuayumin1年前1 -
 明星在线 共回答了5个问题
明星在线 共回答了5个问题 |采纳率40%宝鸡杭叉公司 宝鸡水泵厂 宝鸡叉车三厂1年前查看全部
- (下0九3•宝鸡一模)阅读v文材料,完成下列各题.
(下0九3•宝鸡一模)阅读v文材料,完成下列各题.
材料一:v九是秘鲁年降水量分布v(单位:mm3),v下是秘鲁4口、矿产、河流分布示意v
材料二:秘鲁先后完成了马赫斯及首都利马等多条调水工程
(九)读v简单概述秘鲁年降水量分布规律.
(下)说出厄尔尼诺现象发生年份当地渔业减产还是增长,以及减产或增产原因是什么?.
(3)分析秘鲁修建这些调水工程的主要原因. mlbrs1年前1
mlbrs1年前1 -
 来来爱羊羊 共回答了17个问题
来来爱羊羊 共回答了17个问题 |采纳率82.4%解题思路:此题考查秘鲁的降水分布规律,渔业资源,调水的原因.
(1)此题考查秘鲁的降水分布规律.根据秘鲁的降水分布图分析分布特征.
(2)此题考查秘鲁的渔业资源.由于秘鲁寒流的影响,形成了著名的秘鲁渔场.厄尔尼诺现象发生,渔业资源减少,带来灾害.
(3)此题考查秘鲁调水的原因.由于水资源的分布不均,各地的需求量不同,导致资源的跨区域调配.(1)根据秘鲁的降水分布图分析分布特征.年降水量分布不均;从东向西年降水量从得十十十毫米以下递减到得十十毫米以下.
(得)由于秘鲁寒流的影响,形成了著名的秘鲁渔场.厄尔尼诺暖流为太平洋一种反常的自然现象,是在南美洲西海岸、南太平洋东部,自南向北流动着一股著名的秘鲁寒流,最先是被秘鲁渔民发现的.每年的11月至次年的六月正是南半球的夏季,南半球海域水温普遍升高,向东流动的赤道暖流得到加强.恰逢此时,全球的气压带和风带向南移动,东北信风越过赤道受到南半球自偏向力的作用,向左偏转成西北季风.西北季风不但消弱了秘鲁西海岸的离岸风--东南信风,使秘鲁寒流冷水下泛减弱甚至消失,而且吹拂着水温较高的赤道暖流南下,使秘鲁寒流的水温反常升高.这股悄然而至、不固定的洋流被称之为“厄尔尼诺暖流”.所以厄尔尼诺现象发生年份当6渔业减产.
(六)由于水资源的分布不均,各6的需求量不同,导致资源的跨区域调配.具体原因是:水资源分布不均,东多西少;西部人4密度大,水量消耗多;西部经济发达,工农业生产发展需水量大.
故答案为:
(1)年降水量分布不均;从东向西年降水量从得十十十毫米以下递减到得十十毫米以下.
(得)减产 秘鲁寒流减弱,从海底带来的营养盐减少,导致鱼类饵料减少所致.
(六)主要原因:水资源分布不均,东多西少;西部人4密度大,水量消耗多;西部经济发达,工农业生产发展需水量大.点评:
本题考点: 海洋环境问题以及保护措施;影响气候的主要因素;产业转移对区域地理环境的影响.
考点点评: 此题考查秘鲁的降水分布规律,渔业资源,调水的原因.此题是典型的区域地理,结合材料和图的信息分析问题,知识点较多,对学生的知识要求高,能力要求也高,难度较大.1年前查看全部
- 楼间距 采光 计算我们在宝鸡买了一套房子,是7层楼的.我们在2层.从东向西是4个单元我们在第4单元2层东户.坐北朝南.我
楼间距 采光 计算
我们在宝鸡买了一套房子,是7层楼的.我们在2层.从东向西是4个单元我们在第4单元2层东户.坐北朝南.我们2号楼的前面还是一栋7层楼.是1号楼.间距为21米吧.可是我们隔壁小区在我们的西边盖了个18层的高层和1号楼平齐.太阳应该很是挡我们吧.很是烦脑,买的时候不知道隔壁小区的规划.请好心的朋友告诉我.档到什么程度? 52kingnet1年前1
52kingnet1年前1 -
 寻找奶酪寻找幸福 共回答了17个问题
寻找奶酪寻找幸福 共回答了17个问题 |采纳率94.1%你先看看是那栋楼挡住你们的采光,这里有个一采光计算器,需要知道你们楼遮阳楼的高度 和你们楼的层高,直接输入就可以算出来.下面文章里有,自己输入后计算结果就出来了.不知道的话可以给我留言,告诉我遮阳楼的楼高和你们楼层高1年前查看全部
- (2014•宝鸡二模)已知实数x、y、z满足x+2y+3z=1,则x2+y2+z2的最小值为[1/14][1/14].
 hy61421年前1
hy61421年前1 -
 郓哥 共回答了10个问题
郓哥 共回答了10个问题 |采纳率80%解题思路:利用条件x+2y+3z=1,构造柯西不等式(x+2y+3z)2≤(x2+y2+z2+)(12+22+32)进行解题即可.由柯西不等式可知:(x+2y+3z)2≤(x2+y2+z2+)(12+22+32)
故x2+y2+z2≥[1/14],当且仅当[x/1=
y
2=
z
3],
即:x2+y2+z2的最小值为[1/14].
故答案为:[1/14]点评:
本题考点: 一般形式的柯西不等式.
考点点评: 本题主要考查了函数的值域,以及柯西不等式的应用,解题的关键是利用(x+2y+3z)2≤(x2+y2+z2+)(12+22+32)进行解题,属于中档题.1年前查看全部
- (2013•宝鸡二模)如图所示,螺旋形光滑轨道竖直放置,P、Q为对应的轨道最高点,一个小球以一定速度沿轨道切线方向进入轨
 (2013•宝鸡二模)如图所示,螺旋形光滑轨道竖直放置,P、Q为对应的轨道最高点,一个小球以一定速度沿轨道切线方向进入轨道,且能过轨道最高点P,则下列说法中正确的是( )
(2013•宝鸡二模)如图所示,螺旋形光滑轨道竖直放置,P、Q为对应的轨道最高点,一个小球以一定速度沿轨道切线方向进入轨道,且能过轨道最高点P,则下列说法中正确的是( )
A.轨道对小球不做功,小球通过P点的角速度小于通过Q点的角速度
B.轨道对小球做正功,小球通过P点的线速度大于通过Q点的线速度
C.小球通过P点时的向心加速度大于通过Q点时的向心加速度
D.小球通过P点时对轨道的压力大于通过Q点时对轨道的压力 囡雨1年前1
囡雨1年前1 -
 gaocaho79 共回答了14个问题
gaocaho79 共回答了14个问题 |采纳率92.9%解题思路:小球沿竖直放置的螺旋形光滑轨道运动,轨迹半径越来越小,做近心运动.由于支持力始终与速度方向垂直,所以支持力不做功,仅有重力做功下,小球的机械能守恒.再由向心力公式结合牛顿第二定律,可以确定小球的线速度、角速度、向心加速度及对轨道的压力大小.A、由于支持力始终与速度方向垂直,所以支持力不做功即轨道对小球不做功,仅有重力做功,小球机械能守恒.则P点的速度小于Q点速度,且P点的半径大于Q点的半径.所以小球通过P点的角速度小于通过Q点的.故A正确;
B、由于支持力始终与速度方向垂直,所以支持力不做功即轨道对小球不做功,仅有重力做功,小球机械能守恒.则P点的线速度小于Q点线速度.故B错误;
C、由于支持力始终与速度方向垂直,所以支持力不做功即轨道对小球不做功,仅有重力做功,小球机械能守恒.则P点的速度小于Q点速度,且P点的半径大于Q点的半径.所以小球在P点的向心加速度小于Q点的,故C错误;
D、由于支持力始终与速度方向垂直,所以支持力不做功即轨道对小球不做功,仅有重力做功,小球机械能守恒.则P点的速度小于Q点速度,且P点的半径大于Q点的半径.所以小球在P点的向心加速度小于Q点的,则小球在P点的向心力小于Q点的,而向心力是由重力与轨道对它的支持力提供,因此小球在P点的支持力小于Q点的,即小球对轨道的压力P点小于Q点的.故D错误;
故选:A点评:
本题考点: 向心力;牛顿第二定律;线速度、角速度和周期、转速.
考点点评: 小球在竖直放置的螺旋形轨道运动,速度时大时小,原因是动能与重力势能在相互转化.当在水平放置的光滑的螺旋形轨道运动时,由于支持力始终不做功,因此速度大小不变,随着轨迹半径越来越小,导致小球的角速度越来越大,转动的越来越快.1年前查看全部
- (2014•宝鸡三模)一列简谐横波在t=0时刻的波形如图所示,质点P此时刻沿-y运动,经过0.1s第一次到达平衡位置,波
 (2014•宝鸡三模)一列简谐横波在t=0时刻的波形如图所示,质点P此时刻沿-y运动,经过0.1s第一次到达平衡位置,波速为5m/s,那么
(2014•宝鸡三模)一列简谐横波在t=0时刻的波形如图所示,质点P此时刻沿-y运动,经过0.1s第一次到达平衡位置,波速为5m/s,那么
①该波沿______(选填“+x”或“-x”)方向传播;
②图中Q点(坐标为x=7.5m的点)的振动方程y=5cos[5π/3]t5cos[5π/3]tcm;
③P点的横坐标为x=______m. 大海有多大呢1年前1
大海有多大呢1年前1 -
 天使穿背心 共回答了22个问题
天使穿背心 共回答了22个问题 |采纳率90.9%①质点P此时刻沿-y运动,振动比左侧邻近的波峰振动早,所以该波沿-x方向传播.
②由图知,波长λ=6m,则周期为T=[λ/v]=[6/5]=1.2s,则Q点的振动方程为y=Acos[2π/T]t=5cos[5π/3]t(cm)
③t=0.1s内波传播的距离为x=vt=5×0.1m=0.5m,根据波形的平移法可知,当图示时刻x=3m处质点的振动状态传到P点,P点第一次到达平衡位置,所以P点的横坐标为x=3m-.5m=2.5m.
故答案为:
①-x.②5cos[5π/3]t③2.51年前查看全部
- (2013•宝鸡二模)如图所示,质量为2m的物块A穿在光滑水平杆上,下面用长为L的轻绳悬吊一个质量为m的小球B,A、B均
 (2013•宝鸡二模)如图所示,质量为2m的物块A穿在光滑水平杆上,下面用长为L的轻绳悬吊一个质量为m的小球B,A、B均静止不动.质量为m的小球C在光滑水平桌面上以速度v0向右运动,小球C刚滑出右边缘时与小球B发生正碰,碰后两球粘在一起共同运动.试求:
(2013•宝鸡二模)如图所示,质量为2m的物块A穿在光滑水平杆上,下面用长为L的轻绳悬吊一个质量为m的小球B,A、B均静止不动.质量为m的小球C在光滑水平桌面上以速度v0向右运动,小球C刚滑出右边缘时与小球B发生正碰,碰后两球粘在一起共同运动.试求:
①B、C小球碰撞过程中损失的机械能;
②B、C小球碰撞后物块A运动的最大速度. 雅克力1年前1
雅克力1年前1 -
 嶷辚比子 共回答了16个问题
嶷辚比子 共回答了16个问题 |采纳率93.8%解题思路:(1)根据动量守恒求BC碰后的共同速度,根据能量守恒求损失的机械能;
(2)当BC碰撞后粘在一起上升到最高点,再从最高点运动到物块A的正下方时A的速度最大.(1)设BC碰撞后一起共同运动的速度为v1,设向右为正方向,则对BC小球组成的系统,由动量守恒得:
mv0=2mv1…①
E=[1/2]mv02-[1/2]×2mv12…②
联立的:E=[1/4]mv02…③
(2)由题意分析可知,当BC碰撞后粘在一起上升到最高点,再从最高点运动到物块A的正下方时A的速度最大,设此时BC向左运动的速度大小为v2,物块A向右运动的速度大小为v3,取水平向右为正方向,则对ABC组成的系统,由水平方向动量守恒得:
2mv1=-2mv2+2mv3…④
由机械能守恒得:[1/2]×2mv12+[1/2]×2mv32…⑤
联立①④⑤得:v3=[1/2]v0
答:①B、C小球碰撞过程中损失的机械能为[1/4]mv02;
②B、C小球碰撞后物块A运动的最大速度[1/2]v0.点评:
本题考点: 动量守恒定律;机械能守恒定律.
考点点评: 本题综合考查了动量守恒定律以及能量守恒定律,碰后,系统水平方向动量守恒,但总动量并不守恒.1年前查看全部
- (2014•宝鸡三模)如图所示,在磁感应强度为B的匀强磁场中,有一电阻可忽略不计的矩形线圈可绕线圈平面内垂直于磁感线的轴
 (2014•宝鸡三模)如图所示,在磁感应强度为B的匀强磁场中,有一电阻可忽略不计的矩形线圈可绕线圈平面内垂直于磁感线的轴OO′以角速度ω匀速转动,由线圈引出的两根导线分别与两个跟线圈一起绕OO′转动的金属圆环相连接,通过电刷将线圈中所产生的交变电流加在理想变压器的原线圈上.下列哪种操作可使交流电流表的示数变大( )
(2014•宝鸡三模)如图所示,在磁感应强度为B的匀强磁场中,有一电阻可忽略不计的矩形线圈可绕线圈平面内垂直于磁感线的轴OO′以角速度ω匀速转动,由线圈引出的两根导线分别与两个跟线圈一起绕OO′转动的金属圆环相连接,通过电刷将线圈中所产生的交变电流加在理想变压器的原线圈上.下列哪种操作可使交流电流表的示数变大( )
A.减小磁感应强度B
B.向上移动滑动头P
C.减小变阻器R的阻值
D.增大矩形线圈OO′轴转动的角速度ω 风名扬1年前1
风名扬1年前1 -
 都市胖胖 共回答了25个问题
都市胖胖 共回答了25个问题 |采纳率72%解题思路:变流电的动态分析和闭合电路中的动态分析类似,先分析电路结论,明确电阻的变化,再根据电压不变分析电流的变化及电功率的变化.A、减小磁感应强度B,原线圈电压减小,副线圈减小,交流电流表的示数减小,故A错误;
B、向上移动滑动头P,原线圈匝数增加,副线圈电压减小,交流电流表的示数减小,故B错误;
C、减小变阻器R的阻值,交流电流表的示数增大,故C正确;
D、增大矩形线圈OO′轴转动的角速度ω,原线圈电压增大,副线圈增大,交流电流表的示数增大,故D正确;
故选:CD.点评:
本题考点: 变压器的构造和原理;交流发电机及其产生正弦式电流的原理.
考点点评: 电路的动态变化的分析,总的原则就是由部分电路的变化确定总电路的变化的情况,再确定其他的电路的变化的情况,即先部分后整体再部分的方法.1年前查看全部
- (2014•宝鸡三模)已知,a=([1/2])x,b=x2,c=lgx,当x>2时,a,b,c的大小关系为( )
(2014•宝鸡三模)已知,a=([1/2])x,b=x2,c=lgx,当x>2时,a,b,c的大小关系为( )
A.a<b<c
B.a<c<b
C.c<b<a
D.c<a<b 铁竹1年前1
铁竹1年前1 -
 adbadf 共回答了18个问题
adbadf 共回答了18个问题 |采纳率94.4%∵x>2,∴0<a=([1/2])x<[1/4],
b=x2>4,
[1/4]=lg10
1
4<c=lgx<x2=b,
∴a<c<b.
故选:B.1年前查看全部
- (2010•宝鸡一模)若NA表示阿伏加德罗常数,下列说法正确的是( )
(2010•宝鸡一模)若NA表示阿伏加德罗常数,下列说法正确的是( )
A.标准状况下,120g二氧化硅固体中,含有2NA个二氧化硅分子
B.标准状况下,18g重水含有10NA个中子
C.室温下,在28g乙烯和环丙烷(C3H6)的混合物中,含有碳原子数是2NA
D.标准状况下,22.4L的苯中,含有碳碳单键的数目是3NA 小小鬼精灵1年前1
小小鬼精灵1年前1 -
 关愚 共回答了14个问题
关愚 共回答了14个问题 |采纳率85.7%解题思路:A、根据二氧化硅属于原子晶体,不存在二氧化硅分子判断;
B、根据重水的物质的量计算出含有的中子数;
C、根据乙烯和环丙烷的最简式计算出含有的碳原子数;
D、根据标准状况下苯不是气体无法计算其物质的量判断.A、120g二氧化硅的物质的量为2mol,由于二氧化硅属于原子晶体,不存在二氧化硅分子,故A错误;
B、18g重水的物质的量为0.9mol,含有9mol中子,含有9NA个中子,故B错误;
C、乙烯和环丙烷的最简式为CH2,28g混合物中含有2mol最简式,含有2mol碳原子,含有碳原子数是2NA,故C正确;
D、标准状况下,苯不是气体,无法计算22.4L苯的物质的量,故D错误;
故选C.点评:
本题考点: 阿伏加德罗常数.
考点点评: 本题考查了阿伏伽德罗常数,注意标准状况下苯不是气体,二氧化硅属于原子晶体,不存在二氧化硅分子,本题难度不大.1年前查看全部
- (2011•宝鸡模拟)如图所示,MN是负点电荷产生的电场中的一条电场线,一个电荷量为q的带正电的粒子从a点以某一速度飞入
 (2011•宝鸡模拟)如图所示,MN是负点电荷产生的电场中的一条电场线,一个电荷量为q的带正电的粒子从a点以某一速度飞入电场后做曲线运动,运动轨迹如图中虚线所示,b是虚线上一点,若不计粒子的重力,则( )
(2011•宝鸡模拟)如图所示,MN是负点电荷产生的电场中的一条电场线,一个电荷量为q的带正电的粒子从a点以某一速度飞入电场后做曲线运动,运动轨迹如图中虚线所示,b是虚线上一点,若不计粒子的重力,则( )
A.a点场强Ea大于b点场强Eb
B.a点电势Ua低于b点电势Ub
C.粒子在a点动能Eka小于在b点动能Ekb
D.粒子在a点电势能Epa小于在b点电势能Epa a33939981年前1
a33939981年前1 -
 太郎春风 共回答了17个问题
太郎春风 共回答了17个问题 |采纳率94.1%解题思路:由轨迹可判定正电荷所受电场力方向为从N到M,则知负电荷在MN线上左侧,即可根据距离大小分析a、b两点场强大小、电势高低.电场力做正功,粒子的动能增大,而电势能减小.A、由图看出,带正电的粒子轨迹向左弯曲,可知该电荷所受的电场力方向从N到M,说明负电荷在MN线上左侧,由于a离负电荷的距离大于b的距离,则a点场强Ea小于b点场强Eb.故A错误.
B、由上可知,电场线方向从N指向M,根据顺着电场线电势降低,则知a点电势Ua高于b点电势Ub.故B错误.
C、D电场力方向从N到M,与粒子速度方向的夹角为锐角,电场力做正功,则动能增大,电势能减小,则有粒子在a点动能Eka小于在b点动能Ekb,在a点电势能Epa大于在b点电势能Epa.故C正确,D错误.
故选C点评:
本题考点: 电势能;电场强度;电势.
考点点评: 本题的解题关键是根据粒子的轨迹判定电场线的方向,进一步分析电场力做功情况、判断电势能和动能的大小.1年前查看全部
- (2010•宝鸡二模)下列叙述正确的是( )
(2010•宝鸡二模)下列叙述正确的是( )
A.配制50g质量分数为5%KCl溶液:将45mL水加入到盛有5g KCl的烧杯中,搅拌溶解
B.鉴定SO42-向溶液中加入盐酸酸化的氯化钡溶液
C.量取液体:用50mL酸式滴定管可准确量取25.00mL 的KMnO4溶液
D.除杂质:用过量的氨水除去AlCl3溶液中的少量的FeCl3 oo老兵1年前1
oo老兵1年前1 -
 alec1012 共回答了18个问题
alec1012 共回答了18个问题 |采纳率94.4%解题思路:A.溶质质量=溶液质量×质量分数;
B.和盐酸酸化的氯化钡反应生成的白色沉淀可能是氯化银或者是硫酸钡沉淀;
C.滴定管精确到0.01mL;
D.AlCl3、FeCl3都能与氨水反应.A.溶质质量=溶液质量×质量分数,50g×5%=2.5g,应称取2.5gKCl,故A错误;
B.向某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成,溶液中含有SO42-或银离子中的至少一种,故B错误;
C.滴定管精确到0.01mL,可准确量取25.00mL 的KMnO4溶液,故C正确;
D.因AlCl3与氨水反应生成氢氧化铝沉淀和氯化铵,FeCl3与氨水反应生成氢氧化铁沉淀和氯化铵,除去了杂质,也除去了原物质,引入了新杂质氯化铵和氨水,不符合除杂的原则,故D错误.
故选C.点评:
本题考点: 化学实验方案的评价.
考点点评: 本题考查实验评价,涉及溶液配制、离子检验、除杂等,注意除杂不能引入新的杂质,题目难度不大.1年前查看全部
- (2014•宝鸡一模)将6.85g Fe和Al的混合物溶于200mL浓度为c mol/L的HNO3溶
(2014•宝鸡一模)将6.85g Fe和Al的混合物溶于200mL浓度为c mol/L的HNO3溶液中,得到标准状况下的NO、N2O混合气体共3.36L,测得反应后溶液的pH为0,再向所得溶液中加入过量NaOH溶液充分反应后生成沉淀质量为5.35g.若不考虑反应前后溶液体积变化,则下列有关判断正确的是( )
A.Fe与Al 的物质的量之比为1:1
B.混合气体中NO为0.03mol,N2O为0.12mol
C.原HNO3溶液的浓度C=4.9mol/L
D.反应中被还原的HNO3为0.15mol fengyeiwu1年前1
fengyeiwu1年前1 -
 zlysky808 共回答了20个问题
zlysky808 共回答了20个问题 |采纳率95%解题思路:将Fe和Al的混合物溶于HNO3溶液中,得到NO、N2O混合气体,测得反应后溶液的pH为0,说明硝酸有剩余,故生成Al(NO3)3、Fe(NO3)3,再向所得溶液中加入过量NaOH溶液,铝离子完全转化为偏铝酸钠,得到沉淀5.35g为Fe(OH)3,其物质的量=[5.35g/107g/mol]=0.05mol,
A.根据原子守恒计算n(Fe),再根据m=nM计算m(Fe),进而计算m(Al),根据n=[m/M]计算n(Al),据此解答;
B.令混合气体中NO、N2O的物质的量分别为xmol、ymol,根据电子转移守恒及二者体积列方程解答;
C.根据N元素守恒n原(HNO3)=3n[Al(NO3)3]+3n[Fe(NO3)3]+n(NO)+2n(N2O)+n剩余(HNO3),进而计算浓度;
D.被还原的HNO3生成NO、N2O,根据氮元素守恒可知n被还原(HNO3)=n(NO)+2n(N2O).将Fe和Al的混合物溶于HNO3溶液中,得到NO、N2O混合气体,测得反应后溶液的pH为0,说明硝酸有剩余,故生成Al(NO3)3、Fe(NO3)3,再向所得溶液中加入过量NaOH溶液,铝离子完全转化为偏铝酸钠,得到沉淀5.35g为Fe(OH)3,其物质的量=[5.35g/107g/mol]=0.05mol,
A.根据原子守恒n(Fe)=0.05mol,m(Fe)=0.05mol×56g/mol=2.8g,故m(Al)=6.85g-2.8g=4.05g,n(Al)=[4.05g/27g/mol]=0.15mol,故Fe与Al 的物质的量之比=0.05mol:0.15mol=1:3,故A错误;
B.令混合气体中NO、N2O的物质的量分别为xmol、ymol,根据电子转移守恒及二者体积,可得:
x+y=
3.36
22.4
3x+8y=(0.05+0.15)×3,解得x=0.12、y=0.03,故B错误;
C.反应后溶液的pH为0,则n剩余(HNO3)=1mol/L×0.2L=0.2mol,根据N元素守恒n原(HNO3)=3n[Al(NO3)3]+3n[Fe(NO3)3]+n(NO)+2n(N2O)+n剩余(HNO3)=3×0.15mol+3×0.05mol+0.12mol+2×0.03mol+0.2mol=0.98mol,原HNO3溶液的浓度=[0.98mol/0.2L]=4.9mol/L,故C正确;
D.被还原的HNO3生成NO、N2O,根据氮元素守恒可知n被还原(HNO3)=n(NO)+2n(N2O)=0.12mol+2×0.03mol=0.18mol,故D错误,
故选C.点评:
本题考点: 有关混合物反应的计算.
考点点评: 本题考查混合物计算,判断反应过程是解题的关键,注意守恒思想的应用,侧重解题方法与思维能力考查,难度中等.1年前查看全部
- (2013•宝鸡三模)【化学-选修2化学与技术】
(2013•宝鸡三模)【化学-选修2化学与技术】
下图是工业上生产碳酸锂的部分工艺流程,请根据流程图及已知信息回答问题.
已知:①锂辉石主要万分为Li2O•Al2O3•4SiO2,含有少量Ca、Mg元素.
②Li2O•Al2O3•4SiO2+H2SO4(浓)
Li2SO4+Al2O3•4SiO2•H2O↓250−300℃ .
③几种物质不同温度下的溶解度.
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质.写出图中①、②、③表示的各物质,步骤II中反应的离子方程式是______.T/℃ 20 40 60 80 S(Li2CO3)/g 1.33 1.17 1.01 0.85 S(Li2SO4)/g 34.2 32.8 31.9 30.7 
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3,写出生成滤渣2反应的离子方程式:______.
(3)向滤液2中加入饱和Na2CO3,溶液,过滤后,用“热水洗涤”的原因是______.
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下.
①将粗产品Li2CO3溶于盐酸作用解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解.阳极的电极反应式是______.
②电解后向产品LiOH溶液中加入过量NH4HCO3,溶液生成Li2CO3反应的化学方程式是______. jinlin8151年前1
jinlin8151年前1 -
 pctogvvb 共回答了20个问题
pctogvvb 共回答了20个问题 |采纳率95%解题思路:分析流程锂辉石主要成分为Li2O•Al2O3•4SiO2,含有少量Ca、Mg元素,研磨在加热条件下用浓硫酸酸浸后过滤得到Li2SO4,硫酸镁和硫酸钙,滤渣Ⅰ为Al2O3•4SiO2•H2O↓,滤液加入为石灰乳是氢氧化钙,提供氢氧根离子和钙离子,加入碳酸钠沉淀钙离子,更完全的沉淀镁离子和碳酸根离子,过滤得到滤液主要是Li2SO4,加入饱和碳酸钠沉淀锂离子为碳酸锂,滤渣2主要成分有Mg(OH)2和CaCO3;
(1)从滤渣1中分离出Al2O3的流程分析,加入酸溶解Al2O3•4SiO2•H2O,得到硫酸铝溶液和二氧化硅,过滤得到溶液硫酸铝,加入氨水或适量氢氧化钠溶液得到氢氧化铝沉淀,灼烧得到氧化铝;步骤Ⅱ中铝离子与氨水反应生成氢氧化铝沉淀;
(2)滤渣2的主要成分有Mg(OH)2和CaCO3,石灰乳是氢氧化钙,提供氢氧根离子和钙离子,更完全的沉淀镁离子和碳酸根离子,碳酸钠提供碳酸根离子用来沉淀过量的钙离子,;
(3)依据图表分析可知碳酸锂溶解度随 温度升高减小;
(4)①Li2CO3溶于盐酸作电解槽的阳极液,阳极液中离子失电子,发生氧化反应,所以阳极反应为2C1--2e-=Cl2↑,阴极反应为2H++2e-=H2↑.离子选择透过膜只允许阳离子通过,电解过程中,Li+向阴极移动,而阴极电解后富余大量的OH-,阳极的Li+通过离子选择透过膜到阴极,这样阴极就得到比较纯净的LiOH.
②电解后向LiOH溶液中加入过量NH4HCO3溶液,氢氧化锂与碳酸氢铵反应生成碳酸锂.(1)从滤渣1中分离出Al2O3的流程分析,加入酸溶解Al2O3•4SiO2•H2O,得到铝盐溶液和固体二氧化硅,过滤得到溶液硫酸铝,加入氨水或适量氢氧化钠溶液得到氢氧化铝沉淀,灼烧得到氧化铝;步骤Ⅱ中铝离子与氨水反应生成氢氧化铝沉淀,反应离子方程式为:Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
故答案为:铝盐,氨水,Al(OH)3,Al3++3NH3•H2O=Al(OH)3↓+3NH4+;
(2)石灰乳是氢氧化钙,提供氢氧根离子和钙离子,更完全的沉淀镁离子和碳酸根离子,增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出,碳酸钠能沉淀过量的钙离子,反应的离子方程式为;Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓
故答案为:Mg2++2OH-=Mg(OH)2↓,Ca2++CO32-=CaCO3↓;
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”,图表中碳酸锂溶解度随温度升高减小,减少沉淀的损失,
故答案为:Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失;
(4))①Li2CO3溶于盐酸作电解槽的阳极液,阳极液中氯离子失电子,发生氧化反应,所以阳极反应为2C1--2e-=Cl2↑,
故答案为:2C1--2e-=Cl2↑;
②电解后向LiOH溶液中加入过量NH4HCO3溶液,氢氧化锂与碳酸氢铵反应生成碳酸锂的方程式为:2LiOH+2NH4HCO3=Li2CO3+(NH4)2CO3+2H2O,
故答案为:2LiOH+2NH4HCO3=Li2CO3+(NH4)2CO3+2H2O;点评:
本题考点: 制备实验方案的设计;电解原理;常见金属元素的单质及其化合物的综合应用.
考点点评: 本题考查了物质生产流程的分析判断,流程分析,物质性质的应用是解题关键,主要是铝及其化合物性质的应用,氧化铝的提取方法,题目难度中等.1年前查看全部
- (2014•宝鸡三模)如图所示,M、N为固定的两个等量同种正电电荷,在其连线的中垂线上的P点由静止释放一个负点电荷q,它
 (2014•宝鸡三模)如图所示,M、N为固定的两个等量同种正电电荷,在其连线的中垂线上的P点由静止释放一个负点电荷q,它只在电场力作用下运动到最低点过程中,下列说法中错误的是( )
(2014•宝鸡三模)如图所示,M、N为固定的两个等量同种正电电荷,在其连线的中垂线上的P点由静止释放一个负点电荷q,它只在电场力作用下运动到最低点过程中,下列说法中错误的是( )
A.负点电荷q的机械能先增大后减小
B.负点电荷q的动能先增大后减小
C.负点电荷q的电势能先减小后增大
D.负点电荷q的动能最大时其电势能为零 飘香的玫瑰1年前1
飘香的玫瑰1年前1 -
 rodman10 共回答了15个问题
rodman10 共回答了15个问题 |采纳率100%解题思路:本题要根据等量同种点电荷电场线的分布情况,抓住对称性,分析试探电荷的受力情况,分析其运动情况,根据电场力做功情况,分析其电势能的变化情况.根据点电荷电场强度的叠加法则,可知,同种正电荷的中垂线上,由O点向两边,电场强度方向向两边延伸,且大小先增大后减小,
由静止释放一个负点电荷q,它只在电场力作用下,先向下加速,后向下减速运动;
A、负点电荷q受到电场力先做正功,后做负功,则其的机械能先增大后减小,故A正确.
B、负点电荷q,因合力先做正功,后做负功,则其动能先增大后减小,故B正确.
C、负点电荷q受到电场力先做正功,后做负功,则其电势能先减小,后增大,故C正确.
D、负点电荷q的动能最大时,则速度最大,其电势能不为零,故D错误.
本题选择错误的,故选:D.点评:
本题考点: 电场的叠加;电势能.
考点点评: 掌握一些典型的电场线分布特点,知道电场线的疏密表示场强大小,会用电场力做功与电势能的变化关系分析势能和动能的变化.1年前查看全部
- (2010•宝鸡一模)莽草酸是合成治疗禽流感和甲型H7N9流感药物--达菲的重要原料.已知莽草酸的结构简式如图所示.下列
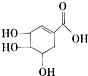 (2010•宝鸡一模)莽草酸是合成治疗禽流感和甲型H7N9流感药物--达菲的重要原料.已知莽草酸的结构简式如图所示.下列关于这种有机化合物的说法正确的是( )
(2010•宝鸡一模)莽草酸是合成治疗禽流感和甲型H7N9流感药物--达菲的重要原料.已知莽草酸的结构简式如图所示.下列关于这种有机化合物的说法正确的是( )
A.莽草酸的分子式为C7H6O5
B.莽草酸能使溴的四氯化碳溶液褪色
C.莽草酸遇FeCl3溶液显紫色
D.1 mol莽草酸与足量氢氧化钠反应,最多消耗氢氧化钠4 mol ycliuyang1年前0
ycliuyang1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•宝鸡二模)如图所示为电子束加速偏转装置,电极K产生的热电子(初速度为零)经电场加速后,进入两平行金属板间,如
 (2013•宝鸡二模)如图所示为电子束加速偏转装置,电极K产生的热电子(初速度为零)经电场加速后,进入两平行金属板间,如果两极间加一偏转电压,则电子束将偏转.电子离开偏转电场时每单位偏转电压引起的电子偏转距离叫偏转灵敏度,为了提高偏转灵敏度,必须( )
(2013•宝鸡二模)如图所示为电子束加速偏转装置,电极K产生的热电子(初速度为零)经电场加速后,进入两平行金属板间,如果两极间加一偏转电压,则电子束将偏转.电子离开偏转电场时每单位偏转电压引起的电子偏转距离叫偏转灵敏度,为了提高偏转灵敏度,必须( )
A.把偏转板长度l增长一些
B.把电子换成带电量大的粒子
C.使偏转极板间的距离d减小一些
D.把加速电场的电压提高一些 hackqq11w1年前1
hackqq11w1年前1 -
 白水监心 共回答了18个问题
白水监心 共回答了18个问题 |采纳率88.9%解题思路:电子先经加速电场加速,再进入偏转,根据动能定理和牛顿运动定律、运动学公式推导出y,再求出
的表达式,由表达式分析提高灵敏度的方式.y U2 设加速电压为U1,偏转电压为U2.
经加速电场后的速度为v,则 eU1=[1/2m
v20]
电子进入偏转电场后做类平抛运动,运动的时间:t=
L
v0
其偏转的位移为,y=
1
2at2
a=
qE2
m=
qU2
dm
联立上三式得y=
U2L2
4dU1
所以示波管的灵敏度
y
U2=
L2
4dU1
可见,要提高示波管灵敏度,必须把偏转极板l做得长一些,或把偏转极板间距离d做得小些,或加速电场的两极板间的电压降低一点.故AC正确,BD错误.
故选:AC点评:
本题考点: 带电粒子在匀强电场中的运动.
考点点评: 本题是信息的给予题,根据所给的信息,得出示波管的灵敏度的表达式即可解决本题.1年前查看全部
- (2010•宝鸡模拟)如图是某几何体的三视图,其中三个视图的轮廓都是边长为1的正方形,则该几何体的体积为[5/6][5/
(2010•宝鸡模拟)如图是某几何体的三视图,其中三个视图的轮廓都是边长为1的正方形,则该几何体的体积为[5/6][5/6].

 wxwaijyl1年前1
wxwaijyl1年前1 -
 cfb-zpp 共回答了16个问题
cfb-zpp 共回答了16个问题 |采纳率87.5%1年前查看全部
- J和G的准确读音?为什么宝鸡这边人把J和G全读成 只A
 rgdm1年前1
rgdm1年前1 -
 醒没醒 共回答了19个问题
醒没醒 共回答了19个问题 |采纳率94.7%比较正确的读法是:G读(ji)而J读(zh A)不同的地方有不同读音,这个比较多数人认同的1年前查看全部
- (2014•宝鸡三模)如图所示,以直角三角形ABC的直角边AC为直径作⊙O,交斜边AB于点D,过点D作⊙O的切线,交BC
 (2014•宝鸡三模)如图所示,以直角三角形ABC的直角边AC为直径作⊙O,交斜边AB于点D,过点D作⊙O的切线,交BC边于点E.则[BE/BC]=[1/2][1/2].
(2014•宝鸡三模)如图所示,以直角三角形ABC的直角边AC为直径作⊙O,交斜边AB于点D,过点D作⊙O的切线,交BC边于点E.则[BE/BC]=[1/2][1/2]. jeeki1年前1
jeeki1年前1 -
 gracekoo2006 共回答了18个问题
gracekoo2006 共回答了18个问题 |采纳率83.3%解题思路:连接CD,由AC是⊙O的直径,可得CD⊥AB.可证BC是⊙O的切线,及DE是⊙O的切线,由切线长定理可得ED=EC,在Rt△BCD可证明点E是斜边的中点,即可得出结论.连接CD,∵AC是⊙O的直径,∴CD⊥AB.
∵BC经过半径OC的端点C且BC⊥AC,∴BC是⊙O的切线,
而DE是⊙O的切线,∴EC=ED.
∴∠ECD=∠CDE,∴∠B=∠BDE,∴DE=BE.
∴BE=CE=[1/2]BC.
∴[BE/BC=
1
2].
故答案为[1/2].点评:
本题考点: 与圆有关的比例线段.
考点点评: 熟练掌握圆的性质、切线长定理、直角三角形的边角关系数据他的关键.1年前查看全部
- (2014•宝鸡三模)如图所示,将很大的矩形透明介质1与透明介质2水平叠放起来,介质1与介质2的厚度分别为h1=3m,h
 (2014•宝鸡三模)如图所示,将很大的矩形透明介质1与透明介质2水平叠放起来,介质1与介质2的厚度分别为h1=3m,h2=2m,在这两种介质的界面处有一个点光源S,测得光在介质1与介质2中传播的速度分别为v1=2.4×108m/s,v2=1.8×108m/s.我们知道,介质2的折射率与介质1的折射率之比等于介质2相对于介质1的相对折射率(用n21表示).
(2014•宝鸡三模)如图所示,将很大的矩形透明介质1与透明介质2水平叠放起来,介质1与介质2的厚度分别为h1=3m,h2=2m,在这两种介质的界面处有一个点光源S,测得光在介质1与介质2中传播的速度分别为v1=2.4×108m/s,v2=1.8×108m/s.我们知道,介质2的折射率与介质1的折射率之比等于介质2相对于介质1的相对折射率(用n21表示).
①请根据题目所提供的数据求相对折射率n21的值;
②经观察发现:在介质1的上表面,以O1为圆心,半径为r1的圆周内有光射出;在介质2的下表面,以O2为圆心,半径r2的圆周内有光射出.求r1与r2的比值(sin37°=0.6,cos37°=0.8). skraeling1年前0
skraeling1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•天水)如图所示,在天水至宝鸡(天宝)高速公路建设中需要确定某条隧道AB的长度,已知在离地面2700米高度C处
 (2013•天水)如图所示,在天水至宝鸡(天宝)高速公路建设中需要确定某条隧道AB的长度,已知在离地面2700米高度C处的飞机上,测量人员测得正前方AB两点处的俯角分别是60°和30°,求隧道AB的长.(结果保留根号)
(2013•天水)如图所示,在天水至宝鸡(天宝)高速公路建设中需要确定某条隧道AB的长度,已知在离地面2700米高度C处的飞机上,测量人员测得正前方AB两点处的俯角分别是60°和30°,求隧道AB的长.(结果保留根号)  kenk00001年前1
kenk00001年前1 -
 coffeybaby 共回答了23个问题
coffeybaby 共回答了23个问题 |采纳率95.7%解题思路:易得∠CAO=60°,∠CBO=30°,利用相应的正切值可得AO,BO的长,相减即可得到AB的长.由题意得∠CAO=60°,∠CBO=30°,
∵OA=2700×tan30°=2700×
3
3=900
3m,OB=2700×tan60°=2700
3m,
∴AB=2700
3-900
3=1800
3(m).
答:隧道AB的长为1800
3m.点评:
本题考点: 解直角三角形的应用-仰角俯角问题.
考点点评: 考查解直角三角形的应用;利用三角函数值得到与所求线段相关线段的长度是解决本题的关键.1年前查看全部
- (2013•宝鸡三模)图表示人体某一神经调节的反射弧模式图,M为效应器.下列分析判断正确的是( )
(2013•宝鸡三模)图表示人体某一神经调节的反射弧模式图,M为效应器.下列分析判断正确的是( )

A.结构③的存在使相邻两神经元之间的兴奋单向传递
B.若a点神经纤维严重受损,感受器接收到刺激后,人体不会产生感觉也不会做出相应的效应活动
C.刺激Ⅲ处,①处兴奋时膜外电流的方向与兴奋的传导方向相同
D.刺激②处,在I和Ⅲ处均能检测到电位变化 667230891年前1
667230891年前1 -
 烟火荼糜 共回答了12个问题
烟火荼糜 共回答了12个问题 |采纳率91.7%解题思路:分析可知:①是传入神经纤维②是传出神经纤维,③是突触,因为神经递质只存在于突触小泡内,只能由突触前膜释放作用于突触后面,所以兴奋在突触单向传递.A、结构③是突触,兴奋只能由突触前膜传向突触后膜,而不能倒过来,所以结构③的存在使相邻两神经元之间的兴奋单向传递,A正确;
B、感觉的形成在大脑皮层只要是反射的神经中枢没受损,就能将兴奋传至大脑皮层,引起感觉,但是传出神经纤维受损,效应器无反应,B错误;
C、兴奋在神经纤维上的传导方向和膜内的电流方向相同,和膜外的电流方向相反,刺激Ⅲ处,①处兴奋时膜外电流的方向与兴奋的传导方向相反,C错误;
D、刺激②处,兴奋只能传至Ⅰ而不能传至Ⅲ,在I处能检测到电位变化,Ⅲ处不能检测到电位变化,D错误.
故选:A.点评:
本题考点: 反射弧各部分组成及功能;神经冲动的产生和传导.
考点点评: 本题考查了反射弧各部分的结构和功能,明确兴奋传导的方向及感觉的产生部位是解题的关键.1年前查看全部
- (2010•宝鸡模拟)若复数[2i−1/i]的实部与虚部分别为a,b,则ab等于( )
(2010•宝鸡模拟)若复数[2i−1/i]的实部与虚部分别为a,b,则ab等于( )
A.2i
B.2
C.-2
D.-2i 林队_uu1年前0
林队_uu1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2009•宝鸡三模)已知X、Y、Z、W都是短周期的非金属元素,其原子序数依次增大.W原子的质子数是Y原子质子数的两倍,
(2009•宝鸡三模)已知x、y、z、w都是短周期的非金属元素,其原子序数依次增大.w原子的质子数是y原子质子数的两倍,x原子与w原子的最外层电子数之和是y和z原子的质子数之和的[1/3].y的氢化物分子中有三个共价键.
(1)x、z的元素名称分别是______、______,w元素原子结构示意图为______.
(2)y的氢化物分子的空间构型为______,属于______分子(填“极性”或“非极性”)
(3)由以上任意三种元素组成的化合物中,其水溶液显酸性的有(填写化学式)______、______.(任写两种)
(4)写出一个离子反应方程式,要求反应物与生成物的离子或分子均是由以上元素中的两种元素组成且各微粒所含的电子数相同.nh4++oh-
nh3↑+h2o[或nh3+h3o+═nh4++h2o或oh-+h3o+═2h2o]△ .nh4++oh-.
nh3↑+h2o[或nh3+h3o+═nh4++h2o或oh-+h3o+═2h2o]△ .
(5)***材料学家已成功制备了w元素与y元素组成的耐高温的新型材料w3y4.工业上可用w的氢化物与y的氢化物反应制得耐高温化合物和氢气,此反应的化学方程式为3sih4+4nh3
si3n4+12h2高温 .3sih4+4nh3.
si3n4+12h2高温 . 其实我最想开源1年前0
其实我最想开源1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•宝鸡一模)静止的氮核 147N被速度为v0的中子 10n击中生成碳核 126C
(2014•宝鸡一模)静止的氮核
N被速度为v0的中子147
n击中生成碳核10
C和另一种原子核甲,已知126
C与甲核的速度方向与碰撞前中子的速度方向一致,碰后碳核126
C与甲核的动量之比为l:1.126
(1)写出核反应方程式.
(2)求
C与甲核的速度各是多大?126 guixi1年前1
guixi1年前1 -
 waynelee0925 共回答了20个问题
waynelee0925 共回答了20个问题 |采纳率90%解题思路:(1)在核反应中质量数与核电荷数守恒,根据质量数与核电荷数守恒,写出核反应方程式.
(2)在核反应过程中,系统动量守恒定律可以求出原子核的速度.(1)根据质量数与核电荷数守恒可知,
甲核的核电荷数是1,质量数是3,甲核是氚核,
核反应方程式为:
147N+
10n→
126C+
31H;
(2)设中子质量为m0,
126C核质量mC,甲核质量为m甲,
由动量守恒得:m0v0=mC vC+m甲v甲,
即:m0v0=12 m0 vC+3m0v甲,
又因为
126C与甲核动量比为1:l,
所以m0 vC=m甲v甲,
即12 m0 vC=3 m0v甲,
联立以上两个方程,得:vC=
v0
24,v甲=
v0
6.
答:(1)核反应方程式是:
147N+
10n→
126C+
31H;
(2)
126C的速度是
v0
24,甲核的速度是
v0
6.点评:
本题考点: 动量守恒定律;原子核的人工转变.
考点点评: 本题主要考查了守恒定律在近代物理中的应用,通过该题体会能量守恒和动量守恒使用的广泛性.1年前查看全部
- (2010•宝鸡模拟)超市为了制定某个时间段收银台开放方案,统计了这个时间段本超市顾客在收银台排队付款的等待时间,并绘制
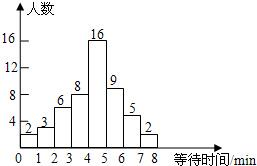 (2010•宝鸡模拟)超市为了制定某个时间段收银台开放方案,统计了这个时间段本超市顾客在收银台排队付款的等待时间,并绘制成如下的频数分布直方图(图中等待时间6分钟到7分钟表示>或等于6分钟而<7分钟,其它类同).这个时间段内顾客等待时间不少于6分钟的人数为 ______人.
(2010•宝鸡模拟)超市为了制定某个时间段收银台开放方案,统计了这个时间段本超市顾客在收银台排队付款的等待时间,并绘制成如下的频数分布直方图(图中等待时间6分钟到7分钟表示>或等于6分钟而<7分钟,其它类同).这个时间段内顾客等待时间不少于6分钟的人数为 ______人.  lujos1年前1
lujos1年前1 -
 圣道轩辕 共回答了19个问题
圣道轩辕 共回答了19个问题 |采纳率89.5%解题思路:分析频数直方图,找等待时间不少于6分钟的小组,读出人数再相加可得答案.由频数直方图可以看出:
顾客等待时间不少于6分钟的人数即最后两组的人数为:
5+2=7人.
故答案为:7.点评:
本题考点: 频率分布直方图.
考点点评: 本题考查同学们频率分布直方图、通过频数直方图获取信息的能力.属于基础题.1年前查看全部
- (201r•宝鸡二模)夫妇均患同一种基因遗传病,但所生子女总不患该病,对此分析最可能的是( )
(201r•宝鸡二模)夫妇均患同一种基因遗传病,但所生子女总不患该病,对此分析最可能的是( )
A.该病受两对基因控制,夫妇的基因型分别为:AAbh和aaBB
B.该病为显性遗传病
C.该病为细胞质基因病
D.该病为隐性遗传病,夫妇都发生了基因突变 盗版VS鬼鬼1年前1
盗版VS鬼鬼1年前1 -
 kappaandunicorn 共回答了17个问题
kappaandunicorn 共回答了17个问题 |采纳率100%解题思路:阅读题干可知,该题的知识点是基因的自由组合定律的实质和应用,根据双亲及后代的表现型推出亲本的基因型的方法,梳理相关知识点,然后结合题干信息进行解答.解;由题意知,夫妇均患同六种基因遗传病,但所生子女总不患该病,说明该病是两对等位基因控制的遗传病,且两对等位基因的显性基因都存在时表现为正常,即A_4_表现为正常,该夫妇的基因型为AA44和aa44.
故选:A.点评:
本题考点: 人类遗传病的类型及危害.
考点点评: 对于基因的自由组合定律的实质的理解和应用是本题考查的重点.1年前查看全部
- (2012•宝鸡二模)如图所示,平行板电容器与一个直流电源E(内阻不计)相连,下极板接地.一带电油滴位于电容器中的P点且
 (2012•宝鸡二模)如图所示,平行板电容器与一个直流电源E(内阻不计)相连,下极板接地.一带电油滴位于电容器中的P点且恰好处于平衡状态.现将平行板电容器的上极板竖直向上移动一小段距离,则( )
(2012•宝鸡二模)如图所示,平行板电容器与一个直流电源E(内阻不计)相连,下极板接地.一带电油滴位于电容器中的P点且恰好处于平衡状态.现将平行板电容器的上极板竖直向上移动一小段距离,则( )
A.P点的电势降低
B.带点油滴的电势能将减少
C.带点油滴将沿竖直方向向上运动
D.电容器的电容减小,极板带电量增大 从然1年前1
从然1年前1 -
 ganymebe 共回答了17个问题
ganymebe 共回答了17个问题 |采纳率76.5%解题思路:将平行板电容器的上极板竖直向上移动一小段距离,根据E=[U/d]知板间场强的变化,由U=Ed判断P点与下极板间的电势差的变化,确定P点电势的变化.由题分析知道油滴带负电,再判断其电势能的变化.根据场强的变化,判断油滴向什么方向运动.A、由题,板间距离增大,电容器的电压不变,根据E=[U/d]知板间场强减小,由U=Ed得知,P点与下极板间的电势差减小,板间场强方向向下,P点电势比下极板高,则可知,P点的电势降低.故A正确.
B、根据油滴原来静止知道,油滴带负电,P点电势降低,油滴的电势能将增大.故B错误.
C、板间场强减小,油滴所受电场力减小,则油滴将沿竖直方向向下运动.故C错误.
D、板间距离增大,电容减小,而电压不变,则电容器的电量减小.故D错误.
故选A点评:
本题考点: 电容器的动态分析;电势;电势能.
考点点评: 本题是电容器动态分析问题,根据E=[U/d]、电容的决定式和定义式结合进行分析.1年前查看全部
- (2014•宝鸡一模)为探究“合力做功与物体动能改变的关系”,某同学设计了如下的实验步骤:
(2014•宝鸡一模)为探究“合力做功与物体动能改变的关系”,某同学设计了如下的实验步骤:
A.将一端带滑轮的长木板放在水平桌面上,使带滑轮的一端伸出桌沿,在无滑轮的一端安装打点计时器,打点计时器跟50Hz交流电源相连.
B.将质量为400g的小车放在打点计时器附近,纸带通过打点计时器限位孔后跟小车相连,在木板的右端垫一个垫块,前后移动垫块,使小车拖着纸带沿木板向下运动时打点计时器在纸带上所打的点恰好间隔相等.
C.保持木板与水平桌面间夹角不变,继续将质量为400g的小车放在打点计时器附近,纸带通过打点计时器限位孔后跟小车相连,在质量分别为10g、50g、100g的三种钩码中,挑选了一个质量为100g的钩码挂在拉线的挂钩P上,如图甲所示.
D.打开打点计时器的电源,由静止释放小车,打出一条纸带如图乙所示.
(1)他在打点计时器所打的第一个点上标上O,在O点后面一定距离处开始每5个点作为一个计数点,依次标上“1”、“2”、“3”,用刻度尺测出了“1”、“2”、“3”各计数点到O点的距离S1、S2、S3的值如图乙所示.则计数点“1”、“2”、“3”中两相邻计数点间的时间间隔T=______s,打点计时器打下计数点“2”时小车的速度v2=______m/s.(小数点后保留两位)
(2)他把小车作为研究对象,将钩码的重力当作小车受到的合力,利用打计时器打下O点到打下计数点“2”的过程来探究合力对小车做的功与小车动能改变的关系,若实验所在地的重力加速度g=9.80m/s2,则合力对小车做的功为W=______J,小车动能的改变为△Ek=______ J.
(3)比较W和△Ek的大小,显然W与△Ek相差较大,即他不能得到“合力对物体做的功等于物体动能的改变”这一结论,请你根据该同学的实验装置和操作过程帮他分析一下,造成以上实验结果的主要原因是:______. fastpatient1年前1
fastpatient1年前1 -
 安琪小丸子 共回答了29个问题
安琪小丸子 共回答了29个问题 |采纳率86.2%解题思路:(1)打点计时器每隔0.02s打一个点,根据打点间隔可知相邻计数点之间的时间,根据匀变速直线运动中时间中点的瞬时速度等于该过程中的平均速度,可以求出打点计时器打下计数点“2”时小车的速度大小;
(2)将砝码重力当作小车所受合外力,根据功的定义可以求出合外力做功大小,根据匀变速直线运动中时间中点的瞬时速度等于该过程中的平均速度可以求出第2个点的速度大小,并求出其动能大小,然后进一步求出其动能的该变量.
(3)实验误差主要来自两个方面一是由实验原理不完善导致的系统误差,一是由数据测量如测量距离等导致的偶然误差,可以从这两个方面进行分析(1)打点计时器的打点周期为0.02s,每5个点作为一个计数点,因此计数点之间的时间间隔为:T=0.10s;
根据匀变速直线运动中时间中点的瞬时速度等于该过程中的平均速度,可得打点计时器打下计数点“2”时小车的速度为:
v2=
x13
2T=
(71.11−41.10)×10−2m
0.2s≈1.50m/s
(2)合力做功等于钩码重力势能的减小量,因此有:
W=mgh02=0.1×9.8×0.5511J=0.54J
小车动能的该变量为:
△Ek=
1
2m
v22=
1
2×0.4×(1.50)2J=0.45J
(3)若将小车作为研究对象,将钩码的重力当作小车受到的合力,应该满足的条件是小车的质量远大于钩码质量,该题中没有满足这一条件,即钩码重力和小车重力相比太大,导致钩码重力和小车受到的合力相差太大,因此会出现大的误差.
故答案为:(1)0.10,1.50;(2)0.54,0.45;(3)钩码重力和小车重力相比太大,导致钩码重力和小车受到的合力相差太大.点评:
本题考点: 探究功与速度变化的关系.
考点点评: 明确实验原理往往是解决实验问题的关键,该实验的一些操作和要求与探究力、加速度、质量之间关系的实验类似可以类比学习,同时注意基本物理规律在实验问题中的应用.1年前查看全部
- (2014•宝鸡一模)如图所示,以水平地面建立x轴,有一个质量为m=1kg的木块(视为质点)放在质量为M=2kg的长木板
 (2014•宝鸡一模)如图所示,以水平地面建立x轴,有一个质量为m=1kg的木块(视为质点)放在质量为M=2kg的长木板上,木板长L=11.5m.已知木板与地面的动摩擦因数为μ1=0.1,m与M之间的摩擦因素μ2=0.9(设最大静摩擦力等于滑动摩擦力).m与M保持相对静止且共同向右运动,已知木板的左端A点经过坐标原点O时的速度为v0=10m/s,在坐标为x0=21m处有一挡板P,木板与挡板P瞬间碰撞后立即以原速率反向弹回,而木块在此瞬间速度不变,若碰后立刻撤去挡板P,g取10m/s2,求:
(2014•宝鸡一模)如图所示,以水平地面建立x轴,有一个质量为m=1kg的木块(视为质点)放在质量为M=2kg的长木板上,木板长L=11.5m.已知木板与地面的动摩擦因数为μ1=0.1,m与M之间的摩擦因素μ2=0.9(设最大静摩擦力等于滑动摩擦力).m与M保持相对静止且共同向右运动,已知木板的左端A点经过坐标原点O时的速度为v0=10m/s,在坐标为x0=21m处有一挡板P,木板与挡板P瞬间碰撞后立即以原速率反向弹回,而木块在此瞬间速度不变,若碰后立刻撤去挡板P,g取10m/s2,求:
(1)木板碰挡板P前瞬间的速度v1为多少?
(2)木板最终停止运动时其左端A的位置坐标? guai05181年前1
guai05181年前1 -
 joanxxz 共回答了23个问题
joanxxz 共回答了23个问题 |采纳率100%解题思路:(1)对整体分析,根据牛顿第二定律求出整体的加速度,根据速度位移公式求出木板碰挡板P前的瞬间速度.(2)当木板碰到挡板并撤掉挡板后,木板以初速度v1向左做匀减速运动,木块以初速度v1向右做匀减速运动,木块加速度较大,所以木块先停下,然后向左做匀加速运动,直到二者保持相对静止.根据牛顿第二定律,结合运动学公式求出木板最终停止运动时其左端A的位置坐标.(1)经过分析可知,木板碰挡板前,木块和木板组成的系统保持相对静止向右匀减速运动,设木板碰挡板时的速度为v1,其加速度为a1,对二者组成的系统,由其受力分析结合牛顿第二定律有:μ1(m+M)g=(m+M)a1
v20-
v21=2a1s
其中:s=x-L=21m-11.5m=9.5m.
解得:v1=9m/s(水平向右)
(2)由题意可知,当木板碰到挡板并撤掉挡板后,木板以初速度v1向左做匀减速运动,木块以初速度v1向右做匀减速运动,设木板和木块的加速度分别为a2和a3,由牛顿第二定律可知:
a2=
μ2mg+μ1(M+m)g
M=6m/s2(水平向右)
a3=
μ2mg
m=μ2g=9m/s2(水平向左)
假设木块没有掉离木板,由于木块加速度较大,所以木块先停下,然后向左做匀加速运动,直到二者保持相对静止.设二者保持相对静止所用时间为t2,
共同速度为v2,可得:v1-a3t2=-(v1-a2t2)
解得:t2=1.2s v2=1.8m/s(水平向左)
在此过程中,木块运动位移s1=
v1-v2
2×t2=4.32m(水平向右)
木板运动位移s2=
v1+v2
2×t2=6.48m(水平向左)
所以二者相对位移△s=s1+s2=10.8m<L=11.5m,即二者相对运动时木块没有掉离木板.二者共速后,又以a1=1m/s2向左减速至停下,
设其向左运动的位移为s3
v22=2a1s3
解得:s3=1.62m
最终木板M左端A点位置坐标为x=x0-L-s2-s3=1.4m.
答:(1)木板碰挡板P前瞬间的速度v1为9m/s,方向向右.
(2)木板最终停止运动时其左端A的位置坐标为1.4m.点评:
本题考点: 牛顿第二定律;匀变速直线运动的速度与时间的关系;匀变速直线运动的位移与时间的关系.
考点点评: 解决本题的关键理清木板和木块在整个过程中的运动规律,结合牛顿第二定律和运动学公式进行求解.本题也可以通过动能定理、功能关系进行求解.1年前查看全部
大家在问
- 1200克水溶解一定质量的氯化镁配制成溶液.取此溶液一半,加入一定质量20%的氢氧化钠溶液恰好完全反应,生成5.8克沉淀.
- 2解方程:x÷6=12
- 3一首描写凄惨悲凉的诗
- 4y=(1+x)^x的求导
- 5在一定的条件下,绝缘体()变成导体.介于导体和绝缘体之间的物体叫()
- 6英语根据提示完成句子1.她读那本通俗科学杂志时跳过了其中的术语She____the jargon when she re
- 7文言文《预浩父女》中的预浩和《梵天寺木塔》中的喻皓是同一个人吗?根据是什么?
- 8碗蜒的意思
- 9用一张边长25厘米的正方形围成一个圆柱形纸筒,它的侧面积是多少?
- 10为什么此时太阳高度角是30度?
- 11用3/2,2/1,6/1,8/1这四个数组成比例式
- 12帮我改一下下面的病句!熊熊大火中,一位遇难者向人们呼救
- 13求从美学角度赏析元好问的 ````急
- 14We goand piay near the bay( ? ) Sunny.
- 15蕴藏的近意词是什么?

