酸雨会给人类带来种种灾害,应该积极进行防治.下列观点错误的是( )
 向东流2022-10-04 11:39:541条回答
向东流2022-10-04 11:39:541条回答A.减少煤和石油等化石燃料的使用
B.可向酸化的湖水中抛洒烧碱进行治理
C.改变能源结构,开发清洁能源
D.氮的氧化物也是形成酸雨的一个重要因素

已提交,审核后显示!提交回复
共1条回复
 米蒂儿_cc 共回答了14个问题
米蒂儿_cc 共回答了14个问题 |采纳率92.9%- 解题思路:A.化石燃料燃烧会生成二氧化硫,减少化石燃料的使用可以减少二氧化硫的排放;
B.烧碱比较贵,可以用廉价的石灰;
C.开发清洁能源,可以减少二氧化硫、氮的氧化物的排放;
D.当空气中含有大量硫、氮氧化物时,与水反应生成亚硫酸、硫酸和硝酸,导致溶液呈酸性.A.化石燃料燃烧会生成二氧化硫,减少化石燃料的使用可以减少二氧化硫的排放,减少酸雨的形成,故A正确;
B.烧碱比较贵,可以用廉价的石灰,故B错误;
C.开发清洁能源,可以减少二氧化硫、氮的氧化物的排放,减少酸雨的形成,故C正确;
D.形成酸雨的主要因素是化石燃料的燃烧,产生大量的二氧化硫及氮的氧化物,当空气中含有大量硫、氮氧化物时,与水反应生成亚硫酸、硫酸和硝酸,导致溶液呈酸性,故D正确;
故选B.点评:
本题考点: 二氧化硫的污染及治理;氮的氧化物的性质及其对环境的影响.
考点点评: 本题考查酸雨的形成与治理,比较基础,主要掌握常见环境污染的成因与治理. - 1年前
相关推荐
- 2009年我省部分地区监测到的雨水平均pH如下表.请回答下列问题: (1)上表列举的5个地区中,没有酸雨污染的地区是 _
2009年我省部分地区监测到的雨水平均pH如下表.请回答下列问题: 
(1)上表列举的5个地区中,没有酸雨污染的地区是 _________ ;导致酸雨的主要气体是 _________ (填序号):
①CO②CO 2 ③SO 2 .
(2)若酸雨的主要成分为H 2 SO 4 和HNO 3 ,请写出下列化学方程式:
①含H 2 SO 4 的酸雨与铁锈反应 _________ ;
②含HNO 3 的酸雨与撒在田地里的熟石灰反应 _________ . 汤水一生1年前1
汤水一生1年前1 -
 ffsdfdf 共回答了17个问题
ffsdfdf 共回答了17个问题 |采纳率100%(1)泰安;③.
(2)①Fe 2 O 3 +3H 2 SO 4 =Fe 2 (SO 4 ) 3 +3H 2 O
②2HNO 3 +Ca(OH) 2 =Ca(NO 3 ) 2 +2H 2 O1年前查看全部
- 英语翻译酸雨可分为“湿沉降”与“干沉降”两大类,前者指的是所有气状污染物或粒状污染物,随着雨、雪、雾或雹等降水型态而落到
英语翻译
酸雨可分为“湿沉降”与“干沉降”两大类,前者指的是所有气状污染物或粒状污染物,随着雨、雪、雾或雹等降水型态而落到地面者,后者则是指在不下雨的日子,从空中降下来的落尘所带的酸性物质而言.
酸雨是含有相对较高酸性的降水.一般的降水,在一个标准大气压、25℃时,它的酸碱度PH值大约为5.65,为弱酸性.而酸雨是指PH小于5.6的降水.因大气中含有天然和人为的污染物,降水过程中把二氧化硫、氮氧化物和其它杂质通过化学反应生成各种酸类,使雨水酸化,降落到地面. kc7f1年前1
kc7f1年前1 -
 Oblivion2007 共回答了19个问题
Oblivion2007 共回答了19个问题 |采纳率89.5%专业性如此之强,内容又超过10个字,还要人免费给你翻译,连个谢字都没有,1年前查看全部
- 矿物能源燃烧时会产生一种刺激性气味的气体,易形成酸雨,因为矿物能源中含有---
矿物能源燃烧时会产生一种刺激性气味的气体,易形成酸雨,因为矿物能源中含有---
工业酒精不能饮用是因为--- qvv771年前1
qvv771年前1 -
 流水铿然 共回答了21个问题
流水铿然 共回答了21个问题 |采纳率95.2%含有硫,工业酒精是甲醇,酒精是乙醇1年前查看全部
- 20世纪70年代中期,在瑞典哥德堡附近的农村陆续发现有些少女的金发慢慢地染上了淡淡的绿色,经分析此种现象与酸雨及当地所用
20世纪70年代中期,在瑞典哥德堡附近的农村陆续发现有些少女的金发慢慢地染上了淡淡的绿色,经分析此种现象与酸雨及当地所用的供水管道为铜制品有关.试解释:
(1)金黄色的头发为何会变为绿色?
(2)在此过程中发生了哪些化学变化?(用化学方程式表示) langping20081年前1
langping20081年前1 -
 恶善人 共回答了16个问题
恶善人 共回答了16个问题 |采纳率81.3%解题思路:根据铜的化学性质,酸雨的成分及性质,去分析回答.铜和空气中的氧气缓慢氧化反应生成氧化铜,酸雨中主要含有硫酸,氧化铜能和硫酸反应生成硫酸铜和水,硫酸铜溶液在一定浓度时为绿色.
故答案为:(1)铜被氧化成CuO,氧化铜与酸反应生成蓝色的铜盐,蓝色和金发在一起就呈绿色;
(2)2Cu+O2=2CuOCuO+H2SO4=CuSO4+H2O.点评:
本题考点: 常见污染物的来源、危害及治理;书写化学方程式、文字表达式、电离方程式.
考点点评: 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.1年前查看全部
- 含硫酸的酸雨腐蚀掉大理石的化学方程式
含硫酸的酸雨腐蚀掉大理石的化学方程式
含硝酸的酸雨与熟石灰反应方程式
请写出NAOH CA(OH)2有哪些相似化学性质
我已经写了具有强腐蚀性
请再写一条
现有失去标签的溶液,它们的稀盐酸和石灰水,请在没有指示剂的方法下鉴别.写出操作步骤和现象结论
计算题
溶质质量分数为36.5%的盐酸40g中含HCL质量为多少G 用该盐酸与足够的烧碱溶液恰好完全反应,需要溶质质量分数为20%的烧碱溶液多少G hyxhdx1年前1
hyxhdx1年前1 -
 90399039 共回答了21个问题
90399039 共回答了21个问题 |采纳率95.2%CaCO3+H2SO4=CaSO4+H2O+CO2↑
Ca(OH)2+2HNO3=Ca(NO3)2+2H2O
能与酸性氧化物反应,能使指示剂变色等.
加入碳酸钠溶液,有气泡产生的为稀盐酸,有白色沉淀产生的为石灰水
40g*36.5%=14.6g
HCl + NaOH=NaCl+H2O
36.5 40
14.6g x*20%
36.5/14.6g=40/x*20%
x=80g1年前查看全部
- 酸雨腐蚀建筑物是什么变化
 afirefly1年前1
afirefly1年前1 -
 独居遥遥 共回答了14个问题
独居遥遥 共回答了14个问题 |采纳率78.6%酸雨腐蚀建筑物有新物质生成,发生了化学反应,属于化学变化.1年前查看全部
- 关于长江,下列说法正确的是?a.“万里长江,险在荆江”,荆江江段水患严重,主要工程措施为加固堤防.b.长江流域酸雨污染最
关于长江,下列说法正确的是?
a.“万里长江,险在荆江”,荆江江段水患严重,主要工程措施为加固堤防.
b.长江流域酸雨污染最严重的地区是华中地区.
c.长江上游山区的水体污染严重. 咋不行呀1年前6
咋不行呀1年前6 -
 mamazhao 共回答了22个问题
mamazhao 共回答了22个问题 |采纳率86.4%a 荆江九曲回肠 易有水患1年前查看全部
- 臭氧空洞、酸雨、汽车尾气、工业废气看到这样的景象你有什么感想?150字以上!
臭氧空洞、酸雨、汽车尾气、工业废气看到这样的景象你有什么感想?150字以上!
急用!急用!速回!速回! taoran20001年前1
taoran20001年前1 -
 chzw123456 共回答了15个问题
chzw123456 共回答了15个问题 |采纳率93.3%大气污染及其防治
自然界清新、洁净的空气,使人心旷神怡、精神振奋.但是随着工业的迅速发展和人口急剧增长,大量燃烧煤炭、石油所产生的化学物质以废气和烟尘等形式排放到大气中,超过了大气环境的容许量,给人类的生活、生产和身体健康带来有害影响.
据统计,全世界每年排入大气的污染物约有6亿多吨.污染源主要是以下三方面:
生活污染源:如家庭、商业服务部门等燃煤排放的烟尘和废气.
交通污染源:如汽车、火车、飞机、船舶等排放的废气.
工业污染源:如发电厂、钢铁厂、水泥厂、氮肥厂、烧碱厂及其它各类化工厂排放的废气和粉尘.
主要大气污染物有两大类:
气态污染物(如二氧化硫、硫化氢、一氧化碳、二氧化碳、二氧化氮、氨、氯气等)
颗粒态污染物(如烟、雾、粉尘)
大气污染会对人类和其它生物造成危害.本世纪以来,不断发生的公害,使人们认识到保护大气不受污染的重要性.如1952年12月5~8日英国伦敦大雾乃为烧煤所产生的烟尘和烟雾散发不出去,造成千万人呼吸道感染,4天中死亡达4000多人.1991年日本四日市石油冶炼和工业燃油所排放的工业废气,使大气中的二氧化硫的浓度超过标准5~6倍,致使全市哮喘病发作.
我国政府十分重视环境保护工作,制订了防治大气污染的法规.例如“大气污染防治法”,“大气环境质量标准”等.人类只有一个地球,应该珍惜它.在不断发展生产的同时学会保护大气不受污染,保护地球环境,以使我们生活的大气永远洁净,天空永远蔚蓝.1年前查看全部
- 以下哪些是空气污染导致的不良后果?1呼吸系统疾病 2全球平均温度上升 3酸雨
 mkf周丽慧1年前1
mkf周丽慧1年前1 -
 怀念老朝晖 共回答了26个问题
怀念老朝晖 共回答了26个问题 |采纳率80.8%都是1年前查看全部
- 酸雨是指什么形式的降雨
 liaowei20461年前4
liaowei20461年前4 -
 娃哈哈d 共回答了16个问题
娃哈哈d 共回答了16个问题 |采纳率100%酸雨是指pH值小于5.0的雨水、冻雨、雪、雹、露等大气降水.现已确认,大气中的二氧化硫和二气化氮是形成酸雨的主要物质.大气中的二氧化硫和二氧化氮主要来源于煤和石油的燃烧,它们在空气中氧化剂的作用下形成溶解于雨水的种酸.据统计,全球每年排放进大气的二氧化硫约1亿吨,二氧化氮的5000万吨,所以,酸雨主要是人类生产活动和生活造成的.
酸雨主要是人类生产活动和生活造成的
A.汽车排放出大量的尾气
(汽车尾气中有上百种不同化合物,当中污染物有固体悬浮微粒、一氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物)
C.工业上大量燃烧含硫燃料
人类自己给自己掘坟墓.因为酸雨主要是人类生产活动和生活造成的.所以提倡保护环境,爱惜我们的生命!1年前查看全部
- 某合作学习小组讨论辨析:①漂白粉和酸雨都是混合物 ②煤和石油都是可再生能源③干冰、水晶、食盐分属分子晶体、原子晶体和离子
某合作学习小组讨论辨析:
①漂白粉和酸雨都是混合物
②煤和石油都是可再生能源
③干冰、水晶、食盐分属分子晶体、原子晶体和离子晶体
④不锈钢和目前流通的硬币都是合金
⑤硫酸、纯碱、醋酸钠和生石灰分 别属于酸、碱、盐和氧化物
⑥豆浆和雾都是胶体。
上述说法正确的是[ ]
A.①②④
B.①⑤⑥
C.①③④⑥
D.②③④⑤ lee_2bwithu1年前1
lee_2bwithu1年前1 -
 xhsunbird 共回答了22个问题
xhsunbird 共回答了22个问题 |采纳率100%C1年前查看全部
- 酸雨的主要成分是二氧化硫还是三氧化硫
 pppfff00161年前5
pppfff00161年前5 -
 kongkongluo 共回答了11个问题
kongkongluo 共回答了11个问题 |采纳率81.8%二氧化硫是酸雨形成的原因之一,二氧化硫进入云雾与水结合为亚硫酸,在粉尘作催化剂是亚硫酸氧化为硫酸.硫酸雨的主要有害成分为硫酸1年前查看全部
- 酸雨往往含有硫酸、盐酸和硝酸等三种成分,但地区不同,成分也不同,要治理酸雨,先要确定其组成,兴趣小组对当地的酸雨进行探究
酸雨往往含有硫酸、盐酸和硝酸等三种成分,但地区不同,成分也不同,要治理酸雨,先要确定其组成,兴趣小组对当地的酸雨进行探究,请你参与探究过程:
(1)若要确定该地区酸雨的pH,最简便的方法是使用 ;
(2)设计实验方案,探究该地区酸雨是否存在硫酸和盐酸,填写下来.(已知硫酸银微溶于水.)限选试剂:NaOH溶液、BaCl 2 溶液、Ba(NO 3 ) 2 溶液、AgNO 3 溶液
 笑对人生19811年前1
笑对人生19811年前1 -
 宝贝carrie 共回答了14个问题
宝贝carrie 共回答了14个问题 |采纳率92.9%(1)pH试纸检测
(2)步骤1: 滴加Ba(NO 3 ) 2 溶液;有白色沉淀生成,说明有硫酸;
步骤2:滴加AgNO 3 溶液;有白色沉淀生成,说明有盐酸;1年前查看全部
- 酸雨的化学式和形成原因!
 此情应否成追忆1年前1
此情应否成追忆1年前1 -
 fhcar 共回答了12个问题
fhcar 共回答了12个问题 |采纳率91.7%酸雨的化学式:SO2 H2SO4·H2O 都可以
2SO2+2H2O =2H2SO3
工业生产中排放的含有SO2的废气,在自然界遇水形成亚硫酸 H2SO3,如果遇到水蒸气则变成酸微粒——酸雾,随着雨水降落到地面而形成酸雨1年前查看全部
- 为什么酸雨渗入地下会使地下水中的重金属元素含量升高?
 我爱颜行书1年前1
我爱颜行书1年前1 -
 y66zh 共回答了17个问题
y66zh 共回答了17个问题 |采纳率100%生成可溶性盐1年前查看全部
- 酸雨的PH值为什么随时间的推移逐渐变小到某一固定值?
 xiha02241年前1
xiha02241年前1 -
 海鸥之子 共回答了15个问题
海鸥之子 共回答了15个问题 |采纳率86.7%酸雨中主要含有的是H2SO3
H2SO3是弱酸,电离不完全,H2SO3会被空气中的O2氧化.
2H2SO3+O2=2H2SO4
H2SO4是强酸,所以酸雨的PH值随时间的推移逐渐变小.
当H2SO3全部被氧化为H2SO4时pH值就固定了.1年前查看全部
- 酸雨是怎么形成的?它有哪些危害?
酸雨是怎么形成的?它有哪些危害?
紧急!字数10---30左右! human221331年前1
human221331年前1 -
 汐儿_ 共回答了20个问题
汐儿_ 共回答了20个问题 |采纳率95%当烟囱排放出的二氧化硫酸性气体,或汽车排放出来的氮氧化物烟气上升到空中与水蒸气相遇时,就会形成硫酸和硝酸小滴,使雨水酸化,这时落到地面的雨水就成了酸雨.酸雨酸化水体可导致水生生物减少甚至绝迹,过食物链而危害人体健康;酸化土壤则使其中钙、镁等元素溶出流失,使土壤的肥力下降,损失一些建筑物和文物胶等产生破坏作用,导致使用寿命缩短.1年前查看全部
- 英语翻译白垩纪末期可能下过强烈的酸雨,使土壤中包括锶在内的微量元素被溶解,恐龙通过饮水和食物直接或间接地摄入锶,出现急性
英语翻译
白垩纪末期可能下过强烈的酸雨,使土壤中包括锶在内的微量元素被溶解,恐龙通过饮水和食物直接或间接地摄入锶,出现急性或慢性中毒,最后一批批死掉了. houzidiai1年前2
houzidiai1年前2 -
 笔芯没有快男 共回答了18个问题
笔芯没有快男 共回答了18个问题 |采纳率72.2%The upper cretaceous period may once strong acid rain,soil including strontium,trace elements being dissolved,dinosaurs through drinking water and food directly or indirectly intake of strontium,appear acute or chronic poisoning,last batch died.1年前查看全部
- 什么是酸雨酸雨是怎么形成,它对人类有什么危害
 puritywater1年前1
puritywater1年前1 -
 king_lx 共回答了17个问题
king_lx 共回答了17个问题 |采纳率88.2%酸雨 是指pH小于5.6的雨雪或其他形式的降水.
一般酸水化学组成中,较重要的物种包括 Cl-、NO3-、SO42-、NH4+、K+、Na+、Ca2+及 Mg2+ 等九种.其来源包括自然来源及人为来源.一般而言,NO3-及 SO42- 为主要的致酸物质,它们是由硫氧化物(SO2)与氮氧化物(NO,NO2)转化而来.在人为污染排放方面,前者与使用化石燃料、火力发电厂、燃烧含硫有机物有关,后者主要来自工厂高温燃烧过程、交通工具排放等因素.Ca2+ 及 NH4+ 为主要的中和(致碱)物质.1年前查看全部
- 英语翻译世界十大环境问题有:1、气候变暖.2、臭氧层破坏.3、生物多样性减少.4、酸雨漫延.5、森林锐减.6、土地荒漠化
英语翻译
世界十大环境问题有:1、气候变暖.2、臭氧层破坏.3、生物多样性减少.4、酸雨漫延.5、森林锐减.6、土地荒漠化.7、大气污染.8、水体污染.9、海洋污染.10、固体废弃物污染 197204081年前4
197204081年前4 -
 蒙塞拉特岛 共回答了17个问题
蒙塞拉特岛 共回答了17个问题 |采纳率88.2%标准地道翻译:
The ten major world environmetal problems are:
1.global warming.
2.ozonosphere destruction.
3.decrease in species diversity.
4.spread of acid rain.
5.forests' sharp decrease
6.land desertification
7.air pollution.
8.water pollution
9.ocean pollution.
10.solid waste pollution.1年前查看全部
- 下列哪一种情况不是由酸雨造成的 [ ] A.森林枯萎
下列哪一种情况不是由酸雨造成的 [ ]A.森林枯萎
B.鱼虾死亡
C.水俣病
D.土壤肥力降低 爱而快乐1年前1
爱而快乐1年前1 -
 Double六六六 共回答了17个问题
Double六六六 共回答了17个问题 |采纳率88.2%C1年前查看全部
- 请回答下列问题(1)酸碱中和反应在生活、生产中有广泛的应用,请举一例说明。(2)酸雨是严重的环境问题之一,治理酸雨刻不容
请回答下列问题
(1)酸碱中和反应在生活、生产中有广泛的应用,请举一例说明。
(2)酸雨是严重的环境问题之一,治理酸雨刻不容缓。请说出酸雨的危害或防治措施(回答一条即可)。 zxcv23ljlkfdajsl1年前1
zxcv23ljlkfdajsl1年前1 -
 SMMCAT 共回答了20个问题
SMMCAT 共回答了20个问题 |采纳率90%(1)氢氧化铝治疗胃酸
(2)开发新能源,减少煤的燃烧1年前查看全部
- 酸雨指PH(小于)5.6的降水.
 jody_gong1年前1
jody_gong1年前1 -
 蓝调灵铃 共回答了25个问题
蓝调灵铃 共回答了25个问题 |采纳率92%我们常说纯净水的PH值是7,但在现实生活中空气中的二氧化碳溶解在水中就使得水的PH值为5.6,当有其他酸性气体溶解在其中时其PH值就小于5.6..故酸雨的PH值是要小于5.6而不是小于7.01年前查看全部
- 植被大面积减少给生物圈带来了许多问题。下列各种环境问题,主要是由植被减少引起的是( ) A.水俣病 B.酸雨 C.沙尘暴
植被大面积减少给生物圈带来了许多问题。下列各种环境问题,主要是由植被减少引起的是( )
A.水俣病 B.酸雨 C.沙尘暴 D.赤潮  zz62651年前1
zz62651年前1 -
 三禾 共回答了21个问题
三禾 共回答了21个问题 |采纳率95.2%C
1年前查看全部
- 化学知识谜语可以增添化学学习的乐趣并能增强记忆.现有一则谜语:“闻有刺激味,含量平均分,酸雨由它造,追捕无影踪”.下列最
化学知识谜语可以增添化学学习的乐趣并能增强记忆.现有一则谜语:“闻有刺激味,含量平均分,酸雨由它造,追捕无影踪”.下列最适合作为谜底的物质是( ) A.一氧化碳 B.二氧化碳 C.二氧化硫 D.二氧化氮  黄钰杭1年前1
黄钰杭1年前1 -
 nanayan 共回答了16个问题
nanayan 共回答了16个问题 |采纳率87.5%一氧化碳、二氧化碳都是无色、无味的气体,二氧化氮是一种红棕色气体;二氧化硫是一种无色、有刺激性气味的气体,是形成酸雨的重要物质,硫元素和氧元素的质量分数相等.
故选C.1年前查看全部
- 酸雨对植物的影响——生物实验人教版七年级下册书中有一个酸雨对植物的影响的实验,需要这个试验的具体步骤.希望再有具体一点的
 cashoo1年前3
cashoo1年前3 -
 wanghu1991 共回答了17个问题
wanghu1991 共回答了17个问题 |采纳率94.1%找两个一样的植物一盆正常浇水 另外一盆浇水时不要浇正常PH值得水 教些酸性的水(可以自己在模拟酸雨造点例如用二氧化硫忽然水)其他的培养条件一样做个对照试验就一切OK了
具体的目的和设计以及结果你自己搞吧 我把方法给你 我的学生都能做的很好1年前查看全部
- 酸雨、温室效应、臭氧空洞是人类面临的三大环境问题,下列说法不准确的是( )
酸雨、温室效应、臭氧空洞是人类面临的三大环境问题,下列说法不准确的是( )
A. 使用液化气代替汽油作汽车燃料,可以减少温室效应
B. 逐步使用核能、风能、氢能,可以减少温室效应
C. 使用无氟冰箱等,可以减少臭氧空洞
D. 对燃煤预先采取脱硫措施,可以减少酸雨 井Q1年前1
井Q1年前1 -
 华广 共回答了9个问题
华广 共回答了9个问题 |采纳率88.9%解题思路:A、液化气是石油分馏的产物,燃烧同样会产生温室气体.
B、根据减少温室效应的措施进行分析判断.
C、电冰箱中的制冷剂“氟里昂”等,会使臭氧层形成空洞.
D、酸雨是因为空气中的污染物二氧化硫、氮氧化合物等过多造成的,二氧化硫、氮氧化合物来自于煤等化石燃料的大量使用.A、液化气是石油分馏的产物,它的燃烧同样会产生温室气体,不会减少温室效应,故选项说法错误.
B、逐步使用核能、风能、氢能等新能源,可以减少二氧化碳的排放量,可以减少温室效应,故选项说法正确.
C、电冰箱中的制冷剂“氟里昂”等,对臭氧层有很大的破坏作用,会使臭氧层形成空洞;使用无氟冰箱等,可以减少臭氧空洞,故选项说法正确.
D、二氧化硫、氮氧化合物等排放会形成酸雨,对燃煤预先采取脱硫措施,可减少二氧化硫等气体的排放,可以减少酸雨,故选项说法正确.
故选A.点评:
本题考点: 常用燃料的使用与其对环境的影响;酸雨的产生、危害及防治;资源综合利用和新能源开发.
考点点评: 环境污染与保护是人们关注的热点,也是中考考查的热点之一,了解当今世界常见的环境污染与防治措施即可正确解答本题.1年前查看全部
- 为什么说 防治酸雨的根本途径是减少二氧化碳和氮氧化物的排放.是不对的
 huanyingshenzhen1年前2
huanyingshenzhen1年前2 -
 x4770403 共回答了15个问题
x4770403 共回答了15个问题 |采纳率93.3%减少二氧化碳是减缓温室效应措施 防治酸雨应嫌少二氧化硫的排放1年前查看全部
- 臭氧层是被什么气体破坏请回答我是说造成酸雨的主要物质有什么
 彩色秦俑1年前1
彩色秦俑1年前1 -
 小卓yzc 共回答了24个问题
小卓yzc 共回答了24个问题 |采纳率79.2%破坏臭氧层物质很多,一般有还原性的物质均有可能使之破坏,因臭氧有强氧化性.如二氧化硫,一氧化氮等.另像氟氯代烷(商品名为氟利昂)、氮的氧化物对臭氧层破坏起到催化剂的作用,其破坏性更强.
造成酸雨的主要物质是氮的氧化物和硫的氧化物.如二氧化硫溶于雨水中,生成亚硫酸,亚硫酸被氧气进一步氧化为硫酸,二氧化氮与雨水反应生成硝酸,这就是酸雨中酸性的来源.1年前查看全部
- “酸雨”产生的原因是由于空气中的那种成分含量过高( )
“酸雨”产生的原因是由于空气中的那种成分含量过高( )
A.二氧化碳
B.二氧化硫
C.二氧化氮
D.硫酸 lawrence_liu1年前1
lawrence_liu1年前1 -
 kkk305145298 共回答了17个问题
kkk305145298 共回答了17个问题 |采纳率88.2%解题思路:pH小于5.6的雨水就算酸雨;正常雨水的pH约为 5.6 (这是由于溶解了二氧化碳的缘故 ),微偏酸.导致酸雨的主要原因是空气中二氧化硫的含量过高,二氧化硫主要是由于燃烧煤产生的,因为煤中含有硫元素.燃烧会生成大量二氧化硫,导致酸雨.酸雨是由于人类大量使用含硫量高的煤、石油、天然气等化石燃料,燃烧后产生的含有二氧化硫等的气体,在大气中经过复杂的化学反应后,形成硫酸或硝酸气溶胶,或为云、雨、雪、雾捕捉吸收,降到地面成为酸雨.
酸雨直接危害植物的芽和叶,使农作物大幅度减产,严重时使成片的植物死亡.在酸雨的作用下,土壤中的营养元素钾、钠、钙、镁会释放出来,并随着雨水被淋掉,所以长期的酸雨会使土壤中大量的营养元素被淋失,造成土壤中营养元素严重不足,变得贫瘠.此外,酸雨能使土壤中的铝从稳定态中释放出来,使活性铝增加而有机络合态铝减少.土壤中活性铝的增加会严重抑制林木的生长.酸雨可抑制某些土壤微生物的繁殖,降低酶活性,土壤中的固氮菌、细菌和放线菌均会明显受到酸雨的抑制.酸雨危害水生生物,它使许多河、湖水质酸化,导致许多对酸敏感的水生生物种群灭绝,湖泊失去生态机能,最后变成死湖.酸雨还杀死水中的浮游生物,破坏水生生态系统此外,酸雨还可使森林的病虫害明显增加.在四川,重酸雨区的马尾松林的病情指数为无酸雨区的2.5倍.减少酸雨主要是要减少烧煤排放的二氧化硫和汽车排放的氮氧化物.对付酸雨,工厂应采取的措施包括采用烟气脱硫装置、提高煤炭燃烧的利用率.
故选B.点评:
本题考点: 酸雨对生物的影响及其防治.
考点点评: 解答此类题目的关键是理解掌握酸雨的形成.1年前查看全部
- 下列说法正确的是( ) A.pH=5.6的降雨是酸雨 B.pH越大溶液的酸性越强 C.健康人体的体液都为弱碱性 D.调
下列说法正确的是( )
A.pH=5.6的降雨是酸雨 B.pH越大溶液的酸性越强 C.健康人体的体液都为弱碱性 D.调节土壤的pH可以改良土壤  青果果冻1年前1
青果果冻1年前1 -
 jay998 共回答了13个问题
jay998 共回答了13个问题 |采纳率100%D
1年前查看全部
- (2009•南昌二模)下图是多种无机物在一定条件下的转化关系(部分产物及反应条件未列出.)K是形成光化学烟雾及形成酸雨的
(2009•南昌二模)下图是多种无机物在一定条件下的转化关系(部分产物及反应条件未列出.)K是形成光化学烟雾及形成酸雨的一种主要气体,N为第三周期元素组成的单质熔点最高的金属,X是一种矿石的主要成份,常用来生产一种常见的化工产品.
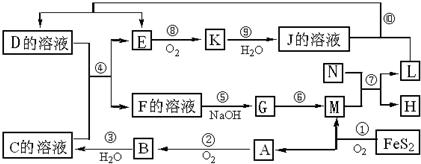
回答:
(1)在周期表,组成单质L的元素位于第______ 周期第______ 族.
(2)K的名称为______,G的化学式______;
(3)已知FeS2的燃烧热为853KJ/mol,写出反应①的热化学方程式:FeS2(s)+[11/4]O2(g)
[1/2]Fe2O3(s)+2SO2(g)△H=-853kJ/mol高温 .FeS2(s)+[11/4]O2(g)
[1/2]Fe2O3(s)+2SO2(g)△H=-853kJ/mol高温 .
(4)写出反应⑤的离子方程式:______写出⑩的离子方程式:______
(5)反应⑦中,若转移9mol电子,生成的L______ g. 分手不远1年前1
分手不远1年前1 -
 momochawu 共回答了10个问题
momochawu 共回答了10个问题 |采纳率90%解题思路:由反应4FeS2+11O2
2Fe2O3+8SO2知A、D为Fe2O3、SO2中的一种,结合A+O2 →B知,A为SO2,M为Fe2O3,B为SO3,C为H2SO4;由N为第三周期中熔点最高的金属知N为Al;L、H为Al2O3和Fe中的一种;由K是形成光化学烟雾及形成酸雨的一种主要气体可知K为NO2,J为HNO3,E为NO;又由L+HNO3 →D+NO↑分析知L为Fe,H为Al2O3;J应为Fe(NO3)3或Fe(NO3)2;联系反应④:D+H2SO4 →F+NO↑知,D为Fe(NO3)2;F为Fe(NO3)3或Fe2(SO4)3;G应为Fe(OH)3,至此全部物质已确定,题目所涉及的问题可顺利解决.高温 .由反应4FeS2+11O2
高温
.
2Fe2O3+8SO2知A、D为Fe2O3、SO2中的一种,结合A+O2 →B知,A为SO2,M为Fe2O3,B为SO3,C为H2SO4;由N为第三周期中熔点最高的金属知N为Al;L、H为Al2O3和Fe中的一种;由K是形成光化学烟雾及形成酸雨的一种主要气体知K为NO2,J为HNO3,E为NO;又由L+HNO3 →D+NO↑分析知L为Fe,H为Al2O3;J应为Fe(NO3)3或Fe(NO3)2;联系反应④:D+H2SO4 →F+NO↑知,D为Fe(NO3)2;F为Fe(NO3)3或Fe2(SO4)3;G应为Fe(OH)3,则
(1)L为Fe,位于周期表第四周期第Ⅷ族,故答案为:四;Ⅷ;
(2)K为NO2,名称为二氧化氮,G为Fe(OH)3,故答案为:二氧化氮;Fe(OH)3;
(3)根据燃烧热的概念可写出反应①的热化学方程式为FeS2(s)+[11/4]O2(g)
高温
.
[1/2]Fe2O3(s)+2SO2(g);
△H=-853kJ/mol,
故答案为:FeS2(s)+[11/4]O2(g)
高温
.
[1/2]Fe2O3(s)+2SO2(g);△H=-853kJ/mol;
(4)反应⑤为Fe3+与NaOH的反应,离子方程式为Fe3++3OH-═Fe(OH)3↓,
反应⑩为Fe在酸性条件下与NO3-的反应,反应的离子方程式为3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O,
故答案为:Fe3++3OH-═Fe(OH)3↓;3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O;
(5)2Al+Fe2O3
高温
.
Al2O3+2Fe 转移电子
112g 6mol
m(Fe) 9mol
m(Fe)=168g,
故答案为:168.点评:
本题考点: 无机物的推断.
考点点评: 本题涉及铁及其化合物,Al、HNO3、H2SO4、NOx等内容,综合考查考生熟练运用元素化合物知识解决问题的能力,题目难度中等.1年前查看全部
- 按要求回答下列问题.(1)SO 2 是形成酸雨的罪魁祸首.64gSO 2 的物质的量为______,在标准状况下的体积约
按要求回答下列问题.
(1)SO 2 是形成酸雨的罪魁祸首.64gSO 2 的物质的量为______,在标准状况下的体积约为______,所含原子数为______.
(2)写出除去下列物质所含杂质(括号内为杂质)所用的试剂或方法:
①Na 2 CO 3 固体(NaHCO 3 )______
②FeCl 3 溶液(FeCl 2 )______
③Mg粉(Al)______
④CO 2 (SO 2 )______. 梨花阵阵1年前1
梨花阵阵1年前1 -
 watch_star 共回答了19个问题
watch_star 共回答了19个问题 |采纳率84.2%(1)64SO 2 的物质的量=
64g
64g/mol =1mol,标况下SO 2 的体积=1mol×22.4L/mol=22.4L,SO 2 分子含有3个原子,含有原子数目=1mol×3×N A mol -1 =3N A ,
故答案为:1mol;22.4L;3N A ;
(2)①由于碳酸氢钠加热分解生成碳酸钠,故可以加热方法除去混有的碳酸氢钠;
②氯气氧化氯化亚铁生成氯化铁,用氯气除去氯化铁溶液中混有的氯化亚铁;
③Al与NaOH溶液(或KOH溶液)反应反应,而Mg不能反应,再进行过滤分离,可以除去混有的Al;
④二氧化硫有还原性,能与酸性高锰酸钾反应生成硫酸;二氧化硫能与饱和的碳酸氢钠反应反应生成二氧化碳,可以用KMnO 4 (H + )溶液(或饱和NaHCO 3 溶液)除去二氧化碳中混有的二氧化硫,
故答案为:①加热;②Cl 2 ;③NaOH溶液(或KOH溶液);④KMnO 4 (H + )溶液(或饱和NaHCO 3 溶液).1年前查看全部
- 据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源不是清洁能源的是( )
据报导,我国某些城市的酸雨严重,为改变这一状况,某市正准备推广使用的清洁能源,下列所列能源不是清洁能源的是( )
A. 太阳能
B. 石油
C. 天然气
D. 酒精 qdlqdl19591年前1
qdlqdl19591年前1 -
 suntao207 共回答了24个问题
suntao207 共回答了24个问题 |采纳率95.8%解题思路:石油属于化石燃料成分比较复杂,燃烧时生成的有害物质较多,不是清洁能源;而天然气和酒精燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮氧化物、一氧化碳等有害物质,太阳能没有污染物,所以都属于清洁能源.A、太阳能无污染,属于清洁能源,故A不选;
B、石油成分比较复杂,燃烧时生成的有害物质较多,不是清洁能源,故B选;
C、天然气燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮的氧化物等有害物质,属于清洁能源,故C不选;
D、酒精燃烧后,只生成水和二氧化碳,没有硫的氧化物(煤的燃烧),没有氮氧化物等有害物质,属于清洁能源,故D不选.
故选B.点评:
本题考点: 清洁能源.
考点点评: 本题考查了清洁能源的使用,题目难度不大,注意能源的开发、利用以及燃烧产物对环境的影响等问题.1年前查看全部
- 工业废水大都是含有有害物质的( ) 酸雨是( )性降水
 李玫儿1年前1
李玫儿1年前1 -
 luosongtj 共回答了23个问题
luosongtj 共回答了23个问题 |采纳率82.6%有害物质:(重金属);酸雨是(酸)性降水.1年前查看全部
- 煤炭燃烧后产物会形成酸雨的
 zth6666661年前2
zth6666661年前2 -
 berryzz 共回答了14个问题
berryzz 共回答了14个问题 |采纳率92.9%含硫煤炭燃烧:
S+O2=点燃=SO2
二氧化硫和水反应:
SO2+H2O=H2SO3
亚硫酸被氧化为硫酸:
2H2SO3+O2=2H2SO41年前查看全部
- 酸雨也称“空中死神”,主要是含硫的煤燃烧时,排放到空气中的二氧化硫随雨水落下而形成的,请回答:
酸雨也称“空中死神”,主要是含硫的煤燃烧时,排放到空气中的二氧化硫随雨水落下而形成的,请回答:
(1)写出硫燃烧时生成二氧化硫的化学方程式______;
(2)若用氢氧化钠溶液吸收二氧化硫,反应的化学方程式为______;
(3)近年来为防治酸雨,工业上常采用“钙基固硫法”,即将生石灰与含硫的煤混合后燃烧,使生石灰、硫、氧气在高温下共同反应生成硫酸钙,写出该反应的化学方程式:______. 项峰1年前1
项峰1年前1 -
 肾亏胆小心衰 共回答了13个问题
肾亏胆小心衰 共回答了13个问题 |采纳率100%(1)硫与氧气在点燃的条件下燃烧时生成二氧化硫的化学方程式为:S+O 2
点燃
.
SO 2 ;
(2)氢氧化钠与二氧化硫反应会生成亚硫酸钠和水,反应的化学方程式为:SO 2 +2NaOH═Na 2 SO 3 +H 2 O;
(3)从题干的叙述可知该反应的反应物为生石灰、硫、氧气条件是高温生成物是硫酸钙,该反应的化学方程式:2CaO+2S+3O 2
高温
.
2CaSO 4 ;
故答案为:(1)S+O 2
点燃
.
SO 2 ;(2)SO 2 +2NaOH═Na 2 SO 3 +H 2 O;(3)2CaO+2S+3O 2
高温
.
2CaSO 4 ;1年前查看全部
- 导致酸雨的主要原因是空气中含有大量的( ) A.由工业燃烧排放的二氧化碳 B.由工业燃烧排放的二氧化硫 C.由人类活动
导致酸雨的主要原因是空气中含有大量的( ) A.由工业燃烧排放的二氧化碳 B.由工业燃烧排放的二氧化硫 C.由人类活动引起的臭氧增加 D.由人类活动排放的含氮物质  l7non1年前1
l7non1年前1 -
 fdsdsaff 共回答了25个问题
fdsdsaff 共回答了25个问题 |采纳率88%酸雨是由于人类大量使用含硫量高的煤、石油、天然气等燃料,燃烧后产生的含有二氧化硫等的气体,在大气中经过复杂的化学反应后,形成硫酸或亚硫酸气溶胶,或为云、雨、雪、雾捕捉吸收,降到地面成为酸雨.
故选:B1年前查看全部
- 含硫煤燃烧排放到空气中的有毒气体主要是二氧化硫,它遇雨形成酸雨降落到地面会带来很大的危害
含硫煤燃烧排放到空气中的有毒气体主要是二氧化硫,它遇雨形成酸雨降落到地面会带来很大的危害
(1)请举出两个方面有危害的实例(2)为减少环境污染,对工厂排放的废气可用烧碱溶液吸收处理,其反应化学方程式为 AtlanticBlue1年前1
AtlanticBlue1年前1 -
 xhn001 共回答了20个问题
xhn001 共回答了20个问题 |采纳率75%1.酸雨降下来腐蚀大理石雕塑
酸雨腐蚀树木
2.2NaOH+SO2=Na2SO3+H2O
如果SO2再多一点
Na2SO3+SO2+H2O=2NaHSO31年前查看全部
- 下列叙述错误的是( )A.炉子上只要放一壶水就能防止煤气中毒B.无铅汽油的使用可以提高城乡空气质量C.酸雨主要是由于受
下列叙述错误的是( )
A.炉子上只要放一壶水就能防止煤气中毒
B.无铅汽油的使用可以提高城乡空气质量
C.酸雨主要是由于受到硫的氧化物或氮的氧化物污染所致
D.人类向空气中排放的一些有害物质(如氟里昂等),使臭氧层受到了破坏 舞梅天下1年前1
舞梅天下1年前1 -
 zjq98666 共回答了21个问题
zjq98666 共回答了21个问题 |采纳率85.7%解题思路:A、根据一氧化碳的性质进行分析判断.
B、根据无铅汽油的使用可以提高城乡空气质量进行分析判断.
C、根据酸雨的形成过程进行分析.
D、根据臭氧层受到破坏的原因进行分析.A、一氧化碳难溶于水,放一壶水不能溶解产生的一氧化碳,故选项说法错误.
B、无铅汽油的使用可以减少空气污染,提高城乡空气质量,故选项说法正确.
C、硫的氧化物或氮的氧化物与空气中的雨水反应生成酸,随雨水降落到地面形成酸雨,故选项说法正确.
D、人类向空气中排放的一些有害物质(如氟里昂等),使臭氧层受到了破坏,故选项说法正确.
故选:A.点评:
本题考点: 一氧化碳的毒性;空气的污染及其危害;酸雨的产生、危害及防治;常用燃料的使用与其对环境的影响.
考点点评: 本题难度不大,掌握一氧化碳的性质、酸雨的形成以及环境保护的有关问题等即可正确解答本题.1年前查看全部
- 3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物
3.下列有关防止或减少酸雨的措施中不可行的是 A.对燃煤及燃煤烟气进行脱硫 ...C.人工收集大气雷电产生的氮的氧化物 D.推广天然气、甲醇等作为汽车的燃料 A ①②③④ B ①②③ C ①②④ D ①③④
 hezhizhang20001年前1
hezhizhang20001年前1 -
 wh_xb 共回答了24个问题
wh_xb 共回答了24个问题 |采纳率83.3%3、C是错误的.1年前查看全部
- 下列有关说法,错误的是( ) A.氮氧化物、二氧化硫都是形成酸雨的主要物质 B.工业合成氨及用NH 3 制化肥(NH
下列有关说法,错误的是()
A.氮氧化物、二氧化硫都是形成酸雨的主要物质 B.工业合成氨及用NH 3 制化肥(NH 4 ) 2 SO 4 都属于氮的固定 C.一定条件下,镁能与一些非金属氧化物反应,铝能与一些金属氧化物反应 D.玻璃中含有硅酸钠和二氧化硅  阳光喜悦1年前1
阳光喜悦1年前1 -
 iudanshaner 共回答了21个问题
iudanshaner 共回答了21个问题 |采纳率100%B
氮的单质生成氮的化合物的反应,才是氮的固定,用NH 3 制化肥(NH 4 ) 2 SO 4 不属于氮的固定。1年前查看全部
- 为了减少酸雨的形成,必须减少二氧化硫的排放量,对废气中的氮的氧化物用什么吸收
 喜欢绿豆沙1年前2
喜欢绿豆沙1年前2 -
 lion13815 共回答了20个问题
lion13815 共回答了20个问题 |采纳率90%氮氧化物用氢氧化钠吸收1年前查看全部
- 由氢氧氮组成的化学式酸 碱 盐 形成酸雨的一种氧化物
 版主的vv1年前5
版主的vv1年前5 -
 鞭策人生 共回答了16个问题
鞭策人生 共回答了16个问题 |采纳率93.8%酸:HNO3
碱:NH4OH
盐:NH4NO3
形成酸雨的一种氧化物:NO21年前查看全部
- 下列对应关系错误的是 a氧气供给呼吸 b稀有气体做霓虹灯 c氮气做保护气 d 二氧化碳造成酸雨
 独语村1年前4
独语村1年前4 -
 wcwcm 共回答了23个问题
wcwcm 共回答了23个问题 |采纳率95.7%d 酸雨是PH<5.6的降水.主要溶解了硫的氧化物和氮的氧化物.虽然二氧化碳溶于水的呈酸性的.但是,二氧化碳却不能造成酸雨1年前查看全部
- 酸雨属于硫酸型酸雨,其主要原因是燃烧的硫的煤产生so2气体,在空气中尘埃的催化作用和阳光照射下转变为so3,再和雨水反应
酸雨属于硫酸型酸雨,其主要原因是燃烧的硫的煤产生so2气体,在空气中尘埃的催化作用和阳光照射下转变为so3,再和雨水反应生成硫酸降落到地面.
问:如果生成的so2全部转化为so3,so3又全部转化为硫酸,最终生成硫酸的质量是多少?
so2质量为50g n0cfed5r1年前4
n0cfed5r1年前4 -
 魔rr 共回答了16个问题
魔rr 共回答了16个问题 |采纳率93.8%根据原子守恒,H2SO4里的S全部来源于SO2,所以SO2- -H2SO4
高中解法:
n(H2SO4)=n(SO2)=25/32mol
硫酸的质量m=25/32×98=76.56g
初中解法:SO2- -H2SO4
64 98
50 X
64/50=98/X
X=76.56g
最终生成硫酸的质量是76.56g1年前查看全部
- 酸雨是大气环境问题之一,北欧近年来森林大面积遭受酸雨危害,而北欧各国把英国告上发庭,是否合理,说...
酸雨是大气环境问题之一,北欧近年来森林大面积遭受酸雨危害,而北欧各国把英国告上发庭,是否合理,说...
酸雨是大气环境问题之一,北欧近年来森林大面积遭受酸雨危害,而北欧各国把英国告上发庭,是否合理,说明理由? 西山蝴蝶1年前3
西山蝴蝶1年前3 -
 wuyiko 共回答了17个问题
wuyiko 共回答了17个问题 |采纳率88.2%不合理,因为酸雨的产生根本是因为SO2,而SO2是气体,会在大气中扩散和转移,因此酸雨也被认为是世界性灾害.所以北欧的酸雨并不一定只是英国产生的,可能是别处飘来的.所以北欧各国把英国告上发庭,不合理1年前查看全部
- 二氧化碳的排放能不能导致酸雨
 0桃花岛主01年前3
0桃花岛主01年前3 -
 9shilling 共回答了17个问题
9shilling 共回答了17个问题 |采纳率94.1%不会1年前查看全部
- 下图是研究酸雨对小麦发芽是否有影响的实验装置.甲,乙 (1)在甲培养皿中加人的是清水,在乙培养皿中加入
下图是研究酸雨对小麦发芽是否有影响的实验装置.甲,乙 (1)在甲培养皿中加人的是清水,在乙培养皿中加入
的是含有酸性物质的溶液.
(2)在实验设计中,可变量是 ,你认为还应控制的影响实验的相关因素
有 . 小丸子11年前1
小丸子11年前1 -
 woshiyouke109 共回答了19个问题
woshiyouke109 共回答了19个问题 |采纳率78.9%可变量是:培养皿中的pH.
还应控制的因素有:温度、氧浓度、水分含量、种子的休眠状态等.1年前查看全部
大家在问
- 1交流电不是电流定期改变方向吗 电流代表正电荷运动方向
- 2海水冰凉 .扩句
- 3∫ (x^7/(x^4+2))dx,求不定积分
- 4一个梯形的两腰相等,都是12厘米,上底比一条腰短5厘米,下底比上底长7厘米,梯形
- 5try to eat a lot of vegetables是什么意思?不是说try to do sth是尽力做某事,t
- 6(2013•茂名模拟)在杠杆上的A点挂一重物,在C点对杠杆施加一个最小的力,使杠杆平衡在图中所示的位置.画出这个力的示意
- 7how long have you been skating?
- 8There ___ a group of people...用is 还是are?
- 9试比较吡啶与吡咯的碱性强弱,并说明理由
- 10下列离子方程式表达正确的是( )
- 11已知定义在(-1,1)上的函数f(x)满足f(log以a为底 x为真数的对数)=(a/a²-1)×(x-x负一
- 12上周我和家人去桂林旅游
- 13根据答句写问句:The brown shoes are Tom's.
- 14Tony is the only one of the students who _____ to europe.A h
- 15如果你有很多钱你会怎莫做?英语作文
