遇水放出易燃气体的物质有哪些除了电石外,还有哪些?
 hxagg2022-10-04 11:39:541条回答
hxagg2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 szksin 共回答了17个问题
szksin 共回答了17个问题 |采纳率100%- 钾 钙 钠 电石等
- 1年前
相关推荐
- 关于热机的物理选择题下面哪一个是正确的A 热值大的燃料比热值小的燃料完全燃烧时放出的热量多B 柴油机工作是,燃料燃烧没放
关于热机的物理选择题
下面哪一个是正确的
A 热值大的燃料比热值小的燃料完全燃烧时放出的热量多
B 柴油机工作是,燃料燃烧没放出1J热量,就可以得到1J的机械能
C 热机的效率越大,它的功率就越大
D 柴油机的效率一般比汽油机高,就是说完成相同的有用功,柴油机所有的燃料完全燃烧放出的能量比汽油机少
要一个个解释原因.
谢谢各位. elephantnj1年前1
elephantnj1年前1 -
 7vde 共回答了21个问题
7vde 共回答了21个问题 |采纳率81%选D
A 表面上是这样,可是你要看热值大的燃料被燃烧的程度,再来做比较
B 热机效率和机械效率是一样的,它们的值都<1
C 热机的效率是和功率无关的
D 他们所比较的,就是额外功,柴油机在做功冲程中,才运用燃料,所消耗的燃料也较少,额外功就比较少
懂了没?还可以再问我哦.1年前查看全部
- 如图所示,纸平面内O点有一离子源,不断向纸面内各个方向放出离子,已知离子速度V=5X10 6 m/s,荷质比 q m =
如图所示,纸平面内O点有一离子源,不断向纸面内各个方向放出离子,已知离子速度V=5X10 6 m/s,荷质比
=2X10 7 C/kg.空间中存在以粒子源为圆心垂直于纸面向里半径R 1 =0.5m的匀强磁场B 1 ,在这个磁场外面还存在着以粒子源为圆心垂直于纸面向外的圆环形匀强磁场B 2 ,外径为R 2 ,B 1 =B 2 =0.5T,(设粒子在运动过程中不相撞,忽略重力和粒子间的相互作用)求:q m
(1)粒子在B 1 中运动时的轨道半径为多少
(2)为了使粒子不离开磁场区域,R 2 的最小值
(3)求粒子从O点出发再回到O点的最短时间.
 rain不停1年前1
rain不停1年前1 -
 hanovo001 共回答了22个问题
hanovo001 共回答了22个问题 |采纳率81.8%1年前查看全部
- 下列变化过程中不能放出热量的是( )
下列变化过程中不能放出热量的是( )
A.Zn与盐酸反应
B.NaOH固体溶于水
C.铁粉生锈
D.NH4NO3固体溶于水 liubo1972001年前1
liubo1972001年前1 -
 fhifat 共回答了16个问题
fhifat 共回答了16个问题 |采纳率93.8%解题思路:根据物质溶于水的基本过程来考虑本题,知道常见放热物质、常见吸热物质,并能灵活运用.金属与酸反应放出热量;铁粉生锈属于缓慢氧化再考虑热量的变化.物质溶于水分为两个过程:构成物质的微粒向水中扩散的过程,这一过程需吸热,构成物质的微粒与水分子形成水和分子的过程,这一过程需放热,如果吸热大于放热则溶于水表现为吸热,如果吸热小于放热则溶于水表现为放热,如果吸热等于放热则表现为溶于水温度不变.常见的溶于水放热的有:浓硫酸、生石灰、氢氧化钠固体.常见吸热的有:硝酸铵.所以C答案氢氧化钠溶于水放热,D答案硝酸铵固体溶于水吸热,锌与盐酸反应发生的是化学变化放出热量,铁粉生锈属于缓慢氧化,缓慢氧化也能放出热量.
故选D.点评:
本题考点: 物质发生化学变化时的能量变化.
考点点评: 本题的易错点是铁粉生锈,不知道它属于缓慢氧化,也能放出热量,缓慢氧化、自燃、燃烧都能放出热量.1年前查看全部
- 25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( ) A.2
25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8kJ热量,表示该反应的热化学方程式正确的是( ) A.2H 2 (g)+O 2 (g)═2H 2 O(1)△H=-285.8kJ/mol B.2H 2 (g)+O 2 (g)═2H 2 O(1)△H=+571.6kJ/mol C.2H 2 (g)+O 2 (g)═2H 2 O(g)△H=-571.6kJ/mol D.H 2 (g)+
O 2 (g)═H 2 O(1)△H=-285.8kJ/mol1 2  雨后白合1年前1
雨后白合1年前1 -
 wgh1983 共回答了28个问题
wgh1983 共回答了28个问题 |采纳率82.1%A、因4g氢气燃烧生成液态水,放出热量571.6kJ,不是285.8kJ,故A错误;
B、因4g氢气燃烧生成液态水,放出热量571.6kJ,放热时焓变值为负值,故B错误;
C、因4g氢气燃烧生成液态水,不是气态水,放出热量571.6kJ,故C错误;
D、因2g氢气燃烧生成液态水,放出285.8kJ热量,放热时焓变值为负值,故D正确;
故选:D.1年前查看全部
- A、B同周期,B元素是该周期原子半径最大的元素,2.7gA与足量HCL反应放出标况下氢气3.36L
A、B同周期,B元素是该周期原子半径最大的元素,2.7gA与足量HCL反应放出标况下氢气3.36L
(1)A是 B是
(2)A、B最高价氧化物对应水化物相互反应的离子方程式为 想对大家说1年前8
想对大家说1年前8 -
 guanghua520 共回答了22个问题
guanghua520 共回答了22个问题 |采纳率86.4%算氢气是0.15mol 说明2.7gA能失去0.3mol电子,推算可能是Al 那么B原子半径最大的话,应该是Na 所以离子方程式为
Al(OH)3 +OH- ==AlO2- + 2H2O1年前查看全部
- 6.5g某金属与过量稀硝酸反应,并无气体放出,向反应后所得溶液中加入过量热碱溶液可放出一种气体,体积为560ml(标准状
6.5g某金属与过量稀硝酸反应,并无气体放出,向反应后所得溶液中加入过量热碱溶液可放出一种气体,体积为560ml(标准状况).求溶于硝酸的物质为何种金属.
怎么确定生成的是氨气? carpenters05061年前1
carpenters05061年前1 -
 我真得很饿 共回答了20个问题
我真得很饿 共回答了20个问题 |采纳率85%生成了氨气 所以氮降低了八价 共降了8*0.025=0.2 假定有该金属01摩尔 所以分子量为65 是锌 假如……错误 只能是锌1年前查看全部
- 煮过的肝脏研磨液与新鲜肝脏研磨液谁放出气泡快,为什么
 xxsjenny04291年前1
xxsjenny04291年前1 -
 sxzhi 共回答了19个问题
sxzhi 共回答了19个问题 |采纳率94.7%煮过的肝脏研磨液与新鲜肝脏研磨液,与过氧化氢反应,新鲜肝脏研磨液体放出气泡快.原因为肝脏中的过氧化物歧化酶为蛋白质,煮过后变性失效.1年前查看全部
- 一钢瓶内储有压缩气体,气体密度为ρ。若从瓶中放出一半质量的气体,则瓶内余下的气体密度会________,这是因为____
一钢瓶内储有压缩气体,气体密度为ρ。若从瓶中放出一半质量的气体,则瓶内余下的气体密度会________,这是因为___________。  kumane1年前1
kumane1年前1 -
 charles4494 共回答了12个问题
charles4494 共回答了12个问题 |采纳率83.3%变小;体积不变,质量减小1年前查看全部
- 问一道化学计算(有过程)将亚硫酸钠和硫化钠的混合物若干克配置成50g溶液,加入50克一定浓度,足量的盐酸,放出气体0.4
问一道化学计算(有过程)
将亚硫酸钠和硫化钠的混合物若干克配置成50g溶液,加入50克一定浓度,足量的盐酸,放出气体0.448L(标况),混合液为96.9克,求混合物中亚硫酸钠和硫化钠的物质的量 大家聚聚1年前1
大家聚聚1年前1 -
 clarkchung 共回答了19个问题
clarkchung 共回答了19个问题 |采纳率89.5%因为Na2SO3+2HCl=2NaCl+SO2↑+H2O ① ,
Na2S+2HCl=2NaCl+H2S↑②,
SO2+2H2S=3S↓+2H2O ,
因此,放出的气体是SO2或H2S.
根据质量守恒定律可知,m(S)+m(气体)=(50g+50g)-96.9g=3.1g,
(1)当放出的气体是SO2时,n1(SO2)=0.448L/(22.4L/mol)=0.02mol,
则m1(SO2)=0.02mol*64g/mol=1.28g,
所以m(S)=3.1g-1.28g=1.82g,
SO2 + 2H2S = 3S↓ + 2H2O
1mol~2mol~3*32g
n2(SO2)~n(H2S)~1.82g
列比例式解得:n2(SO2)=0.019mol,n(H2S)=0.038mol
故n(SO2)=n1(SO2)+n2(SO2)=0.039mol
根据化学方程式①知,n(Na2SO3)=n(SO2)=0.039mol,
根据化学方程式②知,n(Na2S)=n(H2S)=0.038mol.
(2)当放出的气体是H2S时,n1(H2S)=0.448L/(22.4L/mol)=0.02mol,
则m1(H2S)=0.02mol*34g/mol=0.68g,
所以m(S)=3.1g-0.68g=2.42g,
SO2 + 2H2S = 3S↓ + 2H2O
1mol~2mol~3*32g
n(SO2)~n2(H2S)~2.42g
列比例式解得:n(SO2)=0.0252mol,n2(H2S)=0.0504mol
故n(H2S)=n1(H2S)+n2(H2S)=0.0704mol
根据化学方程式①知,n(Na2SO3)=n(SO2)=0.0252mol,
根据化学方程式②知,n(Na2S)=n(H2S)=0.0704mol.
答:混合物中亚硫酸钠与硫化钠的物质的量为0.039mol、0.038mol,或混合物中亚硫酸钠与硫化钠的物质的量为0.0252mol、0.0704mol.1年前查看全部
- (1)已知含11.2g KOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46KJ的热量
(1)已知含11.2g KOH的稀溶液与1L0.1mol•L-1的H2SO4稀溶液反应放出11.46KJ的热量.请写出KOH的稀溶液与的H2SO4稀溶液发生中和反应,表示中和热的热化学方程式为KOH(aq)+[1/2]H2SO4(aq)=[1/2]K2SO4(aq)+H2O△H=-56.3kJ/molKOH(aq)+[1/2]H2SO4(aq)=[1/2]K2SO4(aq)+H2O△H=-56.3kJ/mol
(2)在相同条件下,下列两个反应的反应热分别为△H1和△H2表示:
①2H2 (g)+O2(g)=2H2O(g)△H1,
②2H2 (g)+O2(g)=2H2O(l)△H2,则△H1和△H2的关系为______. 一无所有DD1年前1
一无所有DD1年前1 -
 Goozla 共回答了21个问题
Goozla 共回答了21个问题 |采纳率81%解题思路:(1)根据酸碱的物质的量判断反应的情况,根据中和热的概念书写热化学方程式;
(2)根据物质的不同聚集状态判断反应热的大小.(1)n(KOH)=[11.2g/56g/mol]=0.2mol,n(H2SO4)=1L×0.1mol/L=0.1mol,二者恰好反应生成0.2mol水,放出11.46KJ的热量,
则生成1mol水时放出的热量为[1/0.2]×11.26kJ=56.3kJ,
所以表示中和热的热化学方程式为 KOH(aq)+[1/2]H2SO4(aq)=[1/2]K2SO4(aq)+H2O△H=-56.3kJ/mol,
故答案为:KOH(aq)+[1/2]H2SO4(aq)=[1/2]K2SO4(aq)+H2O△H=-56.3kJ/mol;
(2)物质的聚集状态不同,放出的热量不同,水蒸气液化时放热,则有|△H1|<|△H2|,由于氢气的燃烧为放热反应,
△H<0,则△H1>△H2,故答案为:△H1>△H2.点评:
本题考点: 中和热;热化学方程式.
考点点评: 本题考查中和热的计算以及反应热的大小比较,注意比较反应热时不能忽略“+”“-”.1年前查看全部
- 甲、乙两物体质量、初温都相同,甲的比热大于乙的比热.当它们放出相同的热量后,相互接触,接触以后内能的变化情况是( )
甲、乙两物体质量、初温都相同,甲的比热大于乙的比热.当它们放出相同的热量后,相互接触,接触以后内能的变化情况是( )
A. 甲的内能增加,乙的内能减少
B. 甲的内能减少,乙的内能增加
C. 甲的内能不变,乙的内能减少
D. 甲、乙的内能都不变 zhouhuogen1年前1
zhouhuogen1年前1 -
 conray 共回答了16个问题
conray 共回答了16个问题 |采纳率81.3%解题思路:解决此题要知道热传递发生的条件是要有温度差;质量相同的两种物质,放出相同的热量后,比热容小的物质降低的温度值大.因甲、乙两个不同的物体的质量、温度均相同,甲的比热容大于乙的比热容,所以当它们放出相同的热量后,乙降低的温度值比甲降低的大,所以甲的温度会高于乙的温度;
当它们接触后,温度高的甲会向温度低的乙传递热量,使甲的内能减少,乙的内能增加;
故选B.点评:
本题考点: 热传递.
考点点评: 解决此题要结合比热容知识和热传递的条件进行分析解答.1年前查看全部
- 有一种天然气的热值是3.6×10 7 J/m 3 ,完全燃烧2m 3 这种天然气,可放出的热量为______J.这些热量
有一种天然气的热值是3.6×10 7 J/m 3 ,完全燃烧2m 3 这种天然气,可放出的热量为______J.这些热量相当于热值为1.2×10 7 J/kg、质量为______kg的干木柴完全燃烧放出的热量.  妖精1681年前1
妖精1681年前1 -
 330700085 共回答了19个问题
330700085 共回答了19个问题 |采纳率78.9%2m 3 天然气完全燃烧放出的热量:
Q 放 =Vq 天然气 =2m 3 ×3.6×10 7 J/m 3 =7.2×10 7 J,
∵Q 放 =mq 干木柴 ,
∴放出这些热量需要完全燃烧干木柴的质量:
m=
Q 放
q 干木柴 =
7.2× 10 7 J
1.2× 10 7 J/kg =6kg.
故答案为:7.2×10 7 ;6.1年前查看全部
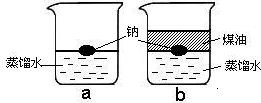
- 把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a所示).可以看到钠块浮在水面上,与水发生剧烈反应,反应放出的热量使钠
把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a所示).可以看到钠块浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,并使生成的氢气燃烧.
如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b所示),同样与水发生剧烈的反应,但是不发生燃烧.
1.金属钠的物理性质有_____ _____ ______
2.通过以上现象可以判断出化学反应伴随的现象之一____________.
3.图b中不发生燃烧现象说明煤油隔绝了_____.
 指着太阳说R1年前4
指着太阳说R1年前4 -
 万里追情 共回答了20个问题
万里追情 共回答了20个问题 |采纳率95%密度比水小(因为钠块浮在水面上)、熔点低(使钠熔成小球)、银白色金属(题目原话)
产生气体 (或 热量变化)
氧气(或 空气)(产生H2,所以有可燃物;放出的热量也没有减少.因此只能是缺少氧气)1年前查看全部
- 用电阻丝加热某种物质,得到如图所示的熔化图象.电阻丝的发热的功率为P,放出的热量有50%被该物质吸收,该物质的质量为m,
用电阻丝加热某种物质,得到如图所示的熔化图象.电阻丝的发热的功率为P,放出的热量有50%被该物质吸收,该物质的质量为m,则这种物质比热容的大小为(假设这种物质固态和液体的比热容相同)( )
 A. 小于
A. 小于P(t4−t1) 2m(t温3−t温1)
B. 大于P(t4−t1) 2m(t温3−t温1)
C. 等于P(t4−t1) 2m(t温3−t温1)
D. 等于P(t3−t2) 2mt温2  毒谷1年前1
毒谷1年前1 -
 jennny007 共回答了12个问题
jennny007 共回答了12个问题 |采纳率100%解题思路:电阻丝从时刻t1加热到时刻t4,放出的热量为Q放=P(t4-t1),
在这一段时间内,该物质的温度由t温1升高到t温3,由于固态和液态的比热容相同,所以该物质用来完成升温所吸收的热量为:Q吸1=cm(t温3-t温1),
但是从图象上看,该物质是晶体,在熔化过程中虽然吸热,但温度不变,所以在熔化过程中还吸收一部分热量,设为Q吸2,
所以该物质在这一段时间内,吸收的总热量为Q吸=Q吸1+Q吸2.
由于电阻丝放出的热量有50%被物质吸收,则有η=
,这样就可以判断该物质的比热容大小了.Q吸 Q放 电阻丝从时刻t1加热到时刻t4,放出的热量为Q放=P(t4-t1),
这一段时间内,该物质吸热的总热量可以分为两部分,一是物质温度升高吸收的热量,二是完成熔化吸收的热量,
则有:Q吸=cm(t温3-t温1)+Q熔
所以η=
Q吸
Q放=
cm(t温3−t温1)+Q熔
P(t4−t1)
所以该物质的比热容为:c=
50%•P(t4−t1)
m(t温3−t温1)+Q熔=
P(t4−t1)
2m(t温3−t温1)+2Q熔<
P(t4−t1)
2m(t温3−t温1 )
故选A.点评:
本题考点: 热量的计算;晶体的熔化和凝固图像;电功率.
考点点评: 该题难度较大,通过晶体的熔化图象考查了热量的计算、电功率、效率等知识,解题的关键是晶体的熔化过程还吸收了一部分热量,必须考虑进去.1年前查看全部
- 取10.5克表面已氧化了的铝片,投入到100毫升氢氧化钠溶液中,两者恰好完全反应,放出氢气6.72升
取10.5克表面已氧化了的铝片,投入到100毫升氢氧化钠溶液中,两者恰好完全反应,放出氢气6.72升
(标准状况下),则该氢氧化钠溶液的物质的量浓度是多少? 法网挥灰5271年前1
法网挥灰5271年前1 -
 俺系小小 共回答了21个问题
俺系小小 共回答了21个问题 |采纳率95.2%2 Al + 2OH- + 2H2O = 3H2↑+ 2AlO2-
2 2 3
x y 0.3mol
x =0.2mol
m Al =0.2*27=5.4g
mAl2O3=5.1g
y=0.2mol
Al2O3 + 6OH- = 2H2O + 2AlO2-
102g 6
5.1g z
z=0.3mol
c=n/V
=(0.3+0.2)/0.1L
=5mol/L1年前查看全部
- 有一瓶白色固体,取少量置于试管中加热,固体逐渐消失,放出水蒸气和其他两种气体,试管内除管口有少量水珠外,没有任何残留物.
有一瓶白色固体,取少量置于试管中加热,固体逐渐消失,放出水蒸气和其他两种气体,试管内除管口有少量水珠外,没有任何残留物.
取0.350g这种固体跟过量的碱液反应,生成一种能使湿润红色石蕊试纸变蓝的气体,这些气体正好能和30.0mL 0.100mol/L H2SO4完全反应;
令以0.350g该固体跟足量盐酸反应,放出一种无色、无臭的气体,将这些气体通入过量的澄清石灰水中,得到0.400g白色沉淀.
(1)计算0.350g固体中含有的阴离子和阳离子的物质的量.
(2)根据实验及计算结果确定白色固体是什么?写出判断的依据. lgvk001年前1
lgvk001年前1 -
 小雨落下 共回答了19个问题
小雨落下 共回答了19个问题 |采纳率94.7%解题思路:能使湿润红色石蕊试纸变蓝的气体为氨气,根据硫酸的物质的量计算出0.350g该固体中含有铵根离子的物质的量;与盐酸反应生成的无色、无味且能够使澄清石灰水变浑浊的气体为二氧化碳,生成的白色沉淀为碳酸钙,根据碳酸钙的物质的量可以计算出白色固体中含有碳酸根或者碳酸氢根离子的物质的量,根据加热固体后完全分解且没有残留物及阴阳离子的物质的量之比可以确定该白色固体为碳酸氢铵和碳酸铵混合物,铵根离子、碳酸根和碳酸氢根离子的物质的量列式计算出白色固体的组成.固体与碱液共热时放出能使湿润红色石蕊试纸变蓝的气体,证明有NH4+存在;
固体与酸反应所生成的无色无臭气体能与石灰水作用产生白色沉淀,证实固体中有CO32-或HCO3-;
n(CO32-或HCO3-)=n(CaCO3)=[0.400g/100g/mol]=0.004mol,n(NH4+)=2×n(H2SO4)=2×0.100mol/L×0.03L=0.006mol,
该固体中阴阳离子物质的量之比为:0.004mol:0.006mol=2:3,
该固体加热分解后,试管内没有任何残留物,以及生成除水蒸气之外只有两种气体,说明该固体中不含任何金属离子和其他酸根离子,
所以该固体为(NH4)2CO3和NH4HCO3的混合物,
设(NH4)2CO3的物质的量为x,NH4HCO3的物质的量为y,根据铵根离子和C原子守恒得:
x+y=0.004mol
2x+y=0.006mol,解得:
x=0.002mol
y=0.002mol,
(1)根据以上分析可知,0.350g固体中含有的阴离子和阳离子的物质的量分别为:n(CO32-)=0.002mol,n(HCO3-)=0.002mol,n(NH4+)=0.006mol,
答:0.350g固体中含有的阴离子和阳离子的物质的量为:n(CO32-)=0.002mol,n(HCO3-)=0.002mol,n(NH4+)=0.006mol;
(2)根据以上计算可知,该固体为(NH4)2CO3和NH4HCO3的混合物,
故答案为:该固体为(NH4)2CO3和NH4HCO3的混合物;该固体加热分解后,试管内没有任何残留物,以及生成除水蒸气之外只有两种气体,说明该固体中不含任何金属离子和其他酸根离子,所以该固体为(NH4)2CO3和NH4HCO3的混合物.点评:
本题考点: 几组未知物的检验.
考点点评: 本题考查了未知物检验,判断与计算相结合,对学生的综合能力要求更高,要注意对基础知识的整合,同时又要善于将题分解成若干个小题,各个击破,然后再综合考虑.1年前查看全部
- 体温计用水银作测温液体,是因为水银的比热容小,当温度变化相同时比其它物质吸收或放出的热量少,这样,一方面不会影响被测物体
体温计用水银作测温液体,是因为水银的比热容小,当温度变化相同时比其它物质吸收或放出的热量少,这样,一方面不会影响被测物体的温度,另一方面吸收相同热量时,比其它物质的温度改变量______,温度计的示数______.
 苏然然1年前3
苏然然1年前3 -
 jiahao03 共回答了18个问题
jiahao03 共回答了18个问题 |采纳率61.1%解题思路:液体温度计是根据液体的热胀冷缩的性质制成的,所用的液体必须是能够吸(放)热少,温度升高或降低的速度快,并且体积变化较大.液体温度计是根据液体的热胀冷缩的性质制成的.水银比热容较小,根据比热容的特点,它们吸收(或放出)较少的热量,就能够升高(或降低)较多的温度,温度变化比较明显;并且它们热膨胀较大,体积变化明显,便于人们观察.
故答案为:大;变化明显,易于观察.点评:
本题考点: 物理学方法;液体温度计的构造与工作原理.
考点点评: 要知道温度计的制作原理,会用比热容的特点和液体的热胀冷缩的性质去分析1年前查看全部
- 绿色植物在阳光照射下进行光合作用,吸收二氧化碳放出氧气。为了
绿色植物在阳光照射下进行光合作用,吸收二氧化碳放出氧气。为了
探究阳光对光合作用的影响。同学们分别在有阳光的白天和太阳未升起的凌晨,从种植蔬菜的大棚中收集空气,比较其中二氧化碳含量的多少。备选器材是:集气瓶,水槽,烧杯,玻璃片和水等。请回答:
(1)选用上述仪器设计一个简单的方法取出大棚内的空气样品。
(2)如果没有上述仪器,是否有其他简单方法,如何操作
(3)对取样后的气体如何进行检验?可以得到什么结论
问题补充:(找不到,帮找找)
 jkdfsfa1年前1
jkdfsfa1年前1 -
 czaj 共回答了16个问题
czaj 共回答了16个问题 |采纳率68.8%1,烧杯中装满水,进入大棚中,把水倒出来,烧杯中的气体即为空气样品。
2,用注射器抽取样品,或把一个完好的塑料袋中的空气挤出来,进入大棚后再张开塑料袋,袋中的气体即为空气样品。
3,把取出的相同体积的气体通入氢氧化钙溶液中,观察沉淀的多少,或把燃烧的蜡烛放进去,观察燃烧的时间长短。
结论:凌晨的气体产生的沉淀多,或蜡烛燃烧的时间短。说明含的二氧化碳多。证明晚上没有光合作用。1年前查看全部
- 小亮初次使用录音机录制了自己的歌声,他感到磁带放出的声音,不像自己的声音( ) A.磁带肯定错了 B.录音效果不好 C
小亮初次使用录音机录制了自己的歌声,他感到磁带放出的声音,不像自己的声音( ) A.磁带肯定错了 B.录音效果不好 C.自己听到声音的响度不同 D.听自己的声音主要是骨骼、肌肉传声,与通过空气传声的磁带声音的音色不同  飞敖1年前1
飞敖1年前1 -
 实实在在的ll 共回答了20个问题
实实在在的ll 共回答了20个问题 |采纳率85%用录音机把自己唱歌的声音录下来后,再播放出来觉得不象自己的声音,主要是因为:平常听自己的声音,依靠的主要传播途径是肌体、骨骼,听录音机声音依靠空气传播;虽然自己的音色没变,但在不同的介质中传播时,音色发生了变化.
故选D.1年前查看全部
- 将铜片、锌片和250mL稀硫酸组成的原电池,假设锌片只发生电化学腐蚀.当在铜片上放出6.72L(标准状况下)的气体时,H
将铜片、锌片和250mL稀硫酸组成的原电池,假设锌片只发生电化学腐蚀.当在铜片上放出6.72L(标准状况下)的气体时,H2S04恰好反应完全.
(1)该原电池的负极反应式为______
(2)原稀硫酸的物质的量浓度是______mol•L-1
(3)列式计算锌片减少的质量. ttQWERss1年前1
ttQWERss1年前1 -
 轩辕行素311 共回答了12个问题
轩辕行素311 共回答了12个问题 |采纳率100%解题思路:(1)该原电池中较活泼的金属锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,写出相应的电极反应式.
(2)锌和稀硫酸反应生成氢气,根据氢气体积和硫酸的关系式计算硫酸的物质的量浓度.
(3)根据锌和氢气之间的关系式计算锌减少的质量.(1)该原电池中较活泼的金属锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,正极上氢离子得电子生成氢气,所以负极上的电极反应式为:Zn-2e-=Zn2+,电池反应式为:Zn+2H+=Zn2++H2↑.
故答案为:Zn-2e-=Zn2+.
(2)设硫酸的物质的量浓度是C.
Zn+H2SO4=ZnSO4+H2↑
1mol22.4L
0.25Cmol 6.72L
C=1.2mol/L.
故答案为:1.2.
(3)设锌减少的质量为m.
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
m6.72L
m=19.5g
故答案为:19.5g.点评:
本题考点: 原电池和电解池的工作原理;氧化还原反应的计算.
考点点评: 本题考查了电极反应式的书写及物质的量的有关计算,难度不大,根据物质的物质的量之间的关系式来解答即可.1年前查看全部
- 原子核发生某种变化时,放出射线,说明
 爱oo1351年前3
爱oo1351年前3 -
 chenchen1313 共回答了30个问题
chenchen1313 共回答了30个问题 |采纳率90%此元素具有放射性,1年前查看全部
- 取质量为14.8g的碳酸钠和碳酸氢钠的固体混合物,与100ml2.50摩尔每升的盐酸恰好完全反应至不再放出气体.
取质量为14.8g的碳酸钠和碳酸氢钠的固体混合物,与100ml2.50摩尔每升的盐酸恰好完全反应至不再放出气体.
求原混合物中碳酸钠的质量分数.每一步最好都有解析, zlbandlj1年前1
zlbandlj1年前1 -
 怀化四中 共回答了20个问题
怀化四中 共回答了20个问题 |采纳率90%设:14.8中有碳酸钠xg,碳酸氢钠yg,x+y=14.8
0.100×2.50=2x/106+y/84.0=2x/106+(14.8-x)/84,解出x=10.6g,则y=4.2g
碳酸钠%=10.6/14.8=71.62%
碳酸氢钠%=4.2/14.8=28.38%1年前查看全部
- 0.05 mol X 能与足量的NaHCO3溶液反应放出22.4L CO2 (标准状况),则X的分子式为( ).A.c2
0.05 mol X 能与足量的NaHCO3溶液反应放出22.4L CO2 (标准状况),则X的分子式为( ).A.c2H2O4 B.C3H6O4 C.C4H8O4 D.C5H10O4
不好意思打错了,是0.5mol x 仲园老大1年前1
仲园老大1年前1 -
 黑点斑斑 共回答了16个问题
黑点斑斑 共回答了16个问题 |采纳率93.8%题目不对吧
因为n(CO2)=22.4/22.4=1mol,所以与NaHCO3反应生成CO2的羧基的量为
n(-COOH)=n(CO2)=1mol,又因为X的量为0.05 mol,
所以1mol/0.05mol=20,即1molX中含有20mol的羧基?
如果X的量为0.5mol,或者CO2为2.24L,1molX中含有2mol的羧基,那么答案为A
X为HOOCCOOH1年前查看全部
- 用惰性电极电解200mL1.5mol/L的Na2SO3溶液,一段时间后,测得两极放出的气体体积之和为20.16L(标准状
用惰性电极电解200mL1.5mol/L的Na2SO3溶液,一段时间后,测得两极放出的气体体积之和为20.16L(标准状况)
则在整个电解过程中转移的电子的物质的量为多少? jacky_cq7411021年前1
jacky_cq7411021年前1 -
 06级311MCT 共回答了16个问题
06级311MCT 共回答了16个问题 |采纳率87.5%设生成氧气的物质的量为X,则生成H2的物质的量为2X
用惰性电极电解活泼金属的含氧酸盐,就是电解水.
则X+2X=20.16L/22.4L/mol
解得X=0.3mol
在反应过程中每生成1摩尔O2失去4摩尔电子,
在整个电解过程中转移的电子的物质的量为0.3mol*4=1.2mol1年前查看全部
- 氢原子的跃迁氢原子从n=5跃迁到n=2时是辐射能量还是吸收能量?还有关于原子辐射放出的光子的波长跟辐射的能级有什么关系?
 Rodgu1年前1
Rodgu1年前1 -
 卡其鱼2006 共回答了11个问题
卡其鱼2006 共回答了11个问题 |采纳率81.8%能级越高 能量越大,所以是放出能量.光子的能量 E=hc/2λ 所以波长跟能量成反比,能级相差越大,波长越短1年前查看全部
- Ca(OH)2溶于水后会不会放出大量的热?
 褐色的貓1年前4
褐色的貓1年前4 -
 海的幻想 共回答了21个问题
海的幻想 共回答了21个问题 |采纳率85.7%理论上讲碱性物质溶于水都会放热,所以氢氧化钙溶于水也会放热.但是氢氧化钙是微溶于水的,所以不会发出大量的热.我试过,在试管中溶解根本感觉不到放热.1年前查看全部
- 足量的稀盐酸与镁、锌、铁反应,当放出的氢气质量相同时,参加反应的镁、锌、铁的质量比为
 黄山之斌1年前2
黄山之斌1年前2 -
 新新VS都都 共回答了17个问题
新新VS都都 共回答了17个问题 |采纳率88.2%因为题目中所有元素在化合物中均为+2价,所以,我们可以设金属为R,
R+2HCl=RCl2+H2↑
R 2
X m
X=Rm/2
可见,当氢气质量相同时,参加反应的金属质量与相对原子质量成正比.
结果:24:65:561年前查看全部
- 硝酸是什么气体溶于水,为何和金属反应不一定放出氢气?
 kundali1年前3
kundali1年前3 -
 forevernan 共回答了15个问题
forevernan 共回答了15个问题 |采纳率93.3%五氧化二氮,是硝酸酸酐不假,但常温下为白色固体,微溶于水,热水才全溶.融水后生成硝酸.
二氧化氮是红棕色气体,溶水生成硝酸.在无氧气条件下还会生成无色气体一氧化氮,有氧气时生成硝酸.以下为化学式:
4NO2+3O2+2H2O=4HNO3 3NO2+H2O=2HNO3+NO1年前查看全部
- 有四种元素:H O Na S写出两种均含四种元素的化合物相互反应放出气体的化学方程式
 Warmheart_0011年前4
Warmheart_0011年前4 -
 Soilphy 共回答了20个问题
Soilphy 共回答了20个问题 |采纳率95%NaHSO3 + NaHSO4 ==== Na2SO4 + H2O + SO2(气体)1年前查看全部
- PH咋算啊!(1),一块表面有氧化钠的金属钠5.4克,放入1000ml水中,放出1.12L氢气(标况),将此溶液稀释为2
PH咋算啊!
(1),一块表面有氧化钠的金属钠5.4克,放入1000ml水中,放出1.12L氢气(标况),将此溶液稀释为2L,此溶液的PH值( ).(2),PH=2的溶液其H+是PH=4的溶液的多少倍?将PH=2的盐酸和PH=10的氢氧化钠混合制PH=7,盐酸和氢氧化钠溶液的体积比?自学者 Paradise_flower1年前1
Paradise_flower1年前1 -
 younijiujingcai 共回答了12个问题
younijiujingcai 共回答了12个问题 |采纳率100%PH值就是氢离子,或氢氧根离子的浓度的对数,但我的对数学的太烂了,现在都忘的差不多了,
你自己算下吧1年前查看全部
- 有难度.一种黑色粉末A,加入盐酸后,粉末溶解得到浅绿色溶液,且有气体放出.将气体通入硫酸铜溶液产生黑色沉淀.在浅绿色溶液
有难度.
一种黑色粉末A,加入盐酸后,粉末溶解得到浅绿色溶液,且有气体放出.将气体通入硫酸铜溶液产生黑色沉淀.在浅绿色溶液中滴入氯水,溶液转为棕黄色,写出以上实验中各步反应的化学方程式. 我是真真1年前5
我是真真1年前5 -
 applede3233 共回答了13个问题
applede3233 共回答了13个问题 |采纳率92.3%FeS+2HCL=FeCL2+H2S(气体)
H2S+CuSO4=CuS(沉淀)+H2SO4
2FeCL2+CL2=2FeCL31年前查看全部
- 电解硫酸钠,pH升高的到底是阴极还是阳极,阴极由于有氢气放出,氢离子减少,但根据异性相吸原理,氢氧根离子会到阳极去,所以
电解硫酸钠,pH升高的到底是阴极还是阳极,阴极由于有氢气放出,氢离子减少,但根据异性相吸原理,氢氧根离子会到阳极去,所以本人感到纠结,求高手赐教.
 雪域凌峰1年前4
雪域凌峰1年前4 -
 hch20911 共回答了23个问题
hch20911 共回答了23个问题 |采纳率91.3%阳极反应 2H2O -4e ==O2 +4H+
阴极反应, 4H+ +4e==2H2
阳极产生H+ pH降低
阴极消耗H+ pH升高
OH-会运动到阳极去,但是运动去的OH-要少于产生的H+
如果有盐桥的话那就更少了.因此不能马上中和,就显示酸碱性了.1年前查看全部
- 200ml0.1mol/lba(oh)2溶液和0.2mol/300ml盐酸混合,放出的热量是多少.
 007_yyc1年前1
007_yyc1年前1 -
 filter999 共回答了24个问题
filter999 共回答了24个问题 |采纳率91.7%0.1*0.2*2*57 kJ1年前查看全部
- 化学反应中的热量变化问题甲烷燃烧放出热量,水的分解要吸收热量,试从化学键变化的角度分析其原因.
 蜡笔小哈1年前1
蜡笔小哈1年前1 -
 gwjawj 共回答了18个问题
gwjawj 共回答了18个问题 |采纳率94.4%甲烷燃烧断裂化学键所要的能量小于形成新化学键放出的能量所以放出热量
水的分解断裂化学键所要的能量大于形成新化学键放出的能量所以吸收热量1年前查看全部
- 一组蓄电池输出电压为12V若输出电能4200000J则放出电荷量为多少
 qamshfufk1年前1
qamshfufk1年前1 -
 geyafei 共回答了16个问题
geyafei 共回答了16个问题 |采纳率93.8%W=UIt,It=W/U=4200000/12库伦1年前查看全部
- 相同质量的钠,镁,铝与足量的盐酸反应时放出氢气的体积比是?急,月快愈好
 snifferback1年前1
snifferback1年前1 -
 pao300 共回答了21个问题
pao300 共回答了21个问题 |采纳率85.7%生成1mol氢气需钠2mol(46g) 镁1mol(24g) 铝2/3mol(18g)
相同物质的量的钠、镁、铝与足量盐酸反应时放出H2的体积比为 (1/2):(1/1):[1/(2/3)]=1:2:3
相同质量的钠、镁、铝与足量盐酸反应时放出H2的体积比是 (1/46):(1/24):(1/18)=108:207:2761年前查看全部
- 为什么水蒸汽液化时要放出热量
 az5391年前1
az5391年前1 -
 yanyurenjia 共回答了15个问题
yanyurenjia 共回答了15个问题 |采纳率100%因为事实就是这样
水蒸气液化的瞬间温度不变,则分子的平均动能可以不变,但状态变化分子间距离减小,势能减小,放出热量,遵守能量守恒1年前查看全部
- 有一根烧红的铁钉质量1.5g温度降低到20度,放出热量是5.38×10²j,铁钉的初温是多少
有一根烧红的铁钉质量1.5g温度降低到20度,放出热量是5.38×10²j,铁钉的初温是多少
 Hogwatts1年前1
Hogwatts1年前1 -
 langhande 共回答了18个问题
langhande 共回答了18个问题 |采纳率100%538/(1.5×0.46)+20=800度1年前查看全部
- 一种白色粉末由碳酸氢钠和碳酸钠混合而成,称取混合物4.42g,加热至恒重,将放出的气体通过过量的石灰水,得白色沉淀2g,
一种白色粉末由碳酸氢钠和碳酸钠混合而成,称取混合物4.42g,加热至恒重,将放出的气体通过过量的石灰水,得白色沉淀2g,加热后的残渣与某浓度盐酸30mL恰好完全作用,求(1)原混合物中碳酸氢钠的质量;(2)盐酸的物质的量浓度.
 绿岛孤舟1年前2
绿岛孤舟1年前2 -
 不回头的天使 共回答了16个问题
不回头的天使 共回答了16个问题 |采纳率100%CO2~2NaHCO3~CaCO3~2HCl 168 100 73 x 2g y x=3.36g,y=1.46g=0.02mol 碳酸氢钠3.36g 碳酸钠1.06g,即0.01mol Na2CO3~2HCl 0.01mol~0.02mol 所以碳酸钠消耗盐酸0.02mol,碳酸钙消耗盐酸0.02mol C=0.04/0.03=1.3mol/L 2:2NaHCO3(加热)====Na2CO3+H2O+CO2 CO2+Ca(OH)2====CaCO3+H2O 列式先算出CO2的质量为0.88克,再由CO2的质量算出NaHCO3的质量为3.36克 CaCO3+2HCl====CaCl2+CO2+H2O 列式算出HCl的物质的量为0.04mol,然后再算物质的量浓度0.04/0.03约为1.3mol/L1年前查看全部
- 质量为m的某种物质,温度升高Δt时吸收热量为Q,当它的温度降低Δt’时,放出的热量等与多少?
 晶城之恋1年前3
晶城之恋1年前3 -
 现实的打击 共回答了13个问题
现实的打击 共回答了13个问题 |采纳率92.3%Q=cm△t
so.
c=Q/m△t
Q2=cmΔt’=QΔt’/Δt1年前查看全部
- 焦碳的燃烧值是3×107焦/千克,其含义是______.完全燃烧300克焦碳,放出的热量是______焦.
 你的小跟班1年前1
你的小跟班1年前1 -
 曉艾 共回答了19个问题
曉艾 共回答了19个问题 |采纳率78.9%解题思路:根据对热值物理意义的掌握分析答题;已知焦炭质量与热值,应用热值公式可以求出焦炭完全燃烧释放的热量.焦碳的燃烧值是3×107焦/千克,其含义是:1kg焦炭完全燃烧释放的热量是3×107J;
300g=0.3kg焦炭完全燃烧释放的热量:Q=mq=3×107J/kg×0.3kg=9×106J;
故答案为:1kg焦炭完全燃烧释放的热量是3×107J;9×106.点评:
本题考点: 燃料的热值.
考点点评: 本题考查了热值的物理意义、求焦炭燃烧释放的热量,是一道基础题,掌握基础知识即可正确解题.1年前查看全部
- 在能使铝放出氢气的溶液中,钾离子、钠离子、氯离子和硝酸根离子能否大量共存?
 老唐自得1年前6
老唐自得1年前6 -
 YANG_0524 共回答了17个问题
YANG_0524 共回答了17个问题 |采纳率100%不一定,是可能共存,不能一定共存.
能使铝放出氢气可能是酸性也可能是碱性.
如果是酸性,不会生成H2,生成的是氮氧化物,不可能.
如果是碱性可以共存.1年前查看全部
- X,Y两种元素的原子,它们分别获得一个电子后,都能形成稀有气体原子的电子层结构,此过程中X放出的能量大于Y,下列推断不正
X,Y两种元素的原子,它们分别获得一个电子后,都能形成稀有气体原子的电子层结构,此过程中X放出的能量大于Y,下列推断不正确的是()
A、X¯的还原性强于Y¯
B、X¯的还原性弱于Y¯
C、Y的氧化性强于X
D、Y的氧化性弱于X
(我只是有一点不明白:老师上课时在黑板上分析此题时写了KLM上分别标2、4、6,他是怎么解得啊?希望大家能用这种方法解答~
246可能是关于能量的吧? 十样蛮笺1年前1
十样蛮笺1年前1 -
 齐齐yy1 共回答了13个问题
齐齐yy1 共回答了13个问题 |采纳率92.3%你们老师讲得不明白,还是听我来讲吧.我也是中学化学老师的.
X放出的能量大于Y
→X更易得电子
→非金属性:X>Y
→B、D正确.1年前查看全部
- 关于铜片和稀硫酸的反应铜粉和稀硫酸加热不反应,但加入化合物X后,溶液逐渐变色.且质量增加,还放出气体,则X可能是?氯化钠
关于铜片和稀硫酸的反应
铜粉和稀硫酸加热不反应,但加入化合物X后,溶液逐渐变色.且质量增加,还放出气体,则X可能是?
氯化钠 硝酸钾 硫酸钠 碳酸钠? 长青131年前2
长青131年前2 -
 korla31g 共回答了21个问题
korla31g 共回答了21个问题 |采纳率81%硝酸钾
NO3-在酸性环境下具有硝酸性质,具有强氧化性
故加入硝酸钾后,会发生氧化还原反应
3Cu+8H+ +3NO3-=2Cu2+ +2NO+4H2O1年前查看全部
- 关于氢化锂特征A.液态时是电的良导体 B.Hˉ具强还原性,遇 H+ 时可反应放出氢气.C.是非电解质
 thindog1年前1
thindog1年前1 -
 ychoo 共回答了25个问题
ychoo 共回答了25个问题 |采纳率92%氢化锂是类盐氢化物,是离子化合物. A.液态时存在自由移动的H-和Li+离子,能导电,属于电解质. B也正确. C错误1年前查看全部
- 某化工厂排出的澄清废水中,加入BaCl2溶液产生白色沉淀,再加入足量稀硝酸,沉淀部分溶解,并放出能使澄清石灰水变浑浊的气
某化工厂排出的澄清废水中,加入BaCl2溶液产生白色沉淀,再加入足量稀硝酸,沉淀部分溶解,并放出能使澄清石灰水变浑浊的气体,下列说法正确的是:
1.废液中一定有CO3(2-) 2.废液中有H2SO4
3.废液中一定有Ag+ 4.废液中一定有SO4(2-)
答案是1和4,可是我不明白为什么说1和3不行呢? lyyong12341年前1
lyyong12341年前1 -
 doudoufly 共回答了22个问题
doudoufly 共回答了22个问题 |采纳率90.9%“俊狼猎英”团队为您解答.
分析:通过“再加入足量稀硝酸,沉淀部分溶解,并放出能使澄清石灰水变浑浊的气体”可知,溶液中一定含有CO3(2-),那么如果有CO3(2-)的话,就一定没有H2SO4和Ag+,因为CO3(2-)和酸是不能共存的(反应会产生二氧化碳),CO3(2-)和Ag+结合会变成碳酸银沉淀,如果没有Ag+的话,那么再加入足量稀硝酸,沉淀部分溶解,说明有不溶于硝酸的沉淀,就不是氯化银,而是硫酸钡沉淀了,所以溶液中一定含有SO4(2-),明白么?不明白可以追问!1年前查看全部
- 食物燃烧时也会生成二氧化碳和水,同时放出热量,这与呼吸作用相类似,你能比较两者的差异吗?
 mickeyyin1年前2
mickeyyin1年前2 -
 baggio1971 共回答了17个问题
baggio1971 共回答了17个问题 |采纳率100%燃烧是一种剧烈氧化的过程,能量以热能形式为主散发掉
呼吸作用是一种温和复杂的氧化过程
呼吸作用产生的能量除了部分以热能散失外,还可以转化成其它生物体可以利用的储能形式(ATP)
呼吸作用是在酶的催化和调节控制下进行的1年前查看全部
- 加热94.8g 高猛酸钾放出的氧气与多少质量的双氧水分解生成的氧气质量相等?
 aa的aass1年前2
aa的aass1年前2 -
 right_t 共回答了25个问题
right_t 共回答了25个问题 |采纳率92%设X克双氧水,依照化学方程式;
2KMnO4---O2---2H2O2
158 34
94.8 X
X=20.41年前查看全部
- 向一定量的Fe,FeO,Fe2O3的混合物中,加入100ml 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(
向一定量的Fe,FeO,Fe2O3的混合物中,加入100ml 1mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准状况)的气体.所得溶液中,加入KSCN溶液无血红色出现,那么若用足量的CO在高温下还原相同质量的此混合物,能得到铁多少克?
 鸿霞饲料1年前3
鸿霞饲料1年前3 -
 的美丽 共回答了18个问题
的美丽 共回答了18个问题 |采纳率94.4%反应后溶液加硫氰化钾没有血红色,说明没有三价铁离子.即溶液中铁元素全部以+2价亚铁离子存在,阴离子都是氯离子,物质的量0.1mol,则铁元素物质的量0.05mol,质量2.8g1年前查看全部
大家在问
- 1if it ——tomorrow.i will go by car A rain b will rain C rains
- 2某班男生是女生的12|13,女生人数是全班人数的( )%?
- 3当固体或气体溶于水后,液体物质被称为
- 4如图示正常生理条件下动物肌肉细胞细胞膜转运部分物质示意图,下列与图中信息相符的说法是( )
- 5ABCD 4人举行足球循环赛,每2人赛1场,胜利得3分,平局1分,负0分.已经知道:
- 6七层,几乎能买到所有想买的东西.这句英文翻译是什么?
- 7已知圆(x-2)2+y2=9和直线y=kx交于A,B两点,O是坐标原点,若向量OA+向量OB=0向量,则向量AB的模=?
- 8用三种不同的关联词,将下列的两句话连接起来
- 9三个5瓦的节能灯亮还是一个15瓦的灯亮?三个5瓦和一个15瓦的灯相等时间...
- 10探究分析:甲、乙两文中和课文《从百草园到三味书屋》中对百草园景物描写的方法和出发点有什么不同?
- 11如图,抛物线y=ax2+bx-4a经过A(-1,0)、C(0,4)两点,与x轴交于另一点B.
- 12继续不断尝试,你会成功的.Try to do it_ _ _ _,you'll successe
- 13解这些词的词义家徒四壁:徒:(这个字的意思)全词的意思:一袭破杉:袭:(这个字的意思)全词的意思:奋笔疾书:疾:(这个字
- 14解方程1- 2x-56 = 3-x4
- 15抛物线y2=4x上一点M到准线的距离为3,则点M的横坐标x为( )

