把几小块木炭放在球形管中,按下图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热
 陈陈辰2022-10-04 11:39:541条回答
陈陈辰2022-10-04 11:39:541条回答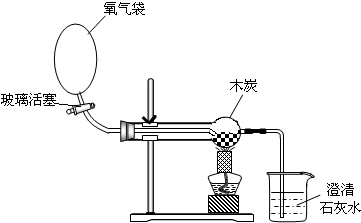 把几小块木炭放在球形管中,按下图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热,木炭同样不燃烧,此时打开玻璃活塞,氧气立即进入球形管,则可以观察到的现象是______.由此得出的结论是:①______;②______.
把几小块木炭放在球形管中,按下图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热,木炭同样不燃烧,此时打开玻璃活塞,氧气立即进入球形管,则可以观察到的现象是______.由此得出的结论是:①______;②______. 
已提交,审核后显示!提交回复
共1条回复
 沧海一诗笑 共回答了8个问题
沧海一诗笑 共回答了8个问题 |采纳率100%- 解题思路:据题意可知木炭燃烧必须同时具备温度达到物质的着火点和与氧气接触两个条件.燃烧是一种剧烈的发光、发热的化学反应.
木炭剧烈燃烧,发出白光,放热,小烧杯中澄清石灰水变浑浊.
①木炭燃烧生成了二氧化碳(CO2能使澄清石灰水变浑浊).
②可燃物燃烧需要同时满足两个条件:一是可燃物要与O2接触;二是温度达到该物质的着火点.
故答案为:木炭剧烈燃烧,发出白光,澄清石灰水变浑浊①木炭燃烧生成了二氧化碳(CO2能使澄清石灰水变浑浊).②可燃物燃烧需要同时满足两个条件:一是可燃物要与O2接触;二是温度达到该物质的着火点点评:
本题考点: 燃烧的条件与灭火原理探究.
考点点评: 本题以实验探究的形式考查了物质燃烧的条件,燃烧的现象,以及燃烧的产物二氧化碳使澄清石灰水变浑浊的现象. - 1年前
相关推荐
- 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答下列问题:
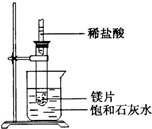
①实验中试管内观察到的现象是______.
②产生该现象的原因是______.
③写出有关反应的离子反应方程式______. fpfba1年前2
fpfba1年前2 -
 yumiao013 共回答了26个问题
yumiao013 共回答了26个问题 |采纳率100%解题思路:如图所示的实验中,所试管内滴入稀盐酸,盐酸与镁剧烈反应放出氢气,同时反应放出的热量使饱和石灰水溶液温度升高,温度升高氢氧化钙溶解度减小,饱和溶液析出固体氢氧化钙而使烧杯中的溶液变浑浊.①镁与盐酸剧烈反应,可观察到产生大量气体,镁片逐渐溶解,
故答案为:镁片上有大量气泡,镁片逐渐溶解;
②镁与盐酸剧烈反应,产生氢气,
故答案为:镁与盐酸反应产生H2;
③镁与盐酸发生置换反应,生成氯化镁和氢气,反应的离子方程式为:Mg+2H+=Mg2++H2↑,
故答案为:Mg+2H+=Mg2++H2↑.点评:
本题考点: 吸热反应和放热反应.
考点点评: 本题考查金属与酸的反应,该反应为放热反应,难度不大.要注意氢氧化钙的溶解度随温度升高而减小,但本题没考到这一点,是一点创新.1年前查看全部
- 向盛满二氧化氮的集气瓶中投入几小块木炭,会发生什么现象?
向盛满二氧化氮的集气瓶中投入几小块木炭,会发生什么现象?
好像是红棕色消失,发生了什么化学反应?瓶内气压为什么会降低?
为什么红棕色会消失咧? miaoguoping1年前1
miaoguoping1年前1 -
 老鼠HS 共回答了20个问题
老鼠HS 共回答了20个问题 |采纳率80%发生了物理变化
木炭多孔结构 表面积大 吸附能力强 会吸附二氧化氮分子 所以红棕色消失
如果集气瓶密封 压强会减小 因为气体分子减少 体积不变 压强减小1年前查看全部
- 如图所示,把试管放入盛25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.
如图所示,把试管放入盛25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.
试完成下列问题(提示:氢氧化钙的溶解度随温度升高而降低)
(1)实验中观察到的现象是______;
(2)产生上述现象的原因是______.
(3)写出有关反应的离子方程式______.
(4)由实验推知,MgCl 2 溶液和H 2 的总能量______(填“大于”“小于”或“等于”)镁片的盐酸的总能量.
 141加菲1年前1
141加菲1年前1 -
 ren1978 共回答了26个问题
ren1978 共回答了26个问题 |采纳率88.5%(1)镁与盐酸剧烈反应,可观察到产生大量气体,反应放出热量使饱和溶液温度升高,析出固体溶质,观察到溶液变浑浊,故答案为:镁片上有大量气泡,镁片逐渐溶解,烧杯中溶液变浑浊;(2)镁与盐酸剧烈反应,产生...1年前查看全部
- (2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图
(2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:

(1)实验中观察到的明显现象有:①剧烈反应,有气泡产生;②镁条逐渐溶解;③______.
(2)产生上述现象③的原因是:
①______;
②______. 水的缘故1年前2
水的缘故1年前2 -
 haikouyong 共回答了19个问题
haikouyong 共回答了19个问题 |采纳率84.2%解题思路:根据物质的性质进行分析,氢氧化钙的溶解度随温度的升高而减小,金属与酸的反应是放热反应.金属镁与盐酸反应放出热量,导致石灰水的温度升高,石灰水中的溶质为氢氧化钙,氢氧化钙的溶解度随温度的升高而减小,故会析出氢氧化钙溶质,导致石灰水变浑浊.
故答案为:
(1)①石灰水变浑浊;
(2)①镁与盐酸反应放出热量,导致石灰水的温度升高;②氢氧化钙的溶解度随温度的升高而减小.点评:
本题考点: 物质发生化学变化时的能量变化;固体溶解度的影响因素.
考点点评: 本题考查了物质间反应时的能量变化以及影响物质溶解度的因素,完成此题,可以依据已有的知识进行.1年前查看全部
- 实验室制取CO 2 一般有以下几个步骤: ①向长颈漏斗中注入稀盐酸 ②向容器放入几小块石灰石 ③按要求组装仪器 ④检查装
实验室制取CO 2 一般有以下几个步骤: ①向长颈漏斗中注入稀盐酸 ②向容器放入几小块石灰石 ③按要求组装仪器 ④检查装置的气密性 ⑤收集气体
下列顺序排列正确的是[ ]A.①②③④⑤
B.④③①②⑤
C.③④②①⑤
D.③④①②⑤ 婊要三个ff还要1年前1
婊要三个ff还要1年前1 -
 飞舞V云端 共回答了16个问题
飞舞V云端 共回答了16个问题 |采纳率87.5%C1年前查看全部
- (2003•哈尔滨)如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块木炭,最终观察到红棕色______(填“变深”
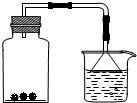 (2003•哈尔滨)如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块木炭,最终观察到红棕色______(填“变深”或“消失”或“不变”),漏斗中液面______(填“上升”或“下降”或“不变”).其原因为:木炭具有______作用,使瓶中气体压强______外界大气压.
(2003•哈尔滨)如图所示,向盛有红棕色二氧化氮气体的集气瓶里投入几小块木炭,最终观察到红棕色______(填“变深”或“消失”或“不变”),漏斗中液面______(填“上升”或“下降”或“不变”).其原因为:木炭具有______作用,使瓶中气体压强______外界大气压.  自作very聪明1年前1
自作very聪明1年前1 -
 mz木子 共回答了14个问题
mz木子 共回答了14个问题 |采纳率100%解题思路:木炭具有吸附性进行分析可得集气瓶内气体变为无色;结合物理知识“瓶中的压强小于外界大气压强”分析可知水在外界大气压强下会被压进漏斗.木炭具有疏松多孔的结构,具有吸附性,将几块经过烘烤并冷却后的木炭,投入到盛满红棕色二氧化氮气体的集气瓶中,轻轻摇动,NO2气体被活性炭吸附,所以集气瓶内气体红棕色逐渐消失;由于瓶中的压强小于外界大气压强,所以水在外界大气压强下会被压进漏斗,即漏斗中的液面上升.
故答案为:消失;上升;吸附;小于.点评:
本题考点: 碳单质的物理性质及用途;反应现象和本质的联系.
考点点评: 解答本题要掌握活性炭的性质方面的知识,只有掌握了木炭的性质才能正确的判断木炭的作用;还考查了物理知识和化学知识融汇贯通的综合能力.1年前查看全部
- (2002•荆门)把几小块木炭放在球形管中,按右图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,
(2002•荆门)把几小块木炭放在球形管中,按右图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热,木炭同样不燃烧,此时打开玻璃活塞,氧气立即进入球形管,则可以观察到的现象是______.由此得出的结论是
①______;
②______.
 rpb0aft1年前1
rpb0aft1年前1 -
 hero-liu 共回答了10个问题
hero-liu 共回答了10个问题 |采纳率80%解题思路:根据单独通氧气或单独加热都不会加热进行分析;根据反应的现象分析得到的结论.单独通氧气和单独加热都不会反应,但是通氧气加热后,可燃物温度达到了着火点又有氧气参加,所以,可以燃烧,生成的二氧化碳会使石灰水变浑浊,
故答案为:木炭剧烈燃烧,澄清石灰水变浑浊;燃烧既需要氧气,可燃物又必须达到着火点;二氧化碳会与氢氧化钙生成碳酸钙沉淀.点评:
本题考点: 探究氧气的性质;氧气与碳、磷、硫、铁等物质的反应现象.
考点点评: 在解此类题时,首先分析题中考查的问题,然后根据学过的知识和题中的装置进行分析解答.1年前查看全部
- 实验室制取CO2一般有几个步骤:①检查装置的气密性,按要求装配好仪器;②向长颈漏斗中注入酸液;③向锥形瓶放人几小块的大理
实验室制取CO2一般有几个步骤:①检查装置的气密性,按要求装配好仪器;②向长颈漏斗中注入酸液;③向锥形瓶放人几小块的大理石;④收集气体.下列操作顺序正确的是( )
A.②①④③
B.①③②④
C.①④②③
D.②③④① 我恨燃烧1年前1
我恨燃烧1年前1 -
 丫丫在上海 共回答了19个问题
丫丫在上海 共回答了19个问题 |采纳率94.7%解题思路:根据制取二氧化碳的步骤(连→查→加→倒→定→收)进行分析解答即可.制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集).
故①③②④.
故选:B.点评:
本题考点: 制取二氧化碳的操作步骤和注意点.
考点点评: 本题难度不大,掌握制取二氧化碳的操作步骤和注意事项是正确解答本题的关键.1年前查看全部
- 向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,为什么红棕色会消失?
向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,为什么红棕色会消失?
除了红棕色消失外,还会有什么现象?木炭是烘烤过的,有什么特别吗? 螃蟹11年前4
螃蟹11年前4 -
 festamma 共回答了19个问题
festamma 共回答了19个问题 |采纳率100%烘烤后的木炭相当于品质较低的活性炭,表面积很大,可以吸附多种有毒气体,二氧化氮的红棕色消失1年前查看全部
- (2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图
(2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:

(1)实验中观察到的明显现象有:①剧烈反应,有气泡产生;②镁条逐渐溶解;③______.
(2)产生上述现象③的原因是:
①______;
②______. 三姑姑1年前3
三姑姑1年前3 -
 娃哈哈p7va 共回答了21个问题
娃哈哈p7va 共回答了21个问题 |采纳率85.7%解题思路:根据物质的性质进行分析,氢氧化钙的溶解度随温度的升高而减小,金属与酸的反应是放热反应.金属镁与盐酸反应放出热量,导致石灰水的温度升高,石灰水中的溶质为氢氧化钙,氢氧化钙的溶解度随温度的升高而减小,故会析出氢氧化钙溶质,导致石灰水变浑浊.
故答案为:
(1)①石灰水变浑浊;
(2)①镁与盐酸反应放出热量,导致石灰水的温度升高;②氢氧化钙的溶解度随温度的升高而减小.点评:
本题考点: 物质发生化学变化时的能量变化;固体溶解度的影响因素.
考点点评: 本题考查了物质间反应时的能量变化以及影响物质溶解度的因素,完成此题,可以依据已有的知识进行.1年前查看全部
- 把试管方入盛有25摄食度的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管...
把试管方入盛有25摄食度的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管...
把试管方入盛有25摄食度的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中会什么现象,原理是什么 梦缘芭比1年前2
梦缘芭比1年前2 -
 嘻哈天堂 共回答了24个问题
嘻哈天堂 共回答了24个问题 |采纳率87.5%会看到澄清的石灰水变浑浊,这是因为Mg+2HCl=MgCl2+H2↑是放热反应,Ca(OH)2的溶解度随着温度的升高而降低,所以会出现浑浊.
由实验得MgCI2溶液和H2的总能量小于镁片和盐酸的总能量.
放热反应,生成物的总能量小于反应物的总能量.
MgCI2溶液和H2的总能量小于镁片和盐酸的总能量1年前查看全部
- 把几小块木炭放在球形管中,按右图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热
把几小块木炭放在球形管中,按右图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热,木炭同样不燃烧,此时打开玻璃活塞,氧气立即进入球形管,则可以观察到的现象是______.由此得出的结论是
①______;
②______.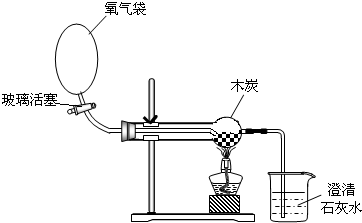
 sanzhxl1年前1
sanzhxl1年前1 -
 xuebin530 共回答了24个问题
xuebin530 共回答了24个问题 |采纳率95.8%单独通氧气和单独加热都不会反应,但是通氧气加热后,可燃物温度达到了着火点又有氧气参加,所以,可以燃烧,生成的二氧化碳会使石灰水变浑浊,
故答案为:木炭剧烈燃烧,澄清石灰水变浑浊;燃烧既需要氧气,可燃物又必须达到着火点;二氧化碳会与氢氧化钙生成碳酸钙沉淀.1年前查看全部
- 某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量
某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试回答:甲同学 乙同学 丙同学 丁同学 所取石灰石样品质量(g) 10.0 10.0 10.0 10.0 加入盐酸的质量(g) 20.0 30.0 45.0 50.0 剩余固体的质量(g) 6.0 4.0 1.0 1.0
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还剩余______(填“是”或“否”),样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?所用稀盐酸的溶质质量分数为多少?(计算结果精确到小数点后两位). Jessie希1年前1
Jessie希1年前1 -
 xuping609609 共回答了23个问题
xuping609609 共回答了23个问题 |采纳率95.7%解题思路:(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②由图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式就可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量,所用稀盐酸的溶质质量分数.(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②样品中碳酸钙的质量分数为[10g−1g/9g]×100%=90%;
(2)设生成二氧化碳的质量为x,所用稀盐酸的溶质质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
1007344
10g×90%y x
[100/44=
10g×90%
x]
x=3.96g.
[100/73=
10g×90%
y]
y=6.57g
所用稀盐酸的溶质质量分数
6.57g
45g×100%=14.6%
答案:
(1)否 90%
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳3.96克,所用稀盐酸的溶质质量分数为14.6%点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生对完全反应的认识,以及利用化学方程式进行计算的能力.考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- (2005•常德)某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0
(2005•常德)某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0g样品,将60.0g稀盐酸分四次加入,测量的有关数据见下表(已知样品中的杂质不溶于水,且不与稀酸盐反应).
求:(1)样品中碳酸钙的质量分数;加入稀盐酸的次序 1 2 3 4 加入稀盐酸的质量(g) 15.0 15.O 15.0 15.0 剩余固体的质量(g) 7.O 4.O 1.O 1.O
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳多少克?(计算结果精确到小数点后两位) 报告xx发现小妞1年前1
报告xx发现小妞1年前1 -
 rainlily000 共回答了16个问题
rainlily000 共回答了16个问题 |采纳率81.3%(1)由图表数据可知,完全反应后剩余杂质质量为lg,则样品中CaCO3的质量分数为:
10g−1g
10g×100%=90%;
(2)设可产生二氧化碳的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
9g x
∴
100
44=
9g
x,
解之得:x=3.96g.
答:(1)样品中碳酸钙的质量分数为90%;
(2)10.0g该样品与足量稀盐酸反应后可产生二氧化碳3.96g.1年前查看全部
- 我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分
我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表: 甲同学 乙同学 丙同学 丁同学 所取石灰石样品质量(g) 10.0 10.0 10.0 10.0 加入盐酸的质量(g) 20.0 30.0 45.0 50.0 剩余固体的质量(g) 6.0 4.0 1.0 1.0试问答:(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余_____ _____ (填“是”或“否”),样品中碳酸钙的质量分数是_______________.(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)问题补充 2010-11-21 09:31拜托,要过程啊~~~~~~~~~~
 wiwi_12211年前1
wiwi_12211年前1 -
 ying07 共回答了15个问题
ying07 共回答了15个问题 |采纳率100%(1)①由图表可知,丙同学加入45g盐酸与10.0g样品反应后剩余固体质量与丁同学加入50g盐酸反应后剩余固体的质量相等,故可判断,丙同学的实验是完全反应.盐酸没有剩余.
②样品中碳酸钙的质量分数为:
10.0g-1.0g
10.0g
×100%=90%;
故答案为;否,90%;
(2)设生成二氧化碳的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g×90% x
∴
100
44
=
10g×90%
x
解之得:x=3.96g.
答:(2)可产生二氧化碳3.96g.1年前查看全部
- (2008•道外区二模)向试管中放人几小块镁片.把试管固定在盛有饱和石灰水(25℃)的烧杯中.再向试管中滴人约5mL盐酸
 (2008•道外区二模)向试管中放人几小块镁片.把试管固定在盛有饱和石灰水(25℃)的烧杯中.再向试管中滴人约5mL盐酸.如右图所示.请回答:
(2008•道外区二模)向试管中放人几小块镁片.把试管固定在盛有饱和石灰水(25℃)的烧杯中.再向试管中滴人约5mL盐酸.如右图所示.请回答:
(1)实验观察到的现象有:______
(2)产生上述现象的原因是______
(3)放置一段时问后,发现烧杯的底部有固体物质出现,产生固体的可能原因是:
①______
②______. 工7721年前1
工7721年前1 -
 justin195 共回答了18个问题
justin195 共回答了18个问题 |采纳率88.9%解题思路:该实验流程是:镁片与稀盐酸反应生成氢气,同时放热,使得饱和石灰水溶解度下降.镁片会与稀盐酸反应,生成氢气,所以有气泡产生,同时该反应放热,而氢氧化钙的溶解度随温度的升高而降低,从而氢氧化钙会析出一部分,所以烧杯内石灰水会变浑浊.
放置一段时问后,发现烧杯的底部有固体物质出现,出现这种现象可能有两个原因,一方面是:氢氧化钙与空气中的二氧化碳反应生成碳酸钙沉淀;另一可能是:溶剂挥发,溶质氢氧化钙析出一部分.
故答案为:(1)镁片不断溶解,其表面有气泡产生,烧杯内石灰水变浑浊
(2)镁片与稀盐酸反应,生成气体,且反应放热,使石灰水温度升高,溶解度减小
(3)①石灰水与空气中的二氧化碳反应生成白色碳酸钙沉淀
②水分蒸发,溶剂量减少,使饱和溶液中溶质析出点评:
本题考点: 固体溶解度的影响因素;金属的化学性质;酸的化学性质;物质发生化学变化时的能量变化;反应现象和本质的联系.
考点点评: 对于大多数固体来说,溶解度随温度的升高而增大,但也有的固体溶解度随温度的升高而降低,如氢氧化钙.1年前查看全部
- 实验室制取CO 2 一般有以下几个步骤:①向长颈漏斗中注入稀盐酸;②向容器放入几小块石灰石;③按要求组装仪器;④检查装置
实验室制取CO 2 一般有以下几个步骤:①向长颈漏斗中注入稀盐酸;②向容器放入几小块石灰石;③按要求组装仪器;④检查装置的气密性;⑤收集气体.下列顺序排列正确的是( ) A.①②③④⑤ B.④③①②⑤ C.③④②①⑤ D.③④①②⑤  sollit1年前1
sollit1年前1 -
 糖果蓝蓝 共回答了15个问题
糖果蓝蓝 共回答了15个问题 |采纳率100%实验室制取CO 2 需要一定的药品和实验仪器,第一步就是安装实验仪器.
为防止CO 2 逸出,必须检查仪器的气密性,这是在做实验前必须的一步.
故选C1年前查看全部
- (2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图
(2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:

(1)实验中观察到的明显现象有:①剧烈反应,有气泡产生;②镁条逐渐溶解;③______.
(2)产生上述现象③的原因是:
①______;
②______. 甲基笨丙安1年前3
甲基笨丙安1年前3 -
 披件tt上TY 共回答了15个问题
披件tt上TY 共回答了15个问题 |采纳率86.7%解题思路:根据物质的性质进行分析,氢氧化钙的溶解度随温度的升高而减小,金属与酸的反应是放热反应.金属镁与盐酸反应放出热量,导致石灰水的温度升高,石灰水中的溶质为氢氧化钙,氢氧化钙的溶解度随温度的升高而减小,故会析出氢氧化钙溶质,导致石灰水变浑浊.
故答案为:
(1)①石灰水变浑浊;
(2)①镁与盐酸反应放出热量,导致石灰水的温度升高;②氢氧化钙的溶解度随温度的升高而减小.点评:
本题考点: 物质发生化学变化时的能量变化;固体溶解度的影响因素.
考点点评: 本题考查了物质间反应时的能量变化以及影响物质溶解度的因素,完成此题,可以依据已有的知识进行.1年前查看全部
- 向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色会消失的原因是______.
 cg62051311年前1
cg62051311年前1 -
 bbkts 共回答了20个问题
bbkts 共回答了20个问题 |采纳率95%解题思路:木炭、活性炭等物质具有吸附作用,能够吸附色素和一些有异味的物质.木炭具有吸附作用,能够吸附色素和异味.向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭时,木炭把二氧化氮气体吸附,从而使得红棕色消失.
故填:木炭吸附了二氧化氮气体,从而使得红棕色消失.点评:
本题考点: 碳单质的物理性质及用途.
考点点评: 解答本题要掌握木炭的性质方面的知识,只有掌握了木炭的性质才能正确的判断木炭的作用.1年前查看全部
- 如图2-25所示,把试管放入盛有25 ℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中
如图2-25所示,把试管放入盛有25 ℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5 mL盐酸于试管中。

图2-25
试完成下列问题:
(提示:氢氧化钙的溶解度随温度升高而降低)
(1)实验中观察到的现象是_______________________________________________________。
(2)产生上述现象的原因是_______________________________________________________。
(3)写出有关反应的离子方程式:________________________________________________。
(4)由实验推知,MgCl 2 溶液和H 2 的总能量______________(填“大于”“小于”或“等于”)镁片和盐酸的总能量。 linweitao19801年前1
linweitao19801年前1 -
 你我mm人 共回答了19个问题
你我mm人 共回答了19个问题 |采纳率94.7%(1)试管中有气泡产生、饱和石灰水中有白色固体析出(2)镁片溶于稀盐酸放出氢气,且此反应为放热反应,而温度升高,Ca(OH) 2 的溶解度变小(3)Mg+2H + ====Mg 2+ +H 2 ↑(4)小于 镁和盐酸的反应产生氢气...1年前查看全部
- “分塞”的读音“他默默从干粮袋掏出那几小块青稞饼,分塞给战士.”分塞在这里是什么意思,读音是什么?是几声啊
 李俊立1年前1
李俊立1年前1 -
 景洋 共回答了14个问题
景洋 共回答了14个问题 |采纳率100%我也做到这道题了,我选的是一声,应该对吧~!1年前查看全部
- 如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入几小块铝片,再用滴管滴加5mL浓NaOH溶液于试
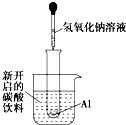 如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入几小块铝片,再用滴管滴加5mL浓NaOH溶液于试管中,试回答下列问题:
如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入几小块铝片,再用滴管滴加5mL浓NaOH溶液于试管中,试回答下列问题:
(1)实验中观察到的现象是______.
(2)产生上述现象的原因是______.
(3)写出有关反应的离子方程式:______.
(4)由实验推知,反应所得溶液和氢气的总能量______(填“大于”、“小于”或“等于”)铝片和NaOH溶液的总能量. 安娜苏蜜粉1年前1
安娜苏蜜粉1年前1 -
 acoolkim 共回答了19个问题
acoolkim 共回答了19个问题 |采纳率94.7%解题思路:金属与酸或碱溶液的置换反应是放热反应,铝与碱液的反应放热更为显著,放出的热量使烧杯中饮料的温度升高,使CO2溶解度减小,从而产生上述现象.根据反应的热效应与化学键的关系可知,放热反应中生成物的总能量小于反应物的总能量.(1)铝与氢氧化钠溶液反应生成氢气并放出热量,溶液温度升高导致二氧化碳的溶解度减小,产生气体的速度加快,
故答案为:铝片上有大量气泡产生,铝片逐渐溶解;烧杯内液体放出气泡的速率加快;
(2)铝与氢氧化钠溶液反应生成氢气并放出热量,溶液温度升高导致二氧化碳的溶解度减小,产生气体的速度加快,
故答案为:铝与NaOH溶液反应生成氢气,且反应放热,碳酸饮料中CO2在水中的溶解度随温度升高而减小,CO2从饮料中逸出的速度加快
(3)铝与强碱反应时有水参与反应,反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)反应放热说明生成物能量和小于反应物能量和,故答案为:小于.点评:
本题考点: 反应热和焓变.
考点点评: 本题考查铝与氢氧化钠溶液的反应,该反应为放热反应,难度不大.要注意气体的溶解度随温度升高而减小.1年前查看全部
- 实验室制取二氧化碳有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③像试管中小心注入适量稀盐酸;④检查装置的气
实验室制取二氧化碳有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③像试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃烧的木条检验集气瓶是否收集满二氧化碳,以上操作按由先至后的顺序排列正确的是( )
A.①②③④⑤⑥
B.①④②③⑤⑥
C.①③②④⑤⑥
D.③①②④⑤⑥ racylll671年前1
racylll671年前1 -
 fzdzxy 共回答了26个问题
fzdzxy 共回答了26个问题 |采纳率92.3%解题思路:根据制取二氧化碳的步骤(连→查→加→倒→定→收→验),进行分析解答即可.制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集)→用燃烧的木条检验集气瓶是否收集满二氧化碳;故正确的操作顺序为:①④②③⑤⑥.
故选:B.点评:
本题考点: 制取二氧化碳的操作步骤和注意点.
考点点评: 本题难度不大,掌握制取二氧化碳的操作步骤和注意事项是正确解答本题的关键.1年前查看全部
- 向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,红棕色会消失的原因是______.
 把爱带走1年前2
把爱带走1年前2 -
 cj1221 共回答了18个问题
cj1221 共回答了18个问题 |采纳率88.9%解题思路:木炭、活性炭等物质具有吸附作用,能够吸附色素和一些有异味的物质.木炭具有吸附作用,能够吸附色素和异味.向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭时,木炭把二氧化氮气体吸附,从而使得红棕色消失.
故填:木炭吸附了二氧化氮气体,从而使得红棕色消失.点评:
本题考点: 碳单质的物理性质及用途.
考点点评: 解答本题要掌握木炭的性质方面的知识,只有掌握了木炭的性质才能正确的判断木炭的作用.1年前查看全部
- 把试管放入盛有25℃的饱和生石灰的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中
 淌混水1年前1
淌混水1年前1 -
 风之子13 共回答了15个问题
风之子13 共回答了15个问题 |采纳率93.3%会发现有气泡产生,烧杯中的溶液变浑浊.
产生气泡是因为Mg+2HCl=MgCl2+H2↑
因为Mg与HCl反应是放热反应,Ca(OH)2的溶解度随温度升高而降低,所以会出现浑浊.1年前查看全部
- (2009•昆明)(1)请回忆教材的习题:向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,看到的现象是____
(2009•昆明)(1)请回忆教材的习题:向盛有红棕色二氧化氮气体的集气瓶里投入几小块烘烤过的木炭,看到的现象是______,原因是______.
(2)某乡镇中学的同学发现水稻大面积倒伏,经分析可能是缺少______肥,农民常用草木灰来补充此肥料,(注:取少量草木灰加到稀盐酸中,发现有气体产生,并可使澄清的石灰石变浑浊),草木灰的主要成分是______,与稀盐酸反应的化学方程式是______. lhjl1231年前1
lhjl1231年前1 -
 majorlost 共回答了19个问题
majorlost 共回答了19个问题 |采纳率94.7%解题思路:(1)根据木炭的性质来解答该题;
(2)常见的肥料为氮磷钾三种,能够根据题给的信息来判断缺少的肥料,并写出化学方程式.(1)物质的性质决定物质的用途,而木炭具有疏松多孔的结构,所以可以吸附二氧化氮气体,故可以观察到红棕色消失;
(2)作物缺少钾肥容易倒伏,而草木灰的主要成分为碳酸钾,碳酸钾可以和盐酸反应生成氯化钾、二氧化碳和水,故可以写出该反应的化学方程式.
故答案为:(1)红棕色消失;木炭具有吸附性;
(2)钾或K;K2CO3或碳酸钾;2HCl+K2CO3═2KCl+H2O+CO2↑.点评:
本题考点: 碳单质的物理性质及用途;常见化肥的种类和作用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的;知道常见的化肥及缺少所引起的后果.1年前查看全部
- (2009•高淳县二模)为了做生石灰与水反应制熟石灰的实验,老师请同事从石灰窑中取出一些白色固体,现带来几小块,我们一起
(2009•高淳县二模)为了做生石灰与水反应制熟石灰的实验,老师请同事从石灰窑中取出一些白色固体,现带来几小块,我们一起来探究一下.
发现和提出问题:石灰窑是工业上用于石灰石高温煅烧制生石灰的,其中发生反应的方程式是探究目的 探究步骤 现象 证明固体是否存在CaO (1)取少量白色固体于烧杯,加入少量水后过滤,向滤液中滴加酚酞试液. __________ 证明固体是否存在CaCO3 (2)向(1)所得滤渣滴加_____溶液 没有气体冒出 CaCO3
CaO+CO2↑高温 .CaCO3.
CaO+CO2↑高温 .
班级的同学提出了以下问题:从中取出的白色固体是什么呢?
假设和猜想:通过对石灰窑中的反应原理进行分析,甲同学猜想该白色固体是碳酸钙,乙同学猜想该白色固体是氧化钙,丙同学猜想该白色固体是______.
查阅资料:氢氧化钙微溶于水
进行实验:
结论:该白色固体是CaO.
深入探究:丁同学做完整个实验后提出了疑问,氧化钙在空气中可能会吸收空气中的水蒸气变成氢氧化钙,现在这份白色固体中存不存在氢氧化钙呢?他为了验证自己的猜想又做了如下实验:
取一定量的纯净的氧化钙固体放在试管中,逐滴加入C%的稀盐酸并震荡,直到固体恰好全部消失,共消耗稀盐酸M1g;
再取相同质量的该白色固体放在试管中,______,根据______这一数据分析,丁同学确定白色固体中存在氢氧化钙.
反思和评价:①化学实验注重仔细观察、严密思考,②定量实验也是化学实验的重要手段,③… fineliu1年前1
fineliu1年前1 -
 fanbo888 共回答了21个问题
fanbo888 共回答了21个问题 |采纳率100%解题思路:欲正确解答本题,须知高温煅烧石灰石的化学方程式,根据化学方程式进行计算,就可得出正确结论.(1)高温煅烧石灰石的化学方程式为:CaCO3
高温
.
CaO+CO2↑;
因为是从石灰窑中取出一些白色固体,故可能是氧化钙和碳酸钙的混合物.
(2)根据化学方程式CaO+2HCl=CaCl2+H2O,Ca(OH)2+2HCl=CaCl2+2H2O可知,等质量的CaO和Ca(OH)2与盐酸完全反应,Ca(OH)2所消耗的盐酸质量比CaO消耗的盐酸的质量少.故如果M2<M1,则说明白色固体中存在氢氧化钙.
故答案为:逐滴加入C%的稀盐酸并震荡,直到固体恰好全部消失,共消耗稀盐酸M2g,M2<M1.点评:
本题考点: 物质的鉴别、推断;猜想与事实验证;药品是否变质的探究;实验数据处理或者误差分析的探究;化学实验方案设计与评价;酸碱指示剂的使用;证明碳酸盐.
考点点评: 本题主要考查学生正确书写化学方程式的能力,以及运用化学方程式进行计算的能力.1年前查看全部
- 英语翻译这道菜是西红柿炒鸡蛋,需要准备的材料,两个鸡蛋,一个西红柿,油,盐和糖.首先,将西红柿切成几小块,把鸡蛋打碎放入
英语翻译
这道菜是西红柿炒鸡蛋,需要准备的材料,两个鸡蛋,一个西红柿,油,盐和糖.首先,将西红柿切成几小块,把鸡蛋打碎放入碗中.然后,将少许油放入锅中,放入鸡蛋炒2分钟,然后将鸡蛋放入碗中.再放入油,炒西红柿,然后放入鸡蛋一起炒几分钟.最后放入盐和糖炒一下.请用西语把上面的文字翻译一下,用最简单的陈述式和最简单的单词就行,别的时态别用,我是初学者. kin20201年前3
kin20201年前3 -
 最爱我的六六 共回答了19个问题
最爱我的六六 共回答了19个问题 |采纳率84.2%Este plato es el revuelto de huevo con tomate.(或者Este plato es El salteado de tomate y huevos)
Ingredientes :dos huevos,un tomate,el aceite,la sal y el azúcar.
El primer paso,cortamos el tomate en trocitos,batimos huevo en un bol.Luego,ponemos una olla con poco de aceite,salteamos huevo durante dos minutos,y lo sacamos en un bol.Volvemos a echar el aceite,salteamos el tomate,y aprovechamos huevo junto con tomate al saltear durante unos minutos.por último,echamos sal y azúcar,movemos bien.
(动词的人称可以是任意的,可以是原型,也可以用你或我们)
请笑纳!1年前查看全部
- (2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图
 (2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:
(2005•镇江)向试管中放入几小块镁片,把试管固定在盛有饱和石灰水(25℃)的烧杯中,再向试管中滴入约5mL盐酸,如图所示.请回答:
(1)实验中观察到的明显现象有:①剧烈反应,有气泡产生;②镁条逐渐溶解;③石灰水变浑浊石灰水变浑浊.
(2)产生上述现象③的原因是:
①镁与盐酸反应放出热量,导致石灰水的温度升高镁与盐酸反应放出热量,导致石灰水的温度升高;
②氢氧化钙的溶解度随温度的升高而减小氢氧化钙的溶解度随温度的升高而减小. LXIN131年前1
LXIN131年前1 -
 4fds5f4d4 共回答了13个问题
4fds5f4d4 共回答了13个问题 |采纳率84.6%金属镁与盐酸反应放出热量,导致石灰水的温度升高,石灰水中的溶质为氢氧化钙,氢氧化钙的溶解度随温度的升高而减小,故会析出氢氧化钙溶质,导致石灰水变浑浊.
故答案为:
(1)①石灰水变浑浊;
(2)①镁与盐酸反应放出热量,导致石灰水的温度升高;②氢氧化钙的溶解度随温度的升高而减小.1年前查看全部
- 如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中(试管中有几小块镁片),再用滴管滴加5ml盐酸于试管中
如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中(试管中有几小块镁片),再用滴管滴加5ml盐酸于试管中
(1)实验现象
(2)产生上述现象原因
(3)相关离子方程式
(4)由实验得Mgcl2溶液与H2总能量是大于/小于/等于Mg与盐酸总能量 呦呦呦呦呦1年前1
呦呦呦呦呦1年前1 -
 承德老鬼 共回答了13个问题
承德老鬼 共回答了13个问题 |采纳率92.3%(1)试管中有气泡产生,镁片逐渐减小;烧杯中有气泡产生
(2)Mg+2HCl=MgCl2+H2;反应放热,二氧化碳溶解度减小.
(3)Mg+2H++2Cl-=Mg2++2Cl-+H2
(4)因为反应放热,所以Mgcl2溶液与H2总能量小于Mg与盐酸总能量1年前查看全部
- 把几小块木炭放在球形管中,按下图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热
把几小块木炭放在球形管中,按下图所示连接装置.打开玻璃活塞,氧气进入球形管,发现木炭不燃烧;关掉氧气,给球形管内木炭加热,木炭同样不燃烧,此时打开玻璃活塞,氧气立即进入球形管,则可以观察到的现象是______.由此得出的结论是:①______;②______.

 szdcv981年前2
szdcv981年前2 -
 weng0313 共回答了22个问题
weng0313 共回答了22个问题 |采纳率81.8%解题思路:据题意可知木炭燃烧必须同时具备温度达到物质的着火点和与氧气接触两个条件.燃烧是一种剧烈的发光、发热的化学反应.木炭剧烈燃烧,发出白光,放热,小烧杯中澄清石灰水变浑浊.
①木炭燃烧生成了二氧化碳(CO2能使澄清石灰水变浑浊).
②可燃物燃烧需要同时满足两个条件:一是可燃物要与O2接触;二是温度达到该物质的着火点.
故答案为:木炭剧烈燃烧,发出白光,澄清石灰水变浑浊①木炭燃烧生成了二氧化碳(CO2能使澄清石灰水变浑浊).②可燃物燃烧需要同时满足两个条件:一是可燃物要与O2接触;二是温度达到该物质的着火点点评:
本题考点: 燃烧的条件与灭火原理探究.
考点点评: 本题以实验探究的形式考查了物质燃烧的条件,燃烧的现象,以及燃烧的产物二氧化碳使澄清石灰水变浑浊的现象.1年前查看全部
- 在一张圆形纸片中画10条直线,最多能把它分成几小块
 庄稼在秋天1年前5
庄稼在秋天1年前5 -
 shoo鱼 共回答了1个问题
shoo鱼 共回答了1个问题 |采纳率100%561年前查看全部
- 灯管这样是烧了吗?就是台灯的灯管,有天突然就不亮了靠近借口一端有几小块灰灰的(拍不到)一端黑黑的像有层黑粉在上面(下图)
灯管这样是烧了吗?
就是台灯的灯管,有天突然就不亮了
靠近借口一端有几小块灰灰的(拍不到)
一端黑黑的像有层黑粉在上面(下图)

没有万用表,请不要回答用万用表测... cqzw54654711年前2
cqzw54654711年前2 -
 江池秋影 共回答了20个问题
江池秋影 共回答了20个问题 |采纳率90%应该是烧了
人就是很奇怪,有些时候自己已经知道答案了,非要从别人口里说出来才相信是真的.1年前查看全部
- 急!求学霸帮忙!有一块大巧克力(每行3个,分3行),第一天吃了1/3,第二天吃了剩下的1/3。第二天吃了几小块巧克力?
 mw99h1年前3
mw99h1年前3 -
 yixiran 共回答了1个问题
yixiran 共回答了1个问题 |采纳率100%1/91年前查看全部
- 把试管放如盛有25度的饱和石灰水的烧杯中,试管中放如几小块镁片,再滴入5ML的HCL于试管中
把试管放如盛有25度的饱和石灰水的烧杯中,试管中放如几小块镁片,再滴入5ML的HCL于试管中
(1)实验中观察至的现象是__________________
(2)产生上述现象的原因
第一题答案是 有大量气泡产生 镁片溶解 烧杯中有晶体析出
第二题答案是 MG与HCL反应产生H2,放热反应,CA(OH)2在水中溶解度减小,析出晶体
但是我有个疑问,为什么Mg与HCL反应生成MgCl2,它为什么不与ca(oh)2反映生成氢氧化镁沉淀? iteyt1年前1
iteyt1年前1 -
 迪克小妖 共回答了15个问题
迪克小妖 共回答了15个问题 |采纳率93.3%镁与盐酸在试管里,试管泡在石灰水里……1年前查看全部
- 某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量
某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试回答:甲同学 乙同学 丙同学 丁同学 所取石灰石样品质量(g) 10.0 10.0 10.0 10.0 加入盐酸的质量(g) 20.0 30.0 45.0 50.0 剩余固体的质量(g) 6.0 4.0 1.0 1.0
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还剩余______(填“是”或“否”),样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?所用稀盐酸的溶质质量分数为多少?(计算结果精确到小数点后两位). daojiancool1年前1
daojiancool1年前1 -
 yxl830316 共回答了26个问题
yxl830316 共回答了26个问题 |采纳率84.6%解题思路:(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②由图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式就可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量,所用稀盐酸的溶质质量分数.(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②样品中碳酸钙的质量分数为[10g−1g/9g]×100%=90%;
(2)设生成二氧化碳的质量为x,所用稀盐酸的溶质质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
1007344
10g×90%y x
[100/44=
10g×90%
x]
x=3.96g.
[100/73=
10g×90%
y]
y=6.57g
所用稀盐酸的溶质质量分数
6.57g
45g×100%=14.6%
答案:
(1)否 90%
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳3.96克,所用稀盐酸的溶质质量分数为14.6%点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生对完全反应的认识,以及利用化学方程式进行计算的能力.考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 带回了几小块石灰石样品
 oceason21年前2
oceason21年前2 -
 流口水999 共回答了16个问题
流口水999 共回答了16个问题 |采纳率81.3%轻质碳酸钙的粉体特点
a、颗粒形状规则,可视为单分散粉体,但可以是多种形状,如纺锤形、立方形、针形、链形、球形、片形和四角柱形.这些不同形状的碳酸钙可由控制反应条件制得.
b、粒度分布较窄.
c、粒径小,平均粒径一般为1-3μm.要确定轻质碳酸钙的平均粒径,可用三轴粒径中的短轴粒径作为表现粒径,再取中位粒径作为平均粒径.以后除说明外,平均粒径,即指平均短轴粒径.
重质碳酸钙的粉体特点
a、颗粒形状不规则,是多分散粉体.
b、粒径分布较宽.
c、粒径大,平均粒径一般为5-10μm.要确定重质碳酸钙的平均粒径,需要测定粒径分布函数和诸如颗粒沉降速度或比表面积之类的粉体现象函数.作为一种简便的方法是在电子显微镜照片上测量颗粒投影的长度和宽度,计算几何平均粒径作为表观粒径,再取中位粒径作为平均粒径.
(3)活性碳酸钙的平均粒径取为表面改性前轻质碳酸钙或重质碳酸钙的平均粒径.1年前查看全部
- 某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0 g样品,将60.
某同学去我市石门县壶瓶山风景区游玩,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,他称取10.0 g样品,将60.Og稀盐酸分四次加入,测量的有关数据见下表
加入稀盐酸的次序
1
2
3
4
加入稀盐酸的质量(g)
20.
30.
45
50
剩余固体的质量(g)
6
4
1
1
求10g样品与45g盐酸充分反应后,盐酸是否还剩余?为什么 玩命天蝎1年前1
玩命天蝎1年前1 -
 hongqi1 共回答了21个问题
hongqi1 共回答了21个问题 |采纳率90.5%应为有表中可知反应2g(6g-4g)石灰石样品需要10g(30g-20g)盐酸,
故1石灰石样品反应需5g盐酸
10g样品与45g盐酸充分反应时,与乙同学比较反应了3g(4g-1g)石灰石样品,所以需15g(3*5)盐酸,因为30+15=45,所以盐酸没有剩余.1年前查看全部
- 向盛有红棕色二氧化氮气体的平底烧瓶中放入几小块活性炭,迅速塞上单孔橡皮塞,观察到的现象是 ,这体现了活性炭具有 .
 zzit1年前1
zzit1年前1 -
 CS1013 共回答了33个问题
CS1013 共回答了33个问题 |采纳率87.9%气体颜色逐渐变淡,最终无色.
活性炭具有吸附性.1年前查看全部
- 某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量
某中学的九年级(1)班同学去太行山春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
试回答:甲同学 乙同学 丙同学 丁同学 所取石灰石样品质量(g) 10.0 10.0 10.0 10.0 加入盐酸的质量(g) 20.0 30.0 45.0 50.0 剩余固体的质量(g) 6.0 4.0 1.0 1.0
(1)10.0g样品与45.0g盐酸充分反应后,盐酸是否还剩余______(填“是”或“否”),样品中碳酸钙的质量分数是______.
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?所用稀盐酸的溶质质量分数为多少?(计算结果精确到小数点后两位). pengxiawei1年前1
pengxiawei1年前1 -
 beautifullinda 共回答了25个问题
beautifullinda 共回答了25个问题 |采纳率88%解题思路:(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②由图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式就可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量,所用稀盐酸的溶质质量分数.(1)①由甲同学可知完全反应的20.0克盐酸消耗了(10-6)克样品中的固体“推导出(10-1)克样品中的固体与45.0克盐酸恰好完全反应,从而判断盐酸没有剩余.
②样品中碳酸钙的质量分数为[10g−1g/9g]×100%=90%;
(2)设生成二氧化碳的质量为x,所用稀盐酸的溶质质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
1007344
10g×90%y x
[100/44=
10g×90%
x]
x=3.96g.
[100/73=
10g×90%
y]
y=6.57g
所用稀盐酸的溶质质量分数
6.57g
45g×100%=14.6%
答案:
(1)否 90%
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳3.96克,所用稀盐酸的溶质质量分数为14.6%点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要考查学生对完全反应的认识,以及利用化学方程式进行计算的能力.考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.1年前查看全部
- 如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用胶头滴管滴入5ml盐酸于试管中,试回答下列问题:

①实验中试管内观察到的现象是______.
②产生该现象的原因是______.
③写出有关反应的离子反应方程式______. 卑鄙教煮饭的1年前3
卑鄙教煮饭的1年前3 -
 奶粉1号 共回答了19个问题
奶粉1号 共回答了19个问题 |采纳率94.7%解题思路:如图所示的实验中,所试管内滴入稀盐酸,盐酸与镁剧烈反应放出氢气,同时反应放出的热量使饱和石灰水溶液温度升高,温度升高氢氧化钙溶解度减小,饱和溶液析出固体氢氧化钙而使烧杯中的溶液变浑浊.①镁与盐酸剧烈反应,可观察到产生大量气体,镁片逐渐溶解,
故答案为:镁片上有大量气泡,镁片逐渐溶解;
②镁与盐酸剧烈反应,产生氢气,
故答案为:镁与盐酸反应产生H2;
③镁与盐酸发生置换反应,生成氯化镁和氢气,反应的离子方程式为:Mg+2H+=Mg2++H2↑,
故答案为:Mg+2H+=Mg2++H2↑.点评:
本题考点: 吸热反应和放热反应.
考点点评: 本题考查金属与酸的反应,该反应为放热反应,难度不大.要注意氢氧化钙的溶解度随温度升高而减小,但本题没考到这一点,是一点创新.1年前查看全部
- 25.(7分)我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲
 xx抽红河1年前1
xx抽红河1年前1 -
 hengshanfan 共回答了21个问题
hengshanfan 共回答了21个问题 |采纳率85.7%10.0g样品与45g盐酸充分反应后,盐酸是否还剩余 _否_ (填“是”或“否”),样品中碳酸钙的质量分数是___90%____.(为什么90%? 因为剩余固体是1g,所以有10-1=9g的碳酸钙反应掉了.所以9/10*100%=90%)
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)
CaCO3+HCl=====CaCl2+H2O+CO2↑
100 44
9g X
X=3.96g1年前查看全部
- 把试管放入盛有25℃时饱和石灰水的烧杯中 试管中开始放入几小块镁片,再用滴滴入m0L盐酸于试管中
把试管放入盛有25℃时饱和石灰水的烧杯中 试管中开始放入几小块镁片,再用滴滴入m0L盐酸于试管中
把试管放入盛有25℃时饱和石灰水的烧杯中 试管中开始放入几小块镁片,再用滴滴入m0L盐酸于试管中 观察到的现像是?有关反应离子方程式! 说事11年前2
说事11年前2 -
 靓龙 共回答了14个问题
靓龙 共回答了14个问题 |采纳率85.7%现象:有大量气泡产生.
离子方程式为:Mg + 2H+ == Mg2+ + H2(气体)1年前查看全部
- 向水中通入CO2再滴入几滴石蕊试液,石蕊试液呈红色.然后放入几小块木炭振荡,溶液变成无色,原因是
 静止空气1年前3
静止空气1年前3 -
 blade2 共回答了10个问题
blade2 共回答了10个问题 |采纳率90%CO2溶于水中生成碳酸是酸性的,所以使石蕊试液呈红色,加入木炭,具有吸附的作用,把石蕊试液中显色的物质吸附,溶液就恢复无色.1年前查看全部
大家在问
- 1巧分应用题一个老人临终留下遗嘱:把家里的17头牛全部分给3个儿子.其中大儿子分得1/2,二儿子分得1/3,三儿子分得1/
- 2初一到初三所有要背的文言文和古诗(所有的名字 别说太多了)人教版
- 3两个相邻的自然数的积是1260求这两个自然数
- 4get get better翻译词组
- 5圆半径为R的外切正方形边长是多少?
- 6英语翻译If you want you can come over tonight and I will take yo
- 7歇后语配对:--两厢情愿 --如鱼得水
- 8有更多的经验翻译成英文
- 9气象气球靠改变自身的什么来实现升降
- 10(本题7分)如图,某校综合实践活动小组的同学欲测量公园内一棵树DE的高度.他们在这棵树正前方一座楼亭前的台阶上A点处测得
- 11如图,点E,F分别是正方形ABCD的边BC,CD上一点,且AE平分∠BEF,连AF.⑴求证:∠EAF=45°⑵若点E为B
- 12长梧封人的成语速度告诉我出自《长梧封人》的成语一定要是成语!不要翻译!只要成语
- 13阅读下文,回答1-2题。 小人无朋 大凡君子与君子,以同道为 朋;小人与小人,以同利为朋:此自然为理也。
- 14下面的材料各表现了怎样的中心?选择中心序号填在材料后的括号里。
- 15如图,下列判断:①∠A与∠1是同位角;②∠A与∠B是同旁内角;③∠4与∠1是内错角;④∠1与∠3是同位角.其中正确的是
