Vml硫酸铁溶液中含wg硫酸跟离子,取此溶液0.5Vml用水稀释到2Vml,稀释后溶液中铁离子的物质的量浓度
 阿乌里2022-10-04 11:39:541条回答
阿乌里2022-10-04 11:39:541条回答A 250w/48v B 250w/72v C 125w/36v D 125w/72v
铁离子的物质的量为2/3*w/96mol
这个怎么求的?

已提交,审核后显示!提交回复
共1条回复
 小王一刀 共回答了18个问题
小王一刀 共回答了18个问题 |采纳率83.3%- 因为是硫酸铁[Fe2(SO4)3]溶液,所以铁离子与硫酸根
离子的质量比等于2*56/96*3=0.389 .
稀释后每升溶液中三价铁离子Fe+++含量:
(0.389*wg*0.5/2vml)*1000ml/L
=(97.3wg/v)/L
稀释后溶液中溶质的物质量浓度:
{[97.3wg/(56g/mol)]/v}mol/L
={1.74w/v}mol/L .可以继续换算:
={72*1.74w/72*v}mol/L
=152w/72v .即选项D正确.
“问题补充”的计算式如何得到的,不清楚. - 1年前
相关推荐
- 下列哪些盐易水解1.氯化铵 2.蓝矾 3.kno3 4.氟化铷 5.醋酸钠 6.氯化铷 7.na2s 8.泻盐9.硫酸铁
下列哪些盐易水解
1.氯化铵 2.蓝矾 3.kno3 4.氟化铷 5.醋酸钠 6.氯化铷 7.na2s 8.泻盐
9.硫酸铁 10.漂白粉 11.小苏打 12.磷酸钾 13.k2cr2o7 14.nahso4 15.cs2so4
要防止这些易水解物质水解需加什么试剂 又过了一年1年前3
又过了一年1年前3 -
 我的他的 共回答了12个问题
我的他的 共回答了12个问题 |采纳率83.3%先总述一下吧,不感兴趣可以选择跳过.
水解的原因:弱酸根离子或弱碱阳离子会部分结合水电离出的H^+或(OH)^-,导致水的电离程度增大,另一种离子浓度增大,溶液呈酸性或碱性.
如此说来,看一种盐能否水解,最简单的方法就是看组成它的阴阳离子所对应的酸或碱是不是弱的,有一个弱就会水解,有两个弱是双水解(水解程度很大).
阳离子水解方程式:B^+ + H_2O =可逆= BOH + H^+
阴离子水解方程式:A^- + H_2O =可逆= HA + (OH)^-
所以要抑制水解的话,阳离子水解就加H^+,阴离子水解就加(OH)^-,双水解无法抑制.
现在来具体看吧.
1.(NH_4)^+对应的碱是NH_3·H_2O,是弱碱,所以是阳离子发生水解,要抑制的话加稀盐酸(HCl)即可.
2.蓝矾是CuSO_4·5H_2O,本身是固体当然没有水解一说,题意应该是说它的水溶液吧.Cu^(2+)对应碱是Cu(OH)_2,弱碱,故阳离子水解,加稀硫酸(H_2SO_4)抑制.
3.两离子皆对应强酸强碱,不水解.
4.F^-对应HF,弱酸,故阴离子水解,加RbOH溶液抑制.
5.(CH_3COO)^-对应CH_3COOH,弱酸,故阴离子水解,加NaOH溶液抑制.
6.两离子皆对应强酸强碱,不水解.
7.S^(2-)对应H_2S,弱酸,故阴离子水解,加NaOH溶液抑制.
8.泻盐是MgSO_4.Mg^(2+)对应Mg(OH)_2,弱碱,故阳离子水解,加稀硫酸(H_2SO_4)抑制.
9.Fe^(3+)对应Fe(OH)_3,弱碱,故阳离子水解,加稀硫酸(H_2SO_4)抑制.
10.漂白粉有效成分是Ca(ClO)_2.(ClO)^-对应HClO,弱酸,故阴离子水解,加Ca(OH)_2溶液抑制.
11.小苏打是NaHCO_3.(HCO_3)^-对应H_2CO_3,弱酸,故阴离子水解,加NaOH溶液抑制.
12.(PO_4)^(3-)对应H_3PO_4,弱酸,故阴离子水解,加KOH溶液抑制.
13.(Cr_2O_7)^(2-)对应H_2Cr_2O_7,弱酸,故阴离子水解,加KOH溶液抑制.
14.两离子皆对应强酸强碱,不水解.
15.两离子皆对应强酸强碱,不水解.1年前查看全部
- 选用试剂稀硫酸,硫酸铁溶液,点极铁铜锌,可构成几种原电池
 z4452513111年前2
z4452513111年前2 -
 e毛钱 共回答了26个问题
e毛钱 共回答了26个问题 |采纳率88.5%1铁锌电极与稀硫酸2铁铜电极与稀硫酸3锌铜电极与稀硫酸4铁锌电极与硫酸铁5铁铜电极与硫酸铁6锌铜电极与硫酸铁7铜和硫酸铁也可以反应,所以也可以做成原电池1年前查看全部
- 硫酸铁水解方程式Fe2(SO4)3 +6H2O =2Fe(OH)3 +3H2SO4 Fe(OH)3是沉淀吗?反应可逆吗?
 zkeyess1年前1
zkeyess1年前1 -
 fanwish168 共回答了20个问题
fanwish168 共回答了20个问题 |采纳率95%大多数水解反应是很微弱的,是可逆反应,生成物如果有不溶的不能打沉淀符号
(因为量很少,不会形成沉淀)
上述反应是可逆反应,Fe(OH)3不是沉淀1年前查看全部
- 主要记什么物质的颜色?如硫酸亚铁溶液为浅绿色硫酸铁溶液为黄色C 为黑色Fe 为银白色还有很多!物质 颜色?记目前我知道的
主要记什么物质的颜色?
如硫酸亚铁溶液为浅绿色
硫酸铁溶液为黄色
C 为黑色
Fe 为银白色
还有很多!物质 颜色?
记
目前我知道的 Cu 紫红色 Fe 银白色 C 黑色 Mg 白色 CuSO4溶液 蓝色 硫酸亚铁溶液 浅绿色 硫酸铁溶液 黄色 四氧化三铁 黑色 三氧化二铁 红色 氧化铜 黑色!还要记点什么其他的吗? whiskeycd1年前2
whiskeycd1年前2 -
 chongrubujing 共回答了15个问题
chongrubujing 共回答了15个问题 |采纳率93.3%硫酸铜 蓝 铜 红 碳酸钙 氯化银 硫酸钡 白 四氧化三铁 黑1年前查看全部
- 怎么分清氯化亚铁和氯化铁?我把这2个东西总是搞混 .比如Fecl2 Fecl3 还有硫酸什么铁的 摸丝硫酸亚铁 硫酸铁
怎么分清氯化亚铁和氯化铁?
我把这2个东西总是搞混 .比如Fecl2 Fecl3 还有硫酸什么铁的 摸丝硫酸亚铁 硫酸铁 3氧化2铁之类的. gw29101年前4
gw29101年前4 -
 鬼狱斩 共回答了18个问题
鬼狱斩 共回答了18个问题 |采纳率100%氯化亚铁的颜色:浅绿
氯化铁的颜色:黄
亚铁:+2价
铁:+3价1年前查看全部
- 铵根离子,铁离子,硝酸根离子,硫酸根离子为什么能共存?铁离子跟硫酸根离子不是会结合成硫酸铁么?
铵根离子,铁离子,硝酸根离子,硫酸根离子为什么能共存?铁离子跟硫酸根离子不是会结合成硫酸铁么?
是不是说只要结合不生成沉淀,气体,水就能共存。
而结合生成其他能容的都无所谓?如:生成Nacl,NaCo3,CuCl。 心净缘1年前6
心净缘1年前6 -
 longhui119 共回答了13个问题
longhui119 共回答了13个问题 |采纳率100%首先,NH4盐全是可容的,NO3盐也全是可容的
SO4是强酸酸根,因此一般来说,硫酸盐都是可容的(除了BASO4难容,AgSO4微溶)
MS得帮LZ好好补补课...
简单地说要结合不生成沉淀,气体,水(弱电解质)就能共存.因为沉淀物和水(弱电解质)是以分子形态存在于水中,即水无法将它们拆成离子.而像NaCl这种,如果形成了沉淀也会被水拆成离子.
如果考虑得复杂点...还要注意氧化还原,双水解等.比如Fe3+和I-不共存,会生成Fe2+和I2.Al3+和CO32-会发生双水解...
注意楼上说的双水解不一定能进行,并不是所有的能水解出H+和OH-的离子在一起都会双水解.1年前查看全部
- 为什么把硫酸铁溶液加热蒸干并灼烧能得到原物质?为什么高锰酸钾、氯化铝不行?这类考虑盐类水解的题怎么做?
 636657151年前1
636657151年前1 -
 alme_522 共回答了21个问题
alme_522 共回答了21个问题 |采纳率81%首先一定要看清题目是加热蒸干还是加热蒸干后再灼烧,拿硫酸铁来说,虽然发生水解但是水解生成的硫酸是难挥发的,所以能得到原物质,但是像氯化铝这样的,水解生成的氯化氢是容易挥发的,所以水解平衡右移导致得不到原物质,灼烧的话得到氧化铝.高锰酸钾应该考虑到它的分解,得到的是锰酸钾和二氧化锰.另外还有的是要考虑到氧化还原反应,例如亚硫酸钠,得到的是硫酸钠.1年前查看全部
- 现有硫酸氯化钡碳酸钾硫酸铁和氯水5种溶液有如图所示的相互关系图中每条连线两端的物质皆可发生化学反应下
现有硫酸氯化钡碳酸钾硫酸铁和氯水5种溶液有如图所示的相互关系图中每条连线两端的物质皆可发生化学反应下
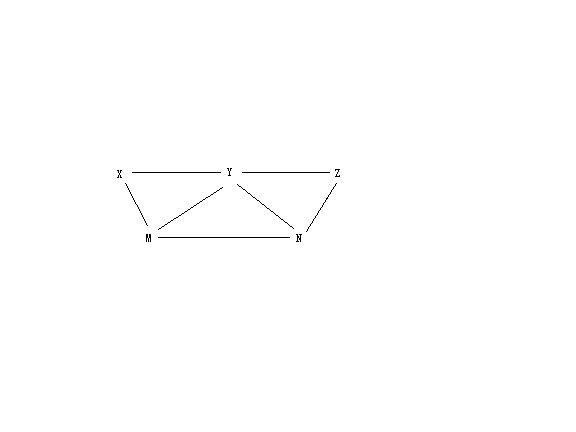
A:X一定为硫酸
B:Y一定为碳酸钾
C:Z可能为氯水
D:M可能为硫酸铁
不合理的是 Flysun_20071年前0
Flysun_20071年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 十二水和硫酸铁按属于危化品吗?
 mimidan11年前1
mimidan11年前1 -
 飞天神经猪 共回答了17个问题
飞天神经猪 共回答了17个问题 |采纳率94.1%不属于1年前查看全部
- 为什么硫酸铁中铁不显+2价
 2148279921年前5
2148279921年前5 -
 lixuyun 共回答了19个问题
lixuyun 共回答了19个问题 |采纳率89.5%因为硫酸属于强酸,与铁发生氧化还原反应时可以将铁元素的外围3个自由电子全部夺得,而一般弱酸与铁反应才生成亚铁离子.这个氧化过程是彻底的,不会产生具有还原性的亚铁离子.1年前查看全部
- 锌和硫酸铁能否反应?不都说置换反应铁二价么
锌和硫酸铁能否反应?不都说置换反应铁二价么
硫酸铁的铁不是三价么,为何能反应 sunnycam1年前3
sunnycam1年前3 -
 rr来上上 共回答了13个问题
rr来上上 共回答了13个问题 |采纳率84.6%铁离子是三价,氧化性很强,而单质铁的还原性很强,
所以他们能反映,根据他们之间的电势差,可以得出它们能够反映,而铁有二价和三价,故三价铁被还原为二价,单质铁被氧化为二价.为归盅反应1年前查看全部
- 硫酸铁是什么颜色的,3价的
 风中小鱼1年前1
风中小鱼1年前1 -
 sdvfeqvewr 共回答了17个问题
sdvfeqvewr 共回答了17个问题 |采纳率76.5%二价亚Fe的溶液是浅绿色、含三价Fe的溶液是黄色
希望有帮助1年前查看全部
- 往2L硫酸铁和硫酸铜的混合溶液中加入30g铁,反应完全后,得固体不溶物26g,在滤液中加入0.5mol氯化钡,恰使硫酸根
往2L硫酸铁和硫酸铜的混合溶液中加入30g铁,反应完全后,得固体不溶物26g,在滤液中加入0.5mol氯化钡,恰使硫酸根沉淀完全,求硫酸铁和硫酸铜的物质的量浓度.
 若空1年前1
若空1年前1 -
 zhuzhu888 共回答了18个问题
zhuzhu888 共回答了18个问题 |采纳率88.9%在滤液中加入0.5mol氯化钡,恰使硫酸根沉淀完全,说明恰好有0.5mol硫酸根离子考虑铁和混合溶液的作用,和三价铁离子作用完后才会和铜离子发生置换反应前者没耗1molFe,(与2mol三价铁作用)固体就减少56g;而后者每耗1mol...1年前查看全部
- 硫酸铁和水在加热条件下反应生成什么?
 没灵魂的躯壳1年前2
没灵魂的躯壳1年前2 -
 bushirchang 共回答了26个问题
bushirchang 共回答了26个问题 |采纳率84.6%在加热条件下硫酸铁水解生成氢氧化铁和硫酸.1年前查看全部
- 制备氢氧化铁时,滴加氢氧化钠的滴管须伸入硫酸铁液面以下吗
 李丹亮1年前1
李丹亮1年前1 -
 comecxs 共回答了14个问题
comecxs 共回答了14个问题 |采纳率85.7%制氢氧化铁不用,但制氢氧化亚铁就要,因为氢氧化亚铁极易氧化成氢氧化铁,滴管口不插入液面很容易带入氧气.1年前查看全部
- 1.硫酸铁和硫酸亚铁的混合物中,若其中铁元素的质量分数为a%,则其中硫元素的质量分数为多少,为什么
 cherio1281年前1
cherio1281年前1 -
 miai5 共回答了19个问题
miai5 共回答了19个问题 |采纳率94.7%处理一下有:Fe(SO4)1.5和FeSO4
所以可以看出剩下的(100-a)%为SO42(硫酸根)
在为SO42(硫酸根)中S占1/3,所以硫元素的质量分数为:(100-a)/3%1年前查看全部
- 硫酸镍,硫酸铁粉末怎么制成晶体还有硫酸铜和氯化铁
 lhfwl1年前1
lhfwl1年前1 -
 孔孔吼吼 共回答了18个问题
孔孔吼吼 共回答了18个问题 |采纳率88.9%去看初中化学书里的结晶实验1年前查看全部
- 在40克密度为dg/cm^3的硫酸铁溶液中,含有1.4g铁离子,则此溶液中铁离子的物质的量浓度为
 shiwei123151年前2
shiwei123151年前2 -
 jldfxy01 共回答了25个问题
jldfxy01 共回答了25个问题 |采纳率84%40克密度为dg/cm^3的硫酸铁溶液,体积为40/1000*d升,1.4g铁离子=0.025摩尔,此溶液中铁离子的物质的量浓度=0.025*1000*d/40=0.625 (摩尔/升)1年前查看全部
- 零点一摩尔硫酸铁溶液和足量的锌充分反应,生成多少摩尔铁单质
 grantxiang1年前1
grantxiang1年前1 -
 haowii 共回答了8个问题
haowii 共回答了8个问题 |采纳率100%Fe2(SO4)3+3Zn=3ZnSO4+2Fe
设生成FeXmol
0.1:X=1:2
X=0.21年前查看全部
- 氯化钙氯化锌氯化钡氯化铝氯化钾氯化银氯化铁氯化亚铁氯化铜氯化亚铜硫酸钠硫酸铜硫酸锌硫酸镁硫酸钡硫酸钙硫酸铝硫酸铁硫酸亚铁
氯化钙
氯化锌
氯化钡
氯化铝
氯化钾
氯化银
氯化铁
氯化亚铁
氯化铜
氯化亚铜
硫酸钠
硫酸铜
硫酸锌
硫酸镁
硫酸钡
硫酸钙
硫酸铝
硫酸铁
硫酸亚铁
硫酸铵
硫酸钾
碳酸钙
碳酸钾
碳酸钠
碳酸银
碳酸钡
碳酸镁
碳酸锌
碳酸铵
硝酸钾
硝酸钠
硝酸银
硝酸钙
硝酸镁
硝酸钡
硝酸锌
硝酸铜
硝酸铁
硝酸亚铁
硝酸铵
硝酸汞 海岸之珠1年前2
海岸之珠1年前2 -
 charmcao 共回答了20个问题
charmcao 共回答了20个问题 |采纳率100%氯化钙CaCl2
氯化锌ZnCl2
氯化钡BaCL2
氯化铝AlCl3
氯化钾KCl
氯化银AgCl
氯化铁FeCl3
氯化亚铁FeCl2
氯化铜CuCl2
氯化亚铜CuCl
硫酸钠Na2SO4
硫酸铜CuSO4
硫酸锌ZnSO4
硫酸镁MgSO4
硫酸钡BaSO4
硫酸钙CaSO4
硫酸铝Al2(SO4)3
硫酸铁Fe2(SO4)3
硫酸亚铁FeSO4
硫酸铵(NH4)2SO4
硫酸钾K2SO4
碳酸钙CaCO3
碳酸钾K2CO3
碳酸钠Na2CO3
碳酸银Ag2CO3
碳酸钡BaCO3
碳酸镁MgCO3
碳酸锌ZnCO3
碳酸铵(NH4)2CO3
硝酸钾KNO3
硝酸钠NaNO3
硝酸银AgNO3
硝酸钙Ca(NO3)2
硝酸镁Mg(NO3)2
硝酸钡Ba(NO3)2
硝酸锌Zn(NO3)2
硝酸铜Cu(NO3)2
硝酸铁Fe(NO3)3
硝酸亚铁Fe(NO3)2
硝酸铵NH4NO3
硝酸汞Hg(NO3)21年前查看全部
- 铁和硫酸铁溶液的离子化学式
 christmaseveday21年前1
christmaseveday21年前1 -
 armyking99 共回答了23个问题
armyking99 共回答了23个问题 |采纳率95.7%Fe+2Fe3+ == 3Fe2+1年前查看全部
- 铁和硫酸铜反应的化学方程式是Fe+CuSO4==FeSO4+Cu 铁的化合价不是负三吗 硫酸铁为什么不应该是Fe(SO4
铁和硫酸铜反应的化学方程式是Fe+CuSO4==FeSO4+Cu 铁的化合价不是负三吗 硫酸铁为什么不应该是Fe(SO4)3
 zhangna20071年前1
zhangna20071年前1 -
 脚气-重 共回答了22个问题
脚气-重 共回答了22个问题 |采纳率86.4%硫酸铁是Fe2(SO4)3,是+3价的Fe
这个叫 做 铁
而FeSO4是硫酸亚铁 这个叫做亚铁,是+2价的1年前查看全部
- 分别用20mL 1mol/L BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸
分别用20mL 1mol/L BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( )
A. 3:2:2
B. 1:2:3
C. 1:3:3
D. 3:1:1 MATOKAYO1年前3
MATOKAYO1年前3 -
 宏光年代 共回答了18个问题
宏光年代 共回答了18个问题 |采纳率100%解题思路:等体积等物质的量浓度的Ba(OH)2溶液,溶质的物质的量相同,利用钡离子与硫酸根离子的关系来计算Fe2(SO4)3、ZnSO4、K2SO4三种溶液中溶质的物质的量,因三种溶液的体积相同,则物质的量之比等于其浓度之比.假设BaCl2的物质的量为1mol,Fe2(SO4)3、ZnSO4、K2SO4三种溶液中的SO42-离子恰好完全转化为沉淀,
设Fe2(SO4)3、ZnSO4、K2SO4三种物质的物质的量为x、y、z,则
由Ba2++SO42-═BaSO4↓,可知
x×3=y×1=z×1=1mol,
则x:y:z=1:3:3,
因三种溶液的体积相同,则物质的量之比等于其浓度之比,
即浓度之比为1:3:3,
故选:C.点评:
本题考点: 离子方程式的有关计算.
考点点评: 本题考查离子的浓度关系,明确钡离子与硫酸根离子的关系及信息中溶液中的SO42-离子恰好完全转化为沉淀是解答本题的关键.1年前查看全部
- .用等体积等物质的量浓度的氯化钡溶液可使相同体积的硫酸铁、硫酸亚铁、硫酸钾三种溶液中的硫酸根离子完全转化为沉淀。则三种溶
.用等体积等物质的量浓度的氯化钡溶液可使相同体积的硫酸铁、硫酸亚铁、硫酸钾三种溶液中的硫酸根离子完全转化为沉淀。则三种溶液的物质的量浓度之比为( )
A.1∶1∶1 B.1∶2∶3 C.3∶1∶1 D.1∶3∶3
答案是D
方法讲下。。
 飞一般享受1年前1
飞一般享受1年前1 -
 sexbaby 共回答了20个问题
sexbaby 共回答了20个问题 |采纳率95%n(Ba2+)=n(SO4 2-)
所以假设这些溶液中每份都含有 3 mol SO42- ,体积为 10L 那么
FeSO4 物质的量为 3 mol,物质的量浓度为 0.3mol/L
Fe2(SO4)3 物质的量为 1 mol,物质的量浓度为 0.1mol/L
K2SO4 物质的量为 3mol,物质的量浓度为 0.3mol/L
所以选 D1年前查看全部
- 不用其他试剂,怎样鉴别硝酸钾、氯化钡、硫酸镁、硫酸铁
 狄雅家1年前4
狄雅家1年前4 -
 qindingsy 共回答了28个问题
qindingsy 共回答了28个问题 |采纳率89.3%各自取样液,分别记为ABCD.
观察颜色,可鉴别出硫酸铁.
往剩余三试管分别滴入硫酸铁,可鉴别出氯化钡.
再用氯化钡去滴入剩余两试管,有沉淀的为硫酸镁,无沉淀为硝酸钾1年前查看全部
- 硫酸铁与氢氧化钡会反应吗?
 monciel1年前4
monciel1年前4 -
 桉桉桉 共回答了20个问题
桉桉桉 共回答了20个问题 |采纳率95%会!这是一个复分解反应!
2Fe2(SO4)3+6Ba(OH)2==4Fe(OH)3+6BaSO41年前查看全部
- 硫酸亚铁溶液被氧气氧化成硫酸铁溶液还是碱式硫酸铁?
 snr192567241年前2
snr192567241年前2 -
 liumangdp111 共回答了11个问题
liumangdp111 共回答了11个问题 |采纳率90.9%硫酸铁溶液 12FeSO4+3O2+6H2O=4Fe2(SO4)3+4Fe(OH)31年前查看全部
- 硝酸 硫酸钡 硫酸镁 硫酸铜 硫酸亚铁 硫酸铁 硫酸铵
硝酸 硫酸钡 硫酸镁 硫酸铜 硫酸亚铁 硫酸铁 硫酸铵
还有碳酸钠 碳酸钾 碳酸钡 碳酸钙 碳酸铵 氢氧化钠 氢氧化钙 氢氧化铁 氢氧化铜 氢氧化铝 氢氧化铵 硝酸钾 硝酸钠 硝酸银 硝酸铜 硝酸铵
有点多啊,我给多点分啊 tgren1年前5
tgren1年前5 -
 小雪是星星 共回答了19个问题
小雪是星星 共回答了19个问题 |采纳率94.7%硝酸 HNO3
硫酸钡 BaSO4
硫酸镁 MgSO4
硫酸铜 CuSO4
硫酸亚铁 FeSO4
硫酸铁 Fe2(SO4)3
硫酸铵 (NH4)2SO4
碳酸钠 Na2CO3
碳酸钾 K2CO3
碳酸钡 BaCO3
碳酸钙 CaCO3
碳酸铵 (NH4)2CO3
氢氧化钠 NaOH
氢氧化钙 Ca(OH)2
氢氧化铁 Fe(OH)3
氢氧化铜 CU(OH)2
氢氧化铝 Al(OH)3
氢氧化铵 NH3.H2O
硝酸钾 KNO3
硝酸钠 NaNO3
硝酸银 AgNO3
硝酸铜 Cu(NO3)2
硝酸铵NH4NO31年前查看全部
- 已知硫酸铁溶液100mL中,铁的质量为2.8g,求硫酸根的c值
 wazt7181年前3
wazt7181年前3 -
 7261606zszzsz 共回答了17个问题
7261606zszzsz 共回答了17个问题 |采纳率88.2%``````铁的物质的量为0.05mol
Fe2(SO4)3 所以SO42-物质的量为0.075mol
c(SO42-) =0.075mol/(100/1000)L=0.75mol/L1年前查看全部
- 实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是( )
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释至所需浓度,如此操作的目的是( )
A. 防止硫酸铁分解
B. 抑制硫酸铁水解
C. 提高硫酸铁的溶解度
D. 提高溶液的PH 1814424911年前1
1814424911年前1 -
 ppq123 共回答了18个问题
ppq123 共回答了18个问题 |采纳率88.9%解题思路:实验室在配制硫酸铁溶液时,铁离子水解生成氢氧化铁变浑浊,先把硫酸铁晶体溶解在稀硫酸中,硫酸抑制铁离子的水解,再加水稀释至所需浓度,得到较纯净的硫酸铁溶液;因为铁离子会水解,生成氢氧化铁,Fe3++3H2O⇌Fe(OH)3+3H+;加入硫酸的目的是在溶液里面形成一种酸性条件,抑制氢氧化铁的生成,使得所配的溶液不会有沉淀,得到较纯净的硫酸铁溶液;
故选B.点评:
本题考点: 盐类水解的应用.
考点点评: 本题考查了盐类水解的应用,水解平衡的影响因素分析是解题关键,题目较简单.1年前查看全部
- 测得某硫酸铁溶液中水分子中铁离子的个数比为100比1,则该溶液中溶质的质量分数?
测得某硫酸铁溶液中水分子中铁离子的个数比为100比1,则该溶液中溶质的质量分数?
要完整的分析过程 ami721年前1
ami721年前1 -
 直觉的三次方 共回答了15个问题
直觉的三次方 共回答了15个问题 |采纳率86.7%1L的同学,努力是必须的,不过要仔细审题这个是硫酸铁,不是硫酸亚铁.Fe2(SO4)3在水中电离,溶液中以Fe3+ 、SO42-存在这个其实可以看为100个H2O分子中有1个Fe3+200个H2O分子中有2个Fe3+,即200个H2O可以溶解1个Fe2(SO4)3...1年前查看全部
- 铁+稀硫酸=硫酸铁+氢气的离子反应方程是?
 冷冷北ll冰1年前1
冷冷北ll冰1年前1 -
 瞬息之城 共回答了25个问题
瞬息之城 共回答了25个问题 |采纳率84%我们学的是生成硫酸亚铁哎!1年前查看全部
- 在硫酸铁和硫酸铜的混合溶液中投入锌粉,出现沉淀,过滤,在沉淀中加入稀硫酸,有气泡出现,那那沉淀可能是?
在硫酸铁和硫酸铜的混合溶液中投入锌粉,出现沉淀,过滤,在沉淀中加入稀硫酸,有气泡出现,那那沉淀可能是?
铁不是比铜活泼吗?怎么还会继续反应 说时快那时迟1年前3
说时快那时迟1年前3 -
 我石头17 共回答了14个问题
我石头17 共回答了14个问题 |采纳率100%反应顺序是:锌先把三价铁离子变成二价亚铁离子,然后再把铜离子变成单质铜,最后把亚铁离子变成单质铁.
现在出现沉淀说明沉淀中有铜,沉淀可和酸反应生成气体说明还有铁甚至有过量的锌(铜不和酸反应放出气体).
所以,沉淀是铜铁混合物或铜铁锌混合物1年前查看全部
- 硫酸铜和硫酸铁中加入锌,充分反应.为什么滤液中一定有硫酸锌?
 xx11年前3
xx11年前3 -
 本方球门里 共回答了16个问题
本方球门里 共回答了16个问题 |采纳率100%由物质活泼性表可知 锌比铁活泼 可置换出铁 得到硫酸锌
硫酸又可以与 锌反应 生成硫酸锌
所以 一定有硫酸锌1年前查看全部
- 硫酸铁水解化学方程式怎么写?我之知道离子方程式是Fe3+ +3H2O←→Fe(OH)3+ 3H+那么化学方程式呢?
 xuahiy20051年前1
xuahiy20051年前1 -
 迷蒙丝丝 共回答了24个问题
迷蒙丝丝 共回答了24个问题 |采纳率91.7%FE2(SO4)3+3H2O==2FE(OH)3+3H2SO41年前查看全部
- 氢氧化钠溶液和硫酸铁溶液反应的化学方程式
 二倍根号三1年前1
二倍根号三1年前1 -
 那年夏天的天 共回答了24个问题
那年夏天的天 共回答了24个问题 |采纳率87.5%6NaOH+Fe2(SO4)3=3Na2SO4+2Fe(OH)3(沉淀)1年前查看全部
- .体积均为AL的硫酸铁,硫酸锌,硫酸钾溶液,均能和BL1摩尔/升BACI2溶液恰好完全反应,则三者的物质的量之比为多少?
.体积均为AL的硫酸铁,硫酸锌,硫酸钾溶液,均能和BL1摩尔/升BACI2溶液恰好完全反应,则三者的物质的量之比为多少?
3.200毫升2摩尔/升的AI2(SO4)3溶液中含有多少摩尔AI2(SO4)3 AI3+的物质的量浓度为多少?SO42—的物质的量浓度为多少?含AI3+的物质的量为多少?质量为多少? ju09131年前1
ju09131年前1 -
 与你有约 共回答了22个问题
与你有约 共回答了22个问题 |采纳率86.4%实际就是Ba2+ +SO42-=BaSO4
均能和BL1摩尔/升BACI2溶液恰好完全反应
BL1摩尔/升这样BaCl2物质的为Bmol,
Ba2+量就为Bmol
这样硫酸铁,硫酸锌,硫酸钾含SO42-的量都一样为Bmol
设B=1mol
含1molSO42-的Fe2(SO4)3的量为1/3mol
含1molSO42-的ZnSO4的量为1mol
含1molSO42-的K2SO4的量为1mol
这3物质物质的量比为1:3:3
如果不考虑水解
3.200毫升2摩尔/升的AI2(SO4)3溶液中含有0.0032x2=0.0064mol的AI2(SO4)3
AI3+的物质的量浓度为2molL-x2=4moL-
SO42-的物质的量浓度为2molL-x3=6moL-
含AI3+的物质的量为0.0064x2=0.0128mol,质量为0.0128x27=0.346克1年前查看全部
- 用化学方程式解释其原理.1.为什么工业上利用氯化铁溶液腐蚀铜制印刷线路板.2.为什么在硫酸铁溶液中常常加入铁粉或铁钉.3
用化学方程式解释其原理.1.为什么工业上利用氯化铁溶液腐蚀铜制印刷线路板.2.为什么在硫酸铁溶液中常常加入铁粉或铁钉.3.工业制漂白粉的反应原理.4.钠与水反应原理.
 木瓜猪1年前1
木瓜猪1年前1 -
 爱上林妹妹 共回答了14个问题
爱上林妹妹 共回答了14个问题 |采纳率100%1, 2FeCl3+Cu=CuCl2+2FeCl2
2, 应该是在硫酸铁溶液中常常加入铁粉或铁钉.
Fe2(SO4)3+Fe=3FeSO4
3, 2Ca(OH)2+Cl2=2Ca(ClO)2+CaCl2+2H2O
4,2Na+2H2O=2NaOH+H2(气体)1年前查看全部
- 铝能置换硫酸铁中的铁吗
 杭州大理双城记1年前1
杭州大理双城记1年前1 -
 12345678jl 共回答了10个问题
12345678jl 共回答了10个问题 |采纳率100%铝和铁的活动性接近,要看环境因素的影响了.比如浓度,温度,电场情况,溶剂情况.1年前查看全部
- 帮忙写下化学反应离子方程式1.氯化铁溶液中通入硫化氢气体.2.向次氯酸钙溶液中通入二氧化硫.3.硫酸铁的酸性溶液中通入足
帮忙写下化学反应离子方程式
1.氯化铁溶液中通入硫化氢气体.
2.向次氯酸钙溶液中通入二氧化硫.
3.硫酸铁的酸性溶液中通入足量硫化氢.
4.氯化铝溶液中加入过量氨水.
5.碳酸钠溶液中加入过量苯酚.
6.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液. wdy442791年前1
wdy442791年前1 -
 lina138 共回答了21个问题
lina138 共回答了21个问题 |采纳率66.7%晕,不会打小加号和小数字,怎么办
算了,应该看得明白吧.
2Fe3+ + H2S ==2H+ + S↓+ 2Fe
2ClO- + Ca2+ +2H2O+2SO2==2Cl- +CaSO4↓+4H+ + SO4 2-
Fe2(SO4)3+ H2S==2 FeSO4+ S↓+ H2SO4
Al3+ +3NH3.H2O=Al(OH)3↓+3NH4+
AlCl3+3NH4.H2O==3NH4Cl+Al(OH)3 ↓
Ca2+ +HCO3- +OH-==CaCO3↓+H2O
打到手累1年前查看全部
- 向盛有硫酸铁溶液的试管中滴加0.1mol/L的KSCN溶液后,呈现红色,发生反应的离子方程式为Fe3+ +3SCN-=F
向盛有硫酸铁溶液的试管中滴加0.1mol/L的KSCN溶液后,呈现红色,发生反应的离子方程式为Fe3+ +3SCN-=Fe(SCN)3;若向反应后的溶液中滴加1mol/L的KSCN溶液,化学平衡___,可以看到的现象是___.
请写明原因谢谢 palyball1年前2
palyball1年前2 -
 真他吗犯贱 共回答了19个问题
真他吗犯贱 共回答了19个问题 |采纳率89.5%化学平衡_正向移动__,可以看到的现象是__颜色更深_.1年前查看全部
- 泥水中加入硫酸铁 静置后上层是透明的清液吗
 jdwxzl1年前2
jdwxzl1年前2 -
 andychg 共回答了16个问题
andychg 共回答了16个问题 |采纳率93.8%是的,Fe3+的盐是混凝剂,加入到泥水中会引起泥沙等发生絮凝沉淀,静置后全部沉淀到下层,上层就是透明的清液.
ls犯了个错误,硫酸铁溶液是有色的,但是也是透明的.有色并不是不透明.1年前查看全部
- Fe的价态问题我想知道,铁在不同的常见化合物中各显几价,怎么制得的..(比如硫酸铁,等等)FeCl2 和FeCl3 中铁
Fe的价态问题
我想知道,铁在不同的常见化合物中各显几价,怎么制得的..(比如硫酸铁,等等)
FeCl2 和FeCl3 中铁各是2价和3价,这是怎么制得的呢? 卧室君囧1年前1
卧室君囧1年前1 -
 nkfw2698 共回答了20个问题
nkfw2698 共回答了20个问题 |采纳率95%铁单质0价,化合物中有+2,+3,+3价更稳定,而Fe3O4实际上是Fe(FeO2)2,其中Fe的价态可以看做是+2,+3,
FeCl2可由铁和盐酸反应制得,FeCl3可由铁与氯气反应得到,或是由FeCl2与cl2反应得到1年前查看全部
- 分类是学习和研究化学物质及其变化的一种常用的基本方法.现有药品硫酸铁,它与下列哪组属于同一类物质( )
分类是学习和研究化学物质及其变化的一种常用的基本方法.现有药品硫酸铁,它与下列哪组属于同一类物质( )
A.盐酸、硫酸
B.氢氧化铝、氢氧化铜
C.氯化镁、碳酸氢钠
D.二氧化碳、四氧化三铁 panhaiping1年前1
panhaiping1年前1 -
 chhlgq 共回答了22个问题
chhlgq 共回答了22个问题 |采纳率86.4%解题思路:根据物质的组成和性质来分析物质的类别,硫酸铁是由铁离子和硫酸根离子构成的,属于盐;利用氧化物、酸、碱、盐的概念来判断物质是否属于同一类别.硫酸铁是由铁离子和硫酸根离子构成的,属于盐.
A、盐酸、硫酸电离时产生的阳离子均全部是氢离子,均属于酸,故选项错误.
B、氢氧化铝、氢氧化铜电离时产生的阴离子均全部是氢氧根离子,均属于碱,故选项错误.
C、氯化镁是由由镁离子和氯离子组成的化合物,属于盐;碳酸氢钠是由钠离子和碳酸根离子组成的化合物,属于盐;故选项正确.
D、二氧化碳、四氧化三铁均是由两种元素组成的且有一种是氧元素的化合物,均属于氧化物,故选项错误.
故选:C.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别.
考点点评: 本题难度不大,考查物质类别的判别,抓住酸、碱、盐的特征、熟悉常见的物质的组成是正确解答本题的关键.1年前查看全部
- 在允许加热的条件下,只用一种试剂就可以鉴别硫酸铁,硫酸亚铁,硫酸钠,氯化铝,氯化铵五种溶液,这种试剂是?
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铁,硫酸亚铁,硫酸钠,氯化铝,氯化铵五种溶液,这种试剂是?
A 硝酸银溶液 B 氯化钡溶液 C氨水 D氢氧化钠溶液
我想问为什么B不可以,硫酸铁和硫酸亚铁可以直接看出,氯化铵加热就可以看出,硫酸钠和氯化铝不可以用B直接鉴别嘛 啸弘1年前3
啸弘1年前3 -
 yo727yo 共回答了15个问题
yo727yo 共回答了15个问题 |采纳率80%氯化铵是不会受热分解的,需要加入氢氧化钠1年前查看全部
- 除去硫酸铁中的硫酸锌,不能用锌,不能用溶解度.
 fire0011年前3
fire0011年前3 -
 新好男人 共回答了21个问题
新好男人 共回答了21个问题 |采纳率81%如果是干净的溶液
加入过量的浓碱,铁全部变成氢氧化铁沉淀,锌在过量碱作用下变成可溶的锌酸盐,然后过滤出固体氢氧化铁,再用硫酸溶解即可1年前查看全部
- 有一个包粉末,可能由氯化钠、硫酸铁、氯化镁、硝酸钠、碳酸钠中的一种或几种组成.
有一个包粉末,可能由氯化钠、硫酸铁、氯化镁、硝酸钠、碳酸钠中的一种或几种组成.
现做下列实验:①取少量粉末,加水溶解得无色透明溶液;②在上述溶液里,加氢氧化钠溶液,无明显变化;③另取少量固体,加稀盐酸,无明显变化.
根据上述实验,试回答:
(1)从实验①推断,不可能存在______(填化学式),原因是_________.
从实验②推断,不可能存在______(填化学式),原因是_________.
从实验③推断,不可能存在______(填化学式),原因是_________.
(2)根据上述实验,可得出初步结论,该粉末中可能含有_________.
(3)若该白色粉末只有一种物质,要证明是什么物质,则需取少量原粉末,装入试管
再加入少量水溶解,然后加入_____试剂,根据____________现象进行判断. 王佳年12041年前3
王佳年12041年前3 -
 小蛋113 共回答了13个问题
小蛋113 共回答了13个问题 |采纳率84.6%①取少量粉末,加水溶解得无色透明溶液;--------没有Fe2(SO4)3,它的溶液是黄色的,另外注意MgCl2与Na2CO3不能共存
②在上述溶液里,加氢氧化钠溶液,无明显变化;-----------没有MgCl2
③另取少量固体,加稀盐酸,无明显变化.----------没有Na2CO3
可能存在NaCl、NaNO3中的1种或2种
(1)从实验①推断,不可能存在___Fe2(SO4)3___(填化学式),原因是____它的溶液显黄色_____.
从实验②推断,不可能存在___MgCl2___(填化学式),原因是_____会与NaOH生成Mg(OH)2白色沉淀____.
从实验③推断,不可能存在___Na2CO3___(填化学式),原因是____会与盐酸反应生成CO2气体_____.
(2)根据上述实验,可得出初步结论,该粉末中可能含有____NaCl和NaNO3中的1种或者2种_____.
(3)若该白色粉末只有一种物质,要证明是什么物质,则需取少量原粉末,装入试管
再加入少量水溶解,然后加入__AgNO3溶液___试剂,根据_____有无白色沉淀_______现象进行判断.1年前查看全部
- 硫酸铁和硫酸亚铁混合物,其中铁元素质量分数a%,硫元素质量分数为
 花开物语1年前1
花开物语1年前1 -
 我凤我凰 共回答了15个问题
我凤我凰 共回答了15个问题 |采纳率93.3%剩下的都是硫酸根百分数等于1-a%
硫酸根中硫百分数等于1/3
所以硫百分数等于1/3乘以(1-a%)1年前查看全部
大家在问
- 1六年级上册苏教版的习作一要用这几个人物:妈妈,王艺璇,爸爸,其他的无所谓
- 2用一张直径为8厘米的圆形纸板剪一个最大的正方形,这个正方形的面积是多少
- 3如图所示.四边形abcd是圆心的内接四边形.ac丄bd于点e.若ab=8.cd=6.则圆0的半径
- 4谁主浮沉——我的十八岁 作文
- 5诗经形容女子漂亮的有哪些如桃夭
- 66.5x+x=1.5
- 7中译英:是金子总会发光;执着地追求理想
- 8孔子教导人要有高尚情操的 和感叹时光的流逝沧海桑田变化句子
- 9已知数f(x)=(2x-a)/(x2+2)(x∈R).1)当f(x)=1时,求函数的单调区间 2)设关于x的方程
- 10若点(-5,b)与点(a,-3)关于y轴对称,则a=( ),b=( ).
- 11听了这个故事,很多同学都感动得流下了激动的热泪.(修改病句)
- 12英语连字符问题一般来说两岁大的男孩用上连字符和不用连字符怎么说..还是两个月的假期..还有讲讲为什么,总是搞混掉,
- 13已知集合A={2,3,a²+1},B={a²+a-4,2a+1,-1},且A∩B={2},求a的值
- 14跪求写一篇《妈妈的笑声》现代诗 要是要押韵的
- 15初三物理公式九年级物理公式,W=Fs=Pt】P=w/t=Fv】W有=Gh=Fs】W额=Gh=fL】W总=Fs】Q=cmΔ
