用双氧水去除氯化铁溶液中的氯化亚铁杂质的反应方程式?
 49gasue2022-10-04 11:39:542条回答
49gasue2022-10-04 11:39:542条回答还有氯化铁得存在于强酸中,加双氧水会有影响吗?
我是这么想的把氯化亚铁氧化的话氯离子一定不够,所以应该有铁以什么形式沉淀出来,而老师说加双氧水的产物是水不会有别的杂质.

已提交,审核后显示!提交回复
共2条回复
 offerme 共回答了15个问题
offerme 共回答了15个问题 |采纳率93.3%- 没有影响.
双氧水对纤维素的氧化,主要是使葡萄糖分子的羟基氧化成酮,即所谓的酮纤维素;次氯酸钠则主要使葡萄糖分子的羟基氧化成醛,而醛基的存在又可使纤维素的降解继续进行,造成纤维大面积的损伤,有关研究资料表明:使纤维素分子断裂所需的耗氧量比较,双氧水大于次氯酸钠和亚氯酸钠,这是双氧水对纤维素损伤程度较轻的一个原因.另外,醛基的存在是导致漂白物泛黄的原因,这说明了氯漂易于泛黄,而氧漂的白度稳定,不易泛黄.又由于双氧水去杂能力强,在几种漂白剂中只有双氧水可以实行煮漂一浴工艺,加上双氧水的分解产物无污染、无毒、不腐蚀设备,这些都使双氧水成为短流程处理工艺中漂白剂的最佳选择.
方程式:3(Fe2+)+2(H+)+H2O2 = 2(FeCl3+)+2H2O - 1年前
 妞妞白书 共回答了107个问题
妞妞白书 共回答了107个问题 |采纳率- 3(Fe2+)+2(H+)+H2O2 = 2(FeCl3+)+2H2O
氯化铁得存在于强酸中,加双氧水不会有影响 - 1年前
相关推荐
- 用长颈漏斗双氧水制氧气 装置检查气密性方法
用长颈漏斗双氧水制氧气 装置检查气密性方法
RT zonson1年前1
zonson1年前1 -
 我想放了你 共回答了21个问题
我想放了你 共回答了21个问题 |采纳率100%将长颈漏斗伸入液面下,将导管处弹簧夹夹紧,从长颈漏斗向下注液体,若液面不下降,则说明气密性良好1年前查看全部
- 双氧水在常温下能缓慢分解,请问是否所有的化合物都能在常温下缓慢分解?
 huangshan79511年前1
huangshan79511年前1 -
 syjbwbb 共回答了17个问题
syjbwbb 共回答了17个问题 |采纳率88.2%有的能分解,有的不能(必须在加热、高温的条件下进行).所以不是所有的化合物在常温下分解.
大理石需在高温下分解 .1年前查看全部
- 消毒液并不是越浓越有效,如双氧水高浓度溶液具有腐蚀性,现需将500克质量分数为30%的双氧水配成3%的溶液,
消毒液并不是越浓越有效,如双氧水高浓度溶液具有腐蚀性,现需将500克质量分数为30%的双氧水配成3%的溶液,
需加水多少克?
要过程!快!
 孙金伟1年前1
孙金伟1年前1 -
 快嘴 共回答了18个问题
快嘴 共回答了18个问题 |采纳率94.4%设:需要水x g
500*30%=(x+500)*3%
x=4500g1年前查看全部
- 在密闭的仪器内,双氧水和二氧化锰,水和硝酸铵,水和氢氧化钠,水和生石灰,哪个反应后会使仪器内的气压小于外界气压
 苏0051年前1
苏0051年前1 -
 fabio2005 共回答了20个问题
fabio2005 共回答了20个问题 |采纳率90%h2o和naoh1年前查看全部
- 请教几个离子方程式1用惰性电极电解硫酸铜溶液2在硫酸铝溶液中加入偏铝酸钠溶液3在酸性高锰酸钾溶液中滴加双氧水产生气体4金
请教几个离子方程式
1用惰性电极电解硫酸铜溶液
2在硫酸铝溶液中加入偏铝酸钠溶液
3在酸性高锰酸钾溶液中滴加双氧水产生气体
4金属镁和氯化铁溶液共热
(能写几个都可以) 含笑31年前3
含笑31年前3 -
 我只喜欢ァ 共回答了17个问题
我只喜欢ァ 共回答了17个问题 |采纳率94.1%1用惰性电极电解硫酸铜溶液
2Cu(2+)+2H2O==2Cu+4H(+)+O2
2在硫酸铝溶液中加入偏铝酸钠溶液
Al(3+)+3AlO2(-)+6H2O=4Al(OH)3
3在酸性高锰酸钾溶液中滴加双氧水产生气体
5H2O2+2MnO4(-)+6H(+)=2Mn(2+)+5O2+8H2O
4金属镁和氯化铁溶液共热
2Fe(3+)+Mg=2Fe(2+)+Mg(2+)
2Fe(3+)+3H2O===2Fe(OH)3+6H(+)
Mg+2H(+)=Mg(2+)+H21年前查看全部
- 双氧水制氧气的方程式,
 ever20011年前0
ever20011年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 已知(16)O和(18)O是氧的同位素,有(16)O、(18)O、H、T、D五种原子,可以构成双氧水分子,其种类有:
已知(16)O和(18)O是氧的同位素,有(16)O、(18)O、H、T、D五种原子,可以构成双氧水分子,其种类有:
A、12种
B、14种
C、16种
D、18种
-------------------------------------------------------------
看起来貌似是排列与组合?如果是这样算的话请给出计算过程 hnxinlan1年前7
hnxinlan1年前7 -
 好玩PKWC笑场 共回答了19个问题
好玩PKWC笑场 共回答了19个问题 |采纳率94.7%H-O-O-H
用1、2、3分别代表H、D、T
用16、18代表(16)O、(18)O
若2个H一样,即3种情况:1-1,2-2,3-3
那么,放在中间的2个O原子各有3种情况,即,16-16,18-18,16-18
所以,有3×3=9种
若2个H不一样,即3种情况:1-2,1-3,2-3
那么,放在中间的2个O原子各有4种情况,即,16-16,18-18,16-18,18-16
所以,有3×4=12种
因此,共有21种
这道题目出来,一直是有问题的,就在于,1-16-18-2与1-18-16-2是不一样的1年前查看全部
- 30%质量分数双氧水溶液如何转换成2.5mmol/L的双氧水溶液
 cqdy51191年前1
cqdy51191年前1 -
 罩色 共回答了21个问题
罩色 共回答了21个问题 |采纳率85.7%取0.26mL的30%双氧水稀释成1L,即得1L的2.5mmol/L的双氧水溶液
计算过程如下:
30%双氧水密度为1.1g/mLl,过氧化氢34g/mol,假设要配制1L溶液,则所需溶质质量为
2.5*1*34=85mg,折合成市售30%双氧水体积为85*10^-3/(1.1*30%)=0.258mL,
即用市售30%双氧水约0.26mL,稀释成1L即为2.5mmol/L的溶液了1年前查看全部
- 双氧水的氧化性是不是大于三价铁离子?
 bbttcom1年前2
bbttcom1年前2 -
 逍遥山庄 共回答了20个问题
逍遥山庄 共回答了20个问题 |采纳率90%H2O2是既具有氧化性又具有还原性的物质(实际上都基于它的不稳定性).
H2O2从氧化性和还原性上说由于H2O2具有“两性”所以很容易自发分解,尤其在有催化剂的作用中.
以Fe3+催化为例:
2Fe3+ + H2O2 ==2Fe2+ + 2H+ + O2↑
2Fe2+ + H2O2 + 2H+ ==2Fe3+ + 2H2O
由于这两个反应进行的速率远远大于H2O2自发分解的速率,所以对H2O2的分解起催化作用,其它催化剂皆类似于此.
如果光说氧化性H2O2大于Fe3+,但是说还原性则H2O2也大于Fe3+.而楼上说的太含糊了.1年前查看全部
- 过氧化氢是一种常见绿色氧化剂,用途广泛,其水溶液俗称双氧水.
过氧化氢是一种常见绿色氧化剂,用途广泛,其水溶液俗称双氧水.
(1)已知液态过氧化氢与水相似,可微弱电离,得到两种等电子微粒.请写出过氧化氢的电离方程式______.
(2)如图所示:两个盛有等量过氧化氢溶液的容器A和B,向A中加入少量MnO2;向B中加入H2SO4和足量MnO2.充分反应后,B中放出气体的量是A中放出气体的2倍(相同状况),则B中反应的化学方程式是______;原因是______.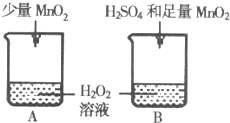
(3)火箭推进器中盛有强还原剂肼(N2H4)和强氧化剂液态双氧水(H2O2).当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应放出256.0kJ的热量.则该反应的热化学方程式是______. bladering9991年前1
bladering9991年前1 -
 jxh__259999 共回答了16个问题
jxh__259999 共回答了16个问题 |采纳率100%解题思路:(1)过氧化氢电离得到的等电子体产物为H3O2+、HO2-;
(2)A中过氧化氢在二氧化锰的催化作用下发生分解反应,B中在酸性条件下,过氧化氢与二氧化锰发生氧化还原反应,B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气;
(3)反应方程式为:N2H4+2H2O2=N2+4H2O,根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,进而写出热化学方程式.(1)过氧化氢电离得到的等电子体产物为H3O2+、HO2-,其电离方程式为:2H2O2
 H3O2++HO2-,
H3O2++HO2-,
故答案为:2H2O2 H3O2++HO2-;
H3O2++HO2-;
(2)A中过氧化氢在二氧化锰的催化作用下发生分解反应,B中在酸性条件下,过氧化氢与二氧化锰发生氧化还原反应,B中反应方程式为MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O,B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气,故B中放出气体是A中2倍,
故答案为:MnO2+H2O2+H2SO4=MnSO4+O2↑+2H2O;B中的MnO2作氧化剂,可将过氧化氢中的-1价氧全部氧化为氧气,而A中的过氧化氢发生歧化反应,只有一半-1价氧被氧化为氧气,故B中放出气体是A中2倍;
(3)反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为[256kJ/0.4]=640kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-640kJ/mol,
故答案为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-640kJ/mol.点评:
本题考点: 过氧化氢;热化学方程式;弱电解质在水溶液中的电离平衡.
考点点评: 本题考查等电子体、氧化还原反应、热化学方程式的书写,题目难度一般,注意热化学方程式与化学方程式的区别.1年前查看全部
- 双氧水制氧气的化学方程式
 下一站感觉1年前3
下一站感觉1年前3 -
 wn2k 共回答了27个问题
wn2k 共回答了27个问题 |采纳率88.9%双氧水制氧气的化学方程式:2H2O2=MnO2=2H2O+O2(气体)1年前查看全部
- 过氧化氢俗称双氧水,可用过氧化钡(BaO 2 )与稀硫酸反应来制备。过氧化氢与过氧化钡都是过氧化物,过氧化物一般可用作氧
过氧化氢俗称双氧水,可用过氧化钡(BaO 2 )与稀硫酸反应来制备。过氧化氢与过氧化钡都是过氧化物,过氧化物一般可用作氧化剂、漂白剂、供氧剂等。阅读下文并回答有关问题:
(1)实验室可用过氧化氢溶液制取氧气,其反应的化学方程式是 。
(2)过氧化钠(Na 2 O 2 )也是一种过氧化物,潜水艇常用过氧化钠作供氧剂,同时维持艇内空气成分的稳定,写出这一反应的化学方程式 。 anniemaymay1年前0
anniemaymay1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 双氧水可以将废水中的氰化物转化为无毒物同时生成NH3的离子方程式
 yingzi3131年前1
yingzi3131年前1 -
 tintin5555 共回答了18个问题
tintin5555 共回答了18个问题 |采纳率88.9%CN- + H2O2 + H2O = HCO3- +NH3↑ (数字都是下标)1年前查看全部
- 一个直径70CM的容器要装400升的双氧水容器的高度要多少?
 efshi1年前0
efshi1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 水和双氧水说法正确的:A都含有氢气B都含有氢元素C都含有氢分子D都含有两个氢原子 为什么答案是B而C 不行
水和双氧水说法正确的:A都含有氢气B都含有氢元素C都含有氢分子D都含有两个氢原子 为什么答案是B而C 不行
对不起问错了,为什么D不行 ponysuit1年前5
ponysuit1年前5 -
 我是你非 共回答了18个问题
我是你非 共回答了18个问题 |采纳率94.4%水和双氧水都含H元素和O元素,或者都是有H原子和O原子组成
氢气分子的化学式为H2,是一种单质,独立存在,而H2O的H2表示是2个H原子,H2O里没有H2分子1年前查看全部
- 水(H2O)被称为“生命之源”,双氧水(H2O2)被称为“绿色氧化剂”.下列关于它们的说法中正确的是( )
水(H2O)被称为“生命之源”,双氧水(H2O2)被称为“绿色氧化剂”.下列关于它们的说法中正确的是( )
A. 都是氧化物
B. 都含有氢分子
C. 都含有氢元素
D. 都含有2个氢原子 stockstar1年前1
stockstar1年前1 -
 halley1972 共回答了13个问题
halley1972 共回答了13个问题 |采纳率100%解题思路:A、根据氧化物的概念可知氧化物只有两种元素,且必须有氧元素;
B、根据化合物的组成考虑;
C、根据物质组成来考虑;
D、根据分子的构成解释.A、H2O和H2O2都是由氢氧两种元素组成,且有氧元素,都属于氧化物,故A正确;
B、H2O和H2O2都是化合物其中含有氢元素,不含有氢分子,如果含有氢分子就成了混合物了,故B错;
C、H2O和H2O2两种物质都是由氢、氧两种元素组成,故C正确;
D、H2O和H2O2两种物质要用元素解释,不能用原子,如果说它们的每个分子中都含有两个氢原子就行了,故D错.
故选AC.点评:
本题考点: 从组成上识别氧化物;分子、原子、离子、元素与物质之间的关系.
考点点评: 要熟记化学式表示的意义,物质要用元素解释,分子要用原子解释.1年前查看全部
- (1)火箭推进器中盛有强还原剂液态肼(N 2 H 4 )和强氧化剂液态双氧水(H 2 O 2 ),当它们混合反应时,即产
(1)火箭推进器中盛有强还原剂液态肼(N 2 H 4 )和强氧化剂液态双氧水(H 2 O 2 ),当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知0.4mol液态肼与足量液态双氧水反应时,放出256kJ的热量.请写出该反应的热化学方程式:______.
(2)工业上由金红石(TiO 2 )制取单质Ti,涉及到的步骤为:TiO 2 →(步骤Ⅰ)TiCl 4
(步骤Ⅱ)TiMg.800℃.Ar
写出步骤Ⅱ中TiCl 4 →Ti的化学反应方程式______.
已知:①C(s)+O 2 (g)=CO 2 (g)△H=-393.5kJ-mol -1
②2CO(g)+O 2 (g)=2CO 2 (g)△H=-566kJ-mol -1
③TiO 2 (s)+2Cl 2 (g)=TiCl 4 (s)+O 2 (g)△H=+141kJ-mol -1
则反应TiO 2 (s)+2Cl 2 (g)+2C(s)=TiCl 4 (s)+2CO(g)的△H=______kJ-mol -1 . 巴雅1年前1
巴雅1年前1 -
 南美漂流瓶 共回答了16个问题
南美漂流瓶 共回答了16个问题 |采纳率100%(1)强还原剂液态肼(N 2 H 4 )和强氧化剂液态双氧水(H 2 O 2 ),当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热;已知0.4mol液态肼与足量液态双氧水反应时,放出256kJ的热量;则1mol液态肼完全反应放出热量为:640KJ;标注物质聚集状态和对应焓变,热化学方程式为:N 2 H 4 (l)+2H 2 O 2 (l)=N 2 (g)+4H 2 O(g)△H=-640KJ/mol
故答案为:N 2 H 4 (l)+2H 2 O 2 (l)=N 2 (g)+4H 2 O(g)△H=-640KJ/mol;
(2)工业上由金红石(TiO 2 )制取单质Ti,涉及到的步骤为:TiO 2 →(步骤Ⅰ)TiCl 4
Mg.800℃.Ar
(步骤Ⅱ)Ti
步骤Ⅱ中TiCl 4 →Ti的化学反应方程式为:TiCl 4 +2Mg=MgCl 2 +Ti;
依据盖斯定律结合热化学方程式计算:
①C(s)+O 2 (g)=CO 2 (g)△H=-393.5kJ?mol -1
②2CO(g)+O 2 (g)=2CO 2 (g)△H=-566kJ?mol -1
③TiO 2 (s)+2Cl 2 (g)=TiCl 4 (s)+O 2 (g)△H=+141kJ?mol -1
①×2-②+③得到:TiO 2 (s)+2Cl 2 (g)+2C(s)=TiCl 4 (s)+2CO(g)的△H=-80KJ/mol;
故答案为:TiCl 4 +2Mg=MgCl 2 +Ti;
TiO 2 (s)+2Cl 2 (g)+2C(s)=TiCl 4 (s)+2CO(g)的△H=-80KJ/mol;1年前查看全部
- 双氧水分解氧气化学反应速率如何测定
 动情木头人1年前2
动情木头人1年前2 -
 taitsi 共回答了18个问题
taitsi 共回答了18个问题 |采纳率83.3%可以考虑在一个封闭体系内进行反应,然后测量体系的压力,建立压力与反应速率的关系,即可测得速率.1年前查看全部
- 过氧化氢(俗名双氧水,化学式H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双
过氧化氢(俗名双氧水,化学式H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶双氧水溶液,用于制取O 2 .其瓶上标签的部分文字如图所示,试解答下列问题:
(1)这瓶溶液可稀释为溶质质量分数为6%的溶液约______克.据标签上的说明文字推测双氧水具有的性质有:______.
(2)根据化学方程式计算:这瓶溶液稀释后理论上可制得多少克氧气?
 何梓欣1年前1
何梓欣1年前1 -
 dumle 共回答了26个问题
dumle 共回答了26个问题 |采纳率92.3%(1)设 这瓶溶液可稀释为溶质质量分数为6%的溶液约 mg,
m×6%=500g×10%,
解答m=833.3g;
根据标签上的说明文字避光,低温密封保存,推测双氧水具有的性质为:见光、受热易分解;
故答案为:833.3; 见光、受热易分解;
(2)设生成的氧气质量为x,据题意得
2H 2 O 2
Mn O 2
.
2H 2 O+O 2 ↑
68 32
500×10%克 x克
∴
68
500×10%克 =
32
x克
解之得:x=23.5克
答:这瓶溶液稀释后理论上可制得23.5克氧气.1年前查看全部
- 某化学兴趣小组利用下图所示装置进行某些气体的实验室制法的研究,学生选用的药品有高锰酸钾固体、石灰石、盐酸、双氧水(H2O
某化学兴趣小组利用下图所示装置进行某些气体的实验室制法的研究,学生选用的药品有高锰酸钾固体、石灰石、盐酸、双氧水(H2O2)、二氧化锰、锌、稀硫酸,已知双氧水常温下是一种无色液体,它在MnO2的催化作用下能迅速分解放出氧气.

(1)甲同学要用高锰酸钾固体来制取O2,应选用______装置(填字母),该反应的化学方程式是2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4.
K2MnO4+MnO2+O2↑△ .
当O2收集满并取出集气瓶后,停止实验的正确操作步骤是______(填字母)
a.先撤导管后撤酒精灯 b.先撤酒精灯后撤导管
(2)乙同学用B装置制取了一瓶无色无味的气体(纯净物),你推测该气体可能是______或______,试用最简便的方法证实你的推测______. zhiguoluo1年前1
zhiguoluo1年前1 -
 狼行孤道 共回答了21个问题
狼行孤道 共回答了21个问题 |采纳率90.5%解题思路:(1)根据反应物状态和反应条件确定发生装置,进行选择,并据加热高锰酸钾制取氧气用排水法收集时的注意事项进行判断;高锰酸钾加热生成锰酸钾、二氧化锰和氧气分析.
(2)B装置是用向上排空气法收集,且制取该气体不需加热,有可能是用双氧水常温制取氧气、还有可能是大理石和稀盐酸常温反应制取二氧化碳,并据氧气的助燃性和二氧化碳不能支持燃烧进行检验.(1)用高锰酸钾制取氧气需要加热,故选发生装置A;当O2收集满并取出集气瓶后,要先移导管后熄灯,防止水倒吸引起试管炸裂;高锰酸钾加热生成锰酸钾、二氧化锰和氧气,故答案:A; 2KMnO4
△
.
.K2MnO4+MnO2+O2↑;a
(2)B装置是用向上排空气法收集,且制取该气体不需加热,有可能是用双氧水常温制取氧气、还有可能是大理石和稀盐酸常温反应制取二氧化碳,并据氧气的助燃性和二氧化碳不能支持燃烧进行检验;故答案:氧气;二氧化碳;用带火星的木条插入集气瓶中,复燃为氧气,熄灭为CO2点评:
本题考点: 氧气的制取装置;氧气的收集方法;制取氧气的操作步骤和注意点;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,了解发生和收集装置的选取方法及氧气、二氧化碳的相关性质等知识即可顺利解答.1年前查看全部
- 如何鉴别双氧水和蒸馏水?
 chars0081年前2
chars0081年前2 -
 zmm1980526 共回答了16个问题
zmm1980526 共回答了16个问题 |采纳率93.8%取样,向其中分别加入二氧化锰固体,放出气体的就是双氧水,无明显现象的就是蒸馏水.1年前查看全部
- 发射宇宙飞船的火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2),当它们混合时,即产生大量的氮气
发射宇宙飞船的火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水(H2O2),当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热,写出该反应的化学方程式______,该反应用于火箭推进器的优点是______.
 臻锋1年前3
臻锋1年前3 -
 liuliju 共回答了20个问题
liuliju 共回答了20个问题 |采纳率85%解题思路:根据偏二甲肼和双氧水反应水生成氮气和水蒸气进行分析;根据化学方程式所表现出的信息进行分析第二个空.液态肼和过氧化氢反应会生成水蒸气和氮气,故答案为:N2H4+2H2O2=4H2O↑+N2↑
因为从液态肼和双氧水反应的化学方程式可以看出,生成物只有水和氮气,不会造成粉尘等污染,故答案为:产物无污染.
故答案为:N2H4+2H2O2=4H2O↑+N2↑;产物无污染.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查学生对所学知识在特殊环境下的应用.学生需充分考虑特定因素,才能正确答题.1年前查看全部
- 双氧水(H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
双氧水(H 2 O 2 )既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.
(1)小明配制了5%的双氧水600g,则600g溶液中溶质为______克,溶剂为______克.
(2)小明倒出了300g双氧水溶液进行消毒,则剩下的溶液中溶质的质量分数为______. 上只角小开1年前1
上只角小开1年前1 -
 小言不分 共回答了28个问题
小言不分 共回答了28个问题 |采纳率82.1%(1)溶质=溶液的质量×溶液中溶质的质量分数=600g×5%=30g;溶剂=溶液-溶质=600g-30g=570g
(2)溶液具有均一性,所以剩下的溶液中的溶质质量分数不变.
故答案:(1)30;570;(2)5%1年前查看全部
- 水和双氧水中化学键的不同点如题
 那个冬天好热1年前2
那个冬天好热1年前2 -
 ronyalter 共回答了16个问题
ronyalter 共回答了16个问题 |采纳率62.5%H2O中只存在H-O之间的极性共价键
H2O2中不光存在H-O之间的极性共价键,还有O-O之间的非极性共价键.1年前查看全部
- 次氯酸钠和双氧水能发生反应吗次氯酸钠跟双氧水能发生反应吗?Naclo+H2O2—?
 日出彩虹1年前1
日出彩虹1年前1 -
 童话20068 共回答了16个问题
童话20068 共回答了16个问题 |采纳率81.3%NaClO+H2O2-----NaCl+H2O+O21年前查看全部
- (14分)过氧化氢H 2 O 2 ,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A
(14分)过氧化氢H 2 O 2 ,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H 2 O 2 的反应,回答相关问题:
A.Na 2 O 2 +2HCl= 2NaCl+H 2 O 2
B.Ag 2 O+ H 2 O 2 =2Ag+O 2 ↑+ H 2 O
C.2 H 2 O 2 ="2" H 2 O+O 2 ↑
D.3 H 2 O 2 +Cr 2 (SO 4 ) 3 +10KOH=2K 2 CrO 4 +3K 2 SO 4 +8 H 2 O
E.H 2 O 2 +MnSO 4 = MnO 2 + H 2 SO 4
F.H 2 O 2 + Fe 2+ + H + ="=" Fe 3+ + H 2 O
(1)上述反应不属于氧化还原反应的是(填代号)_____________。
(2)H 2 O 2 仅体现还原性的反应是(填代号) 。
(3)H 2 O 2 既体现氧化性又体现还原性的反应是(填代号) 。
(4)H 2 O 2 体现酸性的反应是(填代号) 。
(5)上述反应说明H 2 O 2 、Ag 2 O、K 2 CrO 4 氧化性由强到弱的顺序是: 。
(6)通过以上反应分析, H 2 O 2 常称为绿色氧化剂,原因是_______________________。
(7)请配平化学反应F,并画出电子转移情况。
H 2 O 2 + Fe 2+ + H + ="=" Fe 3+ + H 2 O
(8)由于H 2 O 2 有较强氧化性,能使某些有色试剂褪色,具有漂白作用,另外它还有弱酸性,某学生将H 2 O 2 溶液滴入含有酚酞的氢氧化钠溶液中,观察到溶液的红色消失。为了探究溶液褪色的原因,该学生提出了两种假设,然后又设计了一个简单的实验方案,以验证这两种假设。请回答:
(A)该学生提出的两种假设是:
假设①___________________________________________;
假设② _________________________________ 。
(B)将该学生设计的简单实验方案、预测的实验现象及结论填入下表(结论部分只需填①或②):简单实验方案 预测的实验现象 结论 假设____成立 假设____成立  生ff契阔与子同说1年前0
生ff契阔与子同说1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 某同学在做了“用双氧水和二氧化锰制取氧气”的实验后,展开了思考与探究:催化剂二氧化锰的用量对反应速率有没有影响呢?
某同学在做了“用双氧水和二氧化锰制取氧气”的实验后,展开了思考与探究:催化剂二氧化锰的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30毫升10%的H2O2溶液,使用不同量的二氧化锰粉末做催化剂,测定每次收集到0.96克氧气时所用的时间,结果如下:(其他实验条件均相同)
实验次序 1 2 3 4 5 6 7 8 9 10
二氧化锰粉末用量/克
0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0
所用时间/秒
17 8 7 5 4 3 2 2 2 2
(1)从表中的数据看出:二氧化锰的用量对反应速率是有影响的,请描述二氧化锰的用量对反应速率的影响是______ .
(2)如果在实验中忘了加入二氧化锰.下列对实验结果的描述正确的是( )
A、不影响化学反应速度
B、反应速度慢,产生氧气比应有的量少
C、产生氧气总量不少,但反应速度慢
D、无法产生氧气
(3)实验中要产生0.96克氧气至少需要多少克H2O2?(通过化学方程式计算说明) leocw1年前1
leocw1年前1 -
 lcs9 共回答了23个问题
lcs9 共回答了23个问题 |采纳率87%(1)一定量的二氧化锰可以促进反应的进行
(2)C
(3)2h2o2=2h2o+o2
68 32
x 0.96
x=2.04g1年前查看全部
- 介绍一下过氧化氢的化学性质!顺便问一下:双氧水是弱电解质吗?
 好月1年前2
好月1年前2 -
 luyi0507 共回答了15个问题
luyi0507 共回答了15个问题 |采纳率86.7%过氧化氢,俗称双氧水,分子式H2O2,是除水外的另一种氢的氧化物.化学性质不稳定,一般以30%或60%的水溶液形式存放.过氧化氢有很强的氧化性,且具弱酸性.
过氧化氢是非常强的氧化剂,它和其他氧化剂的标准电极电势值列在右面,值越高代表氧化性越强:
分解反应
过氧化氢可自发分解歧化生成水和氧气:
2 H2O2 → 2 H2O + O2
该反应在热力学上自发进行:ΔHo为−98.2 kJ·mol−1,ΔGo为−119.2 kJ·mol−1,ΔS为70.5 J·mol−1·K−1.重金属离子Fe2+、Mn2+、Cu2+等对过氧化氢的分解有催化作用.过氧化氢在酸性和中性介质中较稳定,在碱性介质中易分解.用波长为320~380nm的光照射会使过氧化氢分解速度加快,故过氧化氢应盛于棕色瓶中并放在阴凉处.
H2O2与Fe2+的混合溶液称为Fenton试剂.某些离子如Fe2+、Ti3+催化下,过氧化氢分解反应会生成自由基中间体HO·(羟基自由基)和HOO·.
一般使用的双氧水中都会含有一定量的稳定剂,以减少过氧化氢的分解.常用的稳定剂包括:锡酸钠、焦磷酸钠和有机亚磷酸酯.
氧化还原反应
过氧化氢可在水溶液中氧化或还原很多无机离子.用作还原剂时产物为氧气,用作氧化剂时产物为水.例如酸性溶液中,过氧化氢可将Fe2+氧化为Fe3+:
2 Fe2+(aq) + H2O2 + 2 H+(aq) → 2 Fe3+(aq) + 2H2O(l)
与过氧化氢作用,亚硫酸根(SO32−)可被氧化为硫酸根(SO42−),高锰酸钾在酸性溶液中会被还原为Mn2+.由于标准电极电势的缘故,反应在不同pH环境下进行的方向可能不同,如碱性溶液中,过氧化氢会将Mn2+氧化为MnIV,以MnO2形式生成.
过氧化氢还原次氯酸钠的反应可用于在实验室中制备氧气:
NaOCl + H2O2 → O2 + NaCl + H2O
有机化学中,过氧化氢常用作氧化剂,可将硫醚氧化为亚砜.甲基苯基硫醚与其反应时,会被氧化为甲基苯基亚砜,以甲醇作溶剂或三氯化钛催化,产率为99%:
Ph-S-CH3 + H2O2 → Ph-S(O)-CH3 + H2O
过氧化氢的碱性溶液可用于富电子烯烃(如丙烯酸)的环氧化反应,以及在硼氢化-氧化反应第二步中氧化烷基硼至醇.
过氧化氢与很多无机或有机化合物反应时,过氧链保留并转移到另一分子上,生成新的过氧化物:
过氧化氢在低温下与铬酸或重铬酸盐酸性溶液反应时,会生成不稳定的蓝色过氧化铬CrO(O2)2,可用乙醚或戊醇萃取.水溶液中过氧化铬很快分解为氧气和含铬离子.
过氧化氢与硼砂反应会生成过硼酸钠,可用作消毒剂:
Na2B4O7 + 4 H2O2 + 2 NaOH → 2 Na2B2O4(OH)4 + H2O
过氧化氢可生成很多含有O22-过氧根离子的无机盐类,其中比较重要的如过氧化钙、过氧化钠和过氧化镁.
与羧酸(RC=O-OH)反应,生成具氧化性的过氧酸(RC=O-O-OH),可用于烯烃环氧化反应等用途.与丙酮反应生成炸药三过氧化三丙酮(TATP),与臭氧反应生成三氧化二氢,与尿素反应生成过氧化尿素.
过氧化氢与三苯基氧化膦生成酸碱加合物,有些反应中用作过氧化氢的等同试剂.
与水相比,过氧化氢的碱性要弱得多,只有与很强的酸反应才会生成加合物.超强酸HF/SbF5可将过氧化氢质子化,生成含[H3O2]+离子的产物.1年前查看全部
- 氧化钙与水会不会反应?如果要,氧化钙会和双氧水反应吗?如果要,
 碧露zz1年前1
碧露zz1年前1 -
 smweb 共回答了22个问题
smweb 共回答了22个问题 |采纳率90.9%CaO+H2O====Ca(OH)21年前查看全部
- 双氧水制取氧气为什么放热RT最好用初中知识说明
 小荷荔枝10201年前3
小荷荔枝10201年前3 -
 ww花火 共回答了18个问题
ww花火 共回答了18个问题 |采纳率88.9%应为过氧化氢制取氧气是氧化反应
1.物质与氧发生的反应叫氧化反应;得电子的作用叫还原.狭义的氧化指物质与氧化合;还原指物质失去氧的作用.氧化时氧化值升高;还原时氧化值降低.氧化、还原都指反应物(分子、离子或原子).氧化也称氧化作用或氧化反应.有机物反应时把有机物引入氧或脱去氢的作用叫氧化;引入氢或失去氧的作用叫还原.物质与氧缓慢反应缓缓发热而不发光的氧化叫缓慢氧化,如金属锈蚀、生物呼吸等.剧烈的发光发热的氧化叫燃烧.
2.一般物质与氧气发生氧化时放热,个别可能吸热如氮气与氧气的反应.电化学中阳极发生氧化,阴极发生还原.
所以双氧水制取氧气会放热.1年前查看全部
- 双氧水中氧气为负一价还是氢为正一价
双氧水中氧气为负一价还是氢为正一价
上面打错了 应该为 双氧水中氧为负一价还是氢为正二价 abcabc66771年前3
abcabc66771年前3 -
 helenyaya 共回答了16个问题
helenyaya 共回答了16个问题 |采纳率87.5%H是正1价
O是负1价1年前查看全部
- 用双氧水漂过的食物吃了会有害吗?
用双氧水漂过的食物吃了会有害吗?
哪些食品被双氧水漂过的机率高?
曾阅:
按照《食品添加剂使用卫生标准》有关规定,允许食品级双氧水在食品生产中作为加工助剂使用,在制成成品前应该清除,如果清除不掉应严格控制在规定的范围内.
在国际权威机构认可的限量范围内,食品级双氧水不仅允许使用,也是较为安全的.根据***用的动物种群与人群安全剂量的换算比例(即100比1),则人体每天饮用含有0.26毫克至0.37毫克/公斤双氧水的饮用水是安全的,不会出现任何毒副作用.人群平均体重按照65公斤计算,则相当于每天饮用含有16.9毫克至24.05毫克的双氧水的饮用水是安全的.由于双氧水具有强烈的氧化特性,美国、加拿大、澳大利亚以及新西兰等国家的食品界,均将食品级双氧水作为漂白剂,加工处理某些食物,比如面粉、食用油及蛋白.双氧水也可作为抗菌剂,在牛奶等食物中使用.同时,双氧水可用作消毒剂,用作食物包装等材质的消毒.美国食品药品监督管理局认定,食品级双氧水是一般安全性物质,可以广泛用作直接或间接的食品添加剂 Mr宗1年前1
Mr宗1年前1 -
 ss1309 共回答了19个问题
ss1309 共回答了19个问题 |采纳率94.7%任何东西过量都是不好的,所谓“万物皆有毒”嘛
双氧水一是处理不好有残留,二是双氧水有可能和有的物质反应而产生有害物质
在市场上买的,只要是白得不是本来颜色的东西,都有可能是双氧水泡过的
特别是肉制品,比如猪头,猪肚,百叶
现在纯净水也不允许用臭氧杀毒了.1年前查看全部
- 为了配制实验用的680克5%的过氧化氢溶液,需要20%的双氧水多少克?加水多少ml?
 lanmda1年前1
lanmda1年前1 -
 xc0629 共回答了18个问题
xc0629 共回答了18个问题 |采纳率88.9%m=680*5%/20%=170g
V=680-170=510mL1年前查看全部
- 双氧水发生分解反应的化学方程式
 石头我们回家吧1年前8
石头我们回家吧1年前8 -
 dlut_apple 共回答了19个问题
dlut_apple 共回答了19个问题 |采纳率84.2%2H2O2==MnO2==2H20+O2 ↑1年前查看全部
- 双氧水在常温下不加任何催化剂产生氧气速率多少
 羽习习1年前1
羽习习1年前1 -
 oo上网 共回答了21个问题
oo上网 共回答了21个问题 |采纳率95.2%和压强 表面积等有关1年前查看全部
- 甲醇 乙醇 硝酸 硫酸 双氧水可以用来清洁什么
甲醇 乙醇 硝酸 硫酸 双氧水可以用来清洁什么
清洗什么物品 不把斋的和尚被封1年前2
不把斋的和尚被封1年前2 -
 vampire32167 共回答了17个问题
vampire32167 共回答了17个问题 |采纳率70.6%甲醇 乙醇清洗油污及其他有机物
硝酸洗可除去银镜、铜镜等物质
硫酸洗可除去金属、金属氧化物
双氧水可以除去带有还原性的物质,1年前查看全部
- 下列说法中描述物质的化学性质的是( ) A.水受热变成水蒸气 B.双氧水受热易分解 C.过氧化氢是一种无色液体 D.二
下列说法中描述物质的化学性质的是( ) A.水受热变成水蒸气 B.双氧水受热易分解 C.过氧化氢是一种无色液体 D.二氧化锰不溶于水  3839211年前1
3839211年前1 -
 寒水依痕的梦幻 共回答了20个问题
寒水依痕的梦幻 共回答了20个问题 |采纳率95%A、水受热变成水蒸气的过程中只是水的状态发生改变,没有新物质生成,属于物理变化,故选项错误.
B、双氧水受热易分解,需要通过化学变化才能表现出来,属于化学性质,故选项正确.
C、过氧化氢是一种无色液体,描述的是颜色、状态,不需要通过化学变化就能表现出来,属于物理性质,故选项错误.
D、二氧化锰不溶于水,描述的是溶解性,不需要通过化学变化就能表现出来,属于物理性质,故选项错误.
故选B.1年前查看全部
- 下列关于双氧水(H 2 O 2 )和水(H 2 O)的叙述中不正确的是( ) A.它们都由两种元素组成 B.它们的分子
下列关于双氧水(H 2 O 2 )和水(H 2 O)的叙述中不正确的是( ) A.它们都由两种元素组成 B.它们的分子中都含有氢分子 C.它们发生分解反应时都产生氧气 D.它们都属于氧化物  gghhyaoyun1年前1
gghhyaoyun1年前1 -
 luqingxiang 共回答了23个问题
luqingxiang 共回答了23个问题 |采纳率82.6%A、由双氧水(H 2 O 2 )和水(H 2 O)的组成可知:两物质均有氢氧两种元素组成.
B、双氧水(H 2 O 2 )和水(H 2 O)都是纯净物,不可能含有其它物质的分子;
C、双氧水分解会生成氧气和水,水的分解可生成氢气与氧气;
D、两者均是由两种元素组成且其中一种是氧元素的纯净物,故都属于氧化物;
故选B.1年前查看全部
- 次氯酸钠溶液,氯化铝溶液,双氧水,哪个不具有杀菌消毒作用?
 奕奕铃1年前1
奕奕铃1年前1 -
 天齿铜涯 共回答了15个问题
天齿铜涯 共回答了15个问题 |采纳率86.7%氯化铝溶液1年前查看全部
- 双氧水是酸性的还是碱性的?
 紫绶高轩1年前6
紫绶高轩1年前6 -
 爱在枫季 共回答了19个问题
爱在枫季 共回答了19个问题 |采纳率89.5%双氧水也即是过氧化氢是二元弱酸,具有酸性.
过氧化氢的分子结构 过氧化氢是含有极性键和非极性键的极性分子,其结构式为H—O—O—H,电子式为:H:O:O:H 2、 过氧化氢的物理性质 过氧化氢是一种无色黏稠的液体,它的水溶液俗称双氧水.1年前查看全部
- 氢氧化钙和双氧水在水存在的条件下生成CaO2•8H2O,它在120℃时完全分解为CaO2等.有关化学方程式
氢氧化钙和双氧水在水存在的条件下生成CaO2•8H2O,它在120℃时完全分解为CaO2等.有关化学方程式
1----------------------
2---------------------- 殷杰1年前1
殷杰1年前1 -
 超级棒棒糖 共回答了21个问题
超级棒棒糖 共回答了21个问题 |采纳率90.5%Ca(OH)2 + H2O2 + 6H2O ---> CaO2.8H2O
CaO2.8H2O ---> CaO2 + 8H2O1年前查看全部
- 双氧水加NaOH再加MnSO4.之后往沉淀中加硫酸再加双氧水 的反应方程式
双氧水加NaOH再加MnSO4.之后往沉淀中加硫酸再加双氧水 的反应方程式
快 omeag1年前1
omeag1年前1 -
 性情小子 共回答了17个问题
性情小子 共回答了17个问题 |采纳率82.4%MnSO4+H2O2+2NaOH=Na2SO4+2H2O+MnO2/
4MnO2+H2O2+2H2SO4=2MnSO4+2HMnO4+2H2O
MnO2实际上是MnMnO4.
MnO4(2-)酸根在稀释的过程中会发生歧化反应,就是自身氧化还原反应,生成Mn2+和MnO4-1年前查看全部
- 治牙用双氧水,生理盐水,和次氯酸钠,都有哪些用途
 会唱歌的草1年前2
会唱歌的草1年前2 -
 robbert922 共回答了14个问题
robbert922 共回答了14个问题 |采纳率92.9%双氧水 次氯酸钠 杀菌消毒
生理盐水 正常冲洗 其实用不着 用蒸馏水就行1年前查看全部
- 偏二甲肼和双氧水反应化学式
 不是谁都能爱你1年前1
不是谁都能爱你1年前1 -
 心事如烟 共回答了15个问题
心事如烟 共回答了15个问题 |采纳率93.3%C2H8N2+8H2O2=2CO2(气体符号)+12H2O+N2(气体符号)1年前查看全部
- 双氧水可以转化成水吗?
 天啊救救我吧1年前4
天啊救救我吧1年前4 -
 贝儿爽爽 共回答了26个问题
贝儿爽爽 共回答了26个问题 |采纳率84.6%可以1年前查看全部
- 向等质量双氧水溶液中分别加入绿豆大小的氯化铁和硫酸铜固体,比较二者的催化能力,正确吗?
向等质量双氧水溶液中分别加入绿豆大小的氯化铁和硫酸铜固体,比较二者的催化能力,正确吗?
如果错了,错在哪里呢? lords52661年前1
lords52661年前1 -
 太平洋小宝 共回答了11个问题
太平洋小宝 共回答了11个问题 |采纳率100%错,影响反应速率的条件有反应物浓度,温度,压强,接触面大小等.控制变量法除变量外,其它条件必须相同,这里的变量是催化剂种类,所以必须保证双氧水的浓度相同,而不是质量相同.1年前查看全部
- 帮我写几个离子方程式,硫酸亚铁中加入经硫酸酸化的双氧水小苏打溶液与烧碱溶液反应氯气通入水中三氯化铁与氢碘酸反应氢氧化钡溶
帮我写几个离子方程式,
硫酸亚铁中加入经硫酸酸化的双氧水
小苏打溶液与烧碱溶液反应
氯气通入水中
三氯化铁与氢碘酸反应
氢氧化钡溶液与稀硫酸的反应
用氨水吸收过量二氧化碳
向漂白粉中通入二氧化碳气体
碳酸氢钠中加入少量氢氧化钡溶液
氨水与硝酸作用
硫化亚铁与稀硝酸作用
氯化铁制备氢氧化铁胶体 Jiang_linyan1年前1
Jiang_linyan1年前1 -
 zhanglia 共回答了23个问题
zhanglia 共回答了23个问题 |采纳率82.6%2Fe2+ + H2O2 + 2H+ = 2Fe3+ + 2H2O
HCO3- + OH- = CO32- + H2O
Cl2 + H2O = Cl- + HClO + H+
2Fe3+ + 2I- = 2Fe2+ +I2↓
OH- + H+ =H2O
CO2 + NH3·H2O = NH4+ + HCO3-
Ca2+ + 2ClO- +H2O + CO2 = CaCO3↓+2HClO
或ClO- + H2O + CO2 = HCO3- + HClO
HCO3- + Ba2+ + OH- = BaCO3↓+H2O
NH3·H2O +H+ =NH4+ + H2O
FeS + 6H+ + 3NO3-=Fe3+ + S + 3NO2↑ + 3H2O
Fe3+ + 3OH- = Fe(OH)31年前查看全部
- 加热94.8g 高猛酸钾放出的氧气与多少质量的双氧水分解生成的氧气质量相等?
 aa的aass1年前2
aa的aass1年前2 -
 right_t 共回答了25个问题
right_t 共回答了25个问题 |采纳率92%设X克双氧水,依照化学方程式;
2KMnO4---O2---2H2O2
158 34
94.8 X
X=20.41年前查看全部
- 我能做什么化学实验,求教我有硫酸铜,氢氧化钠,硼酸,小苏打,柠檬酸,双氧水,草酸,DBP,还有一点电池里抠出来的MnO2
 cn_lzy1年前1
cn_lzy1年前1 -
 记忆无恒 共回答了18个问题
记忆无恒 共回答了18个问题 |采纳率88.9%能做双氧水分解制氧气.将二氧化锰丢进双氧水即可获得氧气.
能用小苏打跟柠檬酸调汽水喝,不过你得保证你的原料是食品级.
你的电池没扔吧?可以用电池皮(锌皮)跟硫酸铜玩置换.没有危险.
DBP是邻苯二甲酸丁二酯.跟氢氧化钠可以玩水解反应,不过条件难控制,要恒温,估计你家的烤蛋糕的箱子不行.
草酸跟小苏打可以制二氧化碳,不过不太好玩,二氧化碳干不了啥.氧气还能助燃啥的,二氧化碳平时玩,确实不好玩啊.
硼酸就用来急救吧,强碱掉身上了,用硼酸溶液3%-5%洗洗.
暂时想到就这么多,不过你还要买点其他的玻璃仪器,或者用洗干净的玻璃罐头瓶冒充一些也可以的.1年前查看全部
大家在问
- 1英语翻译In beijing it is one o’clonk.People aren’t having dinner
- 2当X=( )时,3÷X这个算式无意义?
- 3如何提高英语听力我在听听力时老感觉单词很熟,但就是想不起什么意思,看了答案恍然大悟.我单词还比较记得住,就是听力,拼的出
- 4掩饰用英语怎么说
- 5用地球妈妈流泪了.展开联想写一段话.(不超过100字)
- 6一个,密码箱的密码,每个数位上的数都是从0-9的自然数,若要使不知道密码的人一次就拨对密码的概率<1/2010,则密码的
- 75x+8x-13y+13y+(8z-3a+3a-4z) 其中X=3 Y=-2 Z=1.4 怎样解
- 8一个星球的半径是地球的2倍,质量是地球的16倍,那么该星球的重力加速度是地球重力加速度的多少倍?
- 9下列事件中,是必然事件是( ) A.-个星期有9天 B.小红在元月调考中,数学会获得
- 10"知己知彼" 包含的哲学原理"知己知彼 百战不殆"这句话中包含了哪些哲学原理?只要有关的原理 就都列出来 大致的说一下理
- 11在实数范围内分解因式:3x2-6x+1=______.
- 12电阻 电压 电流 电功率 电功之间的关系
- 13关于n阶无穷小的乘积问题(微积分/数学全书)
- 14三单形式,he,she,it后面的动词要加s或es,哪名字后面的动词呢?比如Liming.
- 15某人要到9千米远的地方去,走了一小时后行走有些困难,后一时走的路程都是前一时走的1/2,这样走了4小时才
