溴元素有多种化合价.下列单质或化合物中,溴元素化合价最低的是( )
 rainyday_liang2022-10-04 11:39:542条回答
rainyday_liang2022-10-04 11:39:542条回答A. KBrO3
B. MgBr2
C. Br2
D. HBrO4

已提交,审核后显示!提交回复
共2条回复
 孤竹虚空0359 共回答了13个问题
孤竹虚空0359 共回答了13个问题 |采纳率92.3%- 解题思路:根据在化合物中正负化合价代数和为零计算出指定元素化合价和单质中元素的化合价为0,即可解答本题.
A、KBrO3中溴元素的化合价为:(+1)+a+(-2)×3=0,则a=+5;
B、MgBr2中溴元素的化合价为:+2+2b=0,则 b=-1;
C、根据单质中元素的化合价为0;所以Br2中溴元素的化合价为0;
D、HBrO4中溴元素的化合价为::(+1)+d+(-2)×4=0,则d=+7;
通过比较B中溴元素的化合价最低,故选B.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生对单质中元素的化合价为0和元素化合价的计算方法的理解与掌握,并能灵活应用于解题的能力. - 1年前
 真嗣君 共回答了168个问题
真嗣君 共回答了168个问题 |采纳率- B负1价
- 1年前
相关推荐
- 烫发用的定型剂主要成分是溴酸钠(NaBrO3)对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为______
烫发用的定型剂主要成分是溴酸钠(NaBrO3)对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为______价.
 行走一生1年前1
行走一生1年前1 -
 coldrain9 共回答了19个问题
coldrain9 共回答了19个问题 |采纳率94.7%解题思路:根据在化合物中正负化合价代数和为零,结合溴酸钠(NaBrO3)的化学式进行解答本题.钠元素显+1价,氧元素显-2价,设溴元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5.
故答案为:+5.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- 烫发用的定型剂主要成分是溴酸钠(NaBrOx),对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为+5,则x
烫发用的定型剂主要成分是溴酸钠(NaBrOx),对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为+5,则x( )
A.1
B.2
C.3
D.4 susanYL21年前1
susanYL21年前1 -
 小幺琳琳 共回答了19个问题
小幺琳琳 共回答了19个问题 |采纳率84.2%解题思路:根据在化合物中正负化合价代数和为零,结合溴酸钠(NaBrO3)的化学式进行解答本题.钠元素显+1价,氧元素显-2价,溴元素的化合价是+5,根据在化合物中正负化合价代数和为零,可得:(+1)+(+5)+(-2)x=0,则x=3.
故选:C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- 溴酸钠中 溴元素(Br)的化合价是多少?
 LUYINGDA1年前1
LUYINGDA1年前1 -
 kyachen 共回答了17个问题
kyachen 共回答了17个问题 |采纳率100%溴酸钠化学式为NaBrO3,其中Na化合价为+1价,O的化合价为-2价,根据化合价总数为零,设Br的化合价为x,则+1+x-2*3=0,所以x=+51年前查看全部
- 反应物中,溴元素既被氧化,又被还原的方程式
 沙漠佛祖02021年前1
沙漠佛祖02021年前1 -
 luming1014 共回答了14个问题
luming1014 共回答了14个问题 |采纳率92.9%溴加水:Br2+H2O=HBr+HBrO1年前查看全部
- 为了鉴定溴乙烷中溴元素的存在,试分析①~⑥的各步实验,其中操作顺序合理的是-----------------------
为了鉴定溴乙烷中溴元素的存在,试分析①~⑥的各步实验,其中操作顺序合理的是----------------------------------------------------------------------------------(B)
①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④加入蒸馏水 ⑤用HNO3酸化溶液 ⑥加入NaOH溶液醇溶液
A.①②③⑤ B.②③⑤① C.⑥③⑤① D.④②⑤③
为什么不能先消去(选c)?
HNO3不是会氧化Br2吗?
那如何生成沉淀?
Br2与HNO3不反应? 依凡烟1年前1
依凡烟1年前1 -
 欧阳天平 共回答了23个问题
欧阳天平 共回答了23个问题 |采纳率95.7%严格说起来,应该可以的.
实验方法中卤代烃加氢氧化钠溶液的目的是使卤代烃中的卤素原子变为卤离子,如果卤代烃能在氢氧化钠醇溶液中发生消去反应生成卤离子,则可以用与氢氧化钠醇溶液共热代替氢氧化钠水溶液;否则不可以替换为氢氧化钠醇溶液.1年前查看全部
- 求教溴乙烷中溴元素的检验,要证明溴乙烷中溴的存在,下列各操作步骤顺序正确的是①加入硝酸银溶液 ②加入氢氧化钠水溶液 ③加
求教溴乙烷中溴元素的检验,
要证明溴乙烷中溴的存在,下列各操作步骤顺序正确的是
①加入硝酸银溶液 ②加入氢氧化钠水溶液 ③加热 ④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入氢氧化钠醇溶液
A.④③①⑥ B.②③⑤① C.④⑥③① D.⑥③⑤①
正确答案只有B选项,请问D选项为什么不正确.
加入氢氧化钠醇溶液,加热后发生消去反应,也能生成溴离子,但为什么不对呢? kingjiawei1年前4
kingjiawei1年前4 -
 winwinyy 共回答了13个问题
winwinyy 共回答了13个问题 |采纳率92.3%1乙烷中的溴是成化合态无法用AG检验出拉
2加入加入氢氧化钠水溶液置换出BR离子
3因为加了氢氧化钠和硝酸银生成ag(oh)2
影响鉴别所以加入硝酸使PH为中性
4加入硝酸银
卤化银溶于有机溶解中1年前查看全部
- 海水是一种重要的自然资源.海水中溴元素以Br-形式存在,从海水中提取的溴约占世界1\3.
 DTS55052691年前1
DTS55052691年前1 -
 lhhl2005 共回答了16个问题
lhhl2005 共回答了16个问题 |采纳率87.5%1、原子序数:35,第四周期 VIIA
2、2NaBr+Cl2===Br2+2NaCl
3、Br2 + SO2 + 2H2O=2HBr +H2SO4
4、温度太低的话蒸发比较慢,温度太高的话水蒸气也会出来不少的,影响纯度.
5、第一部分溴的含量比较低,直接提取不经济,最好先富集后再提取.1年前查看全部
- 溴元素的化学性质与哪些元素的化学性质最相似?
 windgone13101年前3
windgone13101年前3 -
 蓝色沙漠ly 共回答了16个问题
蓝色沙漠ly 共回答了16个问题 |采纳率100%同主族元素跟它相似,Br位于第四周期VIIA族,其它:氟、氯、碘1年前查看全部
- 教材显示地球上99%的溴元素存在于海洋中,且海水中Br-的含量一般为0.067g•L-1.从海水中提取溴的工业流程如下:
教材显示地球上99%的溴元素存在于海洋中,且海水中Br-的含量一般为0.067g•L-1.从海水中提取溴的工业流程如下:

(1)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是______.
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:______.
(3)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转化成化合态的溴,其目的是______.
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是______.
a.乙酸b.四氯化碳c.酒精d.苯. lyw_8121年前1
lyw_8121年前1 -
 nilulu1 共回答了11个问题
nilulu1 共回答了11个问题 |采纳率90.9%解题思路:流程分析可知海水通过一定方法淡化得到淡水和卤水,卤水加入氧化剂氧化溴离子为单质溴,通入热空气或水蒸气吹出Br2,利用的是溴单质的易挥发性,再利用酸溶液中溴酸根离子和溴离子发生氧化还原反应得到溴单质;
(1)溴单质具有易挥发性;
(2)溴与二氧化硫水溶液反应生成硫酸和溴化氢;
(3)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质;
(4)依据萃取的原则是萃取剂不溶于水,在水溶液中分层;(1)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是易挥发;
故答案为:挥发性;
(2)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的化学方程式为:
Br2+SO2+2H2O=2HBr+H2SO4;
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(3)步骤I中溴单质的浓度低,若直接蒸馏,生产成本高;经步骤Ⅱ、Ⅲ,实际上是将溴水浓缩,使溴元素的富集;
故答案为:溴元素的富集;
(4)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是和水溶液互溶的试剂;
a.乙酸乙溶于水,不能做萃取剂,故a错误;
b.四氯化碳不溶于水,可以萃取溴单质,故b正确;
c.酒精极易溶于水,不能分层,不能做萃取剂,故c错误;
d.苯是不溶于水比水轻的试剂,可以做萃取溴单质的萃取剂,故d正确;
故答案为:ac;点评:
本题考点: 海水资源及其综合利用.
考点点评: 本题考查了海水资源的利用分析判断,主要是流程操作的理解应用,掌握基础是关键,题目难度中等.1年前查看全部
- 已知溴元素的元素符号为Br,溴原子的原子结构示意图为.问:
已知溴元素的元素符号为Br,溴原子的原子结构示意图为
 .问:
.问:
①X的值为______.该元素的原子在化学反应中易______电子.
②溴元素的化学性质与下列哪种元素的化学性质最相似______(填序号).
A、 B、
B、 C、
C、
③溴化氢的化学式可能是______. aibuaini1年前1
aibuaini1年前1 -
 ad4531cd4e025bda 共回答了20个问题
ad4531cd4e025bda 共回答了20个问题 |采纳率90%解题思路:原子中质子数等于电子数,而质子数不等于电子数的是离子.离子又分为阳离子和阴离子.阳离子中质子数大于电子数,阴离子中质子数小于电子数.①原子中,质子数等于核外电子数,溴原子核外电子数为35,所以核内质子数为35.故X为35;该元素最外层有7个电子,在化学反应中易得到一个电子成为阴离子;
②最外层电子数相等,元素的化学性质相似,故选B
③溴化氢的化学式为HBr
故答案为:①35;得②B;③HB点评:
本题考点: 原子结构示意图与离子结构示意图;核外电子在化学反应中的作用;化学式的书写及意义.
考点点评: 质子数决定元素的种类,而最外层电子数决定元素的化学性质.当最外层电子数小于4个时,易失去最外层电子,达到8个电子的稳定结构.当最外层电子数大于4个时,易得到电子,达到8个电子的相对稳定结构.1年前查看全部
- 高一必修2化学题将一定量氯气通入250毫升KBr溶液中 反应后将固体增干 测得固体中含有溴元素10克 且K+与Cl-的物
高一必修2化学题
将一定量氯气通入250毫升KBr溶液中 反应后将固体增干 测得固体中含有溴元素10克 且K+与Cl-的物质的量之比为2比1求
1)通入氯气的体积标准状况下
2)原溴化钾溶液的物质的量浓度 44771年前2
44771年前2 -
 紫紫小猪猪 共回答了18个问题
紫紫小猪猪 共回答了18个问题 |采纳率100%思路:根据溴元素的质量可计算出他的物质的量,再根据最后一句话可得知在剩余的固体里溴化钾和氯化钾的物质的量相等,这就说明了参加卤素间置换反应的KBr只有一半.再根据相关的方程式计算就行了.后面的就比较简单了,如果不懂可以再问.1年前查看全部
- 溴化镁中溴元素的化合价是 feso4中fe元素的化合价是
 qian_john1年前1
qian_john1年前1 -
 小小雅阁布 共回答了16个问题
小小雅阁布 共回答了16个问题 |采纳率93.8%溴化镁 中溴是-1 硫酸亚铁中 Fe是+21年前查看全部
- 下列离子方程式与所述事实相符且正确的是( ) A.溴乙烷中滴入AgNO 3 溶液检验其中的溴元素:Br - +Ag +
下列离子方程式与所述事实相符且正确的是( ) A.溴乙烷中滴入AgNO 3 溶液检验其中的溴元素:Br - +Ag + ═AgBr↓ B.漂白粉溶液露置在空气中会失效:ClO - +CO 2 +H 2 O═HClO+HCO 3 - C.氯化铝溶液中加入过量氨水:Al 3+ +4NH 3 •H 2 O═AlO 2 - +4NH 4 + +2H 2 O D.CH 3 COOH是弱电解质:CH 3 COO - +H 2 O⇌CH 3 COOH+OH -  gougouee1年前1
gougouee1年前1 -
 rechelwong 共回答了19个问题
rechelwong 共回答了19个问题 |采纳率94.7%A.溴乙烷中滴入AgNO 3 溶液不反应,不能写离子反应,故A错误;
B.漂白粉溶液露置在空气中会失效的离子反应为Ca 2+ +2ClO - +CO 2 +H 2 O═2HClO+CaCO 3 ↓、2HClO
光照
.
2H + +Cl - +O 2 ↑,故B错误;
C.氯化铝溶液中加入过量氨水的离子反应为Al 3+ +3NH 3 •H 2 O═Al(OH) 3 ↓+3NH 4 + ,故C错误;
D.CH 3 COOH是弱电解质,则醋酸根离子水解的离子反应为CH 3 COO - +H 2 O⇌CH 3 COOH+OH - ,故D正确;
故选D.1年前查看全部
- 下列文字表述与反应方程式对应且正确的是 A.溴乙烷中滴入AgNO 3 溶液检验其中的溴元素: B.用醋酸除去水垢: C.
下列文字表述与反应方程式对应且正确的是
A.溴乙烷中滴入AgNO 3 溶液检验其中的溴元素: 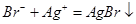
B.用醋酸除去水垢: 
C.苯酚钠溶液中通入少量 
D.实验室用液溴和苯在催化剂作用下制溴苯: 
 在雪地上撒点野1年前1
在雪地上撒点野1年前1 -
 超建 共回答了23个问题
超建 共回答了23个问题 |采纳率91.3%D
1年前查看全部
- 证明溴乙烷中溴元素的存在要怎样操作?外加文字解释啊.
 扬华1年前2
扬华1年前2 -
 紫诺窈 共回答了18个问题
紫诺窈 共回答了18个问题 |采纳率77.8%先加碱并加热,再加入硝酸酸化的硝酸银,若产生淡黄色沉淀,则含有溴元素.
这里一定要先加碱加热,是溴乙烷水解,产生溴离子.
希望对你有所帮助,亲!欢迎追问!1年前查看全部
- 有关溴的反应 化学方程式1 反应物中,溴元素被氧化2 反应物中,溴元素被还原3 反应物中,溴元素既被氧化又被还原4 反应
有关溴的反应 化学方程式
1 反应物中,溴元素被氧化
2 反应物中,溴元素被还原
3 反应物中,溴元素既被氧化又被还原
4 反应物中,溴元素既未被氧化又未被还原
我问的是关于这四种情况,分别举一个例子! mhjlzdy1年前2
mhjlzdy1年前2 -
 刘备先师 共回答了15个问题
刘备先师 共回答了15个问题 |采纳率93.3%1.
Cl2 + 2NaBr == 2NaCl + Br2
2.
Br2 + 2NaI == 2NaBr + I2
3.
Br2 + H2O HBr + HBrO (可逆)
4.
CaBr2 + Na2CO3 == CaCO3(沉淀) + 2NaB1年前查看全部
- 求教溴乙烷中溴元素的检验,要证明溴乙烷中溴的存在,下列各操作步骤顺序正确的是 ①加入硝酸银溶液 ②加入氢氧化钠水溶液 ③
求教溴乙烷中溴元素的检验,
要证明溴乙烷中溴的存在,下列各操作步骤顺序正确的是
①加入硝酸银溶液 ②加入氢氧化钠水溶液 ③加热 ④加入蒸馏水 ⑤加稀硝酸至溶液呈酸性 ⑥加入氢氧化钠醇溶液
A.④③①⑥ B.②③⑤① C.④⑥③① D.⑥③⑤①
正确答案只有B选项,请问D选项为什么不正确. 深圳蜀王1年前1
深圳蜀王1年前1 -
 上落千栀001 共回答了23个问题
上落千栀001 共回答了23个问题 |采纳率87%不能用醇溶液,溴离子可以和醇反应1年前查看全部
- (2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
 (2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
(2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
(1)x的值为______.
(2)溴元素的化学性质与下列哪些元素的化学性质最相似______(填序号).
(3)溴化氢的化学式为______. 天天健身1年前1
天天健身1年前1 -
 lyy319 共回答了24个问题
lyy319 共回答了24个问题 |采纳率83.3%(1)根据:原子核电荷数=核内质子数=核外电子数,则可求x=2+8+18+7=35;
(2)因为元素的化学性质由最外层电子数决定,具有相同最外层电子数的粒子,化学性质相似,故溴元素的化学性质与B的化学性质相似;
(3)由分析知溴元素的化合价为-1价,又知氢元素的化合价为+1价,则利用化合价数值交叉法书写化学式:
+1
H
−1
Br,则其化学式为HBr.
故答为:(1)35;
(2)B;
(3)HB1年前查看全部
- 溴化亚铁与氯气反应,溴元素有三分之一被氧化,写出化学方程式
溴化亚铁与氯气反应,溴元素有三分之一被氧化,写出化学方程式
已知2FeCL2+Cl2=2FeCl3,2KBr+Cl2=2KCl+Br2,Br2+2FeBr2=2FeBr3.
现将FeBr2溶液通入一定量的Cl2充分反应后,经测定溶液中的溴元素有三分之一被氧化,用一个化学方程式表示上述反应. bd95vv1年前2
bd95vv1年前2 -
 jiangyanzhaohuai 共回答了21个问题
jiangyanzhaohuai 共回答了21个问题 |采纳率85.7%18FeBr2+15Cl2=10FeCl3+6Br2+8FeBr3
显然,溶液中存在Br2,哪么溶液中就只有Fe3+,没有Fe2+,方程式就可以写出了.1年前查看全部
- (2003•盐城)溴元素有多种化合价.下列单质或化合物中,溴元素化合价最低的是( )
(2003•盐城)溴元素有多种化合价.下列单质或化合物中,溴元素化合价最低的是( )
A.KBrO3
B.MgBr2
C.Br2
D.HBrO4 carinayao1年前1
carinayao1年前1 -
 湖师941 共回答了19个问题
湖师941 共回答了19个问题 |采纳率94.7%解题思路:根据在化合物中正负化合价代数和为零计算出指定元素化合价和单质中元素的化合价为0,即可解答本题.A、KBrO3中溴元素的化合价为:(+1)+a+(-2)×3=0,则a=+5;
B、MgBr2中溴元素的化合价为:+2+2b=0,则 b=-1;
C、根据单质中元素的化合价为0;所以Br2中溴元素的化合价为0;
D、HBrO4中溴元素的化合价为::(+1)+d+(-2)×4=0,则d=+7;
通过比较B中溴元素的化合价最低,故选B.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生对单质中元素的化合价为0和元素化合价的计算方法的理解与掌握,并能灵活应用于解题的能力.1年前查看全部
- 我一个含有溴元素的化合物的高分辨质谱,现在出现两个同位素峰,我在写文章时,是两个同位素峰都写上,还是只写丰度最高的那个,
我一个含有溴元素的化合物的高分辨质谱,现在出现两个同位素峰,我在写文章时,是两个同位素峰都写上,还是只写丰度最高的那个,没经验请指教.我举个例子:HRMS (MALDI):m/z = 173.9977 [M+H]+,175.9938 [M+2+H]+,这样写,还是只写这个丰度相对高的HRMS (MALDI):m/z = 173.9977 [M+H]+,这个到底遵循什么原则.不要说得太简单,最好举个例子,有帮助一定给金币.
 tompai1年前1
tompai1年前1 -
 逆流fish 共回答了16个问题
逆流fish 共回答了16个问题 |采纳率81.3%前者比较严谨,最好注上Br79及Br81,至于格式,可参照投稿期刊给出的格式要求,若无要求则自己随意,只要表示清楚即可. 查看原帖>>
麻烦采纳,谢谢!1年前查看全部
- 为了鉴定溴乙烷中溴元素的存在,试分析下列各步实验,其中操作顺序合理的是( )
为了鉴定溴乙烷中溴元素的存在,试分析下列各步实验,其中操作顺序合理的是( )
①加入AgNO3溶液②加入NaOH溶液③加热 ④用HNO3酸化溶液⑤加入NaOH溶液醇溶液.
A. ①②③⑤
B. ②③④①
C. ④③⑤①
D. ④②⑤③ 莫非是1年前3
莫非是1年前3 -
 someone150 共回答了24个问题
someone150 共回答了24个问题 |采纳率91.7%解题思路:检验溴乙烷中溴元素使卤代烃中的卤素原子变为卤离子,溴乙烷可以在氢氧化钠水溶液中水解生成卤离子,也可以在氢氧化钠醇溶液中发生消去反应生成卤离子,最后加入硝酸酸化,加入硝酸银,观察是否有黄色沉淀生成,据此即可解答.为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,是因为溴乙烷中不含有溴离子;
检验溴乙烷中含有溴元素一定要将之转化为溴离子,可以采用卤代烃的水解方法或在氢氧化钠醇溶液中发生消去反应生成卤离子,即加入氢氧化钠选②,或加入NaOH溶液醇溶液选⑤,加热,发生水解反应生成NaBr选③,用HNO3酸化溶液至溶液呈酸性选④,最后加入硝酸银溶液,生成淡黄色沉淀,则证明含溴元素选①,
即操作顺序为②③④①或⑤③④①,
故选:B.点评:
本题考点: 常见离子的检验方法.
考点点评: 本题考查有机物的结构和性质,注意溴乙烷中不含溴离子,明确卤离子的转化是解答的关键,水解后加酸至酸性为解答的易错点,题目难度不大.1年前查看全部
- 向溴乙烷中滴加硝酸酸化过的Agno3,以检验其中的溴元素
 goldmoon281年前3
goldmoon281年前3 -
 飞影长海 共回答了18个问题
飞影长海 共回答了18个问题 |采纳率94.4%溴乙烷,有机物,非电解质,不能电离出Br-,加硝酸酸化过的AgNO3,不会有溴化银沉淀.
正确的检验方法:①加入氢氧化钠溶液 ②加热 ③加入稀硝酸至溶液呈酸性 ④加入硝酸银溶液
解释:
1.加NaOH后C2H5Br会水解生成Br-
C2H5Br+NaOH→C2H5OH+NaBr
2.由于此时溶液呈碱性,碱会与AgNO3中的Ag+生成沉淀,从而影响Br-的检验,所以在加入AgNO3前应当先加酸中和掉没反应完的碱1年前查看全部
- (2004•眉山一模)已知溴元素的符号为Br,溴原子结构示意图为,问:
(2004•眉山一模)已知溴元素的符号为Br,溴原子结构示意图为
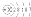 ,问:
,问:
(1)溴元素的化学性质与下列哪种元素的化学性质相似:______(填序号)
A.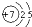 B.
B. C.
C. D.
D.
(2)溴化氢的化学式为______.
(3)溴化氢的水溶液是一种酸,该酸的名称是______. 润辰1年前1
润辰1年前1 -
 UPUU 共回答了23个问题
UPUU 共回答了23个问题 |采纳率82.6%解题思路:(1)决定元素化学性质的是最外层电子数,据此分析解答即可;
(2)根据化合价写出化学式;
(3)根据酸的命名方法进行命名.(1)由最外层电子数相等元素的化学性质相似可知,溴元素与B化学性质相似;
(2)H的化合价是+1价,Br的化合价是-1价,所以化学式是HBr;
(3)溴化氢的水溶液是一种酸,该酸是一种无氧酸,由无氧酸的命名方法可知,该酸的名称是氢溴酸.
故答为:(1)B;(2)HBr;(3)氢溴酸.点评:
本题考点: 原子结构示意图与离子结构示意图;核外电子在化学反应中的作用.
考点点评: 本题考查学生对原子结构示意图含义的理解与在解题中灵活与的能力.难度不大,属于基础知识的内容,应加强基础知识的学习.1年前查看全部
- 高二化学的几个问题1.设计实验证明碳酸酸性强于苯酚酸性.写出简要操作步骤有关化学方程式2.检验溴乙烷溴元素.写出简要操作
高二化学的几个问题
1.设计实验证明碳酸酸性强于苯酚酸性.写出简要操作步骤有关化学方程式
2.检验溴乙烷溴元素.写出简要操作步骤有关化学方程式
谢谢 守候TLP1年前4
守候TLP1年前4 -
 xswy211 共回答了17个问题
xswy211 共回答了17个问题 |采纳率94.1%第1题:向苯酚钠溶液中,通入二氧化碳,二氧化碳使得澄清溶液又变浑浊~这是因为易溶于水的苯酚钠在碳酸的作用下~重新又生成了苯酚.这说明了苯酚的酸性比碳酸弱~
C6H6ONa+CO2=C6H6OH+NaHCO3
第2题:取一只试管,滴入10~15滴溴乙烷,再加入1mL5%的NaOH溶液,充分震荡、静置,待液体分层后,用滴管小心吸取10滴上层水溶液,移入另一盛有10mL稀HNO3溶液的试管中,然后加入2滴到3滴AgNO3溶液,观察反应现象.可以看到,反应中有浅黄色沉淀生成,这种沉淀是AgBr.
C2H5Br+NaOH=C2H5OH+NaBr
NaBr+AgNO3=AgBr+NaNO3
有机反应用箭号~我这里没打出来~你改一下~1年前查看全部
- 工业上利用下列反应进行海水中溴元素的富集:Br2+SO2+2H2O=H2SO4+2HBr.在该反应中,作为氧化剂的物质是
工业上利用下列反应进行海水中溴元素的富集:Br2+SO2+2H2O=H2SO4+2HBr.在该反应中,作为氧化剂的物质是______(填化式),作为还原剂的物质是______(填化学式);若反应中生成了 0.1mol HBr,则转移的电子数为______个.
 KKYO40341年前1
KKYO40341年前1 -
 叶月流辉 共回答了20个问题
叶月流辉 共回答了20个问题 |采纳率95%解题思路:化合价降低元素所在的反应物是氧化剂,化合价升高元素所在的反应物是还原剂,根据化合价的升降来确定转移电子情况.在反应Br2+SO2+2H2O=H2SO4+2HBr中,化合价降低元素Br所在的反应物Br2 是氧化剂,化合价升高元素S所在的反应物 SO2 是还原剂,化合价升高值=化合价降低值=2,所以反应转移电子2mol,反应中生成了2mol HBr,则转移的电子为2mol,若反应中生成了0.1mol HBr,则转移的电子0.1mol,数目为:0.1mol×6.02×1023=6.02×1022,
故答案为:Br2;SO2;6.02×1022.点评:
本题考点: 氧化还原反应;氧化还原反应的电子转移数目计算.
考点点评: 本题考查学生氧化还原反应的基本知识,可以根据所学知识进行回答,难度不大.1年前查看全部
- 常温下溴元素的单质的状态
 郁闷的大尾巴狼1年前2
郁闷的大尾巴狼1年前2 -
 鼻窿 共回答了20个问题
鼻窿 共回答了20个问题 |采纳率95%溴元素符号 Br,原子序 35,是一种卤素.溴分子在标准温度和压力下是有挥发性的红棕色液体,活性介于氯与碘之间.纯溴也称溴素.溴蒸气具有腐蚀性,并且有毒.熔点:-7.2℃ 沸点:58.76℃ 因此常温下是液态的.1年前查看全部
- 地球上99%的溴元素存在于海洋中,资料显示海水中溴含量约为66mg•L-1.从海水中提取溴的工业流程如下:
地球上99%的溴元素存在于海洋中,资料显示海水中溴含量约为66mg•L-1.从海水中提取溴的工业流程如下:

(1)写出海水淡化的一种方法:______.
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是______.
(3)以上步骤I中已获得游离态的溴,步骤Ⅱ又将之转化成化合态的溴,其目的是______.
(4)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.写出溴与二氧化硫水溶液反应的化学方程式:______.
(5)实验室从溴水中分离溴还可以用萃取法,下列可以用作溴的萃取剂的是______.
a.乙酸b.四氯化碳c.裂化汽油d.苯
(6)假设提取过程中溴没有损失,计算1m3海水按上述流程进行实验时,步骤中Ⅱ约需消耗1mol•L-1 Na2CO3溶液______L. dirtylynn1年前1
dirtylynn1年前1 -
 等待中的欣桐 共回答了20个问题
等待中的欣桐 共回答了20个问题 |采纳率95%解题思路:流程分析可知海水通过一定方法淡化得到淡水和卤水,卤水加入氧化剂氧化溴离子为单质溴,通入热空气或水蒸气吹出Br2,利用的是溴单质的易挥发性,再利用酸溶液中溴酸根离子和溴离子发生氧化还原反应得到溴单质;
(1)依据海水得到淡水的方法分析回答;
(2)溴单质具有易挥发性;
(3)过程中得到溴单质,通过热空气吹出后用纯碱吸收得到溴酸根和溴离子,在酸溶液中重新得到溴单质;
(4)溴与二氧化硫水溶液反应生成硫酸和溴化氢;
(5)依据萃取的原则是萃取剂不溶于水,在水溶液中分层;6
(6)海水中溴含量约为66mg•L-1,1m3海水中含有溴离子1000L×66mg/L=66000mg=66g,结合反应过程中的化学方程式定量关系计算;(1)除去海水中的盐分以获得淡水的工艺过程叫海水淡化,亦称海水脱盐.海水淡化的方法,基本上分为两大类:从海水中取淡水,有蒸留法、反渗透法、水合物法、溶剂萃取法和冰冻法,除去海水中的盐分,有电渗拆法、离子交换法和压渗法;
故答案为:蒸馏方法或电渗析方法或离子交换法;
(2)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用到溴的性质是易挥发;
故答案为:挥发性;
(3)步骤I中溴单质的浓度低,若直接蒸馏,生产成本高;经步骤Ⅱ、Ⅲ,实际上是将溴水浓缩,使溴元素的富集;
故答案为:溴元素的富集;
(4)上述流程中吹出的溴蒸气,也可以用二氧化硫水溶液吸收,再用氯气氧化后蒸馏.溴与二氧化硫水溶液反应生成硫酸和溴化氢,反应的化学方程式为:
Br2+SO2+2H2O=2HBr+H2SO4;
故答案为:Br2+SO2+2H2O=2HBr+H2SO4;
(5)实验室从溴水中分离溴还可以用萃取法,下列不可用作溴的萃取剂的是和水溶液互溶的试剂;
a.乙酸乙溶于水,不能做萃取剂,故a错误;
b.四氯化碳不溶于水,可以萃取溴单质,故b正确;
c.酒精极易溶于水,不能分层,不能做萃取剂,故c错误;
d.苯是不溶于水比水轻的试剂,可以做萃取溴单质的萃取剂,故d正确;
故答案为:bd;
(6)海水中溴含量约为66mg•L-1,1m3海水中含有溴离子1000L×66mg/L=66000mg=66g,溴元素物质的量=[66g/80g/mol]=0.825mol,步骤Ⅱ反应为3Br2+3Na2CO3=5NaBr+NaBrO3+3CO2↑,
计算得到需要碳酸钠物质的量=0.825mol×[1/2]=0.4125mol,需消耗1mol•L-1 Na2CO3溶液体积0.4125L;
故答案为:0.4125L;点评:
本题考点: 海水资源及其综合利用;氯、溴、碘及其化合物的综合应用.
考点点评: 本题考查了海水资源的利用分析判断,主要是流程操作的理解应用,掌握基础是关键,题目难度中等.1年前查看全部
- 工业上利用下列反应进行海水中溴元素的富集:Br2+SO2+2H2O=H2SO4+2HBr.在该反应中,氧化剂是_____
工业上利用下列反应进行海水中溴元素的富集:Br2+SO2+2H2O=H2SO4+2HBr.在该反应中,氧化剂是______(填化学式);若反应中生成了 0.2mol HBr,则消耗SO2的体积(标准状况)是______.
 ilikedouzai1年前1
ilikedouzai1年前1 -
 孤单芭蕾922 共回答了19个问题
孤单芭蕾922 共回答了19个问题 |采纳率89.5%解题思路:Br2+SO2+2H2O=H2SO4+2HBr中,Br元素的化合价由0降低为-1价,S元素的化合价由+4升高为+6价,由反应可知,生成2molHBr消耗1molSO2,以此解答.Br2+SO2+2H2O=H2SO4+2HBr中,Br元素的化合价由0降低为-1价,S元素的化合价由+4升高为+6价,则氧化剂为Br2,
由反应可知,生成2molHBr消耗1molSO2,则生成了0.2mol HBr,则消耗SO2的体积为0.1mol×22.4L/mol=2.24L,
故答案为:Br2;2.24L.点评:
本题考点: 氧化还原反应;化学方程式的有关计算.
考点点评: 本题考查氧化还原反应,明确反应中元素的化合价变化是解答本题的关键,注重基础知识的考查,题目难度不大.1年前查看全部
- 烫发用的定型剂主要成分是溴酸钠(NaBrO3),对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为( )
烫发用的定型剂主要成分是溴酸钠(NaBrO3),对皮肤有刺激作用,使用不当会引起皮炎.溴酸钠中溴元素的化合价为( )
A.+1
B.+3
C.+4
D.+5 同甘共苦冰1年前1
同甘共苦冰1年前1 -
 ziainuk 共回答了17个问题
ziainuk 共回答了17个问题 |采纳率82.4%解题思路:根据在化合物中正负化合价代数和为零,结合溴酸钠(NaBrO3)的化学式进行解答本题.钠元素显+1价,氧元素显-2价,设溴元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5.
故选:D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- (2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
 (2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
(2006•雅安)已知溴元素的元素符号为Br,溴原子的结构示意图如图所示,问:
(1)x的值为3535.
(2)溴元素的化学性质与下列哪些元素的化学性质最相似BB(填序号).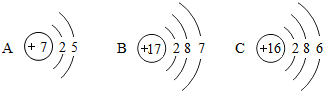
(3)溴化氢的化学式为HBrHBr. 海底好鱼1年前1
海底好鱼1年前1 -
 zgx65 共回答了21个问题
zgx65 共回答了21个问题 |采纳率90.5%解题思路:(1)已知溴原子的结构示意图;根据:原子核电荷数=核内质子数=核外电子数,则可求x的值;
(2)因为元素的化学性质由最外层电子数决定,所以具有相同最外层电子数的粒子,化学性质相似;
(3)已知溴元素的元素符号为Br,溴原子的结构示意图,可知它易得1个电子而带1个负电荷,其化合价为-1价,又知氢元素的化合价为+1价,则利用化合价数值交叉法书写化学式.(1)根据:原子核电荷数=核内质子数=核外电子数,则可求x=2+8+18+7=35;
(2)因为元素的化学性质由最外层电子数决定,具有相同最外层电子数的粒子,化学性质相似,故溴元素的化学性质与B的化学性质相似;
(3)由分析知溴元素的化合价为-1价,又知氢元素的化合价为+1价,则利用化合价数值交叉法书写化学式:
+1
H
−1
Br,则其化学式为HBr.
故答为:(1)35;
(2)B;
(3)HB点评:
本题考点: 原子结构示意图与离子结构示意图;核外电子在化学反应中的作用;化学式的书写及意义.
考点点评: 了解原子结构示意图与离子结构示意图的区别和联系;掌握核外电子在化学变化中的作用和得失电子的规律特点.1年前查看全部
- 溴元素与钠元素形成化合物的化学式是什么,高温灼烧该化合物时,火焰呈什么颜色?谢谢回答咯.
 我是来自南方的狼1年前1
我是来自南方的狼1年前1 -
 藤萝 共回答了16个问题
藤萝 共回答了16个问题 |采纳率87.5%Na B1年前查看全部
- (2008•龙岩)溴酸钾会导致人的中枢神经紊乱、诱发癌变,卫生部明令禁止向面粉中添加溴酸钾.溴酸钾(KBrO3)中溴元素
(2008•龙岩)溴酸钾会导致人的中枢神经紊乱、诱发癌变,卫生部明令禁止向面粉中添加溴酸钾.溴酸钾(KBrO3)中溴元素(Br)的化合价为( )
A.-l
B.+1
C.+3
D.+5 无沔小子1年前1
无沔小子1年前1 -
 敏儿83 共回答了23个问题
敏儿83 共回答了23个问题 |采纳率87%解题思路:根据在化合物中正负化合价代数和为零,结合溴酸钾(KBrO3)的化学式进行解答本题.钾元素显+1价,氧元素显-2价,设溴元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5价.
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- 利用NaOH溶液,AgNO3溶液即可确定有机物中含有溴元素为什么不对
 9ghga1年前2
9ghga1年前2 -
 时间上的尘埃 共回答了15个问题
时间上的尘埃 共回答了15个问题 |采纳率80%OH - + Ag+ =AgOH ↓
AgOH见光分解 成 Ag2O 和H2O,Ag2O是灰白色沉淀会干扰AgBr浅黄色沉淀,使得现象不明显了
1年前查看全部
- 在检验溴乙烷中的溴元素时,为什么要加稀硝酸酸化?
 cat叔叔1年前1
cat叔叔1年前1 -
 想飞ツ 共回答了16个问题
想飞ツ 共回答了16个问题 |采纳率100%稀硝酸酸化,是为了排除其他一些离子对本实验的干扰.如不进行酸化,比如.原溶液中有碳酸根离子,它与硝酸银反应,生成碳酸银沉淀,就破坏了实验的进程.
不是黑色沉淀,生成的AgBr是一种淡黄色沉淀.原理:溴乙烷水解.在酸性条件水解生成HBr.在碱性条件水解生成相应的RBr(R是一种金属元素,如K,Na),然后1年前查看全部
- 2-溴-1-丙醇能被氧化成醛吗?醛不是不能含溴元素吗?
 季风行千里1年前1
季风行千里1年前1 -
 nock123 共回答了13个问题
nock123 共回答了13个问题 |采纳率100%谁说醛不可以带溴元素的.可以被氧化的1年前查看全部
- 溴元素元素最高化合价和最低化合价是多少
 bornformovie71年前2
bornformovie71年前2 -
 陌生的发呆 共回答了19个问题
陌生的发呆 共回答了19个问题 |采纳率100%和氯一样 最低-1最高+7 绝对值相加是81年前查看全部
- NaBrO3中的溴元素的化合价是多少?为什么?
 jimmy3651年前1
jimmy3651年前1 -
 0风中有你0 共回答了19个问题
0风中有你0 共回答了19个问题 |采纳率84.2%溴酸钠化学式为NaBrO3,其中Na化合价为+1价,O的化合价为-2价,根据化合价总数为零,设Br的化合价为x,则+1+x-2*3=0,所以x=+51年前查看全部
- 验证溴乙烷中的溴元素为什么要硝酸硝化?
 blue91141年前2
blue91141年前2 -
 liuke7364 共回答了20个问题
liuke7364 共回答了20个问题 |采纳率85%因为在之前的实验中NaOH是过量的,如果之间加入硝酸银,生成的是氢氧化银沉淀,氢氧化银沉淀光解成氧化银黑色沉淀,无法检验溴离子1年前查看全部
- 反应物中,溴元素既未被还原也没被氧化的化学方程式
 大山cs1年前3
大山cs1年前3 -
 shaoyand 共回答了24个问题
shaoyand 共回答了24个问题 |采纳率95.8%所有溴元素化合价未发生变化的反应.
例:NaBr+AgNO3=NaNO3+AgBr↓1年前查看全部
- 海洋中溴元素多还是氯元素多?应该是氯元素多吧,但为什么海洋元素是溴元素呢?
 诗嘉1年前3
诗嘉1年前3 -
 ynzhangdeshu 共回答了18个问题
ynzhangdeshu 共回答了18个问题 |采纳率83.3%氯元素多很多的,溴元素也是以化合物形式与氯化物之类的混合在一起,但是含量就少很多1年前查看全部
- 反应物中,溴元素既未被氧化,又未被还原的方程式
 lajiaotian1年前3
lajiaotian1年前3 -
 pchuan 共回答了20个问题
pchuan 共回答了20个问题 |采纳率90%溴加水:Br2+H2O=HBr+HBrO1年前查看全部
- 检验溴乙烷中的溴元素为什么要用硝酸酸化
 赵执1年前1
赵执1年前1 -
 hszj2bzjw 共回答了20个问题
hszj2bzjw 共回答了20个问题 |采纳率95%Ag+离子需要在酸性条件下才不会生成沉淀,而用硫酸或盐酸酸化会生成微溶物或难溶物,影响观察1年前查看全部
- 【溴酸钠中溴元素的化合价为____】答案怎么书写?
【溴酸钠中溴元素的化合价为____】答案怎么书写?
我知道是+5价,
那么应该在___中填写 "+5"还是"+5价"
我纠结很久了,大家帮个忙> lihaiboily1年前1
lihaiboily1年前1 -
 温柔与怜悯 共回答了12个问题
温柔与怜悯 共回答了12个问题 |采纳率91.7%+5价1年前查看全部
- 关于溴的化学知识(1)溴单质,溴水的颜色(2)溴元素的还原性和氧化性的排列顺序(3)与溴相关的化学反应
关于溴的化学知识(1)溴单质,溴水的颜色(2)溴元素的还原性和氧化性的排列顺序(3)与溴相关的化学反应
请各位的语言简洁明了…… 8f8a1年前1
8f8a1年前1 -
 xingpo 共回答了25个问题
xingpo 共回答了25个问题 |采纳率92%还是我来吧
Br 第七主族元素,棕红色液体,水溶液为橙黄色,CCl4溶液为橙红色.有毒,易挥发.
还原性S I2 Br2 Cl2 O2 F2 由强到弱
氧化性F O Cl Br I S(-2离子) 由强到弱..除S均为-1离子
1.与金属化合 Br2+Mg=MgBr2
2.与非金属化合 H2+Br2=2HBr 充分加热
3.与碱.生成次溴酸根,溴酸根和水...不想打了,书上有Cl2的
4与H2O Br2+H2O=HBr+HBrO
5卤素 或拟卤素的置换 Br2+2KI=I2+2KBr Cl2+2KBr=Br2+2KCl
我不知道你需要到哪种程度的..不会的再问我吧1年前查看全部
- 溴化钾和溴酸钾在酸性溶液中发生归中反应,溴元素全部变为溴单质的反应方程式是什么?
 zzfrent1年前2
zzfrent1年前2 -
 a310054903 共回答了22个问题
a310054903 共回答了22个问题 |采纳率90.9%5KBr+KBrO3+3H2SO4===3Br2+3H2O+3K2SO41年前查看全部
- 为什么向溴乙烷中滴加Agno3,以检验其中的溴元素
为什么向溴乙烷中滴加Agno3,以检验其中的溴元素
Agno3的作用是什么? zhongyue1年前2
zhongyue1年前2 -
 lrrloveyb 共回答了16个问题
lrrloveyb 共回答了16个问题 |采纳率81.3%AgBr为浅黄色沉淀,容易区分检验.
注意:AgBr 浅黄色沉淀 ,AgI 黄色沉淀1年前查看全部
- (2008•广东)食品添加剂溴酸钾(KBrO3)会致癌,已被禁用,其中溴元素(Br)的化合价为( )
(2008•广东)食品添加剂溴酸钾(KBrO3)会致癌,已被禁用,其中溴元素(Br)的化合价为( )
A.+1
B.+3
C.+5
D.无法确定 清风中的翠竹1年前1
清风中的翠竹1年前1 -
 心如潮 共回答了19个问题
心如潮 共回答了19个问题 |采纳率78.9%解题思路:根据在化合物中正负化合价代数和为零进行解答本题.根据在化合物中正负化合价代数和为零,可得溴酸钾(KBrO3)中溴元素的化合价为:
(+1)+x+(-2)×3=0,
则x=+5;
故选C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的能力.1年前查看全部
- 工业上利用下列反应进行海水中溴元素的富集:Br 2 +SO 2 +2H 2 O=H 2 SO 4 +2HBr.在该反应中
工业上利用下列反应进行海水中溴元素的富集:Br 2 +SO 2 +2H 2 O=H 2 SO 4 +2HBr.在该反应中,作为氧化剂的物质是______(填化式),作为还原剂的物质是______(填化学式);若反应中生成了 0.1mol HBr,则转移的电子数为______个.  anys1661年前1
anys1661年前1 -
 热-HOT 共回答了10个问题
热-HOT 共回答了10个问题 |采纳率90%在反应Br 2 +SO 2 +2H 2 O=H 2 SO 4 +2HBr中,化合价降低元素Br所在的反应物Br 2 是氧化剂,化合价升高元素S所在的反应物 SO 2 是还原剂,化合价升高值=化合价降低值=2,所以反应转移电子2mol,反应中生成了2mol HBr,则转移的电子为2mol,若反应中生成了0.1mol HBr,则转移的电子0.1mol,数目为:0.1mol×6.02×10 23 =6.02×10 22 ,
故答案为:Br 2 ;SO 2 ;6.02×10 22 .1年前查看全部
大家在问
- 1高二(1)班有学生48人,现用系统抽样的方法,抽取一个容量为4的样本,已知学号分别为8,32,44的同学都在样本中,那么
- 2我敬佩的人 作文
- 3(2007•江阴市)计算下面各题,能简算的要简算.
- 4从甲堆煤中取出8分之1给乙堆,这时两堆煤重量就相等了.原来乙堆煤的重量是甲堆煤
- 5找字加一笔或减一笔变成什么字?
- 6“他希望不会有什么坏事发生在他丈夫身上”用英语怎么说 填空
- 7(2009•广东)有关人体内环境稳态的叙述,错误的是( )
- 8竖直平面内的圆周运动物体从低端出发,要超过四分之一圆周,物体末速度要不为0,为什么为什么四分之一圆周以下的末速度就可以为
- 9有相同渐近线的双曲线方程x^2/a^2-y^2/b^2=λ(λ≠0)
- 10英语翻译用英语怎么翻译这句话 “再见等于再也不见”
- 11已知2014年的5月1日是星期四,那么6月1日是星期几?怎么算
- 129×0.45+0.29×4.2+0.029×13怎么样笛简便运算
- 13用洛必达法则求解
- 14读了《郑人买覆》一文,你明白了什么道理?
- 15叛逆的鲁鲁修R2最后C.C说的话是什么意思
