用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。
 爱做一半儿挺郁闷2022-10-04 11:39:541条回答
爱做一半儿挺郁闷2022-10-04 11:39:541条回答| 用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来。 (1)由上述实验现象可得出两条有关过氧化钠跟水反应的结论是: 第一:_____________________;第二:____________________。 (2)某研究性学习小组拟用如下图所示的装置进行实验,以验证上述结论。 |
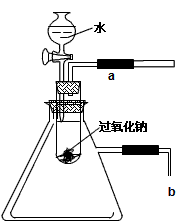 |
| 用以验证第一条结论的实验操作是_________________现象是__________________。为了验证第二条结论,将管口b浸入水中,可观察到的现象为______________________。 |

已提交,审核后显示!提交回复
共1条回复
 dengbo1234 共回答了20个问题
dengbo1234 共回答了20个问题 |采纳率100%- (1)第一:有O 2 放出;第二:有热量放出
(2)将带火星的木条放在导管a处;带火星的木条复燃;有气泡冒出 - 1年前
相关推荐
- 在线求指导:用脱脂棉包住约0.2 g
在线求指导:用脱脂棉包住约0.2 g
用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来. 
(1)由实验现象所得出的有关Na 2 O 2 和H 2 O反应的结论是:a.有氧气生成;b.________.
(2)写出Na 2 O 2 和H 2 O反应的化学方程式并标明电子转移数目:_____________________.
(3)某学校研究性学习小组拟用上图所示装置进行实验,以证明上述结论.
①用以验证结论a的实验操作方法及现象是________________________.
②用以验证结论b的实验操作方法及现象是________________________.
(4)该研究性学习小组的同学认为Na 2 O 2 和H 2 O反应可生成H 2 O 2 ,请你设计一个简单的实验以证明Na 2 O 2 和足量的H 2 O充分反应后的溶液中有H 2 O 2 存在.(只要求列出实验所用的试剂及观察到的现象)
试剂:______________________________. 现象:______________________________.
 rr水瓶人1年前1
rr水瓶人1年前1 -
 snggsara 共回答了16个问题
snggsara 共回答了16个问题 |采纳率87.5%1年前查看全部
- 下列物质的主要成分在氧气中充分燃烧,只生成二氧化碳和水 脱脂棉植物油为什么可以?毛发甘氨酸却不 如何判
 kawai_19811年前1
kawai_19811年前1 -
 wl2868980 共回答了14个问题
wl2868980 共回答了14个问题 |采纳率100%脱脂棉植物油含碳氢氧燃烧生成二氧化碳和水
毛发甘氨酸含氮碳氢氧燃烧生成二氧化碳、二氧化氮和水1年前查看全部
- 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
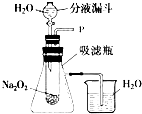 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
【设计装置】如图所示
【实验探究】实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:______
为了证实小军的看法,请你设计一个证明Na2CO3不存在的实验.
(2)小军取反应后所得的溶液于试管中,滴人无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈______性.实验步骤 预期实验现象 用试管取少量的反应后溶液,______
______
______
【表达】由实验探究的结果,写出过氧化钠和水反应的化学方程式______. wwsam2211年前1
wwsam2211年前1 -
 byg3331693 共回答了17个问题
byg3331693 共回答了17个问题 |采纳率88.2%解题思路:由题目的信息可知:打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气,因为氧气具有助燃性;实验中,还观察到伸入烧杯中的导管口有气泡冒出,是因为过氧化钠与水反应放出热量,锥形瓶内气体体积膨胀,因此观察到伸入烧杯中的导管口有气泡冒出;小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:过氧化钠、水中,都没有碳元素,因此根据质量守恒定律,不可能是碳酸钠;设计一个证明Na2CO3不存在的实验:用试管取少量的反应后溶液,然后向试管中滴加过量的稀盐酸,没有气泡冒出,说明碳酸钠不存在;小军取反应后所得的溶液于试管中,滴人无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈碱性,因为酚酞遇到碱性溶液变红色;根据质量守恒定律,过氧化钠和水反应生成氢氧化钠和氧气,配平即可.实验一:(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气,因为氧气具有助燃性;故答案为:氧气;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,是因为过氧化钠与水反应放出热量,锥形瓶内气体体积膨胀,因此观察到伸入烧杯中的导管口有气泡冒出;故答案为:过氧化钠与水反应放出热量,锥形瓶内气体体积膨胀,因此观察到伸入烧杯中的导管口有气泡冒出;
实验一:(1)小张猜想另一种物质是Na2CO3,小军认为不可能;小军的依据是:过氧化钠、水中,都没有碳元素,因此根据质量守恒定律,不可能是碳酸钠;设计一个证明Na2CO3不存在的实验:用试管取少量的反应后溶液,然后向试管中滴加过量的稀盐酸,没有气泡冒出,说明碳酸钠不存在;故答案为:过氧化钠、水中,都没有碳元素,因此根据质量守恒定律,不可能是碳酸钠;实验步骤:然后向试管中滴加过量的稀盐酸,观察现象;没有气泡冒出;
(2);小军取反应后所得的溶液于试管中,滴人无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈碱性,因为酚酞遇到碱性溶液变红色;故答案为:碱;
【表达】根据质量守恒定律,过氧化钠和水反应生成氢氧化钠和氧气,配平即可,故答案为:2Na2O2+2H2O=4NaOH+O2↑;点评:
本题考点: 实验探究物质的性质或变化规律;氧气的检验和验满;盐的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.1年前查看全部
- 请问叶绿素提取实验中过滤在漏斗底部加入脱脂棉的作用是什么?
 mayyy1年前1
mayyy1年前1 -
 yanbo0201 共回答了27个问题
yanbo0201 共回答了27个问题 |采纳率100%过滤碳酸钙和二氧化硅1年前查看全部
- 脱脂棉和非脱脂棉,做纤维素实验用哪一种?
脱脂棉和非脱脂棉,做纤维素实验用哪一种?
实验中棉纤维 与脱脂纤维 是同一种物质吗?我做纤维素负载基团的实验要用哪一种呢? 蓝海蜇1年前3
蓝海蜇1年前3 -
 隐鹰 共回答了19个问题
隐鹰 共回答了19个问题 |采纳率94.7%棉纤维的主要成份是纤维素,纤维素是天然高分子化合物,纤维素的化学结构式由α葡萄糖为基本结构单元重复构成,其元素组成为碳44.44%、氢6.17%、氧49.39%.棉纤维的聚合度在6000~11000间.此外,棉纤维还附有5%左右的其他物质,称为伴生物,伴生物对纺纱工艺与漂练、印染加工均有影响.棉纤维的表面含有脂蜡质,俗称棉蜡,棉蜡对棉纤维具有保护作用,是棉纤维具有良好纺纱性能的原因之一,但在高温时,棉蜡容易熔融.
由于棉纤维的主要组成物质是纤维素,所以它较耐碱而不耐酸.烧碱可使棉纤维剧烈膨化,直径变大,长度缩短,以致引起棉制品的强烈收缩.此时,若施加张力,限制其收缩,棉制品表面会变得平整光亮且大大改善染色性能,此加工称为丝光;若不加张力任其收缩,称为碱缩.针织物经碱缩后会变得紧密而富有弹性,而且保形性好.酸能使棉纤维强度变差,尤其是强酸浓酸应忌用,它可溶于70%以上浓硫酸中,浓盐酸、浓硝酸对其强度也有严重影响.
脱脂棉是指经化学处理去掉脂肪的棉花,比普通棉花容易吸收液体,是卫生用品,也用来制造硝酸纤维.又称药棉.由原棉经除去夹杂物,脱脂、漂白、洗涤、干燥、整理加工制成.脱脂棉应无臭、无味、无色斑,具有很好的吸水性,纤维柔软细长,洁白富有弹性,易于分层,没有酸、碱等有害杂质,质量应符合卫生部制定的技术标准.脱脂棉是棉花经工艺脱脂而成,因表层不含有脂肪,有很好的亲水性,浸泡于75%酒精可作消毒棉球.
综上所述,做纤维素负载基团的实验要用脱脂棉.1年前查看全部
- 在中秋联欢晚会上,某同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很
 在中秋联欢晚会上,某同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行了实验与探究.
在中秋联欢晚会上,某同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行了实验与探究.
【提出问题】过氧化钙与水反应生成了什么物质?为什么滴水后的脱脂棉会燃烧?
【猜想】①可能有种气体和另一种物质生成;②反应过程中可能有能量变化.
【设计实验】如图所示
【实验探究】
【实验一】探究反应后生成什么气体?
(1)打开上图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
【实验二】小明等同学取出反应后试管中的部分澄清液体,用喝饮料用的吸管向该液体中缓缓吹气,观察到澄清液体变白色浑浊,据此你认为该澄清液体可能是______. yaodi10261年前1
yaodi10261年前1 -
 U版西厢记 共回答了17个问题
U版西厢记 共回答了17个问题 |采纳率88.2%解题思路:【实验一】(1)检验氧气要使用带火星的木条;(2)反应放出热量,会导致吸滤瓶内压强增大,烧杯中的水会产生气泡;【实验二】根据“包有过氧化钙(CaO2)粉末的脱脂棉上滴水”,根据质量守恒定律,推测该澄清液体可能组成.在探究实验时,步骤为:提出问题,猜想,设计实验,实验探究,交流.
【实验一】(1)能产生使带火星的木条复燃的气体,说明该气体为氧气;
(2)在此反应中,一定有热量放出,放出的热量使锥形瓶内的压强变大,从而在导管口处有气泡冒出;
【实验二】小明等同学取出反应后试管中的部分澄清液体,用喝饮料用的吸管向该液体中缓缓吹气,观察到澄清液体变白色浑浊,在根据“包有过氧化钙(CaO2)粉末的脱脂棉上滴水”和质量守恒定律得元素守恒,推测该澄清液体可能是澄清石灰水.
故答案为:
【实验一】(1)氧气;
(2)反应放出热量,使瓶中气体体积变大,压强变大;
【实验二】澄清石灰水.点评:
本题考点: 实验探究物质的性质或变化规律;氧气的检验和验满;物质发生化学变化时的能量变化.
考点点评: 在解此类题时,首先分析题中考查的问题,然后根据已有知识,在情景相似的情况下,进行知识地大胆迁移,是解决新问题的一种重要方法,推测相关生成物质的化学式时,要根据质量守恒定律进行判断分析.1年前查看全部
- 包有过氧化钠粉末的脱脂棉上滴水,为什么?脱脂棉燃烧
 koichidomoto1年前2
koichidomoto1年前2 -
 舡鱼 共回答了29个问题
舡鱼 共回答了29个问题 |采纳率93.1%过氧化钠和水反应放出氧气使脱脂棉氧化燃烧1年前查看全部
- 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
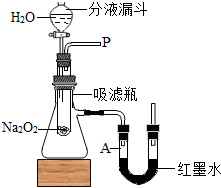 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行探究.
[提出问题]:过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]:①可能有一种气体和另一种物质生成;
②反应过程中可能有能量变化.
[设计装置]:如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)小利猜想生成的气体可能是氢气,也可能是氧气.小利猜想的依据是
______.
(2)小宁打开装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(3)实验过程中,还观察到U型管A端红墨水液面下降,说明本反应是放热反应.
资料:氢氧化钠与稀盐酸有反应但无明显现象,碳酸钠与稀盐酸反应有气体生成.
实验二:继续探究反应后生成的另一种是什么?
(1)小明认为反应生成了碳酸钠,小军认为不可能,应生成氢氧化钠,你认为这两位同学,谁的猜想是正确的______.
(2)为了验证上述同学的想法是否正确,可以取出少量样品于试管中,然后加入______根据是否有______生成来判断.
(3)根据以上实验结论,写出过氧化钠和水反应的化学方程式:______. killmyth1年前1
killmyth1年前1 -
 rockyrap 共回答了16个问题
rockyrap 共回答了16个问题 |采纳率100%解题思路:实验一:(1)小利猜想生成的气体可能是氢气,也可能是氧气.小利猜想的依据是质量守恒定律;
(2)根据氧气有助燃性进行分析;
实验二:(1)根据质量守恒定律的微观解释进行分析;
(2)根据“资料:氢氧化钠与稀盐酸有反应但无明显现象,碳酸钠与稀盐酸反应有气体生成”进行分析;
(3)根据以上实验结论,写出过氧化钠和水反应的化学方程式:根据题中的叙述找出反应物、生成物书写化学方程式.实验一:
(1)小利猜想生成的气体可能是氢气,也可能是氧气.小利猜想的依据是质量守恒定律或元素守恒;
(2)用带火星的木条靠近P处,木条复燃,说明该气体具有助燃性,故知为氧气;
实验二:
(1)在化学反应前后,元素的种类不变,反应物中没有碳元素,生成物中也不会有碳元素;
(2)为了验证上述同学的想法是否正确,可以取出少量样品于试管中,然后加入稀盐酸根据是否有气体生成来判断;
(3)根据以上实验结论,写出过氧化钠和水反应的化学方程式,故为:2Na2O2+2H2O=4NaOH+O2↑.
故答为:实验一、(1)质量守恒定律或元素守恒(2)氧气
实验二、(1)小军(2)稀盐酸气体生成(3)2Na2O2+2H2O=4NaOH+O2↑点评:
本题考点: 实验探究物质的组成成分以及含量;证明碳酸盐;氧气的检验和验满;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 在解此类题时,首先分析题中考查的问题,然后结合题中所给的知识和学过的知识进行分析解答.1年前查看全部
- 用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。
用脱脂棉包住约0.2 g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来。

(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一,有氧气生成;第二,____________。过氧化钠跟水反应的化学方程式是________________________,其中还原剂是________________________。
(2)某研究性学习小组拟用右图装置进行实验,以证明上述结论。
用以验证第一条结论的实验方法是:______________________________。
用以验证第二条结论的实验方法及现象是:_______________________________________。
(3)实验(2)中往试管内加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液变红;振荡后,红色褪去。为探究此现象,该小组同学查阅有关资料得知:Na 2 O 2 与H 2 O反应可生成H 2 O 2 ,H 2 O 2 具有强氧化性和漂白性。请设计一个简单的实验,证明Na 2 O 2 和足量H 2 O充分反应后的溶液中有H 2 O 2 存在。现有Na 2 S溶液、KI溶液、红色布条等,请从中选择试剂,加以验证(只要求列出实验所用的试剂及观察到的现象)。
试剂:______________________________________________________________。
现象:______________________________________________________________。 tangongyong1年前1
tangongyong1年前1 -
 程心1 共回答了22个问题
程心1 共回答了22个问题 |采纳率95.5%(1)是放热反应 2Na 2 O 2 +2H 2 O====4NaOH+O 2 ↑ Na 2 O 2
(2)将带火星的木条靠近导管口p处,木条复燃 将导管q浸入水中,反应过程中导管口有气泡冒出
(3)硫化钠溶液 溶液变浑浊(或者:红色布条 布条褪色)
(1)物质燃烧有两个条件,一是温度达到着火点,二是有氧气等助燃物质存在。由此进行分析可得出:该反应是放热反应。反应的化学方程式为2Na 2 O 2 +2H 2 O====4NaOH+O 2 ↑,其中Na 2 O 2 是还原剂。
(2)该小题实质上是考查氧气的检验、气密性检查等化学实验基本操作方法的运用。将带火星的木条靠进导管口p处,木条复燃。将导管q浸入水中,反应过程中导管口有气泡冒出。
(3)这是在限定范围内考查学生实验探究能力。可以有多组答案,如:硫化钠溶液,溶液变浑浊;红色布条,布条褪色。要注意的是,在氢氧化钠存在条件下检验过氧化氢,最好不要选用硫酸亚铁、碘化钾等作为试剂。1年前查看全部
- 右图所示为一个u型玻璃装置,右侧上部密封左侧上端插有一个植物枝条并用脱脂棉封口
右图所示为一个u型玻璃装置,右侧上部密封左侧上端插有一个植物枝条并用脱脂棉封口
将此装置放在较强的阳光下.1】一段时间后,右侧管中的液面高度将会 ,原因是 .2】水是通过植物枝条中的 向上运输 ufnet1年前1
ufnet1年前1 -
 yangchen549 共回答了24个问题
yangchen549 共回答了24个问题 |采纳率91.7%然后捏?1年前查看全部
- 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有______.
(2)Na 2 O 2 跟水反应的化学方程式为______.此反应中氧化剂是______.
(3)某研究性学习小组拟用右图所示装置(气密性良好)进行实验,以证明上述实验结论.验证第①条结论的实验操作及现象是:向试管中滴入水,______.
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为______.
 chens_dx1年前1
chens_dx1年前1 -
 deli1976 共回答了15个问题
deli1976 共回答了15个问题 |采纳率93.3%(1)根据反应现象可知,该反应为放热反应,放出的热量时脱脂棉燃烧,反应生成的氧气时燃烧更剧烈,故答案为:放出大量的热;(2)过氧化钠与水反应的化学方程式为:2Na 2 O 2 +2H 2 O═4NaOH+O 2 ↑,过氧化钠...1年前查看全部
- (2008•枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观
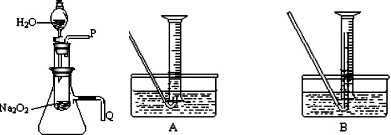 (2008•枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008•枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一:有氧气生成;第二:______.Na2O2跟水反应的化学方程式是______.
(2)某研究性学习小组拟用右图所示装置(气密性良好)
进行实验,以证明上述结论.
用以验证第一条结论的实验操作是:______;
用以验证第二条结论的实验方法是:______.
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该小组同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性.请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:______;现象:______.
(4)该小组同学提出用定量的方法探究Na2O2跟水反应后的溶液中否含有H2O2,其实验方法为:称取2.6g Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论.
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)______(填序号),理由是______.
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为______(选填“100mL”“200mL”“500mL”或“1000mL”). 白矾1年前1
白矾1年前1 -
 giyman 共回答了16个问题
giyman 共回答了16个问题 |采纳率100%解题思路:(1)脱脂棉燃烧除了有氧气外,必须要达到其燃点,据此可判断该反应是放热反应;
(2)该小题实质上是考查氧气的检验、气密性检查等化学实验基本操作方法的运用,将带火星的木条靠进导管口p处,木条复燃,将导管q浸入水中,反应过程中导管口有气泡冒出;
(3)H2O2在MnO2催化条件下会生成氧气;
(4)测量气体体积时,为防止倒吸应将导管尽量插入量筒底部,使用的量筒应是生成氧气的最大值.(1)脱脂棉燃烧除了有氧气外,必须要达到其燃点,则该反应为放热反应,反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:该反应是放热反应; 2Na2O2+2H2O=4NaOH+O2↑;
(2)检验是否有氧气生成,可根据氧气能使带火星的木条复燃进行检验,具体做法是打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成;该反应为放热反应,容器温度升高,容器内气体会膨胀,因此,将导管q浸入水中,反应过程中导管口有气泡冒出;
故答案为:打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O2生成;将导管Q浸入水中,反应过程中导管口有气泡冒出;
(3)H2O2在MnO2催化条件下会生成氧气,加入催化剂,过氧化氢分解生成氧气,溶液中有气泡产生,且能使带火星的木条复燃,证明有氧气生成,故答案为:MnO2; 气泡迅速产生,能使带火星的木条复燃;
(4)①测量气体体积时,为防止倒吸应将导管尽量插入量筒底部,所以应用B装置,
故答案为:B;防止气体冷却时发生倒吸现象;
②n(Na2O2)=[2.6g/78g/mol]=[1/30]mol,
2Na2O2+2H2O=4NaOH+O2↑
2mol 22.4L
[1/30]mol V(O2)
V(O2)=
1
30mol×22.4L
2mol=0.373L=373mL,
所以应用500mL的量筒,
故答案为:500mL.点评:
本题考点: 碱金属及其化合物的性质实验;钠的重要化合物.
考点点评: 本题重视从高中化学课本实验中选取命题素材,重视在课本实验的基础上考查探究能力是化学学科最有吸引力的话题之一.实验题,倾向于考查化学实验基本操作,倾向于把一些课本小实验重组成一个微型的研究课题,所以要提高解答化学实验题的得分率必须从课本中的基本实验入手.1年前查看全部
- 将滴有酚酞事业的滤纸放在试管中,试管口在塞上一团脱脂棉
将滴有酚酞事业的滤纸放在试管中,试管口在塞上一团脱脂棉
1,试管的作用是?
2,做试验时,滤纸没变色而脱脂棉变红.导致错误的操作可能是? 贝雅特丝1年前1
贝雅特丝1年前1 -
 歪歪老夫子 共回答了19个问题
歪歪老夫子 共回答了19个问题 |采纳率89.5%试管是为了避免氨气扩散,错误操作可能是酚酞溶液滴在了脱脂棉上(也只能是这样了)1年前查看全部
- 元旦联欢会上,化学老师给同学们表演了一个“水能生火”的魔术(如图1),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉
元旦联欢会上,化学老师给同学们表演了一个“水能生火”的魔术(如图1),他将包有过氧化钠(Na2O2)粉末的脱脂棉放在石棉网上,向棉花上滴了几滴水,棉花立刻燃烧了起来.同学们产生了浓厚的兴趣,为什么脱脂棉会燃烧起来呢?

提出猜想:
a)小新认为过氧化钠(Na2O2)与水反应生成了可以支持燃烧的物质.
b)小海又根据燃烧的条件,对小新的猜想进行了补充______.
实验与分析:同学们设计了如图2的实验装置.
(1)打开分液漏斗的活塞,控制水滴加的速度,看到试管中有气泡产生,将带火星的木条靠近P出口,看到木条复燃,你推测此气体可能是______.
(2)实验中还观察到,烧杯中的导气管口有气泡冒出,产生这一现象的原因是______.
(3)完成了以上实验,同学们又展开了进一步的研究,继续探究反应后生成的另一种物质是什么?小新猜想另一种物质是Na2CO3,小海认为不可能,小海的依据是______.
老师介绍:
a)过氧化钠和水发生反应生成氧气和氢氧化钠.
b)过氧化钠不仅可以和水发生反应,也可以和二氧化碳反应生成氧气,因而,经常被用于潜水艇和防毒面具中提供氧气.
补充实验:
确定了以上性质,小海同学又设计了一个实验(如图3)将一团包有过氧化钠的粉末的棉花塞到漏斗的管中,漏斗下方点燃一支短蜡烛 (蜡烛火焰与棉花不接触),棉花会燃烧起来吗?简要说明理由______.
反思:结合上述实验事实,同学们对于运输过氧化钠固体提出了安全建议:______.(至少填写一条) huazesu1年前1
huazesu1年前1 -
 丰雪花心 共回答了14个问题
丰雪花心 共回答了14个问题 |采纳率92.9%解题思路:提出猜想:根据燃烧的条件:可燃物、达到物质的着火点、与氧气接触分析解答;
实验与(1)根据氧气有助燃性进行分析;
(2)根据导管口冒出气体的原因进行分析;
(3)根据质量守恒定律,反应前后元素的种类不变进行分析;
补充实验:根据燃烧的条件及发生的化学反应分析解答;
反思:根据实验所得过氧化钠固体的性质分析解答.提出猜想:根据物质燃烧的条件:脱脂棉是可燃物,小新认为过氧化钠(Na2O2)与水反应生成了可以支持燃烧的物质,棉花要燃烧还需达到其着火点,据此分析;
实验与分析:
(1)用带火星的木条靠近P处,木条复燃,说明该气体具有助燃性,是氧气;
(2)导管口冒出气泡,可能生成了气体,也可能气体的温度升高,通过分析没有生成气体,只能是锥形瓶中的气体温度升高,故可知过氧化钠和水反应是放热反应;
(3)在化学反应前后,元素的种类不变,反应物中没有碳元素,生成物中也不会有碳元素,所以不可能生成碳酸钠;
补充实验:蜡烛燃烧生成水和二氧化碳,二氧化碳和水都可以和过氧化钠反应生成氧气,且放热可以使棉花的温度达到着火点,所以棉花能燃烧;
反思:通过上述实验分析可知:过氧化钠固体可以与水、二氧化碳发生反应,所以在运输时一定要隔绝空气、水;
故答案为:
提出猜想:此反应还会放热;
(1)氧气;
(2)过氧化钠与水反应放热使锥形瓶内压强增大;
(3)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3;
【补充实验】能燃烧,因为蜡烛燃烧生成水和二氧化碳,二氧化碳和水都可以和过氧化钠反应生成氧气,且放热可以使棉花的温度达到着火点,即可燃烧;
【反思】隔绝空气(隔绝水、防潮、密封保存…合理即可).点评:
本题考点: 燃烧的条件与灭火原理探究.
考点点评: 本题考查了学生对燃烧条件的掌握,通过解答能很好的考查出学生分析信息、应用知识解决实际问题的能力.1年前查看全部
- 过氧化钠与水反应用脱脂棉包住过氧化钠粉末,往脱脂棉上滴水,脱脂棉剧烈燃烧起来.问:以上得出关于Na2O2和H2O的反应结
过氧化钠与水反应
用脱脂棉包住过氧化钠粉末,往脱脂棉上滴水,脱脂棉剧烈燃烧起来.
问:
以上得出关于Na2O2和H2O的反应结论是:
a:
b:
如何验证以上两个结论
a:
b: leeyueh811年前1
leeyueh811年前1 -
 宗山小子 共回答了17个问题
宗山小子 共回答了17个问题 |采纳率82.4%a.反应放热;用温度计测量温度变化
b.反应有氧气生成;用带火星的木条靠近收集的气体,木条复燃1年前查看全部
- (2013•赤壁市模拟)化学老师在课堂上做了一个小魔术:水能生火.只见老师向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水
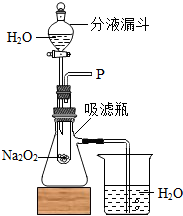 (2013•赤壁市模拟)化学老师在课堂上做了一个小魔术:水能生火.只见老师向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
(2013•赤壁市模拟)化学老师在课堂上做了一个小魔术:水能生火.只见老师向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
【设置装置】如图所示
【实验探究】实验一:探究反应生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,缓慢滴加足量的水,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:______.为了证实自己的看法,小军设计一个简单实验:向反应产物中滴加足量稀硫酸,______,则证明该物质不是碳酸盐.
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈______性.
【表达】由实验探究的结果,写出过氧化钠和水反应的化学方程式______. sgdx9301年前1
sgdx9301年前1 -
 我会等待 共回答了23个问题
我会等待 共回答了23个问题 |采纳率69.6%解题思路:实验一:(1)根据氧气有助燃性,能使带火星的木条复燃进行分析;
(2)根据Na2O2与水反应放热,使吸滤瓶中的空气受热膨胀进行分析;
实验二:(1)根据质量守恒定律,反应物中没有碳元素,碳酸钠和稀盐酸反应能生成二氧化碳气体进行分析;
(2)根据酚酞遇碱变成红色,过氧化钠与水反应后生成氧气和氢氧化钠进行分析.实验一:(1)氧气能使带火星的木条复燃,所以生成的气体是:氧气;
(2)Na2O2与水反应放热,使吸滤瓶中的空气受热膨胀,所以伸入烧杯中的导管口看到有气泡产生;
实验二:(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能含有碳元素,碳酸钠中含有碳元素,设计一个证明Na2CO3不存在的实验:用试管取少量的反应后溶液,然后向试管中滴加过量的稀盐酸,没有气泡冒出,说明碳酸钠不存在;
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈碱性,过氧化钠与水反应后生成氧气和氢氧化钠,化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.
故答案为:实验一:(1)氧气;
(2)过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2C03;没有气泡产生;
(2)碱,2Na2O2+2H2O═4NaOH+O2↑.点评:
本题考点: 实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;证明碳酸盐;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本考点既考查了实验步骤的设计,又考查了化学方程式的书写,还对实验进行了评价,综合性比较强.1年前查看全部
- (2006•赤峰)水能灭火也可以引火.把少量过氧化钠(Na2O2)粉末用干燥脱脂棉包裹(脱脂棉和过氧化钠不反应),将少量
 (2006•赤峰)水能灭火也可以引火.把少量过氧化钠(Na2O2)粉末用干燥脱脂棉包裹(脱脂棉和过氧化钠不反应),将少量水滴到包有过氧化钠的脱脂棉上,则脱脂棉迅速发生燃烧.小明对此现象很感兴趣,于是他和同学们进行如下探究:
(2006•赤峰)水能灭火也可以引火.把少量过氧化钠(Na2O2)粉末用干燥脱脂棉包裹(脱脂棉和过氧化钠不反应),将少量水滴到包有过氧化钠的脱脂棉上,则脱脂棉迅速发生燃烧.小明对此现象很感兴趣,于是他和同学们进行如下探究:
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成.②反应过程中可能有能量变化.
【设计实验】如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中的分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:继续探究反应后生成的另一种物质是什么?
(1)小强猜想另一种物质是Na2CO3,小明认为不可能,小明的依据是______.
为了证实小明的看法,请你设计一个证明CO32-不存在的实验.
(2)小明取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的另一种物质是______(填化学式).实验步骤 实验现象 实验结论 ______ ______ ______
【表达与交流】
小华认为上述装置还能实现用过氧化氢制取氧气的实验.在试管中加入少量的MnO2固体,分液漏斗中加入30%的过氧化氢溶液,请写出此反应的化学方程式:2H2O2
2H2O+O2↑MnO2 .2H2O2.在此反应中MnO2起______ 作用.
2H2O+O2↑MnO2 . 缘份之天使1年前1
缘份之天使1年前1 -
 很酷狂顶 共回答了17个问题
很酷狂顶 共回答了17个问题 |采纳率88.2%解题思路:实验一:(1)能使带火星的木条复燃,说明该气体具有助燃性.
(2)导管口有气泡冒出,说明吸滤瓶内的压强增大,而反应是在试管内发生,不是在吸滤瓶内发生,所以是试管内发生的反应放出热量,使吸滤瓶内温度升高,气体压强增大.
实验二:(1)根据质量守恒定律,化学反应前后元素的种类不变;根据检验碳酸根离子的方法进行分析.
(2)根据酚酞溶液遇酸碱溶液的变色情况进行分析.
表达与交流:熟记常用的化学方程式;催化剂在化学反应中起催化作用.实验一:(1)氧气具有助燃性,能使带火星的木条复燃,说明生成的气体是氧气.故答案为:O2(或氧气)(2)试管内发生的反应放出热量,使吸滤瓶内的温度升高,气体压强增大,所以会看到导管口有气泡冒出.故答案为:反应过程中有热量放出,使吸滤瓶内空气受热膨胀.
实验二:(1)根据质量守恒定律,化学反应前后元素的种类不变,反应物中没有碳元素,因而生成物中也不可能有碳元素;碳酸根离子遇到盐酸会反应生成二氧化碳,有气泡冒出,若没有气泡冒出,则说明没有碳酸根离子.故答案为:根据质量守恒定律,化学反应前后元素的种类不变,而反应物中不含碳元素
实验步骤 实验现象 实验结论
取少量反应后所得溶液于试管中,滴入稀盐酸 没有气泡产生 不存在CO32-(2)酚酞溶液变红说明溶液显碱性,一定有氢氧根离子,而碱一般是由氢氧根离子和金属离子构成的,反应物中的金属元素只有钠元素,所以该物质是氢氧化钠.故答案为:NaOH
表达与交流:过氧化氢以二氧化锰为催化剂生成水和氧气;二氧化锰是过氧化氢制氧气的催化剂,催化剂在化学反应中起催化作用.
故答案为:2H2O2
MnO2
.
2H2O+O2↑ 催化点评:
本题考点: 实验室制取氧气的反应原理;猜想与事实验证;实验探究物质的组成成分以及含量;常见气体的检验与除杂方法;催化剂的特点与催化作用;水的性质和应用;酸碱指示剂及其性质;碳酸钠、碳酸氢钠与碳酸钙;书写化学方程式、文字表达式、电离方程式.
考点点评: 能使酚酞溶液变红的溶液一定显碱性,但不一定是碱溶液,例如:碳酸钠属于盐,其溶液显碱性,也能使酚酞溶液变成红色.1年前查看全部
- 一个化学题在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉
一个化学题
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
【提出问题】过氧化钠与水反应生成了什么物质? 为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成 ②反应过程中可能有热量放出
请填写下表
实验步骤 实验现象 实验结论
( ) ( ) 过氧化钠与水反应,有O2生成
( ) ( ) 过氧化钠与水反应,有热量放出
 风中的BOY1年前1
风中的BOY1年前1 -
 轻舟999 共回答了17个问题
轻舟999 共回答了17个问题 |采纳率94.1%答案:第一个实验:实验步骤:1.取少量过氧化钠与试管中.2.向在滴加少量水,将反应生成的气体收集到集气瓶中.3.将带火星的小木条伸入到集气瓶中.实验现象:试管中有气体生成;带火星的小木条复燃.实验结论:过氧化钠...1年前查看全部
- 如图所示,是某同学用酚酞试液和浓氨水做“氨分子的扩散”实验,结果发现试管内滤纸条上没有变色,而试管口所塞的脱脂棉却变成红
 如图所示,是某同学用酚酞试液和浓氨水做“氨分子的扩散”实验,结果发现试管内滤纸条上没有变色,而试管口所塞的脱脂棉却变成红色.导致这种现象产生错误操作可能是______,这一实验说明,所用的两种试剂中______具有挥发性.
如图所示,是某同学用酚酞试液和浓氨水做“氨分子的扩散”实验,结果发现试管内滤纸条上没有变色,而试管口所塞的脱脂棉却变成红色.导致这种现象产生错误操作可能是______,这一实验说明,所用的两种试剂中______具有挥发性.  txvgc1年前1
txvgc1年前1 -
 jiaxukui5201 共回答了19个问题
jiaxukui5201 共回答了19个问题 |采纳率84.2%试管内滤纸条没有变色,说明滤纸条上没有酚酞试液.脱脂棉变成红色,说明脱脂棉上有酚酞试液.
故答案为:酚酞试液滴在棉花上;浓氨水.1年前查看全部
- 在在学校的毕业典礼上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na 2 O 2 )粉末的脱脂棉上滴水,脱脂棉燃
在在学校的毕业典礼上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na 2 O 2 )粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究. 
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成;②反应过程中可能有能量变化
[实验设计]如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开图中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释该现象产生的原因:______.
实验二:继续探究反应后生成的另一种物质是什么?
小张猜想另一种物质是Na 2 CO 3 ,小军认为不可能.小军的依据是______;
如果用实验证明小军的观点正确,可以选择______(填试剂名称),加以证明. 膜拜5月天1年前1
膜拜5月天1年前1 -
 天蝎妹妹 共回答了24个问题
天蝎妹妹 共回答了24个问题 |采纳率87.5%实验一
(1)能使带火星的木条复燃的气体只能是氧气,故答案为:氧气.
(2)伸入烧杯中的导管口有气泡冒出,说明锥形瓶中的气体压强增大了,但是又没有新的气体生成,只能是里面的温度升高了,故答案为:反应放出的热量使锥形瓶内的气体膨胀;
实验二
(1)根据质量守恒定律,在化学反应前后,元素的种类不会增减,只是原子的重新组合过程.故答案为:根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na 2 CO 3 .
要验证碳酸钠,需要加入盐酸,看是否有气体产生.故答案为:稀盐酸1年前查看全部
- 如右图所示,用脱脂棉包住含少量钠元素的固体A,放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉燃烧起来.①A可以是单质钠,
如右图所示,用脱脂棉包住含少量钠元素的固体A,放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉燃烧起来.①A可以是单质钠,钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑;②A也可能是钠的化合物过氧化钠(化学式为Na2O2),Na2O2与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;

(1)通过实验现象判断,上述两个化学反应都是______反应(填“吸热”或“放热”).
(2)找出上述两个化学反应的其他相似之处(写出其中两点即可)______;______
Ⅱ.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用器,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)A是制取CO2的装置.写出实验室制取CO2的化学方程式:______.
(2)写表中空格:
(3)试管F中收集满气体后,下一步实验操作是:____________.仪器 加入试剂 加入该试剂的目的 发生反应的化学方程式 B 饱和NaHCO3溶液 除去CO2气体中混入的HCl C 过氧化钠 与CO2、水蒸气反应,产生O2 2Na2O2+2CO2=2Na2CO3+O2 D NaOH溶液  石头在跳舞1年前1
石头在跳舞1年前1 -
 纯粹膜拜你的ID 共回答了11个问题
纯粹膜拜你的ID 共回答了11个问题 |采纳率90.9%解题思路:本题通过实验探究分析了物质的性质和变化规律,属于新信息题.根据题目给出的信息和实验现象判断,上述两个化学反应都是放热反应,都是常温下与水反应,都有气体生成等.本题给出的实验装置,既有二氧化碳的制取、物质的除杂,又有二氧化碳气体的吸收,综合性比较强.要注意化学方程式的配平,检验氧气要用带火星的木条.Ⅰ、有题目给出的信息可知,脱脂棉燃烧起来,说明达到了着火点,因此为放热反应;两个化学反应的相似之处有:常温下就能反应;都有气体产生;都与水能发生化学反应等.故答案为:(1)放热(2)常温下就能反应;都有气体产生等(合理答案均可);
Ⅱ、(1)实验室制取CO2,是碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳.故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O
(2)用NaHCO3除去HCl气体时,生成了NaCl和CO2和H2O.用氢氧化钠溶液吸收未反应的CO2气体,生成Na2CO3和H2O,要注意配平.故答案为:NaHCO3+HCl=NaCl+CO2↑+H2O; 吸收未反应的CO2气体;CO2+2NaOH=Na2CO3+H2O.
(3)试管F中收集满气体后,下一步实验操作是:检验试管中的气体是否是氧气.故答案为:把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管.将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.点评:
本题考点: 实验探究物质的性质或变化规律;气体的净化(除杂);二氧化碳的实验室制法;物质发生化学变化时的能量变化.
考点点评: 本考点属于实验探究题,既有气体的制取又有气体的除杂和气体的吸收,还有气体的检验,综合性比较强.本题根据题目提供的信息,结合课本中学过的知识来解决,还要注意化学方程式的书写和配平.本考点主要出现在实验题中.1年前查看全部
- 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
 用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉花包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.
(1)由实验现象所得出的有关Na2O2和H2O反应的结论是:
a:有氧气生成;b:______.
(2)写出Na2O2和H2O反应的化学方程式:______.
(3)某研究性学习小组拟用如图装置进行实验,以证明上述结论.
①用以验证结论a的实验操作方法及现象是:
将带火星的木条靠近______(填p或q)管口,现象为______.
②用以验证结论b的实验操作方法及现象是:将导管______(填p或q)伸入到水槽中,现象为:______. 白菜也有生活1年前1
白菜也有生活1年前1 -
 x77927 共回答了15个问题
x77927 共回答了15个问题 |采纳率93.3%解题思路:(1)燃烧的条件是:a、物质具有可燃性,b、可燃物与氧气接触,c、温度达到可燃物的着火点,根据燃料燃烧的条件分析;
(2)过氧化钠和水反应生成氢氧化钠和氧气;
(3)①氧气具有能使带火星的木条复燃的性质;
②气体具有热胀冷缩的性质,该反应放出的热量能使集气瓶内空气的压强增大,据此分析问题.( 1)脱脂棉剧烈燃烧说明具备燃烧的条件,试管内空气较少,若剧烈燃烧应该有大量氧气,只有该反应是放热反应才能使燃料温度达到着火点,根据题意知该反应有氧气生成且放热,故答案为:反应放热;
(2)过氧化钠和水反应生成氢氧化钠和氧气,方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(3)①氧气具有使带火星的木条复燃的性质,所以可用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成,
故答案为:p;如果木条复燃,则有氧气生成,反之无氧气生成;
②气体具有热胀冷缩的性质,如果该反应放热,放出的热量能使集气瓶内空气的压强增大;如果q导管插入盛水的小烧杯中,有气泡冒出,证明此反应放热.
故答案为:q;有气泡冒出.点评:
本题考点: 碱金属及其化合物的性质实验;实验装置综合.
考点点评: 本题考查了过氧化钠和水反应的实验,难度不大,解答时要从实验现象方面进行分析、判断,从而得出正确的结论.1年前查看全部
- “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来
 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
【设计装置】如图所示
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计一个证明CO32-不存在的实验:
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈______性;实验步骤 实验现象 实验结论
______
______生成物中没有CO32-
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为______. 1宝马1年前1
1宝马1年前1 -
 maggie49 共回答了16个问题
maggie49 共回答了16个问题 |采纳率81.3%解题思路:实验一:氧气能使带火星的木条复燃;实验中,还观察到伸入烧杯中的导管口有气泡冒出,说明有气体逸出,可以判断反应中放出热量,导致吸滤瓶中的空气受热膨胀;实验二:碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;显碱性的溶液能使酚酞试液变红色;【表达】过氧化钠和水反应生成氧气和一种显碱性的物质,这种物质不是碳酸钠,那么应该是氢氧化钠.实验一:
(1)用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气.
故填:氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,说明该反应是放热的,反应放出的热量能使吸滤瓶中的空气受热膨胀,从导管逸出,产生气泡.
故填:反应放出热量,吸滤瓶中的空气受热膨胀,从导管逸出.
实验二:
(1)设计一个证明CO32-不存在的实验为:
实验步骤:取适量反应后的溶液于一试管中,向试管中滴加适量的稀盐酸;
实验现象:不产生气泡;
实验结论:生成物中不含有碳酸根离子.
故填:取适量反应后的溶液于一试管中,向试管中滴加适量的稀盐酸;不产生气泡.
(2)取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液显碱性,既然不是碳酸钠,那么应该是氢氧化钠.
故填:碱.
【表达】过氧化钠和水反应生成氢氧化钠和氧气,反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑.
故填:2Na2O2+2H2O═4NaOH+O2↑.点评:
本题考点: 实验探究物质的组成成分以及含量;证明碳酸盐;氧气的检验和验满;酸碱指示剂及其性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.1年前查看全部
- (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有
 (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:______
(1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na2O2和H2O反应的结论是:______
a:有氧气生成b:反应放热.
(2)Na2O2和H2O反应的化学方程式是______.
(3)某研究性学习小组拟用如图的装置进行实验,以证明上述结论.用以验证结论a的实验方法是:______
(4)用以验证结论b的实验方法及现象是:______. 姑娘就从了uu吧1年前1
姑娘就从了uu吧1年前1 -
 卢wyhs 共回答了19个问题
卢wyhs 共回答了19个问题 |采纳率84.2%解题思路:(1)燃烧的条件是:(1)物质具有可燃性,(2)可燃物与氧气接触,(3)温度达到可燃物的着火点,根据燃料燃烧的条件分析;
(2)过氧化钠和水反应生成氢氧化钠和氧气;
(3)氧气具有能使带火星的木条复燃的性质;
(4)气体具有热胀冷缩的性质,该反应放出的热量能使集气瓶内空气的压强增大,据此分析问题.( 1)脱脂棉剧烈燃烧说明具备燃烧的条件,试管内空气较少,若剧烈燃烧应该有大量氧气,只有该反应是放热反应才能使燃料温度达到着火点,根据题意知该反应有氧气生成且放热,故答案为:ab;
(2)过氧化钠和水反应生成氢氧化钠和氧气,方程式为2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(3)氧气具有使带火星的木条复燃的性质,所以可用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成,
故答案为:打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成.
(4)气体具有热胀冷缩的性质,如果该反应放热,放出的热量能使集气瓶内空气的压强增大;如果q导管插入盛水的小烧杯中,有气泡冒出,证明此反应放热.
故答案为:把q导管插入盛水的小烧杯中,有气泡冒出.点评:
本题考点: 钠的重要化合物;碱金属及其化合物的性质实验.
考点点评: 本题考查了过氧化钠和水反应的实验,难度不大,解答时要从实验现象方面进行分析、判断,从而得出正确的结论.1年前查看全部
- “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来
 “在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.”
小颖看到这段话后非常感兴趣,她和同学们一起对该问题进行了一系列的探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有能量变化
【设计装置】如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:探究反应后生成的另一种物质是什么?
(1)小明猜想另一种物质是Na2CO3,小军认为不可能.为了证实小军的看法,请你设计
一个证明CO32-不存在的实验:
(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现试管中的溶液变成红色,说明反应后所得的溶液呈______性;实验步骤 实验现象 实验结论
______
______生成物中没有CO32-
【表达】小军根据实验探究的结果,写出了过氧化钠和水反应的化学方程式为______.
【发现问题】小娟发现在小军的实验中,试管中的溶液变成红色后,一会儿又变成无色.
【深入探究】实验三:探究滴入无色酚酞试液后,变成红色的溶液为什么会褪色?
小娟经查阅资料,设计了如下实验方案,并将有关现象记录在下表中.
(1)根据小娟的实验探究,过氧化钠和水反应除了小军写出的反应外还存在另一个反应,其化学方程式为______.实验序号 实验方案 实验现象 1 将水滴入盛有过氧化钠固体的试管中,配制成溶液,用带火星的木条检验生成的气体 反应激烈,有大量气体产生,并能使木条复燃 2 取三份实验1所得溶液分装于三支试管中是进行如下实验:
①第一份中加入紫色石蕊试液
②第二份中加入无色酚酞试液
③第三份中先加水再加入无色酚酞试液
①溶液变蓝且长时间不褪色
②溶液显红色,半分钟内褪色
③溶液显红色,半分钟内褪色3 ①称取3.9g过氧化钠固体,逐滴加入约50mL水.
②待不再产生气体,10min以后,加入用小纸片包好的MnO2,迅速塞紧双孔塞,轻轻摇动反应器,纸包自动散开,MnO2与溶液开始接触.①测得氧气体积为185mL左右
②又产生大量氧气,至反应完全以后,又测得产生了374mL氧气(两次测定条件均相同)
(2)综合分析上述实验,猜想使变红的酚酞褪色的物质是______,请你用实验1所得的溶液,设计一个简单实验证明你的猜想______.
(3)根据实验3测得的气体体积说明了水与Na2O2反应生成的H2O2约有[1/3]发生分解水与Na2O2反应生成的H2O2约有[1/3]发生分解.
【反思与评价】根据小娟的实验探究方案,请你再提出一个需要探究的问题______. 似去年1年前1
似去年1年前1 -
 蓉城小女子 共回答了19个问题
蓉城小女子 共回答了19个问题 |采纳率100%解题思路:根据题干提供的信息进行分析,实验一:氧气能使带火星的木条复燃,过氧化钠与水的反应为放热反应,放出的热使温度升高,瓶内的压强增大,实验二:检验碳酸盐可以使用加酸化气的方法,酚酞试液在碱性溶液中变红,实验三:根据实验现象以及质量守恒定律可以推知还可能反应生成了过氧化氢,根据两次反应生成的氧气的体积即可推得反应的物质的量.实验一:(1)用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气,所以本题答案为:氧气;
(2)过氧化钠与水的反应为放热反应,放出的热使温度升高,瓶内的压强增大,气体向外逸出,所以本题答案为:过氧化钠与水反应放出热量,使瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生;
实验二:(1)检验碳酸盐可以使用加酸化气的方法,所以本题答案为:
实验步骤实验现象
取少量反应后所得的溶液于试管中,加入稀盐酸没有气泡产生(2)酚酞试液在碱性溶液中变红,根据质量守恒定律反应除了生成氧气还生成了氢氧化钠,所以本题答案为:碱,2Na2O2+2H2O═4NaOH+O2↑;
实验三:(1)根据实验现象以及质量守恒定律可以推知还可能反应生成了过氧化氢,所以本题答案为:Na2O2+2H2O═2NaOH+H2O2;
(2)氢氧化钠能使酚酞变红,水不能使酚酞褪色,故可能是过氧化氢使酚酞褪色,H2O2,要证明是过氧化氢的原因,可以设计实验将过氧化氢反应掉,而又不生成显碱性的物质,观察酚酞是否变红即可,所以本题答案为:在实验1所得溶液中加入少许MnO2,静置到无气体产生时,再加入无色酚酞试液,溶液变红且不再褪色;
(4)没加二氧化锰之前生成的氧气的体积为185mL,加入二氧化锰之后生成的氧气的体积为374mL,说明水与Na2O2反应生成的H2O2约有[1/3]发生分解,所以本题答案为:水与Na2O2反应生成的H2O2约有[1/3]发生分解;
[反思与评价]针对过氧化氢能使酚酞褪色,可以提出过氧化氢为什么能使酚酞褪色,所以本题答案为:H2O2使变红的酚酞褪色的原因是什么.点评:
本题考点: 常见气体的检验与除杂方法;酸碱指示剂及其性质;物质发生化学变化时的能量变化;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题为信息给予题,完成此类题目,要能够从题干中抽取有用的信息,根据已有的知识进行,同学们要能够从整体上把握题意,综合进行做题.1年前查看全部
- 用脱脂棉包住0.78g过氧化钠粉末,置于石棉网上,往脱脂棉上滴1mL水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住0.78g过氧化钠粉末,置于石棉网上,往脱脂棉上滴1mL水,可观察到脱脂棉剧烈燃烧起来.
如果用嘴通过细管向脱脂棉中吹气,脱脂棉也能燃烧起来,试写出反应的化学方程式. 人人都说我爱笑1年前1
人人都说我爱笑1年前1 -
 YYWIDD 共回答了11个问题
YYWIDD 共回答了11个问题 |采纳率81.8%滴水: 2Na₂O₂+ 2H₂O== 4NaOH +O₂↑
吹气: 2Na₂O₂ + 2CO₂ ==== 2Na₂CO₃ + O₂
因为反应产生O2.并且都是放热的,达到了脱脂棉的燃点,所以燃烧了1年前查看全部
- 医用脱脂棉是一种有机物,把脱脂棉隔绝空气加热时,能生成碳和水,根据这一事实推断:
医用脱脂棉是一种有机物,把脱脂棉隔绝空气加热时,能生成碳和水,根据这一事实推断:
(1)脱脂棉由哪几种元素组成?
(2)若使脱脂棉在足量的纯氧中燃烧,生成的产物应该有哪些?
(3)脱脂棉+水葡萄糖.葡萄糖由哪些元素组成. lm423661年前2
lm423661年前2 -
 Raulzhan 共回答了25个问题
Raulzhan 共回答了25个问题 |采纳率88%1脱脂棉由C,H,O三种元素组成
2.生成的产物应该有CO2 ,H2O
3.脱脂棉+水=葡萄糖
葡萄糖由C,H,O三种元素组成.1年前查看全部
- 10g脱脂棉与浓硫酸,浓硝酸共热得15.6g纤维素硝酸酯.计算并推断该纤维素硝酸酯的结构简式.
10g脱脂棉与浓硫酸,浓硝酸共热得15.6g纤维素硝酸酯.计算并推断该纤维素硝酸酯的结构简式.
如何推断呢? 水蛭shere1年前2
水蛭shere1年前2 -
 爱学习的xxfap 共回答了17个问题
爱学习的xxfap 共回答了17个问题 |采纳率100%嗯,首先,考虑到 计算并推断该纤维素硝酸酯的结构简式 ,那么答案应该是唯一的结构简式. 而我们学习知道,它的预选答案有3个,即一硝酸,二硝酸,三硝酸.
如此,因为先后质量差为15.6-1=5.6g, 而对应是增加1个硝酸基团并且失去一份水,所以硝酸用了 5.6除以(硝酸分子式量-水分子式量)=0.124摩尔.
而脱脂棉(就是纤维素,)式量是180,所以10g脱脂棉=0.055摩尔.
那么 脱脂棉 与 硝酸 反应比例 是 0.055:0.124约等于 1:2 (因为前面的0.124,0.055都是分数化过来的,分数这里打不出来,囧.不过误差有点大啊.)
奇怪了.不是整倍数.
题目有没有错误?1年前查看全部
- 包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧为什么?
包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧为什么?
为什么脱脂棉燃烧?
猜想:①——②——
实验探究:①打开上图装置分液漏斗的活塞,控制滴加水的速度,观察到使馆内有气泡产生,用——.说明生成气体是——. Miracle-M1年前1
Miracle-M1年前1 -
 cnflz3 共回答了17个问题
cnflz3 共回答了17个问题 |采纳率100%①反应放热②反应产生氧气(第二个是猜的)
……观察到使馆内有气泡产生,用(带火星的木条伸到管内,发现复燃).说明生成气体是(氧气).1年前查看全部
- 化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来
化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来。
(1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:
第一:有氧气生成;
第二:______________。
Na 2 O 2 跟水反应的化学方程式是________________________。
(2)某研究性学习小组拟用下图所示装置(气密性良好)进行实验,以证明上述结论。
用以验证第一条结论的实验操作是:___________________________;用以验证第二条结论的实验方法是:______________________________。
(3)实验(2)往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色。为探究其原因,该小组同学从查阅有关资料中得知:Na 2 O 2 与水反应可生成H 2 O 2 ,H 2 O 2 具有强氧化性和漂白性。
请设计一个简单的实验,验证Na 2 O 2 跟足量水充分反应后的溶液中有H 2 O 2 存在。(只要求写出实验所用的试剂及观察到的现象)试剂:_______________________;现象:____________________________。
(4)该小组同学提出用定量的方法探究Na 2 O 2 跟水反应后的溶液中否含有H 2 O 2 ,其实验方法为:称取
2.6g Na 2 O 2 固体,使之与足量的水反应,测量产生O 2 的体积并与理论值比较,即可得出结论。
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的__________ (忽略导管在量筒中所占的体积)(填序号),理由是___________________。
②若在标准状况下测量气体的体积,应选用的量筒的大小规格为____________(选填“100mL”“200 mL”“500 mL”或“1000 mL”)。 vanessa_xw1年前1
vanessa_xw1年前1 -
 大漠狐鹰 共回答了23个问题
大漠狐鹰 共回答了23个问题 |采纳率78.3%(1)该反应是放热反应;2Na 2 O 2 +2H 2 O==4NaOH+O 2 ↑
(2)打开分液漏斗活塞使水流入试管,再将带火星的木条靠近导管口P处,木条复燃,证明有O 2 生成;将导管Q浸入水中,反应过程中导管口有气泡冒出
(3)MnO 2 ;气泡迅速产生,能使带火星的木条复燃
(4)①B;防止气体冷却时发生倒吸现象;②500mL1年前查看全部
- 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
 用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,向脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(1)由上述实验现象所得到的过氧化钠跟水反应的结论是:
①有氧气生成;②反应过程中有______.
(2)Na2O2跟水反应的化学方程式为______.此反应中氧化剂是______.
(3)某研究性学习小组拟用右图所示装置(气密性良好)进行实验,以证明上述实验结论.验证第①条结论的实验操作及现象是:向试管中滴入水,______.
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,现象为______. 末代法盲1年前1
末代法盲1年前1 -
 lkbest 共回答了20个问题
lkbest 共回答了20个问题 |采纳率90%解题思路:(1)脱脂棉剧烈燃烧起来,说明该反应中有氧气放出其该反应为放热反应;
(2)过氧化钠与水反应生成氢氧化钠和氧气,据此写出反应的化学方程式;过氧化钠的化合价为-1价,该反应中过氧化钠既是氧化剂,也是还原剂;
(3)根据实验室中常用的检验氧气的方法进行解答;
(4)反应有氢氧化钠生成,溶液显示碱性,同时反应中有双氧水生成,实验室具有漂白性,据此进行解答.(1)根据反应现象可知,该反应为放热反应,放出的热量时脱脂棉燃烧,反应生成的氧气时燃烧更剧烈,
故答案为:放出大量的热;
(2)过氧化钠与水反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑,过氧化钠的化合价为-1价,在反应中过氧化钠的-1价的O化合价升高被氧化成氧气,同时-1价的O被氧化成-1价的O,所以氧化剂、还原剂但是过氧化钠,
故答案为:2Na2O2+2H2O═4NaOH+O2↑; Na2O2;
(3)检验过氧化钠与水反应有氧气放出,可以将带火星的木条放在P口处,木条会复燃,证明反应中有氧气产生,
故答案为:将带火星的木条放在P口处,木条复燃;
(4)向试管中加水至固体完全溶解且不再有气泡生成后,取出试管,向试管中滴入酚酞试液并振荡,由于溶液为碱性溶液,所以滴入酚酞后溶液变成红色,又由于Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性,所以红色的溶液会褪色,所以现象为:溶液先变红后褪色,
故答案为:溶液先变红后褪色.点评:
本题考点: 碱金属及其化合物的性质实验.
考点点评: 本题考查了过氧化钠的化学性质,题目难度中等,注意掌握钠及其化合物的性质,熟练掌握过氧化钠与水、二氧化碳反应的化学方程式,明确检验氧气的方法.1年前查看全部
- (1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有
(1)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉剧烈燃烧起来.由实验现象所得出的有关Na 2 O 2 和H 2 O反应的结论是:______
a:有氧气生成b:反应放热.
(2)Na 2 O 2 和H 2 O反应的化学方程式是______.
(3)某研究性学习小组拟用如图的装置进行实验,以证明上述结论.用以验证结论a的实验方法是:______
(4)用以验证结论b的实验方法及现象是:______.
 九步之小猫咪1年前1
九步之小猫咪1年前1 -
 wo爱妻 共回答了24个问题
wo爱妻 共回答了24个问题 |采纳率91.7%( 1)脱脂棉剧烈燃烧说明具备燃烧的条件,试管内空气较少,若剧烈燃烧应该有大量氧气,只有该反应是放热反应才能使燃料温度达到着火点,根据题意知该反应有氧气生成且放热,故答案为:ab;
(2)过氧化钠和水反应生成氢氧化钠和氧气,方程式为2Na 2 O 2 +2H 2 O=4NaOH+O 2 ↑,
故答案为:2Na 2 O 2 +2H 2 O=4NaOH+O 2 ↑;
(3)氧气具有使带火星的木条复燃的性质,所以可用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成,
故答案为:打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成.
(4)气体具有热胀冷缩的性质,如果该反应放热,放出的热量能使集气瓶内空气的压强增大;如果q导管插入盛水的小烧杯中,有气泡冒出,证明此反应放热.
故答案为:把q导管插入盛水的小烧杯中,有气泡冒出.1年前查看全部
- 在学校的元旦联欢会上,小王同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
 在学校的元旦联欢会上,小王同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,小王同学表演了“水能生火”的魔术.他向包有过氧化钙(CaO2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很兴趣,于是,他和同学们进行探究.
【提出问题】该魔术是如何给可燃物脱脂棉提供燃烧的另外两个燃烧条件的呢?
【猜想】①过氧化钙与水反应可能有一种气体和另一种物质生成;②反应过程中可能有热量放出
【设计装置】如图所示
【实验探究】
(1)打开装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明过氧化钙与水反应生成了一种气体,这使可燃物脱脂棉满足了燃烧的一个条件是______.
(2)实验过程中,还观察到U型管A端红墨水液面下降,该现象说明______,这使可燃物脱脂棉满足了燃烧的另一个条件是______.
【拓展提高】
(1)CaO2和H2O反应除生成一种气体外,还生成了一种固体,小明认为生成的固体是Ca(OH)2,小红认为是CaCO3,同学们经过思考讨论后认为小红同学的猜想是错误的,你认为他们的理由是:______.
(2)小明设计了一个实验方案来验证过氧化钙和水反应产生的另一种物质是氢氧化钙,请你帮助他完成:
【问题讨论】实验步骤及操作方法 预期的实验现象 结论 ①取少量过氧化钙放入试管中,加足量水,振荡,
②______
______.①产生气泡,
②______
______.过氧化钙和水反应产生的另一种物质是氢氧化钙
(1)小明尝试上述魔术表演时,滴加水的速度太快,发现脱脂棉没有燃烧起来,请你从燃烧的条件分析原因是______.
(2)过氧化钙和水反应的化学方程式为______. soury1年前1
soury1年前1 -
 aloveybbs 共回答了12个问题
aloveybbs 共回答了12个问题 |采纳率91.7%解题思路:【实验探究】
可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
温度越高,气体的压强越大;
【拓展提高】
化学反应前后,元素的种类不变,原子的种类、总个数不变;
氢氧化钙的水溶液显碱性,能使酚酞试液变红色;
氢氧化钙的水溶液又称为石灰水,二氧化碳能使澄清石灰水变浑浊;
【问题讨论】
水蒸发时吸收热量,能使周围的温度降低;
根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式.【实验探究】
(1)过氧化钙和水反应生成的气体能使带火星的木条复燃,说明产生的是氧气,这使可燃物脱脂棉满足了燃烧的一个条件是与氧气接触.
故填:与氧气接触.
(2)实验过程中,还观察到U型管A端红墨水液面下降,该现象说明U型管A端的压强高于右边的压强,进一步说明过氧化钙和水反应放出热量,这使可燃物脱脂棉满足了燃烧的另一个条件是温度达到脱脂棉的着火点.
故填:过氧化钙和水反应放出热量;温度达到脱脂棉的着火点.
【拓展提高】
(1)因为反应物过氧化钙和水中都不含有碳元素,所以产物中不可能含有碳元素,即不可能生成碳酸钙.
故填:过氧化钙和水中不含有碳元素,不可能生成碳酸钙.
(2)实验步骤及操作方法:①取少量过氧化钙放入试管中,加足量水,振荡;
②取两份溶液,向一份中滴加适量的酚酞试液,向另一份中通入二氧化碳.
预期的实验现象:①产生气泡;
②酚酞试液变红色,溶液变浑浊.
实验结论:过氧化钙和水反应产生的另一种物质是氢氧化钙.
故填:取两份溶液;向一份中滴加适量的酚酞试液,向另一份中通入二氧化碳;酚酞试液变红色;溶液变浑浊.
【问题讨论】
(1)如果滴加水的速度太快,过量的水吸热较多,温度不能达到脱脂棉的着火点,会导致脱脂棉没有燃烧起来.
故填:过量的水吸热较多,温度不能达到脱脂棉的着火点.
(2)过氧化钙和水反应的化学方程式为:2CaO2+2H2O═2Ca(OH)2+O2↑.点评:
本题考点: 实验探究物质变化的条件和影响物质变化的因素;碱的化学性质;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式;燃烧与燃烧的条件.
考点点评: 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.1年前查看全部
- 用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加几滴水,结果脱脂棉剧烈燃烧起来。
用脱脂棉包住约0.2g过氧化钠固体粉末,置于石棉网上,然后向包有过氧化钠的位置滴加几滴水,结果脱脂棉剧烈燃烧起来。

试完成下列问题:
(1)写出过氧化钠与水反应的化学方程式
(2)结合脱脂棉剧烈燃烧的实验事实及燃烧的条件可以得出的结论是
(3)某研究性学习小组,为进一步证明上述结论,拟用如图所示的装置进行有关实验。请写出有关的实验操作方法
现象:A处: B处: diaoguoan1年前1
diaoguoan1年前1 -
 hwj1228 共回答了12个问题
hwj1228 共回答了12个问题 |采纳率100%(1) 2Na 2 O 2 + 2H 2 O=4NaOH+O 2 ↑
(2)过氧化钠与水反应放出热量并有助燃气体放出
(3)打开A,并在A处放一带火星的木条;带火星的木条复燃;有气泡放出
1年前查看全部
- (2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水
 (2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
(2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
提出问题:过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
猜想:①可能有一种气体和另一种物质生成②反应过程中可能有热量放出
设计实验:如右图所示
实验探究:
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小蔡认为不可能.小蔡的依据是______.
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色.说明反应后所得的溶液呈______性.
交流:由实验探究的结果,写出过氧化钠和水反应的化学方程式______. 闫成涛1年前1
闫成涛1年前1 -
 xiaobai417 共回答了16个问题
xiaobai417 共回答了16个问题 |采纳率87.5%在探究实验时,步骤为:提出问题,猜想,设计实验,实验探究,交流.
实验一:(1)能产生使带火星的木条复燃的气体,说明该气体为氧气.
(2)在此反应中,一定有热量放出,放出的热量使锥形瓶内的压强变大,从而在导管口处有气泡冒出.
实验二:
(1)化学反应满足质量守恒定律,所以在反应过程中因反应物中没有碳元素,故在生成物中不可能产生碳酸钠.
(2)因滴加酚酞试液后,酚酞试液变为红色.所以溶液呈碱性.
在完成实验时的交流中我们可以来交流在做实验时的注意事项,也可以交流实验中自己的疑惑,或者是交流所用到的实验原理等.
故答案为:
实验一:
(1)氧气(或02)
(2)过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
实验二:
(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3
(2)碱;2Na202+2H2O═4NaOH+02↑1年前查看全部
- 如右图所示,用脱脂棉包住含少量钠元素的固体A,放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉燃烧起来.①A可以是单质钠,
如右图所示,用脱脂棉包住含少量钠元素的固体A,放在石棉网上.在脱脂棉上滴加几滴水,发现脱脂棉燃烧起来.①A可以是单质钠,钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑;②A也可能是钠的化合物过氧化钠(化学式为Na2O2),Na2O2与水反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;
.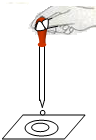
(1)通过实验现象判断,上述两个化学反应都是放热放热反应(填“吸热”或“放热”).
(2)找出上述两个化学反应的其他相似之处(写出其中两点即可)
都有水参加反应都有水参加反应;都生成气体单质(或都生成氢氧化钠)都生成气体单质(或都生成氢氧化钠)
Ⅱ.在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.请选用适当的化学试剂和实验用器,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂.
(1)A是制取CO2的装置.写出实验室制取CO2的化学方程式:CaCO3+2HCl=CaCl2+CO2↑+H2OCaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)写表中空格:
NaHCO3+HCl=NaCl+CO2↑+H2ONaHCO3+HCl=NaCl+CO2↑+H2O、吸收未反应的CO2气体吸收未反应的CO2气体.仪器 加入试剂 加入试剂的目的 发生反应的化学方程式 B 饱和NaHCO3溶液 除去CO2气体中混入的HCl C 过氧化钠 与CO2、水蒸气反应,产生O2 2Na2O2+2CO2=2Na2CO3+O2 D NaOH溶液 吸收没反应的二氧化碳,保证氧气纯净吸收没反应的二氧化碳,保证氧气纯净 2NaOH+CO2=Na2CO3+H2O2NaOH+CO2=Na2CO3+H2O
(3)试管F中收集满气体后,下一步实验操作是:把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管.将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管.将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.. Jlsn121年前1
Jlsn121年前1 -
 nabo118 共回答了16个问题
nabo118 共回答了16个问题 |采纳率100%(1)脱脂棉燃烧起来,说明它达到了着火点,反应给提供的热量,因此反应放热.
(2)由化学方程式为2Na+2H2O=2NaOH+H2↑和2Na2O2+2H2O=4NaOH+O2↑知,都有水参加反应,都生成气体单质,或都生成氢氧化钠.
Ⅱ.(1)A装置制取CO2是利用碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)碳酸氢钠和盐酸反应生成氯化钠、水、二氧化碳,方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O;D中的氢氧化钠溶液是为了吸收没反应的二氧化碳,保证氧气纯净.反应为2NaOH+CO2=Na2CO3+H2O
(3)试管F中收集满气体后,要气体取出,操作是把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管.然后检验气体是氧气,操作是将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
故答案为:(1)CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)NaHCO3+HCl=NaCl+CO2↑+H2O;吸收未反应的CO2气体;2NaOH+CO2=Na2CO3+H2O
(3)把E中的导管移出水面,关闭分液漏斗活塞,用拇指堵住试管口,取出试管.将带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.1年前查看全部
- (2014•思南县模拟)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉
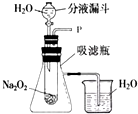 (2014•思南县模拟)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
(2014•思南县模拟)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
【提出问题】过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
【猜想】①可能有一种气体和另一种物质生成
②反应过程中可能有热量放出
【实验装置】如图所示
【实验探究】
实验一:探究反应后生成的气体是什么?
(1)打开如图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是______.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:______.
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小蔡认为不可能.小蔡的依据是______.
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色.说明反应后所得的溶液呈______性.
【表达】由实验探究的结果,写出过氧化钠和水反应的化学方程式______. ffyym1年前1
ffyym1年前1 -
 mimi523 共回答了14个问题
mimi523 共回答了14个问题 |采纳率78.6%解题思路:实验一:氧气能够支持燃烧,能使带火星的木条复燃;
根据实验现象可以判断反应中热量变化情况;
实验二:化学反应遵循质量守恒定律,即反应前后元素的种类不变;
显碱性的溶液能使酚酞试液变红色;
【表达】根据实验现象可以判断过氧化钠和水反应生成氢氧化钠和氧气.【实验探究】实验一:
(1)用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气.
故填:氧气.
(2)过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
故填:反应放出热量,使吸滤瓶中的空气受热膨胀.
实验二:
(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有碳酸钠.
故填:反应物中不含有碳元素.
(2)滴入无色酚酞试液,发现酚酞试液变红色.说明反应后所得的溶液显碱性.
故填:碱.
【表达】由实验探究的结果可知,过氧化钠和水反应生成氢氧化钠和氧气,反应的化学方程式为:2Na202+2H2O═4NaOH+O2↑.
故填:2Na202+2H2O═4NaOH+O2↑.点评:
本题考点: 实验探究物质的组成成分以及含量;氧气的检验和验满;溶液的酸碱性测定;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 过氧化钠与水反应能产生氧气,同时通过氧气具有助燃的性质,来检验过氧化钠与水反应产生的气体是氧气.1年前查看全部
- (2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水
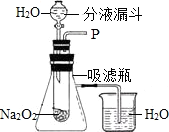 (2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
(2007•泰安)在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
提出问题:过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
猜想:①可能有一种气体和另一种物质生成②反应过程中可能有热量放出
设计实验:如右图所示
实验探究:
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是氧气氧气.
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO3,小蔡认为不可能.小蔡的依据是根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3.
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色.说明反应后所得的溶液呈碱碱性.
交流:由实验探究的结果,写出过氧化钠和水反应的化学方程式2Na202+2H2O═4NaOH+02↑2Na202+2H2O═4NaOH+02↑. 用键盘敲出人生1年前1
用键盘敲出人生1年前1 -
 无限人生 共回答了16个问题
无限人生 共回答了16个问题 |采纳率81.3%解题思路:在过氧化钠上滴加水,脱脂棉燃烧起来,说明满足燃烧的条件,也就是有氧气产生.同时在此反应中有热量放出.由质量守恒定律可猜想生成物中有碳酸钠,然后根据碳酸钠的性质来说明有这种物质生成.在探究实验时,步骤为:提出问题,猜想,设计实验,实验探究,交流.
实验一:(1)能产生使带火星的木条复燃的气体,说明该气体为氧气.
(2)在此反应中,一定有热量放出,放出的热量使锥形瓶内的压强变大,从而在导管口处有气泡冒出.
实验二:
(1)化学反应满足质量守恒定律,所以在反应过程中因反应物中没有碳元素,故在生成物中不可能产生碳酸钠.
(2)因滴加酚酞试液后,酚酞试液变为红色.所以溶液呈碱性.
在完成实验时的交流中我们可以来交流在做实验时的注意事项,也可以交流实验中自己的疑惑,或者是交流所用到的实验原理等.
故答案为:
实验一:
(1)氧气(或02)
(2)过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
实验二:
(1)根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3
(2)碱;2Na202+2H2O═4NaOH+02↑点评:
本题考点: 实验探究物质的性质或变化规律;酸碱指示剂的使用;氧气的检验和验满;物质发生化学变化时的能量变化;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式.1年前查看全部
- 用干净的玻璃管涂有过氧化钠,吹棉,脱脂棉燃烧,说明CO2,H2O和过氧化钠反应是放热的,如果反应是放热的中的一个,而另一
用干净的玻璃管涂有过氧化钠,吹棉,脱脂棉燃烧,说明CO2,H2O和过氧化钠反应是放热的,如果反应是放热的中的一个,而另一个不
 n678431年前1
n678431年前1 -
 我是杨枫 共回答了25个问题
我是杨枫 共回答了25个问题 |采纳率96%如果没有媒体的水,二氧化碳和干过氧化钠不反应实际上,将反应是二氧化碳和过氧化钠,过氧化钠和水,氢氧化钠反应后生成1年前查看全部
- 用脱脂棉包住Na2O2粉末,往上面滴水,观察到脱脂棉剧烈燃烧起来,可得Na2O2与水反应的结论有哪两个
 八妹1年前2
八妹1年前2 -
 yangkeep 共回答了13个问题
yangkeep 共回答了13个问题 |采纳率100%1 该反应是放热反应
2 该反应能产生O21年前查看全部
- 从脱脂棉的燃烧可以推出过氧化钠与二氧化碳反应的结论是
 audioboy1年前3
audioboy1年前3 -
 秋日香气 共回答了19个问题
秋日香气 共回答了19个问题 |采纳率100%反应放出氧气和大量热1年前查看全部
- 过氧化钠和二氧化碳反应使脱脂棉燃烧,有时为什么会失败
 luliyao1年前2
luliyao1年前2 -
 焦作山水 共回答了17个问题
焦作山水 共回答了17个问题 |采纳率94.1%过氧化钠放置的时间长了 会和空气中的水反应 表面会变质 导致试验失败~1年前查看全部
- 加热Cl2和Cu之后、在试管口放脱脂棉的作用是?
加热Cl2和Cu之后、在试管口放脱脂棉的作用是?
还有这个反应的方程式以及现象
还有、之后又有一个集气瓶、集气瓶中的现象是? weiqq198314791年前1
weiqq198314791年前1 -
 mmnn9898 共回答了20个问题
mmnn9898 共回答了20个问题 |采纳率95%防止铜粒堵塞导管,铜在氯气中燃烧,化学方程式:Cu+Cl2=CuCl2 集气瓶中充满棕黄色的烟.实际上是氯化铜的微小晶体造成的1年前查看全部
- 氨气收集问题按其收集满后,可用脱脂棉蘸取下列的______溶液放于试管口,吸收氨气,防止污染空气.A.稀盐酸 B.稀硫酸
氨气收集问题
按其收集满后,可用脱脂棉蘸取下列的______溶液放于试管口,吸收氨气,防止污染空气.
A.稀盐酸 B.稀硫酸 C.稀硝酸 D.稀氢氧化钠溶液
我的疑问是,为什么不选稀硝酸?是因为它挥发么?
还有,选用脱脂棉有什么好处?难道是因为未脱脂的棉花会在酸性条件下水解?棉花不是纤维素么怎么又有脂肪了? foxbubufan1年前2
foxbubufan1年前2 -
 木子88 共回答了16个问题
木子88 共回答了16个问题 |采纳率93.8%稀硝酸会与氨气反应故不能选用
棉花纤维中含有脂肪
脱脂棉更易点燃.
洁净,不会污染化学试剂.
脱去脂质后,吸水性增强.1年前查看全部
- 可以用脱脂棉过滤高锰酸钾溶液吗
 asas151年前1
asas151年前1 -
 阳星 共回答了22个问题
阳星 共回答了22个问题 |采纳率81.8%脱脂棉是什么?有机物;高锰酸钾是什么?强氧化剂.强氧化剂遇到了有机物或还原剂会怎么样?!
在即将迈入21世纪时,联合国教科文组织的负责人这样寄语:“21世纪的文盲不是说他不识字,而是没有掌握良好的学习方式方法.”良好的学习方式方法就包括多观察、多思考!1年前查看全部
- 某化学兴趣小组同学为了研究影响分子运动速率的因素,如图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨
某化学兴趣小组同学为了研究影响分子运动速率的因素,如图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水.浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢(HCl)能发生如下反应,NH3+HCl=NH4Cl.两个注射器同时向脱脂棉靠学科王近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管.根据现象回答问题:

(1)生成物NH4Cl常温下的状态是______(填“固体”、“液体”或“气体”);
(2)有同学认为先在A处产生白烟是因为HCl分子比NH3分子运动速度慢,请你分析影响分子运动速度的因素可能是______;
(3)影响分子运动速率的因素还有温度,请举出生活中的一个实例______;
(4)该实验中的注射器也可改用胶头滴管直接滴入液体,相比较用注射器的优点是______. fxcaphu1年前1
fxcaphu1年前1 -
 鱼翔BUAA 共回答了13个问题
鱼翔BUAA 共回答了13个问题 |采纳率92.3%解题思路:(1)根据实验现象判断氯化铵的状态;(2)根据它们的相对分子质量的区别考虑;(3)根据温度与运动速度的关系考虑;(4)根据注射器的特点考虑.(1)烟是固体颗粒,因为氯化氢与氨气反应生成了氯化铵,且产生白烟,所以氯化铵是固体;
(2)氯化氢的相对分子质量为36.5,氨气的相对分子质量为17,相对分子质量越小运动速度越快;
(3)升高温度分子运动速度就加快,只要能说明温度高了运动速度快了的例子都可以,例如阳光下或者温度高衣服干得快,温度高水蒸发的快,糖在热水里比在冷水里溶解的快等;
(4)由于注射器装入的药品少,现象明显,又是封闭状态,所以可以控制体积节省药品、可以减少气体挥发造成的污染等.
故答案为:(1)固体;
(2)分子的质量大小或者相对分子质量大小(合理即给分);
(3)阳光下或者温度高衣服干得快,温度高水蒸发的快,糖在热水里比在冷水里溶解的快等;
(4)可以控制体积节省药品、可以减少气体挥发造成的污染等点评:
本题考点: 物质的微粒性.
考点点评: 通过回答本题知道了分子的性质和运动速度的影响因素,设计实验要从节约药品、减少污染等方面考虑.1年前查看全部
- 将滴有酚酞试液的滤纸条放在试管里,在试管口上塞一小团脱脂棉
将滴有酚酞试液的滤纸条放在试管里,在试管口上塞一小团脱脂棉
1、用仪器 A 吸取浓氨水,地在试管口的脱脂棉上,A 的仪器名称是什么?
2、实验中往往在试管下方一张白纸,则白纸的作用是什么?
3、实验中看到的现象是什么? runrun061年前1
runrun061年前1 -
 hy5034080 共回答了21个问题
hy5034080 共回答了21个问题 |采纳率90.5%1滴管
2方便与试纸的颜色变化进行对比
3滤纸条编成粉红色1年前查看全部
- 化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化纳(Na202)粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂
 化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化纳(Na202)粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化纳(Na202)粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
( 1)由上述实验现象所得出的有关过氧化钠跟水反应的结论是:第一:有氧气生成;第二:______.
(2)甲、乙两位同学拟用右图所示装置(气密性良好)进行实验. 用以验证第一条结论的实验操作是:______.
(3)甲同学往试管中加水至固体完全溶解且不再有气泡生成后,取出试管,往试管中滴入酚酞试液,发现溶液先变红后褪色.为探究其原因,该同学从查阅有关资料中得知:Na2O2与水反应可生成H2O2,H2O2具有强氧化性和漂白性.请设计一个简单的实验,验证Na2O2跟足量水充分反应后的溶液中有H2O2存在.(只要求写出实验所用的试剂及观察到的现象)
试剂:______;
现象:______.
(4)乙同学提出用定量的方法探究Na2O2跟水反应后 的溶液中否含有H2O2,其实验方法为:称取一定量Na2O2固体,使之与足量的水反应,测量产生O2的体积并与理论值比较,即可得出结论.测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用上图装置中的(忽略导管在量筒中所占的体积)______(填序号),理由是______. 明月居士1年前1
明月居士1年前1 -
 11jin11 共回答了15个问题
11jin11 共回答了15个问题 |采纳率86.7%解题思路:(1)燃烧的条件是:物质具有可燃性、可燃物与氧气接触、温度达到可燃物的着火点,三个条件必须同时具备,缺一不可;
(2)验证氧气用带火星的小木条;
(3)利用过氧化氢分解生成氧气的性质加以验证;
(4)导管太短,气体冷却时易倒吸.(1)脱脂棉燃烧说明具备燃烧的条件,有可燃物且与氧气接触,故猜测该反应是放热的.故填:放出大量的热.
(2)要检验氧气的生成,用带火星打开活塞向试管内过氧化钠上滴几滴水,用带火星的木条靠近p处,如果木条复燃,则有氧气生成,反之无氧气生成.故填:打开活塞向试管内的过氧化钠上滴几滴水,用带火星的木条靠近p处;
(3)依据课本知识:过氧化氢加入二氧化锰可快速产生氧气.故填:二氧化锰;气泡迅速产生,能使带火星的木条复燃;
(4)由于Na2O2固体水反应放出大量的热,为防止气体冷却时水被倒吸,所以选择B装置.故填:B;防止气体冷却时发生倒吸现象.点评:
本题考点: 实验探究物质的性质或变化规律;燃烧与燃烧的条件.
考点点评: 此类题是对实验结论的分析和对实验方案的设计,要认真研究,理解题意理清思路,然后再结合所学知识进行解答.1年前查看全部
- 教材中有一个演示实验:用脱脂棉包住约0.2 g Na 2 O 2 粉末,置于石棉网上,可观察到脱脂棉燃烧起来。
教材中有一个演示实验:用脱脂棉包住约0.2 g Na 2 O 2 粉末,置于石棉网上,可观察到脱脂棉燃烧起来。
(1)由实验现象能得出的有关Na 2 O 2 与水反应的结论是:a.有氧气生成;b._____________。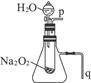
(2)某研究性学习小组拟用如右图所示装置进行实验,以证明上述结论。
①用以验证结论a的实验方法及现象是_____________________________________________。
②用以验证结论b的实验方法及现象是_____________________________________________。 ll51年前1
ll51年前1 -
 mfdyw 共回答了19个问题
mfdyw 共回答了19个问题 |采纳率94.7%(1)该反应是放热反应
(2)①将带火星的木条靠近导管口p处,木条复燃 ②将导管q放入水中,反应过程中导管口有气泡冒出
(1)脱脂棉燃烧的条件:一是有氧气(空气),二是达到其着火点,所以结论b应是该反应是放热反应。
(2)产生的O 2 必定从p口逸出,所以可用带火星的木条在此处检验;反应放热必使试管外锥形瓶内的空气膨胀,故可在q处验证。1年前查看全部
大家在问
- 1我自学口语,一直没有什么太大进步.想提升下自己的口语水平,乐其英语怎么样?价位如何?
- 2Do you have ______ healthy food every day
- 3甲、乙两船从相距240千米的两个港口同时相向而行,甲船顺水,乙船逆水,两船在静水中的速度都是a千米/时
- 4口袋中有6个黄色乒乓球和若干个白色乒乓球,从中任意摸出一个乒乓球,摸出黄色乒乓球的可能性是1/4
- 5He will teach me -----this year?选to skate 还是skating
- 6Looking after yourself is an important thing that is good fo
- 7象的寿命是80年,海龟的寿命比大象的2.5倍还多20年,海龟能活多少年?
- 8I'm thirteen years old,and Li Lei is fifteen 的同义句 Li Lei is
- 9英语翻译转到企不起
- 10请问:“承包了这几座大楼的清洁工作”用英语怎么说!
- 11小肠绒毛壁有几层细胞在小肠内部满了什么?消化和吸收营养物质的主要场所是什么?各种食物含有( ){相同、不同}的营养成分?
- 12若所求的二次函数图象与抛物线y=2x2-4x-1有相同的顶点,并且在对称轴的左侧,y随x的增大而增大,在对称轴的右侧,y
- 13甲、乙两物体分别做匀加速和匀减速直线运动,已知乙的初速度是甲的初速度的2.5倍,且甲的加速度大小是乙的加速度大小的2倍,
- 1478060.40的大写怎么写作,和怎么读作?要大写数字啊
- 15证明牛顿第一定律的生活实例

