在50.6克稀硫酸中放入一小片纯锌,锌作用完了,称得溶液的质量为53.6克,求放入了多少克锌
 lltlmm2022-10-04 11:39:542条回答
lltlmm2022-10-04 11:39:542条回答
在50.6克稀硫酸中放入一小片纯锌,锌作用完了,称得溶液的质量为53.6克,求放入了多少克锌
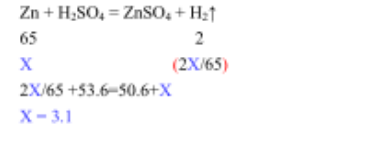
这个貌似是答案但是我不知道2x/65这一步怎么得出来的
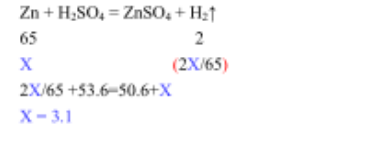
这个貌似是答案但是我不知道2x/65这一步怎么得出来的

已提交,审核后显示!提交回复
共2条回复
 青蛙土豆 共回答了17个问题
青蛙土豆 共回答了17个问题 |采纳率88.2%- 是利用反应式计算出来的假设锌片是X克
- 1年前
 神州英雄 共回答了1个问题
神州英雄 共回答了1个问题 |采纳率- 2x/65是65/x=2/m m=2x/65 m为氢气的质量
- 1年前
相关推荐
- 实验室有一瓶存放时间长的氢氧化钠,其中的一部分已经转化成了碳酸钠.现要用该药品配制10%的氢氧化钠溶液.取50.6克该药
实验室有一瓶存放时间长的氢氧化钠,其中的一部分已经转化成了碳酸钠.现要用该药品配制10%的氢氧化钠溶液.取50.6克该药品,溶于200毫升水中,然后慢慢地滴入17.1%的氢氧化钡溶液,当用去100克氢氧化钡溶液时,碳酸钠恰好完全反应,反应方程为 NaCO3+Ba(OH)2===BaCO3↓+2NaOH.求:
1、50.6克该药品中碳酸钠的质量
2、滤出沉淀后溶液中溶质质量和溶液质量
3、向所得溶液中再加入多少毫升水中才能配成10%的氢氧化钠溶液? yhk11091年前3
yhk11091年前3 -
 追梦客 共回答了15个问题
追梦客 共回答了15个问题 |采纳率86.7%设药品中碳酸钠的质量为x,生成的BaCO3的质量为y,生成的NaOH的质量为z.Na2CO3+Ba(OH)2 ===BaCO3↓+2NaOH
106 171 197 80
x 17.1% *100g y z
得:x =10.6g y=19.7g z=8g
(1)50.6克该药品中碳酸钠的质量为10.6g
(2) 溶液中溶质质量:50.6g-10.6g+8g=48g
溶液质量:50.6g+200g+100g-19.7g=330.9g(总量守恒思想:反应前总物质质量-沉淀质量=反应后溶液质量)
(3) (330.9g+m)*10%=48g
m=149.1g 即需要加水149.1毫升1年前查看全部
- 有一瓶敞口放置过的氢氧化钠固体,取出60克该固体,烘干后质量为50.6克,在于足量稀盐酸反应,生成气体4.4克,试回答:
有一瓶敞口放置过的氢氧化钠固体,取出60克该固体,烘干后质量为50.6克,在于足量稀盐酸反应,生成气体4.4克,试回答:固体中氢氧化钠的质量?反应后的溶液中含有氢氧化钠的多少克?
同学们啊,我已经知道了答案,第一个小问题为40克,第二个为70.2%,重点帮忙回答第二个,
回答的正确的,我会给积分的!
woammei 的我倒是还满意,可是,我不明白Mol是什么,哥哥们写一些初二就看得懂的好吗? zzmoyu1年前5
zzmoyu1年前5 -
 傻晓悦 共回答了20个问题
傻晓悦 共回答了20个问题 |采纳率95%1.敞口放置过的氢氧化钠固体发生变质:2NaOH+CO2==Na2CO3+H2O
滴加稀盐酸:Na2CO3+2HCl==2NaCl+H2O+CO2↑
生成的4.4克气体是二氧化碳气体(分子量44),摩尔量为:4.4/44=0.1mol
又Na2CO3∶CO2=1∶1,所以固体中含0.1molNa2CO3,质量为:0.1×106=10.6g
故固体中所含氢氧化钠为:50.6-10.6=40g
2.氢氧化钠和盐酸反应:NaOH+HCl==NaCl+H2O
所以反应后的溶液中含有应该是氯化钠,氢氧化钠已与盐酸反应完了,题目中求的应该是氯化钠含量吧
由 Na2CO3+2HCl==2NaCl+H2O+CO2↑知产生NaCl:0.2mol
NaOH+HCl==NaCl+H2O 产生NaCl:1 mol
氯化钠相对分子质量:58.5
所以反应后的溶液中含有氯化钠58.5×1.2=70.2g1年前查看全部
- 实验室有一瓶存放时间比较长的氢氧化钠,其中一部分已经转化为碳酸钠.现要用该药品配制10%的氢氧化钠溶液.取50.6克该药
实验室有一瓶存放时间比较长的氢氧化钠,其中一部分已经转化为碳酸钠.现要用该药品配制10%的氢氧化钠溶液.取50.6克该药品,溶于200mL水中,然后慢慢滴入17.1%的氢氧化钡溶液,当用去100克氢氧化钡溶液时,碳酸钠恰好完全反应求
1.50.6克该药品重碳酸钠的质量?
2.滤出沉淀后溶液中溶质的质量和溶液质量?
3.向所得溶液中再加入多少毫升水才能配成10%的氢氧化钠溶液? diaodiao281年前2
diaodiao281年前2 -
 xiaochengxinshi 共回答了12个问题
xiaochengxinshi 共回答了12个问题 |采纳率91.7%与碳酸钠反应的氢氧化钡质量为100*17.1%=17.1G
Na2CO3+Ba(OH)=2NaOH+BaCO3
106 171 80 197
X 17.1 Z Y
解得X=10.6 Y=19.7 Z=8
答1.该药品中碳酸钠的质量为10.6
2.滤出沉淀后溶液中溶质为氢氧化钠的质量为50.6-10.6+8=48G,溶液的质量为50.6+200+100-19.7=330.9
用48G的氢氧化钠配10%的溶液质量为48/10%=480G.已知溶液重为330.9所以需加入水为480-330.9=149.1G1年前查看全部
大家在问
- 1小明将10个数求平均数,再将11个数求平均数(10个数加上平均数)求平均数,再将12个数求平均数(10个数加上2个平均数
- 2照样子写词语 又舒服又暖和的窝 又()又()
- 3数学题目搜索有个百位数.把他的个位数和百位数换下就是原来的两倍,请问这个数是什么
- 4一本书小明第一天读了全书的4分之1第二天读的页数与第一天读的页数比是4:3剩下90
- 5给小蚂蚁做家 作文
- 6雪下着,下着,没有声音,雪下着,下着,一刻不停。照样子写句子
- 7某旅游景点为了吸引游客,推出的团体票收费标准如下:如果团体人数不超过25人,每张票价150元,如果超过25
- 8( )然不顾,( )然不动,括号里填什么
- 9形容人老心不老的成语
- 10I go to school on foot every day.同义句改写 I_____ _____ school e
- 11(x的三次方-2x的二次方+ax+2)除以(X的二次方-4X+1)=X+2 则a 等于
- 12关于电与磁的有关知识,正确的是( )
- 13lt is good for my healthy 这个lt is 必须是这样吗 难道不能把它改成they are
- 14谁有六年级上册的期中英语试卷?冀教版
- 15我今天玩的很开心的英语怎么写?
