向一饱和的硫酸铜溶液中加入A g无水硫酸铜,保持温度不变,充分搅拌后过滤,得到固体B g,将所得到的
 binglang6862022-10-04 11:39:541条回答
binglang6862022-10-04 11:39:541条回答则A、B、C三者之间的大小关系是:______.

已提交,审核后显示!提交回复
共1条回复
 smallpu 共回答了19个问题
smallpu 共回答了19个问题 |采纳率100%- 解题思路:饱和溶液是指在一定温度下,一定量的溶剂里不能再溶解某种溶质的溶液叫做这种溶质的饱和溶液;并结合物质的性质分析解答.
硫酸铜溶于水可与水结合生成五水合硫酸铜,结合了部分结晶水,所以质量增加,B大于A,由于溶液中水的质量减少,所以溶解的硫酸铜的质量减小,则除了原有的Ag析出,还有溶解在减少的水中的硫酸铜析出,故再加热后得到的Cg硫酸铜的质量大于Ag,则有B>C>A;
故答案为:B>C>A.点评:
本题考点: 盐的化学性质;饱和溶液和不饱和溶液.
考点点评: 了解饱和溶液的概念、硫酸铜溶于水生成五水合硫酸铜,五水合硫酸铜受热分解生成水和硫酸铜,并结合题意细心分析解答. - 1年前
相关推荐
- 气体的溶解度是指在一定温度和压强下,某气体在1体积水里达到饱和状态时所溶解的体积.为比较温度对气体溶解度的影响,查得10
气体的溶解度是指在一定温度和压强下,某气体在1体积水里达到饱和状态时所溶解的体积.为比较温度对气体溶解度的影响,查得101kPa时,M、N两气体在不同温度下的溶解度数值:SM.20℃=0.023L/LH2O,SN,40℃=0.023L/LH2O.则在101kPa、30℃时,M、N两种气体的溶解度大小关系正确的是( )
A. SM<SN
B. SM=SN
C. SM>SN
D. 无法比较 ee头等大事1年前1
ee头等大事1年前1 -
 谁都不为 共回答了18个问题
谁都不为 共回答了18个问题 |采纳率94.4%解题思路:弄清气体溶解度的影响因素:随温度的升高而减小,随压强的增大而增大.气体的溶解度随温度的升高而减小,因此,30℃时,M的溶解度比原来减小,N的溶解度比原来增大.故选A
点评:
本题考点: 气体溶解度的影响因素.
考点点评: 主要考查了气体的溶解度和温度之间的关系,培养学生分析问题、解决问题的能力.1年前查看全部
- 下列说法正确的是( )A. 铅蓄电池放电时铅电极发生还原反应B. 电解饱和食盐水在阳极得到氯气,阴极得到金属钠C. 给
下列说法正确的是( )
A. 铅蓄电池放电时铅电极发生还原反应
B. 电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C. 给铁钉镀铜可采用CuSO4作电镀液
D. 生铁浸泡在食盐水中发生析氢腐蚀 雪晶乐乐1年前1
雪晶乐乐1年前1 -
 persha 共回答了19个问题
persha 共回答了19个问题 |采纳率78.9%解题思路:A.铅蓄电池放电时铅电极为原电池的负极;
B.电解饱和食盐水得到氢气、氯气和氢氧化钠;
C.电镀时用含镀层金属的阳离子的盐做电解质溶液;
D.生铁浸泡在食盐水中发生吸氧腐蚀.A.铅蓄电池放电时铅电极为原电池的负极,发生氧化反应,正极发生还原反应,故A错误;
B.电解饱和食盐水得到氢气、氯气和氢氧化钠,阴极上得到氢气和氢氧化钠,故B错误;
C.电镀时用含镀层金属的阳离子的盐做电解质溶液,则给铁钉镀铜可采用CuSO4作电镀液,故C正确;
D.生铁浸泡在食盐水中发生吸氧腐蚀,在酸性溶液中发生析氢腐蚀,故D错误.
故选C.点评:
本题考点: 常见化学电源的种类及其工作原理;原电池和电解池的工作原理.
考点点评: 本题考查电化学知识,题目难度不大,注意原电池的工作原理、电镀以及金属的腐蚀及防护措施.1年前查看全部
- 为什么向硫酸钡沉淀中加入饱和碳酸钠溶液能转化成碳酸钡
 johnsonjohn_2k1年前4
johnsonjohn_2k1年前4 -
 我会让你幸福 共回答了14个问题
我会让你幸福 共回答了14个问题 |采纳率85.7%因为碳酸钡的溶解度小于硫酸钡 就是沉淀转化1年前查看全部
- (8分)一个重100g的洁净烧瓶中,加入两种饱和一元醛A和B的混合液2.55g,向混合液中加入足量的银氨溶液,并水浴加热
(8分)一个重100g的洁净烧瓶中,加入两种饱和一元醛A和B的混合液2.55g,向混合液中加入足量的银氨溶液,并水浴加热,经充分反应后,过滤、仔细洗涤、干燥,称得瓶和固体质量共110.8g。已知B比A的相对分子质量大14。求:
(1)写出A和B的结构简式;(2)求A和B的物质的量之比。 hz_cmin1年前1
hz_cmin1年前1 -
 xiatiandeyu 共回答了16个问题
xiatiandeyu 共回答了16个问题 |采纳率93.8%(1) CH 3 CHO CH 3 CH 2 CHO (2) 1:1
略1年前查看全部
- 工业上用电解饱和食盐水的方法制取氢氧化钠、氢气和氯气.当制取112m(S.T.P)氢气时制取氢氧化钠多少克?氯气多少立方
工业上用电解饱和食盐水的方法制取氢氧化钠、氢气和氯气.当制取112m(S.T.P)氢气时制取氢氧化钠多少克?氯气多少立方米?第二小题我做出来112m.答案上是56m.
 A200121061年前1
A200121061年前1 -
 shenzhenhyj 共回答了16个问题
shenzhenhyj 共回答了16个问题 |采纳率87.5%可以是用电荷守恒做 那样可以算出是 112m 所以是答案错了 相信你自己 我支持你1年前查看全部
- 向饱和BaSO4溶液中加水溶液度为什么不变?加水不是朝着溶解方向移动吗?
向饱和BaSO4溶液中加水溶液度为什么不变?加水不是朝着溶解方向移动吗?
是溶解度为什么不变 题目上打错了 TheEnd_xx1年前1
TheEnd_xx1年前1 -
 客家流云 共回答了18个问题
客家流云 共回答了18个问题 |采纳率83.3%不可能不变的 除非交代你了溶液中有BaSO4沉淀,加水的确是朝着溶解方向移动,但水多了,沉淀溶解的也多了,加多少水就多溶解多少BaSO4,此温度下Ksp是一定的,所以溶液浓度不变
溶解度就更好说了,溶解度指的是100g水溶解溶质的质量,只和温度有关1年前查看全部
- 饱和nacl溶液,滴入浓hcl,是否会因cl离子浓度增大而有晶体析出,为什么
 wannis1年前2
wannis1年前2 -
 srene 共回答了12个问题
srene 共回答了12个问题 |采纳率91.7%不一定,因为HCl可能浓度不够,即浓度小于NaCl中的Cl-的浓度,如果浓度够的话会有c(Na+)*c(Cl-)=Ksp为定值,Cl-浓度增大,显然平衡向沉淀方向移动,除去Cl2中的HCl就是通过饱和NaCl1年前查看全部
- 已知电解池总方程式1已知总方程式写阴阳极,需要知道电解质是酸性还是碱性吗?2为什么电解饱和食盐水我根据总方程式写不出阴极
已知电解池总方程式
1已知总方程式写阴阳极,需要知道电解质是酸性还是碱性吗?2为什么电解饱和食盐水我根据总方程式写不出阴极方程式,因为水拆不了.3冷却结晶和蒸发结晶怎么区分 csallen5001年前2
csallen5001年前2 -
 lcxcyj 共回答了16个问题
lcxcyj 共回答了16个问题 |采纳率87.5%1.高中阶段,我们这边是不要求电解质是酸性还是碱性对电极方程式的影响的,但是大学或者竞赛里就一定要求,或者题目中给出.
而且,知道了总方程式,一般都能根据反应物推出电解质的酸碱性的.
2.电解饱和食盐水:
2NaCl+2H2O==(电解)==2NaOH+Cl2+H2
离子方程式:2H2O+2H2+Cl- ====2OH-+ Cl2+H2
阳极被氧化:Cl- —— Cl2
配平:2Cl-====Cl2+2e-
阴极被还原:H2O——H2+OH-
配平:2H2O+2e-====H2+2OH-
3.冷却结晶一般是跟在加热浓缩之后,也就是“冷却热饱和溶液法”,结晶出来的一般是漂亮的晶体,而且是在溶液中就析出晶体的
蒸发结晶是加热至溶剂全部挥发,出来的一般是粉末,像高中、初中常见的提取粗盐实验中,在坩埚中把粗盐溶液蒸发完全.1年前查看全部
- 电石和饱和食盐水制乙炔能用启普发生器吗?
 chrisliu671年前2
chrisliu671年前2 -
 ywesngyuh0n0 共回答了24个问题
ywesngyuh0n0 共回答了24个问题 |采纳率75%不行
①电石是粉末状的,会从启普发生器中间的间隙中漏到食盐水中.启普发生器条件必须是块状固体,并且不溶于水
②产物Ca(OH)2是微溶物会沉淀出来,堵住固体的那个空间与盛溶液那个空间的连接的小缝隙,使得启普发生器用气压来控制反应的能力丧失1年前查看全部
- 某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列说法正确的是
某温度下,向一定质量的饱和石灰水中加入少量生石灰,当溶液恢复到原温度时,下列说法正确的是
A 溶液的碱性不变 B 溶质的溶解度先变大,后变小 C溶质的质量分数变大 D溶液中溶质质量不变 草原狼4561年前1
草原狼4561年前1 -
 今天改吃馒头 共回答了16个问题
今天改吃馒头 共回答了16个问题 |采纳率93.8%加入生石灰后,CaO+H2O=Ca(OH)2,消耗水,并产生Ca(OH)2
由于原溶液饱和,所以产生的Ca(OH)2并不能溶解.
并且由于消耗了水,Ca(OH)2还要析出一部分
A、正确.加入CaO前后,溶液都是饱和溶液,质量分数不变,碱性不变
B、错误.因为反应放热,温度先升高,后降低,所以Ca(OH)2溶解度先减小后增大
C、错误.质量分数不变,因为溶液恢复到原温度时,溶解度S不变.质量分数 = S/(S+100)也不变
D、错误.由于消耗了水,Ca(OH)2要析出一部分,溶质质量减小,溶剂质量也减小1年前查看全部
- 饱和石灰水石灰水和澄清石灰水有什么区别?饱和石灰水通入空气后会有什么变化
饱和石灰水石灰水和澄清石灰水有什么区别?饱和石灰水通入空气后会有什么变化
最主要的是空气通入饱和石灰水和通入一般石灰水有什么区别,会发生什么反应? 飞越时间1年前2
飞越时间1年前2 -
 转贴专业户 共回答了17个问题
转贴专业户 共回答了17个问题 |采纳率76.5%饱和的石灰石溶液是达到该温度溶解度的水溶夜,澄清的则是保持液体无浑浊的液体可用来检验CO21年前查看全部
- 饱和的NH4CL和水溶液,加热到100度时,NH4CL会分解吗?
 flywinging1年前1
flywinging1年前1 -
 83034414 共回答了20个问题
83034414 共回答了20个问题 |采纳率95%应为当NH4CL分解时NH3,HCL都极易溶于沸水 二者在水中反得NH4CL1年前查看全部
- 不规则的硫酸铜晶体放入饱和的硫酸铜溶液中是否会变成规则的晶体
不规则的硫酸铜晶体放入饱和的硫酸铜溶液中是否会变成规则的晶体
大概要多长时间?
大概要多长时间?较大的 俺的确良1年前1
俺的确良1年前1 -
 mayaren 共回答了23个问题
mayaren 共回答了23个问题 |采纳率91.3%会变成规则的晶体,但很小,8-12小时即可(一夜)
附:
制备晶体方法:
①选用纯净胆矾在洁净的烧杯里制成饱和溶液,制备时的温度可高出室温12~15℃
②取出上层清液倒在洁净的蒸发皿里(溶液浑浊不清则应过滤).当蒸发皿里溶液冷却时,可产生一些较大颗粒的晶体.在这些晶体里选出几何形状比较完整的备用.
③将其余的晶体连同饱和溶液一起倒入洁净的烧杯里,加热并不断搅袢,至晶体全部溶解,停止加热并静止,让其逐渐冷却.
④将挑选出的一颗晶体用细丝系住,悬挂在饱和溶液里,晶体在液面以下约2~3厘米处,静置不动,加盖防止灰尘进入,数天后可获得大晶体.
制备注意事项
①必须用纯净的晶体和蒸馏水配制溶液;
②容器要十分洁净;
③降温速度越慢越好;
④必须静置较长时间;
⑤盛溶液的烧杯必须加盖.
这样即可从硫酸铜溶液中得到大块的硫酸铜晶体1年前查看全部
- 5道化学题1.20°C时,在100g水中溶解11.1gK2SO4恰好达到饱和,此饱和溶液的密度为1.08g/cm³.将3
5道化学题
1.20°C时,在100g水中溶解11.1gK2SO4恰好达到饱和,此饱和溶液的密度为1.08g/cm³.将350mL此温度下的K2SO4饱和溶液用水稀释至500mL.计算稀释后溶液中K2SO4的物质的量的浓度.
2.将一定体积的密度为1.19g/cm³,质量分数为36.5%的浓盐酸稀释至50mL时,溶液中H+的物质的量浓度为1.02mol/L.计算所用浓盐酸的体积.
3.制取500g质量分数为14.6%的盐酸,需要标准状况下HCl气体的体积是多少?
4.在t°C时,ag某化合物饱和溶液的体积为bmL.将其蒸干后得到cg摩尔质量为dg/mol的不含结晶水的固体物质.计算t°C时此化合物的饱和溶液中溶质的物质的量的浓度.
5.将1.721gCaSO4·xH2O加热,使其失去全部结晶水,这时剩余固体物质的质量是1.361g.计算1mol此结晶水合物种所含结晶水的物质的量.
 七七yy1年前1
七七yy1年前1 -
 爱吾爱琴 共回答了18个问题
爱吾爱琴 共回答了18个问题 |采纳率100%1、稀释后溶液中K2SO4的物质的量的浓度
C={1.08*350*[11.1/(100+11.1)]/174}/0.5=0.434 mol/L
2、浓盐酸物质的量浓度=(1000*1.19*36.5%)/36.5=11.9 mol/L
所用浓盐酸的体积=1.02*50/11.9=26.8 mL
3、需要标准状况下HCl气体的体积=[(500*14.6)/36.5]*22.4=44.8 L
4、此化合物的饱和溶液中溶质的物质的量的浓度=1000c/db mol/L
5、x=[(1.721-1.361)/1.361]*(136/18)=21年前查看全部
- (2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴
(2007•番禺区一模)某化工厂常用电解纯净的饱和食盐水的方法来得到烧碱溶液,再经浓缩、蒸发等步骤制造固体烧碱.某化学兴趣小组要分析该化工厂仓库里的固体烧碱样品.
(1)小组成员猜测该样品中含有碳酸钠,支持这种猜测的依据是(用化学方方程式表示)______.小组成员选用了三种不同类别的试剂,进行实验,验证猜想,并得出结论,碳酸钠确实存在.请你将实验过程中涉及的化学方程式填在下表中.
(2)现已知样品中含有氯化钠、氢氧化钠、碳酸钠,设计一个实验方案,来证实一定含有氯化钠存在.化学方程式 试剂1 试剂2 试剂3 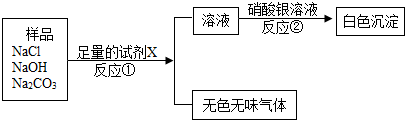
请写出试剂X的化学式______
请写出①反应的化学方程式______
请写出②反应的化学方程式______. 烟雨楼家族之烟灰1年前1
烟雨楼家族之烟灰1年前1 -
 钱之光 共回答了20个问题
钱之光 共回答了20个问题 |采纳率85%解题思路:(1)烧碱易潮解,潮解之后容易和空气中的二氧化碳反应,检验烧碱变质的方法就是根据碳酸钠的化学性质来选择合适的试剂来鉴别
(2)加入试剂A后生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,可以据此答题(1)烧碱露置于空气中时易于空气中的二氧化碳反应而变质,在验证烧碱是否变质实际上就是验证碳酸钠的存在,故可以据其性质来区分,要注意的是当用盐酸时要向把氢氧化钠反应掉,然后才会有气体产生,故本题的答案为:CO2+2NaOH=Na2CO3+H2O
化学方程式
试剂1 Na2CO3 +CaCl2═2NaCl+CaCO3↓
试剂2 Na2CO3+Ca(OH)2═2NaOH+CaCO3↓
试剂3
NaOH+HCl=NaCl+H2O
Na2CO3+2HCl=2NaCl+CO2↑+H2O (2)加入X生成了气体可知X为酸,但是考虑到后边的反应中加入了硝酸银,所以此时要排除氯离子和硫酸根离子的干扰,故应该选择稀硝酸,当加入稀硝酸时除了和碳酸钠反应,还要和氢氧化钠发生中和反应,在混合物中能和硝酸银生成白色沉淀的是氯化钠,
故本题答案为:HNO3 NaOH+HNO3=NaNO3+H2O; Na2CO3+2HNO3=2NaNO3+CO2↑+H2ONaCl+AgNO3=AgCl↓+NaNO3点评:
本题考点: 酸、碱、盐的鉴别;电解水实验.
考点点评: 解答本题要求学生熟练掌握酸、碱、盐的化学性质,并能根据物质之间能否反应及其反应的实验现象来得出结论,熟记化学方程式:CO2+2NaOH=Na2CO3+H2O;Na2CO3+Ca(OH)2═2NaOH+CaCO3↓; NaOH+HCl=NaCl+H2O.1年前查看全部
- 1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
2 20度时,200克溶液浓度为15%,若保持在T度,再溶解4克该溶质或蒸发25克水后都可以使其饱和,求该物质在T度的溶解度
3 把5.9克氯酸钾和二氧化锰的混合物加热,直到不再产生气体为止,得到残余固体3.98克,求氧气得到多少升,残余固体的祖成
4 现有10克含杂质5%的大理石跟100克盐酸恰好完全反映,求盐酸的浓度,生成物溶液的浓度
- - dzhdhz1年前2
dzhdhz1年前2 -
 心若无底洞 共回答了23个问题
心若无底洞 共回答了23个问题 |采纳率91.3%1 T度时某物质的溶液120g,若将该溶液蒸发掉20克水或再溶解5克溶质都可以使其达到饱和,求T度时溶解度
解析:设T度其溶解度为x有:120*x/100/(120-20)=(120*x/100+5)/(120+5) 解得x=16.7g
注意:其中120*x/100表示溶液120g中含有该物质的质量;120*x/100/(120-20)表示该物质蒸发掉20g水后饱和时的质量分数;(120*x/100+5)表示溶液120g再溶解5克溶质后溶质的总质量;(120*x/100+5)/(120+5)表示加5g溶质后溶液达饱和时的浓度.
2 20度时,200克溶液浓度为15%,若保持在T度,再溶解4克该溶质或蒸发25克水后都可以使其饱和,求该物质在T度的溶解度
解析:此题和上题类似,但不需要列方程,主要考查学生对溶解度和浓度的概念有没有弄清楚.
200克溶液浓度为15%则溶液中含有溶质的质量为:200*15%=30g,溶剂水的质量为200-30=170g,加4g溶质溶液饱和,则其溶解度为:(30+4)g/170g * 100=20g.
没弄懂以上两个概念不访再看看书.
3 把5.9克氯酸钾和二氧化锰的混合物加热,直到不再产生气体为止,得到残余固体3.98克,求氧气得到多少升,残余固体的祖成
解析:要知道发生的反应是:KClO3(加热和二氧化锰催化)=KCl+O2↑
有反应可知,反应物减少的质量是生成的氧气的质量5.9-3.98=1.92g锰催化,不参与反应,所以剩余固体应该为二氧化锰和氯化钾.知道了生成的氧气质量1.92查氧气的密度,就可以知道生成的氧气的体积了,我没有资料查,通过其他方法算的是1.344L
4 现有10克含杂质5%的大理石跟100克盐酸恰好完全反映,求盐酸的浓度,生成物溶液的浓度
大理石的主要成分是碳酸钙,其含杂质5%则10克大理石中碳酸钙的含量为10*95%=9.5g.
反应方程式:CaCO3+2HCL=CaCl2+H2O+CO2
100 73 111 44
知道了CaCO3的质量则反应中消耗的盐酸的质量为:9.5*73/100=6.94g,生成物氯化钙的质量为10.54g,生成的二氧化碳的质量为4.18g(以上数据的取舍原则采取分析化学中的四舍六入五成双的原则)所以盐酸的浓度为:6.94/100*%=6.94% 生成物氯化钙的浓度为:10.54/(100+9.5-4.18)*%=10%1年前查看全部
- 问个关于溶解度的初三化学题在一定温度下,物质X和Y具有相同溶解度,则在该温度下X、Y的饱和合溶液中含X、Y两种物质的质量
问个关于溶解度的初三化学题
在一定温度下,物质X和Y具有相同溶解度,则在该温度下X、Y的饱和合溶液中含X、Y两种物质的质量相等 这句话对吗?如果不对为什么?请举个例子~ aifza1年前2
aifza1年前2 -
 我想好了 共回答了22个问题
我想好了 共回答了22个问题 |采纳率86.4%不对.例如现有X饱和溶液100g,Y饱和溶液500g,两者含有的X、Y两种物质的质量显然不相等.
正确的描述:在一定温度下,物质X和Y具有相同溶解度,则在该温度下X、Y的饱和合溶液中含X、Y两种物质的质量分数相等1年前查看全部
- 在一定温度下,将少量生石灰放入一定的饱和石灰水中,搅拌并冷却、到原来的温度,下列说法中正确的是( )
在一定温度下,将少量生石灰放入一定的饱和石灰水中,搅拌并冷却、到原来的温度,下列说法中正确的是( )
A. 溶剂质量不变
B. 溶质质量增加
C. 溶液浓度不变
D. 溶解度增加 luohanmi1年前5
luohanmi1年前5 -
 回天剑客2004 共回答了20个问题
回天剑客2004 共回答了20个问题 |采纳率100%解题思路:根据温度不变饱和石灰水不能再继续溶解氢氧化钙的特点,判断对于此溶液的说法中正确的选项.A、生石灰遇水和水反应生成熟石灰,因此,加入生石灰后溶液中的水会减少;
B、由于溶液中水的减少,会有少量固体析出,所以,溶质的质量减少;
C、由于溶液温度不变,并且溶液仍为饱和溶液,所以,溶液的浓度(即溶质质量分数)不变;
D、固体物质的溶解度只受外界条件中温度的影响,而此题中溶液温度不变,所以溶解度也不变;
故选C点评:
本题考点: 饱和溶液和不饱和溶液;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 生石灰遇水生成的氢氧化钙因溶液已为饱和溶液,所以不能继续溶解,溶液中溶质质量不会增大.1年前查看全部
- 某饱和一元醛1.5g和足量的银氨溶液发生银镜反应时,生成21.6 g银,则该醛是
某饱和一元醛1.5g和足量的银氨溶液发生银镜反应时,生成21.6 g银,则该醛是
A.丙醛
B.丁醛
C.3-甲基丁醛
D.甲醛 gdaz1年前1
gdaz1年前1 -
 huwanlin 共回答了14个问题
huwanlin 共回答了14个问题 |采纳率92.9%答案D
由RCHO~2Ag可算出此醛的式量为15,各选项均不符合,所以为甲醛,它1mol可以得到4mol银,HCHO~4Ag1年前查看全部
- 20摄氏度,饱和石灰水(甲溶液)加入适量氧化钙粉末,充分反应.
20摄氏度,饱和石灰水(甲溶液)加入适量氧化钙粉末,充分反应.
溶液未恢复到20摄氏度时,为什么溶质质量分数比甲溶液小呢, chenoon1年前1
chenoon1年前1 -
 zhangzhi 共回答了15个问题
zhangzhi 共回答了15个问题 |采纳率80%因为氢氧化钙的溶解度的变化规律是“随温度的升高而下降”
但加入氧化钙反应后消耗了水(与其反应)而且增加了溶质
显然是饱和的,又因为温度高于20度,溶解度随温度的升高而下降
所以溶质质量分数比甲溶液小1年前查看全部
- 碘离子达到饱和结构为何还会有强还原性
碘离子达到饱和结构为何还会有强还原性
碘离子最外层电子不是已经达到8个了吗,那么为什么还会有强还原性呢,强还原性不就是***很容易失电子吗,
并且氯离子处于最低价负一价时,为什么不具备有强还原性呢,那什么情况下,氯离子会反应变成氯气呢 ypy_01年前1
ypy_01年前1 -
 ynynyn999 共回答了21个问题
ynynyn999 共回答了21个问题 |采纳率95.2%是这样的:Cl和I同位于第七主族,但是Cl的电子层数少,I的电子层数多,可想而知,电子层数多了,原子核对外层电子的吸引能力就下降了,所以易失去电子,所以I-最外层电子已经达到8个了,还会有强还原性;而Cl-电子层数少,核...1年前查看全部
- 室温下,将盛有接近饱和的硝酸钾溶液的小烧杯放在盛水的大烧杯中,若使硝酸钾溶液变为饱和溶液,可想大烧杯中加入的固体物质是(
室温下,将盛有接近饱和的硝酸钾溶液的小烧杯放在盛水的大烧杯中,若使硝酸钾溶液变为饱和溶液,可想大烧杯中加入的固体物质是( )
A.硝酸钾 B 氯化钠 C,硝酸铵 D.氢氧化钠
这道题的道理应该是,硝酸钾溶液溶解度减小变为饱和溶液,即温度减小,需要一个吸热的物体,我的疑问是A 和C都是吸热的物体,应该都选,为什么正确答案选C? dcboysky1年前2
dcboysky1年前2 -
 柳叶刀等号 共回答了20个问题
柳叶刀等号 共回答了20个问题 |采纳率90%你的思路是对的,但是吸热的只有硝酸铵,一般铵盐溶于水都吸热,而硝酸钾溶解并没有明显的吸热或放热,氯化钠也没有明显吸热或放热,氢氧化钠放热1年前查看全部
- 在其他条件不变的情况下,向一定量的饱和NaCl溶液中加入少量的KCl固体,则溶液的质量会怎样?
 shypool1年前1
shypool1年前1 -
 butterfly路过 共回答了18个问题
butterfly路过 共回答了18个问题 |采纳率100%查看两种盐的溶解度,如果KCl的溶解度比NaCl大,则溶液质量增加,相反则减小1年前查看全部
- 将饱和氯化铁溶液分别加入到下列液体中,能形成胶体的是( )
将饱和氯化铁溶液分别加入到下列液体中,能形成胶体的是( )
A. 冷水
B. 沸水
C. 氢氧化钠溶液
D. 饱和食盐水 ruoruo191年前2
ruoruo191年前2 -
 爱着猪的猫 共回答了20个问题
爱着猪的猫 共回答了20个问题 |采纳率90%解题思路:根据氢氧化铁胶体的制备方法:将饱和氯化铁溶液加入沸水中.A、因FeCl3溶液在冷水中水解程度较小,不能形成胶体,故A错误,B、因FeCl3溶液与沸水发生水解反应,水电离出来的极少量OH-离子与Fe3+结合形成氢氧化铁胶体,故B正确;C、因FeCl3溶液与NaOH溶液生成红褐色的Fe(OH)3...
点评:
本题考点: 胶体的重要性质.
考点点评: 本题主要考查了氢氧化铁胶体的制备方法,比较简单.1年前查看全部
- 30℃时,将30克A物质投入50克水中充分搅拌恰好饱和,求30℃时A物质的溶解度及溶液的溶质质量分数
 linderxlj1年前1
linderxlj1年前1 -
 pgly 共回答了19个问题
pgly 共回答了19个问题 |采纳率100%溶解度指100克水中能够溶解的溶质的最大质量,所以溶解度为60克.
质量分数=溶质质量/溶液质量=30/(30+50)=37.5%1年前查看全部
- 除去混在CO2中的少量HCl气体,不用饱和Na2CO2溶液的原因是?
 清池塘主1年前3
清池塘主1年前3 -
 mchzh 共回答了11个问题
mchzh 共回答了11个问题 |采纳率90.9%除杂质的基本要求是需要得到的物质不反应,HCl可以和Na2CO3生成CO2,但CO2也和Na2CO2反应,所以用它的酸式盐.1年前查看全部
- 在饱和的H2S水溶液中硫离子浓度为什么等于ka2?
 曾为县吏民知否1年前1
曾为县吏民知否1年前1 -
 小强特攻队 共回答了21个问题
小强特攻队 共回答了21个问题 |采纳率100%既然是饱和的溶液了,就不存在浓度的变化了,浓度一定了,在外间条件不变的条件下,那么他对应的PH就一定了,电离的平衡就一定了,而且就是Ka2
希望读你能有帮助!1年前查看全部
- 加热溶解醋酸钠直到饱和,然后取溶液放冰箱里静置冷却到室温下.拿出来后向里面再丢一点醋酸钠,你说会发生什么现象?
 amyy7001年前3
amyy7001年前3 -
 vlcky 共回答了18个问题
vlcky 共回答了18个问题 |采纳率88.9%醋酸钠的溶解度是随温度升高而增加的.所以你从冰箱里拿出来的时侯有部分晶体析出了,但是你再扔进去它也是会溶解的,因为溶解析出是个动态平衡状态.饱和了不是就没有溶解发生了,只是析出的多于溶解的.
意思是溶液中溶解和析出是时时刻刻在发生.1年前查看全部
- 制取氢氧化铁时为什么必须使用饱和氯化铁溶液而不能用稀氯化铁溶液?
 guoliang88581年前3
guoliang88581年前3 -
 深水绯蓝 共回答了17个问题
深水绯蓝 共回答了17个问题 |采纳率88.2%制氢氧化铁胶体利用的是氯化铁水解反应.
氯化铁水解反应:
FeCl3+3H2O=Fe(OH)3+3HCl,这是一个可逆反应
选用饱和溶液的目的是增加铁离子的浓度,有利于平衡向右移动
这样更有利于氢氧化铁胶体的制备1年前查看全部
- 电解饱和食盐水50mL,某时刻测得H2体积为16.8mL(标准状况),此时溶液pH约为____.(lg2=0.3,lg3
电解饱和食盐水50mL,某时刻测得H2体积为16.8mL(标准状况),此时溶液pH约为____.(lg2=0.3,lg3=0.5,lg5=0.7)
麻烦写出详细过程及原因, 瘦月断肠人1年前2
瘦月断肠人1年前2 -
 Hicc_p 共回答了24个问题
Hicc_p 共回答了24个问题 |采纳率91.7%2H20+2NaCl=2NaOH+H2↑+Cl↑
2mol 22.4L
Xmol 16.8ml
X=1.5×10*-3mol
水的消耗应该是忽略不记的吧·要的话你再加上吧·
C=n/V=1.5×10*-3mol÷0.05L=0.03mol/L
pOH=-lg0.03=2-lg3=1.5
pH=14-pOH=12.51年前查看全部
- 一道有关饱和食盐水的题目在饱和食盐水中存在的离子有 通电时向阴极的离子是用pt电极电解氯化铜,氯化钠的混合溶液,阴极和阳
一道有关饱和食盐水的题目
在饱和食盐水中存在的离子有 通电时向阴极的离子是
用pt电极电解氯化铜,氯化钠的混合溶液,阴极和阳极上分别析出的物质是()
a.氢气和氯气 b,氢气和氧气c.铜和氯气 d.铜和氧气 xueliqin1年前2
xueliqin1年前2 -
 d3221837 共回答了18个问题
d3221837 共回答了18个问题 |采纳率100%在饱和食盐水中存在的离子有(H+,OH-,Na+,Cl-)( 电离方程式为2NaCl+2H2O===电解====2NaOH+H2+Cl2 )通电时向阴极(得电子)的离子是H+
用pt电极电解氯化铜,氯化钠的混合溶液,阴极和阳极上分别析出的物质是
当电解质中含氯化铜,氯化钠两种物质时析出的物质是c.铜(阴)和氯气(阳)
又当电解完氯化铜(由阳离子析出顺序可知氯化铜首先被电离完),剩氯化钠时析出的物质是a.氢气(阴)和氯气(阳),当氯化钠被电解完后电解质中剩下氢氧化钠和水,电解的实质就是电解水,此时析出物为b,氢气(阴)和氧气(阳)
1.要注意水的电离中H+,OH-对电解的影响
2.要熟记电离中阳离子析出的先后顺序Ag+>Hg2+>Cu2+>H+>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+1年前查看全部
- 葡萄糖穿越细胞膜进入红细胞的运输速度存在一个饱和值,该值的大小取决于( )
葡萄糖穿越细胞膜进入红细胞的运输速度存在一个饱和值,该值的大小取决于( )
A. 细胞内的氧浓度
B. 细胞膜外的糖蛋白数量
C. 细胞膜上相应载体的数量
D. 细胞内外葡萄糖浓度差值 79深谷悠蓝1年前1
79深谷悠蓝1年前1 -
 lucky33 共回答了18个问题
lucky33 共回答了18个问题 |采纳率94.4%解题思路:葡萄糖穿越细胞膜进入红细胞属于协助扩散,特点是高浓度运输到低浓度,需要载体,不需要能量,则相关因素是载体和浓度差.葡萄糖穿越细胞膜进入红细胞的运输方式是协助扩散,运输速度与细胞膜上载体的数量和浓度差有关,而运输速度的饱和值与细胞膜上相应载体的数量有关.
故选:C.点评:
本题考点: 物质跨膜运输的方式及其异同.
考点点评: 本题考查协助扩散的条件和影响因素等相关知识,旨在考查学生的识记和理解能力.1年前查看全部
- 为什么滴加浓盐酸可鉴别饱和碳酸氢钠,碳酸钾,亚硫酸钠,氯化钠,硝酸钾五种无色溶液
 xiangxcy1年前1
xiangxcy1年前1 -
 2068963 共回答了26个问题
2068963 共回答了26个问题 |采纳率88.5%解析:
浓盐酸滴加饱和碳酸氢钠,反应式:NaHCO3+HCl = NaCl + CO2(气体) + H2O 现象为:有无色无味的气体生成.
浓盐酸滴加饱和碳酸钾溶液中,反应式:K2CO3 + HCl = KCl + KHCO3 ,KHCO3+HCl=KCl + CO2(气体) + H2O 现象为:先没有气体,后产生无色无味的气体.
浓盐酸滴加饱和亚硫酸钠溶液中,反应式:Na2SO3 + HCl = NaCl + NaHSO3 ,NaHSO3+HCl=NaCl + SO2(气体) + H2O 现象为:先没有气体,后产生无色有刺激性气味的气体.
浓盐酸滴加饱和NaCl溶液中,同离子效应,NaCl = Na+ + Cl- HCl=Cl- +H+ 饱和NaCl中C(Cl-)浓度增大,使饱和NaCl溶液有晶体析出.现象为:有晶体析出.
浓盐酸滴加饱和硝酸钾溶液中,只吸收HCl.无明显现象.1年前查看全部
- 乙酸乙酯在饱和碳酸钠溶液中的溶解度
 秋水亭1年前1
秋水亭1年前1 -
 delphi506 共回答了17个问题
delphi506 共回答了17个问题 |采纳率82.4%乙酸乙酯在水中电离出乙酸和乙醇.乙酸自身存在电离平衡,产生一定量的氢离子和乙酸根离子.那么也就相当于乙酸乙酯和水最终产生了氢离子.
在饱和碳酸钠溶液中,由于碳酸钠的水解,产生大量OH-.其量的大小远大于乙酸乙酯和水产生的H+的量.因为酸碱中和,所以对于醋酸的电离,其H+不停被消耗,平衡右移,醋酸不断生成再消耗,导致乙酸乙酯的电离也不断进行.最终,溶解在水中的乙酸乙酯经过上述过程,剩余量已经很少了,即低.
因为溶解度低,那么溶液中乙酸乙酯的量很少.又因为乙酸乙酯的密度比水小,所以会浮在水面上形成"油层".于是水溶液与油层(乙酸乙酯)便有很明显的界限,几乎不会互溶,便于分层.因为以上平衡进行得很缓慢,所以是可以看到明显分层的.但时间一长,油层,即乙酸乙酯逐渐消耗,便看不到5层,只看到水层了.
乙酸乙酯在水中溶解度不大,且溶解很缓慢,其速率取决于水溶液的酸碱性.PH越大,溶解越快.在纯水中,速率还是很慢的.
另外,值得注意的是,这里的溶解不同于像食盐等物质.乙酸乙酯溶解后,就很难重新收集,一方面是挥发性等,另一方面,乙酸乙酯在溶解中由于存在水解与电离平衡,使得想恢复液态的乙酸乙酯很难做到.1年前查看全部
- 区分蒸馏水和饱和食盐水为什么不能用光学显微镜来区分
 黄桃蛋塔1年前4
黄桃蛋塔1年前4 -
 winmeagain 共回答了12个问题
winmeagain 共回答了12个问题 |采纳率75%饱和食盐水中的NaCL是已离子形式存在的,光学显微镜不能看到离子形式的东西.
所以在光学显微镜下,蒸馏水和饱和食盐水没有区别1年前查看全部
- 常温下饱和碘化铅溶液和饱和氯化氨溶液的浓度各是多少?
 lrongx1年前1
lrongx1年前1 -
 dd公贼 共回答了14个问题
dd公贼 共回答了14个问题 |采纳率92.9%室温时,碘化铅的容度积(Ksp)为1.7×10的负9次方mol/L负3次,溶液浓度1.19×10^(-3)mol/L.
氯化铵在水中溶解度列表:
0℃:29.4g
10℃:33.3g
20℃:37.2g
30℃:41.4g
40℃:45.8g
50℃:50.4g
60℃:55.2g
70℃:60.2g
80℃:65.6g
90℃:71.3g
100℃:77.3g
常温按20℃,溶解度s=37.2g,饱和溶液中氯化铵的质量分数为27.1%,没有密度不好计算物质的量浓度.1年前查看全部
- 如题,在水溶液中溶解磷酸一铵,达到饱和后,还能再溶进磷酸二铵去吗?
如题,在水溶液中溶解磷酸一铵,达到饱和后,还能再溶进磷酸二铵去吗?
如果还能溶解进磷酸二铵,那还能溶解多少而不会析出? 莎柠1年前1
莎柠1年前1 -
 超级火炮 共回答了23个问题
超级火炮 共回答了23个问题 |采纳率95.7%能溶进磷酸二铵去.理论上讲,任何一种物质达到溶解平衡的时候,都会有一个对应的Ksp.当磷酸一铵溶解达到饱和的时候,根据这个定值Ksp可以算出溶液中的铵根和磷酸二氢根的浓度.磷酸二氢根会电离生成磷酸一氢根,根据平衡常数和质子守恒可以求算出此时磷酸一氢根的浓度.理论上磷酸二铵也存在对应的K sp2,由于电离是微弱的,饱和的磷酸一铵中磷酸一氢根的很低,致使磷酸二铵的浓度积达不到Ksp2.因而会继续溶解磷酸二铵.当然也可以这样理解,当磷酸一铵达到饱和的时候,此时溶液中不会有磷酸二铵沉淀,因而会继续溶解磷酸二铵直至有磷酸二氨沉淀析出.但是,至于具体还能溶解多少的磷酸二铵,只要知道两个Ks的值和磷酸二氢根的电离平衡常数以及铵根的水解平衡常数即可求出.但是在大学无机课本上后两个平衡常数能够查到,但是前两个Ksp却无法找到.因而无法计算出能够继续溶解多少的磷酸二铵.你也可以通过热力学从理论上计算出两个Ksp的值,但是我认为这样做意义不大.首先,理论计算出两个Ksp过于复杂.就算求出来了,之后的计算涉及多部平衡,求解过于繁琐.因而我认为只需知道能继续溶解即可.至于能溶解多少也没有太大的用途1年前查看全部
- 将1摩尔每升饱和的FeCl3溶液中滴入沸水时,液体变为什么色,得到什么,反应方程式为
 huanfeiyansh1年前1
huanfeiyansh1年前1 -
 bjbb7 共回答了18个问题
bjbb7 共回答了18个问题 |采纳率77.8%液体变成红褐色,
反应方程式为 FeCl3+3H2O 可逆符号 Fe(OH)3(胶体) + 3HCL
这是制Fe(OH)3胶体的实验1年前查看全部
- 一道八上的科学提,求答▁▁是溶解能力的定量表示,▁▁是溶液组成的定量表示.在一定温度下同种溶液饱和的一定比不饱和的质量分
一道八上的科学提,求答
▁▁是溶解能力的定量表示,▁▁是溶液组成的定量表示.在一定温度下同种溶液饱和的一定比不饱和的质量分数要▁▁. 今天我发烧1年前1
今天我发烧1年前1 -
 wang5741571 共回答了13个问题
wang5741571 共回答了13个问题 |采纳率100%溶解度
浓度
大1年前查看全部
- 下列实验目的可以达到的是:1、浓硫酸与溴化钠共热制取溴化氢2、饱和碳酸钠溶液出去二氧化碳的氯化氢含大量Al3+的溶液中:
下列实验目的可以达到的是:
1、浓硫酸与溴化钠共热制取溴化氢
2、饱和碳酸钠溶液出去二氧化碳的氯化氢
含大量Al3+的溶液中:硝酸根、钠离子、氯离子、次酸根离子为什么不能大量共存?
下列各组有机物只用一种试剂无法鉴别的是:
A、乙醇、甲苯、硝基苯
B、苯、苯酚、己烯
C、苯、甲苯、环己烷
D、甲酸、乙醛、乙酸
这几个问题,希望能一个个细的解答,很细很细~ ╃浪漫已nn╃1年前1
╃浪漫已nn╃1年前1 -
 泰兰德 共回答了21个问题
泰兰德 共回答了21个问题 |采纳率90.5%1、浓硫酸与溴化钠共热制取溴化氢
溴会被氧化成单质.
如果是稀硫酸,这个反应可以看作是一个可逆反应,根据 勒夏特列原理,生成物中溴化氢因为遇热而溢出,反应向正向移动.
2、饱和碳酸钠溶液除去二氧化碳中氯化氢
二氧化碳能与碳酸钠反应生成碳酸氢钠.
4.A用水,将水慢慢倒入烧杯中,乙醇互溶,甲苯会在上层,硝基苯在下层,(有界面,可以根据体积来判断)
B苯和溴水发生萃取,分层,上层为红棕色苯层,苯酚和浓溴水反应生成白色不溶于水的三溴苯酚沉淀,己烯和溴水反应,分层后退色(加成)
C Cu(OH)2
甲酸,Cu(OH)2溶解,得到蓝色甲酸铜溶液,加热煮沸后,还能产生红色沉淀Cu2O,即甲酸中存在醛基,可以被Cu(OH)2氧化.
乙酸,Cu(OH)2溶解,得到蓝色的乙酸铜溶液,但是加热煮沸,没有其它变化
乙醛,Cu(OH)2不能溶解,但是加热煮沸后,出现红色沉淀Cu2O1年前查看全部
- 几道关于科学的选择题,1、小明用热水配制了大半杯的饱和硝酸钾水溶液,溶液的温度是70摄氏度,一个密度均匀的实心小球恰能悬
几道关于科学的选择题,
1、小明用热水配制了大半杯的饱和硝酸钾水溶液,溶液的温度是70摄氏度,一个密度均匀的实心小球恰能悬浮在溶液中.在室温下放置一段时间后,小球将
a、上浮 b、下沉
c、悬浮 d、无法确定
2、有四个500毫升的瓶子,分别装满海水、纯水、酒精和汽油.其中装的质量最多的是.(海水密度大于纯水密度大于酒精密度大于汽油密度)
a、海水 b、纯水
c、酒精 d、汽油
3、两条长度相等、横截面积不等的同种材料制成的电阻丝,串联在电路中,则粗电阻丝
a、电流强度较大 b、电流强度较小
c、电压较大 d、电压较小 风中曾经的承诺1年前1
风中曾经的承诺1年前1 -
 ethanhua 共回答了21个问题
ethanhua 共回答了21个问题 |采纳率85.7%第一题选B
因为当温度降低,硝酸钾溶解度变小,溶液密度变小,所以浮力小于重力,小球下沉
第二题选A
M=V×P 质量=体积×密度
第三题选D
因为是串联所以电流一样大,电阻越粗,其阻值越小,所以粗电阻串联分压的少1年前查看全部
- 20℃时,有二杯饱和的A溶液:甲杯盛100g,乙杯盛150g,在下列条件下,两杯溶液中析出晶体质量相同的是( )
20℃时,有二杯饱和的A溶液:甲杯盛100g,乙杯盛150g,在下列条件下,两杯溶液中析出晶体质量相同的是( )
A. 两杯溶液都降温至10℃
B. 同温下,甲杯蒸发掉10g水,乙杯蒸发掉60g水
C. 甲杯加25gA溶液,乙杯减少25gA溶液
D. 同温下,两杯都蒸发掉30g水 xbl20021年前1
xbl20021年前1 -
 明明强人一个 共回答了23个问题
明明强人一个 共回答了23个问题 |采纳率91.3%解题思路:A、根据降温后析出晶体的影响因素考虑;B、根据饱和溶液蒸发水,析出晶体的质量的影响因素考虑;C、根据加入溶液和减少溶液后溶液的变化情况考虑;D、根据饱和溶液蒸发水,析出晶体的质量的影响因素考虑.A、饱和溶液降温后析出晶体,与降温后的溶解度有关,还与原来溶液中的溶剂和溶解的溶质的多少有关,由于原来溶液的总质量不同,溶液中含有的溶质和溶剂各不相同,所以降温后析出的晶体的质量也不同,故A错;
B、饱和溶液蒸发溶剂析出晶体的原因是:被蒸发的水中,原来溶解的溶质不能继续被溶解,就以晶体的形式析出,所以析出晶体的质量与蒸发的水有关,与原来溶液的质量无关,因为甲杯蒸发掉10g水,乙杯蒸发掉60g水,蒸发水的质量不同,所以析出晶体的质量也不同,故B错;
C、甲杯加25gA溶液,因为加入的溶液和原来的溶液性质相同,溶液不会析出晶体,乙杯减少25gA溶液,也不会析出晶体,因为溶液是均一的,故C错;
D、饱和溶液蒸发溶剂析出晶体的原因是:被蒸发的水中,原来溶解的溶质不能继续被溶解,就以晶体的形式析出,所以析出晶体的质量与蒸发的水有关,与原来溶液的质量无关,因为两杯都蒸发掉30g水,所以析出晶体质量相同.
故选D.点评:
本题考点: 晶体和结晶的概念与现象.
考点点评: 解答本题关键是要知道饱和溶液蒸发溶剂,析出晶体的质量与原溶液质量无关,只与蒸发水的质量大小有关.1年前查看全部
- 乙醇乙酸和笨能用饱和Na2CO3溶液鉴别么 解析下
 村歌_悠扬1年前4
村歌_悠扬1年前4 -
 十年修为 共回答了12个问题
十年修为 共回答了12个问题 |采纳率100%乙醇、乙酸和苯能用饱和Na2CO3溶液来鉴别
三者现象各不相同
1、乙酸可以和饱和Na2CO3反应
有气泡生成
2、乙醇和饱和Na2CO3不反应
但是乙醇易溶于水
无明显现象
3、苯也不和饱和Na2CO3反应
但是苯不溶于水
而且密度比水小
漂浮在液面上
满意请采纳
谢谢1年前查看全部
- 用三种不同的方法鉴别蒸馏水和饱和食盐水.例:操作方法 取少量液体蒸干 结论 能留下固体颗粒的是饱和食盐
 将mm香烟1年前1
将mm香烟1年前1 -
 xinwen0412 共回答了17个问题
xinwen0412 共回答了17个问题 |采纳率100%1.滴加AgNo3,出现沉淀的是饱和盐溶液.2.降低温度到10摄氏度,出现固体的是饱和盐溶液.3.加盐搅拌,若能溶解则是水,不能则是饱和盐溶液.1年前查看全部
- 某温度下.A克溶质溶解在A克水中恰好饱和.此溶质在该温度下溶解度是多少
 ok4l1年前5
ok4l1年前5 -
 gzhzh987 共回答了18个问题
gzhzh987 共回答了18个问题 |采纳率88.9%溶解度是100克水中溶解的溶质的质量,既然A克溶质溶解在A克水中恰好饱和,那么100克水中最多能溶解100克溶质,即溶解度为100克1年前查看全部
- 一定温度下,取某物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半.给另一份溶液里加入原溶质的
一定温度下,取某物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半.给另一份溶液里加入原溶质的晶体(该溶质的晶体不含结晶水),当达到饱和时,所加晶体的质量恰好是此份溶液质量的1/8.求此温度下的物质的溶解度.
我们没有学过质量分数,可以使用别的方法吗?
比如用m质/m剂=s/100的解法 jeansmine1年前1
jeansmine1年前1 -
 紫夜V枫叶 共回答了14个问题
紫夜V枫叶 共回答了14个问题 |采纳率92.9%第一份溶液的操作可以理解成把纯水部分都蒸干了,剩下了饱和溶液.这样可知纯水部分质量为M/4.第二部分溶液的操作可以理解成向纯水里加溶质达到饱和.这样可知纯水部分里加质量为M/16的溶质即可饱和.
由此可以算出,饱和时水和溶质的比例为(M/4):(M/16) = 4:1.按照溶解度的定义可以算出溶解度是25g.1年前查看全部
- 关于溶解度的小问题(化学)`已知NaCl在60度时的溶解度是37.1g,现电解60度的精致饱和食盐水1371g,答案中有
关于溶解度的小问题(化学)`
已知NaCl在60度时的溶解度是37.1g,现电解60度的精致饱和食盐水1371g,
答案中有写到 60度饱和食盐水1371g,含有371克NaCl
请问为什么? yuhan37771年前1
yuhan37771年前1 -
 烟雾在消散 共回答了22个问题
烟雾在消散 共回答了22个问题 |采纳率68.2%溶解度的定义:100g溶剂能溶解的溶质的质量.在这里,溶剂是水,溶质是NaCl,故而每100g水能溶解37.1gNaCl,从而1000g水能溶解371gNaCl.1年前查看全部
- 实验探究是学习化学的重要方法.某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,
实验探究是学习化学的重要方法.某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,
某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,反应后将浑浊的液体过滤,得到无色澄清的滤液,为了确定滤液的成分,进行下列的实验探究.
(1)[提出问题] 探究滤液中(除氢氧化钠和水外)是否还有其他物质.
(2)[猜想]①王晓认为滤液中可能含有氢氧化钙;
②李娜认为滤液中可能含有________(填物质的名称,下同).
(3)[设计方案并实验]为了验证王晓的猜想,应该选用的试剂是______.为了验证李娜的猜想,应选用的试剂是______,可观察到的现象是________________,该反应的化学方程式为______________________ zdz0121年前1
zdz0121年前1 -
 406812597 共回答了10个问题
406812597 共回答了10个问题 |采纳率100%①王晓认为滤液中可能含有氢氧化钙;
②李娜认为滤液中可能含有__碳酸钠__(填物质的名称,下同).问题补充:
(3)[设计方案并实验]为了验证王晓的猜想,应该选用的试剂是__碳酸钠溶液_.为了验证李娜的猜想,应选用的试剂是_氯化钙溶液_,可观察到的现象是__有白色沉淀生成____,该反应的化学方程式为___CaCl2+Na2CO3==CaCO3↓+2NaCl___1年前查看全部
- ①饱和一元醇的通式②饱和二元醇的通式③饱和三元醇的通式④芳香一元醇的通式⑤一定量的乙醇在氧气不足的情况下燃烧,的CO,C
①饱和一元醇的通式
②饱和二元醇的通式
③饱和三元醇的通式
④芳香一元醇的通式
⑤一定量的乙醇在氧气不足的情况下燃烧,的CO,CO2和水的总质量为27.6g,若水的质量为10.8g,求co的质量
回答前四个就给分 黄瓜大1年前1
黄瓜大1年前1 -
 快哉风神 共回答了18个问题
快哉风神 共回答了18个问题 |采纳率88.9%CnH2n+2O
CnH2n+2O2(n>1)
CnH2n+2O3(n>2)
CnH2n-6O(n>6)1年前查看全部
大家在问
- 1”耳朵里有不可琢磨的声响,极远的又是极近的,极洪大的又是极细切的.”把这句话中的”又是”改为”还是”,行不行?为什么?说
- 2应用题.A.B.C.D.E.F.G七盏灯各自装有一个拉线开关.开始B.D.F是亮着的.小华从A到G依次拉七盏灯的开关,一
- 3The little cat in the box was ill.划线部分是in the box(对划线部分提问)
- 4有一列单项式 -a,2a的二次方,-3a的三次方,4a的四次方.(1)写出第2009项和第2010项;
- 5小红班的人数比30多,比60少.可以分成6个小组,也可以分成8个小组,正好分完.你知道小红所在的班级有多少人吗?
- 6“声一无听,
- 7如图5所示,有垂直纸面向外的匀强磁场,磁感应强度为B。在匀强磁场中做匀速圆周运动的一个电子,动量为P,电量为e,在A、C
- 8儒家学派的代表人物
- 9如图,一次函数y=ax+b的图像与x轴、y轴交于A、B两点,与反比例函数y=k/x的图像相交于C、D两点作y轴、x轴的垂
- 10感人的故事200字求求你们快点短点
- 11英语 (18 22:19:13)
- 12用2、6、0、8四个数字可以组成6个不同的四位数.______.(判断对错)
- 13一个长方形的棱长和是108,长和宽的比是2:1,宽与高的比是2:3.长宽高个是多少分米?
- 14(2011•南安市质检)如图是a、b、c三种物质的溶解度曲线,下列说法中正确的是( )
- 15一个长方体的宽和高都是五厘米把它从长的中点截成两个相同的小长方体其中一个小长方体的表面积比原来大长方体的表面积减少了12
