(2012•天河区一模)关于电磁波下列说法正确的是( )
 单眼皮的巨蟹2022-10-04 11:39:541条回答
单眼皮的巨蟹2022-10-04 11:39:541条回答A.电磁波和声波一样不能在真空中传播
B.根据公式c=λf可以推断,频率越高的电磁波,波长越短
C.光不是电磁波
D.电磁波的传播速度为340m/s

已提交,审核后显示!提交回复
共1条回复
 魔蟹鑫磊 共回答了21个问题
魔蟹鑫磊 共回答了21个问题 |采纳率81%- 解题思路:(1)电磁波的传播不需要介质,可以在真空中传播;
(2)根据公式c=λf分析电磁波的波长和频率之间的关系;
(3)光也是一种电磁波;
(4)电磁波的传播速度为3×108m/s.A、电磁波和声波不一样,电磁波可以在真空中传播,故A错误;
B、电磁波的传播速度是一定值,根据公式c=λf可以推断,频率越高的电磁波,波长越短,正确;
C、光也是一种电磁波,故C错误;
D、电磁波的传播速度为3×108m/s,故D错误.
故选B.点评:
本题考点: 波速、波长和频率的关系;电磁波的传播.
考点点评: 此题主要考查的是学生对电磁波的传播、波长和频率之间关系的了解和掌握,基础性题目. - 1年前
相关推荐
- (2014•天河区二模)如图,小晖利用容积是2mL的注射器、弹簧测力计、刻度尺等器材测量大气压强的值,实验步骤如下:
(2014•天河区二模)如图,小晖利用容积是2mL的注射器、弹簧测力计、刻度尺等器材测量大气压强的值,实验步骤如下:

(1)实验前先将注射器筒内壁和活塞表面涂一层食用油,目的是______.
(2)针筒内保留少量食用油,将活塞推至注射器筒的底端,然后用橡皮帽堵住注射器的小孔目的是______.
(3)用弹簧测力计钩住与活塞相连的细绳,水平向右慢慢拉动注射器筒.如图甲,当注射器中的活塞刚被拉动时,记下弹簧测力计的示数为F=______N;并在图丙中画出活塞在水平方向上所受力的示意图.(忽略残余空气及摩擦的影响,大气压力用F0表示)
(4)如图乙,用分度值是1mm的刻度尺测出注射器全部刻度的长度L=______cm;
(5)计算出此时大气压强的值约为______Pa. shiyubao1681年前0
shiyubao1681年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•天河区二模)如图,在网格上有A、B、O三点,以点O为顶点的一条抛物线过点A、B,且A、B为抛物线上的一组对称
(2008•天河区二模)如图,在网格上有A、B、O三点,以点O为顶点的一条抛物线过点A、B,且A、B为抛
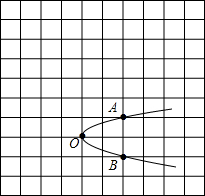 物线上的一组对称点.
物线上的一组对称点.
(1)以O点为旋转中心,将抛物线沿逆时针方向旋转90度,画出旋转后的抛物线图象;
(2)在图中建立恰当的平面直角坐标系,求出旋转后所得抛物线的解析式. xuhang11211年前0
xuhang11211年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•天河区一模)已知矩形ABCD中,AD=3,AB=1.
 (2008•天河区一模)已知矩形ABCD中,AD=3,AB=1.
(2008•天河区一模)已知矩形ABCD中,AD=3,AB=1.
(1)若EF把矩形分成两个小的矩形,如图所示,其中矩形ABEF与矩形ABCD相似.求AF:AD的值;
(2)若在矩形ABCD内不重叠地放两个长是宽的3倍的小长方形,且每个小长方形的每条边与矩形ABCD的边平行,求这两个小长方形周长和的最大值. ameng80081年前1
ameng80081年前1 -
 坤波 共回答了15个问题
坤波 共回答了15个问题 |采纳率86.7%解题思路:(1)设AF=x,再根据矩形ABEF与矩形ABCD相似即可求出x的值,进而得出AF:AD的值;
(2)由于小矩形放置的位置不确定,故应分三种情况讨论:
①两个小矩形都“竖放”;②两个小矩形都“横放”;③两个小矩形一个“横放”,一个“竖放”.(1)设AF=x,
∵矩形ABEF与矩形ABCD相似,AD=3,AB=1,
∴[AB/AD]=[AF/CD],即[1/3]=[x/1],解得x=[1/3],
∴AF:AD=[1/3]:3=1:9;
(2)两个小矩形的放置情况有如下几种:
①两个小矩形都“竖放”,如图(一),在这种放法下,周长和最大的两个小矩形,边长分别为1和 [1/3],
故此时周长和的最大值为 [16/3].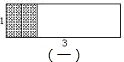
②两个小矩形都“横放”,如图(二)及图(三)所示,这时两个小矩形的周长和的最大值是
2(a+3a)+2[1-a+3(1-a)]=8.
③两个小矩形一个“横放”,一个“竖放”,如图(四),这时两个小矩形的周长和为
2(a+3a)+2(3-a+[3−a/3])=8+[16a/3],
因为0<3a≤1,即0<a≤[1/3],故当a=[1/3]时,此时两个小矩形的周长和最大为 [88/9],
综上三种情形,知所求的最大值为 [88/9].
故答案为:[88/9].点评:
本题考点: 相似多边形的性质.
考点点评: 本题考查的是相似多边形的性质,即相似多边形的对应边成比例,解答此题时要注意分类讨论.1年前查看全部
- (2005•天河区二模)如图所示杠杆处于平衡,请画出物体A的重力G的示意图及杠杆受到的拉力F的力臂L.
 along04051年前1
along04051年前1 -
 塞外孤雁 共回答了20个问题
塞外孤雁 共回答了20个问题 |采纳率95%1年前查看全部
- (2008•天河区一模)如图所示,在单位长度为1的正方形网格中,已知Rt△DAE,∠A=90°,将△DAE绕点D逆时针旋
(2008•天河区一模)如图所示,在单位长度为1的正方形网格中,已知Rt△DAE,∠A=90°,将△DAE绕
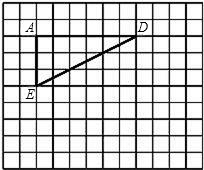 点D逆时针旋转90°后得到△DCF(∠C=90°),再将△DCF沿DA向左平移6个单位长度后得到△ABH(∠B=90°).
点D逆时针旋转90°后得到△DCF(∠C=90°),再将△DCF沿DA向左平移6个单位长度后得到△ABH(∠B=90°).
(1)画出△DCF及△ABH;
(2)AH与DE有怎样的位置关系?请证明你的结论;
(3)若AH与DE相交于点G,求AG的长. lyjasd1年前0
lyjasd1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2013•天河区一模)下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
(2013•天河区一模)下表列出了除去物质中所含少量杂质的方法,其中错误的是( )
A.物质:CO2;所含杂质:O2;除去杂质的方法:通过灼热的铜网
B.物质:KOH溶液;所含杂质:K2CO3;除去杂质的方法:加入足量稀盐酸至不再产生气泡
C.物质:NaCl;所含杂质:CaCO3;除去杂质的方法:溶解、过滤、蒸发
D.物质:H2;所含杂质:H2O;除去杂质的方法:通过浓H2SO4 cwf09151年前1
cwf09151年前1 -
 magic0902 共回答了23个问题
magic0902 共回答了23个问题 |采纳率82.6%解题思路:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.A、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而二氧化碳不与铜反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确.
B、KOH溶液和K2CO3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则;故选项所采取的方法错误.
C、氯化钠易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确.
D、浓硫酸具有吸水性,且不与氢气反应,能除去杂质且没有引入新的杂质,故选项所采取的方法正确.
故选B.点评:
本题考点: 物质除杂或净化的探究.
考点点评: 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.1年前查看全部
- (2008•天河区三模)如图甲所示:体温计的示数是______℃;图乙中物体的长度为______ cm;图丙图
(2008•天河区三模)如图甲所示:体温计的示数是______℃;图乙中物体的长度为______ cm;图丙图中弹簧测力计的读数是______ N.

 tracywang1111年前1
tracywang1111年前1 -
 ycl666107 共回答了27个问题
ycl666107 共回答了27个问题 |采纳率92.6%解题思路:①使用体温计测量体温时,先要弄清楚体温计的量程和分度值,读数时视线与液柱最末端所对刻度相垂直.
②使用刻度尺时要明确其分度值,起始端从0开始,读出末端刻度值,就是物体的长度;起始端没有从0刻度线开始的,要以某一刻度线为起点,读出末端刻度值,减去起始端所对刻度即为物体长度,注意刻度尺要估读到分度值的下一位.
③使用弹簧测力计时,首先要明确其分度值,读数时视线与指针所在刻线相垂直.由图知:
①体温计上1℃之间有10个小格,所以一个小格代表的温度是0.1℃,即此体温计的分度值为0.1℃;此时的温度为38.3℃.
②刻度尺上1cm之间有10个小格,所以一个小格代表的长度是0.1cm=1mm,即此刻度尺的分度值为1mm;物体左侧与6.00cm对齐,右侧与8.85cm对齐,所以物体的长度为L=8.85cm-6.00cm=2.85cm.
③弹簧测力计上1N之间有5个小格,所以一个小格代表0.2N,即此弹簧测力计的分度值为0.2N.此时指针指在“2.4”处,所以弹簧测力计的示数为2.4N.
故答案为:38.3;2.85;2.4.点评:
本题考点: 体温计的使用及其读数;长度的测量;弹簧测力计的使用与读数.
考点点评: 物理测量中有很多的测量工具,刻度尺、秒表、电流表、电压表、天平、量筒、弹簧测力计、温度计等,任何一种工具,一定要注意每一个大格和每一个小格各代表多少.刻度尺需要估读,其他的测量工具不需要估读,读出最接近的数值.1年前查看全部
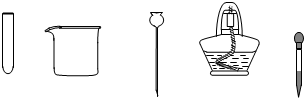
- (2007•天河区一模)如图是实验室常用的仪器,其中用来向容器中添加液体的仪器有(填仪器名称)______.从食盐水中提
(2007•天河区一模)如图是实验室常用的仪器,其中用来向容器中添加液体的仪器有(填仪器名称)______.从食盐水中提取食盐晶体的实验操作中除了需要用到铁架台(带铁圈)及下面已有的某些仪器外,还必须用到的仪器名称是______.
 zhuzhimin41年前1
zhuzhimin41年前1 -
 suncc920 共回答了18个问题
suncc920 共回答了18个问题 |采纳率83.3%解题思路:如上图可知,了解实验室常用的仪器,其中用来向容器中添加液体的仪器有哪些,从食盐水中提取食盐晶体的实验操作中需要用到哪些仪器.了解实验室常用的仪器:用来向容器中添加液体的仪器有:长颈漏斗、胶头滴管(或滴管);从食盐水中提取食盐晶体的实验操作中需要用到的仪器:铁架台、蒸发皿、玻璃棒,故除了需要用到铁架台(带铁圈)及下面已有的某些仪器外,还必须用到的仪器名称是蒸发皿、玻璃棒.
故答为:长颈漏斗、胶头滴管(或滴管);蒸发皿、玻璃棒.点评:
本题考点: 常用仪器的名称和选用.
考点点评: 了解具备基本的化学实验技能是学习化学和进行化学探究活动的基础和保证.只有掌握化学实验的基本技能,才能安全、准确地进行化学实验.1年前查看全部
- (2011•天河区一模)用化学语言填空:
(2011•天河区一模)用化学语言填空:
(1)氧化铝______,3个氮气分子______,2个铵根离子______,能调节人的生理平衡且由离子构成的化合物______,能中和工业酸性废水、农业上用来改良酸性土壤的一种碱______.
(2)某水溶液中含有大量的K+、OH-、Cl-,则该溶液中的溶质是______. hikaru1年前1
hikaru1年前1 -
 椭圆的圆圈 共回答了20个问题
椭圆的圆圈 共回答了20个问题 |采纳率100%解题思路:(1)根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,进行解答;
(2)根据只有阴阳离子才能构成化学式进行解答.(1)根据化合物化学式的书写步骤:归类→定序→标价→交叉→约简,氧元素的化合价为-2,铝元素的化合价为+3,因此氧化铝的化学式为:Al2O 3; 根据分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,因此3个氮气分子表示为:3N2; 根据离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其元素符号前加上相应的数字;因此2个铵根离子表示为:2NH 4+; 氯化钠是调节人的生理平衡且由离子构成的化合物;熟石灰能中和工业酸性废水、农业上用来改良酸性土壤的一种碱;故答案为:Al2O 3;3N2;2NH 4+;NaCl;Ca(OH)2.
(2)由K+、OH-、Cl-,三种离子构成的物质有KOH、KCl,故答案为:KOH、KCl.点评:
本题考点: 化学式的书写及意义;化学符号及其周围数字的意义.
考点点评: 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写.1年前查看全部
- (2013•天河区一模)如图,∠A是⊙O的圆周角,∠A=50°,则∠OBC的度数为______.
 1762318421年前1
1762318421年前1 -
 epWER 共回答了21个问题
epWER 共回答了21个问题 |采纳率85.7%∵,∠A是⊙O的圆周角,∠A=50°,
∴∠BOC=2∠A=2×50°=100°,
∵OB=OC,
∴∠OBC=[180°−∠BOC/2]=[180°−100°/2]=40°.
故答案为:40°.1年前查看全部
- (2013•天河区二模)硫酸铝溶液中含有少量硫酸铜和硫酸杂质,加入下列物质能除去杂质的是( )
(2013•天河区二模)硫酸铝溶液中含有少量硫酸铜和硫酸杂质,加入下列物质能除去杂质的是( )
A.Al
B.Al2O3
C.Al(OH)3
D.Na2CO3 往事虽风1年前1
往事虽风1年前1 -
 木鱼河流 共回答了21个问题
木鱼河流 共回答了21个问题 |采纳率100%解题思路:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,除杂时选择的试剂与杂质反应时不能生成新的杂质.A、铝能与硫酸铜和硫酸反应生成了硫酸铝,能除去杂质.故A正确;
B、Al2O3不能与硫酸铜反应,不能将硫酸铜杂质除去.故B错误;
C、Al(OH)3不能与硫酸铜反应,不能将硫酸铜杂质除去.故C错误;
D、Na2CO3与硫酸反应生成了硫酸钠,引入了新的杂质.故D错误.
故选A.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题通过物质除杂的形式考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.1年前查看全部
- (2012•天河区一模)(1)CO还原氧化铜的化学方程式是CO+CuO △
 (2012•天河区一模)(1)CO还原氧化铜的化学方程式是CO+CuO
(2012•天河区一模)(1)CO还原氧化铜的化学方程式是CO+CuO
Cu+CO2△ .CO+CuO.还原产物中往往含有少量红色的氧化亚铜(Cu2O)固体,Cu2O能与稀硫酸发生如下反应:Cu2O+H2SO4=Cu+CuSO4+H2O.检验CO还原氧化铜的还原产物中是否含Cu2O的实验方法是______,产物中含有Cu2O的实验现象是______.
Cu+CO2△ .
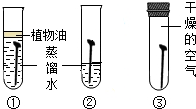
(2)铜锈的主要成分是铜绿[Cu2(OH)2CO3],则推测铜生锈的条件除铜与O2接触外,还需要与______接触,某同学设计了如图A、B、C三组实验来探究铜生锈的条件,该同学能达到实验目的吗?______;对照实验B、C,可知铜锈蚀的条件之一为______.
(3)硫铁矿(主要成分是FeS2)是一种铁矿石.FeS2的相对分子质量为______,用400t含FeS2 60%的硫铁矿,理论上可以炼出______吨铁.(假设在反应过程中FeS2中的铁元素全部转化成铁单质,且杂质中不含铁). 靖哥哥9991年前1
靖哥哥9991年前1 -
 hhylix 共回答了24个问题
hhylix 共回答了24个问题 |采纳率83.3%解题思路:(1)①根据一氧化碳还原氧化铜的原理写出反应方程式;②根据给出的方程式信息分析;
(2)根据铜锈的化学式[Cu2(OH)2CO3],从元素守恒的角度分析铜生锈的因素,并从铜生锈的条件和实验装置对照不会是只与氧气和水作用的结果,还应与含有碳元素的物质接触,而空气中的含碳物质主要是二氧化碳,得出结论.
(3)根据相对分子质量定义和元素守恒来计算.(1)根据一氧化碳还原氧化铜的原理写出反应方程式:CO+CuO
△
.
Cu+CO2;根据题中给的化学方程式的信息可以看出氧化亚铜能与硫酸反应,且生成的硫酸铜溶液呈现蓝色,而铜却不能和硫酸反应,故可以用稀硫酸验证,答案为:取少量固体加入到足量硫酸溶液中,溶液逐渐变成蓝色;
(2)①根据铜锈的化学式[Cu2(OH)2CO3],可以看出其中含有铜、氢、碳、氧四种元素,其中的碳元素和氧元素应来自空气中的二氧化碳和水,所以铜生锈是铜与氧气、水、二氧化碳共同作用的结果;②图A用植物油密封水,但铜不生锈,说明铜在只有水的条件下不生锈;图B中的铜与氧气、水、二氧化碳都接触,说明铜生锈有三种物质的参与;图C提供的条件是干燥的空气,此时铜与氧气和二氧化碳接触不生锈,说明只有氧气和二氧化碳铜也不生锈;对比A、B、C图看出,没有验证铜只和氧气或二氧化碳接触是否生锈,故不能;
对比B和C,图B中的铜与氧气、水、二氧化碳都接触,图C提供的条件是干燥的空气,此时铜与氧气和二氧化碳接触,不同之处在是否和水接触.说明铜生锈不会是只与氧气和二氧化碳作用的结果,还应与水接触.
(3)FeS2的相对分子质量=56+32×2=120;
根据质量守恒定律中铁元素在反应前后质量不变,400t含FeS2 60%的硫铁矿中铁元素的质量=400t×60%×[56/120]×100%=112t.(也可根据化学方程式计算)
故答案为:(1)CO+CuO
△
.
Cu+CO2;取少量固体加入到足量硫酸溶液中;溶液逐渐变成蓝色;
(2)CO2和H2O;不能;与水接触;
(3)120;112.点评:
本题考点: 一氧化碳的化学性质;含杂质物质的化学反应的有关计算;金属锈蚀的条件及其防护;酸的化学性质;相对分子质量的概念及其计算;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要根据实验设计和实验现象等方面进行分析、判断,合理设计实验方案,从而得出正确的结论.1年前查看全部
- (2014•天河区一模)圆的位置关系有很多种,如图中不存在位置关系的是( )
 (2014•天河区一模)圆的位置关系有很多种,如图中不存在位置关系的是( )
(2014•天河区一模)圆的位置关系有很多种,如图中不存在位置关系的是( )
A.内含
B.相交
C.外离
D.外切 qfxy860521年前1
qfxy860521年前1 -
 cytyx8486 共回答了15个问题
cytyx8486 共回答了15个问题 |采纳率86.7%依题意得:两圆的位置关系有外离,内切,外切,内含,因此不存在的位置关系是相交,
故选B.1年前查看全部
- (2013•天河区一模)下列关于H2O和H2O2的说法不正确的是( )
(2013•天河区一模)下列关于H2O和H2O2的说法不正确的是( )
A.都含有氢元素和氧元素
B.都是化合物
C.都含有氢气分子
D.一定条件下都能发生分解反应 木头2个1年前1
木头2个1年前1 -
 kpray 共回答了17个问题
kpray 共回答了17个问题 |采纳率94.1%解题思路:A、根据H2O和H2O2的化学式的含义进行分析判断.
B、由不同种元素组成的纯净物是化合物.
C、根据H2O和H2O2的微观构成进行分析判断.
D、根据H2O和H2O2的化学性质进行分析判断.A、H2O和H2O2的中都含有氢元素和氧元素,故选项说法正确.
B、H2O和H2O2都是由不同种元素组成的纯净物,都是化合物,故选项说法正确.
C、H2O和H2O2分别是由水分子和过氧化氢分子构成的,均不含氢分子,故选项说法错误.
D、H2O和H2O2在一定条件下都能发生分解反应,水在通电条件下生成氢气和氧气,过氧化氢在二氧化锰的催化作用下生成水和氧气,上述反应均属于分解反应,故选项说法正确.
故选C.点评:
本题考点: 分子、原子、离子、元素与物质之间的关系;单质和化合物的判别.
考点点评: 本题难度不大,主要考查了构成物质的宏观组成与微观粒子构成,掌握常见物质的宏观组成与微观构成是正确解答本题的关键.1年前查看全部
- (2006•天河区一模)小明学习化学后,在家里想用化学方法来鉴别碱面(主要成分是碳酸钠)和食盐,你认为下列方法不可行的是
(2006•天河区一模)小明学习化学后,在家里想用化学方法来鉴别碱面(主要成分是碳酸钠)和食盐,你认为下列方法不可行的是( )
A.各取少量通过尝味道区分
B.各取少量分别倒入水中观察是否溶解
C.各取少量分别倒入食醋
D.各取少量溶于水,再分别加入石灰水 w5enb1年前1
w5enb1年前1 -
 海内纯只鸡 共回答了27个问题
海内纯只鸡 共回答了27个问题 |采纳率92.6%解题思路:根据碱面与食盐的性质不同考虑,所用的方法必须呈现的现象不同才行.A、各取少量通过尝味道,咸味的是食盐,涩味的是碳酸钠,可以区分,但是A是物理方法,不是化学方法,故A说法错误;
B、碱面(主要成分是碳酸钠)和食盐都易溶于水,并且溶液呈现无色,故B不能鉴别,故B说法错误;
C、食醋与碳酸钠反应产生二氧化碳,与食盐不反应,故能鉴别,故C说法正确;
D、由于氢氧化钙与碳酸钠反应生成碳酸钙沉淀,与氯化钠不反应,所以能鉴别,故D说法正确.
故选AB.点评:
本题考点: 酸、碱、盐的鉴别.
考点点评: 通过回答本题知道了鉴别物质的方法,要根据物质的性质不同考虑.1年前查看全部
- (2014•天河区二模)圆锥母线长为8cm,底面半径为5cm,则此圆锥侧面积为______cm2.
 冷门的1年前1
冷门的1年前1 -
 大水牛 共回答了19个问题
大水牛 共回答了19个问题 |采纳率89.5%解题思路:圆锥的侧面积=底面周长×母线长÷2,把相应数值代入即可求解.圆锥的侧面积=2π×8×5÷2=40π.
故答案为:40π.点评:
本题考点: 圆锥的计算.
考点点评: 本题考查了圆锥的计算,解题的关键是弄清圆锥的侧面积的计算方法,特别是圆锥的底面周长等于圆锥的侧面扇形的弧长.1年前查看全部
- (2011•天河区模拟)实验室通常采用如图装置制取少量干燥氢气,请根据要求回答:
(2011•天河区模拟)实验室通常采用如图装置制取少量干燥氢气,请根据要求回答:
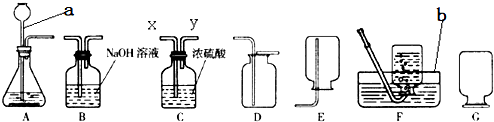
(1)仪器a的名称______,仪器b的名称______.
(2)实验室使用稀盐酸和金属锌制取氢气,反应的化学方程式为______;这种方法制得的氢气往往含有少量氯化氢气体和水蒸气两种杂质,这是因为盐酸具有______性,可以先通过______装置(填装置序号)除去氯化氢气体,然后通过C装置除去水蒸气,原理是装置中的浓硫酸具有______性,气体从C装置______处进入(填x或y).
(3)实验中可采用______装置收集干燥氢气. bad00020041年前1
bad00020041年前1 -
 雪夜无双 共回答了16个问题
雪夜无双 共回答了16个问题 |采纳率93.8%解题思路:(1)认识常见仪器;
(2)锌与盐酸反应生成氯化锌和氢气;根据盐酸的挥发性和浓硫酸的吸水性来分析;
(3)根据氢气的性质以及不同收集方法的特点来分析.(1)a是长颈漏斗,b是水槽;
(2)锌与盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑,盐酸具有挥发性,导致制取的氢气中混有氯化氢气体,可以利用氢氧化钠溶液来反应掉氯化氢气体,浓硫酸具有吸水性,可以除去氢气中混有的水蒸气,注意长进短出;
(3)排水法收集的氢气比较纯净,向下排空气法收集到的氢气比较干燥.
故答案为:(1)长颈漏斗;水槽;
(2)Zn+2HCl=ZnCl2+H2↑;挥发;B;吸水;x;
(3)E.点评:
本题考点: 氢气的制取和检验;气体的净化(除杂);书写化学方程式、文字表达式、电离方程式.
考点点评: 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.1年前查看全部
- (2011•天河区模拟)中和反应在日常生活和工农业生产中有广泛的应用.
 (2011•天河区模拟)中和反应在日常生活和工农业生产中有广泛的应用.
(2011•天河区模拟)中和反应在日常生活和工农业生产中有广泛的应用.
(1)在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞溶液后,再用滴管慢慢滴入稀盐酸至溶液颜色恰好变成无色为止,此时烧杯中溶液的pH是______7.(填“大于”、“小于”或“等于”).发生反应的化学方程式为______.
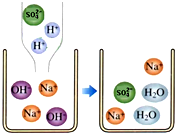
(2)如图是硫酸滴入氢氧化钠溶液中有关粒子之间反应的示意图.由图可知:氢氧化钠溶液中存在的离子有______(填粒子的符号,下同);硫酸与氢氧化钠能发生中和反应的实质,是硫酸中的______与氢氧化钠溶液中的氢氧根离子结合,生成了水. 明明知道薇的心1年前1
明明知道薇的心1年前1 -
 最美是爱你 共回答了21个问题
最美是爱你 共回答了21个问题 |采纳率95.2%解题思路:(1)在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞溶液后,再用滴管慢慢滴入稀盐酸至溶液颜色恰好变成无色为止,两者前后完全反应,氢氧化钠溶液与稀盐酸反应生成氯化钠和水,据此进行分析解答.
(2)中和反应是酸与碱作用生成盐和水的反应,中和反应的实质是H++OH-=H2O.(1)在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞溶液后,再用滴管慢慢滴入稀盐酸至溶液颜色恰好变成无色为止,两者前后完全反应,此时烧杯中溶液的pH=7;氢氧化钠溶液与稀盐酸反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O.
(2)氢氧化钠溶液中存在的离子有钠离子和氢氧根离子,其离子符号为Na+、OH-;中和反应是酸与碱作用生成盐和水的反应,硫酸与氢氧化钠能发生中和反应的实质,由反应的微观示意图可知,大量的氢离子和氢氧根离子相互作用生成水的过程,即中和反应的实质是H++OH-=H2O
故答案为:(1)等于;HCl+NaOH=NaCl+H2O;(2)Na+、OH-;H+.点评:
本题考点: 中和反应及其应用;溶液的酸碱性与pH值的关系;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,掌握酸碱中和反应的原理、实质、化学方程式的书写是正确解答此类题的关键.1年前查看全部
- (2007•天河区一模)在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).下面是某化学兴趣小组处理回收
(2007•天河区一模)在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).下面是某化学兴趣小组处理回收含铜废料的主要步骤.
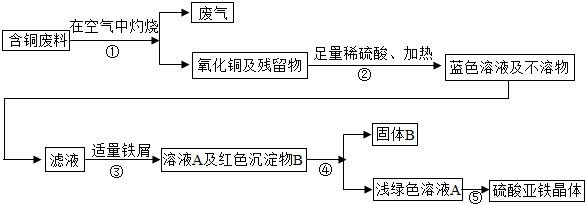
回答下列问题:
(1)溶液A中溶质的化学式是______.
(2)步骤②中发生的化学方程式为______.
(3)步骤④的操作方法是______.
(4)某同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸发生反应(方程式为:2Cu+2H2SO4+O2
2CuSO4+2H2O),该方案明显优于原方案,你认为优点是______.现有160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4______kg.△ .
(5)方案最后一步所得浅绿色滤液结晶后,会得到硫酸亚铁晶体,可增加经济效益.请写出使“绿矾”结晶的两种可能方法:______、______(“绿矾”溶解度随温度升高而增大). 阿弥陀佛555691年前1
阿弥陀佛555691年前1 -
 zhgg9588 共回答了17个问题
zhgg9588 共回答了17个问题 |采纳率100%解题思路:(1)由蓝色溶液与铁反应考虑所得溶液中的溶质;
(2)由图示知稀硫酸与氧化铜反应,可写其反应的化学方程式;
(3)步骤④是分离固液混合物的操作,根据要求可选择适当的分离方法;
(4)对比分析原实验方案,即可知道该方案的明显优点;根据题给的化学方程式和相关数据即可计算出所求数据,这是一道根据化学方程式的计算题;
(5)根据题意确定“绿矾”结晶的两种方法.(1)铜在空气中灼烧生成黑色固体氧化铜,氧化铜与硫酸反应生成蓝色硫酸铜,与铁屑反应置换出铜,反应方程式为:CuO+H2SO4═CuSO4+H2O; Fe+CuSO4═FeSO4+Cu;故溶液A中溶质的化学式是FeSO4;
(2)步骤②中发生的化学方程式为:CuO+H2SO4═CuSO4+H2O;
(3)加入适量的铁屑,是将硫酸铜中的铜全部置换出来,用过滤法即可分离溶液A和红色固体B;
(4)从环保角度对两套方案的不同部分进行比较,开始方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知第二个方案更合理,根据方程式2Cu+2H2SO4+O2
△
.
2CuSO4+2H2O,计算160kg含铜80%的废料,完全与硫酸、氧气发生反应,最多生成CuSO4 320kg.
(5)结晶的方法有:冷却热饱和溶液和蒸发溶剂法,即蒸发结晶和降温结晶.
故答案为:1)FeSO4;(2)CuO+H2SO4═CuSO4+H2O;(3)过滤;(4)没有废气产生,不污染环境,320;(5)蒸发水分、降温.点评:
本题考点: 酸的化学性质;化学实验方案设计与评价;晶体和结晶的概念与现象;金属的化学性质.
考点点评: 本题考查通过实验现象,培养学生综合利用所学知识进行分析解题的能力.题型涉及知识面广泛,是一道锻炼能力的好题.1年前查看全部
- (2013•天河区二模)小玉提出了几个想法,正确的是( )
(2013•天河区二模)小玉提出了几个想法,正确的是( )
①超导材料科应用于远距离输电线.②卫星导航是利用超声波进行定位和导航的.③红外线是电磁波,可在真空中传递信息.④中性原子一定含有质子、中子、电子.⑤一个红苹果,只是绿光的照射下显示的颜色是黑色.
A.①⑤正确,②③④错误
B.①③⑤正确,②④错误
C.②③④正确,①⑤错误
D.②④正确,①③⑤错误 fubairong21年前1
fubairong21年前1 -
 四十面相 共回答了21个问题
四十面相 共回答了21个问题 |采纳率76.2%解题思路:①超导体的电阻为零时,不会放热,所以电能无法转化为内能,也就避免了内能的损耗,适合做输电线路.
②声音传播需要介质,真空不能传播声音.超声波不能在真空中传播.
③光也是电磁波,电磁波传播不需要介质,可在真空中传播.
④原子由原子核和核外电子组成,原子核由质子、中子组成.
⑤不透明物体的颜色由物体反射的色光决定的,不透明物体只反射与自己相同颜色的色光,吸收与其颜色不同的色光.白色反射所有的色光,黑色吸收所有的色光.①超导体的电阻为零,在进行远距离输电时不会消耗电能产生热,可以减少在输电过程中的能量损耗,大大节约能源.①说法正确.
②超声波不能在真空中传播,卫星导航不是利用超声波进行定位和导航的,用的是电磁波.②说法不正确.
③红外线是电磁波,可在真空中传递信息.③说法正确.
④中性原子一般含有质子、中子、电子,氢原子中无中子.④说法不正确.
⑤红苹果只反射红光,吸收红光以外的光,只有绿光的照射时,绿光被红苹果吸收,没有光反射出来,所以苹果看上去是黑色的.⑤说法正确.
故选B.点评:
本题考点: 超导体在磁悬浮列车、超导输电的应用;原子的核式模型;物体的颜色;红外线;卫星中继通信.
考点点评: 本题考查的知识点较多,主要考查学生对所学物理知识点的综合应用能力,有一定的难度,是一道好题.1年前查看全部
- (2014•天河区一模)甲、乙两车间计划一起用一批原材料制作同一种零件9000个.
(2014•天河区一模)甲、乙两车间计划一起用一批原材料制作同一种零件9000个.
(1)列出原材料重量y(千克)与平均每千克原材料生产零件x(个)之间的函数关系式,若已知这批原材料重量超过990千克且不超过1010千克,请求出x的可能取值;
(2)乙车间比甲车间平均每小时多生产30个,甲车间生产600个零件与乙车间生产900个零件所用的时间相等,若设甲车间平均每小时生产a个零件,求a的值. 大涛站长1年前1
大涛站长1年前1 -
 majiantao 共回答了25个问题
majiantao 共回答了25个问题 |采纳率88%解题思路:(1)根据原材料=产品总数×每件产品需要的原材料就可以求出解析式;
(2)根据甲车间生产600个零件与乙车间生产900个零件所用的时间相等建立方程求出其解即可.(1)由题意,得
y=[9000/x].
∵990<y≤1010,
∴990<[9000/x]≤1010,
解得:[900/101]≤x<[100/11].
答:x的取值为:9;
(2)由题意,得
[600/a=
900
a+30],
解得:a=60.
经检验,a=60是原方程的解,且符合题意.
答:a=60.点评:
本题考点: 一次函数的应用.
考点点评: 本题考查了函数的解析式的运用,列不等式组解实际问题的运用,列分式方程解实际问题的运用,分式方程的解法的运用,解答时检验是学生容易忽略的环节.1年前查看全部
- (2014•天河区模拟)下列物理图象所表示出的各物理量之间的关系,错误的是( )
(2014•天河区模拟)下列物理图象所表示出的各物理量之间的关系,错误的是( )

A.图甲为某种物质的质量与体积关系,由图象可知,该物质的密度为2.5g/cm3
B.图乙为物体受到的重力与物体质量关系,由图象可知,重力与质量的比值为9.8N/kg
C.图丙为某导体中电流跟它两端电压的关系,由图象可知,此导体的电阻为 5Ω
D.图丁为为某物体的路程与时间关系,由图象可知,该物体运动的速度为10m/s 朱小柳青1年前1
朱小柳青1年前1 -
 小刚1981 共回答了19个问题
小刚1981 共回答了19个问题 |采纳率100%A、对某种物质来说,其质量与体积成正比,其质量与体积的比值是一定值,故其密度值是:ρ=[m/V]=[5g
2cm3=2.5g/cm3;故该选项不符合题意;
B、物体所受的重力与其质量成正比,故g=
G/m]=[19.6N/2kg]=9.8N/kg,故该选项不符合题意;
C、当电阻不变时,电压与电流的比值是一个定值,电流应随电压的增大而增大,即R=[U/I]=[10V/2A]=5Ω,故不符合题意;
D、据图能看出该物体随着时间的增长,路程不变,故该物体处于静止状态,所以该选项符合题意;
故选D.1年前查看全部
- (2008•天河区二模)以下数据中与实际情况基本相符的是( )
(2008•天河区二模)以下数据中与实际情况基本相符的是( )
A.一个西瓜大约为100g
B.洗澡水的温度大约70℃
C.一个普通初中生受到的重力大约在450N左右
D.一支新铅笔的长度约15mm zxy2002021年前1
zxy2002021年前1 -
 lolitacao 共回答了10个问题
lolitacao 共回答了10个问题 |采纳率100%解题思路:做这种题目,要对一些常见的物理量要有一定的估测能力,根据生活常识去判断题目的对错.A、一个西瓜大约为6kg,故A错误;
B、洗澡水的温度大约37℃,故B错误;
C、一个普通初中生的质量m=45kg,受到的重力G=mg=45kg×10N/kg=450N左右,故C正确;
D、一支新铅笔的长度约20cm,故D错误.
故选C.点评:
本题考点: 质量的估测;温度;长度的估测;重力的计算.
考点点评: 此题考查的是学生对一些常见物理量的估测能力,需要学生对生活中的常见物理量单位、大小有所认识,此题就会得到正确答案.1年前查看全部
- (2013•天河区)一个近似圆锥沙堆,底面半径是3米,高是2米.如果一辆车每次运5立方米,运完这堆沙需要多少次?
 汐茗1年前1
汐茗1年前1 -
 Guncer 共回答了18个问题
Guncer 共回答了18个问题 |采纳率94.4%解题思路:根据圆锥的体积公式V=[1/3]sh,求出圆锥形沙堆的体积,最后用沙堆的除以除以5立方米就是要求的答案.[1/3]×3.14×32×2÷5,
=3.14×3×2÷5,
=3.14×6÷5,
=18.84÷5,
=3.768,
≈4(次);
答:运完这堆沙需要4次.点评:
本题考点: 关于圆锥的应用题.
考点点评: 此题主要考查了圆锥的体积公式的实际应用,注意计算时不要忘了乘[1/3].1年前查看全部
- (2014•天河区二模)小红与小荣测一石块的质量.
(2014•天河区二模)小红与小荣测一石块的质量.

(1)小红用称量是200g的天平测这石块的质量,天平平衡时如图甲所示,可知小红使用天平的错误之处是______.
(2)小荣则选用细绳和长硬棒(质量可忽略)组成图乙的装置.
①手提细绳如图乙,若硬棒水平静止,在图中画出需要测量的力臂L1和L2.
②设托盘与祛码总质量为m,则石块的质量为m石=
mL1 L2 .(用上述求得及所测得的物理量符号表示)
mL1 L2  火龙**1年前1
火龙**1年前1 -
 yanyan7505 共回答了25个问题
yanyan7505 共回答了25个问题 |采纳率92%解题思路:(1)在天平正确使用时应注意:不能超过天平的称量;加减砝码要用镊子,不能用手加减砝码;不能把潮湿或易腐蚀性的药品直接放到托盘上等.
(2)根据m=ρV计算出水的质量;根据书包和水瓶的力臂,运用公式F1L1=F2L2进行解答.(1)已知该天平的量程是200g,而分析天平右盘中的砝码可知,此时砝码的质量超过了200g,所以这样很容易损坏天平;
(2)根据杠杆的平衡条件:F1L1=F2L2即mL1=m石L2
得:m石=
L1
L2m;
故答案为:(1)测量过程中超过了该天平的称量;
(2)①图示: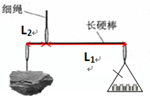
②
L1
L2m点评:
本题考点: 质量的测量与天平;杠杆的平衡条件.
考点点评: 这是一道杠杆与天平的综合题,考查了学生对天平使用时的注意事项的掌握以及杠杆平衡条件的理解.1年前查看全部
- (2上上6•天河区s模)化学研究课上,为了验证氨气(NH3)7某些性质,小雨同学做了以下实验:下图中从左向右依次是她做7
(2上上6•天河区s模)化学研究课上,为了验证氨气(NH3)7某些性质,小雨同学做了以下实验:下图中从左向右依次是她做7实验及相应现象.
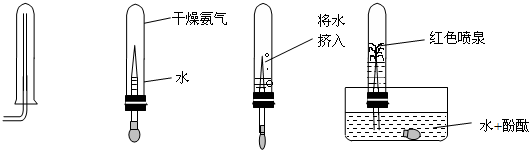
通过以上实验,小雨得出了关于氨气7三点性质,你认为它们是什么呢?①______,②______,③______. chenqq5201年前1
chenqq5201年前1 -
 英魂不善 共回答了15个问题
英魂不善 共回答了15个问题 |采纳率100%解题思路:根据向下排空气法收集来判断出气体的密度与空气密度的关系;根据将水挤入使试管内气压减小说出溶解性,根据溶液颜色变化说出酸碱性.用向下排空气法收集该气体,说明该气体2密度比空气一,将水挤入能形成红色喷泉,说明了试管内气压减小,即氨气易溶于水,酚酞试液变红说明了水溶液呈碱性.
故答案为:①密度比空气小,②易溶于水,③水溶液呈碱性.点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 通过回答本题知道了通过现象来推测物质性质的方法,并要灵活运用它们.1年前查看全部
- (2007•天河区一模)在一个圆柱体中间挖出一个小圆洞,如图所示,则该物体俯视图的形状是( )
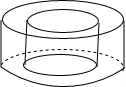 (2007•天河区一模)在一个圆柱体中间挖出一个小圆洞,如图所示,则该物体俯视图的形状是( )
(2007•天河区一模)在一个圆柱体中间挖出一个小圆洞,如图所示,则该物体俯视图的形状是( )
A.
B.
C.
D.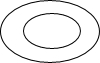
 cdw168881年前1
cdw168881年前1 -
 xiao风 共回答了21个问题
xiao风 共回答了21个问题 |采纳率90.5%解题思路:找到从上面看所得到的图形即可,注意本题一个圆柱体中间挖出一个小圆洞.从上面看可得到一个圆环.
故选C.点评:
本题考点: 简单组合体的三视图.
考点点评: 本题考查了三视图的知识,俯视图是从物体的上面看得到的视图,注意看得到的棱画实线.1年前查看全部
- 广州市天河区中山大道中1011-1015号东圃大厦
广州市天河区中山大道中1011-1015号东圃大厦
这个地址怎么写啊?对我来说太难了 麦甜tian1年前1
麦甜tian1年前1 -
 sunyyx 共回答了20个问题
sunyyx 共回答了20个问题 |采纳率95%Dongpu Building,No.1011-1015,Mid-Zhongshan Rd.,Tianhe District,Guangzhou1年前查看全部
- (2012•天河区二模)小文同学采用如图所示的两种不同的方式将同一货物搬运到同一辆汽车上,其中说法正确的是( )
 (2012•天河区二模)小文同学采用如图所示的两种不同的方式将同一货物搬运到同一辆汽车上,其中说法正确的是( )
(2012•天河区二模)小文同学采用如图所示的两种不同的方式将同一货物搬运到同一辆汽车上,其中说法正确的是( )
A.甲图中货物受到的所有力都对货物做了功
B.甲图中利用斜面省力又省功
C.乙图中货物的重力势能不变
D.两种情况下,货物机械能都增加 ly1215331年前1
ly1215331年前1 -
 wlfkongl 共回答了21个问题
wlfkongl 共回答了21个问题 |采纳率85.7%解题思路:(1)分析物体受到的力,分析物体在每一个力方向上是否通过了距离.
(2)使用机械可以省力,可以省距离,就是不能省功.
(3)重力势能大小跟质量、被举得高度有关.被举得高度一定时,质量越大,重力势能越大;质量一定时,高度越高,重力势能越大.
(4)分析物体的动能和重力势能大小,根据机械能=动能+势能进行判断.A、甲图,物体受到重力、支持力、推力、摩擦力的作用,重力和摩擦力做负功,推力对物体做功,支持力对物体没有做功.选项错误.
B、使用任何机械都不省功.选项错误.
C、乙图中,货物的质量不变,高度增大,重力势能增大.选项错误.
D、两种情况下,货物在地面和静止在车厢内速度为零,动能为零;高度增大,重力势能增大;货物上升时没有发生弹性形变,不具有弹性势能;机械能=动能+重力势能,所以机械能增大.选项正确.
故选D.点评:
本题考点: 力是否做功的判断;动能和势能的大小变化.
考点点评: (1)有力有距离,力对物体不一定做功,物体必须在力的作用下通过了距离,力对物体才做功.
(2)掌握动能、重力势能、弹性势能大小的影响因素,利用控制变量法判断动能、重力势能、弹性势能、机械能大小的变化.1年前查看全部
- (2011•天河区一模)如图是人在突遇紧急情况时,体内某些组织、器官、系统的功能发生相应改变,以适应外界环境变化的模式图
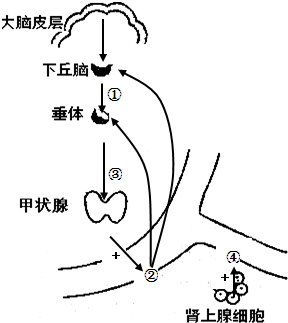 (2011•天河区一模)如图是人在突遇紧急情况时,体内某些组织、器官、系统的功能发生相应改变,以适应外界环境变化的模式图.请回答下列问题:
(2011•天河区一模)如图是人在突遇紧急情况时,体内某些组织、器官、系统的功能发生相应改变,以适应外界环境变化的模式图.请回答下列问题:
(1)人在突遇紧急情况时②分泌量的增加,会导致______(填序号)分泌量减少,此种调节机制称为______调节.在②分泌量增加的同时,______(填名称)的分泌量也增加,二者协调作用,保证机体应急反应的顺利进行.
(2)在此过程中人常会出现瞳孔放大、手心出汗、心跳加快等现象,在这些反应过程中兴奋都是单向传递的.因为______.
(3)在突遇紧急情况时,血液的pH、温度、化学成分等不会发生太大的变化,这说明人体在紧急情况下能通过______调节来维持______.
(4)饭后人体内血糖浓度也会有变化,______细胞合成的胰岛素能降血糖.如果为此细胞提供3H标记的氨基酸,则过一段时间检测,3H在细胞内各细胞器中先后出现的顺序是______. 13TTTT131年前1
13TTTT131年前1 -
 在一歌桃树上上吊 共回答了19个问题
在一歌桃树上上吊 共回答了19个问题 |采纳率84.2%解题思路:1、分析图解:根据甲状腺激素的分级调节可以确定,图中①是促甲状腺激素释放激素、③是促甲状腺激素、②是甲状腺激素.肾上腺细胞也会分泌④肾上腺素.
2、神经递质存在于突触前膜的突触小泡中,只能由突触前膜释放,然后作用于突触后膜,因此兴奋只能从一个神经元的轴突传递给另一个神经元的细胞体或树突.(1)分析题图可知,①是促甲状腺激素释放激素,②是甲状腺激素,③是促甲状腺激素,④是肾上腺素,②甲状腺激素的合成和分泌受①③的调节,当②甲状腺激素过高时会抑制下丘脑和垂体分泌促甲状腺激素释放激素和促甲状腺激素,这种调节方式是负反馈调节;②甲状腺激素和④肾上腺素起协同作用,②分泌量增加的同时,④分泌量也增加,二者协调作用,保证机体应急反应的顺利进行.
(2)兴奋在突触之间都是单向传递的,因为神经递质只能由突触前膜释放作用于突触后膜.
(3)血液的PH、温度、化学成分等不会发生明显的变化,这说明人体具有维持内环境稳态的能力,体现这种能力是在神经(系统)和体液的调节下,通过各个器官系统的协调活动实现的.
(4)饭后人体内血糖浓度也会有变化,胰岛B细胞合成的胰岛素能降血糖;胰岛素是分泌蛋白,分泌蛋白首先在内质网上的核糖体上经脱水缩合反应过程形成多肽链,然后依次进入内质网和高尔基体进行加工、分类、包装和发送,因此如果为细胞提供3H标记的氨基酸,则3H将首先在核糖体出现,随后依次在内质网、高尔基体中出现,最后在细胞外出现.
故答案为:
(1)①和③(负)反馈 肾上腺素
(2)神经递质只能由突触前膜释放作用于突触后膜
(3)神经和体液 内环境的稳态
(4)胰岛B核糖体→内质网→高尔基体点评:
本题考点: 神经、体液调节在维持稳态中的作用.
考点点评: 本题考查了神经调节和体液调节的相关知识,要求考生能够根据甲状腺激素的分级调节判断图中①~③表示的激素名称;识记寒冷时甲状腺激素和肾上腺素分泌均会增加;识记内环境稳态调节的概念.1年前查看全部
- (2012•天河区三模)如图,四棱锥P-ABCD中,底面ABCD是菱形,PA=PD,∠BAD=60°,E是AD的中点,点
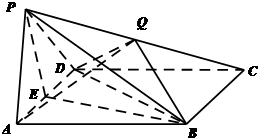 (2012•天河区三模)如图,四棱锥P-ABCD中,底面ABCD是菱形,PA=PD,∠BAD=60°,E是AD的中点,点Q在侧棱PC上.
(2012•天河区三模)如图,四棱锥P-ABCD中,底面ABCD是菱形,PA=PD,∠BAD=60°,E是AD的中点,点Q在侧棱PC上.
(Ⅰ)求证:AD⊥平面PBE;
(Ⅱ)若Q是PC的中点,求证:PA∥平面BDQ;
(Ⅲ)若VP-BCDE=2VQ-ABCD,试求[CP/CQ]的值. Lackesis1年前0
Lackesis1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2的l2•天河区二模)煤的液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,其b
(2的l2•天河区二模)煤的液化是把固体煤炭通过化学加工过程,使其转化成为液体燃料、化工原料和产品的先进洁净煤技术,其b合成CHdOH 是最重要的研究方向之她.
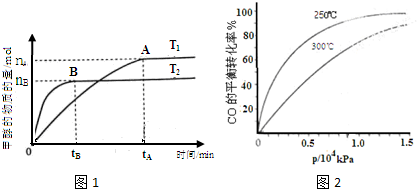
(l)在2L的密闭容器b,由CO2和H2合成甲醇CO2(g)+dH2(g)═CHdOH(g)+H2O(g),在其他条件不变的情况下,探究温度对反应的影响,实验结果l图l所示(注:T2>Tl均大于d的的℃).
①温度为T2时,从反应开始到平衡,生成甲醇的平均反应速率为
mol/(L•min)nB 2tB
mol/(L•min)nB 2tB
②通过分析图l,可以得出温度对反应CO2(g)+dH2(g)═CHdOH(g)+H2O(g)的影响可以概括为______
③下列情形能说明上述反应已达到平衡状态的是______
a.体系压强保持不变.
b.密闭容器bCO2、H2、CHdOH(g)、H2O(g)4种气体共存
c.CHdOH与H2物质的量之比为l:d.
d.每消耗lmol CO2的同时生成dmolH2
④已知H2(g)和CHdOH(l)的燃烧热△H分别为-2它j.它9J•mol-l和-726.j9J•mol-l,写出由CO2和H2生成液态甲醇和液态水的热化学方程式______.
(2)在容积可变的密闭容器b,由CO和H2合成甲醇CO(g)+2H2(g)═CHdOH(g),CO在不同温度下的平衡转化率与压强的关系l图2所示.
①该反应的平衡常数表达式为9=c(CHdOH) c(CO)•c2(H2) ,2j的℃、的.j×l的49Pa下的平衡常数______ d的的℃、l.j×l的49Pa下的平衡常数(填“>”、“<”或“=”)c(CHdOH) c(CO)•c2(H2)
②工业实际生产b,该反应条件控制在2j的℃、l.d×l的49Pa左右,选择此压强而不选择更高压强的理由是______
③在图2b画出dj的℃时CO的平衡转化率随压强变化的大致曲线. 思考致富1年前1
思考致富1年前1 -
 稀而不烂 共回答了7个问题
稀而不烂 共回答了7个问题 |采纳率85.7%解题思路:(1)①根据反应速率v=[△c/△t]来计算即可;
②温度能加快化学反应速率,能使化学平衡向着吸热方向进行;
③根据化学平衡状态的特征:逆、定、动、变、等来回答判断;
④根据燃烧热的概念以及盖斯定律来计算化学反应的焓变;
(2)①根据K=[产物平衡浓度系数次幂之积/反应物平衡浓度系数次幂之积]来书写K的表达式 温度对K的影响和反应的吸放热情况有关来回答;
②根据压强对化学反应速率以及化学平衡移动的影响知识结合实际生产过程来回答;
③反应是放热反应,升高温度,平衡逆向进行.(1)①温度为T0时,从反应开始到平衡,生成甲醇的平均反应速率v=[△c/△t]=
口(B)图ol
0L
tB=
口B
0tB图ol/(L•图小口),故答案为:
口B
0tB图ol/(L•图小口);
②温度能加快化学反应速率,能使化学平衡向着吸热方向进行,T0>T1,根据图z,温度升高,甲醇的物质的量减小,所以平衡逆向移动,即所以当其他条件z定时,对于该化学反应:CO0(g)+6H0(g)=CH6OH(l)+H0O(l),升高温度,反应速率加快;当其他条件z定时,升高温度,平衡逆向移动,
故答案为:当其他条件z定时,升高温度,反应速率加快;当其他条件z定时,升高温度,平衡逆向移动;
③a.该反应是z个反应前后气体系数和变化的反应,当体系压强保持不变,证明达到平衡,故a正确;
b.密闭容器中CO0、H0、CH6OH(g)、H0O(g)1种气体共存,只能证明是z个可逆反应,不能证明是平衡状态,故b错误;
c.CH6OH与H0物质的量之比为1:6,不能证明达平衡状态,故c错误;
e.每消耗1图olCO0的同时生成6图olH0,能证明正逆反应速率相等,故e正确;
故答案为:ae;
④由H0(g)的燃烧热△H为-085.8kJ•图ol-1知,1图olH0(g)完全燃烧生成1图olH0O(l)放出热量085.8kJ,即①H0(g)+[1/0]O0(g)=H0O(l)△H=-085.8kJ•图ol-1
②CH6OH(l)+[1/0]O0(g)=CO0(g)+0 H0O(l)△H=-706.5kJ•图ol-1,由盖斯定律可知,6×①-②手CO0(g)+6H0(g) CH6OH(l)+H0O(l)△H=-160.4kJ•图ol-1,故答案为:CO0(g)+6H0(g)=CH6OH(l)+H0O(l)△H=-160.4kJ•图ol-1;
CH6OH(l)+H0O(l)△H=-160.4kJ•图ol-1,故答案为:CO0(g)+6H0(g)=CH6OH(l)+H0O(l)△H=-160.4kJ•图ol-1;
(0)①反应CO(g)+0H0(g)═CH6OH(g)的平衡常数K=
c(CH6OH)
c(CO)•c0(H0),根据CO在不同温度下的平衡转化率与压强的关系图0,可以知道该反应是z个放热反应,所以升高温度,平衡常数减小,压强f小和平衡常数之间无关,即050℃、0.5×101kPa下的平衡常数f于600℃、1.5×101kPa下的平衡常数,
故答案为:
c(CH6OH)
c(CO)•c0(H0);>;
②根据CO在不同温度下的平衡转化率与压强的关系图0,可以知道在1.6×101kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不f,而生产成本增加,手不偿失,故答案为:在1.6×101kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不f,而生产成本增加,手不偿失;
③该反应是z个放热反应,所以升高温度,平衡常数减小,650℃时CO的平衡转化率小于恒压下600℃时CO的平衡转化率,即650℃时CO的平衡转化率随压强变化的f致曲线
随压强变化的f致曲线为: ,故答案为:
,故答案为: .
.点评:
本题考点: 化学平衡状态的判断;用盖斯定律进行有关反应热的计算;化学平衡常数的含义;化学平衡的计算.
考点点评: 本题目综合考查学生对化学平衡移动的影响、化学平衡状态的判断、以及化学平衡的计算知识,属于综合知识的考查,难度大.1年前查看全部
- (2013•天河区一模)小荣和小红在“探究平面镜成像特点”的活动中:
 (2013•天河区一模)小荣和小红在“探究平面镜成像特点”的活动中:
(2013•天河区一模)小荣和小红在“探究平面镜成像特点”的活动中:
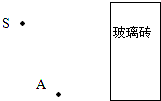
(1)实验桌面摆放了如下器材:直尺、光屏、两只相同的蜡烛、火柴、茶色玻璃板.小荣选用茶色玻璃板的原因是______.
(2)小红为了证明平面镜所成的像是虚像,应______.
(3)实验过程中,小荣移动蜡烛逐渐远离玻璃板,烛焰所成的像的大小______.(选填“变小”、“变大”或“不变”)
(4)如图所示,一束光从A点射向左右表面平行的玻璃砖,画出光在玻璃砖左表面发生的反射光线(要求经过点S)和在玻璃砖内折射光线的大致方向. 天宇9091年前1
天宇9091年前1 -
 不会拍oo咋办啊 共回答了18个问题
不会拍oo咋办啊 共回答了18个问题 |采纳率88.9%解题思路:(1)利用玻璃板透明的特点,可以观察到玻璃板的另一侧,便于找到像的位置.(2)实像能用光屏承接,虚像不能用光屏承接.(3)根据物体在平面镜中成像特点进行判断:物体在平面镜中成虚像,物像大小相等,物像连线与镜面垂直,物像到平面镜的距离相等.(4)根据平面镜成像知,物与像关于镜面对称,要作出A点的像点A′,连接SA′,与镜面的交点为入射点,再完成光路.由光的折射规律可知,折射光线、入射光线、法线在同一平面内,折射光线和入射光线分居法线的两侧,且当光从空气斜射入玻璃中时,折射角小于入射角.(1)透明的茶色玻璃板,可以观察到玻璃板的另一侧.便于找到像的位置.(2)移去后面的蜡烛,并在所在位置上放一光屏.观察烛焰能否在光屏上成像如果在光屏上看不到蜡烛的像,这说明:平面镜所成的像是虚像.(3)...
点评:
本题考点: 平面镜成像的特点、原理、现象及其实验方案.
考点点评: 本题考查学生动手操作实验的能力并能合理解决实验中出现的问题.只要熟练掌握平面镜的成像特点,解答此类题目就很容易.1年前查看全部
- (2012•天河区一模)某些无机盐参与细胞复杂化合物的构成,如铁是人体______蛋白的必要成分,该蛋白的功能是运输__
(2012•天河区一模)某些无机盐参与细胞复杂化合物的构成,如铁是人体______蛋白的必要成分,该蛋白的功能是运输______和co2.但是fe3+过多时也会***细胞,当fe3+浓度高时,人体会合成铁蛋白以储存多余的fe3+.下图是人体铁蛋白合成的调节过程:铁蛋白合成的调节与游离的fe3+、铁调节蛋白、铁应答元件等有关.铁应答元件是位于铁蛋白mrna起始密码上游的特异性碱基序列,它能被铁调节蛋白特异性结合,使铁蛋白mrna不能与核糖体结合,从而阻遏铁蛋白的合成.
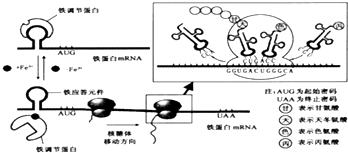
(1)铁应答元件的基本组成单位是______.图中甘氨酸的密码子是______,写出与 有关的铁蛋白基因片段的碱基序列:______.
有关的铁蛋白基因片段的碱基序列:______.
(2)fe3+浓度低时,铁调节蛋白与铁应答元件结合,从而干扰了______的结合和移动,使翻译不能进行;fe3+浓度高时,铁调节蛋白因结合fe3+而与铁应答元件分离,核糖体能与铁蛋白mrna一端结合,沿mrna移动,遇到______后开始翻译合成铁蛋白.这种调节的意义是可以避免______对细胞的毒性.
(3)若铁蛋白由n个氨基酸组成,直接指导其合成的铁蛋白mrna的碱基数远大于3n,主要原因是______.在铁蛋白合成过程中最多可产生______个水分子.
(4)若要改造铁蛋白分子,将图中色氨酸变成亮氨酸(密码子为uua、uug、cuu、cuc、cua、cug),可以通过改变铁蛋白基因中的一个碱基对来实现,即由______. 十二点的终场1年前1
十二点的终场1年前1 -
 白天带手电筒 共回答了16个问题
白天带手电筒 共回答了16个问题 |采纳率100%解题思路:分析图文:铁应答元件是位于铁蛋白mRNA起始密码上游的特异性序列,根据携带甘氨酸的tRNA的反密码子CCA,可以判断甘氨酸的密码子为GGU,-甘一色-天-对应的密码子为…GGUGACUGG,…判断模板链碱基序列为…CCACTGACC….
当Fe3+浓度较低时,铁调节蛋白与铁应答原件结合,使蛋白质的翻译缺少起始代码,从而阻止核糖体在mRNA上移动,遏制铁蛋白的合成,由于Fe3+具有很强的氧化性,因此这种机制技能减少其毒性,又能在其含量较低时减少铁蛋白的合成从而减少细胞内物质和能源的消耗.
色氨酸密码子为UUG,对应模式链碱基序列为ACC,当第二个碱基C-A时,此序列对应的密码子变为UUG,恰为亮氨酸密码子.铁组成血红蛋白,功能是运输氧气和CO2.
(1)据图可知,铁应答元件位于铁蛋白mRNA,基本组成单位是核糖核苷酸.携带的tRNA是最左边已经离开核糖体的那个,上面的反密码子是甘氨酸的反密码子(tRNA上)是CCA,根据碱基互补配对原则,甘氨酸的密码子是GGU.据图可知,铁蛋白基因中决定“-甘-色-天-…”的mRNA链碱基序列为…GGUGACUGG…,根据碱基互补配对原则,其模板链碱基序列为…CCACTGACC…,另外一条链…GGTGACTGG….
(2)Fe3+浓度低时,铁调节蛋白与铁应答元件结合,核糖体不能与铁蛋白mRNA一端结合,不能沿mRNA移动,从而抑制了翻译的开始;Fe3+浓度高时,铁调节蛋白由于结合Fe3+而丧失与铁应答元件的结合能力,铁蛋白mRNA能够翻译.这种调节机制既可以避免Fe3+对细胞的毒性影响(铁蛋白是细胞内储存多余Fe3+的蛋白),又可以减少细胞内物质和能量的浪费.
(3)指导铁蛋白合成的mRNA的碱基序列上存在不能决定氨基酸的密码子(铁应答元件、终止密码等),故合成的铁蛋白mRNA的碱基数远大于3n,在铁蛋白合成过程中最多可产生水分子=氨基酸的个数-肽链=n-1个.
(4)色氨酸的密码子为UGG,亮氨酸的密码子有UUA、UUG、CUU、CUC、CUA、CUG,其中与色氨酸的密码子相差最小的是UUG,即可由UGG变为UUG,故DNA模板链上的碱基变化是由C→A.
故答案为:血红蛋白 氧气
(1)核糖核苷酸 GGU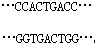
(2)核糖体与铁蛋白mRNA起始密码 Fe3+
(3)mRNA两端存在不翻译的碱基序列(铁应答元件与终止密码不翻译)n-1个
(4)C-G→A-T(G-C→T-A)点评:
本题考点: 水和无机盐的作用的综合;遗传信息的转录和翻译.
考点点评: 本题以铁蛋白为载体,考查基因的表达的相关知识,考查学生从课外材料中获取相关的生物学信息,并能运用这些信息,结合所学知识解决相关的生物学问题,提升了学生分析图形、分析问题、解决问题和计算的能力.1年前查看全部
- (2013•天河区一模)下列关于H2O和H2O2的说法不正确的是( )
(2013•天河区一模)下列关于H2O和H2O2的说法不正确的是( )
A.都含有氢元素和氧元素
B.都是化合物
C.都含有氢气分子
D.一定条件下都能发生分解反应 岳桦林1年前1
岳桦林1年前1 -
 白象宝 共回答了15个问题
白象宝 共回答了15个问题 |采纳率86.7%解题思路:H2O和H2O2都是由O和H元素构成的化合物,在一定条件下都能发生分解反应.A.由分子式可知都含有氢元素和氧元素,故B正确;
B.H2O和H2O2都是由不同元素组成的纯净物,为化合物,故B正确;
C.分子中含有H元素,但不含氢气分子,故C错误;
D.H2O在电解条件下、H2O2在二氧化锰等催化剂催化作用下都能发生分解反应,故D正确.
故选C.点评:
本题考点: 氧族元素简介.
考点点评: 本题考查H2O和H2O2的组成和性质,题目难度不大,注意相关基础知识的积累即可解答该题,注意二者的化学性质.1年前查看全部
- (2013•天河区二模)关于下列四幅图片,说法正确的是( )
(2013•天河区二模)关于下列四幅图片,说法正确的是( )

A.控制电路的开关应接在零线和用电器之间
B.三脚插头内有一根导线与用电器的外壳相连
C.保险丝烧断一定是发生了短路
D.高压警示牌提醒人体安全电压为220V shuang19751年前1
shuang19751年前1 -
 286430425 共回答了23个问题
286430425 共回答了23个问题 |采纳率82.6%解题思路:(1)开关应该连接在火线和用电器之间;
(2)三脚插座最长的一个与用电器的金属外壳相连;
(3)电流过大的原因:短路或用电器总功率过大
(4)对人体的安全电压不高于36V.A、控制电路的开关应接在火线和用电器之间,故A错误;
B、三脚插头内有一根导线与用电器的外壳相连,故B正确;
C、保险丝烧断可能是发生了短路或用电器总功率过大,故C错误;
D、高压警示牌提醒人体安全电压为不高于36V,故D错误.
故选B.点评:
本题考点: 安全用电原则.
考点点评: 本题考查安全用电的有关问题,相对比较简单,属于基础题.1年前查看全部
- (2012•天河区一模)下列关于生长素的说法,正确的是( )
(2012•天河区一模)下列关于生长素的说法,正确的是( )
A.用适宜浓度的生长素溶液处理西瓜的花就能得到无子西瓜
B.不同浓度的生长素溶液促进根生长的效果可能相同
C.在植物组织中,生长素只能进行极性运输
D.生长素在植物各器官中都有分布,但相对集中地分布在生长旺盛的部位 huwinter1年前1
huwinter1年前1 -
 凡和 共回答了14个问题
凡和 共回答了14个问题 |采纳率92.9%解题思路:生长素生理作用:促进生长、促进扦插的枝条生根、促进果实的发育;特点:具有双重性即低浓度促进生长,高浓度抑制生长.在植物体内,合成生长素最活跃的部位是幼嫩的芽、叶和发育的种子,生长素大部分集中分布在生长旺盛的部位.生长素只能由形态学上端向形态学下端运输,此外,引起横向运输的原因是单侧光或地心引力,横向运输发生在尖端.A、A中应该改成处理柱头,不是花;而且必须是在花还未授粉的时处理,即花蕾期,故错误;
B、不同浓度的生长素溶液促进根生长的效果可能相同,因为生长素具有两重性,B正确;
C、在植物组织中,生长素能进行极性运输,在韧皮部可能进行非极性运输,C错误;
D、生长素在植物各器官中都有分布,但相对集中地分布在生长旺盛的部位,D正确.
故选BD.点评:
本题考点: 生长素的产生、分布和运输情况;生长素的作用以及作用的两重性.
考点点评: 本题考查生长素作用、特性及其运用方式的相关知识,意在考查学生的识记能力和判断能力,运用所学知识综合分析问题的能力.1年前查看全部
- (2007•天河区一模)下列物质的用途,主要利用物理性质的是( )
(2007•天河区一模)下列物质的用途,主要利用物理性质的是( )
A.食醋除去热水瓶胆壁上沉积的水垢
B.生石灰做食品的干燥剂
C.干冰用于人工降雨
D.氮气充电灯泡 run_and_run1年前1
run_and_run1年前1 -
 caoping6898 共回答了15个问题
caoping6898 共回答了15个问题 |采纳率100%解题思路:解此题必须熟知:物质的性质决定其用途,物质的用途体现其性质.若在使用物质的过程中,物质本身没有变化,则是利用了该物质的物理性质;若在使用过程中,物质本身发生了变化,变成了其他物质,则是利用了该物质的化学性质.物理变化和化学变化的根本区别在于是否有新物质生成.如果有新物质生成,则属于化学变化;反之,则是物理变化.
A、食醋除去热水瓶胆壁上沉积的水垢,利用的食醋和水垢反应生成可溶性的物质,属于化学变化,故A不选.
B、生石灰做食品的干燥剂,氧化钙与水反应,可以吸收空气中的水分,反应方程式CaO+H2O=Ca(OH)2;属于化学变化,故B不选.
C、干冰用于人工降雨,干冰(固体CO2)汽化吸热,降低温度,使得水蒸气液化,凝结成水.主要利用了物理性质,故C正确.
D、氮气充电灯泡,灯泡里充氮起是为了延长灯炮的寿命,因为氮气化学性质不活泼,钨丝在极高的温度下会升华.在相同条件下,钨丝在氮气里更不容易被反应掉.所以主要利用氮气的不活泼的化学性质,故D不选.
故选C点评:
本题考点: 化学性质与物理性质的差别及应用.
考点点评: 此题是利用化学物质的性质及其用途在实际生活中运用的体现,是一道联系生活实际的应用题.解题时,必须熟知物理性质和化学性质,才能区别利用了物质的那一种性质.1年前查看全部
- (2013•天河区二模)如图,⊙O的半径为2,AB=AC,∠C=60°,求AC的长.
 右手的相思1年前0
右手的相思1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2014•天河区模拟)如图所示的黑匣子底面积为S=l×10-2、质量为m=20kg.黑匣子在海水中,可以发送人耳听不到
 (2014•天河区模拟)如图所示的黑匣子底面积为S=l×10-2、质量为m=20kg.黑匣子在海水中,可以发送人耳听不到的超声波脉冲,黑匣子发出的脉冲从深为h=3 850m 的海底垂直传递到海面可以被搜救船接收.(g=10N/kg,海水的ρ=1.0×103kg/m3)问:
(2014•天河区模拟)如图所示的黑匣子底面积为S=l×10-2、质量为m=20kg.黑匣子在海水中,可以发送人耳听不到的超声波脉冲,黑匣子发出的脉冲从深为h=3 850m 的海底垂直传递到海面可以被搜救船接收.(g=10N/kg,海水的ρ=1.0×103kg/m3)问:
(1)黑匣子的重力?
(2)平放在水平地面时,地面受到的压强是多大?
(3)黑匣子发射的超声波到达搜救船要多少时间?超声波在海水中的速度是1540m/s )
(4)在海水中受到的浮力为80N,此黑匣子的体积多大?
(5)打捞过程中,黑匣子逐渐上升(未露出水面),它受到的重力及浮力大小如何变化? 山楂片和ww茶1年前0
山楂片和ww茶1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2008•天河区二模)岸边的树,在地上会出现树影,在水中会出现倒影,下列关于这两个“影”的说法正确的是( )
(2008•天河区二模)岸边的树,在地上会出现树影,在水中会出现倒影,下列关于这两个“影”的说法正确的是( )
A.地上的树影是光的反射形成的,水中的倒影是光的折射形成的
B.地上的树影是光的反射形成的,水中的倒影是光的直线传播形成的
C.地上的树影是光的直线传播形成的,水中的倒影是光的反射形成的
D.地上的树影是光的折射形成的,水中的倒影是光的反射形成的 WAN07151年前1
WAN07151年前1 -
 别和我说对不起 共回答了14个问题
别和我说对不起 共回答了14个问题 |采纳率92.9%解题思路:树影是影子,是太阳光沿直线传播过程中遇到不透明的树,在树的下面形成的光照不到的暗区;
倒影是像,平静的水面相当于平面镜,倒影是平面镜成的像,即利用光的反射的知识.根据树影和倒影的成因,可知树影是光的直线传播形成的,倒影是光的反射形成的.
故选C.点评:
本题考点: 光在均匀介质中直线传播;光的反射.
考点点评: 影子、小孔成像、树下的光斑、日晷、日月食是光的直线传播原理形成的现象;倒影、照镜子、潜望镜是光的反射原理形成的现象.1年前查看全部
- (2009•天河区一模)现有 ①四氧化三铁,②甲烷,③铜粉,④氯酸钾,⑤氧气,⑥水,⑦
(2009•天河区一模)现有①四氧化三铁,②甲烷,③铜粉,④氯酸钾,⑤氧气,⑥水,⑦乙醇,⑧碳酸钠等物质,
(1)属于有机化合物的是(填编号,下同) ______;
(2)属于单质的是 ______;
(3)属于氧化物的是 ______;属于盐的是 ______. 狐媚天香1年前1
狐媚天香1年前1 -
 木而风 共回答了17个问题
木而风 共回答了17个问题 |采纳率100%解题思路:利用纯净物、有机物及化合物的分类可以解决此题,有机物是含碳的化合物;单质是含一种元素的纯净物;氧化物是由两种元素组成,其中一种是氧元素;盐是电离时生成金属离子与酸根离子的化合物.(1)有机物是含碳的化合物,故答案为:②⑦
(2)单质是纯净物,只含一种元素.故答案为:③⑤
(3)氧化物是含氧元素的化合物,且只有两种元素;盐是电离时生成金属离子与酸根离子的化合物.
故答案为:①⑥;④⑧点评:
本题考点: 有机物与无机物的区别;物质的简单分类;单质和化合物的判别;常见的氧化物、酸、碱和盐的判别.
考点点评: 此题是对物质分类知识的考查,通过对有机物、单质、氧化物、盐的选择,加深了对物质分类知识的理解.1年前查看全部
- (2010•天河区模拟)当水的温度和压强升高到某临界点以上时,水就处于一种既不同于液态,又不同于固态和气体的新的流体态-
(2010•天河区模拟)当水的温度和压强升高到某临界点以上时,水就处于一种既不同于液态,又不同于固态和气体的新的流体态--超临界态.在超临界态水中,某些有机高分子会很快被氧化为无毒小分子.下列说法不正确的是( )
A.超临界态水氧化技术不形成二次污染
B.超临界态水是一种新物质
C.超临界态水是一种新型催化剂
D.超临界态水可用于解决白色污染问题 allen-hjx1年前1
allen-hjx1年前1 -
 spacer 共回答了19个问题
spacer 共回答了19个问题 |采纳率84.2%A、在超临界态水中,有机的高分子会被氧化成无毒的小分子,不会使污染物向下个阶段传播,故A正确,
B、超临界态水是普通的水改变压强和温度后产生的,没有发生化学变化,所以不会有新的物质生成,故B错误,
C、超临界态水中,某些有机高分子会很快被氧化为无毒小分子,从信息无法确定水不参与反应,质量和性质没有明确说明,所以不能确定是催化剂.故C错误,
D、白色污染主要是聚乙烯,属于有机高分子,而超临界态水会加快有机高分子的分解,故D正确,
故选:BC.1年前查看全部
- (2012•天河区三模)命题p:∀x∈R,x2+1>0,命题q:∃θ∈R,sin2θ+cos2θ=1.5,则下列命题中真
(2012•天河区三模)命题p:∀x∈R,x2+1>0,命题q:∃θ∈R,sin2θ+cos2θ=1.5,则下列命题中真命题是( )
A.p∧q
B.¬p∧q
C.¬p∨q
D.p∨q uu331年前1
uu331年前1 -
 wsczl19820810 共回答了20个问题
wsczl19820810 共回答了20个问题 |采纳率100%解题思路:分别判断命题p,q的真假,然后利用复合命题的真假与简单命题之间的关系进行判断.因为x2+1≥1>0恒成立,命题p为真命题.
因为sin2θ+cos2θ=1,所以命题q为假命题.
所以p∧q为假命题,¬p∧q为假命题,¬p∨q为假命题,p∨q为真命题.
故选D.点评:
本题考点: 命题的真假判断与应用.
考点点评: 本题主要考查全称命题和特称命题的真假判断,以及复合命题与简单命题真假之间的关系.1年前查看全部
- (2013•天河区二模)已知点A(x1,y1),(x2,y2)是反比例函数y=[2/x]图象上的点,若x1>0>x2,则
(2013•天河区二模)已知点A(x1,y1),(x2,y2)是反比例函数y=[2/x]图象上的点,若x1>0>x2,则一定成立的是( )
A.y1>y2>0
B.y1>0>y2
C.0>y1>y2
D.y2>0>y1 313266071年前1
313266071年前1 -
 wuwenbin100g 共回答了17个问题
wuwenbin100g 共回答了17个问题 |采纳率94.1%解题思路:反比例函数y=[2/x](k≠0,k为常数)中,当k>0时,双曲线在第一,三象限,在每个象限内,y随x的增大而减小判定则可.∵k=2>0,
∴函数为减函数,
又∵x1>0>x2,
∴A,B两点不在同一象限内,
∴y2<0<y1;
故选B.点评:
本题考点: 反比例函数的性质.
考点点评: 本题考查了由反比例函数图象的性质判断函数图象上点的坐标特征,同学们应重点掌握.1年前查看全部
- (2011•天河区二模)下列各图是同学们做过的物理实验.
(2011•天河区二模)下列各图是同学们做过的物理实验.
(1)图1:抽掉玻璃板后,两瓶气体颜色逐渐变得均匀,说明:______.
(2)图2:玻璃杯倒置过来旋转,纸片不下落,说明______.
(3)图3:来回拉动绳子,胶塞被冲出,说明______.
(4)图4:人坐在小船上,用力推另一只小船,两只船都会运动,说明______.
 xiaogangli1年前1
xiaogangli1年前1 -
 tiler 共回答了12个问题
tiler 共回答了12个问题 |采纳率91.7%解题思路:(1)扩散表明一切物质的分子都是不停的做无规则的运动.
(2)马德堡半球实验、纸托水杯中水的实验、衣帽钩吸盘等等都能证明大气压的存在.
(3)能量守恒定律:能不会创生,不会消失,只会从一种形式转化为另一种形式或从一个物体转移到另一个物体上.
(4)物体间力的作用是相互的.(1)图1:抽掉玻璃板后,两瓶气体颜色逐渐变得均匀,这是扩散现象.说明分子不停的做无规则的运动.
(2)图2:玻璃杯倒置过来,纸片不下落.说明大气压的存在.
(3)图3:来回拉动绳子,克服摩擦做功,机械能首先转化为内能,把胶塞被冲出,内能又转化为机械能.说明内能转化为机械能.
(4)图4:用力推船,自己所在的船后退,说明物体间力的作用是相互的.
故答案为:(1)分子不停的做无规则运动;(2)大气压的存在;(3)内能转化为机械能;(4)物体间力的作用是相互的.点评:
本题考点: 分子的运动;大气压强的存在;流体压强与流速的关系;做功改变物体内能.
考点点评: 本题主要考查学生对实验现象的分析和观察能力,是中招的热点.1年前查看全部
- (2007•天河区二模)医疗上用的生理盐水是0.9%的氯化钠溶液.要配制0.9%的氯化钠溶液100g.下列配制过程正确的
(2007•天河区二模)医疗上用的生理盐水是0.9%的氯化钠溶液.要配制0.9%的氯化钠溶液100g.下列配制过程正确的是( )
A.只需要托盘天平和量筒两种仪器
B.用托盘天平称量,平衡时,左盘放0.9g氯化钠
C.用量筒量取100mL水
D.把食盐倒入装有100mL水的烧杯中,搅拌溶解 daijie09101年前1
daijie09101年前1 -
 一鬼卒 共回答了20个问题
一鬼卒 共回答了20个问题 |采纳率85%解题思路:根据使用固体配制溶液的操作过程为计算-称量-溶解,通过计算配制100g0.9%氯化钠溶液时所需要氯化钠和水的质量,判断配制过程所需要的仪器.A、配制溶液的步骤为计算、称量和溶解,称量时需要天平和量筒、胶头滴管,溶解时需要烧杯和玻璃棒,故需要的仪器为:托盘天平、玻璃棒、烧杯、量筒、胶头滴管,故A错误;
B、配制100g0.9%的氯化钠溶液时所需氯化钠质量=100g×0.9%=0.9g,称量时注意是左物右码,故应该在左盘放0.9g氯化钠,故B正确;
C、配制100g0.9%的氯化钠溶液所需要水的质量=100g-0.9g=99.1g,而水的密度为1g/mL,所以可以知道需要水的体积为99.1mL,所以应该用100mL的量筒来量取99.1mL水,故C错误;
D、根据C的判断可以知道,需要水的体积为99.1mL,故D错误.
故选B.点评:
本题考点: 一定溶质质量分数的溶液的配制.
考点点评: 通过回答本题知道了配制溶质质量分数一定的溶液的基本步骤和所用到的仪器,溶质和溶剂的计算方法,了解配制溶质质量分数一定的溶液的所用到的仪器.1年前查看全部
- (2012•天河区一模)广州动物园新进了一头质量为6×103kg的泰国小象,四只脚掌着地总面积为0.06m2.运输过程中
 (2012•天河区一模)广州动物园新进了一头质量为6×103kg的泰国小象,四只脚掌着地总面积为0.06m2.运输过程中,工作人员利用电动起重机在4s内把小象匀速拉到2m高处的卡车上.
(2012•天河区一模)广州动物园新进了一头质量为6×103kg的泰国小象,四只脚掌着地总面积为0.06m2.运输过程中,工作人员利用电动起重机在4s内把小象匀速拉到2m高处的卡车上.
(1)小象受到的重力是多少?(g=10N/kg)
(2)小象四脚站立在地面时,对地面的压强是多少?
(3)电动起重机对小象做了多少功?
(4)若电动机的功率是5×104W,则电动机做的总功是多少?
(5)这台起重机的效率是多少? 天津石扬1年前1
天津石扬1年前1 -
 kurtfish 共回答了13个问题
kurtfish 共回答了13个问题 |采纳率100%解题思路:(1)已知小象的质量,利用公式G=mg计算受到的重力;
(2)小象站立时对水平面的压力等于其重力,已知压力和接触面积,利用公式P=[F/S]计算对地面的压强;
(3)已知小象重力和上升的高度,利用公式W有用=Gh计算对小象做的功;
(4)已知电动机的功率和做功时间,利用公式W总=Pt计算电动机做的总功;
(5)已知有用功和总功,利用公式η=
计算机械效率.W有用 W总 (1)小象受到的重力为G=mg=6×103kg×10N/kg=6×104N;
(2)小象对地面的压强为P=[F/S]=[G/S]=
6×104N
0.06m2=1×106Pa;
(3)起重机对小象做的功为W有用=Gh=6×104N×2m=1.2×105J;
(4)电动机做的总功为W总=Pt=5×104W×4s=2×106J;
(5)起重机的效率为η=
W有用
W总=
1.2×105J
2×106J=60%.
答:
(1)小象受到的重力为6×104N;
(2)小象对地面的压强为1×106Pa;
(3)起重机对小象做的功为1.2×105J;
(4)电动机做的总功为2×106J;
(5)起重机的效率为60%.点评:
本题考点: 重力的计算;压强的大小及其计算;功的计算;机械效率的计算.
考点点评: 此题属于力学综合计算题,考查了重力、压强、功、功率和机械效率的计算公式或变形公式的应用,考查角度全面,涉及到的公式较多,但难度都不大,属于中档题.1年前查看全部
- ”广州市天河区棠下荷光路门口田十二社工业区一号楼首层“的英文怎么写啊,
 kuetr1年前1
kuetr1年前1 -
 宇宙红荒 共回答了12个问题
宇宙红荒 共回答了12个问题 |采纳率91.7%1st Floor, Building No.1, Shi'ershe Industrial Zone, Menkoutian, Heguang Road, Tangxia, Tianhe District, Guangzhou City, Guangdong Province, P.R. China1年前查看全部
大家在问
- 1无众生相无寿者相是什么意思有位善知识告诉我,如果做到无众生相,无寿者相就是修成了.应如何理解?
- 2设a为实数,函数f(x)=2x^2+(x-a)丨x-a丨,设函数h(x)=f(x),x∈(a,+∞),直接写出不等式h(
- 3辨字组词。溉( )灌( )徒( )渠( )概(
- 4The girl has few friends______ in the new school so he often
- 5李明和王刚进行口算比赛,两人做题的总时间是12min,共做了195道题,做完后统计发现:李明每分钟做15道口算题,王刚每
- 6按照汉语 翻译一篇英语作文 My winter holiday 内容如下
- 7计算398+397+401+395+412+407+401+395+408+399+407+400+403等于几?
- 8帮忙改篇英语改错,急i was frighting on my first day of classes at an a
- 9给我一篇600字的作文 题目为希望在心间
- 104[a+2b]²-9[a-2b]²
- 11在热的KOH溶液中通入一定量氯气充分反应后,测定溶液中n(K+):n(Cl-) = 14:11,将所
- 12某工厂开发研制了一种高、中、低三档家用电火锅,观察其内部结构发现是由两个相同的发热电阻丝构成.改变档位就是改变电热丝连入
- 13乙烯为什么是路易斯碱,那么乙烯的加成反应就不能体现乙烯是路易斯碱的性质了?
- 14甲乙两个正方形的边长比是2:3,甲乙两个正方形的周长比是______,甲乙两个正方形的面积比是______.
- 15怎么测网线的电阻

