(2009•端州区模拟)某化学活动小组以“酸碱盐的性质”为主题,进行探究学习,请你作为该小组成员来解决下列问题:
 irks2022-10-04 11:39:541条回答
irks2022-10-04 11:39:541条回答(1)小刚同学说:“酸溶液呈酸性,碱溶液呈碱性,则盐溶液一定呈中性”.你认为这种推理______(填“正确”或“不正确”).
(2)小丽同学从某一欠收农田里取回一份土壤样品,请你用两种不同的方法帮小丽测出该土壤样品浸出液的酸碱性(只写出所用试剂的名称即可):①______;②______.
如果检测的结果呈酸性,那么要改良此土壤,应该向农田里施加______.
(3)在不提供指示剂的情况下,若要除去氯化钙溶液中混有的少量稀盐酸,你所选择的试剂是______.
A.生石灰B.熟石灰C.石灰石D.纯碱固体
写出该反应的化学方程式:______.

已提交,审核后显示!提交回复
共1条回复
 adew 共回答了15个问题
adew 共回答了15个问题 |采纳率93.3%- 解题思路:本题是探究酸碱盐的性质及根据性质来除杂.
(1)正确区分酸碱盐和酸碱性.
(2)根据试剂所呈的不同颜色来确定溶液的酸碱性;酸性土壤要改良需加入能与酸反应的物质,来降低酸性.
(3)除杂主要是利用盐酸的化学性质,但要遵循除杂的原则,不能引入新的杂质,本题还要求有清晰可见的现象,所以有气体或沉淀或颜色变化是首选的.(1)酸性、碱性溶液不一定是酸液、碱液,也有可能是盐溶液,如Na2CO3、K2CO3的水溶液呈碱性.
(2)酸碱指示剂及pH试纸都可判断土壤的酸碱性.改良酸性土壤一般加易得的熟石灰或生石灰.
(3)除去CaCl2溶液中混有的少量稀盐酸,加石灰石反应有气体生成,现象明显且不引入杂质,当过量时碳酸钙不溶于水,而其它三项如果过量就会使溶液呈碱性.
故答案为:(1)不正确;(2):①pH试纸;②紫色石蕊试液.熟石灰或生石灰.
(3)C; CaCO3+2HCl=CaCl2+H2O+CO2↑.点评:
本题考点: 溶液的酸碱性测定;酸的化学性质;中和反应及其应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查酸碱盐的性质及利用性质除去物质中混有的杂质,是常见习题,考查学生考虑问题的全面性,尤其注意在除杂时不要引入新的杂质. - 1年前
相关推荐
- (2009•端州区模拟)用化学符号填空.
 (2009•端州区模拟)用化学符号填空.
(2009•端州区模拟)用化学符号填空.
(1)用化学符号表示:2个氢原子______;氯化镁中镁元素的化合价为+2价的
Cl2+2 Mg .
Cl2+2 Mg
(2)右图是元素周期表中的一种元素.①则该元素相对原子质量是______.②该元素的微粒结构示意图为 ,则该元素原子的最外层电子数为______.
,则该元素原子的最外层电子数为______.  mkaixx1年前1
mkaixx1年前1 -
 xfqxtck 共回答了17个问题
xfqxtck 共回答了17个问题 |采纳率88.2%(1)根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字. 2个氢原子表示为:2H;
根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氯化镁中镁元素的化合价为+2价表示为:
+2
MgCl2;故答案为:2H;
+2
MgCl2 ;
(2)根据元素周期表中的元素信息可知,该元素相对原子质量是40.08;
由微粒结构示意图可知,该元素原子的最外层电子数为:20-18=2;
故答案为:40.08; 2.1年前查看全部
- (2009•端州区模拟)用化学符号填空.
 (2009•端州区模拟)用化学符号填空.
(2009•端州区模拟)用化学符号填空.
(1)用化学符号表示:2个氢原子2H2H;氯化镁中镁元素的化合价为+2价的
Cl2+2 Mg
Cl2.+2 Mg
(2)右图是元素周期表中的一种元素.①则该元素相对原子质量是40.0840.08.②该元素的微粒结构示意图为 ,则该元素原子的最外层电子数为22.
,则该元素原子的最外层电子数为22.  restle1年前1
restle1年前1 -
 laifengxiaoxiao 共回答了11个问题
laifengxiaoxiao 共回答了11个问题 |采纳率100%(1)根据原子的表示方法:用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字. 2个氢原子表示为:2H;
根据元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,因此氯化镁中镁元素的化合价为+2价表示为:
+2
MgCl2;故答案为:2H;
+2
MgCl2 ;
(2)根据元素周期表中的元素信息可知,该元素相对原子质量是40.08;
由微粒结构示意图可知,该元素原子的最外层电子数为:20-18=2;
故答案为:40.08; 2.1年前查看全部
- (2009•端州区模拟)在我们的日常生活中,出现了含氟牙膏、高钙牛奶、加碘食盐、增铁酱油、富硒茶叶等商品,这些商品中的氟
(2009•端州区模拟)在我们的日常生活中,出现了含氟牙膏、高钙牛奶、加碘食盐、增铁酱油、富硒茶叶等商品,这些商品中的氟、钙、碘、铁、硒应理解为( )
A.元素
B.分子
C.单质
D.原子 liq2161年前1
liq2161年前1 -
 爱情是个P520 共回答了19个问题
爱情是个P520 共回答了19个问题 |采纳率94.7%解题思路:物质组成中涉及到的含氟、补铁等说法,都是关注物质的组成元素,而与该元素具体的存在形态无关,所以都是指元素.含氟牙膏、高钙牛奶、加碘食盐、增铁酱油、富硒茶叶等商品,这些商品中所强调的氟、钙、碘、铁、硒,都是说明这些物质的存在,而不关注以什么形式存在,或者便于说明如何存在,所以就用宏观的元素种类来说明.因此理解为元素.
故选A.点评:
本题考点: 元素的概念.
考点点评: 一般商品标注都是说明物质的组成元素的,而不是强调分子还是原子甚至离子的具体存在形式.1年前查看全部
- (2009•端州区模拟)右图为NH4Cl和NaCl的溶解度曲线图,请回答:
 (2009•端州区模拟)右图为NH4Cl和NaCl的溶解度曲线图,请回答:
(2009•端州区模拟)右图为NH4Cl和NaCl的溶解度曲线图,请回答:
(1)20℃时,NaCl物质的溶解度是______.
(2)______℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等. 我是影子丢丢1年前1
我是影子丢丢1年前1 -
 yl_bz5 共回答了16个问题
yl_bz5 共回答了16个问题 |采纳率81.3%解题思路:(1)根据由固体物质的溶解度曲线可以出某物质在某温度下的溶解度的大小,据此来解答即可;
(2)两种物质的饱和溶液溶质质量分数相等,则说明两种溶液的溶解度相等;根据溶解度曲线,找出曲线的交点即为溶解度相等的点,此时对应的温度即为质量分数相等时的温度.(1)由NaCl的溶解度曲线可知:在20℃时,NaCl物质的溶解度是36g;
(2)因为NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等;
所以,NH4Cl和NaCl这两种物质的溶解度相等;
由NH4Cl和NaCl的溶解度曲线可知:在t℃时,NH4Cl和NaCl的溶解度相等;
故t℃时,NH4Cl饱和溶液和NaCl饱和溶液溶质质量分数相等.
故答案为:
(1)36g;
(2)t.点评:
本题考点: 固体溶解度曲线及其作用.
考点点评: 本题主要考查了固体溶解度曲线所表示的意义,并根据溶解度曲线解决相关的问题;对于饱和溶液的溶质质量分数可以根据[溶解度/100g+溶解度]×100%来计算.1年前查看全部
- (2009•端州区模拟)下列食品中蛋白质含量最高的是( )
(2009•端州区模拟)下列食品中蛋白质含量最高的是( )
A.米饭
B.黄瓜子
C.虾
D.面条 打_zz_日_本_人1年前1
打_zz_日_本_人1年前1 -
 无语蝶飞 共回答了18个问题
无语蝶飞 共回答了18个问题 |采纳率88.9%解题思路:动物产品一般比植物产品中蛋白质的含量高.米饭、黄瓜子和面条都是植物产品;
虾是动物产品;
动物产品一般比植物产品中蛋白质的含量高.
故选C.点评:
本题考点: 生命活动与六大营养素.
考点点评: 本题主要考查动植物产品中蛋白质的含量,难度较小.1年前查看全部
- (2009•端州区模拟)下图分别表示四种化学实验操作,其中没有错误的是( )
(2009•端州区模拟)下图分别表示四种化学实验操作,其中没有错误的是( )
A.稀释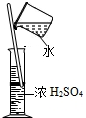
B.
读数
C.
称量
D.
溶解 winhph1年前1
winhph1年前1 -
 爱陈好 共回答了20个问题
爱陈好 共回答了20个问题 |采纳率90%解题思路:A、量筒不能作为反应容器,更不能稀释浓硫酸,会引起受热不均,引起炸裂;稀释浓硫酸,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌;
B、量取液体时,视线与液体的凹液面最低处保持水平;
C、氢氧化钠溶液是强碱,具有很强的腐蚀性,应放在玻璃器皿中盛放;
D、溶解操作中要用玻璃棒加快溶解.A、图中错误两处:量筒不能作为反应容器,水不能倒入浓硫酸,故A错误;
B、量取液体时,视线与液体的凹液面最低处保持水平,图中操作正确,故B正确;
C、氢氧化钠溶液是强碱,具有很强的腐蚀性,不能放在纸片上,应放玻璃器皿中,图中操作错误,故C错误;
D、溶解操作中要用到烧杯和玻璃棒,其中玻璃棒用于搅拌,可加快物质的溶解,不可摇动烧杯加快溶解,会使液体溅出,故图中操作错误.
故选B.点评:
本题考点: 实验操作注意事项的探究;测量容器-量筒;称量器-托盘天平;浓硫酸的性质及浓硫酸的稀释;一定溶质质量分数的溶液的配制.
考点点评: 了解具备基本的化学实验技能是学习化学和进行化学探究活动的基础和保证.只有掌握化学实验的基本技能,才能安全、准确地进行化学实验.1年前查看全部
- (2009•端州区模拟)通过近一年的化学学习,你已经掌握了实验室制取气体和气体跟固体反应的有关规律,请结合下图回答问题:
(2009•端州区模拟)通过近一年的化学学习,你已经掌握了实验室制取气体和气体跟固体反应的有关规律,请结合下图回答问题:

(1)写出图中标号仪器的名称①______;②______.
(2)实验室制取氧气的一个化学方程式是2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3.根据该反应原理我选用制取氧气的发生装置是______(填装置字母代号).若用G收集氧气,气体应从______ 进入(填接口字母)
2KCl+3O2↑MnO2 .△
(3)若用大理石和浓盐酸反应制取一瓶纯净干燥的二氧化碳,你选择的装置(按排列顺序填写装置字母代号)B接F接______接C,其中F装置的作用是______;
(4)该兴趣小组查资料得知:亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取SO2,同时生成硫酸钠和水;常温下SO2是无色有刺激性气味的气体,它的密度比空气大,可溶于水生成亚硫酸(H2SO3),H2SO3能使湿润的pH试纸变红.请回答:
制取二氧化硫,你选择的反应发生装置是______(填代码);检验SO2是否已收集满的操作方法是:______. 潇洒游鹰1年前1
潇洒游鹰1年前1 -
 l888888880 共回答了17个问题
l888888880 共回答了17个问题 |采纳率100%解题思路:(1)熟悉常见仪器的图形、名称、用途;
(2)回顾制取氧气的原理,写出其中的一个方程式,根据反应物的状态和反应条件确定发生装置;用G收集氧气,根据氧气和水的密度关系,分析进气口;
(3)根据大理石和浓盐酸反应的二氧化碳中混有的杂质,分析若要制取一瓶纯净干燥的二氧化碳,应除掉的杂质及装置连接顺序;
(4)根据制取二氧化硫的反应物的状态和反应条件确定反应的发生装置,根据二氧化硫的性质分析验满的方法.(1)由标号仪器的图形可知:①酒精灯,②试管;
(2)实验室可用加热氯酸钾和二氧化锰的方法制取氧气,反应的方程式是:2KClO3
MnO2
.
△2KCl+3O2↑;是加热固体制取氧气,选用制取氧气的发生装置是 A;若用G收集氧气,气体应从b 进入;
(3)用大理石和浓盐酸反应的二氧化碳中混有氯化氢气体、水,要制取一瓶纯净干燥的二氧化碳,应先除去氯化氢气体,再除去水,所以,选择的装置连接顺序是B接F接E接C,其中F装置的作用是除去氯化氢气体;
(4)亚硫酸钠(Na2SO3)固体与稀硫酸在常温下反应制取SO2,属于固液反应制取气体,反应不需加热,可选用发生装置B,因为H2SO3能使湿润的pH试纸变红,所以检验SO2是否已收集满的操作方法是:将湿润的pH试纸放入集气瓶口处,若pH试纸变红,则证明收集满了;
故答为:(1)酒精灯,试管;(2))2KClO3
MnO2
.
△2KCl+3O2↑,A,b;(3)E,除去氯化氢气体;(4)B,将湿润的pH试纸放入集气瓶口处,若pH试纸变红,则证明收集满了.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常见气体的检验与除杂方法;气体的净化(除杂);常用仪器的名称和选用;实验室制取氧气的反应原理;氧气的收集方法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查了实验室制取气体的装置,应根据气体的制取原理来组装、选配、判断或者选择气体的发生装置;再根据气体的溶解性、密度及其是否与水或者空气发生反应等来判断、选用收集装置;1年前查看全部
- (2009•端州区模拟)酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性.据此你觉得下列试剂的存
(2009•端州区模拟)酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性.据此你觉得下列试剂的存放方法正确的是( )
A.
H2SO4溶液
B.
Na2CO3溶液
C.
NaOH溶液
D.
Ca(OH)2溶液 沐流尘步怀真1年前1
沐流尘步怀真1年前1 -
 西湖处鱼 共回答了24个问题
西湖处鱼 共回答了24个问题 |采纳率100%解题思路:根据酸性溶液对橡胶制品具有较强的腐蚀作用,碱性溶液对玻璃制品也有一定的腐蚀性进行分析.A、硫酸会腐蚀橡胶塞,使橡胶塞和玻璃瓶粘在一起不易打开,故A错误;
B、碳酸钠显碱性,会腐蚀玻璃瓶塞,使两者粘在一起不易打开,故B错误;
C、碱会腐蚀玻璃,但是瓶塞是橡胶的,故C正确;
D、氢氧化钙显碱性,会腐蚀玻璃瓶塞,使两者粘在一起不易打开,故D错误;
故选C.点评:
本题考点: 碱的化学性质;酸的化学性质.
考点点评: 在解此类题时,首先分析碱性液体和酸性液体的性质,然后结合瓶中液体的酸碱性进行分析判断.1年前查看全部
- (2009•端州区模拟)下列物质在氧气中燃烧,放出耀眼的白光,并生成白色固体的是( )
(2009•端州区模拟)下列物质在氧气中燃烧,放出耀眼的白光,并生成白色固体的是( )
A.木炭
B.红磷
C.镁条
D.硫 zf7771年前1
zf7771年前1 -
 北的开端 共回答了26个问题
北的开端 共回答了26个问题 |采纳率84.6%解题思路:根据已有的知识进行分析,碳与氧气反应生成二氧化碳气体,红磷与氧气反应生成五氧化二磷白色固体,镁与氧气反应生成氧化镁白色固体,硫与氧气反应生成二氧化硫.A、碳与氧气反应生成二氧化碳气体,故A错误;
B、红磷与氧气反应生成五氧化二磷白色固体,但是反应时发出的是黄光,故B错误;
C、镁与氧气反应发出耀眼的白光,生成氧化镁白色固体,故C正确;
D、硫与氧气反应生成二氧化硫气体,故D错误;
故选C.点评:
本题考点: 氧气与碳、磷、硫、铁等物质的反应现象.
考点点评: 本题考查了常见物质与氧气反应的实验现象以及生成物的颜色和状态,完成此题,可以依据已有的知识进行,要求同学们加强实验现象的识记,以便灵活应用.1年前查看全部
- (2009•端州区模拟)请你从二氧化碳、甲烷、氢气、聚乙烯塑料、聚氯乙烯塑料、氧气中选择适当物质填空.
(2009•端州区模拟)请你从二氧化碳、甲烷、氢气、聚乙烯塑料、聚氯乙烯塑料、氧气中选择适当物质填空.
(1)可供给人类呼吸的是______.
(2)可用于食品包装的材料是______.
(3)正在推广使用、比较清洁高效的化石燃料是______. 26693321年前1
26693321年前1 -
 98朵玫瑰 共回答了20个问题
98朵玫瑰 共回答了20个问题 |采纳率95%解题思路:物质的性质决定用途,可依据物质的性质进行分析.氧气可供人呼吸,聚乙烯塑料可用于食品包装,作为燃料的物质需可燃.(1)氧气可供人呼吸;
(2)可用于包装的材料有聚乙烯塑料和聚氯乙烯塑料,其中聚乙烯塑料用于食品包装,而聚氯乙烯不能,因为聚氯乙烯有毒;
(3)氢气、甲烷都可以燃烧,故都可作为燃料,但是,氢气不是化石燃料,三大化石燃料是煤、石油、天然气.
故答案为:
(1)氧气;
(2)聚乙烯塑料;
(3)甲烷.点评:
本题考点: 氧气的用途;常用燃料的使用与其对环境的影响;塑料制品使用的安全.
考点点评: 此题考查了我们身边常见物质的用途,熟悉化学中常见物质的性质及用途,就能轻松解题.1年前查看全部
- (2009•端州区模拟)下列家庭钢铁物品防锈措施无效的是( )
(2009•端州区模拟)下列家庭钢铁物品防锈措施无效的是( )
A.菜刀上撒盐水
B.铁栅栏表面刷油漆
C.自行车链条涂油
D.保持铁锅表面干燥 天山雾风小时候1年前1
天山雾风小时候1年前1 -
 mdjjczx_sxg 共回答了18个问题
mdjjczx_sxg 共回答了18个问题 |采纳率83.3%解题思路:根据钢铁生锈的条件分析,钢铁生锈是因为与氧气和水充分接触,酸、碱、盐可以加快钢铁的锈蚀;钢铁制品常用的防锈方法是使钢铁与水和氧气隔绝.A、菜刀上撒盐水能加快菜刀的锈蚀,不能防锈;
B、铁栅栏表面刷油漆能使铁与水隔绝,可以防锈;
C、链条涂油能使铁与水隔绝,可以防锈;
D、铁锅表面保持干燥能起到防锈的作用,可以防锈;
故选A.点评:
本题考点: 金属锈蚀的条件及其防护.
考点点评: 此题是对钢铁生锈知识的考查,主要利用生锈的条件进行探讨解题,属基础性考查题.1年前查看全部
大家在问
- 1用铜钱在一根小棒上绕线圈,绕50圈时,测得铜线还余下21.2厘米,若再绕10圈,铜线差10.2厘米,这跟铜线的长度是多少
- 2计算:(a根号b+b根号a)^2-(a根号b-b根号a)^2
- 3已知M={2,a,b},N={2a,2,b²},且M=N,求a,b的值
- 4Thank you ____________ me so much help. [ &
- 5有几个问题.1.12月22日,太阳直射南回归线,则12月9日太阳直射点约位于20°S.请问这个直射点是怎么算的.2.B地
- 6用建议怎么造句?(在句子中间。)
- 7I'd全写是什么
- 81,已知a.b为一元二次方程x²
- 9数列an的通项公式为an=19-2n(n∈N),则{|an|}的前30项和为多少?
- 10没分了,答对了追加分.已知椭圆x^2/a^2+y^2/(a^2-1)=1和直线y=x-1相交于A,B两点,且以AB为直径
- 11造句 marry sb
- 121、Would you please ________ something to drink for me (find)
- 13读材料一、材料二,回答下列问题。(12分)
- 14澳大利亚东南部是什么气候类型
- 15设fx是定义在R上的一个函数,则函数fx=fx-f(-x)在R一定是什么函数?
