(2010•平谷区二模)如图,在方格纸(每个小方格都是边长为1个单位长度的正方形)中,我们称每个小正方形的顶点为格点,以
 wsyxb2022-10-04 11:39:541条回答
wsyxb2022-10-04 11:39:541条回答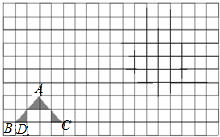 (2010•平谷区二模)如图,在方格纸(每个小方格都是边长为1个单位长度的正方形)中,我们称每个小正方形的顶点为格点,以格点为顶点的图形称为格点图形.如图中的△ABC称为格点△ABC.
(2010•平谷区二模)如图,在方格纸(每个小方格都是边长为1个单位长度的正方形)中,我们称每个小正方形的顶点为格点,以格点为顶点的图形称为格点图形.如图中的△ABC称为格点△ABC.(1)如果A,D两点的坐标分别是(1,1)和(0,-1),请你在方格纸中建立平面直角坐标系,并直接写出点B,点C的坐标;
(2)把“格点△ABC图案”向右平移10个单位长度,再向上平移5个单位长度,以点P(11,4)为旋转中心旋转180°,请你在方格纸中画出变换后的图案.

已提交,审核后显示!提交回复
共1条回复
相关推荐
- (2012•平谷区二模)某同学做了以下两个实验.
(2012•平谷区二模)某同学做了以下两个实验.

(1)实验1中,若液体X为稀盐酸.向盛有液体Y的烧杯中滴入适量液体X,液体Y中有气泡产生,一段时间后澄清石灰水变浑浊,气球鼓起,液体Y可能为______.实验后取下胶塞将烧杯取出,塞紧胶塞再向瓶内滴加适量盐酸,观察到的现象有______,原因是______.
(2)实验2中,若液体X为水,将其滴入盛有固体的烧杯中,一段时间后澄清石灰水变浑浊,固体可能为______,石灰水变浑浊的原因是______.若将瓶中浑浊的液体变澄清,可采取的方法有______ (至少写出三种). tamadefeiren1年前1
tamadefeiren1年前1 -
 lufeng429 共回答了12个问题
lufeng429 共回答了12个问题 |采纳率75%解题思路:该题中(1)主要考查碳酸盐的化学性质,遇酸会产生二氧化碳,且二氧化碳能与石灰水反应生成碳酸钙沉淀.另外根据学过的知识生石灰和水反应,会放出大量的热,而熟石灰的溶解度随着温度的升高而减小对(2)进行分析即可(1)x与y混合能产生使澄清石灰水变浑浊的气体,所以可判断y可能是碳酸盐的溶液,如碳酸钠或碳酸氢钠的溶液;二氧化碳与氢氧化钙反应会生成碳酸钙的沉淀,所以溶液浑浊,二氧化碳的产生也使瓶内压强变大,气球膨胀,实验后取下胶塞将烧杯取出,塞紧胶塞再向瓶内滴加适量盐酸,观察到的现象有:白色固体消失,有气泡产生,气球变鼓;
(2)由于氢氧化钙的溶解度随温度的升高而降低,所以可以知道水与固体反应时放热使氢氧化钙析出而导致溶液浑浊;要使该溶液变为澄清可以使溶液饱和或加酸使碳酸钙溶解;
故答案为:(1)碳酸钠或碳酸氢钠;白色固体消失,有气泡产生,气球变鼓;碳酸钙与盐酸反应生成二氧化碳
(2)生石灰或氢氧化钠;生石灰和水反应放热且氢氧化钙的溶解度随温度的升高而降低;加水 过滤 降温 加酸等点评:
本题考点: 酸的化学性质;溶解时的吸热或放热现象;饱和溶液和不饱和溶液相互转变的方法;固体溶解度的影响因素;生石灰的性质与用途;碱的化学性质.
考点点评: 本考点主要考查碳酸盐的性质,同时也考查了溶解度随温度的变化情况,是一道综合性较强的好题.1年前查看全部
- (2006•平谷区二模)某中学综合实践活动小组在进行“诚信商品”研究时,检验商品签所列成分及含量与实际是否相符.随机取出
 (2006•平谷区二模)某中学综合实践活动小组在进行“诚信商品”研究时,检验商品签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠.准确称取样品10.9克,加入足量的氯化钙溶液使其完全反应.将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到白色固体10克.试通过计算判断此纯碱是否可列入“诚信商品”.
(2006•平谷区二模)某中学综合实践活动小组在进行“诚信商品”研究时,检验商品签所列成分及含量与实际是否相符.随机取出市售某种“纯碱”样品(成分说明见图),经检验杂质仅是氯化钠.准确称取样品10.9克,加入足量的氯化钙溶液使其完全反应.将反应生成的沉淀物经过滤,洗涤,烘干,干燥后得到白色固体10克.试通过计算判断此纯碱是否可列入“诚信商品”.  139928399401年前1
139928399401年前1 -
 webflying 共回答了26个问题
webflying 共回答了26个问题 |采纳率96.2%解题思路:写出化学方程式并代入数据计算出碳酸钠的质量,然后算出样品中氯化钠的质量分数并和包装上的含量进行比较即可.碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钙不溶于水,氯化钠溶于水,所以经过过滤,洗涤,烘干的白色固体是碳酸钙,即碳酸钙的质量是10g;
设生成10克碳酸钙需要碳酸钠的质量为x.
Na2CO3+CaCl2=2NaCl+CaCO3↓
106 100
x 10g
[106/x=
100
10g]
x=10.6g
∴样品中氯化钠的质量=10.9g-10.6g=0.3g;样品中氯化钠的质量分数=[0.3g/10.9g]×100%═2.75%<5%.
∴该纯碱可以列入“诚信商品”.
答:此纯碱是否可列入“诚信商品”.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 本题主要考查学生对物质质量分数的计算能力.学生需正确书写出化学方程式,然后根据化学方程式找出比例关系,列出比例式,并正确分析各物质之间的关系,才能正确答题.1年前查看全部
- (2010•平谷区二模)请你根据提供的实验仪器和药品参与实验室气体制备的研究与实践.实验仪器如下图所示(导管、橡皮塞等未
(2010•平谷区二模)请你根据提供的实验仪器和药品参与实验室气体制备的研究与实践.实验仪器如下图所示(导管、橡皮塞等未画出):

实验药品:二氧化锰、5%双氧水、大理石、稀盐酸、稀硫酸、高锰酸钾
【比较探究】请填写下表
【实践研究】制取气体 反应物状态 反应条件 收集方法和依据 氧气 固体 加热 _______集气法 O2不易溶于水 二氧化碳 _________ 不需加热 向上排空气法 __________
(1)某同学选用a、c、d、f、j等组装制取和收集氧气的装置,该同学选用的药品是______.
(2)下列是该同学部分实验操作,其中不合理的是______.
A.先检查装置的气密性,后加药品B.先固定试管,后放置酒精灯
C.先将导管伸入集气瓶,后加热试管D.实验结束先熄灭酒精灯,后将导管移出水面
(3)四位同学根据提供的实验仪器分别设计了下列四套制取和收集二氧化碳的装置.
他们对设计的装置相互进行了交流评价.其中可能收集不到二氧化碳气体的装置是______;D装置能够使反应随时停止和发生,其中铜网兜换成铁制的后果是______. 红豆林1年前1
红豆林1年前1 -
 天下tt 共回答了18个问题
天下tt 共回答了18个问题 |采纳率94.4%解题思路:【比较研究】表中需要完成的是氧气的收集方法和收集二氧化碳的理论依据,还有制取二氧化碳的反应物状态.收集装置有三种:排水集气法(适用于不溶或难溶于水的且不能与水反应的气体)、向上排空气法(密度大于空气)和向下排空气法(密度小于空气);
【实践研究】(1)要回答选用药品需要分析所选发生装置,根据发生装置判断反采取的反应原理,再由反应原理来推断所取用药品;
(2)对操作中的先后进行分析,要熟悉实验中常见问题;
(3)对装置进行评价,本题要对装置正确性“能否利用该装置完成制取实验”进行评价;铁网会与稀盐酸反应,生成氢气.【比较研究】氧气不易溶于水,所以用排水集气法收集;制取二氧化碳是固体石灰石与液体稀盐酸之间的反应,所以反应物的状态是固体和液体;二氧化碳气体密度比空气大,能溶于水,收集时应采取向上排空气法.故答案为:排水、固体和液体、密度比空气大.
【实践研究】(1)根据“选用a、c、d、f、j等组装制取和收集氧气的装置”进行分析,仪器中出现了f酒精灯和g水槽,可知该同学制取氧气的发生装置为固体加热型,则所使用的药品应为高锰酸钾;收集方法采取了排水集气法.
故答案为:高锰酸钾.
(2)操作先后 A、制取气体的操作中,在确定装置不漏气后再加入药品,以防装置因漏气需要更换仪器而造成药品浪费;故此操作顺序正确;
B、固定仪器时一般是“从下向上”的原则,如果不考虑酒精灯就随意固定试管,可能会出现试管高度过低而放不下酒精灯的情况;当然也可能出现试管过高酒精灯火焰不能加热到试管的情况;故此顺序属于错误操作;
C、先伸入导管再加热进行反应,会造成装置内空气没能排出而和氧气混在一起被收集,收集氧气不纯;故此操作顺序错误;
D、该同学是采取排水法收集氧气的,在收集完成后,应先熄灭酒精灯再把导管从水中移出,可能会引起水倒流,导致热的试管炸裂;故此操作属不正确操作.
故选:BCD.
(3)装置A中发生装置部分,玻璃导管几乎伸到试管底部,加入一定稀盐酸后,导管口可能被液封,产生的二氧化碳气体不能排出,故使用此装置将有可能收集不到二氧化碳气体;如果换成铁网,铁会与稀盐酸反应生成氢气,氢气混入二氧化碳气体中,使收集的二氧化碳气体不纯.
故答案为:A、制得的二氧化碳中会含有氢气.点评:
本题考点: 气体制取装置的探究;常用气体的发生装置和收集装置与选取方法;常用气体的收集方法;氧气的制取装置;制取氧气的操作步骤和注意点;二氧化碳的实验室制法.
考点点评: 对实验室制取气体注意从原理-装置-操作的相互关系的角度进行理解与掌握.本题以实验探究的形式既考查了对课本知识的运用能力,又培养同学们的动脑、动手的能力.1年前查看全部
- (2008•平谷区一模)利用磁场对通电导体产生的作用制造的装置是( )
(2008•平谷区一模)利用磁场对通电导体产生的作用制造的装置是( )
A.电动机
B.发动机
C.电铃
D.电磁铁 snowxxsnow1年前1
snowxxsnow1年前1 -
 雨渡凡 共回答了25个问题
雨渡凡 共回答了25个问题 |采纳率96%解题思路:磁场对通电导体产生的作用内容是:通电导体在磁场中受力.A、电动机的原理是通电导体在磁场中受力,故A符合题意;
B、发动机是指汽油机、柴油机等,发电机的原理是电磁感应现象,故B不符合题意;
C、电铃的主要元件是电磁铁,其原理是电流的磁效应,故C不符合题意;
D、电磁铁的原理是电流的磁效应,故D不符合题意.
故选A.点评:
本题考点: 直流电动机的原理.
考点点评: 记住几个常见的问题:
①电动机、扬声器的原理是通电导体在磁场中受力;②发电机、动圈式话筒的原理是电磁感应现象;③电磁铁、奥斯特实验原理是电流的磁效应.1年前查看全部
- (2008•平谷区二模)如图,直线AB∥CD,EG平分∠BEF交CD于G,若∠1=40°,则∠2的度数为( )
 (2008•平谷区二模)如图,直线AB∥CD,EG平分∠BEF交CD于G,若∠1=40°,则∠2的度数为( )
(2008•平谷区二模)如图,直线AB∥CD,EG平分∠BEF交CD于G,若∠1=40°,则∠2的度数为( )
A.40°
B.60°
C.70°
D.80° yuanxiaoyang3211年前0
yuanxiaoyang3211年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2011•平谷区二模)在宏观、微观和符号之间建立联系是化学学科的特点.现有A、B、C、D四种物质,其微观示意图见下表.
(2011•平谷区二模)在宏观、微观和符号之间建立联系是化学学科的特点.现有A、B、C、D四种物质,其微观示意图见下表.
(1)1个B物质分子中有______原子.物质 A B C D  --氢原子
--氢原子 --碳原子
--碳原子 --氧原子
--氧原子微观示意图 



(2)上述物质中属于单质的是______,属于有机物的是______.[填写化学式]
(3)C物质中两种元素的质量比为______.
(4)将一定质量的A、B、C、D四种物质放在一密闭的容器内中,在电火花作用下,发生充分反应,测得反应前后各物质的质量如下:
其中,a值为______,该反应的化学方程式中A与D的化学计量数之比为______.A B C D 反应前质量/g 25 1 10 74 反应后质量/g 9 37 a 10  空灵珂1年前1
空灵珂1年前1 -
 lfgege 共回答了19个问题
lfgege 共回答了19个问题 |采纳率100%解题思路:(1)根据B物质的分子结构图,判断B物质分子中原子个数;
(2)根据单质的分子由同种原子构成,利用分子结构图,判断属于单质的物质,用化学式表示;根据不同种原子构成的分子为化合物分子且该分子中含有C原子的物质才属于有机物,判断有机物并写出化学式;
(3)根据C物质的分子构成,利用各元素的相对原子质量计算其中组成元素的质量比;
(4)运用质量守恒定律,计算反应后C物质的质量;根据反应前后的质量关系判断反应物和生成物,并结合分子构成图,写出反应的化学方程式,完成A与D的化学计量数之比的判断.(1)B物质的分子由2个H原子、1个O原子共3个原子构成;
(2)物质D的分子由2个氧原子构成,D物质O2为单质;物质A、C的分子都是由不同种原子构成的化合物分子且都含有C原子,但物质C为二氧化碳,不属于有机物,因此只有A物质CH4为有机物;
(3)C物质的分子由1个C原子、2个O原子构成,该物质中C、O元素质量比=12:(16×2)=3:8;
(4)根据质量守恒定律,反应后C物质的质量a=(25+1+10+74)-(9+37+10)=54;根据A、D两物质变化前后质量减少,可判断A物质CH4、D物质O2为该反应的反应物,而物质B、C变化后质量增加,B物质H2O、C物质CO2为该反应的生成物,反应的化学方程式为CH4+2O2
点燃
.
2H2O+CO2,则A与D的化学计量数之比为1:2;
故答案为:
(1)3;(2)O2;CH4;(3)3:8;(4)54;1:2.点评:
本题考点: 微粒观点及模型图的应用;单质和化合物的判别;化学式的书写及意义;质量守恒定律及其应用.
考点点评: 根据变化微观示意图及粒子构成模拟图,利用分子由原子构成等特点,明确反应前后分子的构成、种类及个数;根据质量守恒定律,判断反应中所表现出的规律.1年前查看全部
- (2014•平谷区二模)有分别写数字1、2、3、4、5的五张卡片,除数字不同外其它均相同,从中任意抽取一张,那么抽到的数
(2014•平谷区二模)有分别写数字1、2、3、4、5的五张卡片,除数字不同外其它均相同,从中任意抽取一张,那么抽到的数是奇数的概率是( )
A.[1/5]
B.[2/5]
C.[3/5]
D.[4/5] 后天真的好听1年前1
后天真的好听1年前1 -
 cat8317 共回答了16个问题
cat8317 共回答了16个问题 |采纳率81.3%解题思路:先找出分别标有数字1,2,3,4,5的,五张卡片中奇数的个数,再根据概率公式解答即可.标有数字1,2,3,4,5的五张卡片中,有两张标有奇数;任意抽取一张,数字为奇数的概率是[3/5].
故选C.点评:
本题考点: 概率公式.
考点点评: 此题考查概率的求法:如果一个事件有n种可能,而且这些事件的可能性相同,其中事件A出现m种结果,那么事件A的概率P(A)=[m/n].1年前查看全部
- (2011•平谷区二模)如图是实验室中用于制取和收集气体的装置图,请回答以下问题:
(2011•平谷区二模)如图是实验室中用于制取和收集气体的装置图,请回答以下问题:

(1)写出上图中标号①仪器的名称:______.
(2)用高锰酸钾制取氧气,发生装置选择______(填字母序号,下同),反应的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4.
K2MnO4+MnO2+O2↑△ .
(3)实验室制取二氧化碳,应选用的固体药品是______,收集装置选择______.
(4)如图是某同学放置在桌面上的一瓶无色纯净气体,已知它可能是氧气或二氧化碳,用化学方法确定该气体的方法是______(写出一种方法即可). 哦宣宣1年前1
哦宣宣1年前1 -
 凛然的呵 共回答了17个问题
凛然的呵 共回答了17个问题 |采纳率88.2%解题思路:(1)①为实验室常用的仪器,熟记常用仪器的名称即可轻松作答.
(2)根据反应物的状态和反应条件确定实验室制取气体的发生装置,熟记常用的化学方程式.
(3)根据实验室制取二氧化碳的反应原理进行分析;根据气体的密度和溶水性确定气体的收集装置.
(4)根据氧气和二氧化碳的化学性质进行分析.(1)熟记常用仪器的名称可知①为铁架台.
(2)反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置;高锰酸钾加热生成锰酸钾、二氧化锰和氧气.
(3)实验室通常用稀盐酸与大理石反应制取二氧化碳,其中大理石是固体;二氧化碳的密度比空气大,能溶于水,只能用向上排空气法收集.
(4)氧气具有助燃性,能使燃着的木条燃烧更旺,二氧化碳能使燃着的木条熄灭.因此可用燃着的木条来确定该气体的成份.
故答案为:(1)铁架台
(2)A;2KMnO4
△
.
K2MnO4+MnO2+O2↑
(3)大理石;E
(4)把燃着的木条伸入集气瓶中,若木条燃烧更旺,则是氧气,若木条熄灭,则是二氧化碳.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常用仪器的名称和选用;实验室制取氧气的反应原理;二氧化碳的实验室制法;二氧化碳的检验和验满.
考点点评: 解答本题关键是掌握实验制取氧气和二氧化碳的原理、装置、操作等内容,对两者加以比较,便于理解记忆.1年前查看全部
- (2012•平谷区二模)在空气不流通的房间内有人吸烟,一会儿整个房间就会充满烟味,这种现象称为______ 现
(2012•平谷区二模)在空气不流通的房间内有人吸烟,一会儿整个房间就会充满烟味,这种现象称为______ 现象.
 七窍升烟1年前1
七窍升烟1年前1 -
 VV淡定qq 共回答了19个问题
VV淡定qq 共回答了19个问题 |采纳率68.4%解题思路:不同物体互相接触时彼此进入对方的现象叫扩散.扩散现象说明了:①一切物质的分子都在不停地做无规则运动;②分子之间有间隙.房间内有人吸烟时.烟气分子会在空气中发生扩散现象,使得屋子中到处充满了烟味,扩散现象说明了:一切物质的分子都在不停地做无规则运动.
故答案为:扩散.点评:
本题考点: 扩散现象.
考点点评: 此题考查的知识点有两个:一是扩散现象的定义;二是扩散现象说明的物理问题.充分体现了物理来源于生活,又服务于社会的新课程理念.1年前查看全部
- (2005•平谷区一模)水被污染后会严重影响人类的身体健康.下列行为不会对水质造成污染的是( )
(2005•平谷区一模)水被污染后会严重影响人类的身体健康.下列行为不会对水质造成污染的是( )
A.扩大自然保护区范围
B.向河中倾倒垃圾
C.生活废水直接排入河中
D.大量施用农药、化肥 泡沫爱情801年前1
泡沫爱情801年前1 -
 fengyin9t 共回答了19个问题
fengyin9t 共回答了19个问题 |采纳率68.4%解题思路:A、扩大自然保护区范围不会造成水污染;
B、向河中倾倒垃圾会污染水资源;
C、生活污水是污染水体的主要原因之一;
D、大量使用农药、农药会污染水体.A、扩大自然保护区范围不会造成水污染,故A符合题意;
B、向河中倾倒垃圾会污染水资源,故B不符合题意;
C、生活污水是污染水体的主要原因之一,故C不符合题意;
D、大量使用农药、农药会污染水体,故D不符合题意.
故选A.点评:
本题考点: 水资源的污染与防治.
考点点评: 保护环境不受污染,已经是社会的焦点,更应该是我们青少年关心的问题,保护环境从我们做起.1年前查看全部
- (2013•平谷区二模)如图所示,电能表的示数是______kW•h.
 yyss夜1年前1
yyss夜1年前1 -
 leon0706 共回答了18个问题
leon0706 共回答了18个问题 |采纳率94.4%解题思路:电能表的读数方法:(1)月末的减去月初的示数.(2)最后一位是小数.(3)单位kW•h.电能表的示数为:1963.2kW•h.
故答案为:1963.2.点评:
本题考点: 电能表参数的理解与电能的求法.
考点点评: 本题考查了电能表的读数方法,关键是知道电能表的最后一位是小数,单位是kW•h.1年前查看全部
- (2014•平谷区一模)在某次活动课中,甲、乙两个学习小组于同一时刻在阳光下对校园中一些物体进行了测量.下面是他们通过测
 (2014•平谷区一模)在某次活动课中,甲、乙两个学习小组于同一时刻在阳光下对校园中一些物体进行了测量.下面是他们通过测量得到的一些信息:如图1,甲组测得一根直立于平地,长为80cm的竹竿的影长为60cm.如图2,乙组测得学校旗杆的影长为900cm.则旗杆的长为( )
(2014•平谷区一模)在某次活动课中,甲、乙两个学习小组于同一时刻在阳光下对校园中一些物体进行了测量.下面是他们通过测量得到的一些信息:如图1,甲组测得一根直立于平地,长为80cm的竹竿的影长为60cm.如图2,乙组测得学校旗杆的影长为900cm.则旗杆的长为( )
A.900cm
B.1000cm
C.1100cm
D.1200cm dghdgh1年前1
dghdgh1年前1 -
 aininini 共回答了14个问题
aininini 共回答了14个问题 |采纳率92.9%解题思路:根据同一时刻物高与影长成正比即可求出旗杆的高度;∵同一时刻物高与影长成正比,
∴[80/60]=[旗杆的高度/900],
解得旗杆的高度=1200cm;
故选D.点评:
本题考点: 勾股定理的应用.
考点点评: 本题考查了把实际问题抽象到相似三角形中,利用相似三角形的相似比,列出方程,通过解方程求解,体现了转化的思想.此题的文字叙述比较多,解题时要认真分析题意.1年前查看全部
- (2006•平谷区一模)下列属于化学变化的是( )
(2006•平谷区一模)下列属于化学变化的是( )
A.矿石粉碎
B.空气液化
C.干冰气化
D.酒精燃烧 xiathing1年前1
xiathing1年前1 -
 95步枪 共回答了19个问题
95步枪 共回答了19个问题 |采纳率73.7%解题思路:本题考查学生对物理变化和化学变化的确定.判断一个变化是物理变化还是化学变化,要依据在变化过程中有没有生成其他物质,生成其他物质的是化学变化,没有生成其他物质的是物理变化.A、矿石粉碎只是形状发生变化,没有新物质生成,属于物理变化,故A错;
B、空气液化只是状态发生了变化,没有新物质生成,属于物理变化,故B错;
C、干冰气化由固态变为气态,只是状态发生了变化,没有新物质生成,属于物理变化,故C错;
D、酒精燃烧生成水和二氧化碳,有新物质生成,属于化学变化,故D正确.
故选D.点评:
本题考点: 化学变化和物理变化的判别.
考点点评: 要熟记物理变化与化学变化的本质区别:是否有新物质生成,有新物质生成属于化学变化,没有新物质生成属于物理变化.1年前查看全部
- (2010•平谷区二模)用笔画线代替导线,把带有开关的电灯、插座分别正确地接入如图所示的家庭电路中.
 觅糖1年前0
觅糖1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2005•平谷区一模)符合下列物质变化要求的甲物质是( )
(2005•平谷区一模)符合下列物质变化要求的甲物质是( )

A.Cu
B.Na20
C.Mg
D.CuO 娃哈哈ax4621年前1
娃哈哈ax4621年前1 -
 power7597 共回答了15个问题
power7597 共回答了15个问题 |采纳率86.7%解题思路:解答本题的突破口是丁与氧气反应生成甲,所以甲属于含氧化合物,然后再将属于含氧化合物的两个答案B、D进行代入法进行验证.由丁与氧气反应生成甲,所以甲属于含氧化合物,把A、C答案排出,假设是氧化钠的话,氧化钠与盐酸反应生成氯化钠和水,乙是氯化钠,与硝酸银反应生成氯化银沉淀和硝酸钠,所以丙只能是硝酸钠,因为氯化银属于不溶于酸的沉淀,由于铁排在了钠的后面,所以与硝酸钠不反应,所以甲不能是氧化钠,假设是氧化铜,氧化铜与盐酸反应生成氯化铜和水,乙是氯化铜,氯化铜与硝酸银反应生成氯化银沉淀和硝酸铜,所以丙是硝酸铜,铁与硝酸铜反应生成铜和硝酸亚铁,所以丁是铜,铜和氧气反应又生成了氧化铜,所以甲是氧化铜.
故选D.点评:
本题考点: 物质的相互转化和制备.
考点点评: 解答本题不需要每个答案都代入,要根据题给信息推出甲中一定含氧元素,再将含氧元素的答案代入即可.1年前查看全部
- (2014•平谷区二模)如图,在四边形ABCD中,对角线BD平分∠ABC,∠A=120°,∠C=60°,AB=5,AD=
 (2014•平谷区二模)如图,在四边形ABCD中,对角线BD平分∠ABC,∠A=120°,∠C=60°,AB=5,AD=3.
(2014•平谷区二模)如图,在四边形ABCD中,对角线BD平分∠ABC,∠A=120°,∠C=60°,AB=5,AD=3.
(1)求证:AD=DC;
(2)求四边形ABCD的周长. 1987591年前0
1987591年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2012•平谷区二模)小英按图甲所示的电路图连接实验电路,测量电阻R的阻值.闭合开关S,调节滑动变阻器的滑片P后,观察
(2012•平谷区二模)小英按图甲所示的电路图连接实验电路,测量电阻R的阻值.闭合开关S,调节滑动变阻器的滑片P后,观察到电压表和电流表的示数分别如图乙、丙所示,则电流表的示数为______A,电阻R的阻值为______Ω.

 mimibbq1年前1
mimibbq1年前1 -
 木头小人 共回答了18个问题
木头小人 共回答了18个问题 |采纳率94.4%由甲图可知,电流表测电路中的电流,电压表测电阻R两端的电压;
由图乙可知,电压表的量程为0~15V,分度值为0.5V,电阻R两端的电压U=4V,
由图丙可知,电流表的量程为0~3A,分度值为0.1A,通过电阻的电流I=0.8A,
电阻R的阻值:R=[U/I]=[4V/0.8A]=5Ω.
故答案为:(1)0.8;(2)5.1年前查看全部
- (2010•平谷区一模)如图所示,锤头松动时,用力敲锤柄是利用______使锤头套紧.
 瑛子子1年前1
瑛子子1年前1 -
 猪之梦 共回答了16个问题
猪之梦 共回答了16个问题 |采纳率93.8%解题思路:应用惯性知识解释生活中现象的步骤是:先分析物体的原来的运动状态,当受到力的作用,物体的一部分的运动状态发生了改变,没受到力的那部分由于惯性要保持原来的运动状态.因为锤与柄原来都向下运动,柄撞在地上受到阻力作用,改变了它的运动状态,就停止了运动,
锤头没受阻力仍保持原来运动状态,继续向下运动,这样锤头就紧套在锤柄上了.
故答案为:惯性.点评:
本题考点: 惯性.
考点点评: 本题主要考查学生用惯性知识解释生活中一些现象的能力,惯性在生活中有很多的应用,在生活中注意总结.1年前查看全部
- (2009•平谷区二模)某同学在做“用伏安法测定小灯泡电功率”的实验时,在其中的一次正确操作中,由图甲、乙可知:电路中的
(2009•平谷区二模)某同学在做“用伏安法测定小灯泡电功率”的实验时,在其中的一次正确操作中,由图甲、乙可知:电路中的电流为______A,小灯泡两端的电压为______ V.

 无爱-zz1年前1
无爱-zz1年前1 -
 shixianglu 共回答了19个问题
shixianglu 共回答了19个问题 |采纳率89.5%解题思路:电压表和电流表的读数:确定使用的量程,确定每一个大格和每一个小格各代表多少.电流表使用的0~0.6A量程,每一个大格代表0.2A,每一个小格代表0.02A,电流为0.2A.电压表使用的0~3V量程,每一个大格代表1V,每一个小格代表0.1V,电压为2.5V.
故答案为:0.2;2.5.点评:
本题考点: 电流表的读数方法;电压表的读数方法.
考点点评: 电压表和电流表读数时,首先确定使用的量程,然后进行读数.1年前查看全部
- (2011•平谷区二模)已知x2-3x-6=0,求[1/x−3−x+1x2+x]的值.
 funnychaochao1年前0
funnychaochao1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2005•平谷区一模)俗名“生石灰”的物质是( )
(2005•平谷区一模)俗名“生石灰”的物质是( )
A.氧化钙
B.氢氧化钙
C.碳酸钙
D.氯化钙 131333035461年前1
131333035461年前1 -
 无言城 共回答了16个问题
无言城 共回答了16个问题 |采纳率75%解题思路:根据常见化学物质的名称、俗称、化学式进行分析判断即可.A、氧化钙俗称生石灰,其化学式为CaO,故选项正确.
B、氢氧化钙俗称熟石灰或消石灰,其化学式为:Ca(OH)2,故选项错误.
C、碳酸钙是大理石或石灰石的主要成分,故选项错误.
D、“生石灰”是氧化钙的俗称,不是氯化钙的俗称,故选项错误.
故选A.点评:
本题考点: 生石灰的性质与用途.
考点点评: 本题难度不大,熟练掌握生石灰、熟石灰、石灰石的区别是正确解答本题的关键.1年前查看全部
- (2010•平谷区二模)已知:如图,梯形ABCD中,AD∥BC,AD+BC=10,M是AB的中点,MD⊥DC,D是垂足,
 (2010•平谷区二模)已知:如图,梯形ABCD中,AD∥BC,AD+BC=10,M是AB的中点,MD⊥DC,D是垂足,sin∠C=[4/5],求梯形ABCD的面积.
(2010•平谷区二模)已知:如图,梯形ABCD中,AD∥BC,AD+BC=10,M是AB的中点,MD⊥DC,D是垂足,sin∠C=[4/5],求梯形ABCD的面积.  dzs6911年前0
dzs6911年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2009•平谷区一模)已知a是方程x2-2x-3=0的根,求代数式a(a+1)2-a(a2+a)-3a-2的值.
 xx盈1年前1
xx盈1年前1 -
 Z咖啡的灵魂 共回答了19个问题
Z咖啡的灵魂 共回答了19个问题 |采纳率89.5%解题思路:首先由已知可得a2-2a-3=0,即a2-2a=3.然后化简代数式,注意整体代入,从而求得代数式的值.原式=a(a+1)2-a(a2+a)-3a-2=a3+2a2+a-a3-a2-3a-2=a2-2a-2,
∵a是方程x2-2x-3=0的根,
∴a2-2a-3=0,
∴原式=1.点评:
本题考点: 一元二次方程的解;整式的混合运算—化简求值.
考点点评: 注意解题中的整体代入思想.1年前查看全部
- (2010•平谷区一模)关于磁现象,下列说法中错误 的是( )
(2010•平谷区一模)关于磁现象,下列说法中错误 的是( )
A.用磁感线可以方便、直观地描述磁场的分布
B.地球周围存在磁场,地磁场的北极在地理南极附近
C.一根锯条靠近磁铁的磁极时,它们相互吸引,说明锯条有磁性
D.磁体和电流周围都存在磁场,磁场中不同点的磁场方向一般不同 怜61年前1
怜61年前1 -
 莲花渡心 共回答了20个问题
莲花渡心 共回答了20个问题 |采纳率85%解题思路:根据磁感线、地磁场、磁性和磁场方向、电流的磁效应等基础知识可以确定各选择项的正误.A、磁感线是为了描述看不见又客观存在的磁场而引入的,它的方向可以描述磁场的方向;其疏密程度描述磁场的强弱.故A的说法正确.
B、根据地磁场的相关知识可知,地球周围存在磁场,地磁场的北极在地理南极附近,地磁的南极在地理的北极附近.故B的说法是正确的.
C、一根锯条靠近磁铁的磁极时,它们相互吸引,即使锯条没有磁性,磁极也会吸引锯条,故C的说法是错误的.
D、根据奥斯特实验可知,电流的周围存在磁场.磁场中的不同位置,磁场的方向也不相同.故D的说法是正确的.
综上分析故选C.点评:
本题考点: 物体是否具有磁性的判断方法;磁场;磁感线及其特点.
考点点评: 若两个磁性材料制成的物体相互排斥,可以确定这两个物体一定都有磁性.若两者相互吸引,则不能确定两者一定都有磁性,只要有一个物体具有磁性也可出现这种情况,因为磁性能够吸引磁性材料制成的物体.考虑问题要全面.1年前查看全部
- (2012•平谷区二模)如图所示,在水平平衡的杆杆的A点挂10N的钩码,用调好的弹簧测力计竖直向上拉杠杆的A点是杠杆在水
 (2012•平谷区二模)如图所示,在水平平衡的杆杆的A点挂10N的钩码,用调好的弹簧测力计竖直向上拉杠杆的A点是杠杆在水平位置平衡,则测力计的示数是______N,如果将测力计沿虚线方向拉,仍使杠杆在水平位置平衡,则测力计的示数应变______.(选填“大”或“小”)
(2012•平谷区二模)如图所示,在水平平衡的杆杆的A点挂10N的钩码,用调好的弹簧测力计竖直向上拉杠杆的A点是杠杆在水平位置平衡,则测力计的示数是______N,如果将测力计沿虚线方向拉,仍使杠杆在水平位置平衡,则测力计的示数应变______.(选填“大”或“小”)  zhangwen5233a1年前1
zhangwen5233a1年前1 -
 lf606 共回答了20个问题
lf606 共回答了20个问题 |采纳率90%解题思路:(1)设杠杆的分度值是L,知道阻力、阻力臂、动力臂,根据杠杆平衡条件求出动力.
(2)当弹簧测力计竖直向上拉动杠杆,杠杆在水平位置平衡,力臂在杠杆上,力臂最长,当弹簧测力计向右倾斜时,力臂变小,阻力和阻力臂不变,拉力会变大.(1)设杠杆的分度值为 L,
根据杠杆平衡条件F1L1=F2L2得,F1×8L=10N×4L,∴F1=5N.
(3)当弹簧测力计竖直向上拉动杠杆,杠杆在水平位置平衡,力臂为OB,当弹簧测力计向右倾斜时,力臂变小,阻力和阻力臂不变,拉力会变大.
故答案为:5;大.点评:
本题考点: 杠杆的平衡条件.
考点点评: 杠杆在水平位置平衡,力竖直作用在杠杆时,力臂在杠杆上,当力倾斜作用在杠杆上,力臂变小,力变大,这个知识点经常考查,一定要掌握.1年前查看全部
- (2010•平谷区二模)在以下的“四连环”图中,每环代表一种物质,相连环间所代表的物质在一定条件下可以发生反应,下表的选
 (2010•平谷区二模)在以下的“四连环”图中,每环代表一种物质,相连环间所代表的物质在一定条件下可以发生反应,下表的选项中,符合这一要求的是( )
(2010•平谷区二模)在以下的“四连环”图中,每环代表一种物质,相连环间所代表的物质在一定条件下可以发生反应,下表的选项中,符合这一要求的是( ) A B C D 甲 Cu HCl O2 Na2CO3 乙 HCl NaOH CO HCl 丙 Fe2O3 CaCO3 Fe2O3 NaOH 丁 Mg NaCl HCl H2SO4
A.Cu HCl Mg Fe2O3
B.HCl NaOH CaCO3 NaCl
C.O2 CO Fe2O3 HCl
D.Na2CO3 HCl NaOH H2SO4 我是蓝色风暴1年前1
我是蓝色风暴1年前1 -
 etfrommoon 共回答了20个问题
etfrommoon 共回答了20个问题 |采纳率90%解题思路:根据表中A、B、C、D四个选项中甲、乙、丙、丁所代表的种四物质间能否相互反应,判断四个选项中所包括的物质及排序是否合理,最后找到正确选项.A、铜与镁和盐酸不反应(即甲与乙和丁都不反应),所以错误.
B、碳酸钙与氢氧化钠和氯化钠都不反应,(即丙与乙和丁都不反应),所以错误.
C、氧气与盐酸不反应(即甲与丁不反应),所以错误.
D、各物质间和反应情况均符合,所以正确.
故选D.点评:
本题考点: 酸的化学性质;金属的化学性质;碱的化学性质;盐的化学性质.
考点点评: 酸、碱、盐是初中化学的重点内容,是教学难点,也是考查的重点和热点,透彻理解掌握酸、碱、盐及氧化物的化学性质,了解反应现象、物质状态和颜色,明确各类反应发生的条件,是解题的前提条件.1年前查看全部
- 2011年平谷区二模初三物理第23题的解题过程
 纯粹的鱼1年前2
纯粹的鱼1年前2 -
 sumi_ko 共回答了24个问题
sumi_ko 共回答了24个问题 |采纳率91.7%设甲、乙球的体积为V,水对容器底的压强变化是由甲球露出液面的2/5造成的,
因此有P水2/5Vg=40Pa0.005m2,则甲的体积V=0.00005m3
绳剪断前,甲、乙悬浮,因而有F浮=G,即P水g2V=G甲+G乙 (1)
绳剪断后,甲漂浮,有G甲=P水g3/5V (2)
将(1)(2)式整理后得G乙=7/5P水gV,代入数值得G乙=0.7N,则m乙=70g1年前查看全部
- (2013•平谷区模拟)根据如图回答问题.
(2013•平谷区模拟)根据如图回答问题.

(1)写出标有序号的仪器名称:①______,②______.
(2)实验室制取二氧化碳应选用的发生装置为______(填序号,下同).
(3)用高锰酸钾制取氧气的化学方程式为2KMnO4
K2MnO4+MnO2+O2↑△ .2KMnO4,应选用的发生装置为______,收集一瓶干燥的氧气,可选用的收集装置为______.
K2MnO4+MnO2+O2↑△ . eyewindows1年前1
eyewindows1年前1 -
 wpeter215 共回答了24个问题
wpeter215 共回答了24个问题 |采纳率87.5%解题思路:(1)直接写出图中所标的仪器的名称;
(2)实验室制取气体的发生装置主要由反应物的状态和反应条件决定;根据实验室制取二氧化碳的反应原理来进行选择;
(3)实验室制取气体的发生装置主要由反应物的状态和反应条件决定;根据高锰酸钾分解的条件来选择发生装置,要收集干燥的气体通常选择排空气收集,所以可以根据氧气的密度来选择合适的收集装置.(1)图中所给仪器的名称为:①长颈漏斗;②集气瓶;
(2)实验室中制取二氧化碳不需要加热,为固液常温型的反应,所以应该选择B装置作为发生装置;
(3)用高锰酸钾制取氧气,反应物的状态是固态,反应条件是加热,应选固-固加热型的发生装置,即A装置;其反应的化学方程式为:2KMnO4
△
.
K2MnO4+MnO2+O2↑;要收集干燥的气体通常选择排空气收集,而氧气的密度比空气大,所以应该选择向上排空气法收集,即C装置.
故答案为:(1)长颈漏斗;集气瓶;
(2)B;
(3)2KMnO4
△
.
K2MnO4+MnO2+O2↑;A;C.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常用仪器的名称和选用;实验室制取氧气的反应原理;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答此题的关键是要明白实验室制取气体时,应该根据反应物的状态和反应的条件选择需要什么样的发生装置;根据制取气体的溶解性和密度的大小选择收集气体的方法.1年前查看全部
- (2005•平谷区二模)将足量的铁粉投入硫酸铜和硫酸的混合溶液中,反应完毕后过滤,在滤液里含有的物质是( )
(2005•平谷区二模)将足量的铁粉投入硫酸铜和硫酸的混合溶液中,反应完毕后过滤,在滤液里含有的物质是( )
A.Fe2(SO4)3
B.CuSO4
C.FeSO4
D.H2SO4 HBONDRFRIND1年前1
HBONDRFRIND1年前1 -
 mimi1669 共回答了20个问题
mimi1669 共回答了20个问题 |采纳率100%解题思路:在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.A、铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,不能生成硫酸铁,故A错误;
B、铁粉足量,能与硫酸铜完全反应,故不会含有硫酸铜,故B错误;
C、铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,故C正确;
D、铁粉足量,能与硫酸完全反应,故不会含有硫酸,故D错误.
故选C.点评:
本题考点: 金属活动性顺序及其应用.
考点点评: 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行,要充分考虑参加反应的物质的量对反应程度的影响.1年前查看全部
- (2012•平谷区一模)图甲所示的实验用来测定空气中氧气的体积分数.实验时要先关闭止水夹,将过量红磷在空气中点燃后迅速插
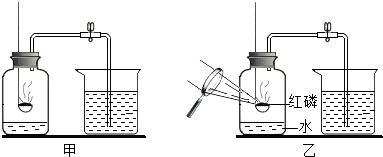 (2012•平谷区一模)图甲所示的实验用来测定空气中氧气的体积分数.实验时要先关闭止水夹,将过量红磷在空气中点燃后迅速插入集气瓶中,盖紧胶塞,待红磷熄灭后,冷却至室温,打开止水夹,观察现象.
(2012•平谷区一模)图甲所示的实验用来测定空气中氧气的体积分数.实验时要先关闭止水夹,将过量红磷在空气中点燃后迅速插入集气瓶中,盖紧胶塞,待红磷熄灭后,冷却至室温,打开止水夹,观察现象.
(1)写出实验中有关反应的化学方程式为4P+5O2
2P2O5点燃 .4P+5O2.
2P2O5点燃 .
(2)若按如图甲所示的实验测定的氧气体积分数大于[1/5],你认为可能的原因是______.
(3)此实验中不能用木炭代替红磷的理由是______.
(4)用图乙所示的装置代替图甲所示的装置进行实验,其优点是______. 大萝卜哥哥991年前1
大萝卜哥哥991年前1 -
 iorizj 共回答了13个问题
iorizj 共回答了13个问题 |采纳率92.3%解题思路:根据质量守恒定律正确书写化学方程式;进入广口瓶中是水的体积可看做是氧气的体积,算出水占集气瓶容积的分数即氧气的体积分数,结果偏大可从空气因受热膨胀而部分排出;根据木炭燃烧后的生成物的状态分析第3题,根据图乙避免了向广口瓶中伸入燃烧匙时空气因受热膨胀而部分排出而造成的结果不准确进行分析解答.(1)反应物为红磷和氧气,生成物是五氧化二磷,反应条件为点燃,反应的化学方程式为:4P+5O2
点燃
.
2P2O5;
(2)向广口瓶中伸入燃烧匙时空气因受热膨胀而部分排出可造成测定的氧气体积分数大于五分之一;
(3)不能用木炭代替红磷,理由是碳与氧气反应,生成二氧化碳气体,不会造成装置压强减小
(4)图乙避免了向广口瓶中伸入燃烧匙时空气因受热膨胀而部分排出而造成的结果不准确,其优点为更科学、准确;
故答案为:(1)4P+5O2
点燃
.
2P2O5;(2)向广口瓶中伸入燃烧匙时空气因受热膨胀而部分排出;(3)生成二氧化碳气体,不会造成装置压强减小;(4)更科学、准确.点评:
本题考点: 空气组成的测定.
考点点评: 只有熟悉用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,才能正确解答本题.1年前查看全部
- (2012•平谷区二模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )
(2012•平谷区二模)如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )

A.甲的溶解度大于乙的溶解度
B.乙的不饱和溶液升温可变成饱和溶液
C.将50℃时甲、乙的饱和溶液降温到20℃时,甲、乙的两种物质的溶质质量分数相等
D.50℃时,甲的饱和溶液中溶质的质量分数为40% 天行12341年前1
天行12341年前1 -
 sp770718 共回答了18个问题
sp770718 共回答了18个问题 |采纳率94.4%解题思路:A、比较溶解度大小须确定温度;
B、乙的溶解度随温度降低而增大,所以升温可使其不饱和溶液变为饱和溶液;
C、据甲、乙的溶解度随温度变化及饱和溶液中 溶质的质量分数分析解答;
D、饱和溶液中溶质的质量分数的计算式[溶解度/溶解度+100g]×100%.A、比较溶解度大小须确定温度,故错误;
B、乙的溶解度随温度降低而增大,所以升温可使其不饱和溶液变为饱和溶液,正确;
C、甲的溶解度随温度降低而减小,乙的溶解度随温度降低而增大;所以将50℃时甲、乙的饱和溶液降温到20℃时,甲析出晶体,溶质的质量分数减小,乙的溶解度增大,变为不饱和溶液,溶质的质量分数不变,与降温前相等;据饱和溶液中溶质的质量分数的计算式[溶解度/溶解度+100g]×100%可知:溶解度大则溶质的质量分数大,而20℃时甲的溶解度大于50℃时乙的溶解度,所以甲的溶质质量分数大于乙的溶质质量分数,故错误;
D、50℃时甲的溶解度是40g,据饱和溶液中溶质的质量分数的计算方法可知:该温度下甲的饱和溶液中溶质的质量分数为[40g/140g]×100%<40%,故错误;
故选:B.点评:
本题考点: 固体溶解度曲线及其作用;饱和溶液和不饱和溶液相互转变的方法;溶质的质量分数、溶解性和溶解度的关系.
考点点评: 饱和溶液中溶质的质量分数的计算式[溶解度/溶解度+100g]×100%可知:溶解度大则溶质的质量分数大,同时明确溶解度曲线的意义才能灵活分析解答.1年前查看全部
- (2010•平谷区一模)除去下列物质中含有的少量杂质(括号内为杂质),所用试剂及主要操作均合理的是( )
(2010•平谷区一模)除去下列物质中含有的少量杂质(括号内为杂质),所用试剂及主要操作均合理的是( )
A.CO2(CO):通氧气、点燃
B.Cu粉(CuO):足量稀硫酸、过滤
C.NaCl固体(KCl):水、过滤
D.NaOH溶液(Na2CO3):稀盐酸、过滤 假如11年前1
假如11年前1 -
 klj520 共回答了18个问题
klj520 共回答了18个问题 |采纳率83.3%A、杂质一氧化碳中通氧气,无法点燃,因为二氧化碳多,关键是除气体中的杂质不能使用气体.故选项错误;
B、铜与硫酸不反应,氧化铜与硫酸反应,过滤即可,故选项正确;
C、NaCl固体和KCl都溶于水,因此不可行,故选项错误;
D、NaOH溶液和Na2CO3都与盐酸反应,因此不可行,故选项错误;
故选B1年前查看全部
- (2009•平谷区二模)实验桌上有如下实验器材:如图所示的一个带支架的杠杆、一个量程为0~1N的弹簧测力计、两个质量均为
 (2009•平谷区二模)实验桌上有如下实验器材:如图所示的一个带支架的杠杆、一个量程为0~1N的弹簧测力计、两个质量均为100g的钩码和两小段细绳(细绳质量不计).请利用上述实验器材设计一个实验,证明“当把两个钩码挂在杠杆的A点处,用弹簧测力计的拉力作为动力,当杠杆水平平衡时,弹簧测力计的拉力跟这个拉力的力臂成反比”.(g 取10N/kg)
(2009•平谷区二模)实验桌上有如下实验器材:如图所示的一个带支架的杠杆、一个量程为0~1N的弹簧测力计、两个质量均为100g的钩码和两小段细绳(细绳质量不计).请利用上述实验器材设计一个实验,证明“当把两个钩码挂在杠杆的A点处,用弹簧测力计的拉力作为动力,当杠杆水平平衡时,弹簧测力计的拉力跟这个拉力的力臂成反比”.(g 取10N/kg)
(1)在你所设计的实验中,如果用点B表示弹簧测力计作用在杠杆上的位置,请在图中的杠杆上标出弹簧测力计示数最大时B点的位置.
(2)写出主要实验步骤. shmily21211年前1
shmily21211年前1 -
 夜色阑珊wsz 共回答了19个问题
夜色阑珊wsz 共回答了19个问题 |采纳率84.2%解题思路:求出两个钩码在重力作为阻力,设杠杆一个小格为L,又知道弹簧测力计的量程是1N,先确定动力臂的大小,确定B的位置即最小动力臂,阻力臂和阻力不动时,增大动力臂,可以探究“当把两个钩码挂在杠杆的A点处,用弹簧测力计的拉力作为动力,当杠杆水平平衡时,弹簧测力计的拉力跟这个拉力的力臂成反比”.实验步骤:
①用细绳做成两个绳套,将一个绳套栓牢在杠杆的A点,记录阻力臂l阻在表格中;在A点处挂2个钩码,计算出它的重力G,即为它的阻力F阻并记录在表格中.
②在支点左侧施加一个力使杠杆在水平位置平衡,这个力向上,要使力臂在杠杆上,这个力要竖直向上,所以将另一个绳套拴在B点处,用弹簧测力计竖直向上拉B处绳套,使杠杆在水平位置平衡,记下弹簧测力计的示数F1和动力臂L1,记录在表格中.
③依次在C、D点的位置,仿照步骤②再做实验,分别记下弹簧测力计示数为F2、F3和L2、L3,并记录在表格中.
实验次数 1 2 3
L阻/cm
F阻/N
L动/cm
F动/N
点评:
本题考点: 杠杆的平衡条件.
考点点评: 本题知道两个钩码的质量求出两个钩码的重力为2N,知道阻力臂、和拉力最大值,根据杠杆平衡条件求出最小的动力臂,这是关键.1年前查看全部
- (2010•平谷区一模)下列物质中既能与盐酸反应,又能与石灰水反应的是的是( )
(2010•平谷区一模)下列物质中既能与盐酸反应,又能与石灰水反应的是的是( )
A.纯碱溶液
B.铁锈
C.NaOH
D.CO2 黄鳝耳朵1年前1
黄鳝耳朵1年前1 -
 a006972 共回答了19个问题
a006972 共回答了19个问题 |采纳率84.2%解题思路:依据物质间的反应规律分析解答即可;具体可通过酸的化学性质以及碱的化学性质进行探讨;A、纯碱即碳酸钠,碳酸钠能与盐酸反应生成二氧化碳,也能与氢氧化钙生成碳酸钙的白色沉淀;
B、铁锈的主要成分是氧化铁,氧化铁能与盐酸反应但不能与氢氧化钙反应;
C、氢氧化钠能与盐酸发生中和反应,但不能与氢氧化钙反应;
D、二氧化碳能与氢氧化钙反应生成碳酸钙沉淀,但不能与盐酸反应;
故选A点评:
本题考点: 酸的化学性质;碱的化学性质.
考点点评: 此题是对物质性质的考查题,解题的关键是掌握各物质间反应的规律,属基础性知识考查题.1年前查看全部
- (2010•平谷区二模)某化工厂发生硫酸泄漏事故.为减少污染,可向事故现场喷洒( )
(2010•平谷区二模)某化工厂发生硫酸泄漏事故.为减少污染,可向事故现场喷洒( )
A.食盐
B.干冰
C.熟石灰
D.硫酸铜 水蓝雁1年前1
水蓝雁1年前1 -
 minjianyiyao 共回答了14个问题
minjianyiyao 共回答了14个问题 |采纳率78.6%解题思路:A、食盐不和硫酸反应,无法减少硫酸污染,还造成人为浪费.
B、干冰是固态的二氧化碳,二氧化碳不与硫酸反应,亦无法减少硫酸污染.
C、熟石灰是一种常见的碱能与硫酸发生中和反应生成硫酸钙和水,可减少硫酸的污染.
D、硫酸铜与硫酸不反应,无法减少硫酸污染.A、食盐不和硫酸反应,无法减少硫酸污染,还造成人为浪费.因此答案不能选 A;
B、干冰是固态的二氧化碳,二氧化碳不与硫酸反应,亦无法减少硫酸污染.因此答案不能选 B;
C、熟石灰是一种常见的碱能与硫酸发生中和反应生成硫酸钙和水,可减少硫酸的污染.因此答案能选 C;
D、硫酸铜与硫酸不反应,无法减少硫酸污染.因此答案不能选 D.
故选:C点评:
本题考点: 酸的化学性质.
考点点评: 考查酸分别与氧化物、碱、盐的反应关系,建议学生掌握好复分解反应的条件,并能熟练应用,还要把握好氧化物与酸碱的反应情况.1年前查看全部
- (2011•平谷区一模)烧杯中盛有溶质质量分数一定的NaCl溶液,溶液全部倒出后,用蒸馏水洗涤2次,每次用20mL蒸馏水
(2011•平谷区一模)烧杯中盛有溶质质量分数一定的NaCl溶液,溶液全部倒出后,用蒸馏水洗涤2次,每次用20mL蒸馏水,若烧杯内每次残留0.5mL溶液,经2次洗涤后烧杯内残留的NaCl溶液中溶质的质量分数约为原NaCl溶液的(NaCl溶液的密度均按1g/cm3计算)( )
A.[1/81]
B.[1/400]
C.[1/820]
D.[1/1681] 四营长1年前1
四营长1年前1 -
 张小杰贴身小小乖 共回答了16个问题
张小杰贴身小小乖 共回答了16个问题 |采纳率87.5%解题思路:对溶液加水稀释时,溶液中溶质质量不变,利用稀释后所得溶液的溶质质量分数=[稀释前溶液中的溶质质量/稀释前溶液质量+稀释所加入水的质量]×100%,分别计算每次加水洗涤后溶液的溶质质量分数;把第二次洗涤后溶液的溶质质量分数与原溶液的溶质质量分数进行对比.根据NaCl溶液的密度均按1g/cm3计算,0.5mL氯化钠溶液即0.5g;20mL蒸馏水的质量为20g
假设原氯化钠溶液的质量分数为a,
经过第一次洗涤后溶液的质量分数=[0.5g×a/0.5g+20g]×100%=[a/41];
再进行第二次洗涤,洗涤后溶液的质量分数=
0.5g×
a
41
0.5g+20g×100%=[a/1681];
经2次洗涤后烧杯内残留的NaCl溶液中溶质的质量分数约为原NaCl溶液的[1/1681];
故选D.点评:
本题考点: 有关溶质质量分数的简单计算.
考点点评: 分析清楚本题所进行的操作对计算起决定作用,计算过程并不复杂,但需要足够的细心.1年前查看全部
- (2013•平谷区一模)下列用字母表示的物质由H、C、O、Na、Cl、Ca、Fe中的一种或几种元素组成,它们是初中化学常
(2013•平谷区一模)下列用字母表示的物质由H、C、O、Na、Cl、Ca、Fe中的一种或几种元素组成,它们是初中化学常见的物质.
(1)A是单质,与B混合后生成一种在标准状况下密度最小的气体,则A与B反应的化学方程式为______;
(2)C与B反应后溶液为黄色,则C的化学式为______;
(3)D可在工业上制造洗涤产品,与B混合时需借助酚酞等指示剂来证明发生反应,则D与B反应的化学方程式为______;
(4)E溶液即可与B反应,又可与F溶液混合生成D,则E与B、E与F反应的化学方程式分别为______、______;将两个反应后的所有物质到在同一个废液缸中,废液澄清透明,此时废液中的溶质组成为(写出所有可能)______;
(5)将固体G放入饱和F溶液中,溶液温度生高变浑浊,降到原温度后过滤,此时滤液的溶质质量分数比原溶液______(填升高、降低或不变) xiaoqizk1年前1
xiaoqizk1年前1 -
 xzm0542 共回答了22个问题
xzm0542 共回答了22个问题 |采纳率81.8%解题思路:(1)根据金属与酸反应产生氢气分析
(2)根据黄色溶液中含有有Fe3+分析
(3)根据酸碱中和反应分析
(4)根据已知元素组成的物质及酸、碱、盐的化学性质分析
(5)根据生石灰溶于水放热分析(1)标准状况下密度最小的气体是氢气,A是单质,与B反应生成氢气,因此A是铁,B是盐酸,化学方程式为
Fe+2HCl═FeCl2+H2↑
(2)黄色溶液中含有Fe3+,因此C为氧化铁,与盐酸反应生成氯化铁溶液为黄色,C的化学式为Fe2O3
(3)氢氧化钠可在工业上制造洗涤产品,与B混合时生成氯化钠和水,没有明显的实验现象,需借助酚酞等指示剂来证明发生反应,化学方程式为NaOH+HCl═NaCl+H2O
(4)E溶液能与B(盐酸)反应,又可与F溶液混合生成D(氢氧化钠),由上述元素组成的物质中碳酸钠能与盐酸反应生成氯化钠,与氢氧化钙反应生成氢氧化钠,故E为碳酸钠,F为氢氧化钙,E与B,E与F反应的化学方程式分别
Na2CO3+2HCl═2NaCl+H2O+CO2↑;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH将两个反应后的所有物质倒在同一个废液缸中,废液澄清透明,说明盐酸过量,将碳酸钙沉淀完全反应,此时废液中的溶质中一定含有氯化钠,氯化钙,若完全反应后盐酸和氢氧化钠都没有剩余,则溶质为NaCl、CaCl2;盐酸剩余,则溶质中还含有盐酸;因废液澄清透明,因此氢氧化钠不可能剩余,因氢氧化钠和氯化钙会结合成微溶的氢氧化钙,故组成情况有三种,NaCl、CaCl2;或NaCl、CaCl2、HCl;
(5)固体G放入饱和氢氧化钙溶液中,溶液温度升高,因此G为氧化钙,氧化钙溶于水温度升高,氢氧化钙的溶解度随温度升高而减小,当降到原温度后过滤,此时滤液仍然是饱和溶液,因此溶质质量分数不变
故答案为:(1)Fe+2HCl═FeCl2+H2↑;
(2)Fe2O3;
(3)NaOH+HCl═NaCl+H2O;
(4)Na2CO3+2HCl═2NaCl+H2O+CO2↑;、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH; NaCl、CaCl2;或NaCl、CaCl2、HCl;(5)不变点评:
本题考点: 物质的鉴别、推断.
考点点评: 本题是一道物质推断题,只有熟记各种物质的性质、反应过程才可正确解答本题.1年前查看全部
- (2014•平谷区一模)在探究“滑动摩擦力大小与哪些因素有关”的实验时;小青同学猜想:滑动摩擦力大小除了与接触面的粗糙程
(2014•平谷区一模)在探究“滑动摩擦力大小与哪些因素有关”的实验时;小青同学猜想:滑动摩擦力大小除了与接触面的粗糙程度以及接触面之间的压力大小有关外,可能还与物体的______有关.如果要用已调好的弹簧测力计、符合实验要求的两端带滑轮的木板、带钩的正方体木块等器材,对此猜想进行探究,请你写主要的实验步骤.
 55749981年前1
55749981年前1 -
 冰灵幻 共回答了29个问题
冰灵幻 共回答了29个问题 |采纳率89.7%可以猜想:滑动摩擦力的大小可能与物体的运动方向有关;
实验步骤:
(1)将带钩的木块放在带滑轮的木板上,细线的一端系在木块挂钩上,另一端绕过滑轮系在弹簧测力计的挂钩上,水平向左匀速拉动测力计,使木块在水平力作用下沿水平木板向某一方向匀速直线运动,读出测力计的示数F1并记录;
(2)仿照步骤(1)向相反方向使木块匀速直线运动,读出测力计的示数F2并记录;
(3)比较F1、F2的大小,如果相等,则滑动摩擦力大小与运动方向无关,如果不相等,则滑动摩擦力大小与运动方向有关.
故答案为:运动方向;如上所述.1年前查看全部
- (2013•平谷区一模)如图所示,温度计的示数是______℃.
 deadfish121年前1
deadfish121年前1 -
 goodonion 共回答了20个问题
goodonion 共回答了20个问题 |采纳率90%解题思路:此题温度计的示数在量程的范围内,且分度值为1℃,可根据这两点读出此温度计的示数.由图知:温度计的最小刻度值是1℃,因此该温度计的示数是26℃+0.2℃=26.2℃;
故答案为:26.2.点评:
本题考点: 温度计的使用及其读数.
考点点评: 在对温度计进行读数时,要首先观察温度计的量程和分度值,并且视线要与温度计的液柱上表面持平.1年前查看全部
- (2012•平谷区二模)实验桌上提供了如下器材:符合实验要求的电源一个、定值电阻R0一只、滑动变阻器一个、量程满足实验要
 (2012•平谷区二模)实验桌上提供了如下器材:符合实验要求的电源一个、定值电阻R0一只、滑动变阻器一个、量程满足实验要求的电压表、电流表各一只;开关一个.小刚想利用实验桌上的器材,设计一个实验证明:“定值电阻的电功率与电压的平方成正比”.
(2012•平谷区二模)实验桌上提供了如下器材:符合实验要求的电源一个、定值电阻R0一只、滑动变阻器一个、量程满足实验要求的电压表、电流表各一只;开关一个.小刚想利用实验桌上的器材,设计一个实验证明:“定值电阻的电功率与电压的平方成正比”.
(1)在答题卡中的虚线框内画出实验电路图.
(2)写出实验步骤.
(3)根据实验要求,设计一个记录实验数据的表格. 热凉皮1年前1
热凉皮1年前1 -
 和风一起飞 共回答了18个问题
和风一起飞 共回答了18个问题 |采纳率94.4%解题思路:(1)用一个电压表、一个电流表做实验,验证“定值电阻的电功率与电压的平方成正比”,可把定值电阻与电流表串联在电路中,用电压表测出定值电阻两端的电压,用滑动变阻器与定值电阻串联来改变定值电阻两端的电压,据此设计电路图.
(2)做实验时,先按实验的原理图连接实物图,用电流表测电流,电压表测出定值阻值两端的电压,改变滑动变阻器的阻值,再多测几组数据记在表格中,最后计算定值电阻的功率,分析实验数据.
(3)表格应包含:每次实验的电压值、电流值、电功率等内容.(1)实验电路图;

(2)实验步骤
①按电路图连接实验电路;
②闭合开关,将滑片滑到某一位置,记录电压表与电流表示数I1和U1;
③改变变阻器滑片位置,记录电压表与电流表示数I2和U2;
④仿照步骤③再做四次实验,记录电压表与电流表示数分别为I3、I4、I5、I6,U3、U4、U5、U6.
⑤根据P=UI分别计算各电压时的电功率,P1=U1I1;P2=U2I2;P3=U3I3;P4=U4I4;P5=U5I5;P6=U6I6;
⑥整理实验器材.
(3)实验数据记录表:
U/V
I/A
P/W点评:
本题考点: 电功率与电压、电流的关系;电路图设计.
考点点评: 本题考查在给定实验器材、实验目的情况下,设计实验电路、安排实验步骤、设计实验数据记录表,难度较大,对考生的能力要求较高,是一道难题.1年前查看全部
- (2005•平谷区一模)根据下列实验装置,请回答:
(2005•平谷区一模)根据下列实验装置,请回答:

(1)实验室制O2的化学方程式为2H2O2
2H2O+O2↑MnO2 .2H2O2,应选择的发生装置是(填代号)______;收集装置是(填代号)______.
2H2O+O2↑MnO2 .
(2)实验室制CO2的化学方程式为______,应选择的发生装置是(填代号)______.若选用图2装置,采用排空气法收集CO2时,气体应从(填a或b)______口进入,原因是______. it68871年前1
it68871年前1 -
 刷QQB 共回答了17个问题
刷QQB 共回答了17个问题 |采纳率88.2%解题思路:(1)根据反应物的状态和反应条件选择发生装置,写出相应的反应原理;根据气体的密度和溶解性选择收集装置;
(2)根据反应物的状态和反应条件选择发生装置,写出相应的反应原理;根据二氧化碳的密度选择进气口.(1)实验室制取氧气常用过氧化氢溶液和二氧化锰的混合物来制取,反应的方程式为:2H2O2
MnO2
.
2H2O+O2↑;可以选择的发生装置是乙固液常温型的简易装置;因为氧气的密度比空气大,故可以采用向上排空气法收集;
(2)实验室制取二氧化碳常用石灰石和稀盐酸反应来制取,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;可以选择的发生装置是乙固液常温型的简易装置;因为二氧化碳的密度比空气大,聚集在集气瓶的下方,故应该从短管a进入.
故答案为:(1)2H2O2
MnO2
.
2H2O+O2↑;乙;丙;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;乙;a;二氧化碳的密度比空气大.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题考查了常见气体氧气和二氧化碳的制取和收集,属于基础性的考查;对于图2装置可以代替排水法、排空气法收集气体,关键是明确气体的密度和溶解性.1年前查看全部
- (2013•平谷区一模)小利在做同一直线上二力合成的实验时,他要探究分力F2与分力F1的关系,将实验数据填在了数据记录表
(2013•平谷区一模)小利在做同一直线上二力合成的实验时,他要探究分力F2与分力F1的关系,将实验数据填在了数据记录表中,请你分析表中数据,归纳出F2与F1的关系式:______.
F1/N 2 4 6 8 10 12 F2/N 48 46 44 42 40 38  gzw77585211年前1
gzw77585211年前1 -
 赵中樯 共回答了17个问题
赵中樯 共回答了17个问题 |采纳率88.2%解题思路:比较两个力的大小变化可以看出,F2随F1的增大而减小,但两个力的和不变.在第一组数据中F1+F2=50N,F2=50N-F1;
在第二组数据中F1+F2=50N,F2=50N-F1;
在第三组数据中F1+F2=50N,F2=50N-F1;
…
所以F2与力F1的关系式为F2=50N-F1.
故答案为:F2=50N-F1.点评:
本题考点: 力的合成与应用.
考点点评: 解决此类问题一般分两步:先横比,判断不同物理量的变化规律;再纵比,确定两者之间的对应关系.1年前查看全部
- (2014•平谷区一模)在图中属于光的反射现象的是( )
(2014•平谷区一模)在图中属于光的反射现象的是( )
A.
夜晚用手电筒照路
B.
透过放大镜看到眼睛变大
C.
聪聪在照镜子
D.
插入水中的筷子在水面处向上弯折 真心小龟1年前1
真心小龟1年前1 -
 fengying95733 共回答了23个问题
fengying95733 共回答了23个问题 |采纳率91.3%解题思路:解答此题要从以下知识点入手:
①平面镜成像,成因是光的反射.
②光的折射现象.由物体发出的光透过不同介质时,会发生折射,使光路发生改变,因此我们看到的是物体的虚像,放大镜是凸透镜成像,是光的折射.
③光的直线传播.知道光在同一均匀介质中是沿直线传播的.A、夜晚用手电筒照路,是由于光的直线传播.所以不符合题意.
B、用放大镜看到眼睛变大,属于凸透镜成像,是由于光的折射形成的.故本选项不符合题意.
C、聪聪在照镜子,属于平面镜成像,是由于光的反射形成的,符合题意.
D、插入水中的筷子在水面处“弯折”,是因为光从水中斜射入空气中时,发生折射,故本选项不符合题意;
故选C.点评:
本题考点: 光的反射.
考点点评: 此题主要考查了光的直线传播、光的折射、光的反射现象.光的直线传播是光在同一均匀介质中的传播,光的反射是光照射到物体表面又返回的现象,光的折射是由于光从一种介质斜射入另一种介质或在不均匀介质中传播时,传播方向发生变化的现象.它们之间有本质的区别,要注意区分.1年前查看全部
- (2014•平谷区二模)如图,扇形OAB的半径OA=6,圆心角∠AOB=90°,C是AB上不同于A、B的动点,过点C作C
 (2014•平谷区二模)如图,扇形OAB的半径OA=6,圆心角∠AOB=90°,C是
(2014•平谷区二模)如图,扇形OAB的半径OA=6,圆心角∠AOB=90°,C是
上不同于A、B的动点,过点C作CD⊥OA于点D,作CE⊥OB于点E,连接DE,点H在线段DE上,且EH=[2/3]DE.设EC的长为x,△CEH的面积为y,选项中表示y与x的函数关系式的图象可能是( )
AB
A.
B.
C.
D.
 c119ralph1年前0
c119ralph1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- (2009•平谷区一模)下列做法中,为了增大摩擦的是( )
(2009•平谷区一模)下列做法中,为了增大摩擦的是( )
A.缝衣针表面做得很光滑
B.自行车刹车时用力捏紧车闸
C.旅行箱下装有小轮子
D.鞋底上刻有凹凸不平的花纹 黑白ff1年前1
黑白ff1年前1 -
 cxjyf 共回答了25个问题
cxjyf 共回答了25个问题 |采纳率96%A、缝衣针表面做得很光滑,是在压力一定时,减小接触面的粗糙程度减小摩擦,不符合题意.
B、自行车刹车时用力捏紧车闸,是在接触面的粗糙程度一定时,通过增大压力增大摩擦,符合题意.
C、旅行箱下安装两个轮子,是用滚动代替滑动减小摩擦力,不符合题意;
D、鞋底刻有凹凸不平的花纹,是在压力一定时,增大接触面的粗糙程度增大摩擦力,符合题意.
故选BD.1年前查看全部
- (2013•平谷区模拟)下列实验操作能达到实验目的是( )
(2013•平谷区模拟)下列实验操作能达到实验目的是( )
A.A
B.B
C.C
D.D 杀你吧1年前1
杀你吧1年前1 -
 skyhuang11 共回答了19个问题
skyhuang11 共回答了19个问题 |采纳率94.7%A、不宜用点燃的方法除去CO2中的少量CO,是因为少量的一氧化碳在二氧化碳中可能不能燃烧,一般采用通过灼热的氧化铜来除去一氧化碳.
B、由于氧化钙能与水反应生成氢氧化钙,所以用水除去CaO中的CaCO3时在除掉碳酸钙的同时也导致了氧化钙的变质,所以该方法不可取,一般采用高温加热的方法除掉CaO中的CaCO3.
C、羊毛在点燃时会产生出焦羽毛味,而合成纤维没有焦羽毛味,所以采用点燃,闻气味的方法可区分该两者;
D、由于稀盐酸和稀硫酸两种溶液均呈酸性,所以都能使石蕊试液变红色,所以滴加紫色石蕊溶液不能区分稀盐酸和稀硫酸;
故选C.1年前查看全部
- (2010•平谷区一模)现有一瓶纯碱样品其中含有少量NaCl杂质,课外化学小组同学将100g盐酸分5次加入到20g纯碱样
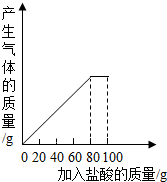 (2010•平谷区一模)现有一瓶纯碱样品其中含有少量NaCl杂质,课外化学小组同学将100g盐酸分5次加入到20g纯碱样品中,得到如图部分数据和图象(假设产生的气体全部逸出).
(2010•平谷区一模)现有一瓶纯碱样品其中含有少量NaCl杂质,课外化学小组同学将100g盐酸分5次加入到20g纯碱样品中,得到如图部分数据和图象(假设产生的气体全部逸出).
请计算:次数 第1次 第2次 第3次
加入盐酸的质量/g20 20 20 烧杯中剩余物的质量/g 38.24 a 74.72
(1)第2次加入盐酸后,a为______g.
(2)16%的NaCl溶液可用于生物小组进行选种.欲将第5次实验后的溶液配成16%的NaCl溶液,可先向此溶液中加入适量的碳酸钠粉末,至无气泡产生为止,这时还需要向溶液中加入水多少克?(假设实验过程中溶液损失忽略不计) brianming1年前1
brianming1年前1 -
 松海520 共回答了17个问题
松海520 共回答了17个问题 |采纳率94.1%解题思路:(1)根据反应的图象可知,在加入80g稀盐酸即第4次加入后,恰好反应完全,此后再加稀盐酸也不再会反应放出二氧化碳了;因此,前四次实验稀盐酸都得到充分反应;据第1次反应的数据可推知每加入20g稀盐酸,充分反应后产生二氧化碳的质量,据此规律可推断a值;
(2)先根据表格数据计算出每反应掉20g稀盐酸所产生二氧化碳的质量,根据二氧化碳的质量写方程式计算出每20克稀盐酸可消耗Na2CO3质量和生成NaCl质量;然后计算第5次实验后氯化钠的总质量以及溶液的总质量;据此计算16%的氯化钠溶液总质量与反应后所得氯化钠溶液质量差即为还需加水量.(1)每加入20g稀盐酸会产生气体的质量为20g+20g-38.24g=1.76g;
所以,第2次加入20g稀盐酸后,也会产生1.76g气体;
则第2次加入20g稀盐酸后烧杯中剩余物的质量=20g+20g+20g-1.76g-1.76g=56.48g;
故答案为:56.48g;
(2)每20克稀盐酸反应后产生M(CO2)=20g+20g-38.24g=1.76g;
设每20克稀盐酸可消耗Na2CO3质量为x,生成NaCl质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 1.76g
[106/x]=[117/y]=[44/1.76g]
x=4.24g; y=4.68g;
纯碱中杂质NaCl=20g-4.24g×4=3.04g;
所得溶液中NaCl总质量=4.68g×5+3.04g=26.44g;
所得溶液中NaCl溶液总质量=20g+100g+4.24g-1.76g×5=115.44g;
16%的NaCl溶液的质量为:[26.44g/16%]=165.25g;
则需要加水质量为165.25g-115.44g=49.81g;
答:还需要向溶液中加入水49.81g.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算;碳酸钠、碳酸氢钠与碳酸钙.
考点点评: 分析实验室数据时,根据质量守恒定律可发现每次加入盐酸所放出气体的质量,由此计算出每次完全反应所放出二氧化碳的质量;再以二氧化碳的质量为突破口来解答即可.1年前查看全部
- (2010•平谷区二模)图所示,电能表的示数是______kW•h.
 ganyx071年前1
ganyx071年前1 -
 小羽毛球 共回答了11个问题
小羽毛球 共回答了11个问题 |采纳率81.8%解题思路:电能表的读数方法:(1)月末的减去月初的示数,(2)最后一位是小数,(3)单位kW•h.电能表的读数为1964.3kW•h.
故答案为:1964.3kW•h.点评:
本题考点: 电能表参数的理解与电能的求法.
考点点评: 本题考查了电能表的读数方法,关键是知道电能表的最后一位是小数,单位是kW•h.1年前查看全部
- (2005•平谷区一模)下列物质中属于碱的是( )
(2005•平谷区一模)下列物质中属于碱的是( )
A.纯碱[Na2CO3]
B.烧碱[NaOH]
C.胆矾[CuSO4•5H2O]
D.碱式碳酸铜[Cu2(OH)2CO3] bibi畅1年前1
bibi畅1年前1 -
 无一1122 共回答了19个问题
无一1122 共回答了19个问题 |采纳率94.7%解题思路:碱是指在电离时产生的阴离子全部是氢氧根离子的化合物,据此进行分析判断.A、Na2CO3是由钠离子和碳酸根离子组成的化合物,属于盐,故选项错误.
B、Na0H是由钠离子和氢氧根离子组成的化合物,属于碱,故选项正确.
C、CuSO4•5H2O是由铜离子和硫酸根离子组成的结晶水合物,属于盐,故选项错误.
D、Cu2(OH)2CO3是由铜离子、氢氧根离子和碳酸根离子组成的化合物,含有金属离子和酸根离子,属于盐,故选项错误.
故选B.点评:
本题考点: 常见的氧化物、酸、碱和盐的判别.
考点点评: 本题难度不大,考查物质类别的判别,抓住酸、碱、盐的特征、熟悉常见的物质的组成是正确解答本题的关键.1年前查看全部
大家在问
- 1(2008•莆田)从“南海Ⅰ号”沉船打捞出的文物中发现,金器保存完好,铜器表面有锈迹,而铁器则锈迹斑斑.这说明金、铜、铁
- 2以君为长者故不错意也翻译成现代汉语
- 3(2012•菏泽二模)如图甲所示,是某同学验证动能定理的实验装置.其步骤如下:
- 4英语翻译自己写了2个句子,但都觉得不对.1.the amount of tourists who visted Engl
- 5贾平凹的《风雨》 阅读题风雨 贾平凹树林像一块面团子,四面都在鼓,鼓了就陷,陷了再鼓;接着就向一边倒,漫地而行的;忽的又
- 6If we had taken such effective measures much earlier, the ri
- 7小学五年级数学.甲港和乙港相距665Km,上午9时"寒山"号快艇从甲港开往乙港,"天远"号快艇从乙港开往甲港,到16时两
- 890-x =90-x-12怎么解这个算式?
- 910的a次方等于5,10的b次方等于6求10的2a+3b的值
- 10夏天是(),是(),我爱夏天.冬天是(),是(),我爱冬天.
- 11已知A=4x^2-4xy+y^2,B=x^2+xy-5y^2,求a-b的值
- 12At Christmas time,many people go into the woods to get their
- 13一批零件有560个,经检验有15个不合格,合格产品占这批零件的几分之几?
- 14A survey was carried out last year by the British medical As
- 15请问变压器6-7的r125电阻,4-5的R124电阻在整流桥起到什么作用?R133电阻和R134是输入电阻吗?解释详细点


