在稀硫酸、熟石灰、食盐、纯碱、硫酸铜、硝酸钾、硝酸铵中选择合适的物质将其化学式填入下列空格中:可检验无水酒精中是否含水的
 跟你有一腿2022-10-04 11:39:541条回答
跟你有一腿2022-10-04 11:39:541条回答| 在稀硫酸、熟石灰、食盐、纯碱、硫酸铜、硝酸钾、硝酸铵中选择合适的物质将其化学式填入下列空格中:可检验无水酒精中是否含水的是_______;可作复合肥的是_______;可除去金属表面氧化物的是_______;可作食品防腐剂的是________;可改良酸性土壤的是________;可作厨房洗涤剂的是__________。 |

已提交,审核后显示!提交回复
共1条回复
 娃哈哈zh 共回答了28个问题
娃哈哈zh 共回答了28个问题 |采纳率89.3%- CuSO 4 、KNO 3 、 H 2 SO 4 、 NaCl、 Ca(OH) 2 、 Na 2 CO 3
- 1年前
相关推荐
- 将13g锌放入100g稀硫酸溶液中恰好完全反应,可生成氢气多少mol?
 挖挖的耐耐1年前1
挖挖的耐耐1年前1 -
 胖胖月球球 共回答了19个问题
胖胖月球球 共回答了19个问题 |采纳率100%设生成氢气的质量为X
Zn + H2SO4 = ZnSO4 + H2↑
65 2
13g X
65/2=13g/X
X=0.4g1年前查看全部
- 稀硫酸敞口放置,其中水会挥发?为什么?
 sz102391年前3
sz102391年前3 -
 mjkn976 共回答了25个问题
mjkn976 共回答了25个问题 |采纳率84%只有浓硫酸有较强的吸水性,希硫酸就没浓的吸水性强,要比强的弱的多,相当于没有吸水性(酸是比较稀的情况下),由于稀硫酸里面水较多,所以水会挥发,挥发大于吸收,因此稀硫酸会挥发1年前查看全部
- 某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过
某化学探究小组称取6g镁铜合金样品于烧杯中,然后将80g稀硫酸分四次加入,充分反映后过滤,洗涤,干燥,称重,得到的实验过程中有关物质的用量及质量测定记录如下.
第一次加入稀硫酸的质量 20g
剩余固体的质量4.8g
第二次加入稀硫酸的质量 20g
剩余固体的质量mg
第三次加入稀硫酸的质量 20g
剩余固体的质量2.4g
第四次加入稀硫酸的质量 20g
剩余固体的质量1.8g
问题:
1.上述表格中m的值
2.该合金中Mg的质量分数
3.实验操作结束后的溶液中溶质的化学式
4.所用稀硫酸中溶质的质量分数
5.反映后所得溶液的总质量
希望能有人给出解答过程,不要只给答案,谢谢.
 发骚男人1年前1
发骚男人1年前1 -
 zihuoyanyan 共回答了13个问题
zihuoyanyan 共回答了13个问题 |采纳率100%第四次加入稀硫酸,剩余固体的质量还减小,所以第三次加入稀硫酸,镁还过量,
前后次加入稀硫酸,每次减小0.12克,所以
1.上述表格中m=3.6克
2.该合金中Mg的质量分数=(6-1.8)/6=70%
3.实验操作结束后的溶液中溶质的化学式:MgSO4
Mg + H2SO4 = MgSO4 + H2
24 98
6-4.8=1.2 X
X=4.9g
4.所用稀硫酸中溶质的质量分数=1.2/20=6%
Mg + H2SO4 = MgSO4 + H2
24 120 2
6-1.8=4.2 Y Z
Y=21g
Z=0.35g
5.反映后所得溶液的总质量=4.8+80-0.35=84.45g1年前查看全部
- 能鉴别甲烷和乙烯的试剂是溴的四氯化碳溶液还是稀硫酸?
 lanlianhua_1231年前1
lanlianhua_1231年前1 -
 伽萘僧伽 共回答了11个问题
伽萘僧伽 共回答了11个问题 |采纳率100%溴的四氯化碳溶液.甲烷与溴的四氯化碳溶液不反应.溴的四氯化碳溶液加入乙烯颜色褪去.1年前查看全部
- 区分稀盐酸、氯化钠溶液、氢氧化钠溶液的方法 区分石灰水、氢氧化钠溶液可以滴入什么溶液 区别石灰水、氢氧化钠、稀硫酸的方法
区分稀盐酸、氯化钠溶液、氢氧化钠溶液的方法 区分石灰水、氢氧化钠溶液可以滴入什么溶液 区别石灰水、氢氧化钠、稀硫酸的方法是滴入什么溶液,相关化学方程式
 谁dd谁1年前1
谁dd谁1年前1 -
 水里窒息的鱼 共回答了22个问题
水里窒息的鱼 共回答了22个问题 |采纳率81.8%1、区分稀盐酸、氯化钠溶液、氢氧化钠溶液的方法
取三种样品,各加入少量的碳酸钠,气泡产生的,是稀盐酸.无现象的另外两种溶液.
2HCl+Na2CO3=2NaCl+H2O+CO2↑
再另个两种溶液样品,加入少量的硫酸钠,有蓝色沉淀生成是氢氧化钠,无现象是氯化钠.
2NaOH +CuSO4=Cu(OH)2↓+Na2SO4
2、区分石灰水、氢氧化钠溶液可以滴入什么溶液
通入二氧化碳气体,有沉淀生成的是石灰水,无沉淀生成的是氢氧化钠.
CO2+Ca(OH)2=CaCO3↓+H2O
3、区别石灰水、氢氧化钠、稀硫酸的方法是滴入什么溶液,相关化学方程式
通入二氧化碳气体,有沉淀生成的是石灰水.CO2+Ca(OH)2=CaCO3↓+H2O
无沉淀是另个两种溶液.在另个两种溶液中加入铁块,有气体生成是稀硫酸.无气体生成是氢氧化钠.Fe+H2SO4=FeSO4+H2↑1年前查看全部
- 把98%,密度为1.84克每立方厘米的浓硫酸稀释成3mol/l的稀硫酸100mi求浓硫酸多少毫升
 蓝子lan1年前3
蓝子lan1年前3 -
 暗夜流星天边过 共回答了20个问题
暗夜流星天边过 共回答了20个问题 |采纳率85%这是一道典型的关于溶液稀释的计算题.涉及两种浓度,综合性较强.解答这类题目的原理很简单,不管是稀释,还是不同浓度间的换算,溶质是不变的.比如:硫酸的物质的量不变——(V*1.84*98%/98 = 3*0.1或者硫酸的质量不变—...1年前查看全部
- 室温下,用铁片与1mol•L-1稀硫酸反应制取氢气时,改用下列措施不能使氢气生成速率加快的是( )
室温下,用铁片与1mol•L-1稀硫酸反应制取氢气时,改用下列措施不能使氢气生成速率加快的是( )
A.改用热的稀硫酸
B.改用98%的浓硫酸
C.改用铁粉
D.改用2 mol•L-1硫酸 yoat1年前1
yoat1年前1 -
 荔枝后援1号 共回答了21个问题
荔枝后援1号 共回答了21个问题 |采纳率90.5%解题思路:增大反应速率可增大浓度、升高温度或增大固体的表面积,注意不能用浓硫酸,也可形成原电池反应,以此解答.A.改用热的稀硫酸,温度升高,活化分子的百分数增大,反应速率增大,故A不选;
B.改用98%的浓硫酸,铁在室温下与浓硫酸发生钝化反应,不能加快生成氢气的反应速率,故B选;
C.改用铁粉,固体表面积增大,反应速率增大,故C不选;
D.改用2 mol•L-1硫酸,浓度增大,且不影响硫酸的性质,反应速率增大,故D不选.
故选B.点评:
本题考点: 化学反应速率的影响因素.
考点点评: 本题考查化学反应速率的影响因素,为高考高频考点,侧重于学生的分析能力的考查,注意浓硫酸与铁发生钝化反应的性质,为易错点.1年前查看全部
- 铜和氧气 稀硫酸制取硫酸铜的化学方程式拜托了各位
铜和氧气 稀硫酸制取硫酸铜的化学方程式拜托了各位
还有离子方程式 谢桥女1年前1
谢桥女1年前1 -
 就是来黑你的 共回答了17个问题
就是来黑你的 共回答了17个问题 |采纳率94.1%楼上错了.不能合起来写 应该是2Cu+O2=2CuO(条件是△) CuO+H2SO4=CuSO4+H2O1年前查看全部
- 将铜片、锌片和250mL稀硫酸组成的原电池,假设锌片只发生电化学腐蚀.当在铜片上放出6.72L(标准状况下)的气体时,H
将铜片、锌片和250mL稀硫酸组成的原电池,假设锌片只发生电化学腐蚀.当在铜片上放出6.72L(标准状况下)的气体时,H2S04恰好反应完全.
(1)该原电池的负极反应式为______
(2)原稀硫酸的物质的量浓度是______mol•L-1
(3)列式计算锌片减少的质量. ttQWERss1年前1
ttQWERss1年前1 -
 轩辕行素311 共回答了12个问题
轩辕行素311 共回答了12个问题 |采纳率100%解题思路:(1)该原电池中较活泼的金属锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,写出相应的电极反应式.
(2)锌和稀硫酸反应生成氢气,根据氢气体积和硫酸的关系式计算硫酸的物质的量浓度.
(3)根据锌和氢气之间的关系式计算锌减少的质量.(1)该原电池中较活泼的金属锌作负极,负极上锌失电子发生氧化反应生成锌离子进入溶液,正极上氢离子得电子生成氢气,所以负极上的电极反应式为:Zn-2e-=Zn2+,电池反应式为:Zn+2H+=Zn2++H2↑.
故答案为:Zn-2e-=Zn2+.
(2)设硫酸的物质的量浓度是C.
Zn+H2SO4=ZnSO4+H2↑
1mol22.4L
0.25Cmol 6.72L
C=1.2mol/L.
故答案为:1.2.
(3)设锌减少的质量为m.
Zn+H2SO4=ZnSO4+H2↑
65g 22.4L
m6.72L
m=19.5g
故答案为:19.5g.点评:
本题考点: 原电池和电解池的工作原理;氧化还原反应的计算.
考点点评: 本题考查了电极反应式的书写及物质的量的有关计算,难度不大,根据物质的物质的量之间的关系式来解答即可.1年前查看全部
- 向下列分散系中滴加稀硫酸,先生成沉淀继而沉淀又溶解的是:A、Fe(OH)3胶体 B、H2SiO3胶体 C、Na2SiO3
向下列分散系中滴加稀硫酸,先生成沉淀继而沉淀又溶解的是:A、Fe(OH)3胶体 B、H2SiO3胶体 C、Na2SiO3溶液D、Ba(HCO3)2溶液.
 mh1683691年前1
mh1683691年前1 -
 李小军202 共回答了18个问题
李小军202 共回答了18个问题 |采纳率88.9%答案是A
A中先是氢氧化铁聚沉,后硫酸过量,氢氧化铁溶解
B中硅酸聚沉
C中变成硅酸沉淀
D中变成硫酸钡,1年前查看全部
- 已知1 molZn与1 mol H2SO4的能量大于1 mol ZnSO4与1 mol H2的能量,但是Zn与稀硫酸的反
已知1 molZn与1 mol H2SO4的能量大于1 mol ZnSO4与1 mol H2的能量,但是Zn与稀硫酸的反应不一定放出热量
 jotony1年前2
jotony1年前2 -
 小小孩的无奈 共回答了18个问题
小小孩的无奈 共回答了18个问题 |采纳率88.9%Zn与H2SO4能发生反应是因为该反应吉布斯自由能△G0
△H=△G+△S,不能确定.Zn与稀硫酸的反应不一定放出热量(△H为焓变,决定放热与否)1年前查看全部
- 甲、乙两烧杯中分别盛放500mL等物质的量浓度的稀硫酸,向甲烧杯中加入mg铁粉,向乙烧杯加mg锌粒,完全反应后发现有一烧
甲、乙两烧杯中分别盛放500mL等物质的量浓度的稀硫酸,向甲烧杯中加入mg铁粉,向乙烧杯加mg锌粒,完全反应后发现有一烧杯中仍有金属剩余,若H2SO4的物质的量浓度为xmol·L-1,则x的范围是
 桃花梦梦1年前1
桃花梦梦1年前1 -
 ho6ho630 共回答了22个问题
ho6ho630 共回答了22个问题 |采纳率95.5%因为锌的相对原子质量为64,铁为56,故剩余的为铁,因为H2SO4的物质的量浓度为xmol·L-1,所以H2SO4为0.5xmol,反应的铁为28xg,锌为32xg,所以28x<m,32x≥m,联立解得m/28>x≥m/321年前查看全部
- 化学初三关于溶液这类的问题生铁加入足量的稀硫酸,恰好完全反应,剩余黑色固体是什么?溶液中溶质?溶液中存分析一下
 jijimela1年前7
jijimela1年前7 -
 毕恭毕敬的人 共回答了12个问题
毕恭毕敬的人 共回答了12个问题 |采纳率83.3%生铁主要是由Fe和C两种物质组成.
加入稀硫酸,恰好反应,方程式为:Fe + H2SO4===FeSO4 + H2(气体)
所以,溶液中的溶质是FeSO4.
剩余的黑色固体是不和酸反应的碳颗粒.1年前查看全部
- 把100毫升98%的浓硫酸稀释成10%的稀硫酸,需要加水多少毫升?
把100毫升98%的浓硫酸稀释成10%的稀硫酸,需要加水多少毫升?
98%的浓硫酸的密度为1.84克每立方厘米
10%的稀硫酸的密度为1.07克每立方厘米 farmerdavid1年前1
farmerdavid1年前1 -
 liyouting1 共回答了19个问题
liyouting1 共回答了19个问题 |采纳率73.7%100*1.84*98%=w*10%
m=w-100*1.841年前查看全部
- 暗绿色固体A不溶于水,将A与NaOH固体共熔得易溶于水的化合物B.将B溶于水后加入H2O2得黄色溶液C.向C中加入稀硫酸
暗绿色固体A不溶于水,将A与NaOH固体共熔得易溶于水的化合物B.将B溶于水后加入H2O2得黄色溶液C.向C中加入稀硫酸至酸性后转化为橙色溶液D.向酸化的D溶液中滴加Na2SO4溶液得绿色溶液E.向E中加入氨水得灰蓝色沉淀F,再加入氯化铵并微热则F溶解得紫红色溶液G.请给出字母所代表的物质并写出相关的反应方程式.
 yuhuat1年前2
yuhuat1年前2 -
 guiwawa0428 共回答了15个问题
guiwawa0428 共回答了15个问题 |采纳率93.3%A:Cr2O3
B:NaCrO2
C:Na2CrO4
D:Na2Cr2O7
E:Cr2(SO4)3
F:Cr(OH)3
G:[Cr(NH3)2(H2O)4]3+1年前查看全部
- 向两只烧杯中各加入含有4.9g硫酸的稀硫酸,并将烧杯分置于天平的两个托盘上调节天平使之达到平衡.若向一只烧杯中加入ag金
向两只烧杯中各加入含有4.9g硫酸的稀硫酸,并将烧杯分置于天平的两个托盘上调节天平使之达到平衡.若向一只烧杯中加入ag金属锌,试讨论a的取值范围不同时,需向另一只烧杯中加入多少克金属镁,反应完毕时,天平仍能保持平衡?
十分钟以内答复加20分,二十分钟以内答复10分, 小绵杨1年前6
小绵杨1年前6 -
 暴打美眉 共回答了13个问题
暴打美眉 共回答了13个问题 |采纳率92.3%天平仍保持平衡,说明两边加入金属的质量与放出气体的质量差值相等.
先看两个极限情况,锌刚好反应消耗3.25g,镁刚好反应消耗1.2g.
(1)a>=3.25,硫酸完全反应,放出气体质量相等,所以加入金属质量也相等.
镁的质量为a
(2)a1年前查看全部
- (水解基础问题)稀氨水逐滴加入稀硫酸中 解释得好的追加
(水解基础问题)稀氨水逐滴加入稀硫酸中 解释得好的追加
生成硫酸铵 按根离子会水解成一水合氨 那么请问这水解生成的一水合氨能和硫酸共存么? 战锋1年前2
战锋1年前2 -
 -分花拂柳- 共回答了19个问题
-分花拂柳- 共回答了19个问题 |采纳率89.5%(NH4)2SO4+2H2O==2NH3·H2O+H2SO4
首先你要知道水解是微弱进行的,硫酸铵的水解很微弱,以至生成的氨水和硫酸的浓度很小,发生化学反应需要达到一定的浓度,这里的氨水,硫酸浓度太小了,以至于不能发生反应,所以可以共存.
求采纳1年前查看全部
- 我要准确的(越快越好!)1.稀盐酸与铁锈 2.氢氧化钠与稀硫酸 3.纯碱溶液与石灰水 4.硫酸铜溶液与氢氧化钠溶液 6.
我要准确的(越快越好!)
1.稀盐酸与铁锈 2.氢氧化钠与稀硫酸 3.纯碱溶液与石灰水 4.硫酸铜溶液与氢氧化钠溶液 6.氯化铁溶液和氢氧化钠溶液反应(以上操作的试验现象反应前后) 梓辰1年前1
梓辰1年前1 -
 yipengfei 共回答了13个问题
yipengfei 共回答了13个问题 |采纳率92.3%1.铁锈渐渐消失,溶液变黄色2.没有现象3.一开始没现象,然后出现沉淀4.出现蓝色沉淀,溶液澄清5.先生成灰白色沉淀,然后沉淀变红色,溶液变无色1年前查看全部
- 除杂质 求答鉴别物质的方法如:氢氧化钠固体和氢氧化钙固体 ;氢氧化钠溶液和石灰水 ;稀盐酸和稀硫酸 ;氢氧化钠和碳酸钠
除杂质 求答
鉴别物质的方法如:氢氧化钠固体和氢氧化钙固体 ;氢氧化钠溶液和石灰水 ;稀盐酸和稀硫酸 ;氢氧化钠和碳酸钠 ;
9、除杂质的方法如:氧化铜(铁) ;食盐(泥沙) ;稀盐酸(稀硫酸) ;
氢氧化钠(碳酸钠) .氢气(氯化氢) . 七分之一1年前1
七分之一1年前1 -
 kgdapscc 共回答了10个问题
kgdapscc 共回答了10个问题 |采纳率90%氢氧化钠固体和氢氧化钙固体加入Na2CO3 (有沉淀的是氢氧化钙) 氢氧化钠溶液和石灰水(亲,石灰水就是氢氧化钙啊!)稀盐酸和稀硫酸 加入AgCl(有沉淀的是盐酸) 氢氧化钠和碳酸钠 加盐酸(有气体生成的是碳酸钠)
氧化铜(铁)用磁铁, 食盐(泥沙)蒸发结晶, 稀盐酸(稀硫酸) 加入BaCl2然后过滤,氢氧化钠(碳酸钠)加入氢氧化钙然后过滤, 氢气(氯化氢) 这个我也不知道 .1年前查看全部
- 区分稀盐酸和稀硫酸,应选用的药品是什么
 chenlei5191年前1
chenlei5191年前1 -
 janeli 共回答了26个问题
janeli 共回答了26个问题 |采纳率88.5%BaCl21年前查看全部
- 实验室制取二氧化碳不能使用稀硫酸的原因是
 小胖雪爱大头飞1年前1
小胖雪爱大头飞1年前1 -
 rilson 共回答了19个问题
rilson 共回答了19个问题 |采纳率78.9%硫酸钙是微溶于水的,多了之后会阻碍反应进行1年前查看全部
- 某校进行化学实验需要1000g质量分数为19.6%的稀硫酸,但是实验室中只有质量分数为98%的浓硫酸,则需要进行的操作如
某校进行化学实验需要1000g质量分数为19.6%的稀硫酸,但是实验室中只有质量分数为98%的浓硫酸,则需要进行的操作如下
需要浓硫酸的质量为 需要加入水的质量为 藏珍斋1年前1
藏珍斋1年前1 -
 dingshaoning 共回答了21个问题
dingshaoning 共回答了21个问题 |采纳率95.2%浓硫酸稀释一定要将浓硫酸慢慢倒入水中,并且不停的搅拌.
需要浓硫酸的量=1000*19.6%/98%=
1000克减去浓硫酸的量,就是需要加水的量.1年前查看全部
- 把锌片放入下列溶液,溶液颜色有明显变化的是 A稀硫酸 B氯化铜溶液 C硝酸银溶液 D稀盐酸
把锌片放入下列溶液,溶液颜色有明显变化的是 A稀硫酸 B氯化铜溶液 C硝酸银溶液 D稀盐酸
反应的化学方程式是什么? lihao05161年前3
lihao05161年前3 -
 lapers 共回答了14个问题
lapers 共回答了14个问题 |采纳率85.7%当然是氯化铜溶液了
CuCl2+Zn=ZnCl2+Cu 置换反应
锌片溶解,铜析出1年前查看全部
- 用于造纸、纺织等行业的酸碱盐是( ) 1)熟石灰 2)食盐 3)稀硫酸 4)稀盐酸 5)纯碱
 hao87fei1年前2
hao87fei1年前2 -
 myqaq123 共回答了16个问题
myqaq123 共回答了16个问题 |采纳率93.8%5)纯碱1年前查看全部
- 稀硫酸为电解液 白金电极加入10A的电流流动电解时间为64分20秒 阴极生成气体在27度 1atm时是多少升?
稀硫酸为电解液 白金电极加入10A的电流流动电解时间为64分20秒 阴极生成气体在27度 1atm时是多少升?
A2.5 B4.5 C4.9 D9.0 E10 F13
急得很 无限感激 钟吾手心1年前1
钟吾手心1年前1 -
 传说断 共回答了16个问题
传说断 共回答了16个问题 |采纳率100%10A的电流流动电解时间为64分20秒,则电量为38600C,即0.4mol电子.
2H+ +2e-=H2
所以生成0.2molH2,阴极生成气体在27度 1atm时是4.9升1年前查看全部
- 工人师傅用98%的浓硫酸,稀释成500g19.6%的稀硫酸除铁锈问需要98%的浓硫酸多少毫升,加水多少毫升
 hank00720071年前1
hank00720071年前1 -
 fei8531953 共回答了14个问题
fei8531953 共回答了14个问题 |采纳率78.6%500*19.6%=98g
98/98%=100g 98%的硫酸98%硫酸的密度是1.84
100g/1.84=54.3ml 98%的硫酸
需要加水500-54.3=445.7ML水1年前查看全部
- 铜的电解精炼为什么电解质一定得用含铜离子的盐溶液,像用稀硫酸不可以吗?
 ntlsfw1年前3
ntlsfw1年前3 -
 垂垂老去 共回答了27个问题
垂垂老去 共回答了27个问题 |采纳率81.5%一定.粗铜Cu变Cu2+,而溶液中的Cu2+变精铜
如果溶液中没有Cu2+,电解可能无法进行.因为阳极上存在的杂质也发生了电极反应,而阴极上只有铜析出.1年前查看全部
- 以锌.稀硫酸.氧化铜制取铜的方案最简单的是
 捻花郎1年前1
捻花郎1年前1 -
 kemior 共回答了16个问题
kemior 共回答了16个问题 |采纳率87.5%CuO+H2SO4=CuSO4+H2O
Zn+CuSO4=ZnSO4+Cu1年前查看全部
- 1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为
1.用还原赤铁矿可得到一种具有银白色金属光泽的单质A,A在纯氧中燃烧得到一种黑色固体B,将B投入到稀硫酸中,可得到溶质为C和D的混合溶液,则A、B、C、D的化学式分别是:
2. 将一定质量的镁铝合金投入100mL一定物质的量浓度HCl中,合金全部溶解,向所得溶液中滴加5mol/L的NaOH溶液到过量,生成沉淀的质量与加入的NaoH溶液的体
积关系如图:
求A点为多少?具体的方程式和式子)
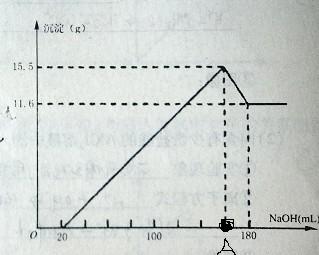
图上有个地方错了。A点的地方,沉淀是19.4... 5513600011年前1
5513600011年前1 -
 alexissui 共回答了19个问题
alexissui 共回答了19个问题 |采纳率94.7%赤铁矿被还原生成铁单质,A是Fe.Fe在纯氧中燃烧生成四氧化三铁B为Fe3O4.Fe3O4可视为FeO·Fe2O3所以C和D分别为FeSO4和Fe2(SO4)3.就是这个分析,真的没有计算方法.
2.当加入体积为20ml的时候把盐酸完全的中和了,在A点的时候生成Mg(OH)2和Al(OH)3,在180的时候Al(OH)3反应生成AlO2^-
Al(OH)3 + OH- = AlO2^- + 2H2O.得到Al(OH)3的质量为15.5 - 11.6 = 3.9g 氢氧化铝的物质的量为3.9/78 = 0.05mol,消耗氢氧根为0.05mol
11.6为氢氧化镁的质量Mg(OH)2,物质的量为11.6/58 = 0.2mol,则消耗氢氧根的量为0.4mol
共消耗氢氧化钠0.45mol.体积为0.45/5 x 1000 = 90ml
加上一开始中和盐酸的20ml,则在A点的体积为90+20 = 110ml
不够详细,很多都是文字,请见谅.
有问题欢迎追问.
希望我的回答能够对你有所帮助1年前查看全部
- 将质量分数为百分之a,物质的量浓度为c1 mol/L 的稀硫酸蒸发掉一定量的水,使其质量分数为百分之2a 此时若物质的量
将质量分数为百分之a,物质的量浓度为c1 mol/L 的稀硫酸蒸发掉一定量的水,使其质量分数为百分之2a 此时若物质的量浓度为c2 mol/L,则 C1 和 C2 关系为:A C2=2C1 B C1>2C2 C C2>2C1 D C1=2C2 .
还有一道:标准状况下 ,1体积水可溶解500体积HCl 气体,现用一只充满干燥 HCl 气体的烧瓶倒置在足量的水中,请回答下列问题:
若烧瓶中溶液没有扩散,其物质的量浓度为 :.
要有过程阿,我都想半天了,就是不会做.
还有就是顺便问一下 ,用量筒量取液体时 仰视和俯视 读数 会使测量结果 偏大或偏小的问题? 洞天杯蓝丝带1年前1
洞天杯蓝丝带1年前1 -
 fan樊 共回答了18个问题
fan樊 共回答了18个问题 |采纳率83.3%1、c
2、设烧瓶体积为V,物质的量浓度为:V/22.4/V=1/22.41年前查看全部
- 把氧化铜和铁粉的混合物放在一定量的稀硫酸中,反应停止后过滤除去不溶物,向滤液中加入一块薄铁片,观察不到
把氧化铜和铁粉的混合物放在一定量的稀硫酸中,反应停止后过滤除去不溶物,向滤液中加入一块薄铁片,观察不到
A.滤出的不溶物中只有铜,不可能含铁
B.滤出的不溶物中只有铁,不可能含铜
C.滤出的不溶物中一定含有铜,也可能含有铁
D.滤液中一定含有FeSO4,不可能有CuSO4和H2SO4
为什么答案上说C也是对的呢?哪有Cu? zhangyying1年前1
zhangyying1年前1 -
 若渝 共回答了22个问题
若渝 共回答了22个问题 |采纳率90.9%稀硫酸先和氧化铜反应生成CuSO4,因为稀硫酸是一定量的所以还有铁粉剩下,剩下的铁粉再和CuSO4发生反应,所以有Cu.1年前查看全部
- 称取软锰矿试样0.5000g,加入0.7500gH2C2O4·2H2O及稀硫酸,加热至反应完全.过量的草酸用30.00m
称取软锰矿试样0.5000g,加入0.7500gH2C2O4·2H2O及稀硫酸,加热至反应完全.过量的草酸用30.00mL0.02000mol/L的KMnO4溶液滴定至终点,求软锰矿的氧化能力(以已知)(8分)
 c1dt1ybg1年前1
c1dt1ybg1年前1 -
 youbear 共回答了24个问题
youbear 共回答了24个问题 |采纳率91.7%哦,擅长领域还是化学的呢?!
5H2C2O4.2H2O :2KMnO4
5*126.07 2
X 30/1000*0.02 X = 5*126.07*0.02/2/1000 = 0.1891g
MnO2 :H2C2O4.2H2O
86.94 126.07
Y 0.1891 Y = 86.94*0.1891/126.07 = 0.1304g
……1年前查看全部
- 依次向滤纸喷洒AB两种无色试剂.当喷洒A时,纸上出现一朵红色玫瑰.喷洒B时玫瑰消失.若B稀硫酸,则A为
 冬天戴草帽1年前1
冬天戴草帽1年前1 -
 程吟 共回答了26个问题
程吟 共回答了26个问题 |采纳率92.3%A是氢氧化钠,滤纸上有无色酚酞,酚酞遇到酸不变色,遇到碱变红色,所以一开始为红色,但后来喷了稀硫酸,将氢氧化钠反应了生成正盐NaCl,所以又变无色了.1年前查看全部
- 金属活动性的比较比较Fe、Cu、Ag的金属活动性,将三种金属片用导线两两连接,插入稀硫酸中为什么不行呢?
 余向秋1年前2
余向秋1年前2 -
 ee机遇安徽 共回答了15个问题
ee机遇安徽 共回答了15个问题 |采纳率93.3%铁的金属性可以利用原电池原理分别和铜、银连接鉴别活泼性,实际上氧化还原反应中是铁和硫酸制取氢的反应;而铜、银的活泼性比氢弱,故铜银两种金属的导线相连时,两种金属都排在氢后面两个电极都相当于不活泼电极.1年前查看全部
- 化学提问网站7克含杂质的锌可以跟100克9.8%稀硫酸溶液恰好反应,计算 1,该稀硫酸的溶质的质量是多少?2,可制的多少
化学提问网站
7克含杂质的锌可以跟100克9.8%稀硫酸溶液恰好反应,计算 1,该稀硫酸的溶质的质量是多少?2,可制的多少克氧气?3,反应后所得的溶液中溶质的质量分数是多少? 734530f9af070c471年前1
734530f9af070c471年前1 -
 风流不在人知 共回答了13个问题
风流不在人知 共回答了13个问题 |采纳率76.9%1.100X9.8%=9.8 g
2.m/M=9.8/98=0.1mol
由氢守恒 0.1mol H2SO4~0.1mol H2
0.1×2=.0.2 g
3.0.1mol H2SO4~0.1molZnSO4
溶质质量0.1×65=6.5 g
总的溶液质量 100+7-0.2=106.8 g
质量分数=6.5÷106.8=6.09%1年前查看全部
- 取50毫升稀硫酸与一定质量的镁铝合金反应,合金全部溶解,向所得溶液中滴加5mol/L的氢氧化钠溶液至过量,
取50毫升稀硫酸与一定质量的镁铝合金反应,合金全部溶解,向所得溶液中滴加5mol/L的氢氧化钠溶液至过量,
生成沉淀质量与加入氢氧化钠溶液体积关系如图,则原合金中镁的质量为?(沉淀最大值19.4克,沉淀最大值对应氢氧化钠的量为160毫升,最后沉淀为11.6克,对应氢氧化钠的量为180毫升.) 爱情三分球1年前1
爱情三分球1年前1 -
 习他们的 共回答了13个问题
习他们的 共回答了13个问题 |采纳率92.3%最后的沉淀为氢氧化镁,可以算出氢氧化镁物质的量为 11.6/58=0.2mol 所以Mg为0.2mol,为4.8g 沉淀最大时,应该是氢氧化铝和氢氧化镁共存,所以氢氧化铝质量为19.4-11.6=7.8g 其物质的量为 7.8/78=0.1mol 所以铝为2.7g1年前查看全部
- 了测定黄铜(铜,锌混合物)的组成,某研究性学习小组称取黄铜样品10g,向其中加入19.5百分号的稀硫酸50g
了测定黄铜(铜,锌混合物)的组成,某研究性学习小组称取黄铜样品10g,向其中加入19.5百分号的稀硫酸50g
完全反应后,称得烧杯中剩余的物质质量为59.9g.
①10g+50g-59.9g=0.1g表示( )的质量
②样品中铜的质量分数为( )
③通过计算反应后的溶液溶质中有无硫酸
麻烦哪位高手给我细细讲解下,我的化学真的不好~ 2727843451年前1
2727843451年前1 -
 clmmiky 共回答了17个问题
clmmiky 共回答了17个问题 |采纳率76.5%①10g+50g-59.9g=0.1g表示( 生成氢气 )的质量
铜与稀硫酸不反应
Zn+H2SO4=ZnSO4+H2
65 98 2
x y 0.1g
65/x=98/y=2/0.1g
x=3.25g
y=4.9g
②样品中铜的质量分数为(10g-3.25g)/10g*100%=67.5%
50g*19.5%=9.75g>4.9g
③反应后的溶液溶质中有硫酸1年前查看全部
- 取配置200g24.5%的稀硫酸,需_____g98%浓硫酸和_____g水,实际操作时,取98%浓硫酸____mL(精
取配置200g24.5%的稀硫酸,需_____g98%浓硫酸和_____g水,实际操作时,取98%浓硫酸____mL(精确到1mL)
 zrpbt20051年前1
zrpbt20051年前1 -
 好久没吃串串香 共回答了13个问题
好久没吃串串香 共回答了13个问题 |采纳率92.3%浓硫酸:200×0.245=49g
49÷0.98=50g
水:200-49=151g
v=50÷1.84=27.1ml
ok、1年前查看全部
- 将Cu与CuO固体混合物粉末放入烧杯中,当加入100克稀硫酸时,CuO与H2SO4好完全反应,过滤后所得溶液的质量为10
将Cu与CuO固体混合物粉末放入烧杯中,当加入100克稀硫酸时,CuO与H2SO4好完全反应,过滤后所得溶液的质量为108克,(不考虑过滤过程中溶液质量的损失).请分析并计算
(1)反应后溶液增加的质量为参加反应▁▁▁的质量.
(2)稀硫酸中含H2SO4的质量分数. 逍遥灵子1年前1
逍遥灵子1年前1 -
 aiya3602 共回答了19个问题
aiya3602 共回答了19个问题 |采纳率89.5%(1)cuo
(2)9.8%
因为反应后的物质没有气体等会溢出的东西,故增加的即为cuo质量
因为刚好完全反应,故列出反应式即可求得h2so4有9.8g1年前查看全部
- 〔急〕市售 黄金粉 是由Zn和Cu组成的合金粉,将此粉20g与93.7g稀硫酸充分反应,可得氢气0.2g.将反应后的混合
〔急〕
市售 黄金粉 是由Zn和Cu组成的合金粉,将此粉20g与93.7g稀硫酸充分反应,可得氢气0.2g.将反应后的混合物过虑,所虑出固体中只含Cu
1.求黄金粉中Zn的质量分数 amyloveamyhoho1年前1
amyloveamyhoho1年前1 -
 48480501 共回答了20个问题
48480501 共回答了20个问题 |采纳率100%Zn+H2SO4=ZnSO4+ H2↑
65 2
x 0.2
65/x=2/0.2,解得x=6.5
故黄金粉中含有6.5gZn,且质量分数为6.5/20*100%=32.5%1年前查看全部
- 小塑料块放在稀硫酸中,投入锌片塑料块上浮还是下沉
 天山牧羊1231年前3
天山牧羊1231年前3 -
 z0111 共回答了23个问题
z0111 共回答了23个问题 |采纳率95.7%上浮.
原来塑料的重力等于浮力.
投入锌片后,发生反应H2SO4 +Zn=ZnSO4 +H2
溶质是ZnSO4,密度变大,所以浮力变大.
那么塑料上浮.1年前查看全部
- 在天平的两个托盘上,分别放上质量相等的两只烧杯,在烧杯中分别加入同组成、同体积的稀硫酸(过量),此时天平呈平衡状态,然后
在天平的两个托盘上,分别放上质量相等的两只烧杯,在烧杯中分别加入同组成、同体积的稀硫酸(过量),此时天平呈平衡状态,然后分别向两只烧杯中加入等质量的碳酸钠和碳酸氢钠,反应终止后,天平两端的情况是?
A、 放Na2CO3的一端重
B、同样重
C、放NaHCO3的一端重
D、无法判断 乖乖的呆呆1年前4
乖乖的呆呆1年前4 -
 玻璃心馨 共回答了13个问题
玻璃心馨 共回答了13个问题 |采纳率92.3%因为酸过量,则产生气体的多少决定天平的高低.因为碳酸钠与碳酸氢钠质量相同,而摩尔质量碳酸钠是106g/mol,碳酸氢钠是84g/mol,所碳酸氢钠产生的CO2多.则放碳酸钠的一端重.1年前查看全部
- 关于铜片和稀硫酸的反应铜粉和稀硫酸加热不反应,但加入化合物X后,溶液逐渐变色.且质量增加,还放出气体,则X可能是?氯化钠
关于铜片和稀硫酸的反应
铜粉和稀硫酸加热不反应,但加入化合物X后,溶液逐渐变色.且质量增加,还放出气体,则X可能是?
氯化钠 硝酸钾 硫酸钠 碳酸钠? 长青131年前2
长青131年前2 -
 korla31g 共回答了21个问题
korla31g 共回答了21个问题 |采纳率81%硝酸钾
NO3-在酸性环境下具有硝酸性质,具有强氧化性
故加入硝酸钾后,会发生氧化还原反应
3Cu+8H+ +3NO3-=2Cu2+ +2NO+4H2O1年前查看全部
- 为了测定奶粉中蛋白质的含量,我们把蛋白质中的氧元素完全转化成氨气(化学式:NH3),再有稀硫酸吸收氨气,反应的化学方程式
为了测定奶粉中蛋白质的含量,我们把蛋白质中的氧元素完全转化成氨气(化学式:nh3),再有稀硫酸吸收氨气,反应的化学方程式为:
2nh3+h2so4=====(nh4)2so4,再根据蛋白质中氮元素的质量分数(约为16%)进行计算.
某监测站对某品牌奶粉检测时,取一定量该奶粉样品分解其中的蛋白质,产生的氨气用10g溶质质量分数为4.9%的稀硫酸恰好完全吸收.计算并回答下列问题.
(1)经过这种方法测的该奶粉样品中约含有蛋白质的质量是多少?(计算结果精确到0.01g,下同)
(2)如果该奶粉样品,有不法商贩向其中添加1g三聚***胺(c3n6h6),相当于增加蛋白质的质量为多少?
要过程啊! 逍遥情愿1年前1
逍遥情愿1年前1 -
 wangyang32 共回答了17个问题
wangyang32 共回答了17个问题 |采纳率88.2%根据 那个方程式 2NH3 +H2SO4 == (NH4)2SO4 10克 百分之4.9 的稀硫酸 10*百分之4.9 得到 稀硫酸的质量0.49克 稀硫酸的物质的量是98克每MOL 0.49 就是 0.05 MOL 根据方程式 计算 氨气 再算蛋白质
2 NH3 + H2SO4 =(NH4)2SO4
34 98 132
X 0.49
可求出 X=0.17g
(1)0.86
(2)0.831年前查看全部
- 33.如图是一个用来测定液密度的装置,A管插人的甲烧杯中,B管插人盛放加有紫色石蕊试液的稀硫酸的乙烧杯中
 nnlx1年前1
nnlx1年前1 -
 然犯 共回答了24个问题
然犯 共回答了24个问题 |采纳率91.7%A为两端开口的试管,B为一轻塑料片,烧杯中装有盐水,B在盐水中的深度是你的问题说清楚了吗?如果开始时将B堵在试管的一段,放在盐水中,由于盐水1年前查看全部
- 如何检验一种溶液是稀硫酸请带上化学方程式
 猴塞因1年前3
猴塞因1年前3 -
 gxwst 共回答了17个问题
gxwst 共回答了17个问题 |采纳率100%先加Ba(OH)2,如果得到不溶于酸的固体,说明有SO4(2-)根
再加Na2CO3,如果生成能使澄清石灰水变浑浊的气体,就说明有H+
所以就是H2SO4
Ba(OH)2+H2SO4=2H20+BaSO4↓
Na2CO3+H2SO4=H20+CO2↑+Na2SO4
CO2+Ca(OH)2=CaCO3↓+H201年前查看全部
- 现用质量分数为98%的浓硫酸配制280g质量分数为14%的稀硫酸时,需要在浓硫酸中加____毫升水.
 清茶微风1年前1
清茶微风1年前1 -
 xunuonn 共回答了10个问题
xunuonn 共回答了10个问题 |采纳率80%设需要98%的浓硫酸的质量为X
则:X*98%=280g*14% X=40克
水的质量为:280-40=240克
水的体积为240/1=240毫升1年前查看全部
- 氧化铜加稀硫酸 加热硫酸铜晶体 搅拌食盐 三个实验的实验报告单,
 wzhao888881年前1
wzhao888881年前1 -
 edwardzs 共回答了17个问题
edwardzs 共回答了17个问题 |采纳率82.4%CuO+H2SO4=CuSO4+H2O 固体氧化铜被溶解掉了生成蓝色溶液CuSO4
CuSO4.5H2O=△=CuSO4+5H2O 熔融产生水,持续加热水分完全蒸发,只剩下CuSO4
水中加入食盐的话搅拌可以使溶解更快1年前查看全部
- 除去二氧化氮中的少量氨气,用浓硫酸还是稀硫酸,为什么?
 zier1年前4
zier1年前4 -
 yc_nicson 共回答了5个问题
yc_nicson 共回答了5个问题 |采纳率100%用浓硫酸; 稀硫酸含水多会和二氧化氮反应H2O+3NO2=2HNO3+NO .浓硫酸含水极少不和二氧化氮反应、但和氨反应2NH3+H2SO4=(NH4)2SO41年前查看全部
大家在问
- 1谁能帮我用中文翻译一下这段英文?
- 2初一上学期的数学题把12的两个数字对调,得到21.一个两位数,十位上的数字是a,个位上的数字是b,把他们对调,得到另一个
- 3(2012•恩施州)某一反应微观示意图如图所示,已知乙是双原子分子.则从图示获得的信息中,错误的是 ( )
- 4两滴水银互相接近时能自动结合成一滴较大的水银,这一事实说明分子之间存在______.
- 5He is very cool.改感叹句(what,how两句)
- 6读“亚洲大陆地形剖面图”,回答13--14题.
- 7用杠杆把400N的物体提高0.5m,此时动力作用点下降了2m,如果动力是120N,求动力做的总功、有用功、额外功和机械效
- 8夺冠100分作业本第38页第7题,2个长方形,2个正方形,2个圆柱,2个球形可以有那三种分法
- 9以巜新学期学习一个月来的感受》为题写一篇作文
- 10在新世纪,在历史的神韵和现代文明下将使杭州成为一个充满希望、最具潜力的城市.
- 11测电流表·电压表内阻的问题【追加】
- 12Fe在空气中变成Fe(OH)2的化学方程式
- 13如图所示,下列说法中错误的是( )
- 14下列说法错误的是( ) A.冬天教室内二氧化碳的含量比夏天教室内的二氧化碳含量高 B.晚上树林中二氧化碳的含量比阳光下
- 15我对英语很感兴趣 翻译成英语
