Na2O2做供氧剂时,能不能仿照H2O2,把化学式写成2Na2O2=(催化剂)=2H2O+O2?
 爱如空气k2022-10-04 11:39:543条回答
爱如空气k2022-10-04 11:39:543条回答我在书上看到化学方程式为2Na2O2+2CO2=2Na2CO3+O2

已提交,审核后显示!提交回复
共3条回复
 苏州第一次 共回答了16个问题
苏州第一次 共回答了16个问题 |采纳率93.8%- 因为过氧化钠做供氧剂时,通常是在航天飞船中或航海船舱中,要把人呼出的二氧化碳除去并重新利用,所以书上的化学方程式会那样写.过氧化钠还可以和水反应生成氢氧化钠,方程式你以后会学到.所以应该还是按照课本来写,因为你的方程式原理并不正确.
- 1年前
 蚂蚁的爱情820 共回答了179个问题
蚂蚁的爱情820 共回答了179个问题 |采纳率- 要根据实际反应来,不能随便替换。比如你写的那个方程式中Na2O2变成H2O和O2根本是不可能的,Na去哪了?H是从哪来的?
- 1年前
 ekenlin 共回答了3个问题
ekenlin 共回答了3个问题 |采纳率- 因为过氧化钠做供氧剂时,通常是在航天飞船中或航海船舱中,要把人呼出的二氧化碳除去并重新利用,所以书上的化学方程式会那样写。过氧化钠还可以和水反应生成氢氧化钠,方程式你以后会学到。所以应该还是按照课本来写,因为你的方程式原理并不正确。是不是化学方程式只能靠背?
我在解题过程中倘若忘记课本怎么写,怎么办?
这道题前有一道题是问H2O2的方程式,我在写Na2O2时就被误导了其实经过一段时... - 1年前
相关推荐
- 下列说法不正确的是( ) A.钠在氧气中燃烧生成淡黄色的固体Na 2 O 2 ,可做为呼吸面具的供氧剂 B.液氯是氯气
下列说法不正确的是( ) A.钠在氧气中燃烧生成淡黄色的固体Na 2 O 2 ,可做为呼吸面具的供氧剂 B.液氯是氯气的水溶液,它能使干燥的有色布条褪色 C.氯气能与大多数金属化合,生成金属氯化物(盐) D.氯水具有杀菌、漂白作用是因氯水中含有强氧化性的次氯酸  michael__x1年前1
michael__x1年前1 -
 鱼过冬 共回答了15个问题
鱼过冬 共回答了15个问题 |采纳率80%A、过氧化钠和人呼出的二氧化碳气体发生反应:2Na 2 O 2 +2CO 2 =Na 2 CO 3 +O 2 ↑可作为呼吸面具中的供氧剂,故A正确;
B、液态氯是纯净物,没有水不能生成次氯酸,不能使干燥的有色布条褪色,故B错误;
C、氯气是典型的具有强氧化性的非金属单质,易与大多数金属化合生成氯化物,故C正确;
D、氯水中发生反应Cl 2 +H 2 O=HCl+HClO,次氯酸是一种强氧化性的漂白剂,具有杀菌、消毒、漂白的作用,故D正确;
故选B.1年前查看全部
- 潜水面具中的供氧剂是
 libzhi1年前1
libzhi1年前1 -
 aaaa678678 共回答了19个问题
aaaa678678 共回答了19个问题 |采纳率84.2%Na2O21年前查看全部
- 潜水艇中常用过氧化钠作为供氧剂,因为过氧化钠可吸收co2生成碳酸钠放出氧气求44克co2与na2o2所释放氧气
潜水艇中常用过氧化钠作为供氧剂,因为过氧化钠可吸收co2生成碳酸钠放出氧气求44克co2与na2o2所释放氧气
2Na2O2==2Na2CO3+O2 qno5847s_f_373c1年前1
qno5847s_f_373c1年前1 -
 a19820829 共回答了10个问题
a19820829 共回答了10个问题 |采纳率100%2Na2O2+2CO2==2Na2CO3+O2
88 32
44g xg
设产生x克氧气.
44g/88=xg/32
x=16
所以产生氧气16g1年前查看全部
- 供氧剂与二氧化碳反应的方程式
 y_seven1年前1
y_seven1年前1 -
 黔龙家园 共回答了17个问题
黔龙家园 共回答了17个问题 |采纳率94.1%2Na2O2 +2CO2 ==2Na2CO3 +O21年前查看全部
- 用于潜水艇或防毒面具作为供氧剂的是什么?
 pwzsu1年前1
pwzsu1年前1 -
 stsw2046 共回答了19个问题
stsw2046 共回答了19个问题 |采纳率94.7%Na2O21年前查看全部
- 在呼吸面具和潜水艇中可以用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,用图中实验装置,进行实验来
在呼吸面具和潜水艇中可以用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,用图中实验装置,进行实验来证明过氧化钠可作供氧剂.其中,A是实验室制取CO 2 的装置,D中装有过氧化钠固体. 
(1)写出A装置中发生反应的离子方程式:______;
(2)填写表中空格:
(3)若无C装置,对实现该实验目的是否有影响______(填“是”或“否”),原因______;仪器 加入试剂 加入该试剂的目的 B 饱和NaHCO 3 溶液
______C
______除去CO 2 中的水蒸气 E
______
______
(4)试管F中收集满气体并从水中取出后,下一步实验操作为:______. 发财金宝11年前1
发财金宝11年前1 -
 llllaaaa02 共回答了22个问题
llllaaaa02 共回答了22个问题 |采纳率81.8%(1)A为由CaCO 3 和盐酸反应生成CO 2 ,反应的化学方程式为CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2 ↑,
故答案为:CaCO 3 +2HCl=CaCl 2 +H 2 O+CO 2 ↑;
(2)产生气体通过饱和NaHCO 3 溶液,以除去CO 2 气体中混入的HCl,然后过氧化钠与CO 2 和水气反应,产生O 2 ,由于生成的氧气中混有二氧化碳气体,应用NaOH溶液洗气,吸收未反应的CO 2 气体,用排水法收集O 2 ;
故答案为:
仪器 加入试剂 加入该试剂的目的
B 除去CO 2 气体中混入的HCl
C 浓硫酸
D NaOH溶液 除去O 2 中的CO 2 (3)若无C装置,对实现该实验目的无影响,因为水蒸气和过氧化钠也反应生成氧气,反应的化学方程式为:2Na 2 O 2 +2H 2 O=4NaOH+O 2 ;
故答案为:否,2Na 2 O 2 +2H 2 O=4NaOH+O 2 ;
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气;
故答案为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.1年前查看全部
- 与学过的制氧气的方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是(从两个不同角度回
 我已麻木麻木1年前1
我已麻木麻木1年前1 -
 浮如流水 共回答了13个问题
浮如流水 共回答了13个问题 |采纳率92.3%1.反应在常温下进行2.消耗人体呼出的二氧化碳,并且反应不断持续1年前查看全部
- 已知,过氧化钠(化学式为Na 2 O 2 )是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂利用人呼出的二氧化碳与过氧化钠
已知,过氧化钠(化学式为Na 2 O 2 )是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂利用人呼出的二氧化碳与过氧化钠反应放出氧气,供给人的正常生命活动,该反应的化学方程式为:2Na 2 O 2 +2CO 2 =2 +O 2 (在横线上填写化学式)。某同学利用该反应原理制取氧气,设计实验装置如下图所示:

(1)装置①中CO 2 的制取方法有多种:
若用加热NaHCO 3 固体制取CO 2 ,应该选用的发生装置为 (选填下图字母)
(2)装置③中盛装的试剂为 ,作用是 。
(3)④为O 2 的收集装置,可选用装置 (选填上图字母)。 sdgerew1年前1
sdgerew1年前1 -
 必吐 共回答了19个问题
必吐 共回答了19个问题 |采纳率89.5%Na 2 CO 3 ;(1)A;(2)氢氧化钠溶液;除去二氧化碳。(3)D。
1年前查看全部
- 超氧化钾和二氧化碳反应生成氧气,在医院,矿井,潜水,飞行中用作供氧剂.13.2L(标况下)二氧化碳和超氧化钾反应后,气体
超氧化钾和二氧化碳反应生成氧气,在医院,矿井,潜水,飞行中用作供氧剂.13.2L(标况下)二氧化碳和超氧化钾反应后,气体体积变为18.8L(标况),计算反应消耗的超氧化钾质量,我知道结果是71g,网上查过了,就是不理解,麻烦讲的详细些
 羲和1年前1
羲和1年前1 -
 lixiaoyun123 共回答了9个问题
lixiaoyun123 共回答了9个问题 |采纳率88.9%4KO2(s)+2CO2(g)=2K2CO3(s)+3O2 (g)每四MOL的KO2 造成1mol的体积增大 现在体积增大
18.8-13.2=0.25 所以有0.25*4=1mol的KO2反应 所以 是71g1年前查看全部
- 呼吸面具中常用的供氧剂是过氧化钠(化学式为Na 2 O 2 ),它与人呼出的CO 2 能反应产生氧气,反应的化学方程式为
呼吸面具中常用的供氧剂是过氧化钠(化学式为Na 2 O 2 ),它与人呼出的CO 2 能反应产生氧气,反应的化学方程式为2Na 2 O 2 +2CO 2 ═Na 2 CO 3 +O 2 .过氧化钠还能与盐酸、水等物质发生反应产生氧气.为了验证Na 2 O 2 能和CO 2 反应产生氧气,某化学兴趣小组的同学设计了如图所示的实验. 
(1)写出有标号仪器的名称:a______,b______.
(2)实验室用石灰石和稀盐酸反应制取CO 2 的化学方程式是______,装置A可选用下面提供的______ (填序号)装置.
(3)连接好实验装置后,应先______,再装入药品.
(4)装置B中盛放的饱和NaHCO 3 溶液的作用是______.
(5)为了吸收未反应的CO 2 ,装置D中应盛放的试剂是______,反应的化学方程式为:______.
(6)装置E中收集气体的方法是______;为了验证收集到的气体是氧气,仪器a中收集满气体后接下来的实验操作是______.
(7)通过以上实验能否确定收集到的O 2 是由Na 2 O 2 与CO 2 反应生成的?______(填“能”或“不能”).若能,请简述理由;若不能请提出你对实验的改进意见:______. 快乐笨宝宝1年前1
快乐笨宝宝1年前1 -
 Li761200 共回答了22个问题
Li761200 共回答了22个问题 |采纳率68.2%(1)题中所给的仪器名称为:a、试管,b、水槽;
(2)碳酸钙与稀盐酸反应生成了二氧化碳、氯化钙和水,所以可以写出该反应的化学方程式,该反应在常温下即可反应,所以应该选择装置③作为发生装置;
(3)在装入药品之前应该先检查装置的气密性;
(4)在二氧化碳逸出的过程中会带出一部分氯化氢气体,所以为了防止氯化氢干扰实验现象,所以用饱和的碳酸氢钠溶液来吸收氯化氢;
(5)吸收二氧化碳常用氢氧化钠溶液,它们反应生成了碳酸钠和水,可以写出该反应的化学方程式;
(6)氧气难溶于水,所以装置图中用的是排水法收集的,而氧气可以支持燃烧,所以检验该气体是否为氧气,可以用带火星的木条来进行检验;
(7)从题给的信息可以知道,水也可以和过氧化钠反应生成氧气,所以不能确定该气体是二氧化碳与过氧化钠反应得到的,为了排除水的干扰,使实验结果更有说服力,应该在B和C装置之间添加一个除水的装置.
故答案为:(1)试管;水槽;
(2)CaCO 3 +2HCl═CaCl 2 +H 2 O+CO 2 ↑;③;
(3)检查装置的气密性;
(4)吸收二氧化碳中混有的氯化氢;
(5)氢氧化钠溶液;2NaOH+CO 2 ═Na 2 CO 3 +H 2 O;
(6)排水法;用拇指堵住试管口,取出试管,将带火星的木条伸入试管中,木条复燃,证明收集到的气体时氧气;
(7)不能;再B和C之间添加一个除水的装置.1年前查看全部
- K2O2是一种常见氧化剂、供氧剂,下列说法中正确的是( )
K2O2是一种常见氧化剂、供氧剂,下列说法中正确的是( )
A.1mol的K2O2中含有3NA个σ键
B.将一定量K2O2是投入含酚酞的水溶液中,反应剧烈,溶液先变红后可能褪色
C.K2O2是一种碱性氧化物
D.1mol K2O2参加的氧化还原反应中,完全转化,转移的电子数一定为2NA smx6881年前1
smx6881年前1 -
 happy_lxy 共回答了21个问题
happy_lxy 共回答了21个问题 |采纳率76.2%解题思路:K2O2和Na2O2相似,含有离子键和非极性共价键,具有强氧化性,可与水反应生成氢氧化钾和氧气,结合反应的方程式2K2O2+2H2O=4KOH+O2解答该题.A.K2O2和Na2O2相似,含有离子键和非极性共价键,1mol的K2O2中含有1NA个σ键,故A错误;
B.K2O2具有强氧化性,可与水反应生成氢氧化钾和氧气,投入含酚酞的水溶液中,反应剧烈,溶液先变红后可能褪色,故B正确;
C.与水反应生成氢氧化钾和氧气,不是碱性氧化物,故C错误;
D.反应的方程式为2K2O2+2H2O=4KOH+O2,反应物K2O2中,O元素化合价分别由-1价变化为0价、-2价,1mol K2O2参加的氧化还原反应中,完全转化,转移的电子数一定为1NA,故D错误.
故选B.点评:
本题考点: 氧化还原反应;共价键的形成及共价键的主要类型.
考点点评: 本题考查过氧化钾知识,为高频考点,侧重于学生的分析能力的考查,注意对比过氧化钠的性质解答该题,难度中等.1年前查看全部
- 过氧化钠作为供氧剂的最大优点是什么
 goodzyh1年前1
goodzyh1年前1 -
 啊恩恩 共回答了18个问题
啊恩恩 共回答了18个问题 |采纳率88.9%除去可能过量的二氧化碳呗!,你肯定知道 用
作为供氧剂,原理是:2Na2O2 + 2H2O ====4NaOH + O2,生成氧气后,把氧气通入NaOH显然是除去二氧化碳,保证氧气纯净1年前查看全部
- 过氧化钠用于航空航天和潜水艇中作为供氧剂的主要原因?
 9680561年前2
9680561年前2 -
 Roger1001 共回答了15个问题
Roger1001 共回答了15个问题 |采纳率93.3%过氧化钠即能吸收人类呼吸产生的二氧化碳,又能生成人类生存活动所必需的氧气,故能作为供氧剂.反应方程式如下:
2Na2O2+2C02=2Na2CO3+O21年前查看全部
- 为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.
 为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.
为证明Na2O2可作为潜水艇的供氧剂,某化学小组在实验室模拟CO2与Na2O2反应产生氧气的实验.
(1)生成CO2的化学反应方程式:______
(2)饱和碳酸氢钠溶液的作用是除去CO2中混有的HCl气体,浓H2SO4的作用是______
(3)U形管中的现象是______,反应方程式为______. 伊人遥遥1年前1
伊人遥遥1年前1 -
 我猜火车 共回答了14个问题
我猜火车 共回答了14个问题 |采纳率92.9%解题思路:(1)实验室用CaCO2和稀HCl制取CO2;
(2)浓硫酸具有吸水性;
(3)CO2和Na2O2反应生成白色固体Na2CO3,同时生成无色气体.(1)实验室用CaCO2和稀HCl制取CO2,反应方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O,故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;(2)浓硫酸具有吸水性,且和二氧化碳不反应,所以浓硫酸作干燥剂,故答案为:作干燥剂;(3)...
点评:
本题考点: 钠的重要化合物.
考点点评: 本题考查了探究过氧化钠和二氧化碳的反应,明确二氧化碳制取、过氧化钠和二氧化碳的反应原理即可解答,能从整体上分析装置中各个仪器的作用,题目难度不大.1年前查看全部
- Na2o2可作为潜水密封舱中的供氧剂,计算1kgna2o2可供养给潜水员多少升氧气,在标准状况下
 无薪侩语1年前4
无薪侩语1年前4 -
 狼族伊 共回答了21个问题
狼族伊 共回答了21个问题 |采纳率76.2%2 Na2O2 + 2 H2O== 4 NaOH + O2
1000/78*2 x
1000/78*2=x
x=25.64mol
V=25.64*22.4=574L1年前查看全部
- (4分)(2012•广东)下列应用不涉及氧化还原反应的是( ) A.Na 2 O 2 用作呼吸面具的供氧剂 B.工业上
(4分)(2012•广东)下列应用不涉及氧化还原反应的是( )
A.Na 2 O 2 用作呼吸面具的供氧剂 B.工业上电解熔融状态的Al 2 O 3 制备Al C.工业上利用合成氨实现人工固氮 D.实验室用NH 4 Cl和Ca(OH) 2 制备NH 3  韩45131年前1
韩45131年前1 -
 dd客与剑客 共回答了19个问题
dd客与剑客 共回答了19个问题 |采纳率89.5%D
氧化还原反应的本质特征是反应前后元素化合价的发生变化;依据元素化合价变化分析判断;
A、Na 2 O 2 用作呼吸面具的供氧剂,过氧化钠和二氧化碳反应生成碳酸钠和氧气,发生了氧化还原反应,故A不符合;
B、工业上电解熔融状态的Al 2 O 3 制备Al,是电解氧化铝发生氧化还原反应,故B不符合;
C、工业上利用合成氨实现人工固氮,是单质气体单质和氢气化合生成氨气,发生了氧化还原反应,故C不符合;
D、NH 4 Cl和Ca(OH) 2 制备NH 3 是复分解反应,故D符合;
故选D.1年前查看全部
- (2011•石景山区二模)超氧化钾(KO2)能与二氧化碳反应生成氧气,常用于医疗、潜水、高空飞行中的供氧剂,该反应的化学
(2011•石景山区二模)超氧化钾(KO2)能与二氧化碳反应生成氧气,常用于医疗、潜水、高空飞行中的供氧剂,该反应的化学方程式为4KO2+2CO2═2K2CO3+3O2.若要得到9.6g氧气,请计算参加反应的超氧化钾质量.
 言岩1年前1
言岩1年前1 -
 宁水花园的双鱼 共回答了20个问题
宁水花园的双鱼 共回答了20个问题 |采纳率80%解题思路:依据题给化学方程式及已知氧气质量,求得参加反应的超氧化钾质量设参加反应的超氧化钾质量为x.
4KO2+2CO2═2K2CO3+3O2
284 96
x 9.6g
[284/x=
96
9.6g]
x=28.4g
答:参加反应的超氧化钾质量为28.4g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题依据题给信息,根据化学方程式进行解答计算即可,注意解题格式、步骤.1年前查看全部
- 为什么过氧化钠可作供氧剂而氧化钠不行?
 optc21年前1
optc21年前1 -
 annzeng041129 共回答了17个问题
annzeng041129 共回答了17个问题 |采纳率88.2%过氧化钠和水或二氧化碳能生成氧气;氧化钠和水只能生成氢氧化钠,与二氧化碳生成碳酸钠1年前查看全部
- 过氧化钠常用作呼吸面具和潜水艇中的供氧剂,是由于过氧化钠与二氧化碳反应生成碳酸钠和氧气.写出该反应的
 上网四顾心茫然1年前2
上网四顾心茫然1年前2 -
 贝贝1923 共回答了15个问题
贝贝1923 共回答了15个问题 |采纳率100%2Na2O2+2CO2=2Na2CO3+O21年前查看全部
- (2009•泸州)过氧化钠(Na2O2)固体是登山队员常用的供氧剂,它能和CO2反应生成Na2CO3和O2(2Na2O2
(2009•泸州)过氧化钠(Na2O2)固体是登山队员常用的供氧剂,它能和CO2反应生成Na2CO3和O2(2Na2O2+2CO2=2Na2CO3+O2↑),产生O2供人呼吸.试计算:(计算结果保留一位小数)
(1)312gNa2O2与足量CO2反应可产生氧气______g;
(2)若将156gNa2O2投入500g水中,发生反应(2Na2O2+2H2O=4NaOH+O2↑)后,溶液中NaOH溶质的质量是多少克?所得NaOH溶液的质量分数是多少? caffer1年前1
caffer1年前1 -
 灰猫王 共回答了20个问题
灰猫王 共回答了20个问题 |采纳率95%解题思路:(1)化学反应中,反应物和生成物之间存在一定的质量关系,这种质量关系与物质的相对分子量和物质的化学计量密不可分.因此,化学反应中的有关计算,可以根据化学方程式中物质之间恒定的质量比进行.Na2O2与CO2反应可产生氧气,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2↑,根据过氧化钠和氧气的相对分子量,列比利式即可求得312gNa2O2与足量CO2反应可产生氧气的质量.
(2)将156gNa2O2投入500g水中,一要考虑156gNa2O2是不是全部反应掉;二要注意反应后产生的氧气会逃逸掉,不存在溶液中.再根据发生反应的化学方程式:2Na2O2+2H2O=4NaOH+O2↑找出已知质量和未知量之间的关系,由溶质的质量分数=[溶质的质量/溶液的质量]×100%
即可求得正确答案.(1)根据化学方程式,找出已知质量和未知量之间的关系
2Na2O2+2CO2=2Na2CO3+O2↑
2×782×16
312 x
列比利式求解
[2×78/2×16]=[312/x]
x=[312×8/39]=64.0(克)
故答案为:64.0克
(2)设156gNa2O2充分反应需水x克,根据化学方程式,找出已知质量和未知量之间的关系
2Na2O2+2H2O=4NaOH+O2↑
2×78 2×18
156 x
列比利式求解
[2×78/2×18]=[156/x]
x=[156×9/39]=36(克)
解得156gNa2O2充分反应需水36克,36克远远小于500克,也就是说156gNa2O2投入500g水中会全部反应掉.
再设156gNa2O2投入500g水中生成NaOH y克、O2z克,根据化学方程式,找出已知质量和未知量之间的关系
2Na2O2+2H2O=4NaOH+O2↑
2×78 4×40 2×16
156 y z
列比利式求解
[2×78/4×40]=[156/y]
[2×78/2×16]=[156/z]
y=[156×40/39]=160(克) z=[156×8/39]=32(克)
解得156gNa2O2投入500g水中生成NaOH160克、氧气32克.而氧气不易溶于水会逃逸掉,不存在反应后的溶液中.
由 溶质的质量分数=[溶质的质量/溶液的质量]×100%
得NaOH溶液的质量分数=[160/156+500−32]×100%≈25.6%
答:溶液中NaOH溶质的质量是160克,所得NaOH溶液的质量分数约为25.6%.点评:
本题考点: 根据化学反应方程式的计算;有关溶质质量分数的简单计算.
考点点评: 本题主要是结合溶质的质量分数,考察了化学反应中根据化学方程式的有关计算.元素的相对原子量一般会在题干之外注明,但是常见原子的相对原子量一定要熟记,它便于我们在计算中应用.本题设置生活情境,使我们曾强了对这一学科实用性的认识.这将会成为今后命题的一个趋向.1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某课外小组模拟其原理选用适当的化学试剂和实验用品,用下图中的实验装置进行实验
 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某课外小组模拟其原理选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明潮湿的CO2可与过氧化钠反应生成O2.
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某课外小组模拟其原理选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明潮湿的CO2可与过氧化钠反应生成O2.
可供选择的药品有:石灰石、盐酸、饱和NaHCO3溶液、NaOH溶液、Na2O2固体
(1)A是制取CO2的装置,写出A中发生反应的化学方程式______.
(2)填写表中空格:
(3)写出过氧化钠与二氧化碳反应的化学方程式______.仪器 加入试剂 加入该试剂的目的 B 饱和NaHCO3溶液 ______ C ______ ______ D ______ ______
(4)试管F中收集满气体后,要用拇指堵住试管口,移出水面,接下来的操作是______. johnson19841年前1
johnson19841年前1 -
 火舞云霄 共回答了14个问题
火舞云霄 共回答了14个问题 |采纳率85.7%解题思路:由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,用排水法收集O2,最后取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.(1)A为由CaCO3和盐酸反应生成CO2,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,或由NaHCO3和盐酸反应生成CO2,方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑;
故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑或NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,由于生成的氧气中混有二氧化碳气体,应用NaOH溶液洗气,吸收未反应的CO2气体,用排水法收集O2,
故答案为:
仪器 加入试剂 加入该试剂的目的
B 饱和NaHCO3溶液 除去CO2气体中混入的HCl
C 过氧化钠 与CO2和水气反应,产生O2
D NaOH溶液 吸收未反应的CO2气体(3)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气,
故答案为:立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.点评:
本题考点: 钠的重要化合物.
考点点评: 本题考查过氧化钠的性质的实验设计,题目难度不大,解答本题注意把握实验原理和相关实验的基本操作,注意除杂的先后顺序和检验氧气的操作方法.1年前查看全部
- (2013•烟台)过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供氧剂,人呼出气体主要成分有氮气、二氧化碳
(2013•烟台)过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供氧剂,人呼出气体主要成分有氮气、二氧化碳、水蒸气和氧气,
Na2O2能分别与CO2、H2O反应,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2↑;2Na2O2+2H2O=4NaOH+O2↑.某化学兴趣小组的同学开展了以下探究活动.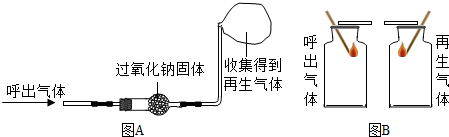
【实验探究一】将呼出气体通过下图A 中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如下图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较______来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是______.
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH;猜想Ⅱ:溶质是______;猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,产生______的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
实验步骤和现象 结论 猜想Ⅲ成立  单翼女子1年前1
单翼女子1年前1 -
 dakylau 共回答了18个问题
dakylau 共回答了18个问题 |采纳率88.9%【分析讨论】图B的实验是将燃着的木条分别伸入呼出气体和再生气体中,通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少;过氧化钠能与二氧化碳反应生成氧气,因此呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点:吸收呼吸产生的二氧化碳,同时生成氧气;
故答案为:木条燃烧的剧烈程度;吸收呼吸产生的二氧化碳,同时生成氧气;
【提出猜想】人呼出气体中有二氧化碳、水蒸气,而过氧化钠和二氧化碳反应生成碳酸钠,和水反应生成氢氧化钠
,因此图A装置中的残留固体溶于水,可能形成的是碳酸钠溶液、可能是氢氧化钠溶液、也可能是两着的混合溶液;
故答案为:Na2CO3;
【实验探究二】碳酸钠和氢氧化钙反应生成碳酸钙沉淀,因此取上述溶液少许于试管中,滴加澄清石灰水,产生石灰水变浑浊,说明溶液中含有碳酸钠,可证明猜想Ⅰ不成立;
氯化钙溶液显中性,氯化钙可与碳酸钠反应产生白色沉淀,因此取无色溶液少许于试管中,向其中加入过量(目的是将碳酸钠完全反应掉)的氯化钙溶液,有白色沉淀产生,说明有碳酸钠,过滤,再向滤液中加入无色酚酞试液,溶液变红,说明有氢氧化钠,证明猜想Ⅲ成立;
故答案为:Na2CO3;
取无色溶液少许于试管中,向其中加入过量的氯化钙溶液,有白色沉淀产生,过滤,再向滤液中加入无色酚酞试液,溶液变红1年前查看全部
- 已知过氧化钠(Na2O2)是一种淡黄色固体,常温下可与二氧化碳反应生成碳酸钠和氧气,因而常用在防毒面具里作为供氧剂.请写
已知过氧化钠(Na2O2)是一种淡黄色固体,常温下可与二氧化碳反应生成碳酸钠和氧气,因而常用在防毒面具里作为供氧剂.请写出该反应的化学方程式:______.
 guoling1年前1
guoling1年前1 -
 cheng8791 共回答了15个问题
cheng8791 共回答了15个问题 |采纳率86.7%解题思路:根据题意,过氧化钠(Na2O2)常温下可与二氧化碳反应生成碳酸钠和氧气,写出反应的化学方程式即可.过氧化钠(Na2O2)常温下可与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2.
故答案为:2Na2O2+2CO2═2Na2CO3+O2.点评:
本题考点: 书写化学方程式、文字表达式、电离方程式.
考点点评: 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.1年前查看全部
- (2010•南沙区一模)Na2O2常用作潜艇中的供氧剂,是由于它和人呼出的CO2、水蒸气反应可放出氧气,下列有关对该化合
(2010•南沙区一模)Na2O2常用作潜艇中的供氧剂,是由于它和人呼出的CO2、水蒸气反应可放出氧气,下列有关对该化合价判断正确的是( )
A.Na、O均呈0价
B.Na呈+2价,O呈-1价
C.Na呈+1价,O呈-2价
D.Na呈+1价,O呈-1价 丁在右耳的鱼1年前1
丁在右耳的鱼1年前1 -
 wude1213 共回答了20个问题
wude1213 共回答了20个问题 |采纳率85%解题思路:根据物质Na2O2的化学式及钠在化合物中的化合价为+1价,只要符合化合物中元素的正负化合价的代数和为0即为正确答案.A、因在单质中元素的化合价为0,而在化合物中Na为正价、O为负价,故A错误;
B、由化学式,根据化合价计算原则,(+2)×2+(-1)×2≠0,故B错误;
C、由化学式,根据化合价计算原则,(+1)×2+(-2)×2≠0,故C错误;
D、由化学式,根据化合价计算原则,(+1)×2+(-1)×2=0,故D正确;
故选D.点评:
本题考点: 有关元素化合价的计算;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 本题考查物质中元素化合价的计算,学生应能根据化学式和提供的元素的化合价及化合物中元素的正负化合价的代数和为0来分析判断.1年前查看全部
- 下列应用不涉及氧化还原反应的是 A.Na 2 O 2 用作呼吸面具的供氧剂 B.实验室用浓盐酸和MnO 2 制备Cl 2
下列应用不涉及氧化还原反应的是
A.Na 2 O 2 用作呼吸面具的供氧剂 B.实验室用浓盐酸和MnO 2 制备Cl 2 C.工业上利用硫酸吸收氨气制备氮肥 D.自来水厂用C lO 2 杀菌消毒  乱侃魏晋1年前1
乱侃魏晋1年前1 -
 赵婷蕾 共回答了17个问题
赵婷蕾 共回答了17个问题 |采纳率94.1%C
1年前查看全部
- (2013•烟台)过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供氧剂,人呼出气体主要成分有氮气、二氧化碳
(2013•烟台)过氧化钠(Na2O2)为淡黄色固体,可作为潜水艇或呼吸面具的供氧剂,人呼出气体主要成分有氮气、二氧化碳、水蒸气和氧气,
Na2O2能分别与CO2、H2O反应,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2↑;2Na2O2+2H2O=4NaOH+O2↑.某化学兴趣小组的同学开展了以下探究活动.
【实验探究一】将呼出气体通过下图A 中的装置,收集得到一瓶再生气体.在收集一瓶呼出的气体.将两支燃着的同种木条分别同时伸入呼出气体和再生气体中,如下图B,比较分析呼出气体和再生气体中氧气含量的多少.
【分析讨论】图B的实验是通过比较木条燃烧的剧烈程度木条燃烧的剧烈程度来比较两种气体中氧气含量的多少.请说明呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点是吸收呼吸产生的二氧化碳,同时生成氧气吸收呼吸产生的二氧化碳,同时生成氧气.
实验探究一结束后,同学们将图A装置中的残留固体溶于水,得到了一杯无色溶液,他们对溶液的溶质成分进行探究:
【提出猜想】猜想Ⅰ:溶液是NaOH;猜想Ⅱ:溶质是Na2CO3Na2CO3;猜想Ⅲ:溶质是NaOH和Na2CO3
【实验探究二】取上述溶液少许于试管中,滴加澄清石灰水,产生浑浊浑浊的现象,证明猜想Ⅰ不成立.
同学们经过实验探究证明猜想Ⅲ成立,请你写出证明猜想Ⅲ成立的实验步骤和现象.
实验步骤和现象 结论 猜想Ⅲ成立  思hh高娃1年前1
思hh高娃1年前1 -
 xrdswu 共回答了21个问题
xrdswu 共回答了21个问题 |采纳率90.5%【分析讨论】图B的实验是将燃着的木条分别伸入呼出气体和再生气体中,通过比较木条燃烧的剧烈程度来比较两种气体中氧气含量的多少;过氧化钠能与二氧化碳反应生成氧气,因此呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点:吸收呼吸产生的二氧化碳,同时生成氧气;
故答案为:木条燃烧的剧烈程度;吸收呼吸产生的二氧化碳,同时生成氧气;
【提出猜想】人呼出气体中有二氧化碳、水蒸气,而过氧化钠和二氧化碳反应生成碳酸钠,和水反应生成氢氧化钠
,因此图A装置中的残留固体溶于水,可能形成的是碳酸钠溶液、可能是氢氧化钠溶液、也可能是两着的混合溶液;
故答案为:Na2CO3;
【实验探究二】碳酸钠和氢氧化钙反应生成碳酸钙沉淀,因此取上述溶液少许于试管中,滴加澄清石灰水,产生石灰水变浑浊,说明溶液中含有碳酸钠,可证明猜想Ⅰ不成立;
氯化钙溶液显中性,氯化钙可与碳酸钠反应产生白色沉淀,因此取无色溶液少许于试管中,向其中加入过量(目的是将碳酸钠完全反应掉)的氯化钙溶液,有白色沉淀产生,说明有碳酸钠,过滤,再向滤液中加入无色酚酞试液,溶液变红,说明有氢氧化钠,证明猜想Ⅲ成立;
故答案为:Na2CO3;
取无色溶液少许于试管中,向其中加入过量的氯化钙溶液,有白色沉淀产生,过滤,再向滤液中加入无色酚酞试液,溶液变红1年前查看全部
- 下列关于物质的用途叙述不正确的是 A.过氧化钠可用作供氧剂 B.高纯硅用来制造光导纤维 C.镁铝合金可用作制造飞机的材料
下列关于物质的用途叙述不正确的是
A.过氧化钠可用作供氧剂 B.高纯硅用来制造光导纤维 C.镁铝合金可用作制造飞机的材料 D.Cl 2 可与石灰乳反应制取漂白粉  hurry6241年前1
hurry6241年前1 -
 永和的杯子 共回答了17个问题
永和的杯子 共回答了17个问题 |采纳率82.4%B
1年前查看全部
- 已知,过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂利用人呼出的二氧化碳与过氧化钠反应放出
已知,过氧化钠(化学式为Na2O2)是一种浅黄色固体粉末,可用作呼吸面具里的供氧剂利用人呼出的二氧化碳与过氧化钠反应放出氧气,供给人的正常生命活动,该反应的化学方程式为:2Na2O2+2CO2=2______+O2(在横线上填写化学式).某同学利用该反应原理制取氧气,设计实验装置如图1所示:

(1)装置①中CO2的制取方法有多种:若用加热NaHCO3固体制取CO2,应该选用的发生装置为______(选填图2字母)
(2)装置③中盛装的试剂为______,作用是______.
(3)④为O2的收集装置,可选用装置______(选填上图字母). 只说一次11年前1
只说一次11年前1 -
 apple-pan 共回答了20个问题
apple-pan 共回答了20个问题 |采纳率90%解题思路:化学反应前后原子的种类和数目不变,据此判断物质的化学式;
(1)加热NaHCO3固体制取CO2,属于固体加热型,故选发生装置A;
(2)通入的二氧化碳不可能被全部反应掉,为了得到较纯净的氧气,应该在③中加入氢氧化钠溶液来吸收二氧化碳,可以据此解答;
(3)氧气难溶于水且密度比空气大,所以可以选择排水法或是向上排空气法来收集,可以据此选择装置.化学反应前后原子的种类和数目不变,由反应的方程式2Na2O2+2CO2═2 +O2可知反应前有4个钠原子,8个氧原子,2个碳原子,生成物中有2个氧原子,所以物质的化学式是Na2CO3;
(1)碳酸氢钠在加热的条件下分解产生二氧化碳,所应该选择固体加热型的反应装置即A装置;
(2)通入的二氧化碳不可能被全部反应掉,为了得到较纯净的氧气,应该在③中加入氢氧化钠溶液来吸收二氧化碳;
(3)氧气不易溶于水且密度比空气大,所以可以选择排水法或向上排空气法来收集,不能用向下排空气法收集;
故答案为:Na2CO3;
(1)A;
(2)NaOH溶液;除去二氧化碳;
(3)D.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;常见气体的检验与除杂方法;氧气的制取装置;质量守恒定律及其应用.
考点点评: 本题考查了过氧化钠与二氧化碳的反应及其反应产物氧气和气体的除杂,完成此题,可以依据质量守恒定律和题干提供的信息等知识进行解答.1年前查看全部
- (2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素
(2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,B、E、G是常见的气体,E、F是非金属单质,B能使澄清石灰水变浑浊.回答下列问题:

(1)写出反应⑤的化学方程式3CO+Fe2O3
2Fe+3CO2高温 .3CO+Fe2O3;
2Fe+3CO2高温 .
(2)如何证明高温下C物质发生了部分分解?答:首先,取少量③反应后的固体______;然后,再取少量③反应后的固体,______.
(3)氧化物X是______.(写化学式) 西民小生1年前1
西民小生1年前1 -
 trainhead 共回答了21个问题
trainhead 共回答了21个问题 |采纳率85.7%解题思路:I为目前使用最广泛的金属,可确定I的成份;B能使澄清的石灰水变浑浊,可确定B的成份;根据⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,G为气体,可确定G的成份;进而确定H的成份;E和F点燃生成G,E为单质,可确定E、F的成份;C高温生成B和D,可确定C、D的成份;根据A和B反应生成C和水又可确定A的成份.
(1)根据上述分析可知道⑤发生的反应,熟记一些常用的化学方程式.
(2)C物质为碳酸钙,要证明碳酸钙部分分解,也就是要证明反应后的固体中即有未分解的碳酸钙,又有分解生成的氧化钙.可根据检验碳酸根离子的方法来检验是否有碳酸钙,可根据加水溶解后的溶液是否显碱性来确定是否有氧化钙.
(3)根据元素质量比比上相对原子质量比为原子数目之比求出这两种元素的角码之比,然后根据化学式的写法特点写出该物质的化学式.I为目前使用最广泛的金属,则I为铁;B能使澄清的石灰水变浑浊,则B为二氧化碳;⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,G为气体,生成物中还有二氧化碳,则G为一氧化碳;H为氧化铁;E和F点燃生成G一氧化碳,E为气体单质,则E为氧气;F为碳;C高温生成B二氧化碳和D,则C为碳酸钙;D为氧化钙;A和B二氧化碳反应生成C碳酸钙和水,则A为氢氧化钙.
(1)根据上述分析可知⑤发生的反应为一氧化碳和氧化铁高温生成铁和二氧化碳.
故答案为:3CO+Fe2O3
高温
.
2Fe+3CO2
(2)根据上述分析可知C为碳酸钙,碳酸钙高温生成氧化钙和二氧化碳,向反应后的固体中加入稀盐酸,若有气泡冒出,则说明碳酸钙未分解完;取少量反应后的固体,加少量水,滴入无色的酚酞溶液,若溶液变成红色,说明反应后的固体中有氧化钙生成,碳酸钙发生分解.从而说明碳酸钙部分发生了分解.
故答案为:加入稀盐酸,如果产生气泡,说明碳酸钙有剩余;加入少量的水,搅拌,滴入几滴酚酞试液,如果变红色,说明已有氧化钙生成,碳酸钙发生了分解.
(3)根据上述分析可知A为氢氧化钙,E为氧气,根据质量守恒定律,化学反应前后元素的种类不变可知,X中一定含有钙元素,可能含有氢元素和氧元素,又知X为氧化物,则X中含有钙元素和氧元素.
X中钙元素和氧元素的原子数目比=[5/40:
4
16]=1:2,则X为化学式为:CaO2.
故答案为:CaO2点评:
本题考点: 物质的鉴别、推断;碳酸钠、碳酸氢钠与碳酸钙;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题综合考查物质推断题的解题能力.解题关键是挖掘“题眼”,熟悉所学的基本化学反应,并能根据题干信息很快联想相应的特征反应.1年前查看全部
- 过氧化钠可以做潜水的供氧剂吗
 camelchow1年前3
camelchow1年前3 -
 蔚蓝的瞬 共回答了18个问题
蔚蓝的瞬 共回答了18个问题 |采纳率83.3%理论上是可以的,但是要看经济因素,假如很贵的话就没意思了,你说是吧…………
我记得教材上好像说过这句话,过氧化钠是潜水艇中和航空航天中的供氧剂,记不太清楚了,不好意思哈1年前查看全部
- 淡黄色粉末过氧化钠常做潜水员的供氧剂,在其供养反应中,被氧化和被还原的物质的质量比为?
淡黄色粉末过氧化钠常做潜水员的供氧剂,在其供养反应中,被氧化和被还原的物质的质量比为?
(供养反应是Na2O2分别与CO2和H2O反应:
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2↑) knightstar21年前1
knightstar21年前1 -
 差点淹ee的鱼 共回答了18个问题
差点淹ee的鱼 共回答了18个问题 |采纳率88.9%1:1
不论是哪个反应,过氧化钠一半做氧化剂,一半作还原剂1年前查看全部
- 过氧化钠因为能与水、二氧化碳等反应产生氧气而作为供氧剂,现将39克的氧化钠投入到足量的水中.
过氧化钠因为能与水、二氧化碳等反应产生氧气而作为供氧剂,现将39克的氧化钠投入到足量的水中.
2NaO2+2H2O=4NaOH+O2↑
(1)计算生成氢氧化钠和氧气的质量
(2)若开始反应时水的质量为69克,求反应后所得溶液溶质的质量分数.
第二问怎样做,第一问不用. 不必提醒我1年前1
不必提醒我1年前1 -
 lzg8585 共回答了13个问题
lzg8585 共回答了13个问题 |采纳率92.3%2Na2O2+2H2O=4NaOH+O2↑
2*78 2*18 4*40 32
39 m3 m1 m2
m1=40g
m2=8g
m3=9g
所以溶质氢氧化钠的质量为40克,溶液的质量为69-9+40=100g
反应后所得溶液溶质的质量分数为40/100*100%=40%1年前查看全部
- 工业制取供氧剂的化学方程式
 hyyhyy1年前1
hyyhyy1年前1 -
 ljshzhg521 共回答了18个问题
ljshzhg521 共回答了18个问题 |采纳率94.4%制取:2Na+O2===Na2O2 ;
使用:2Na2O2+2CO2==2Na2CO3+O21年前查看全部
- 超氧化钾(KO2)能与二氧化碳反应生成氧气,常用于医疗、潜水、高空飞行中的供氧剂,该反应的化学方程式为4KO2+2CO2
超氧化钾(KO2)能与二氧化碳反应生成氧气,常用于医疗、潜水、高空飞行中的供氧剂,该反应的化学方程式为4KO2+2CO2═2K2CO3+3O2.若要得到9.6g氧气,请计算参加反应的超氧化钾质量.
 仙度拉wen1年前4
仙度拉wen1年前4 -
 cliangjin 共回答了14个问题
cliangjin 共回答了14个问题 |采纳率85.7%解题思路:依据题给化学方程式及已知氧气质量,求得参加反应的超氧化钾质量设参加反应的超氧化钾质量为x.
4KO2+2CO2═2K2CO3+3O2
284 96
x 9.6g
[284/x=
96
9.6g]
x=28.4g
答:参加反应的超氧化钾质量为28.4g.点评:
本题考点: 根据化学反应方程式的计算.
考点点评: 此题依据题给信息,根据化学方程式进行解答计算即可,注意解题格式、步骤.1年前查看全部
- 呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.为了探究其反应原理,兴趣小组同学在老师的指导下,进行了如下探究,
呼吸面具和潜水艇中可用过氧化钠(Na2O2)作为供氧剂.为了探究其反应原理,兴趣小组同学在老师的指导下,进行了如下探究,请你一起参与.
[查阅资料]过氧化钠在常温下与水或二氧化碳反应都放出氧气,并分别生成氢氧化钠、碳酸钠.
[设计实验]浩明同学想通过下图装置探究过氧化钠与二氧化碳的反应,并验证反应产物.
(1)下列是实验室常用的仪器:
①A是二氧化碳气体的发生装置,装配该装置时,应选用的仪器除带导管的双孔橡皮塞外,还需要的仪器有(填名称)
锥形瓶
、
长颈漏斗
.实验室制取二氧化碳的化学方程式
CaCO3+2HCl=CaCl2+H2O+CO2↑
.该装置在实验室还可以用来制取氧气,写出用该装置制取氧气的化学方程式
2H2O22H2O+O2↑
.
②实验室选择制取气体的发生装置,主要依据是
反应物的状态
、
反应是否需要加热(或反应条件)
.
(2)用D所示的方法收集氧气,其依据是
氧气不易溶于水
.
(3)C中氢氧化钠的作用是吸收没有参与反应的CO2,如果没有连接这个装置,可能导致的后果是
影响氧气的检验
.
(4)检验B中反应后剩余固体的成分.
实验现象 实验结论及方程式
①取少量B中反应后的固体于试管中;
②____________;
③____________. ②____________
③____________ 反应后生成的固体是碳酸钠
[反思与评价](1)通过上述实验,浩明同学认为Na2O2与CO2反应除了生成Na2CO3和O2,
还有可能生成NaHCO3.你认为他的结论
不正确
(选填“正确”或“不正确”).
写出Na2O2与二氧化碳反应的化学方程式
2Na2O2+2CO2=2Na2CO3+O2
.
(2)请说说呼吸面具或潜水艇用过氧化钠作为供氧剂的最大优点
吸收呼吸产生的二氧化碳,同时生成氧气
. liufeifei171年前1
liufeifei171年前1 -
 反对浮夸风 共回答了15个问题
反对浮夸风 共回答了15个问题 |采纳率86.7%[设计实验]
(1)从所给图可知,此题制取气体的反应物是固体和液体,反应不需要加热,故答案为:①锥形瓶、长颈漏斗;化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2.氧气能使带火星的木条复燃,故用燃着的木条伸入试管中,木条复燃,该气体是氧气
(2)如果不通过氢氧化钠溶液,则D收集的气体除了氧气,还有二氧化碳气体,故其作用是吸收多余二氧化碳气体.
[反思与评价]
(1)Na2O2与二氧化碳反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2
(2)过氧化钠能吸收呼吸产生的二氧化碳,同时生成氧气.
故答案为:(1)锥形瓶长颈漏斗CaCO3+2HCl=CaCl2+H2O+CO2↑
用带火星的木条伸入试管中,观察木条能否复燃.
(2)除去多余的CO2
【反思与评价】
(1)2Na2O2+2CO2=2Na2CO3+O2↑
(2)将呼出的CO2转化成O2 祝您开心愉快,希望对您有帮助,谢谢!~~1年前查看全部
- (2014•曲阜市模拟)呼吸面具和潜水艇中可用过氧化钠Na2O2作为供氧剂,某兴趣小组的同学对过氧化钠(Na2O2)可以
(2014•曲阜市模拟)呼吸面具和潜水艇中可用过氧化钠Na2O2作为供氧剂,某兴趣小组的同学对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动.
【提供资料】①2Na2O2+2H2O═4NaOH+O2↑
②过氧化钠与二氧化碳反应生成碳酸钠和氧气
证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气,同学们在老师的指导下设计了如图所示装置.
(1)氢氧化钠溶液的作用是除去未反应的二氧化碳,若观察到______,说明二氧化碳已经除尽.
(2)若收集了32克氧气,反应掉过氧化钠的质量是______克. 倩娜1年前1
倩娜1年前1 -
 pangshufang 共回答了16个问题
pangshufang 共回答了16个问题 |采纳率100%解题思路:(1)通常用澄清的石灰水来检验二氧化碳的存在;
(2)根据过氧化钠和二氧化碳之间的反应方程式进行计算即可.(1)当气体通过澄清的石灰水时,看不到变浑浊,就说明二氧化碳已经除尽;
(2)设生成32g氧气,需要过氧化钠的质量为x
2Na2O2+2CO2═2Na2CO3+O2
156 32
x 32g
[156/32=
x
32g]
x=156g
答:收集了32克氧气,反应掉过氧化钠的质量是156g.
故答案为:(1)澄清的石灰水未变浑浊;(2)156.点评:
本题考点: 制取气体的反应原理的探究;气体的净化(除杂);根据化学反应方程式的计算.
考点点评: 本题考查过氧化钠和二氧化碳之间的反应以及根据化学方程式进行计算知识,注意知识的应用是关键,难度不大.1年前查看全部
- 在呼吸面具中可用Na2O2作为供氧剂,其原理是(用化学反应方程式表示):______.
 杨柳清1年前1
杨柳清1年前1 -
 shelley冰 共回答了19个问题
shelley冰 共回答了19个问题 |采纳率84.2%解题思路:过氧化钠可以和人体呼出的气体:水以及二氧化碳之间反应生成氧气,在呼吸面具中可用Na2O2作为供氧剂.过氧化钠可以和水或是二氧化碳反应生成氢氧化钠或是碳酸钠和氧气,即2Na2O2+2CO2=2Na2CO3+O2↑,2Na2O2+2H2O=4NaOH+O2↑,
故答案为:2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2↑.点评:
本题考点: 钠的重要化合物.
考点点评: 物质的性质决定物质的性质,过氧化钠可以和人体呼出的气体之间反应生成供人体的呼吸用的氧气,常用作供氧剂.1年前查看全部
- 请解释过氧化钠作为供氧剂的最大优点,为什么?
 有点CJ1年前1
有点CJ1年前1 -
 虚掩的人生 共回答了10个问题
虚掩的人生 共回答了10个问题 |采纳率80%可直接将二氧化碳转化为氧气,方便简洁1年前查看全部
- 高锰酸钾能氧化芬顿试剂吗高锰酸钾和芬顿试剂的氧化性哪个更强一点呢?我在测一种供氧剂,里面含有双氧水,但是在用高锰酸钾滴定
高锰酸钾能氧化芬顿试剂吗
高锰酸钾和芬顿试剂的氧化性哪个更强一点呢?
我在测一种供氧剂,里面含有双氧水,但是在用高锰酸钾滴定的时候有沉淀析出,不知道这个沉淀是什么物质?滴加氯化钡有沉淀析出,说明里面有硫酸根,我觉得是芬顿试剂,用氢氧化钠检验里面有没有铁离子,加入氢氧化钠后反应很剧烈但是没有沉淀。取经高锰酸钾氧化后的上清液滴加氢氧化钠有褐色沉淀析出。 黑胡子乌黑1年前2
黑胡子乌黑1年前2 -
 xlzy36 共回答了20个问题
xlzy36 共回答了20个问题 |采纳率95%芬顿试剂中的氧化剂是H2O2,而H2O2的氧化性比MnO4-强:
H2O2 + 2e + 2H+ = 2H2O,E=1.776V
MnO4- + 5e + 8H+ = Mn2+ + 4H2O,E=1.57V1年前查看全部
- 人类在探索自然和科学考察的活动中,经常要面临无氧环境,在你熟悉的物质中,可以选用作为供氧剂的是( )
人类在探索自然和科学考察的活动中,经常要面临无氧环境,在你熟悉的物质中,可以选用作为供氧剂的是( )
A. NaOH
B. Na2O2
C. Al2O3
D. NaHCO3 lltommy1年前2
lltommy1年前2 -
 蔻蔻蔸儿 共回答了19个问题
蔻蔻蔸儿 共回答了19个问题 |采纳率94.7%解题思路:可以选用作为供氧剂的物质能与二氧化碳、水反应生成氧气,结合各物质的性质进行判断.A、氢氧化钠与二氧化碳反应生成碳酸钠,不能产生氧气,不能与水反应,故A不符合;
B、过氧化钠与二氧化碳、水反应都会生成氧气,故过氧化钠可以作为供氧剂,故B符合;
C、氧化铝与二氧化碳、水不反应,故C不符合;
D、碳酸氢钠与二氧化碳、水不反应,故D不符合.
故选B.点评:
本题考点: 钠的重要化合物.
考点点评: 本题以供氧剂为载体,考查物质的性质,难度较小,注意基础知识的掌握.1年前查看全部
- 人类在探索自然和科学考察的活动中,经常要面临无氧环境,在你熟悉的物质中,可以选用作为供氧剂的是( )
人类在探索自然和科学考察的活动中,经常要面临无氧环境,在你熟悉的物质中,可以选用作为供氧剂的是( )
A. NaOH
B. Na2O2
C. Al2O3
D. NaHCO3 罗家英1年前3
罗家英1年前3 -
 78007406 共回答了13个问题
78007406 共回答了13个问题 |采纳率92.3%解题思路:可以选用作为供氧剂的物质能与二氧化碳、水反应生成氧气,结合各物质的性质进行判断.A、氢氧化钠与二氧化碳反应生成碳酸钠,不能产生氧气,不能与水反应,故A不符合;
B、过氧化钠与二氧化碳、水反应都会生成氧气,故过氧化钠可以作为供氧剂,故B符合;
C、氧化铝与二氧化碳、水不反应,故C不符合;
D、碳酸氢钠与二氧化碳、水不反应,故D不符合.
故选B.点评:
本题考点: 钠的重要化合物.
考点点评: 本题以供氧剂为载体,考查物质的性质,难度较小,注意基础知识的掌握.1年前查看全部
- NA2O2用作呼吸面具的供氧剂,没有氧化还原反应?
 荔枝姑娘1年前4
荔枝姑娘1年前4 -
 lovoinfo 共回答了15个问题
lovoinfo 共回答了15个问题 |采纳率86.7%2Na2O2 + 2CO2 = 2Na2CO3 + O2
其中O2-为负二价,O2单质为0价
单线桥由Na2O2中的O2出发并指向Na2O2中的O2
此反应为氧化还原反应1年前查看全部
- 用于潜艇中午供氧剂是什么
 36257001年前1
36257001年前1 -
 帅帅的骡子 共回答了11个问题
帅帅的骡子 共回答了11个问题 |采纳率90.9%潜艇供氧主要有三种方法:
1 电解水制氧,基本原理是用电离分解法把水(H2O)分解为氢(H)和氧(O),氧气通过全船通风换气系统输送到船舱,而氢气则被储存在氢气罐里.由于电解水制氧装置需消耗大量的电能,所以常规潜艇上不用此法制氧
2 氧气再生药板,气再生药板是由一片片涂有过氧化钠的薄板组成,使用时产生化学反应,吸收二氧化碳,释放出氧气,每箱药板可供40人使用1.5小时左右
3 液态氧气罐供氧,这是常规潜艇的主要供氧方式1年前查看全部
- 为避免被敌方发现,潜艇经常会长时间下潜到海洋的深处隐蔽接敌.艇内战斗人员常用过氧化钠作为供氧剂.某同学查阅过氧化钠的相关
为避免被敌方发现,潜艇经常会长时间下潜到海洋的深处隐蔽接敌.艇内战斗人员常用过氧化钠作为供氧剂.某同学查阅过氧化钠的相关资料如下:
过氧化钠是一种淡黄色粉末状固体,熔点460℃,沸点657℃.它具有较强的氧化性,能与水反应生成氢氧化钠和氧气,也能与二氧化碳发生反应生成碳酸钠和氧气.
请根据上述材料回答以下问题:
(1)过氧化钠的物理性质有______(答一点即可,下同);
过氧化钠的化学性质有______.
(2)写一个涉及过氧化钠参与反应的文字表达式:______. yimingfei91年前1
yimingfei91年前1 -
 k型yy1 共回答了20个问题
k型yy1 共回答了20个问题 |采纳率95%解题思路:化学性质与物理性质的差别是它们是否需要发生化学变化表现出来,物质不需要发生化学变化就表现出来的性质是物理性质;物质在化学变化中表现出来的性质是化学性质,应用这个差别可以来判别某一性质是化学性质,还是物理性质.(1)物质的颜色、状态、熔点、沸点、密度等不需要化学变化就变现出来,属于物理变化,过氧化钠的物理性质有:淡黄色粉末状固体,熔点460℃,沸点657℃;过氧化钠的化学性质有:具有氧化性、能与水反应、能与二氧化碳反应.
(2)能与水反应生成氢氧化钠和氧气,也能与二氧化碳发生反应生成碳酸钠和氧气,其文字表达式为:
过氧化钠+水→氢氧化钠+氧气;过氧化钠+二氧化碳→碳酸钠+氧气.
故答案为:
(1)淡黄色粉末状固体(或熔点460℃,沸点657℃);
过氧化钠具有氧化性(或能与水反应、能与二氧化碳反应);
(2)过氧化钠+水→氢氧化钠+氧气(或过氧化钠+二氧化碳→碳酸钠+氧气).点评:
本题考点: 化学性质与物理性质的差别及应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题要分析物质的性质是否需要通过化学变化表现出来,如果需要通过化学变化表现出来就属于物质的化学性质;如果不需要通过化学变化表现出来就属于物质的物理性质.1年前查看全部
- 某淡黄色粉末常用作潜水员的供氧剂,在供氧反应中,被氧化和被还原的物质的质量比为?答案好像1比1,为什
某淡黄色粉末常用作潜水员的供氧剂,在供氧反应中,被氧化和被还原的物质的质量比为?答案好像1比1,为什
可不可以讲解下 渡口等船1年前3
渡口等船1年前3 -
 浪漫左右 共回答了21个问题
浪漫左右 共回答了21个问题 |采纳率90.5%黄色粉末为过氧化钠,其中1个氧被氧化,另一个被还原,属典型歧化反应,答案1:1 .
过氧化钠中两个氧化合价均为-1,和潜水员呼出的二氧化碳反应后生成碳酸钠和氧气,即一个氧从-1变为0价,另一个变为-2价!1年前查看全部
- 在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,A是用大理石和稀盐酸制取CO
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,A是用大理石和稀盐酸制取CO2的装置,用下图中实验装置,进行实验来证明过氧化钠可作供氧剂.
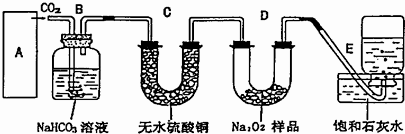
(1)B装置的作用是______,写出该装置中发生反应的离子方程式______;
(2)C装置内的现象是______;
(3)写出D装置中发生反应的化学方程式______;
(4)若无C装置,D装置可能发生的干扰反应的化学方程式为______;
(5)为了检验E中收集到的气体,在取出集气瓶后,______. huxiang03291年前1
huxiang03291年前1 -
 刘正风 共回答了22个问题
刘正风 共回答了22个问题 |采纳率90.9%解题思路:(1)根据实验目的来分析仪器B加入饱和的NaHCO3溶液的目的,根据溶液中的反应写出方程式;
(2)无水硫酸铜变蓝;
(3)D装置中为过氧化钠与二氧化碳反应;
(4)若无C装置,则前面溶液中挥发出来的水蒸气进入D与过氧化钠反应;
(5)根据检验氧气的方法分析.(1)用稀盐酸与大理石反应制得的二氧化碳中含有氯化氢气体,B中饱加入和NaHCO3溶液除去二氧化碳中的氯化氢;溶液中NaHCO3与HCl反应生成二氧化碳,其反应的离子方程式为:HCO3-+H+=H2O+CO2↑,
故答案为:除去CO2中的混有的HCl;HCO3-+H+=H2O+CO2↑;
(2)C装置中的无水硫酸铜遇到水会生成蓝色的硫酸铜晶体,故答案为:无水硫酸铜固体由白色变为蓝色;
(3)D装置中为过氧化钠与二氧化碳反应,其反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2,故答案为:2Na2O2+2CO2═2Na2CO3+O2;
(4)若无C装置,则前面溶液中挥发出来的水蒸气进入D与过氧化钠反应;所以其反应方程式为:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(5)一般用带火星的木条检验氧气,其操作为:立即将带火星的木条放在试管口,看木条是否复燃,故答案为:立即将带火星的木条放在试管口,看木条是否复燃.点评:
本题考点: 碱金属及其化合物的性质实验.
考点点评: 本题主要考查了过氧化钠的性质,考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力,题目难度一般.1年前查看全部
- 过氧化钠和超氧化钾都可以作供氧剂和氧化剂,
过氧化钠和超氧化钾都可以作供氧剂和氧化剂,
宇航员呼出的气体是二氧化碳和水蒸气的混合物,若用过氧化钠吸收该混合气体,转移的电子数为N,则下列物理量能确定的是
A、固体净增质量 B、参加反应的过氧化钠质量 C、产生氧气总体积
D、参加反应的气体总物质的量 雨人_1年前1
雨人_1年前1 -
 evian_shui 共回答了22个问题
evian_shui 共回答了22个问题 |采纳率90.9%过氧化钠与二氧化碳和水蒸气反应的化学方程式分别是:
2Na2O2 + 2 CO2 == 2 Na2CO3 + O2 2Na2O2 + 2 H2O == 4 NaOH + O2
从电子得失的角度分析,两个反应都是每转移2mol电子,产生1mol氧气,所以转移的电子数为N时,产生气体的量固定(可以求出)2 :1 == N :x x = N/2 mol.同时,也能求出过氧化钠的质量B.由于不知道呼出气体中CO2和H2O的比例,无法求出A和D.答案是:BC.1年前查看全部
- (2014•常州)过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其
(2014•常州)过氧化钠(Na2O2)可用作呼吸面具中的供氧剂,实验室有一瓶放置较长时间的过氧化钠样品,某研究小组对其成分和性质进行了如下探究.
【查阅资料】过氧化钠能与空气中的水和二氧化碳反应生成氧气:2Na2O2+2H2O═4NaOH+O2↑,2Na2O2+2CO2=2NaCO3+O2.
【提出问题】过氧化钠是否变质?
【猜想与假设】
假设1:过氧化钠未变质;假设2:过氧化钠部分变质;假设3:过氧化钠全部变质.
【实验探究】
【提出新问题】部分变质的过氧化钠样品中是否含有氢氧化钠呢?序号 实验步骤 实验现象 实验结论 ① 取部分固体于试管中,加入适量的水,在试管口插入带火星的木条 固体完全溶解,木条复燃 假设______不成立 ② 取少量①中溶液于试管中,滴加足量的______,振荡 有气泡生成 假设2成立
【实验探究】
实验③:取少量①中溶液于试管中,加入足量的氯化钙溶液,有白色沉淀生成,静置,向上层清液中滴加2滴无色酚酞试液,溶液变红.
【定性分析】
(1)由实验③可以确定①中溶液含有的溶质是______(填化学式).
(2)小明认为,由上述实验无法确定原固体药品中是否含有氢氧化钠,理由是______.
【定量分析】
称取6.04g过氧化钠药品于锥形瓶中,加入适量蒸馏水使固体完全溶解,共收集到0.64g气体;再向上述锥形瓶中加入足量的澄清石灰水,充分反应,经过滤、干燥等操作,称量固体质量为2.00g.
(1)写出加入澄清石灰水发生反应的化学方程式:______;
(2)6.04g上述样品中含有NaOH的质量为______g.
【反思提高】
过氧化钠长时间露置在空气中会全部变质,最终转化为______(填化学式). jeanvirgo1年前1
jeanvirgo1年前1 -
 gregli 共回答了22个问题
gregli 共回答了22个问题 |采纳率90.9%解题思路:【猜想与假设】根据气体的检验方法可知是氧气,根据有气泡产生,说明含有碳酸钠;
【定性分析】
(1)根据加入足量的氯化钙溶液,有白色沉淀生成,说明含有碳酸钠;静置,向上层清液中滴加2滴无色酚酞试液,溶液变红,说明含有氢氧化钠解答;
(2)根据过氧化钠与水反应能生成氢氧化钠,可推出结论是否正确;
【定量分析】
(1)根据碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠解答;
(2)根据氧气的质量利用化学方程式求出样品中过氧化钠的质量,利用碳酸钙的质量求出样品中碳酸钠的质量;
【反思提高】根据过氧化钠易与二氧化碳反应,还能和水反应变质解答.【猜想与假设】①取部分固体于试管中,加入适量的水,在试管口插入带火星的木条,固体完全溶解,木条复燃,可知是氧气,故假设3不正确;
②取少量①中溶液于试管中,滴加足量的稀盐酸,有气泡生成,说明含有碳酸钠;
【定性分析】
(1)加入足量的氯化钙溶液,有白色沉淀生成,说明含有碳酸钠;静置,向上层清液中滴加2滴无色酚酞试液,溶液变红,说明含有氢氧化钠,以确定①中溶液含有的溶质是NaOH、Na2CO3;
(2)滤液中滴加无色酚酞试液,若液体变红,不能证明原粉末中有NaOH,因为过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在.
【定量分析】
(1)石灰水的溶质是氢氧化钙,碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(2)设样品中含有Na2O2的质量为x,
2Na2O2+2H2O═4NaOH+O2↑
156 32
x 0.64g
[156/32=
x
0.64g]
x=3.12g
经过滤、干燥等操作后得到的固体是CaCO3,质量为2.00g,设样品中含有的Na2CO3的质量为y,
Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
106100
y 2.00g
[106/100=
y
2.00g] y=2.12g
则样品中NaOH的质量=6.04g-3.12g-2.12g=0.8g
【反思提高】过氧化钠易与二氧化碳反应,还能和水反应变质,最终转化为Na2CO3
答案:
【猜想与假设】
序号实验步骤实验现象实验结论
①取部分固体于试管中,加入适量的水,在试管口插入带火星的木条固体完全溶解,木条复燃假设 3不成立
②取少量①中溶液于试管中,滴加足量的 稀盐酸,振荡有气泡生成假设2成立【定性分析】
(1)NaOH、Na2CO3;
(2)过氧化钠与水反应能生成氢氧化钠,不能说明原来是否存在;
【定量分析】
(1)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(2)0.8;
【反思提高】Na2CO3.点评:
本题考点: 药品是否变质的探究;氧气的检验和验满;碱的化学性质;盐的化学性质;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 该考点的命题方向主要是以实验探究题的形式,给出有关的信息提示和相关数据,让学生通过实验探究,分析推断出该物质的组成成分;中考的重点是考查学生通过实验的方法来研究物质的组成成分以及含量能力.1年前查看全部
- (2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素
(2006•南通模拟)氧化物X(初中化学未学过)是一种安全无毒的物质,常用作长途运输时鱼苗的供氧剂.已知X含有的两种元素的质量比为5:4.由X出发有下列转化关系,其中⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,B、E、G是常见的气体,E、F是非金属单质,B能使澄清石灰水变浑浊.回答下列问题:
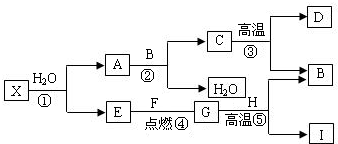
(1)写出反应⑤的化学方程式3CO+Fe2O3
2Fe+3CO23CO+Fe2O3高温 .
2Fe+3CO2;高温 .
(2)如何证明高温下C物质发生了部分分解?答:首先,取少量③反应后的固体加入稀盐酸,如果产生气泡,说明碳酸钙有剩余加入稀盐酸,如果产生气泡,说明碳酸钙有剩余;然后,再取少量③反应后的固体,加入少量的水,搅拌,滴入几滴酚酞试液,如果变红色,说明已有氧化钙生成,碳酸钙发生了分解加入少量的水,搅拌,滴入几滴酚酞试液,如果变红色,说明已有氧化钙生成,碳酸钙发生了分解.
(3)氧化物X是CaO2CaO2.(写化学式) 老三到了1年前1
老三到了1年前1 -
 wxb163 共回答了13个问题
wxb163 共回答了13个问题 |采纳率92.3%I为目前使用最广泛的金属,则I为铁;B能使澄清的石灰水变浑浊,则B为二氧化碳;⑤是工业中冶炼目前使用最广泛的一种金属I 的反应,G为气体,生成物中还有二氧化碳,则G为一氧化碳;H为氧化铁;E和F点燃生成G一...1年前查看全部
大家在问
- 1从3个红球,7个黑球的袋子中按顺序摸出3个球,恰好第三个才出现黑球的概率为 7/40
- 2实验室常用稀盐酸和大理石制取二氧化碳气体.现需收集4瓶(每瓶以125mL计算)二氧化碳气体,问至少需要多少克大理石(含碳
- 3点M到x轴的距离与它到y轴的距离之比3:1,同点M的轨迹方程两直线交点不能取吧?
- 4课桌面的面积大约是0.42( ).
- 5in a short time中time讲可数吗?
- 6除去fe中的Al应该用什么试剂?离子方程式是什么?
- 7They play table tennis in afternoon.改写成进行时
- 8使它的内项相等,而且两个比的比值都是3分之1 是它的两个内项互为倒数
- 9修一条高速公路,已修和未修长度比为1:3,再修30km,已修就是未修的二分之一,这条铁路长多少km?
- 10里中有病脚疮者告诉了我们什么道理?急.请尽快解答,
- 11在5000多年的历史发展中,中华民族形成了伟大的民族精神。中华民族精神的核心是 [ &
- 12A是地球的同步卫星,另一卫星B也位于赤道平面内,离地高度为h,运行周期为T.已知地球半径为R,地球自转角速度
- 13为什么英语里既有in the school 又有at school之说
- 14— What should we do first if we want to develop our vil
- 15关于遇到困难,又得到脱险的名言警句
