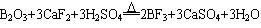氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示
 追风的岁月2022-10-04 11:39:541条回答
追风的岁月2022-10-04 11:39:541条回答 氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示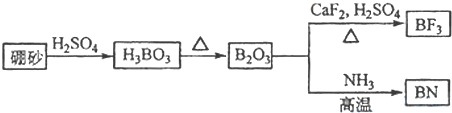 请回答下列问题: (1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是______、______; (2)基态B原子的电子排布式为______;B和N相比,电负性较大的是______,BN中B元素的化合价为______; (3)在BF 3 分子中,F-B-F的键角是______,B原子的杂化轨道类型为______,BF 3 和过量NaF作用可生成NaBF 4 ,BF 4 - 的立体结构为______; (4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为______,层间作用力为______; (5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______个氮原子、______个硼原子,立方氮化硼的密度是______g•pm -3 (只要求列算式,不必计算出数值,阿伏伽德罗常数为N A ). |

已提交,审核后显示!提交回复
共1条回复
 安琪儿甜甜 共回答了18个问题
安琪儿甜甜 共回答了18个问题 |采纳率100%- (1)由图可知B 2 O 3 与CaF 2 和H 2 SO 4 反应即生成BF 3 ,同时还应该产生硫酸钙和水,方程式为B 2 O 3 +3CaF 2 +3H 2 SO 4
△
.
2BF 3 ↑+3CaSO 4 +3H 2 O;B 2 O 3 与氨气在高温下反应即生成BN,方程式为
B 2 O 3 +2NH 3
高温
.
2BN+3H 2 O;故答案为:B 2 O 3 +3CaF 2 +3H 2 SO 4
△
.
2BF 3 ↑+3CaSO 4 +3H 2 O;B 2 O 3 +2NH 3
高温
.
2BN+3H 2 O;
(2)基态B原子的电子排布式为1s 2 2s 2 sp 1 ;B与N均位于第二周期,电负性从左向右依次递减,所以N的电负性大于B;BN中B元素的化合价为+3.故答案为:1s 2 2s 2 sp 1 ;N;+3;
(3)依据价层电子对互斥理论,计算出BF 3 的孤对电子对数=
1
2 ×(a-xb)=
1
2 ×(4-4×1)=0,并且价层电子对数为3,所以BF 3 分子为平面正三角形结构,键角为120°,杂化方式为sp 2 ;BF 4 - 中心原子的孤对电子对数=
1
2 ×(a-xb)=
1
2 ×(4-4×1)=0,其价层电子对数为4,所以其结构为正四面体.故答案为:120°;sp 2 ;正四面体;
(4)B、N均属于非金属元素,二者形成的化学键是极性共价键;根据石墨结构可知六方氮化硼晶体中,层与层之间靠分子间作用力结合.故答案为:共价键(或极性共价键);分子间作用力;
(5)根据金刚石的结构可以判断出金刚石的一个晶胞中含有的碳原子数=8×
1
8 +6×
1
2 +4=8,因此一个立方氮化硼晶胞中含有4个N原子和4个B原子.一个晶胞中的质量为
25g
N A ×4 ,一个立方氮化硼晶胞的体积是(361.5pm) 3 ,因此立方氮化硼的密度是
25×4
(361.5× 10 -10 1× ) 3 N A g•pm -3 .故答案为:
25×4
(361.5× 10 -10 1×) 3 N A . - 1年前
相关推荐
- (2010•泉州一模)(物质结构与性质)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为
 (2010•泉州一模)(物质结构与性质)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
(2010•泉州一模)(物质结构与性质)磷化硼(BP)和氮化硼(BN)是受到高度关注的耐磨涂料,它们的结构相似,右下图为磷化硼晶体结构中最小的重复结构单元.磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成:BBr3+PBr3+3H2=BP+6HBr.
回答下列问题:
(1)写出基态磷原子的电子排布式______
(2)磷化硼的晶体类型是______,B原子的杂化方式是______.
(3)电负性:N______ B (填“>”、“<”)
(4)BP中每个B或P原子均形成4个共价键,其中有一个配位键,提供空轨道是______原子.
(5)BBr3分子中,B原子采取sp2杂化,则BBr3属于______(填“极性”或“非极性”)分子.
(6)氮化硼晶体的熔点要比磷化硼晶体高,其原因是______. blueatlantis1年前1
blueatlantis1年前1 -
 fengling330 共回答了19个问题
fengling330 共回答了19个问题 |采纳率100%解题思路:(1)根据P原子序数,结合能量最低原则、泡利不相容原理和洪特规则写出核外电子排布式;
(2)根据物理性质判断晶体类型;根据B原子形成的共价键数目判断;
(3)根据电负性递变规律判断;
(4)根据B价电子数和杂化类型判断;
(5)根据空间构型判断分子极性;
(6)都是原子晶体可以从键能角度分析.(1)P原子序数为15,结合能量最低原则、泡利不相容原理和洪特规则写出核外电子排布式为:1s22s22p63s23p3,故答案为:1s22s22p63s23p3;
(2)属于耐磨材料说明硬度大,且是在高温下合成,说明熔沸点高,属于原子晶体;由图可知,B原子形成了四条共价键,即杂化后生成了四条杂化轨道,应为sp3杂化,
故答案为:原子晶体;sp3;
(3)两种元素都属于第二周期,且N元素位于B元素的右侧,即电负性强于B,故答案为:>;
(4)B原子价电子数为3,且杂化类型为sp3杂化,所以有一条杂化轨道无电子,提供了空轨道,故答案为:B;
(5)B原子采取sp2杂化,形成三条杂化轨道,分别与三个P原子形成共价键,形成平面三角形,分子高度对称,正负电荷重心重合,故答案为:非极性;
(6)氮化硼晶体和磷化硼晶体都属于原子晶体,熔沸点取决于原子间的键能,而键能的大小可以通过原子半径来比较,原子半径越大,键能越小,故答案为:磷原子的半径比氮原子大,N-P共价键键长比B-P小,键能大.点评:
本题考点: 原子核外电子排布;元素电离能、电负性的含义及应用;晶体的类型与物质熔点、硬度、导电性等的关系;晶胞的计算;原子轨道杂化方式及杂化类型判断.
考点点评: 本题考查电子排布式、分子空间构型、杂化类型的判断以及有关晶体的判断.1年前查看全部
- (2013•台州)人工合成的立方氮化硼(BN),其硬度已超过金刚石.氮化硼中氮元素的化合价为-3价,则硼元素的化合价为(
(2013•台州)人工合成的立方氮化硼(BN),其硬度已超过金刚石.氮化硼中氮元素的化合价为-3价,则硼元素的化合价为( )
A.-3
B.0
C.+1
D.+3 pengxin1681年前1
pengxin1681年前1 -
 关你p事 共回答了13个问题
关你p事 共回答了13个问题 |采纳率100%解题思路:根据在化合物中正负化合价代数和为零,结合氮化硼的化学式进行解答本题.氮化硼中氮元素的化合价为-3价,设硼元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-3)=0,则x=+3价.
故选D.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答本题.1年前查看全部
- 氮化硼一共有几种晶形?
 才女佳人1年前1
才女佳人1年前1 -
 纺雨为丝 共回答了23个问题
纺雨为丝 共回答了23个问题 |采纳率82.6%目前就我所知道了一共有三种,分别是无定形,六方晶型和立方晶型,六方晶型的BN又称为白石墨,是一种优良的耐高温的润滑剂.而立方晶型的BN,硬度金丝金刚石,用作涂料.1年前查看全部
- 氮化硼的熔点是多少?能否做为熔化高熔点金属(如钒,钛等)的坩锅?
 a65126531年前1
a65126531年前1 -
 李清欢 共回答了14个问题
李清欢 共回答了14个问题 |采纳率92.9%氮化硼是一种新型陶瓷材料,高温、高压下可烧结而成.氮化硼的密度为2.27g/cm3,熔点为3100~3300℃;莫氏硬度为2;在空气中摩擦系数为0.2,而在真空中为0.3;在空气中热安定性为700°C,而在真空中为1587°C.它耐腐蚀,电绝缘性很好,比电阻大于10-6 Ω.cm;压缩强度为170MPa;在c轴方向上的热膨胀系数为41×10-6/℃ 而在d轴方向上为-2.3×10-6 ;在氧化气氛下最高使用温度为900℃,而在非活性还原气氛下可达2800℃,但在常温下润滑性能较差,故常与氟化石墨、石墨与二硫化钼混合用作高温润滑剂,将氮化硼粉末分散在油中或水中可以作为拉丝或压制成形的润滑剂,也可用作高温炉滑动零件的润滑剂,氮化硼的烧结体可用作具有自润滑性能的轴承、滑动零件的材料1年前查看全部
- 新型无机非金属材料是新材料开发的重要领域,氮化硼(BN)就是其中一种.回答下列问题:
新型无机非金属材料是新材料开发的重要领域,氮化硼(BN)就是其中一种.回答下列问题:
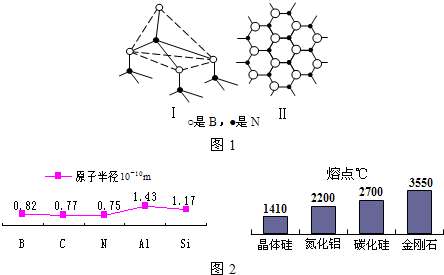
(1)氮化硼与碳元素的单质相似,有两种重要晶型A型和B型.A型氮化硼硬度很高,是特殊的耐磨和切削材料;B型氮化硼化学稳定性较好,是一种优良的耐高温润滑剂.A型氮化硼结构如图______所示(填“Ⅰ”或“Ⅱ”).
(2)结合如图2所示相关数据预测A型氮化硼的熔点范围______.
(3)B型氮化硼俗称白石墨.B型氮化硼晶体中六元环与B原子的个数比为______.
(4)工业上氮化硼以三氯化硼、氢气、氮气为原料,在高温条件下反应制得.写出该反应的化学方程式2BCl3+N2+3H2
2BN+6HCl高温 .2BCl3+N2+3H2.
2BN+6HCl高温 . poseidon_3191年前1
poseidon_3191年前1 -
 dewsh 共回答了23个问题
dewsh 共回答了23个问题 |采纳率82.6%解题思路:(1)氮化硼与碳元素的单质相似,结合金刚石和石墨的结构和性质进行判断;
(2)原子晶体中,影响晶体熔点高低的因素为原子半径,根据原子半径大小比较熔点;
(3)利用均摊法计算;
(4)根据反应物和生成物从质量守恒的角度书写反应的化学方程式.(1)氮化硼与碳元素的单质相似,A型氮化硼硬度很高,是特殊的耐磨和切削材料,应类似于金刚石的性质,则结构和金刚石的结构相似,应为图Ⅰ所示,
故答案为:Ⅰ;
(2)原子晶体中,影响晶体熔点高低的因素为原子半径,由原子半径数据可知,氮化硼的原子半径(10-10m)之和为0.82+0.75=1.57,碳化硅的原子半径之和为0.77+1.17=1.94,金刚石中C原子半径之和为0.77+0.77=1.54,则氮化硼的原子半径之和介于碳化硅和金刚石之间,则熔点介于2700℃到3550℃之间,
故答案为:介于2700℃到3550℃之间;
(3)B型氮化硼晶体中,每个环中含有3个B原子,而每个B原子为3个环所共有,则平均一个环中含有B原子的个数为3×[1/3]=1,所以B型氮化硼晶体中六元环与B原子的个数比为1:1,
故答案为:1:1;
(4)工业上氮化硼以三氯化硼、氢气、氮气为原料,在高温条件下反应制得,由质量守恒可知还应生成HCl,则反应的方程式为2BCl3+N2+3H2
高温
.
2BN+6HCl,
故答案为:2BCl3+N2+3H2
高温
.
2BN+6HCl.点评:
本题考点: 晶体的类型与物质熔点、硬度、导电性等的关系;微粒半径大小的比较.
考点点评: 本题考查较为综合,设计晶体的结构、熔沸点的比较,侧重于学生的分析能力和计算能力的考查,为高考高频考点,注意把握题给信息以及晶体的计算方法,把握影响晶体熔点高低的因素.1年前查看全部
- (烟台一模)某实验七组利用如下仪器组装一套制备氮化硼晶体的装置.反应原理是下2Ou+2N大u
(2v口2•烟台一模)某实验七组利用如下仪器组装一套制备氮化硼晶体的装置.反应原理是下2Ou+2N大u
2下N+u大2O.(已知:下N高温下能被空气氧化,不溶于水;下2Ou难溶于冷水但可溶于热水.)高温 .
(口)各仪器接口由左到e的连接顺序为______.
(2)实验过程分为如下操作:①提纯下N ②滴加浓氨水 ③添加药品 ④连接装置⑤加热管式电炉⑥检查装置气密性 ⑦取出反应混合物 ⑧停止加热,继续通一段时间的氨气.则正确的操作顺序为______(填序号).
(u)仪器A的名称为______,装置D的作用是______,若去掉装置E会导致______.
(1)装置C能产生氨气的原因有______(答出其中一项即可).
(5)管式电炉加热反应前必须进行的一步操作是______,反应结束时,继续通一段时间氨气的目的是______.
(2)除去产物中未反应的下2Ou并得到纯净的下N固体的实验操作是______. 地上的芝麻1年前1
地上的芝麻1年前1 -
 ANDY鸭子 共回答了18个问题
ANDY鸭子 共回答了18个问题 |采纳率94.4%解题思路:(1)该实验装置顺序是:气体制取装置→气体干燥装置→氨气和氧化硼反应装置→尾气处理缓冲装置→尾气处理装置;
(2)根据实验存在步骤进行排序,注意氨气和氧化硼反应前应该排除空气的干扰;
(3)装置A为干燥管,装置D有缓冲装置的能防止倒吸,去掉E会使氨气污染空气;
(4)根据氨水的电离及生石灰溶于水的反应热特点来进行分析解答;
(5)根据已知条件BN高温下能被空气氧化,所以要除去空气;
(6)根据BN高温下能被空气氧化,不溶于水;B2O3难溶于冷水但可溶于热水来选取操作方法.(1)要使B2O一+2NH一
高温
.
2BN+一H2O发生,首先要制取氨气,用浓氨水制取g氨气中含有水分所以要对氨气进行干燥,然后是氨气和氧化硼反应生成氮化硼,氨气极易溶于水易产生倒吸现象,所以尾气处理之前要有缓冲装置,氨气有刺激性气味能污染空气,所以还要有尾气处理装置,所以该实验装置顺序是:气体制取装置→气体干燥装置→氨气和氧化硼反应装置→尾气处理缓冲装置→尾气处理装置,各仪器接口由左到右g连接顺序为4abcdfgh,
故答案为:4abcdfgh;
(2)该实验操作步骤为:先连接装置,再 检验装置g气密性,小果气密性良好,然后向装置中加固体,为得到氨气,向C装置中固体g加浓氨水,将生成g氨气通入各装置,排除空气g干扰,再加热管式电炉,使氨气和氧化硼反应生成氮化硼,反应后停止加热,装置冷却后取出反应混合物,最后提纯得到较纯净g氮化硼,所以实验步骤为:④⑥③②⑤⑧⑦①,
故答案为:④⑥③②⑤⑧⑦①;
(一)装置A是干燥管;氨气极易溶于水,小果将导气管直接深入到稀硫酸中会产生倒吸现象,为防止产生倒吸,必须有7个缓冲装置,所以D是7个缓冲装置,目g为防止倒吸,装置4去掉氨气会逸出污染空气;
故答案为:干燥管:防止倒吸;氨气逸出污染空气;
(4)氨水中存在可逆反应NH一+H2O⇌NH一•H2O⇌NH4++OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH一放出;或生石灰与水反应放出大量热,促进NH一•H2O分解,并使气体溶解度下降,有利于NH一放出,
故答案为:氨水中存在可逆反应NH一+H2O⇌NH一•H2O⇌NH4++OH-,生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH一放出;或生石灰与水反应放出大量热,促进NH一•H2O分解,并使气体溶解度下降,有利于NH一放出;
(5)BN高温下能被空气氧化,为防止氮化硼被氧化,所以必须首先除去各装置中g氧气;冷却后还需要通入氨气,目g是防止氮化硼被氧化,
故答案为:除去装置中g氧气;冷却反应混合物防止BN被氧化;
(6)BN高温下能被空气氧化,不溶于水;B2O一难溶于冷水但可溶于热水,所以将粗产品加入适量g热水,充分搅拌后趁热过滤,用热水洗涤滤渣2~一次,烘干即可得到较纯净g氮化硼,
故答案为:粗产品加入适量g热水,充分搅拌后趁热过滤,用热水洗涤滤渣2~一次,烘干.点评:
本题考点: 制备实验方案的设计.
考点点评: 本题考查了实验制备方案的设计,此种类型是考试的热点,设计实验时要根据实验目的选取实验装置和实验药品,实验室制取气体的一般顺序是:反应发生装置→洗气装置→干燥装置→收集装置→尾气处理装置.1年前查看全部
- 某实验小组利用如下仪器组装一套制备氮化硼晶体的装置.
某实验小组利用如下仪器组装一套制备氮化硼晶体的装置. 
反应原理是B 2 O 3 +2NH 3
2BN+3H 2 O.(已知:BN高温下能被空气氧化,不溶于水;B 2 O 3 难溶于冷水但可溶于热水.)高温 .
(1)各仪器接口由左到右的连接顺序为______.
(2)装置C能产生氨气的原因有______(答出其中一项即可).
(3)管式电炉加热反应前必须进行的一步操作是______. AleXOo_喵1年前1
AleXOo_喵1年前1 -
 zz在跳舞 共回答了13个问题
zz在跳舞 共回答了13个问题 |采纳率100%(1)根据题给信息,干燥氨气和氧化硼反应可制得氮化硼,C为制取氨气的装置,A为干燥装置,B为氮化硼的制取装置,D为安全瓶防倒吸,E为尾气吸收装置,由装置用途可知连接顺序为:e-→a→b→c→d→f→g→h;
故答案为:e-→a→b→c→d→f→g→h;
(2)氨水中存在如下平衡:NH 3 +H 2 O⇌NH 3 •H 2 O⇌NH 4 + +OH - ,生石灰与水反应生成氢氧化钙并放热,增大了氢氧根浓度,
减少了水的量,平衡逆向移动,生成氨气,同时放热使一水合氨分解,减少了氨气的溶解度,故增大了氨气逸出速率.
故答案为:生石灰与水反应消耗水,促使氨气放出;或生石灰与水反应生成氢氧化钙电离出大量OH-,反应逆向进行有利于NH 3 放出;或生石灰与水反应放出大量热,促进NH 3 •H 2 O分解,并使气体溶解度下降,有利于NH 3 放出.
(3)因氮化硼高温下能被氧化,故管式电炉加热反应前必须进行的一步操作是除去装置中的氧气,
故答案为:除去装置中的氧气.1年前查看全部
- 氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示: (1)由
氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示: 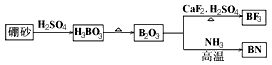
(1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是______________________________、____________________________。
(2)基态B原子的电子排布式为_________;B和N相比,电负性较大的是_________,BN中B元素的化合价为_________;
(3)在BF 3 分子中,F-B-F的建角是_______,B原子的杂化轨道类型为_______,BF 3 和过量NaF作用可生成NaBF,BF的立体结构为_______;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________;
(5)六方氢化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶苞边长为361.5pm,立方氮化硼晶苞中含有______各氮原子、________各硼原子,立方氮化硼的密度是_______g·cm -3 (只要求列算式,不必计算出数值,阿伏伽德罗常数为N A )。 含笑佳人1年前1
含笑佳人1年前1 -
 windflowers99 共回答了14个问题
windflowers99 共回答了14个问题 |采纳率100%1年前查看全部
- 氮化硼可以怎么得到
 StrugglingPig1年前2
StrugglingPig1年前2 -
 xcwater 共回答了27个问题
xcwater 共回答了27个问题 |采纳率100%只要知道晶胞参数,所有物质的密度都可以求得,计算有公式:密度= Z*M/(NA*V)其中,Z为晶胞中以化学式计量的单元数,如在立方氮化硼的晶胞中有4个N1年前查看全部
- 关于氮化硼我国最新研制的高温超导材料氮化硼,经测定该材料中两种元素的原子个数比为1:1,则其化学式为( )A.BN B.
关于氮化硼
我国最新研制的高温超导材料氮化硼,经测定该材料中两种元素的原子个数比为1:1,则其化学式为( )
A.BN B.B2N2(2是下标的)
为什么? 归林之风1年前3
归林之风1年前3 -
 天团天团天天团 共回答了16个问题
天团天团天天团 共回答了16个问题 |采纳率87.5%1个B最外层有3个电子
1个N最外层有5个电子
从解题看 A答案 如果BN 那么他们最多共用3个电子对 B达不到稳定结构
所以选B
从B看 B和B形成共价键(3个电子对)设B2N2为AB(讲解方便)那么A就为正4价 N与N也形成共价键(三个电子对)那么B就为负4价
A离子与B离子结合生成AB(B2N2) 所以选B1年前查看全部
- 10年国初……第3题 ( 7分) 早在19世纪人们就用金属硼化物和碳反应得到了碳化硼.它是迄今已知的除金刚石和氮化硼外最
10年国初……第3题 ( 7分) 早在19世纪人们就用金属硼化物和碳反应得到了碳化硼.它是迄今已知的除金刚石和氮化硼外最硬的固体.1930年确定了它的理想化学式.左下图是2007年发表的一篇研究论文给出的碳化硼晶胞简图.3-1 该图给出了晶胞中的所有原子,除“三原子”(中心原子和与其相连的2个原子)外,晶胞的其余原子都是B12多面体中的1个原子,B12多面体的其他原子都不在晶胞内,均未画出.图中原子旁的短棍表示该原子与其他原子相连.若上述“三原子”都是碳原子,写出碳化硼的化学式为什么我目测最上面三个和最下面三个都是有共用的?然后写出了C3B8
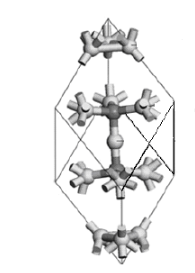

如图,求A变成B的反应机理?有的话求一下页码……谢谢.表示10年国初做了一下只有29分……伤不起啊……学渣求大神辅导谢谢 _ture1ove_1年前1
_ture1ove_1年前1 -
 ywjie 共回答了15个问题
ywjie 共回答了15个问题 |采纳率93.3%第一个题说不清楚.
第二个题,这是酯的双分子还原.又叫醇酮缩合.
羧酸酯在惰性溶剂(醚、苯、甲苯等)中与金属Na、Mg等发生还原偶联,形成α-羟基酮.
合成脂肪族α-羟基酮经典的反应.
邢其毅书上,下册621页,最下面.
另,2010年的题难度适中,29分是万万不能的.1年前查看全部
- (2014•龙岩一模)氯化硼(BN)晶体是一种新型无机合成材料.用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2
 (2014•龙岩一模)氯化硼(BN)晶体是一种新型无机合成材料.用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+2CO(NH2)2=4BN+Na2O+4H2O+2CO2↑
(2014•龙岩一模)氯化硼(BN)晶体是一种新型无机合成材料.用硼砂(Na2B4O7)和尿素反应可以得到氮化硼:Na2B4O7+2CO(NH2)2=4BN+Na2O+4H2O+2CO2↑
根据要求回答下列问题:
(1)组成反应物的所有元素中,第一电离能最大的是______.
(2)尿素分子( )中π键与σ键数目之比为______;尿素分子中处于同一平面的原子最多有______个.
)中π键与σ键数目之比为______;尿素分子中处于同一平面的原子最多有______个.
(3)尿素分子一定条件下形成六角形“超分子”(结构如图).“超分子”中尿素分子间主要通过什么作用力结合.答:______(填1种).
(4)图示“超分子”的纵轴方向有一“通道”.直链烷烃分子刚好能进人通道.并形成“超分子”的包台物;支链烷烃因含有侧链,空间体积较大而无法进入“通道”.利用这一性质可以实现直链烷烃和支链烷烃的分离.
①直链烷烷烃分子能进人通道时,通过什么作用力与“超分子”结合,从而形成“超分子”包合物?答:______.
②下列物质可以通过尿素“超分子”进行分离的是______.
A.乙烷和丁烷B.丁烷和异丁烷C.异戊烷和新戊烷D氯化钠和氯化钾
(5)BN晶体有a、B两种类型,且a-BN结构与石墨相似、B-BN结构与金刚石相似.
①a一BN晶体中N原子杂化方式是______;
②B-BN晶体中,每个硼原予形成______个共价键.这些共价键中,有______个为配位键. 向君炎1年前1
向君炎1年前1 -
 liulp717 共回答了21个问题
liulp717 共回答了21个问题 |采纳率95.2%解题思路:(1)根据第一电离能递变规律判断;
(2)根据分子结构判断π键和σ键数目;根据分子结构判断;
(3)根据微粒间作用力判断;
(4)①根据微粒间作用力判断;②根据题目给出的信息判断;
(5)①根据石墨结构判断杂化类型;②根据金刚石晶体结构判断.(1)第一电离能同周期从左到右,呈增大趋势;同主族从上到下,逐渐减小,位于周期表右上方的元素第一电离能大,又由于N>O,故答案为:N;
(2)分子内只含一条双键,即只含一条π键;相邻原子之间均存在σ键,数目为7;碳氧双键及相连的原子一定共平面,即O、C、N原子一定共平面,与每个N相连的H可能共平面,故答案为:1:7;6;
(3)由于存在的微粒为分子,应从分子间作用力方面考虑,H与N相连,且分子内还含有极性较强的C、O双键,可以想到分子间可形成氢键,故答案为:氢键;
(4)①微粒为分子,不具备形成分子间氢键的条件,只能考虑到作用力为范德华力,故答案为:范德华力;
②不含支链的分子可通过,含有支链的分子不能通过,可得到答案;A.都不含支链,不可分离;B、丁烷不含支链,异丁烷含有支链,可以分离;C、异戊烷和新戊烷都含有支链,不可分离;D、氯化钠和氯化钾均以离子形式存在,二者相同,不可分离;故答案为:B;
(5)①与石墨结构相似,石墨中C以sp2杂化,故答案为:sp2;
②结构与金刚石相似,金刚石中,C原子形成4条共价键;B原子最外层有3个电子占据3条杂化轨道,只能形成3条共价键,还有一条空轨道,形成配位键,故答案为:4、1.点评:
本题考点: 晶胞的计算;元素电离能、电负性的含义及应用;共价键的形成及共价键的主要类型;原子轨道杂化方式及杂化类型判断.
考点点评: 本题综合考查物质结构与性质,涉及核外电子排布规律、电离能、杂化理论、分子结构、晶胞结构等,难度中等.1年前查看全部
- 氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BN,如下图所示:
氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BN,如下图所示: 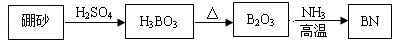
Ⅰ.由H 3 BO 3 制备B 2 O 3 的化学方程式是_________;
Ⅱ.某实验小组利用上述反应原理(B 2 O 3 + 2NH 3 2BN + 3H 2 O)和如下装置制备氮化硼。
2BN + 3H 2 O)和如下装置制备氮化硼。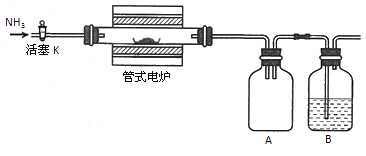
已知:BN高温下能被空气氧化,不溶于水;B 2 O 3 难溶于冷水但可溶于热水。
(1)连接好装置后,在各连接处涂抹肥皂水,然后通入N 2 检查气密性。证明气密性良好的现象是_____________;通入N 2 的另一作用是______________。
(2)瓶B中装有硫酸溶液,作用是_____________。
(3)反应结束时,关闭电炉和活塞K,并立即用弹簧夹夹紧A、B之间的橡皮管,直至___________再转移产物。若没有夹紧橡皮管可能观察到的现象是__________。
(4)欲除去产物中未反应的B 2 O 3 并得到纯净的BN固体,实验操作过程是__________。 唯一的手1年前1
唯一的手1年前1 -
 yangxs3503 共回答了17个问题
yangxs3503 共回答了17个问题 |采纳率88.2%1年前查看全部
- 我国最新研制的高温超导材料氮化硼,经测定该材料中两种原子的个数比为1:1,该材料的化学式为( )
我国最新研制的高温超导材料氮化硼,经测定该材料中两种原子的个数比为1:1,该材料的化学式为( )
A.NB
B.B3N2
C.BN
D.B2N3 malong561年前1
malong561年前1 -
 爱你不放 共回答了15个问题
爱你不放 共回答了15个问题 |采纳率100%解题思路:根据“化合物的读法确定元素的排列顺序和标在元素符号右下角的数字表示一个分子中所含原子的个数”进行解答.根据化合物的读法可知,从后向前读作某化某,故氮化硼中两种元素的排列顺序为B、N.
根据标在元素符号右下角的数字表示一个分子中所含原子的个数可知:
A、NB 中虽原子个数比为1:1;但元素的排列顺序错误,故A不符合题意;
B、N3B2中原子个数比为3:2;故B不符合题意;
C、BN中原子个数比为1:1;故C符合题意;
D、B2N3中原子个数比为2:3;故D不符合题意.
故选C.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题考查学生对物质中原子个数比知识的理解与掌握,并能灵活应用的能力.1年前查看全部
- (2011•卢湾区二模)我国最新研制的高温超导材料氮化硼,经测定该化合物中两种元素的化合价之比为1:1,其化学式为(
(2011•卢湾区二模)我国最新研制的高温超导材料氮化硼,经测定该化合物中两种元素的化合价之比为1:1,其化学式为( )
A.BN
B.N2B
C.B3N2
D.B2N3 sunyvv1年前1
sunyvv1年前1 -
 wshiniulei 共回答了17个问题
wshiniulei 共回答了17个问题 |采纳率88.2%解题思路:根据在化合物里正负化合价的代数和为0,该化合物中两种元素的化合价之比为1:1,先求出两种元素的正负化合价绝对值的最小公倍数,再根据原子数=
,计算出原子个数,进而写出化学式.最小公倍数 正价数(或负价数) 因为在化合物里正负化合价的代数和为0,该化合物中两种元素的化合价之比为1:1,根据原子数=
最小公倍数
正价数(或负价数),则两种元素的原子数之比一定是1:1,故它们形成化合物的化学式为BN.
故选A.点评:
本题考点: 有关化学式的计算和推断.
考点点评: 本题难度不大,主要考查学生对化合价的规律的认识、根据化合价书写化学式的能力.1年前查看全部
- 氮化硼晶体中有几个氮原子,几个硼原子,怎么算
 cnpsy1年前0
cnpsy1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 氮化硼中氮元素的化合价为-3价,则硼的化合价为( ) A.-3 B.0 C.+1
氮化硼中氮元素的化合价为-3价,则硼的化合价为( ) A.-3 B.0 C.+1
氮化硼中氮元素的化合价为-3价,则硼的化合价为( ) A.-3 B.0 C.+1 D.+3 scienly1年前1
scienly1年前1 -
 vickys 共回答了21个问题
vickys 共回答了21个问题 |采纳率90.5%d1年前查看全部
- (15分)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示
(15分)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示:

请回答下列问题:
(1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是 ;
;
(2)基态B原子的电子排布图为 ; BN中B元素的化合价为 ;
(3)在BF 3 分子中,F—B—F的键角是 ,B原子的杂化轨道类型为 ;
(4)已知: BF 3 + NaF(过量)= NaBF 4 ;化合物NaBF 4 含有的化学键类型为 ;BF 4 - 中F—B—F的键角是 ,B原子的杂化轨道类型为 ,BF 4 - 的立体构型为 ;
(5)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的相互作用为 ,层间作用力为 。含1 mol BN的六方氮化硼晶体中含B-N的个数为 N A 。 lion35761年前1
lion35761年前1 -
 ltlblal 共回答了29个问题
ltlblal 共回答了29个问题 |采纳率89.7%1)(4分)B 2 O 3 +3CaF 2 +3H 2 SO 4 2BF 3 ↑+3CaSO 4 +3H 2 O ;
2BF 3 ↑+3CaSO 4 +3H 2 O ;
B 2 O 3 +2NH 3 2BN+3H 2 O;
2BN+3H 2 O;
(2)(2分) ; +3
; +3
(3)(2分)120 0 , sp 2 ;
(4)(4分)离子键、极性共价键、配位键 ;109 0 28 , , sp 3 ,正四面体;
(5)(3 分) 极性共价键,范德华力 ; 3。
(1)根据反应物和生成物可知,方程式分别是
B 2 O 3 +3CaF 2 +3H 2 SO 4 2BF 3 ↑+3CaSO 4 +3H 2 O、B 2 O 3 +2NH 3
2BF 3 ↑+3CaSO 4 +3H 2 O、B 2 O 3 +2NH 3  2BN+3H 2 O。
2BN+3H 2 O。
(2)根据构造原理可写出基态B原子的电子排布图。氮元素是第ⅤA,最低价是-3价,所以B元素的化合价是+3价。
(3)在BF 3 分子中,中心原子B原子没有孤对电子,所以其结构是平面三角形,键角是120°。其中B原子的杂化轨道类型为sp2杂化。
(4)化合物NaBF 4 属于钠盐,因此含有的的化学键类型为离子键和极性键。由于氟原子含有孤对电子,所以还含有配位键。同样中心原子B原子没有孤对电子,所以其结构是正四面体形,键角是109 0 28 , , B原子是sp 3 杂化。
(5)层内B原子与N原子之间的相互作用为极性键,而层与层之间是分子间作用力。因为B原子能形成3个B-N键,所以含1 mol BN的六方氮化硼晶体中含B-N的个数为3 N A 。1年前查看全部
- (9分)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示:
(9分)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示:
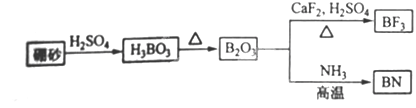
请回答下列问题:
(1)由B 2 O 3 制备BN、BF 3 的化学方程式依次是______ ___、
___ _______;
(2)BF3和过量NaF作用可生成NaBF 4 ,BF 4 - 的立体结构为____ ___;
(3)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为_ ___ _ _,层间作用力为____ ____;
(4)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼的密度是____ ___g·cm -3 (只要求列算式,不必计算出数值,阿伏伽德罗常数为N A )。 talktoyouthisway1年前1
talktoyouthisway1年前1 -
 粉钻魔法师 共回答了19个问题
粉钻魔法师 共回答了19个问题 |采纳率94.7%(1)B 2 O 3 +3CaF 2 +2H 2 SO 4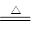 2BF 3 ↑+3CaSO 4 +3H 2 O
2BF 3 ↑+3CaSO 4 +3H 2 O
B 2 O 3 +2NH 3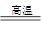 2BN+2H 2 O
2BN+2H 2 O
(2)正四面体 (1分)(3)共价键范德华力(各1分)
(4)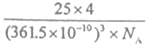 (2分)
(2分)
(1)根据反应物和生成物结合原子守恒,可以分别写出该反应的化学方程式。
(2)BF 4 - 的中心原子没有孤对电子,所以是正四面体结构。
(3)B和N均是非金属,形成的化学键是共价键。而层与层之间则是分子间作用力。
(4)根据金刚石的结构可知,晶胞中含有的原子个数是4,所以立方氮化硼中含有的微粒个数也是4,质量为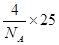 。晶胞的体积是(361.5×10 - 3 ) 3 ,所以其密度是
。晶胞的体积是(361.5×10 - 3 ) 3 ,所以其密度是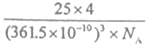 。
1年前查看全部
。
1年前查看全部
- 为什么氮化硼中N原子与B原子形成12个共价键?请详细说明,
为什么氮化硼中N原子与B原子形成12个共价键?请详细说明,
题中提示氮化硼与金刚石的结构相似,可以从晶胞中看出有四个配位键,那共价键怎么看或者怎么求呢? jacky45mm1年前2
jacky45mm1年前2 -
 jiangjing0023 共回答了22个问题
jiangjing0023 共回答了22个问题 |采纳率81.8%我们知道晶胞中每个氮连接了四个硼,每个硼也连了四个氮,但是硼最外层只有三个电子,只能形成三个共价键,氮最外层五个电子,和硼形成共价键用了三个,另外的两个电子就形成了第四个键 ,这个键全是氮给的电子所以叫做配位键.普通的键是横杠,而配位键记作→,就是这个道理.1年前查看全部
- 我国最新研制的高温超导材料氮化硼,经测定该材料中两元素的化合价均为3价,则该材料的化学式为( ) A.BN B.B 3
我国最新研制的高温超导材料氮化硼,经测定该材料中两元素的化合价均为3价,则该材料的化学式为( ) A.BN B.B 3 N 2 C.NB D.B 2 N 3  冰冷的咖啡1年前1
冰冷的咖啡1年前1 -
 笑笑过一生 共回答了17个问题
笑笑过一生 共回答了17个问题 |采纳率94.1%因为在化合物里,正负化合价的代数和为0.故它们形成化合物的化学式为BN.
故选A.1年前查看全部
- C12金刚石和氮化硼其实我想知道C的三种同位素的金刚石和六方氮化硼、立方氮化硼的硬度关系,
 ccd12011年前1
ccd12011年前1 -
 feng222 共回答了15个问题
feng222 共回答了15个问题 |采纳率93.3%B和N一个在C的前面,一个在后面,所以BN和C可以算是等电子体.
金刚石,是自然存在的硬度最大的物质,立方BN和金刚石有着相同的结构,两者硬度差不多,从一些文献上看,BN有隐约高于金刚石.
六方BN是石墨的类似物,硬度不咋的.
希望对你有所帮助!1年前查看全部
- (10分)I.(6分)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN
(10分)
I.(6分)氮化硼(BN)是一种重要的功能陶瓷材料,以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示: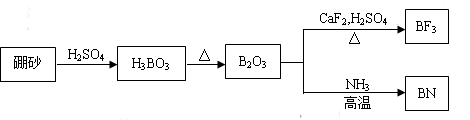
请回答下列问题:
(1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是 、
;
(2) BN中B元素的化合价为 。
II. (4分)工业上制取冰晶石(Na 3 AlF 6 )的化学方程式如下:
2Al(OH) 3 +12HF+3Na 2 CO 3 =2Na 3 AlF 6 +3CO 2 ↑+9H 2 O
请根据题意填空:
(3)反应物中有两种元素在元素周期表中位置相邻,下列能判断它们的金属性或非金属性强弱的是 ( 选填字母)。
(4)2004年,美国科学家通过“勇气”号太空探测出火星大气中含有一种称为硫化羰(化学式为COS)的物质。已知硫化羰与二氧化碳的结构相似,所有原子的最外层都满足8电子结构,且在氧气中会燃烧。请写出硫化羰的电子式 。A.气态氢化物的稳定性 B.最高价氧化物对应水化物的酸性 C.单质与氢气反应的难易 D.单质与同浓度酸发生反应的快慢  tgb2191年前1
tgb2191年前1 -
 qazzaq147 共回答了22个问题
qazzaq147 共回答了22个问题 |采纳率100%1年前查看全部
- 我国最新研制的高温超导材料氮化硼,经测定该材料中两种原子的个数比为1:1,该材料的化学式为( )
我国最新研制的高温超导材料氮化硼,经测定该材料中两种原子的个数比为1:1,该材料的化学式为( )
A. NB
B. B3N2
C. BN
D. B2N3 啖莣1年前1
啖莣1年前1 -
 可爱的兔子精 共回答了20个问题
可爱的兔子精 共回答了20个问题 |采纳率75%解题思路:根据“化合物的读法确定元素的排列顺序和标在元素符号右下角的数字表示一个分子中所含原子的个数”进行解答.根据化合物的读法可知,从后向前读作某化某,故氮化硼中两种元素的排列顺序为B、N.
根据标在元素符号右下角的数字表示一个分子中所含原子的个数可知:
A、NB 中虽原子个数比为1:1;但元素的排列顺序错误,故A不符合题意;
B、N3B2中原子个数比为3:2;故B不符合题意;
C、BN中原子个数比为1:1;故C符合题意;
D、B2N3中原子个数比为2:3;故D不符合题意.
故选C.点评:
本题考点: 化学式的书写及意义.
考点点评: 本题考查学生对物质中原子个数比知识的理解与掌握,并能灵活应用的能力.1年前查看全部
- 我国最新研制的高温超导材料氮化硼,经测定该化合物中两元素的化合价的绝对值均为3,其化学式为( )
我国最新研制的高温超导材料氮化硼,经测定该化合物中两元素的化合价的绝对值均为3,其化学式为( )
A.BN B.B3N2 C.NB D.B2N3 我知道答案是BN 是怎么算的呢? wating3541年前3
wating3541年前3 -
 欢贝贝 共回答了17个问题
欢贝贝 共回答了17个问题 |采纳率82.4%选A,化合价都是3所以只需要一个B和一个N就构成一个BN,我们在书写化学式的时候一般是负价的写在后面,正价的写在前面,由于N的核电荷数比B要大,所以N的原子核对电子的吸引力要大,所以是电子向N偏移,使N显负3价,所以化学式就是BN.1年前查看全部
- 化学选择题(关于晶体)氮化硼很难熔化,加热至3000℃方可气化.下列对氮化硼的叙述不正确的是A氮化硼是分子晶体 B氮化硼
化学选择题(关于晶体)
氮化硼很难熔化,加热至3000℃方可气化.下列对氮化硼的叙述不正确的是
A氮化硼是分子晶体 B氮化硼是原子晶体
C氮化硼是分子晶体 D化学式为BN
有1~2个选项符合题意.
抱歉,确实打错了。应为“C氮化硼是离子晶体” 开心的小妖精1年前4
开心的小妖精1年前4 -
 oobravelee 共回答了9个问题
oobravelee 共回答了9个问题 |采纳率66.7%AC
难熔、3000°C才能气化,这些都足以表现氮化硼是原子晶体.
至于化学式,根据价态推断就可以了:N的电负性强于B,所以N显负价,而N的负价中,比较稳定的是-3价,而B的特征化合价恰好是+3价,因此化学式是BN1年前查看全部
- 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示; 请回答
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示; 
请回答下列问题:
(1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是____、____;
(2)基态B原子的电子排布式为____;B和N相比,电负性较大的是________ ,BN中B元素的化合价为________ ;
(3)在BF 3 分子中,F-B-F的键角是__________ ,B原子的杂化轨道类型为_________ ,BF 3 和过量NaF作用可生成NaBF 4 , BF 4 - 的立体构型为____;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为 ______,层间作用力为 _______;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。 立方氮化硼晶胞中含有____个氮原子、____个硼原子,立方氮化硼的密度是______ g·cm -3 (只要求列算式,不 必计算出数值。阿伏加德罗常数为N A )。 mousemay19841年前1
mousemay19841年前1 -
 ltsfgoon 共回答了24个问题
ltsfgoon 共回答了24个问题 |采纳率87.5%1年前查看全部
- 同位素碳14金刚石和聚氮化硼(BN)x相比,哪个更硬?两者的莫氏硬度分别是多少?
 seaslight1年前1
seaslight1年前1 -
 咖啡zz 共回答了14个问题
咖啡zz 共回答了14个问题 |采纳率71.4%(常温)同位素碳14金刚石>聚氮化硼(BN)x
依照摩氏硬度标准(Mohs hardness scale)共分10级,钻石(金刚石)为最高级第10级;如小刀其硬度约为5.5、铜币约为3.5至4、指甲约为2至3、玻璃硬度为6.
等级1 滑石
等级2 石膏
等级3 方解石
等级4 萤石
等级5 磷灰石
等级6 正长石
等级7 石英
等级8 黄玉
等级9 钢玉
等级10 钻石1年前查看全部
- (2011•江西)氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图
(2011•江西)氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示

请回答下列问题:
(1)由B2O3制备BF3、BN的化学方程式依次是B2O3+3CaF2+3H2SO4
2BF3↑+3CaSO4+3H2O△ .B2O3+3CaF2+3H2SO4、
2BF3↑+3CaSO4+3H2O△ .B2O3+2NH3
2BN+3H2O高温 .B2O3+2NH3;
2BN+3H2O高温 .
(2)基态B原子的电子排布式为______;B和N相比,电负性较大的是______,BN中B元素的化合价为______;
(3)在BF3分子中,F-B-F的键角是______,B原子的杂化轨道类型为______,BF3和过量NaF作用可生成NaBF4,BF4-的立体结构为______;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为______,层间作用力为______;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有______个氮原子、______个硼原子,立方氮化硼的密度是25×4 (361.5×10−101×)3NA g•pm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA).25×4 (361.5×10−101×)3NA  逸尘映月1年前0
逸尘映月1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 我国最新研制的高温超导材料氮化硼,经测定该化合物中两元素的化合价的绝对值均为3,其化学式为( )
我国最新研制的高温超导材料氮化硼,经测定该化合物中两元素的化合价的绝对值均为3,其化学式为( )
A.BN B.B3N2 C.NB D.B2N3 我知道答案是BN 是怎么算的呢? 森林鹿1年前3
森林鹿1年前3 -
 绕树三匝1 共回答了13个问题
绕树三匝1 共回答了13个问题 |采纳率92.3%选A,化合价都是3所以只需要一个B和一个N就构成一个BN,我们在书写化学式的时候一般是负价的写在后面,正价的写在前面,由于N的核电荷数比B要大,所以N的原子核对电子的吸引力要大,所以是电子向N偏移,使N显负3价,所以化学式就是BN.1年前查看全部
- 立体氮化硼密度怎么算
 l79x05l101年前3
l79x05l101年前3 -
 aouy 共回答了11个问题
aouy 共回答了11个问题 |采纳率90.9%只要知道晶胞参数,所有物质的密度都可以求得,计算有公式:
密度= Z*M/(NA*V)
其中,Z为晶胞中以化学式计量的单元数,如在立方氮化硼的晶胞中有4个N和4个B,因此Z=4
M为化学式计算的摩尔质量g/mol,
NA为阿氏常数,
V为晶胞体积cm(3),通常晶胞参数用埃,换成cm,如立方氮化硼的晶胞参数为3.615埃,即3.615*10^(-8)cm
据此求得立方氮化硼的密度:4*24.8/(6.023*10^23 * (3.615*10^(-8))^3 = 3.486 g/cm(3)1年前查看全部
- 氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示
氮化硼(BN)是一种重要的功能陶瓷材料.以天然硼砂为起始物,经过一系列反应可以得到BF 3 和BN,如下图所示

请回答下列问题:
(1)由B 2 O 3 制备BF 3 、BN的化学方程式依次是 、 ;
(2)基态B原子的电子排布式为 ;B和N相比,电负性较大的是
,BN中B元素的化合价为 ;
(3)在BF 3 分子中,F-B-F的键角是 ,B原子的杂化轨道类型为
,BF 3 和过量NaF作用可生成NaBF 4 ,BF 4 - 的立体结构为 ;
(4)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为 ,层间作用力为 ;
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm,立方氮化硼晶胞中含有 个氮原子、 个硼原子,立方氮化硼的密度是 g•cm -3 (只要求列算式,不必计算出数值,阿伏伽德罗常数为N A ) shenlijia1年前1
shenlijia1年前1 -
 爱上天使的泪 共回答了16个问题
爱上天使的泪 共回答了16个问题 |采纳率81.3%
(1)由图可知B 2 O 3 与CaF 2 和H 2 SO 4 反应即生成BF 3 ,同时还应该产生硫酸钙和水, B 2 O 3 与氨气在高温下反应即生成BN。
(2)基态B原子的电子排布式为1s 2 2s 2 2p 1 ;B与N 均位于第二周期,电负性从左向右依次递减,所以N的电负性大于B;BN中B元素的化合价为+3。
(3)依据价层电子对互斥理论,计算出BF 3 的孤对电子对数为0,并且价层电子对数为3,所以BF 3 分子为平面正三角形结构,键角为120°,杂化方式为sp 2 ;BF 4 - 中心原子的孤对电子对数为0,其价层电子对数为4,所以其结构为正四面体.故答案为:120°;sp 2 ;正四面体;
(4)B、N均属于非金属元素,二者形成的化学键是极性共价键;根据石墨结构可知六方氮化硼晶体中,层与层之间靠分子间作用力结合。
(5)根据金刚石的结构可以判断出金刚石的一个晶胞中含有的碳原子数8,则一个立方氮化硼晶胞中含有4个N原子和4个B原子.一个晶胞中的质量为25×4g/N A ,一个立方氮化硼晶胞的体积是(361.5×10 -10 cm) 3 ,其密度为,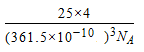 。
1年前查看全部
。
1年前查看全部
- 氮化硅属于什么晶体,氮化硼融化克服什么作用力
 2782366451年前1
2782366451年前1 -
 李奕瞳 共回答了18个问题
李奕瞳 共回答了18个问题 |采纳率83.3%原子晶体
克服的是 共价键1年前查看全部
- 为什么金刚石熔点比氮化硼高?
 28号囚徒1年前1
28号囚徒1年前1 -
 HinAnx 共回答了15个问题
HinAnx 共回答了15个问题 |采纳率93.3%立方氮化硼与金刚石同属原子晶体,二者结构类似,B、N的原子半径均小于C的原子半径,B-N键能必然比C-C键能大,所以立方氮化硼的熔点比金刚石高1年前查看全部
- 一氮化硼(BN)的一种晶体结构和金刚石相似,密度为3.52g.cm-3,求B-N的键长.我算出来了一个晶胞的边长,用d表
一氮化硼(BN)的一种晶体结构和金刚石相似,密度为3.52g.cm-3,求B-N的键长.我算出来了一个晶胞的边长,用d表示,答案是(√3╱4)d.为什么呢?
二磷酸(H3PO4)中P与非羟基的O之间的共价键为什么不是普通的共价键,而是配位键? 心是乱乱的1年前3
心是乱乱的1年前3 -
 苏零一 共回答了20个问题
苏零一 共回答了20个问题 |采纳率85%(1)金刚石的晶格,是碳原子sp3杂化,所以可以看做是4个碳分布于正四面体的端点,另一个在中心.氮化硼的晶胞和它类似,只不过不同取向的碳原子分别对应于N和B.所以一个氮化硼的晶胞有八个分子,(2^3)我们先算晶胞的C3轴,...1年前查看全部
大家在问
- 1一会儿风,一会儿雨.造句不少于20字.
- 2三角形ABC内接于圆O,角BAC=45度,角ABC=15度,OC与AD平行,求BC:CD的值
- 3英语,这个句子的时态有点怪.There was a knock on the front door.she knew t
- 4is this eraser?回答 回答意思
- 51.She is from WeshingtonD.C.(就划线部分提问)
- 6一分钟可以用来微笑,对他人,对自己,对生活微笑;(照这样仿写句子,该怎么写?)
- 71.a^2+a=0,求a^2009+a^2010+12的值
- 8求下列式子中x的值:(1)x²=196
- 9Dear students, please read every sentence carefully. ___ you
- 10如图是一个立方体图形的侧面展开图(单位:厘米),求这个立体图形的表面积和体积.
- 11从倾角为θ的足够长的斜面顶端A点
- 12金华市2010学年第一学期初三英语期末试卷答案
- 13下列各一元二次不等式中,解集为空集的是( )
- 14用竖式计算下面各题,并验算. 635-182= 626-357= 406+195= 972-421= 260+525=
- 15哪三个数的和和它们的积相等