用FeTiO3与Na在一定条件下生成TI和NaCl.化学反应方程式是?
 庄佳汉2022-10-04 11:39:541条回答
庄佳汉2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 ltw5dj 共回答了10个问题
ltw5dj 共回答了10个问题 |采纳率90%- 两者不是直接反应的,FeTiO3是钛铁矿的主要成分,得先经过处理,发生多步反应,生成TiCl4,然后用Na去置换.TiCl4+4Na=高温=4NaCl+Ti 该反应是工业制取钛的最后一步反应.
工业上常用硫酸分解钛铁矿的方法制取二氧化钛,再由二氧化钛制取金属钛.浓硫酸处理磨碎的钛铁矿(精矿),发生下面的化学反应:FeTiO3+3H2SO4 == Ti(SO4)2+FeSO4+3H2O FeTiO3+2H2SO4 == TiOSO4+FeSO4+2H2O FeO+H2SO4 == FeSO4+H2O Fe2O3+3H2SO4 == Fe2(SO4)3+3H2O 为了除去杂质Fe2(SO4)3,加入铁屑,Fe3+ 还原为Fe2+,然后将溶液冷却至273K以下,使得FeSO4·7H2O(绿矾)作为副产品结晶析出.Ti(SO4)2和TiOSO4水解析出白色的偏钛酸沉淀,反应是:Ti(SO4)2+H2O == TiOSO4+H2SO4 TiOSO4+2H2O == H2TiO3+H2SO4 锻烧偏钛酸即制得二氧化钛:H2TiO3 == TiO2+H2O 工业上制金属钛采用金属热还原法还原四氯化钛.将TiO2(或天然的金红石)和炭粉混合加热至1000~1100K,进行氯化处理,并使生成的TiCl4,蒸气冷凝.TiO2+2C+2Cl2=TiCl4+2CO- 在1070K 用熔融的镁在氩气中还原TiCl4可得多孔的海绵钛:TiCl4+2Mg=2MgC12+Ti 这种海绵钛经过粉碎、放入真空电弧炉里熔炼,最后制成各种钛材.也可以通过反应:Ti+2I2=TiI4 得到的TiI4经过高温(1250℃左右)情况下分TiI4=Ti+2I2
你可以百度一下“钛”,或得更多相关信息. - 1年前
相关推荐
- 科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3)资源.人类有望利用月球上的水资源,并通过
科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3)资源.人类有望利用月球上的水资源,并通过电解获取氢气为火箭提供燃料,获取的氧气可逐渐形成可供呼吸的大气层,用来满足植物和人类所需.下图是根据科学家设想的有关人类利用月球资源的流程图.
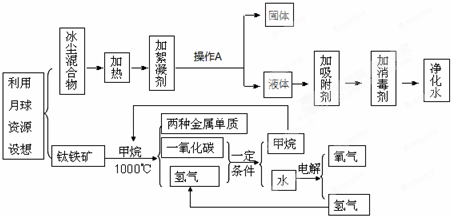
(1)操作A的名称______.
(2)所加的吸附剂通常为______(填名称).
(3)钛铁矿与甲烷反应的化学方程式FeTiO3+3CH4
Fe+Ti+3CO+6H21000℃ .FeTiO3+3CH4.
Fe+Ti+3CO+6H21000℃ .
(4)该流程图中可循环利用的物质是______和______. 比妮白1年前1
比妮白1年前1 -
 若不是因为爱着你 共回答了25个问题
若不是因为爱着你 共回答了25个问题 |采纳率84%解题思路:(1)通过操作A后得到了沉淀和溶液,可以据此判断操作A为过滤,可以据此解答.
(2)在净化水的过程中,常用活性炭来净水,可以据此解答该题.
(3)根据钛铁矿中的主要成分可以知道,在与甲烷反应时生成了氢气、一氧化碳以及两种金属,可以据此结合质量守恒定律来完成该化学方程式的书写.
(4)根据流程图中可以知道可以循环利用的物质为甲烷和氢气,可以据此解答该题.(1)通过操作A后得到了沉淀和溶液,可以据此判断操作A为过滤.
(2)活性炭具有吸附性,故在净化水的过程中,常用活性炭来净水.
(3)根据钛铁矿中的主要成分可以知道,在与甲烷反应时生成了氢气、一氧化碳以及两种金属,可以据此结合质量守恒定律可以知道生成的金属为铁和钛,该反应的化学方程式为:FeTiO3+3CH4
1000℃
.
Fe+Ti+3CO+6H2.
(4)根据流程图中可以知道可以循环利用的物质为甲烷和氢气.
故答案为:(1)过滤.
(2)活性炭.
(3)FeTiO3+3CH4
1000℃
.
Fe+Ti+3CO+6H2.
(4)甲烷和氢气.点评:
本题考点: 物质的相互转化和制备.
考点点评: 要想解答好这类题目,首先,要理解和熟记物质的相互转化和制备方法,以及与之相关的知识.然后,根据所给的实验、问题情景,结合所学的相关知识和技能,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.1年前查看全部
- (2011•江宁区一模)科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3)资源.人类有望利
(2011•江宁区一模)科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3)资源.人类有望利用月球上的水资源,并通过电解获取氢气为火箭提供燃料,获取的氧气可逐渐形成或供呼吸的大气层,用来满足植物和人类所需.下图是根据科学家设想的有关人类利用月球资源的流程图.

(1)得到净化水的过程中,可做吸附剂的物质有______(填一种物质名称)
(2)该流程图中可循环利用的物质是______和______
(3)推测流程图中的“金属单质”是______
(4)根据流程图的信息,写出CO和H2反应的化学方程式CO+3H2
CH4+H2O一定条件 .CO+3H2.
CH4+H2O一定条件 .
(5)纯水的导电能力极弱.电解水时可加入硫酸、氢氧化钠等物质增加导电性.给10%的硫酸溶液通电(实质为电解水,硫酸不发生化学变化)时,获得下列四组实验数据,你认为其中最接近理论值的一组是______(填字母序号)
氧气质量/g 氢气质量/g 硫酸的质量分数 A 64 8 10% B 10 2 10% C 16 2 11% D 16 32 11%  june_88240861年前1
june_88240861年前1 -
 迷途小书虫 共回答了25个问题
迷途小书虫 共回答了25个问题 |采纳率72%解题思路:(1)活性炭具有吸附作用,能够吸附水中的色素和异味;
(2)根据图中信息可以判断各种物质的用途;
(3)根据质量守恒定律可以判断生成物;
(4)一氧化碳和氢气在一定条件下反应能生成甲烷和水;
(5)通过计算可以判断相关方面的问题.(1)活性炭能够吸附水中的杂质,可以用来净化水.故填:活性炭.
(2)由图中信息可知,甲烷和氢气可以循环利用.故填:甲烷、氢气.
(3)钛铁矿中含有金属元素铁和钛,和甲烷反应后能够生成铁和钛.故填:铁和钛.
(4)一氧化碳和氢气反应的化学方程式为:CO+3H2
一定条件
.
CH4+H2O.
(5)电解水的化学方程式及其反应物和生成物的质量关系为:2H2O
通电
.
2H2↑+O2↑,
36 4 32
由质量关系可知,生成的氢气和氧气的质量比是1:8,A和C中,生成的氢气和氧气的质量比是1:8,电解过程中,水的质量减小,硫酸的质量不变,硫酸的质量分数增大,C符合.故填:C.点评:
本题考点: 水的净化;电解水实验;物质的相互转化和制备;书写化学方程式、文字表达式、电离方程式.
考点点评: 本题主要考查净化水的方法和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- (2013•漳州二模)钛铁矿的主要成分为FeTiO3(可表示为FeO•TiO2),含有少量MgO、CaO、SiO2等杂质
(2013•漳州二模)钛铁矿的主要成分为FeTiO3(可表示为FeO•TiO2),含有少量MgO、CaO、SiO2等杂质.利用钛铁矿制备锂离子电池电极材料(钛酸锂Li4Ti5O12和磷酸亚铁锂LiFePO4)的工业流程如图所示:

已知:FeTiO3与盐酸反应的离子方程式为:FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
(1)化合物FeTiO3中铁元素的化合价是______.
(2)滤渣A的成分是______.
(3)滤液B中TiOCl42-转化生成TiO2的离子方程式是______.
(4)反应②中固体TiO2转化成(NH4)2Ti5O15溶液时,Ti元素的浸出率与反应温度的关系如图所示.反应温度过高时,Ti元素浸出率下降的原因是______.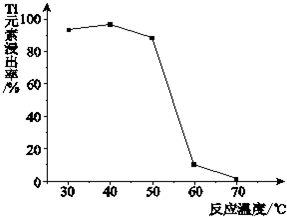
(5)反应③的化学方程式是______.
(6)由滤液D制备LiFePO4的过程中,所需17%双氧水与H2C2O4的质量比是______.
(7)若采用钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)作电极组成电池,其工作原理为:Li4Ti5O12+3LiFePO4⇌
+3FePO4该电池充电时阳极反应式是______.充电Li7Ti5O12放电  梦吾1年前1
梦吾1年前1 -
 _fdg2f3css5f00 共回答了21个问题
_fdg2f3css5f00 共回答了21个问题 |采纳率100%解题思路:(1)根据反应FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O,不是非氧化还原反应,可以判断铁元素化合价为+2价;
(2)MgO、CaO、SiO2等杂质中,二氧化硅不溶于稀盐酸,成为滤渣A;
(3)根据流程图示,TiOCl42-在溶液中加热与水反应生成二氧化钛沉淀;
(4)二氧化钛与氨水、双氧水反应生成NH4)2Ti5O15,温度过高,双氧水和氨水都容易分解;
(5)反应3是(NH4)2Ti5O15与强氧化锂反应生成Li2Ti5O15沉淀和氨水;
(6)根据电子守恒找出双氧水与草酸的关系式,然后列式计算计算出17%双氧水与H2C2O4的质量比;
(7)充电时按照电解槽进行分析,阳极氧化阴极还原,写出阳极放电的电解方程式即可.(1)反应FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O中,不是非氧化还原反应,可以判断铁元素化合价为+2价,
故答案为:+2;
(2)由于杂质中二氧化硅不溶于盐酸,所以滤渣A成分是二氧化硅,
故答案为:SiO2;
(3)根据流程可知,TiOCl42-在溶液中加热与水反应生成二氧化钛沉淀,反应的离子方程式为:TiOCl42-+H2O=TiO2↓+2H++4Cl-,
故答案为:TiOCl42-+H2O=TiO2↓+2H++4Cl-;
(4)由于二氧化钛与氨水、双氧水反应生成NH4)2Ti5O15时,温度过高,双氧水和氨水都容易分解,所以反应温度过高时,Ti元素浸出率下降,
故答案为:温度过高时,反应物氨水(或双氧水)受热易分解;
(5)根据流程图示可知,反应3是(NH4)2Ti5O15与强氧化锂反应生成Li2Ti5O15沉淀和氨水,反应的化学方程式为:(NH4)2Ti5O15+2 LiOH=Li2Ti5O15↓+2NH3•H2O(或2NH3+2H2O),
故答案为:(NH4)2Ti5O15+2 LiOH=Li2Ti5O15↓+2NH3•H2O(或2NH3+2H2O);
(6)根据电子守恒,氧化铁元素转移的电子就等于铁离子氧化草酸转移的电子数,
因此可得关系式:H2O2~H2C2O4,设双氧水质量为x,草酸质量为y,
34 90
x×17% y
34y=90×x×17%,x:y=20:9,
17%双氧水与H2C2O4的质量比为20:9,
故答案为:20:9;
(7)充电时,阳极发生氧化反应,LiFePO4失去电子生成FePO4,电极反应为:LiFePO4-e-=FePO4+Li+,
故答案为:LiFePO4-e-=FePO4+Li+.点评:
本题考点: 制备实验方案的设计;电解原理;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题借助利用钛铁矿制备锂离子电池电极材料流程,考查了化合价判断、离子方程式书写、电极方程式书写、化学计算等知识,涉及的内容较多,综合性较强,充分考查了学生的综合能力,本题难度中等.1年前查看全部
- (2010•上杭县模拟)雄伟壮观的国家大剧院主体建筑表面使用的是钛合金板.工业上常用钛铁矿(FeTiO3)来冶炼钛.已知
(2010•上杭县模拟)雄伟壮观的国家大剧院主体建筑表面使用的是钛合金板.工业上常用钛铁矿(FeTiO3)来冶炼钛.已知钛酸亚铁中铁的化合价是+2价,则钛的化合价是( )
A.+2
B.+3
C.+4
D.+5 打火机与烟灰缸1年前1
打火机与烟灰缸1年前1 -
 vollmer 共回答了13个问题
vollmer 共回答了13个问题 |采纳率92.3%解题思路:根据在化合物中正负化合价代数和为零,结合钛酸亚铁[FeTiO3]的化学式进行解答本题.根据在化合物中正负化合价代数和为零,铁元素显+2价,氧元素显-2价,设钛元素的化合价是x,可知钛酸亚铁[FeTiO3]中钛元素的化合价:(+2)+x+(-2)×3=0,则x=+4.
故选C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.1年前查看全部
- (2012•金山区二模)钛铁矿主要成分的化学式为FeTiO3,其中铁元素化合价显+3价,则Ti化合价为( )
(2012•金山区二模)钛铁矿主要成分的化学式为FeTiO3,其中铁元素化合价显+3价,则Ti化合价为( )
A.+2
B.+3
C.+4
D.+6 83hgf81年前1
83hgf81年前1 -
 那一贱的风采 共回答了12个问题
那一贱的风采 共回答了12个问题 |采纳率100%解题思路:根据主要成分的化学式为FeTiO3,及铁元素的化合价为+3,利用化合物中元素的正负化合价代数和等于0来解答.在FeTiO3中,铁元素的化合价为+3,氧元素的化合价为-2,
设Ti的化合价为x,
由化学式为FeTiO3,并根据化合物中元素的正负化合价代数和等于0,则
(+3)+x+(-2)×3=0
解得x=+3
故选B.点评:
本题考点: 常见元素与常见原子团的化合价;化合价规律和原则;有关元素化合价的计算.
考点点评: 本题考查根据化学式确定元素的化合价,学生应利用好习题中的化学式及铁元素的化合价,注重与课本知识的结合来解决信息中的同类问题.1年前查看全部
- 钛是一种重要的金属,工业上用钛铁矿(主要成分为FeTiO3,含FeO、Al2O3、SiO2 等杂质)为原料制钛
钛是一种重要的金属,工业上用钛铁矿(主要成分为fetio3,含feo、al2o3、sio2 等杂质)为原料制钛***(tio2),tio2常通过两种方法可制得 ti.

其中,2h2so4+fetio3=tioso4+feso4+2h2o.回答下列问题.
(l)净化钛矿石时,需用浓氢氧化钠溶液来处理,该过程中发生反应的化学方程式有:
sio2+2naoh=na2sio3+h2o 和______
(2)滤液①中的溶质主要是 feso4,检验其中fe2+的方法是:______.
(3)从 tioso4→h2tio3需要加热,则加热的目的是:______.
(4)电解 tio2来获得 ti 是以 tio2作阴极,石墨为阳极,熔融cao为电解液,用碳块作电解槽池.其阴极反应的电极反应式为:______.
(5)从化学平衡的角度解释:往tio2和cl2反应体系中加入焦炭后,能使反应 tlo2(s)+2cl2(g)═tlcl4(l)+o2(g)顺利进行的原因是:______. senyan1年前1
senyan1年前1 -
 cclei 共回答了14个问题
cclei 共回答了14个问题 |采纳率85.7%解题思路:(1)根据钛铁矿中的杂质氧化铝与碱反应生成可溶的铝盐溶液来回答;
(2)根据Fe2+能被氧化剂掩盖为三价铁离子,铁离子遇到硫氰酸根离子显示红色;
(3)根据TiOSO4的水解平衡的影响因素知识来回答;
(4)根据电解原理:阴极上是发生得电子的还原反应;
(5)从平衡移动的原理:减少生成物的浓度,化学平衡向着正反应方向移动.(1)钛铁矿含FeO、Al2O3、SiO2等杂质,能与碱反应物质除了SiO2还有Al2O3,故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(2)因滤液①中的溶质主要是FeSO4,所一先加几滴KSCN溶液,再加几滴氯水,观察溶液是否变为红色,故答案为:取少许滤液①于试管中,滴入几滴KSCN溶液,无明显现象,然后滴入几滴氯水,溶液变为红色,说明其中含有Fe2+;
(3)从 TiOSO4→H2TiO3是物质水解的过程,加热能够促进水解的进行,故答案为:促进TiOSO4的水解;
(4)因TiO2作阴极,得到电子,被还原,得到单质Ti,故答案为:TiO2 +4e-=Ti+2O2-;
(5)因减少生成物的浓度,平衡正向移动,故答案为:碳单质与氧气反应减小产物浓度使平衡向右移动,导致反应顺利进行.点评:
本题考点: 金属冶炼的一般原理;电解原理;二价Fe离子和三价Fe离子的检验;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题涉及金属的冶炼原理、电解原理、亚铁离子的检验以及化学平衡的移动原理等方面的知识,属于综合知识的考查,难度不大.1年前查看全部
- 四氧化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料.由钛铁矿(主要成为是FeTiO3)制备TiCl4
 躺而求坐1年前1
躺而求坐1年前1 -
 haim8888 共回答了20个问题
haim8888 共回答了20个问题 |采纳率85%(1)粉碎的目的:减小钛铁矿粒度,增大其表面积,以利于钛铁矿在酸溶过程中能以较快的速度和较彻底的程度发生.
(2)Fe + 2H+ = Fe2+ + H2
(3)硫酸亚铁
(4)分解反应
(5)TiO2 + 2C + Cl2 = TiCl4 + 2CO
(6)工艺流程中有较多的“三废”排放.
(7)烧杯、漏斗、玻璃棒1年前查看全部
- 四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品
四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
加入铁屑的作用是______.
(2)在②→③工艺中需要控制条件以形成TiO2•n H2O溶胶,该分散质颗粒直径大小在______范围.
(3)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流程中存在的不足之处是______(只要求写出一项).
(4)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用______方法.
TiCl4 SiCl4 熔点/℃ -25.0 -68.8 沸点/℃ 136.4 57.6  小雨两三朵1年前1
小雨两三朵1年前1 -
 莫莫无畏 共回答了11个问题
莫莫无畏 共回答了11个问题 |采纳率100%解题思路:(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm);
(3)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(4)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,通常采取蒸馏方法分离.(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+,加入铁屑作还原剂,将Fe3+还原为Fe2+,防止Ti3+被Fe3+氧化成TiO2+,
故答案为:防止Ti3+被Fe3+氧化成TiO2+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm),
故答案为:10-9~10-7m(或1nm-100nm);
(3)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(4)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,要精制含少量SiCl4杂质的TiCl4,可采用蒸馏(或分馏)方法,
故答案为:蒸馏(或分馏).点评:
本题考点: 制备实验方案的设计.
考点点评: 本题考查学生阅读题目获取信息能力、氧化还原反应、绿色化学、胶体、物质分离提纯等,难度不大,注意基础知识的掌握利用.1年前查看全部
- (2014•甘肃二模)工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示.钛铁矿主要成分为钛酸亚铁(FeTiO3),
(2014•甘肃二模)工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示.钛铁矿主要成分为钛酸亚铁(FeTiO3),其中一部分铁元素在风化过程中会转化为+3价.
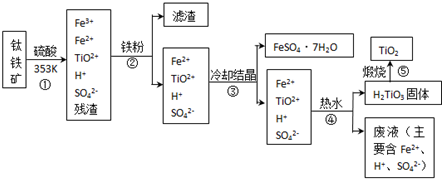
已知:TiOSO4遇水会水解.
(1)步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为______.
(2)步骤③中,实现混合物的分离是利用物质的______(填字母序号).
a.熔沸点差异 b.溶解性差异c.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是______(填操作名称).
(4)请结合化学用语用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:______.
(5)可以利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),该反应的离子方程式为______.
(6)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如下图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛.
①写出阳极所发生反应的电极反应式:______.
②在制备金属钛前后,CaO的总量不变,其原因是(请结合化学用语解释)制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2
Ti+2CaO,由此可见,CaO的量不变;一定条件 .制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2.
Ti+2CaO,由此可见,CaO的量不变;一定条件 . yokoo1年前1
yokoo1年前1 -
 lnn1123 共回答了23个问题
lnn1123 共回答了23个问题 |采纳率95.7%解题思路:(1)铁粉将Fe3+转化为Fe2+;
(2)溶液中析出晶体是利用物质溶解度的不同得到;
(3)②③④都是从溶液中得到固体的分离过程,需要用过滤装置;
(4)依据溶液中存在平衡:TiO2++2H2O⇌H2TiO3+2H+,平衡影响因素和平衡移动原理分析判断;
(5)废液主要是亚铁离子、氢离子和二氧化锰反应发生氧化还原反应生成锰离子和铁离子;
(6)①依据装置图分析判断,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳;
②制备TiO2时,在电解槽发生如下反应:阴极:2Ca2++4e-═2Ca 阳极:2O2--4e-═O2↑,2Ca+TiO2
Ti+2CaO,由此可见,CaO的量不变.一定条件 .(1)故答案为:步骤②中,用铁粉将Fe3+转化为Fe2+的反应的离子方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe═3Fe2+;
(2)步骤③冷却结晶得到硫酸亚铁晶体,利用的是物质溶解度的不同,通过冷却热饱和溶液得到,故答案为:b;
(3)②③④步骤的操作过程中都得到沉淀或晶体,所以需要过滤得到固体和溶液,故答案为:过滤;
(4)④中使用热水的目的是促进TiO2+水解生成H2TiO3,分离出固体加热得到TiO2;溶液中存在平衡:TiO2++2H2O⇌H2TiO3+2H+,当加入热水稀释、升温后,
平衡正向移动,生成H2TiO3;
故答案为:溶液中存在平衡:TiO2++2H2O⇌H2TiO3+2H+,当加入热水稀释、升温后,平衡正向移动,生成H2TiO3.
(5)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应生产硫酸锰(MnSO4,易溶于水),利用二氧化锰的氧化性氧化亚铁离子为三价铁离子,反应的离子方程式为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(6)①用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,阳极发生氧化反应,阴极析出钙金属发生还原反应,阳极图示产物可可知,阳极生成二氧化碳气体,是电解质中的氧离子失电子生成氧气,氧气和阳极石墨反应生成的二氧化碳,所以电极反应为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
故答案为:2O2--4e-=O2↑,或C+2O2--4e-=CO2↑;
②制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2
一定条件
.
Ti+2CaO,由此可见,CaO的量不变;
或:制备TiO2时,在电解槽发生如下反应:阴极:2Ca2++4e-═2Ca阳极:2O2--4e-═O2↑;2Ca+TiO2
一定条件
.
Ti+2CaO,由此可见,CaO的量不变;
故答案为:制备TiO2时,在电解槽发生如下反应:2CaO═2Ca+O2↑,2Ca+TiO2
一定条件
.
Ti+2CaO,由此可见,CaO的量不变.点评:
本题考点: 制备实验方案的设计;电解原理;物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查了物质分离的流程分析判断,物质性质的应用,离子性质的应用,分离操作的方法,氧化还原反应的离子方程式的书写方法,电解池原理的应用,电极反应的书写原则.1年前查看全部
- 科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3 )资源.人类有望利用月球上的水
科学探测发现月球贮存有一定数量的冰尘混合物、甲烷和钛铁矿(主要成分FeTiO3 )资源.人类有望利用月球上的水资源,并通过电解获取氢气为火箭提供燃料,获取的氧气可逐渐形成可供呼吸的大气层,用来满足植物和人类所需.如图是根据科学家设想的有关人类利用月球资源的流程图.

(1)得到净化水的过程中,可做吸附剂的物质有______(填一种物质名称)
(2)该流程图中可循环利用的物质是______和______
(3)推测流程图中的“两种金属单质”是______
(4)根据流程图的信息,写出CO和H2反应的化学方程式CO+3H2
CH4+H2O一定条件 .CO+3H2
CH4+H2O一定条件 .
(5)若电解水得到氧气的质量为8千克,同时得到氢气______千克. 不哭的猪1年前1
不哭的猪1年前1 -
 solomicky 共回答了21个问题
solomicky 共回答了21个问题 |采纳率95.2%解题思路:(1)活性炭具有吸附作用,能够吸附水中的色素和异味;
(2)根据图中信息可以判断各种物质的用途;
(3)根据质量守恒定律可以判断生成物;
(4)一氧化碳和氢气在一定条件下反应能生成甲烷和水;
(5)根据氧气的质量可以求出生成氢气的质量进行解答.(1)活性炭能够吸附水中的杂质,可以用来净化水.
(2)由图中信息可知,甲烷和氢气可以循环利用.
(3)钛铁矿中含有金属元素铁和钛,和甲烷反应后能够生成铁和钛.
(4)一氧化碳和氢气反应生成甲烷和水,反应的化学方程式为:CO+3H2
一定条件
.
CH4+H2O.
(5)设生成氢气的质量为x.
2H2O
通电
.
2H2↑+O2↑
432
x8kg
[4/x=
32
8kg]
x=1kg
答:生成氢气的质量为1kg.
故答案为:(1)活性炭;
(2)CH4;H2;
(3)铁和钛;
(4)CO+3H2
一定条件
.
CH4+H2O;
(5)1.点评:
本题考点: 物质的相互转化和制备;水的净化;质量守恒定律及其应用;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
考点点评: 本题主要考查净化水的方法和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律.1年前查看全部
- 单质钛的机械强度高,抗腐蚀能力强,有“未来金属”之称.工业上常用硫酸分解钛铁矿(主要成分是钛酸亚铁FeTiO3)的方法来
单质钛的机械强度高,抗腐蚀能力强,有“未来金属”之称.工业上常用硫酸分解钛铁矿(主要成分是钛酸亚铁FeTiO3)的方法来制取TiO2,再由TiO2制金属钛.主要反应有:
①FeTiO3+3H2SO4═Ti(SO4)2+FeSO4+3H2O
②Ti(SO4)2+3H2O═H2TiO3↓+2H2SO4
③H2TiO3
TiO2+H2O△
④TiO2+2C+2Cl2
TiCl4+2CO△
⑤TiCl4+2Mg
2MgCl2+Ti△
下列叙述正确的是( )
A.反应①是氧化还原反应
B.反应②是氧化还原反应
C.反应④中TiO2是氧化剂
D.反应⑤中TiCl4是氧化剂 xaxia1年前1
xaxia1年前1 -
 haha25 共回答了17个问题
haha25 共回答了17个问题 |采纳率94.1%解题思路:A、依据反应前后元素化合价的变化分析判断;
B、依据反应前后元素化合价的变化判断;
C、钛元素化合价未变;
D、钛元素化合价降低作业环境;A、①反应前后无化合价的变化,不是氧化还原反应,故A错误;
B、反应②前后无元素化合价的变化,不是氧化还原反应,故B错误;
C、反应④中 钛元素化合价无变化,故C错误;
D、反应⑤钛元素从+4价变化为0价,做氧化剂,故D正确;
故选D.点评:
本题考点: 氧化还原反应.
考点点评: 本题考查氧化反应、化合价、反应类型及原子与离子的关系,考查知识点全面,题目适中.1年前查看全部
- 四氯化钛(TiCl4)是制取航天航空工业的材料--钛合金的重要原料.由钛铁矿(主要成份是FeTiO3)制备TiCl4等产
四氯化钛(TiCl4)是制取航天航空工业的材料--钛合金的重要原料.由钛铁矿(主要成份是FeTiO3)制备TiCl4等产品的一种工艺流程示意图如下:

(1)步骤①钛铁矿加硫酸前经过选矿、洗涤、粉碎,其中粉碎的目的是______.
(2)步骤②加入铁屑,发生反应的化学方程式有______和Fe2(SO4)3+Fe═3FeSO4.
(3)步骤③制得的副产品是(填名称)______晶体.
(4)步骤⑤灼烧发生的反应类型是______反应.
(5)步骤⑥TiO2和焦炭、氯气反应生成TiCl4和CO的化学方程式:TiO2+2C+2Cl2
TiCl4+2CO高温 .TiO2+2C+2Cl2.
TiCl4+2CO高温 .
(6)上述工艺具有成本低、可以用低品位的矿物为原料等优点,但依据绿色化学理念,该工艺流程中存在的不足之处是______.
(7)上述流程中多次进行过滤操作,在实验室中,过滤必须用到的玻璃仪器有______. annehechen1年前1
annehechen1年前1 -
 melikexing 共回答了21个问题
melikexing 共回答了21个问题 |采纳率95.2%解题思路:(1)根据加快反应速度的方法考虑;(2)根据混合液中的物质考虑;(3)根据铁与硫酸反应、铁与硫酸铁反应的生成物考虑;(4)根据反应物和生成物的种类考虑;(5)根据方程式的写法考虑;(6)根据排放的物质考虑;(7)根据过滤时用到的仪器考虑.(1)增大可燃物接触面积可以使反应速度加快,反应充分,粉碎的目的是增大接触面积,使反应充分;
(2)由于混合物中含有硫酸,所以加入铁后,铁与硫酸反应生成硫酸亚铁和氢气,氢气后面标上上升符号;
(3)由于在步骤②中铁与硫酸反应生成硫酸亚铁和氢气,铁与硫酸铁反应生成硫酸亚铁,所以趁热过滤后可得到硫酸亚铁晶体;
(4)步骤⑤灼烧发生的反应的反应物是H2TiO3,生成物是TiO2和H2O,反应物只有一种物质,生成物有两种,属于分解反应;
(5)反应物是TiO2和焦炭、氯气,生成物是四氯化钛和一氧化碳,用观察法配平,反应条件是高温写在等号的上边;
(6)该工艺流程能释放出废液、废气、废渣污染环境;
(7)过滤用到的仪器有:铁架台、烧杯、漏斗、玻璃棒;所以玻璃仪器有:漏斗、烧杯、玻璃棒.
故答案为:(1)增大接触面积,使反应充分;(2)H2SO4+Fe═FeSO4+H2↑;(3)硫酸亚铁;(4)分解;(5)TiO2+2C+2Cl2
高温
.
TiCl4+2CO;(6)产生三废;(7)漏斗、烧杯、玻璃棒.点评:
本题考点: 物质的相互转化和制备;过滤的原理、方法及其应用;绿色化学;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答本题关键是要熟悉加快反应速度的方法,方程式的书写方法,分解反应的特点,知道过滤操作用到的仪器,尤其是主要的玻璃仪器.1年前查看全部
- (2012•河西区一模)月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为( )
(2012•河西区一模)月球表面富含钛铁矿,其主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为( )
A.+1
B.+2
C.+3
D.+4 疯叻1年前1
疯叻1年前1 -
 381986665 共回答了16个问题
381986665 共回答了16个问题 |采纳率93.8%解题思路:根据在化合物中正负化合价代数和为零,进行解答.根据在化合物中正负化合价代数和为零,可得钛酸亚铁(FeTiO3)中钛元素的化合价为:
(+2)+x+(-2)×3=0,x=+4;故选D.点评:
本题考点: 化学式的书写及意义;常见元素与常见原子团的化合价;化合价规律和原则.
考点点评: 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.1年前查看全部
- (2008•大庆)月岩中钛铁矿主要成分的化学式为FeTiO3,其中铁元素的化合价为+3,钛元素化合价为( )
(2008•大庆)月岩中钛铁矿主要成分的化学式为FeTiO3,其中铁元素的化合价为+3,钛元素化合价为( )
A.+1
B.+2
C.+3
D.+4 云雨er1年前1
云雨er1年前1 -
 rinchen 共回答了23个问题
rinchen 共回答了23个问题 |采纳率95.7%解题思路:根据主要成分的化学式为FeTiO3,及铁元素的化合价为+3,利用化合物中元素的正负化合价代数和等于0来解答.在FeTiO3中,铁元素的化合价为+3,氧元素的化合价为-2,
设Ti的化合价为x,
由化学式为FeTiO3,并根据化合物中元素的正负化合价代数和等于0,则
(+3)+x+(-2)×3=0
解得x=+3
故选:C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查根据化学式确定元素的化合价,学生应利用好习题中的化学式及铁元素的化合价,注重与课本知识的结合来解决信息中的同类问题.1年前查看全部
- (2011•福建)四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制
(2011•福建)四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
加入铁屑的作用是______.
(2)在②→③工艺中需要控制条件以形成TiO2•nH2O溶胶,该分散质颗粒直径大小在______范围.
(3)若把③中制得的固体TiO2•nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉.已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+⇌Fe3++H2O的平衡常数K=______.
(4)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ•mol-1;2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:______.
(5)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流程中存在的不足之处是______(只要求写出一项).
(6)依据如表信息,要精制含少量SiCl4杂质的TiCl4,可采用______方法.
TiCl4 SiCl4 熔点/℃ -25.0 -68.8 沸点/℃ 136.4 57.6  两个小肥肥1年前1
两个小肥肥1年前1 -
 fatexuanwu 共回答了9个问题
fatexuanwu 共回答了9个问题 |采纳率88.9%解题思路:(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm);
(3)依据平衡常数的概念结合反应写出计算式计算平衡浓度得到;
(4)依据热化学方程式和盖斯定律计算分析得到;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,通常采取蒸馏方法分离.(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+,加入铁屑作还原剂,将Fe3+还原为Fe2+,防止Ti3+被Fe3+氧化成TiO2+,
故答案为:防止Ti3+被Fe3+氧化成TiO2+;
(2)控制条件以形成TiO2•n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm),
故答案为:10-9~10-7m(或1nm-100nm);
(3)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=2.79×10-39,反应Fe (OH)3+3H+⇌Fe3++H2O的平衡常数K=
c(Fe3+)
c3(H+)=
c(Fe3+)
(
10−14
c(OH−))3=c(Fe3+)×c3(OH-)×1042=2.79×10-39×1042=2.79×103.
故答案为:2.79×103;
(4)①TiO2 (s)+2Cl2 (g)═TiCl4(l)+O2(g)△H=+140KJ•mol-1
②2C(s)+O2(g)═2CO(g)△H=-221KJ•mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ•mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ•mol-1
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,要精制含少量SiCl4杂质的TiCl4,可采用蒸馏(或分馏)方法,
故答案为:蒸馏(或分馏);点评:
本题考点: 制备实验方案的设计;热化学方程式;化学平衡常数的含义;难溶电解质的溶解平衡及沉淀转化的本质;常见金属元素的单质及其化合物的综合应用;物质的分离、提纯和除杂.
考点点评: 本题考查学生阅读题目获取信息能力、氧化还原反应、绿色化学、胶体、物质分离提纯,平衡常数计算,溶度积常数的计算应用,盖斯定律的计算应用等,难度不大,注意基础知识的掌握利用.1年前查看全部
- 3.钛酸亚铁(FeTiO3)可用来冶炼金属钛(未来将替代钢铁),其中钛元素的化合价是
3.钛酸亚铁(FeTiO3)可用来冶炼金属钛(未来将替代钢铁),其中钛元素的化合价是
是+4,为什么啊 yuyan1101年前1
yuyan1101年前1 -
 潜艇潜啊 共回答了16个问题
潜艇潜啊 共回答了16个问题 |采纳率87.5%既然是亚铁那么一定是二价的,而氧元素一般都是负二价,所以ti一定是正四价的...1年前查看全部
- 钛和钛合金,在许多领域被广泛的应用,被称为21世纪的金属.钛铁矿的主要成分为FeTiO3,已知其中Fe元素为+2价,O元
钛和钛合金,在许多领域被广泛的应用,被称为21世纪的金属.钛铁矿的主要成分为FeTiO3,已知其中Fe元素为+2价,O元素为-2价,那么FeTiO3中钛(Ti)元素的化合价为( )
A.+4
B.+3
C.+2
D.+1 xuediffu1年前1
xuediffu1年前1 -
 ss_2008 共回答了11个问题
ss_2008 共回答了11个问题 |采纳率90.9%解题思路:根据在化合物中正负化合价代数和为零,进行解答本题.根据在化合物中正负化合价代数和为零,已知Fe元素为+2价,O元素为-2价,则FeTiO3中钛(Ti)元素的化合价为:(+2)+x+(-2)×3=0,解答 x=+4;
故选A.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题考查学生根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.1年前查看全部
- 月球表面富含钛铁矿,钛铁矿的主要成分是钛酸亚铁(FeTiO3),其中钛元素的化合价为多少
 啊飞啊1年前3
啊飞啊1年前3 -
 系統默認 共回答了9个问题
系統默認 共回答了9个问题 |采纳率88.9%铁以亚铁形式存在,化合价为+2,氧的化合价是-2,三个氧就是-6,根据化合价守恒,钛的化合价是+41年前查看全部
大家在问
- 1“买书······”省略号的作用
- 2我妈妈每无花费1小时做运动.用英语怎么说
- 3甲,乙两支排球队进行比赛,约定先胜3局者获胜,然后比赛结束.第五局甲胜的概率为1/2,其余每局为2/3.假设每局相互独立
- 4用 know,tell ,speak ,give ,be like ,help 的适当形式完成
- 5有人认为三峡壮美,也有人说三峡秀美
- 6如果不等式组x>a+2,x2-a,x
- 7“态度决定高度.”怎么理解
- 8You must get enough sleep so that you can have a good rest.(
- 9昼夜的变化对我们生活的影响
- 10a person you admier 英语作文
- 11(2008•惠州一模)2008年北京奥运会吉祥物是由鱼、大熊猫、奥林匹克圣火、藏羚羊以及燕子组成的五人“福娃”.其中的藏
- 12如图,AC是四边形ABCD的一条对角线,角BAD=30度,角BCD=60度,BC=CD
- 13X+X/13=2分之1 这个方程咋解
- 14希望之星英语七年级一分钟自我介绍,结尾如(我很想和你们成为朋友,你们呢?)
- 15会碰到...用英语怎么说
