硝酸铈铵如何鉴别?在实验室里如何鉴别?
 2nnyy2022-10-04 11:39:541条回答
2nnyy2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 csjxx 共回答了22个问题
csjxx 共回答了22个问题 |采纳率86.4%- 物理方法就可以吧 :
1.外观判断:
硝酸铈铵是桔红色单斜晶系细小结晶,在空气中易潮解;
2.溶解性:
硝酸铈铵易溶于水、乙醇,不溶于浓硝酸,在浓硝酸中不会溶解的物质应该不多吧. - 1年前
相关推荐
- (2014•广州一模)硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如图1:
(2014•广州一模)硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如图1:

(1)已知(NH4)2Ce(NO3)6受热易分解,某科研小组认为反应原理如下,请补充完整:
(NH4)2Ce(NO3)6
CeO2•8OH+8______↑;CeO2•8OH△ .
CeO2+4H2O↑+2O2↑.△ .
在空气中加热(NH4)2Ce(NO3)6,除固体颜色有变化外,还可观察到的现象是______.
(2)步骤Ⅰ中,将Ce(NO3)3•6H2O配成溶液,保持pH到4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀.该过程中参加反应的氧化剂与还原剂物质的量之比为______.
(3)298K时,Ksp[Ce(OH)4]=1×10-29.Ce(OH)4的溶度积表达式为Ksp=______.为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10-5mol•L-1,需调节pH为______以上.
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如图2.从图2中可得出三条主要规律:
①(NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
②______;
③______. 麦天儿1年前1
麦天儿1年前1 -
 ANGELI123 共回答了22个问题
ANGELI123 共回答了22个问题 |采纳率95.5%解题思路:(1)根据质量守恒可确定未知物分子式应为NO,NO不稳定,易被氧化生成红棕色的NO2;
(2)Ge元素化合价由+3价升高到+4价,被氧化,Ce(NO3)3•6H2O为还原剂,H2O2为氧化剂,O元素化合价由-1价降低到-2价,以此可确定氧化剂和还原剂的物质的量之比;
(3)根据溶度积定义书写表达式,结合溶度积计算离子浓度;
(4)根据曲线的变化趋势判断温度、浓度对溶解度的影响.(1)由质量守恒定律可知反应的方程式应为(NH4)2Ce(NO3)6
△
.
CeO2•8OH+8NO↑,生成的另一种物质为NO,NO不稳定,易被氧化生成红棕色的NO2,
故答案为:NO;产生红棕色气体;
(2)Ge元素化合价由+3价升高到+4价,被氧化,Ce(NO3)3•6H2O为还原剂,H2O2为氧化剂,O元素化合价由-1价降低到-2价,由化合价升降总数相等可知氧化剂和还原剂的物质的量之比应为1:2,
故答案为:1:2;
(3)溶度积为溶液离子浓度的幂次方的乘积,Ce(OH)4的溶度积表达式为c(Ce4+)•[c(OH-)]4,残留在溶液中的c(Ce4+)小于1×10-5mol•L-1,
则c(OH-)>[Ksp
c(Ce4+)=
4
1×10−29
1×10−5/]mol/L=1×10-6mol/L,则pH=8,
故答案为:c(Ce4+)•[c(OH-)]4;8;
(4)由曲线的变化趋势可得出规律有:
①(NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
②其它条件相同时,S随c(HNO3)减小而增大;
③c(HNO3)越小,温度对S的影响越大或c(HNO3)越大,温度对S的影响越小.
故答案为:②其它条件相同时,S随c(HNO3)减小而增大;③c(HNO3)越小,温度对S的影响越大或c(HNO3)越大,温度对S的影响越小.点评:
本题考点: 制备实验方案的设计;氧化还原反应的计算;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查物质的制备方案的设计,为高考常见题型和高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,注意从守恒的角度解答相关计算,把握难溶电解质的溶解特点,难度中等.1年前查看全部
- 硝酸和硝酸铈铵的混合液硝酸和硝酸铈铵的混合液,怎么检验出各自的含量.硝酸铈铵分子式是Ce(NH4)2(NO3)6.Ce是
硝酸和硝酸铈铵的混合液
硝酸和硝酸铈铵的混合液,怎么检验出各自的含量.硝酸铈铵分子式是Ce(NH4)2(NO3)6.Ce是正四价,有橙黄色.它和正二价的铁反应生成正三价的铁和正三价的铈. 盗帅马超1年前1
盗帅马超1年前1 -
 马立当栋 共回答了16个问题
马立当栋 共回答了16个问题 |采纳率100%氢氧化铈如果是沉淀就好办了``不是也可以
先加氢氧化钠,加热,让氨气出来,并滴定.
剩余溶液先加二价铁,反应完全分离出铁元素(沉淀)
溶解后加碘化钾,最后用硫代硫酸钠滴定碘...
计算相当麻烦``1年前查看全部
- 我想知道用硝酸铈铵刻蚀铬膜时发生了怎样的化学反应,刻蚀速度是否和硝酸铈铵的浓度成正比
我想知道用硝酸铈铵刻蚀铬膜时发生了怎样的化学反应,刻蚀速度是否和硝酸铈铵的浓度成正比
我猜想是Ce(4+)+Cr==>Ce(3+)+Cr(3+),那么铬离子有没有和硝酸铈铵中的铵根形成络和物?随着反应的进行,Ce(4+)在慢慢消耗,浓度降低,使反应速度变慢.Ce(3+)和Cr(3+)浓度越来越高,这是否也是使反应速度降低的一个原因. qq9879879871年前1
qq9879879871年前1 -
 aarr户 共回答了16个问题
aarr户 共回答了16个问题 |采纳率100%Ce(IV)酸性条件下的氧化性很强,Ce(IV)/Ce(III)的标准电极电势在1.61V左右,足以把Cr(III)氧化成Cr(VI)(1.23V),所以虽然反应会比较慢,但是不易停留在Cr(3+)阶段.
铵根一般不和阳离子形成络和物,因为它没有孤对电子,不是一个路易斯碱,况且铵根和铬离子同样带正电荷,很难结合的.
根据动力学原理,Ce(3+)和Cr(3+)浓度越来越高只会导致平衡的移动,速度的降低主要还是由反应物浓度的降低引起的.1年前查看全部
- 硝酸铈铵[(NH 4 ) 2 Ce(NO 3 ) 6 ]广泛应用于电子、催化工业,其合成路线如下:
硝酸铈铵[(NH 4 ) 2 Ce(NO 3 ) 6 ]广泛应用于电子、催化工业,其合成路线如下:

(1)已知(NH 4 ) 2 Ce(NO 3 ) 6 受热易分解,某科研小组认为反应原理如下,请补充完整:(NH 4 ) 2 Ce(NO 3 ) 6 CeO 2 ·8OH + 8_____↑;CeO 2 ·8OH
CeO 2 ·8OH + 8_____↑;CeO 2 ·8OH CeO 2 + 4H 2 O↑+2O 2 ↑。
CeO 2 + 4H 2 O↑+2O 2 ↑。
在空气中加热(NH 4 ) 2 Ce(NO 3 ) 6 ,除固体颜色有变化外,还可观察到的现象是_________。
(2)步骤Ⅰ中,将Ce(NO 3 ) 3 ·6H 2 O配成溶液,保持pH到4~5,缓慢加入H 2 O 2 溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH) 4 沉淀。该过程中参加反应的氧化剂与还原剂物质的量之比为___________。
(3)298K时,K sp [Ce(OH) 4 ]=1×10 —29 。Ce(OH) 4 的溶度积表达式为K sp =___________。
为了使溶液中Ce 4 + 沉淀完全,即残留在溶液中的c(Ce 4+ )小于1×10 —5 mol·L -1 ,需调节pH为______以上。
(4)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH 4 ) 2 Ce(NO 3 ) 6 在不同温度、不同浓度硝酸中的溶解度,结果如图。从图中可得出三条主要规律: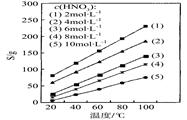
① (NH 4 ) 2 Ce(NO 3 ) 6 在硝酸中的溶解度随温度升高而增大;
② _____________________________________________;
③ _____________________________________________。 lujx5211年前1
lujx5211年前1 -
 清皊 共回答了23个问题
清皊 共回答了23个问题 |采纳率95.7%(1)NO ;产生红棕色气体 (4分,每空2分)
(2)1:2 (3分)
(3)c(Ce 4+ )•[c(OH — )] 4 (3分) ;8 (2分)
(4)②其它条件相同时,S随c(HNO 3 )减小而增大 (2分)
③c(HNO 3 )越小,温度对S的影响越大或c(HNO 3 )越大,温度对S的影响越小 (2分)
1年前查看全部
- 硝酸铈铵在实验室里如何鉴别?
 ljp20034030251年前1
ljp20034030251年前1 -
 527417190 共回答了15个问题
527417190 共回答了15个问题 |采纳率80%主要成分:含量:分析纯≥99%、化学纯≥97%.
外观与性状:桔红色单斜晶系细小结晶,在空气中易潮解.
溶解性:易溶于水、乙醇,不溶于浓硝酸.
主要用途:用作烯烃聚合催化剂和分析试剂.
直接观察外观即可鉴别1年前查看全部
- (2012•珠海)稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域,硝酸铈铵[(NH4)2Ce(NO3
(2012•珠海)稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域,硝酸铈铵[(NH4)2Ce(NO3)6]是稀土元素铈(Ce)的化合物,其中铈元素的化合价是( )
A.+2
B.+3
C.+4
D.+5 sarah02211年前1
sarah02211年前1 -
 牟牟林 共回答了21个问题
牟牟林 共回答了21个问题 |采纳率95.2%解题思路:根据在化合物中正负化合价代数和为零,结合硝酸铈铵[(NH4)2Ce(NO3)6]的化学式进行解答本题.铵根显+1,硝酸根显-1,设铈元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-1)×6=0,则x=+4.
故选:C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.1年前查看全部
- 稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域,硝酸铈铵[(NH4)2Ce(NO3)6]是稀土元素铈
稀土元素又称“21世纪黄金”,广泛应用于电子、军事、石油化工等领域,硝酸铈铵[(NH4)2Ce(NO3)6]是稀土元素铈(Ce)的化合物,其中铈元素的化合价是( )
A. +2
B. +3
C. +4
D. +5 ranxiao1年前1
ranxiao1年前1 -
 as幻觉 共回答了15个问题
as幻觉 共回答了15个问题 |采纳率93.3%解题思路:根据在化合物中正负化合价代数和为零,结合硝酸铈铵[(NH4)2Ce(NO3)6]的化学式进行解答本题.铵根显+1,硝酸根显-1,设铈元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-1)×6=0,则x=+4.
故选:C.点评:
本题考点: 有关元素化合价的计算.
考点点评: 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.1年前查看全部
大家在问
- 1MALI KUILISIMASI是什么意思啊?
- 2不及物动词和及物动词 哪个需要加介词?在前面加还是后面加?
- 3一道初一的单选题Would you please __________ some water.A.bring us B.
- 4下表记录了一次试验中时间和温度的数据 时间/min: 0 5 10 15 20 25 温度/℃: 10 25 40 55
- 5一个圆锥形小麦堆,量得底面直径是4米,高比直径少4分之1.每立方米小麦重约600千克,这堆小麦约重多少千克
- 6you are allowed thirty minutes to write an E-mail to contact
- 7随着互联网的日益盛行,网上商店遍地开花,网上购物正在悄悄地改变着人们的生活方式。对于网上购物的认识正确的是
- 8在日常生活中经常发生下列变化,其中属于化学变化的是 [ ] A.木材燃烧
- 9请说明无论x.y取和值,代数式5x^2+2y^2-4xy-2x-4y+6的值总是正数
- 10求这两道题的过程和结果
- 11荷塘一角(转载) 作文
- 12如何做好差生转化工作,提高数学教学质量
- 13(2011•南通)下表为“探究种子萌发的外界条件”的实验设计,请根据表中提供的信息,回答下列问题.
- 14英语作文写一篇 120个以上单词的作文 要求是:不同文化有不同的肢体语言,谈谈我们如何在日常生活中有效的使用肢体语言和不
- 15焓变的公式是?焓变的公式:反应物的总能量—生成物的总能量=ΔH 还是生成物的总能量-反应物的总能量=ΔH
