KI淀粉溶液,KI溶液,淀粉溶液有什么区别?都能检验Cl2,
 qdjiawei2022-10-04 11:39:541条回答
qdjiawei2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 rechar 共回答了20个问题
rechar 共回答了20个问题 |采纳率90%- 只有淀粉碘化钾溶液可以.
肯定有区别,碘化钾溶液没有淀粉.淀粉溶液中没有碘化钾.
检验Cl2或者Br2的原理是:Cl2或者Br2能够氧化碘离子,生成I2,I2又能够使淀粉溶液变蓝.Cl2或Br2不能使淀粉变蓝.
使用淀粉碘化钾溶液,如果变蓝则说明I2被氧化了. - 1年前
相关推荐
- 加碘食用盐的检验怎么用盐酸酸化的KI淀粉检验
 灯海1年前3
灯海1年前3 -
 春熙刀客 共回答了10个问题
春熙刀客 共回答了10个问题 |采纳率100%因为反应是
6HCl+5KI+KIO3====3I2+6KCl+3H2O1年前查看全部
- (5分)用下图所示的装置进行电解。通电一会儿,发现湿润的KI淀粉试纸的C端变为蓝色。则:
(5分)用下图所示的装置进行电解。通电一会儿,发现湿润的ki淀粉试纸的c端变为蓝色。则:
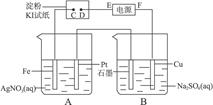
(1)a中发生反应的化学方程式为_________________________________。
(2)在b中观察到的现象是__________________________、______________________、______________________。
(3)室温下,若从电解开始到时间t s时,a、b装置***收集到标准状况下的气体0.168 l,若电解过程中无其他副反应发生,经测定电解后a中溶液体积恰为1000 ml,则a溶液的ph为______________________。 zgbb1年前1
zgbb1年前1 -
 笑天犬骂人44 共回答了24个问题
笑天犬骂人44 共回答了24个问题 |采纳率83.3%1年前查看全部
- 已知氧化性强弱顺序是Bro3->Clo3->Cl2>IO3->I2.现将饱和氯水逐渐滴入KI淀粉溶液中
已知氧化性强弱顺序是Bro3->Clo3->Cl2>IO3->I2.现将饱和氯水逐渐滴入KI淀粉溶液中
2方程式 我刚预习到这,请求帮忙把理由写全、、、、、谢谢 pangpang11年前3
pangpang11年前3 -
 wyyxhpm 共回答了15个问题
wyyxhpm 共回答了15个问题 |采纳率100%①不过量时:
溶液先变蓝,氯将碘离子氧化成单质碘,淀粉遇碘变蓝
其反应是:
KI+Cl2==I2+KCl
②加氯水至过量时
蓝色褪成无色
5Cl2+I2+6H2O==2HIO3-+10HCl
理由么:第一步书上都有的吧
第二步的原因就是强氧化剂+强还原剂=弱还原剂+弱氧化剂
里面Cl2是强氧化剂,I2强还原剂,CI-是还原产物,IO3-是氧化产物
因为CL2的氧化性大于IO3-,这反应才得以进行1年前查看全部
- 酸性KI淀粉溶液久置后变蓝是发生了 .酸性KI淀粉溶液久置后变蓝是发生了4I-+O2+4H+=2I2+2H2O为什么不是
酸性KI淀粉溶液久置后变蓝是发生了 .酸性KI淀粉溶液久置后变蓝是发生了4I-+O2+4H+=2I2+2H2O为什么不是 4I-+O2+2H2O=2I2+4OH-
 MAVIS02021年前1
MAVIS02021年前1 -
 紫蔓清葭 共回答了16个问题
紫蔓清葭 共回答了16个问题 |采纳率100%酸性的溶液里不能有氢氧根的,1年前查看全部
- 在KI淀粉溶液中通入氯气,溶液变-------------,原因是----------------------
 多孜多彩1年前1
多孜多彩1年前1 -
 Jeany_oy 共回答了16个问题
Jeany_oy 共回答了16个问题 |采纳率93.8%蓝色 因为氯气具有强氧化性 能把I-氧化成I2 淀粉遇到I2就显蓝色了
方程式Cl2+2KI=2KCl+I21年前查看全部
- 淀粉溶液,KI淀粉溶液是什么哦
 顺航吉祥物1年前3
顺航吉祥物1年前3 -
 反目成Q离 共回答了19个问题
反目成Q离 共回答了19个问题 |采纳率100%淀粉溶液是可溶性淀粉溶于水所得的溶液
淀粉KI溶液是淀粉溶液与KI溶液的混合液
淀粉溶液用来检验碘单质(变蓝)
淀粉KI溶液用来检验Cl2Br2等氧化性物质(变蓝)1年前查看全部
- 往KBr溶液中加入氯水,振荡,加入CCl,现象怎样?往KI淀粉溶液中加入氯水或溴水,现象怎样?
往KBr溶液中加入氯水,振荡,加入CCl,现象怎样?往KI淀粉溶液中加入氯水或溴水,现象怎样?
请说明原因
2、KI淀粉溶液中,生成了碘单质不会变蓝吗? sunyi12021年前1
sunyi12021年前1 -
 只用身体爱你 共回答了19个问题
只用身体爱你 共回答了19个问题 |采纳率100%1、生成溴单质、氯化钾.加入四氯化碳后,上层为橙黄色(溴的四氯化碳溶液),下层为淡黄色(溶解了少量的溴和氯化钾的水溶液)
2、溶液变成棕色了(生成了棕色的碘单质)1年前查看全部
- 如何检验碘酸根利用KI淀粉试纸及厨房日常用品可以检验食盐中是否含有碘酸根,请用化学方程式说明反应原理.
 yyyy老大1年前1
yyyy老大1年前1 -
 summercheng 共回答了22个问题
summercheng 共回答了22个问题 |采纳率90.9%原理应该是这样的:
KIO3 + 5KI +6CH3COOH = 3I2 +3H2O +6CH3COOK
实际上是利用厨房里的食醋(乙酸),这是题目的要求中提到的,发生归中反应,得到碘单质后再用淀粉,看到蓝色.1年前查看全部
- Cl2为什么不能漂白KI淀粉溶液?
Cl2为什么不能漂白KI淀粉溶液?
Cl2可使溶液变蓝,接着为什么不能漂白? tony7501年前1
tony7501年前1 -
 mudan0101 共回答了15个问题
mudan0101 共回答了15个问题 |采纳率80%Cl2可以与KI反应生成I2(碘单质),而I2(碘单质)可以使淀粉溶液变蓝
Cl2的漂白作用主要是靠它的氧化性,而Cl2已不能再氧化I2(碘单质)和淀粉了,
故,溶液不可能再次变澄清1年前查看全部
- 酸性ki淀粉溶液久置后变蓝方程式
 starhishwz1年前3
starhishwz1年前3 -
 吻虫旋踢 共回答了12个问题
吻虫旋踢 共回答了12个问题 |采纳率83.3%被空气中的O2氧化了
方程式
4 KI + O2+2H2SO4 = 2 K2SO4 + 2 H2O + 2 I2
4 I- + O2 + 4 H+ = 2 H2O + 2 I21年前查看全部
- 进行化学实验,观测实验现象,通过分析推理得出正确的结论是学习化学的方法之一。对下列实验事实的解释正确的是 A.在KI淀粉
进行化学实验,观测实验现象,通过分析推理得出正确的结论是学习化学的方法之一。对下列实验事实的解释正确的是
A.在KI淀粉溶液中通入Cl 2 ,溶液变蓝,说明氯气能与淀粉发生显色反应 B.浓硝酸在光照条件下变黄,说明浓硝酸不稳定,有有色产物生成且能溶于浓硝酸 C.在某溶液中加入HNO 3 酸化的BaCl 2 溶液有白色沉淀产生,说明溶液中含有SO 4 2- D.将铜片放入浓硫酸中无明显实验现象,说明铜在冷的浓硫酸中发生钝化  gggg1年前1
gggg1年前1 -
 夏森 共回答了20个问题
夏森 共回答了20个问题 |采纳率100%B
A 错误,Cl 2 +2KI=2KCl+I 2 碘遇淀粉发生显色反应。
B 正确,在光照下,4HNO 3 =4NO 2 +O 2 +2H 2 O NO 2 为红棕色,溶于浓硝酸显黄色
C 错误,溶液中可能含有SO 4 2 - 、也可能含有SO 3 2 -
D 错误,铜在冷的浓硫酸中并没有生成致密的氧化膜,没有发生钝化,在加热时才反应。1年前查看全部
- ki淀粉溶液是什么颜色的?KI溶液呢?
 lclclc002051年前1
lclclc002051年前1 -
 五只洋 共回答了20个问题
五只洋 共回答了20个问题 |采纳率90%乳白色
KI溶液无色1年前查看全部
- 臭氧可使湿润的KI淀粉试纸变蓝 进行用CO还原CuO的实验时,尾气可用点燃的方法除去(判断题)
 wanglm1961年前1
wanglm1961年前1 -
 yiyiyaa 共回答了16个问题
yiyiyaa 共回答了16个问题 |采纳率100%原理为强氧化剂臭氧( O 3 )与碘化钾( KI )水溶液反应生成游离碘( I 2 ).臭氧还原为氧气.反应式为:
O 3 + 2KI + H 2 O → O 2 + I 2 + 2KOH
游离碘显色,依在水中浓度由低至高呈浅黄至深红色.
一题正确1年前查看全部
- KI淀粉试纸为什么不能检验Br2?
KI淀粉试纸为什么不能检验Br2?
看到这题挺奇怪的,KI淀粉试纸为什么不能检验Br2的存在 youyou200620061年前1
youyou200620061年前1 -
 夜之冥 共回答了18个问题
夜之冥 共回答了18个问题 |采纳率66.7%根据元素的活泼性
Br2能把I置换出来
但是Br2有颜色 不能证明是I2出来了 使试纸变色1年前查看全部
- KI淀粉溶液是什么 求大神解释
 judysworld1年前2
judysworld1年前2 -
 南海发展323 共回答了29个问题
南海发展323 共回答了29个问题 |采纳率89.7%淀粉溶液是可溶性淀粉溶于水所得的溶液 淀粉KI溶液是淀粉溶液与KI溶液的混合液 淀粉溶液用来检验碘单质(变蓝) 淀粉KI溶液用来检验Cl2Br2等氧化性物质(变蓝)1年前查看全部
- 通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实解释正确的是( ) A.现象:KI淀粉
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一.对下列实验事实解释正确的是( ) A.现象:KI淀粉溶液中通入Cl 2 ,溶液变蓝;解释:Cl 2 能与淀粉发生显色反应 B.现象:浓HNO 3 在光照条件下变黄;解释:浓HNO 3 不稳定,生成有色产物能溶于浓硝酸 C.现象:某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成;解释:说明该溶液中含有SO 4 2- D.现象:向盐酸中加入浓硫酸时产生白雾;解释:说明浓硫酸具有脱水性  音乐and咖啡1年前1
音乐and咖啡1年前1 -
 dfh3ngi 共回答了15个问题
dfh3ngi 共回答了15个问题 |采纳率93.3%A.KI淀粉溶液中通入Cl 2 ,生成I 2 ,淀粉遇I 2 变蓝色,氯气和淀粉不反应,故A错误;
B.硝酸在光照条件下分解生成NO 2 ,NO 2 溶于水而导致溶液变黄,故B正确;
C.SO 3 2- 可被硝酸氧化为SO 4 2- ,不能判断一定含有SO 4 2- ,故C错误;
D.向盐酸中加入浓硫酸时产生白雾.是盐酸加入浓硫酸时,溶解温度升高,使氯化氢挥发出来,遇到水蒸气产生白雾,不是浓硫酸的脱水性,故D错误;
故选B.1年前查看全部
- 1820年德贝莱纳用MnO2催化KClO3分解制氧,发现制得氧气有异常的气味,使该气体通过KI淀粉溶液,溶液变蓝.则该氧
1820年德贝莱纳用MnO2催化KClO3分解制氧,发现制得氧气有异常的气味,使该气体通过KI淀粉溶液,溶液变蓝.则该氧气中可能混有( )
A. Cl2
B. Br2
C. HCl
D. CO2 suliaow1年前1
suliaow1年前1 -
 changgong2910 共回答了21个问题
changgong2910 共回答了21个问题 |采纳率90.5%解题思路:该气体能使淀粉碘化钾溶液变蓝,即能氧化I-成I2或该气体中就有I2存在,但根据化学反应的特点,不可能有新的元素产生;本题中的KClO3在MnO2的催化作用下分解反应的副反应不熟悉,故此题可用淘汰法进行筛选,选出正确答案.使KI淀粉溶液变蓝的实质是强氧化剂氧化KI为I2,I2单质能使淀粉显蓝色,因此除卤素中F2、Cl2、Br2之外,具有强氧化性的O3、HNO3、KMnO4、Fe3+等都能使KI淀粉溶液变蓝色.
A、氯气有刺激性气味,通过KI淀粉溶液能氧化碘离子为单质碘,遇到淀粉变蓝,故A正确;
B、反应物里没有溴元素,故不可能生成,故B错误;
C、氯化氢虽有刺激性气味,但反应物里没H元素,故C错误;
D、二氧化碳没有气味,CO2不能使KI淀粉溶液变蓝,故D错误;
故选A.点评:
本题考点: 氯气的实验室制法;氯气的化学性质.
考点点评: 本题考查了氯气的性质应用,解题的关键是“气体能使KI淀粉溶液变蓝”.1年前查看全部
- 淀粉试纸遇酸显什么色NO2是一种易于水与水反应的气体,能使湿润的KI淀粉试纸变___
 独孤ye1年前1
独孤ye1年前1 -
 nancyu 共回答了14个问题
nancyu 共回答了14个问题 |采纳率92.9%变蓝,3NO2+H2O=2HNO3+NO↑
HNO3有强氧化性.把I-氧化成I21年前查看全部
- 二氧化锰氯酸钾制氧气异常气体二氧化锰氯酸钾制氧气,发现制得氧气有异常气味,使气体通过KI淀粉溶液,溶液变蓝,则氧气中可能
二氧化锰氯酸钾制氧气异常气体
二氧化锰氯酸钾制氧气,发现制得氧气有异常气味,使气体通过KI淀粉溶液,溶液变蓝,则氧气中可能混有?
答案是Cl2,
那么为什么气体通过KI淀粉溶液,溶液变蓝 lxj2431年前1
lxj2431年前1 -
 大速度ss 共回答了15个问题
大速度ss 共回答了15个问题 |采纳率86.7%这是连续反应.
二氧化锰先和氯酸钾反应生成高锰酸钾和氯气和氧气,
2MnO2+2KClO3=2KMnO4+Cl2+O2
高锰酸钾再分解生成锰酸钾、二氧化锰和氧气,
2KMnO4=K2MnO4+MnO2+O2
锰酸钾再和氯气反应生成氯化钾、二氧化锰和氧气.
K2MnO4+Cl2=2KCl+MnO2+O2
三个加起来就是
2KClO3=2KCl+3O2(MnO2催化)1年前查看全部
- 溴水能使湿润的KI淀粉试纸变蓝,为什么?
 bh小米粥1年前3
bh小米粥1年前3 -
 xzyva 共回答了25个问题
xzyva 共回答了25个问题 |采纳率88%Br2 + 2KI == 2KBr + I2
❤您的问题已经被解答~~(>^ω^1年前查看全部
- 1.下列物质中,不能使湿润的KI淀粉试纸变蓝的是?
1.下列物质中,不能使湿润的KI淀粉试纸变蓝的是?
A碘水 B嗅水 C氯水 D碘化钾溶液
2.在NAOH溶液中通入少量的CO2,和在NAOH溶液通入过量CO2时所发生的反应生成物不一样,现在用1L 1.0MOL/L NAOH溶液吸收0.8MOL CO2,所得溶液中NA2CO3和NAHCO3的物质的量之比是多少?
3.食盐中必须加碘,其中碘以KIO3形式存在,已知KIO3和KI在酸性条件下会生成碘单质.因此可用试纸和一些生活中的常见物质进行实验,证明食盐中存在IO~3,可供选择的物质有1.自来水,2.蓝色石蕊试剂 3KI淀粉试纸,4淀粉 5食糖 6食醋 7白酒.进行实验时必须使用的是( )
A13 B36 C245 D12456 fumei200458481年前1
fumei200458481年前1 -
 seman888 共回答了15个问题
seman888 共回答了15个问题 |采纳率93.3%1 D
若能使湿润的KI淀粉试纸变蓝,说明有碘分子
A显然有碘分子
你若学过卤素,就知道氯气有强氧化性,可将KI中的I氧化成I2
而溴也是卤素,化学性质和氯类似
所以B和C也对
所以选D
2 1:3
用碳和钠的守恒做
设NA2CO3有xmol,NAHCO3有ymol
2x+y=1
x+y=0.8
解得x=0.2y=0.6
物质的量之比为1:3
3 B
显然要KI,就要有3
要有酸性条件,还应有醋酸,即食醋
所以是3,61年前查看全部
- 高一化学题能使湿润的KI淀粉试纸变蓝的最正确组合是()1、溴水 2、氯水 3、碘酒 4、 氯化钾 5 高锰酸钾溶液(酸性
高一化学题
能使湿润的KI淀粉试纸变蓝的最正确组合是()
1、溴水 2、氯水 3、碘酒 4、 氯化钾 5 高锰酸钾溶液(酸性)
A 1 2 3 B 1 5
C 1 2 3 5 D 3 4 5
答案是什么?说明一下 lhh24201年前2
lhh24201年前2 -
 音乐的耳朵 共回答了13个问题
音乐的耳朵 共回答了13个问题 |采纳率92.3%C 1 2 3 5
1 2 5 都可以将I-氧化成I2,能使淀粉变蓝.
3 含有I2,能使淀粉变蓝.1年前查看全部
- 碘的添加剂是KIO3,可用盐酸酸化的KI淀粉混合液检验食盐是否加I2,其反应的离子方程式是什么
 Qd-shan1年前1
Qd-shan1年前1 -
 tequilagao 共回答了15个问题
tequilagao 共回答了15个问题 |采纳率93.3%KIO3 + 5KI + 6HCl = 6KCl + 3H2O + 3I2
这是一个氧化还原反应,碘化钾被氧化,碘酸钾被还原.盐酸提供稳定酸性环境.
碘与淀粉反应显蓝色1年前查看全部
- KIO3,盐酸酸化的KI淀粉混合液检验食盐是否加I2的离子方程式怎么写?
 罗嗦蛋1年前1
罗嗦蛋1年前1 -
 qinjingtai 共回答了14个问题
qinjingtai 共回答了14个问题 |采纳率92.9%KIO3 + 5KI + 6HCl = 6KCl + 3H2O + 3I2 这是一个氧化还原反应,碘化钾被氧化,碘酸钾被还原1年前查看全部
- 现将饱和氯水逐滴滴入KI淀粉溶液中至过量,可看到的现象化学方程式是什么,请解释一下反应原理,谢谢.
 邵敬伟1年前2
邵敬伟1年前2 -
 abgfc 共回答了20个问题
abgfc 共回答了20个问题 |采纳率90%先显蓝色后褪去
显蓝色是因为氯气将碘置换出来,碘遇淀粉变蓝
褪色是因为氯水中次氯酸的强氧化性1年前查看全部
- 下列实验过程中,始终无明显现象的是 A.O 2 通入酸化的KI淀粉溶液中 B.CO 2 通入CaCl 2 溶液中 C.0
下列实验过程中,始终无明显现象的是
A.O 2 通入酸化的KI淀粉溶液中 B.CO 2 通入CaCl 2 溶液中 C.0.1mol • L -1 稀 H 2 SO 4 滴入0.1 mol • L -1 Na 2 S 2 O 3 溶液中 D.SO 2 通入已酸化的Ba(NO 3 ) 2 溶液中  小笨小乖1年前1
小笨小乖1年前1 -
 695727696 共回答了25个问题
695727696 共回答了25个问题 |采纳率96%B
1年前查看全部
- 用二氧化锰作催化剂分解氯酸钾制的得氧气,往往具有特殊的异味,这种气体通过KI淀粉溶液时溶液变蓝
用二氧化锰作催化剂分解氯酸钾制的得氧气,往往具有特殊的异味,这种气体通过KI淀粉溶液时溶液变蓝
氧气中可能含有A.cl2 B.o3 C.Br2 D.F2 香橙小甜米1年前2
香橙小甜米1年前2 -
 limpbone 共回答了15个问题
limpbone 共回答了15个问题 |采纳率93.3%首先,题目中不存在b、c选项所说的元素.
然后,能使KI淀粉溶液变蓝,就意味着生成碘单质.也就是说,要产生具有氧化性的物质.选项a、b符合.
通常情况下,此反应方程式为KClO3——KCl+3/2 O2
但是,也存在5 KCl+KClO3——3 Cl2+3 K2O
Cl2+2 KI——2 KCl +I2 所以选项a正确
至于选项b,氯气在高温下(此反应需加热)会产生游离态Cl原子(最外层带7个电子).而此时的氯原子具有很强的氧化性.并作为催化剂产生并分解臭氧.所以存在此方程式:3/2 O2——O3(催化剂为氯原子)
H2O+O3+2 KI——I2+O2+2 KOH 所以选项b正确1年前查看全部
- 在饱和的NACL溶液中,滴入KI淀粉溶液和石蕊溶液,然后插入石墨电极进行电解,经一定时间后,两极附近溶液的颜色变为 阳极
在饱和的NACL溶液中,滴入KI淀粉溶液和石蕊溶液,然后插入石墨电极进行电解,经一定时间后,两极附近溶液的颜色变为 阳极变蓝 阴极变蓝 为什么?
 勾魂帮副帮主1年前4
勾魂帮副帮主1年前4 -
 yingzi1972 共回答了22个问题
yingzi1972 共回答了22个问题 |采纳率95.5%反应式为 2NaCl+2H2O=通电=2NaOH+H2+Cl2
Cl2是在阳极生成的,因为Cl-失电子 所以有Cl2+2KI=I2+2KCl
而在阴极则是生成H2和NaOH
因为NaOH是碱性的,所以加入石蕊是变蓝1年前查看全部
- 湿润的KI淀粉试纸接触某气体而显兰色,改气体可能是
湿润的KI淀粉试纸接触某气体而显兰色,改气体可能是
1,Cl2/2,NO2/3,SO2/4,Br2(g)/5,O2/6,HI
答案是1245
为什么SO2不可以? 卒就脯醢1年前1
卒就脯醢1年前1 -
 philipdan 共回答了18个问题
philipdan 共回答了18个问题 |采纳率88.9%SO2有漂白性 会在漂白1年前查看全部
- 实验室制氯气 二氧化锰和浓盐酸反应生成二氧化锰、氯气和水.这之后为什么要依次连接饱和食盐水、浓硫酸、湿润的KI淀粉试纸、
实验室制氯气
二氧化锰和浓盐酸反应生成二氧化锰、氯气和水.这之后为什么要依次连接饱和食盐水、浓硫酸、湿润的KI淀粉试纸、干色布、湿色布、石蕊、FeCl2,AgNo3、KI淀粉试纸、再最后用NaOH尾气处理啊?这每一步的作用都是什么啊?麻烦死掉了,制个氯气怎么要把生成的气体通过这么多装置?
每一步的现象是什么啊?
可不可以省略期中一些步骤? 邪王_石之轩1年前1
邪王_石之轩1年前1 -
 汐情 共回答了10个问题
汐情 共回答了10个问题 |采纳率100%饱和食盐水:除氯化氢气体
浓硫酸:除水
湿润的KI淀粉试纸:检验氧化性
干色布、湿色布,石蕊:漂白性
FeCl2:检验氧化性
AgNo3:检验氯负离子
KI淀粉试纸:检验氧化性
NaOH尾气处理:吸收多余的氯气1年前查看全部
- 湿润的KI淀粉试纸接触某气体而显蓝色,该气体可能是
湿润的KI淀粉试纸接触某气体而显蓝色,该气体可能是
a.Cl2
b.NO2
c.SO2
d.Br2 (g)
e.O3
f.HI
选哪些?为什么? zyhmft1年前1
zyhmft1年前1 -
 lqjdsg 共回答了19个问题
lqjdsg 共回答了19个问题 |采纳率78.9%a :kI与CL反应生成I2,变蓝.
b :NO2与KI反应生成I2,变蓝.
c :不反应,KI与SO2都是还原性物质.
d :KI与BR2反应生成I2,变蓝.(原理同a,BR的非金属性即氧化性比I强)
e :2KI+O3+H2O==2KOH+O2+I2 ,变蓝.
f :HI和KI不反应.(如同HCl和KCl不反应一样)
选择:a b d e1年前查看全部
- 高锰酸颊溶液能使湿润的KI淀粉试纸变蓝吗?
 幸福着快乐着1年前3
幸福着快乐着1年前3 -
 问题符号 共回答了12个问题
问题符号 共回答了12个问题 |采纳率100%因为高锰酸钾溶液氧化碘化钾产生游离碘(I2),碘跟淀粉之间形成络合物而产生蓝色.而单纯的高锰酸钾(KMnO4)不含碘,所以不会使淀粉变蓝.
所以,高锰酸钾溶液遇到淀粉碘化钾试纸可以变蓝.1年前查看全部
- 能使湿润的KI淀粉试纸变篮的是:溴水 氯气 碘酒 氯化钾 高锰酸钾
 传说5542131年前2
传说5542131年前2 -
 sha11 共回答了17个问题
sha11 共回答了17个问题 |采纳率94.1%溴水 氯气 高锰酸钾有氧化性,可以将碘离子氧化为碘单质,所以能使湿润的KI淀粉试纸变篮
碘酒含碘单质,也能使湿润的KI淀粉试纸变篮
氯化钾没有氧化性,也没有碘单质,所以不能使湿润的KI淀粉试纸变篮1年前查看全部
- 把溴水滴加到KI淀粉溶液中
 白了了1年前1
白了了1年前1 -
 ttion326 共回答了11个问题
ttion326 共回答了11个问题 |采纳率81.8%Br2+2KI=I2+2KBr
红棕色变紫黑色1年前查看全部
- KI溶液和KI淀粉溶液一样吗RT
 小王子疼玫瑰1年前4
小王子疼玫瑰1年前4 -
 hh2266018 共回答了15个问题
hh2266018 共回答了15个问题 |采纳率86.7%KI溶液就是碘化钾水溶液
淀粉KI溶液是淀粉溶液与KI溶液的混合液
淀粉KI溶液用来检验Cl2Br2等氧化性物质(变蓝)1年前查看全部
- NO2与湿润的ki淀粉试纸会怎样变化 是如何变化的
NO2与湿润的ki淀粉试纸会怎样变化 是如何变化的
NO2与湿润的ki淀粉试纸会怎样变化 volcanodc1年前1
volcanodc1年前1 -
 SMCC126 共回答了24个问题
SMCC126 共回答了24个问题 |采纳率87.5%纸变蓝,因为NO2将KI化合生成KNO3与I1年前查看全部
- 下列不能用湿润的KI淀粉试纸鉴别的是
下列不能用湿润的KI淀粉试纸鉴别的是
A溴水及碘水 B 溴水及KBr溶液 C 碘水及NaI溶液 D氯水及KCl溶液 xianzxh1年前2
xianzxh1年前2 -
 lpf58 共回答了18个问题
lpf58 共回答了18个问题 |采纳率77.8%A原因,此和前者可以生成单质典使变色,而后者本来就可以使变色,故不行1年前查看全部
- hcl和ki淀粉溶液反应吗
 弦动我心20081年前1
弦动我心20081年前1 -
 py6126 共回答了19个问题
py6126 共回答了19个问题 |采纳率89.5%不反应.
HCl是酸,KI 是盐,交换成分后没有气体、沉淀、弱电解质
不发生复分解反应1年前查看全部
- 淀粉溶液、KI淀粉溶液、KI溶液、溴水不必用其它试剂便可以鉴别出来吗?
 hglws1年前1
hglws1年前1 -
 菲儿2000 共回答了22个问题
菲儿2000 共回答了22个问题 |采纳率81.8%溴水是橙红色的,鉴别出溴水后,将溴水取样分别加入其他溶液中,溴会置换出KI中的碘,碘遇淀粉变蓝,即鉴别出KI淀粉溶液,那个KI溶液因为碘的原因显紫红色,淀粉溶液没反应,应该是这样1年前查看全部
- 高中阶段那些物质可用湿润KI淀粉试纸检验 还有其原理 请帮我归纳一下
 xiangxianni1年前1
xiangxianni1年前1 -
 beer010 共回答了23个问题
beer010 共回答了23个问题 |采纳率91.3%可检测强氧化性物质
高中阶段是检验氯气
方法:在试管口,放置湿润的淀粉碘化钾试纸,如试纸变蓝,则有氯气.
原理:氯气具有氧化性可将KI中碘离子氧化为碘单质,碘单质遇淀粉变蓝.
这基本可视为一个特征反应,要检验氯气直接用湿润KI淀粉试纸就行1年前查看全部
- 下列说法错误的是下列说法错误的是:A、臭氧可使湿润的KI淀粉试纸变蓝B、石英玻璃是以纯碱、石灰石和石英为原料制成的C、用
下列说法错误的是
下列说法错误的是:
A、臭氧可使湿润的KI淀粉试纸变蓝
B、石英玻璃是以纯碱、石灰石和石英为原料制成的
C、用渗析法可分离淀粉胶体和碘化钾溶液的混合物
D、氯化亚铁溶液久置于空气中因被氧化而呈黄色 李里123451年前4
李里123451年前4 -
 四川曾颖 共回答了20个问题
四川曾颖 共回答了20个问题 |采纳率100%选B.是二氧化硅和纯碱.没有石灰石1年前查看全部
- 检验KIO3的化学方程式?防治碘缺乏病的碘添加剂是KIO3,可用盐酸酸化的KI淀粉混合液检验食盐是否加碘,它的化学方程式
检验KIO3的化学方程式?
防治碘缺乏病的碘添加剂是KIO3,可用盐酸酸化的KI淀粉混合液检验食盐是否加碘,它的化学方程式或离子方程式怎样写? 狼儿20051年前3
狼儿20051年前3 -
 KF92316 共回答了19个问题
KF92316 共回答了19个问题 |采纳率84.2%化学反应方程式:KIO3+5KI+6HCl=6KCl+3I2+3H2O
离子反应方程式:(IO3 -)+(5I-)+(6H+)=3I2+3H2O
另外还可以用稀硫酸:
化学反应方程式:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
离子反应方程式:(IO3 -)+(5I-)+(6H+)=3I2+3H2O1年前查看全部
大家在问
- 1人教版6年级上册的数学期中试卷带答案
- 2对读书有阴影了,老觉得书读得多的都是好人,可并不是如此,大学里照样很乱,我该怎么
- 3正方的对角线长10厘米,则此正方形的面积为多少?
- 4已知如图 在平面直角坐标系中 点c(0.2)以c为圆心 以4为半径的圆与x轴相交于点A B 与X轴相
- 5不等式ax²+bx+c>0 的解集为{x丨-1
- 6写春景、夏景、球景、冬景、梅花、竹子、柳树、长江、黄河、泰山、边塞风光的诗句
- 7已知三角形ABC的三个内角ABC成等差数列,其外接圆半径为1,且sinA-sinC+(√2/2)cos(A-C)=√2/
- 8在图所示的U形管中装有水银,当把扎有橡皮膜的金属盒放在距水面34cm时,U形管中水银面的高度差是多少?
- 9设函数fx=1-x-1分之一 判断并证明fx在(1,+无穷大)的单调性和最小值
- 10文言文阅读(共8分)阅读《扁鹊见蔡桓公》,完成12—14小题。扁鹊见蔡桓公,立有间,扁鹊曰:“君有疾在腠理,不治将恐深。
- 11如图所示,一光束包含两种不同频率的单色光,从空气射向两面平行玻璃砖的上表面,玻璃砖下表面有反射层,光束经两次折射和一次反
- 123次根号a分之b等于多少 化简下
- 13强酸制弱酸 要怎么理解?就比如给一个方程式,要怎么比较强弱?
- 14某学生做这张数学卷,用1/2时做好了口算·填空题和选择题,用1/6时做好了计算题,最后用3/5时完成了解答题
- 15–John had a short walk after lunch,__________? A.didn’t he B


