硫酸铁铵和六水合硫酸铁铵是一个吗?
 liuf1214462022-10-04 11:39:541条回答
liuf1214462022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 yunxi13 共回答了15个问题
yunxi13 共回答了15个问题 |采纳率80%- 前者指无水硫酸铁铵,与后者不同
- 1年前
相关推荐
- 一道化学题21.向硫酸铁铵溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是 A.Fe2++SO42-+B
一道化学题
21.向硫酸铁铵溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.Fe2++SO42-+Ba2++2OH-→BaSO4↓+Fe(OH)2↓
B.NH4++Fe3++ 2SO42-+ 2Ba2++ 4OH-→2BaSO4↓+ Fe(OH)3↓+ NH3·H2O
C.2Fe3++ 3SO42-+ 3Ba2++6OH-→3BaSO4↓+ 2Fe(OH)3↓
D.3NH4++ Fe3++3SO42-+ 3Ba2++ 6OH-→3BaSO4↓+Fe(OH)3↓+3NH3·H2O 我爱三儿1年前3
我爱三儿1年前3 -
 神秘的玛雅 共回答了22个问题
神秘的玛雅 共回答了22个问题 |采纳率81.8%楼主
答案是B,C(你这是多选题吗?怎么感觉有两个答案……)
其实硫酸铁铵你这样看就行了.
铵离子需要1mol的氢氧根离子,而铁离子是需要3mol氢氧根离子的(假设硫酸铁铵是1mol)
那么也就是说如果需要把铁敲好完全沉淀就正好需要3mol的氢氧根离子.
但是而因为铵根离子需要1mol的氢氧根离子,所以若敲好完全反应就是需要4mol的氢氧根离子.
那么也就是2mol的氢氧化钡.
即硫酸铁铵比氢氧化钡是1比2反应
而这正是B
若是C.
则是2比3反应.
那么溶液生成的是硫酸钡和庆阳忽而贴还有硫酸铵.
因为硫酸铵可以拆开(在化学反应式前后可以约掉)
那么就是C
感觉有两个答案不合理……
但是看了十分钟还是感觉应该有两个答案
因为现在大学了……有些忘了 如果跟标答不对的话,楼主请见谅哦
同时也希望告诉我我错在那里
谢谢了1年前查看全部
- 物质的量浓度相同的碳酸铵,硫酸铵,硫酸铁铵溶液中pH由小到大的顺序
 俺们屯俺最拽1年前1
俺们屯俺最拽1年前1 -
 部件401 共回答了13个问题
部件401 共回答了13个问题 |采纳率100%越弱越水解,根据碱根离子最弱的是硫酸铁,可知道硫酸铁的酸性最强,PH最小.
硫酸铵次之,而碳酸铵是两个弱根,水解程度差不多,接近中性,所以PH最大.1年前查看全部
- 配制硫酸铁铵溶液时,能否直接用水溶解?为什么?
 今晚陪你过1年前2
今晚陪你过1年前2 -
 不能象你这么南 共回答了17个问题
不能象你这么南 共回答了17个问题 |采纳率100%可以的.
http://baike.baidu.com/view/454173.htm
因为铵盐显酸性的,可以一定程度抑制铁离子的水解,所以和其他单纯铁盐不同,一般配置是就直接加水溶解的.
希望对你有帮助O(∩_∩)O~1年前查看全部
- 二氧化钛含量检测中加硫酸铁铵什么作用?
二氧化钛含量检测中加硫酸铁铵什么作用?
是“二氧化钛含量检测中加硫酸铵什么作用?” njsfzxy1年前1
njsfzxy1年前1 -
 hsh5018 共回答了20个问题
hsh5018 共回答了20个问题 |采纳率100%助熔.因为滴定法测二氧化钛含量其实滴定的是钛离子,所以必须要将二氧化钛溶解至浓硫酸中,浓硫酸溶解二氧化钛花费的时间太长,而且很难全部溶解,必须加入硫酸铵助熔.1年前查看全部
- 某化工厂以硫酸亚铁[含少量的Ca(NO3)2]的硫酸铵为原料,设计了一种流程制取硫酸铁铵[aFe2(SO4)3•b(NH
某化工厂以硫酸亚铁[含少量的Ca(NO3)2]的硫酸铵为原料,设计了一种流程制取硫酸铁铵[aFe2(SO4)3•b(NH4)2SO4•cH2O].请回答下列问题:
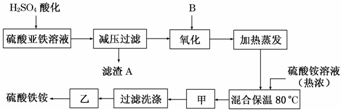
(1)硫酸亚铁溶液加H2SO4酸化的主要目的是______,滤渣A的主要成分是______.
(2)下列物质中最适合的氧化剂B是______(填字母编号):其反应的离子方程式为______.
a.NaClO b.H2O2 c.KMnO4 d.K2Cr2O7
(3)操作甲、乙的名称分别是:甲______,乙______.
(4)检验硫酸铁铵中NH4+的方法是______.
(5)称取14.00g样品,将其溶于水配置成100mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14g沉淀;向另一份溶液中加入0.05mol Ba(NO3)2溶液,恰好完全反应.则该硫酸铁铵的化学式为______. rian7551年前1
rian7551年前1 -
 ll侠 共回答了19个问题
ll侠 共回答了19个问题 |采纳率89.5%解题思路:原料中加入硫酸酸化,可生成硫酸钙沉淀,减压过滤后加入过氧化氢氧化可生成硫酸铁,加入硫酸铵,在80℃下反应可生成硫酸铁铵,经蒸发浓缩、冷却结晶、过滤洗涤,最后经常温晾晒可到纯净的硫酸铁铵,结合对应物质的性质以及题目要求可解答该题.原料中加入硫酸酸化,可生成硫酸钙沉淀,减压过滤后加入过氧化氢氧化可生成硫酸铁,加入硫酸铵,在80℃下反应可生成硫酸铁铵,经蒸发浓缩、冷却结晶、过滤洗涤,最后经常温晾晒可到纯净的硫酸铁铵,
(1)加入硫酸,可增大溶液中SO42-浓度,将Ca2+转化为沉淀,生成CaSO4,同时抑制Fe2+水解,
故答案为:增大溶液中SO42-浓度,将Ca2+转化为沉淀或抑制Fe2+水解;CaSO4;
(2)为避免引入新杂质,应加入过氧化氢为氧化剂,反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O,故答案为:b;H2O2+2Fe2++2H+=2Fe3++2H2O;
(3)在80℃下反应可生成硫酸铁铵,经蒸发浓缩、冷却结晶、过滤洗涤,最后经常温晾晒可到纯净的硫酸铁铵,温度不能过高,防止分解,
故答案为:冷却结晶;常温晾晒;
(4)检验NH4+的方法是加入强碱反应、加热能够产生使湿润的红色石蕊试液变蓝的气体,该气体是氨气,从而证明原溶液中一定含有NH4+,
故答案为:在试管中加入样品和氢氧化钠固体,在试管口用湿润的红色石蕊试液检验,看到试纸变蓝色;
(5)称取14.00g样品,将其溶于水配置成100mL溶液,分成两等份,向其中一份中加入足量NaOH溶液,过滤洗涤得到2.14g沉淀,应为Fe(OH)3,
n(Fe(OH)3)=[2.14g/107g/mol]=0.02mol,
向另一份溶液中加入0.05mol Ba(NO3)2溶液,恰好完全反应,则n(SO42-)=0.05mol,
所以14.00g样品中含有Fe2(SO4)30.02mol,n(SO42-)为0.1mol,则(NH4)2SO4为0.1mol-0.02mol×3=0.04mol,
则m(H2O)=14.00g-0.02mol×400g/mol-0.04mol×132g/mol=0.72g,
n(H2O)=[0.72g/18g/mol]=0.04mol,
n(Fe2(SO4)3):n((NH4)2SO4):n(H2O)=0.02:0.04:0.04=1:2:2,
所以化学式为Fe2(SO4)3•2(NH4)2SO4•2H2O,
故答案为:Fe2(SO4)3•2(NH4)2SO4•2H2O.点评:
本题考点: 物质分离和提纯的方法和基本操作综合应用.
考点点评: 本题考查考查物质的分离、提纯制备,为高考常见题型,侧重于学生的分析能力、实验能力和计算能力的考查,注意根据物质的性质把握实验原理和方法,难度中等.1年前查看全部
- 用硫氰酸铵滴定中和过量硝酸银,以硫酸铁铵为指示剂,溶液颜色怎么变化的?还有反应方程式怎么写的?
 Rebecca_Yan1年前1
Rebecca_Yan1年前1 -
 yzh88 共回答了17个问题
yzh88 共回答了17个问题 |采纳率82.4%这个滴定是这样的 把硝酸银和硫酸铁铵放在锥形瓶里 然后用滴定管滴下硫氰酸铵 一开始滴下的硫氰酸铵都和硝酸银反应了 等把硝酸银反应完了 过量的一滴硫氰酸铵就和指示剂硫酸铁铵反应了 就是铁离子与硫氰根反应了 溶液变为血红色 所以颜色变化就是无色变为血红色
方程式就是 Ag+ + 2NH3·H2O Fe(SCN)31年前查看全部
- 硫酸铁铵的饱和溶液如何配置,注意是饱和溶液.
 yusiliu1年前2
yusiliu1年前2 -
 xxhh030914 共回答了24个问题
xxhh030914 共回答了24个问题 |采纳率95.8%一定温度下,在一定量蒸馏水中,不断搅拌加入硫酸铁铵晶体,直到有少量晶体析出时,配成饱和溶液成功,我们在大学做实验配饱和溶液基本都是用这种方法的1年前查看全部
- 硫酸铵和硫酸铁铵的ph值大小
 奇怪的膝盖骨头1年前1
奇怪的膝盖骨头1年前1 -
 stanworks 共回答了16个问题
stanworks 共回答了16个问题 |采纳率93.8%硫酸铁铵ph值小于硫酸铵,硫酸铁铵的水解程度大于硫酸铵1年前查看全部
- 英语翻译醋酸正丁酯的合成硫酸铁铵被催化剂和水是分开的环己烷反应体系.结果表明,硫酸铁铵具有良好的催化作用.n-Butyl
英语翻译
醋酸正丁酯的合成硫酸铁铵被催化剂和水是分开的环己烷反应体系.结果表明,硫酸铁铵具有良好的催化作用.
n-Butyl acetate was synthesized with ammonium ferric sulfate being catalyst and the water was separated from reaction system by cyclohexane.The results indicate that ammonium ferric sulfate is possessed of good catalysis.
谁帮我把中文翻译的字词排个序,懂行的来 fgw0071年前1
fgw0071年前1 -
 niuniufish 共回答了24个问题
niuniufish 共回答了24个问题 |采纳率83.3%醋酸正丁酯是以硫酸铁铵为催化剂合成的,生成的水用环己烷移出反应体系(不过怎么用环己烷移出啊?共沸除水吗?).结果表明硫酸铁铵是一种良好的催化剂1年前查看全部
- 电镀液的测定误差问题用重铬酸钾法测定电镀液中的甲基磺酸锡含量:步骤如下:称样0.7g加25ml硫酸铁铵,加10ml浓硫酸
电镀液的测定误差问题
用重铬酸钾法测定电镀液中的甲基磺酸锡含量:步骤如下:称样0.7g加25ml硫酸铁铵,加10ml浓硫酸,反应2min,加70ml水,加10ml浓磷酸,反应2min,以二苯胺磺酸钠为指示剂,用重铬酸钾滴定至溶液由绿色变蓝紫色为终点。在实验中平行样间误差较大,求教高手,各步骤的反应机理和实验中所需注意的细节问题 ,以减少平行样间的误差问题。
 青草饭团1年前1
青草饭团1年前1 -
 Bernadette 共回答了19个问题
Bernadette 共回答了19个问题 |采纳率89.5%找找看有没有国标方法或ISO方法,或甲基磺酸锡产品的标准分析方法1年前查看全部
- 关于制备亚硫酸铁铵1.将10%Na2CO3溶液和铁屑混合煮沸,冷却,洗涤,过滤得铁屑.其中10%Na2CO3溶液作用是什
关于制备亚硫酸铁铵
1.将10%Na2CO3溶液和铁屑混合煮沸,冷却,洗涤,过滤得铁屑.
其中10%Na2CO3溶液作用是什么?
2.处理过的铁屑和3mol·L-1 H2SO4混合加热,反应基本完成后,再加入3mol·L-1 H2SO4,过滤得FeSO4溶液.
其中第二次加入H2SO4的作用是什么?
3.将足量硫酸铵溶液加入到硫酸亚铁溶液中,同时将Fe屑与稀H2SO4反应产生的H2通入混合溶液中,结晶得到莫尔盐.
其中H2的作用是什么? wqscl1年前1
wqscl1年前1 -
 张家有女 共回答了24个问题
张家有女 共回答了24个问题 |采纳率95.8%1.除去铁屑表面的油污.
2.不知道
3.防止亚铁离子被空气氧化成铁离子.1年前查看全部
- 什么是硫酸铁铵标准溶液氧化还原滴定法?
 rosicky19811年前1
rosicky19811年前1 -
 q582574597 共回答了16个问题
q582574597 共回答了16个问题 |采纳率87.5%用铵根离子与氢氧根离子反应生成氨气的原理1年前查看全部
- 25℃时,浓度为1摩每升硫酸铵,碳酸铵,亚硫酸铁铵三种溶液中,测得其中铵根离子的浓度分别是ABC则三个浓
 终于我1年前2
终于我1年前2 -
 ghfnghnfghnfgh 共回答了19个问题
ghfnghnfghnfgh 共回答了19个问题 |采纳率89.5%这道题要考虑到铵根离子的水解平衡,硫酸铵中硫酸根离子不影响铵根离子的水解平衡,所以以它为参考,碳酸铵、亚硫酸铵中碳酸根离子与亚硫酸根离子都要与铵根离子发生双水解,所以要考虑到哪个水解程度大,亚硫酸是中强酸所以亚硫酸根离子的水解程度要小于碳酸根离子的水解程度,所以答案应是硫酸铵〉亚硫酸铵〉碳酸铵1年前查看全部
- 零点零一摩尔每升的硫酸铁铵溶液与零点零二氢氧化钡溶液的体积混合
 ode2me1年前1
ode2me1年前1 -
 gbiea1 共回答了13个问题
gbiea1 共回答了13个问题 |采纳率76.9%生成硫酸钡沉淀,氨水和氢氧化铁沉淀,若加热则将氨水改为氨气和水.1年前查看全部
- 水的的微量铁的测定中为什么用硫酸铁铵配制标准溶液?而不能用如氯化铁之类的铁盐?
 linolupeng1年前1
linolupeng1年前1 -
 zisu2677 共回答了19个问题
zisu2677 共回答了19个问题 |采纳率94.7%我的理解是硫酸铁铵应该比较稳定,氯化铁应该容易被还原成氯化亚铁吧1年前查看全部
- 硫酸铁铵溶液的配制方法?
 结束就是开始1年前1
结束就是开始1年前1 -
 曾经是 共回答了15个问题
曾经是 共回答了15个问题 |采纳率86.7%计算
称量
溶解
转移
洗涤
定容
摇匀1年前查看全部
大家在问
- 1氢氧化铜的颜色变化
- 2英语阅读理解We parents often take material things for love.“I give
- 3用英语写一篇介绍学习英语有何意义的短文 一百二十字
- 4谁能帮我把古诗改写成记叙文?(300字)
- 5请高手帮我在星期一以前,改一下这篇英语作文,我要交给老师改的……
- 6一毫米水柱=多少帕
- 7某工程队修一条水渠,第一天修了3/5千米,比第二天少修1/5千米,两天修的正好是全长的2/5,这条水渠长多少
- 8“我曾经猜想过他会不会问这个问题,终于...他开口了” 英文怎么表达?I need ur help.thx to ans
- 9I do not know what clothes I can wear to the party.同义句
- 10在等式y=x的平方+mx+n中,当x=3时,y=5;当x=-4 y=-9.求当x=-5时,y的值
- 11帮我把山东省费县建设西路2号2号楼1单元110室翻译成英文地址格式
- 12What do you usually eat the festival
- 13第一题可不做
- 14英语!急Mr. Clarke is a very busy man. He always works hard. He
- 15已知(a-2)²+丨b+1丨=0,求2(2ab+5a²b)-3(a²b-ab)的值
