温度不变恒容时充入惰性气体,可逆反应的平衡怎么变化,
 link82022-10-04 11:39:541条回答
link82022-10-04 11:39:541条回答充入气体压强应该增大,为什么平衡不变?速率变不变?若在恒压时充入惰性气体呢?恒压时充入气体,容器体积变大,从而浓度减小,反应变慢,可是应该朝哪个方向变化?还有怎么判断反应物的体积分数增大减小或者气体密度变化情况?谢 【注意共有七问,请勿少答】

已提交,审核后显示!提交回复
共1条回复
 520liouyu 共回答了20个问题
520liouyu 共回答了20个问题 |采纳率95%- 温度不变恒容时充入惰性气体,可逆反应的(1)平衡不变,(2)速率不变.,(3)体积不变,充入不参与反应的气体根本没用的,参与反应的气体压强不会增加.(4)恒压就不一样了,冲入了惰性气体,要保持恒压体积必须增加,这时...
- 1年前
相关推荐
- 以废硫化碱液和硫磺为原料,合成硫代硫酸钠时,首先要合成二硫化钠,在这一步上有什么关键点,比如温度,浓度等,
 落叶常飞1年前1
落叶常飞1年前1 -
 会tt的_鱼 共回答了21个问题
会tt的_鱼 共回答了21个问题 |采纳率95.2%碱性环境.1年前查看全部
- 在环己烯制备实验中,为什么要控制分妞柱顶温度不超过73
 玉麟麒1年前1
玉麟麒1年前1 -
 我是阿邋 共回答了14个问题
我是阿邋 共回答了14个问题 |采纳率92.9%环己烯的制备
一、实验目的
1、 学习以浓磷酸催化环己醇脱水制取环己烯的原理和方法;
2、 初步掌握分馏和热水浴蒸馏的基本操作技能.
3、 有机物萃取洗涤方法及干燥方法.
二、反应原理
主反应:
副反应:
三、主要化学试剂、产物、副产物的物理和化学性质
名 称
分子量
状 态
熔点
(℃)
沸点
(℃)
密度
d420
折射率
nD20
溶解度
水
醇
醚
环己醇
100.16
无色液体
25.15
161.1
0.9624
1.4641
溶
溶
溶
环己烯
82.15
无色液体,易挥发
-103.5
82.98
0.8102
1.4465
不
∞
∞
四、化学试剂的用量及产物的产量:
名 称
实际用量
理论用量
过量(%)
理论用量
环己醇
10ml(9.6g,0.096mol)
10ml(9.6g,0.096mol)
磷 酸
5.0ml(7.16g,0.073mol)
6.57ml(8.00g,0.096mol)
环己烯
7.89g (0.096mol)
五、仪器装置图
图1 分馏装置 图2 常压蒸馏装置
六、流程图
七、实验记录
在50ml圆底烧瓶中,加入10ml(0.096mol)环己醇及5ml85%磷酸,充分振荡使液体混合均匀,投入少许沸石,安装分馏装置,用25ml 量筒作接收器.
缓慢加热至沸腾,控制分馏柱顶温度不超过73℃.直到无馏出液滴为止.这时烧瓶内出现白雾,停止加热,记下粗产品中油层和水层的体积.
将粗产品放到小锥形瓶中,用滴管吸去水层,加入等体积的饱和食盐水,充分振荡后静置待液体分层.用吸管吸去水层.油层转移到干燥的小锥形瓶中,加入少量无水氯化钙干燥之.将干燥后的粗制环己烯用水浴蒸馏,收集82~85℃的馏分.产量:约4-5g.
纯环己烯为易燃有刺激性气味的无色液体.沸点bp= 82.98℃,折光率 =1.4465.
八、实验记录
时间
操 作 步 骤
现 象
解 释 或 备 注
10:50
按图安装实验装置.用25ml 量筒作接收器.
11:16
加入10.0ml环己醇
5.0ml85%磷酸
加沸石2粒.
为无色液体,略有粘稠.
无色,此时反应液为无色.
11:30
开始缓慢加热.
11:42
沸腾,保持沸腾而不蒸出馏出液20min.
瓶内反应液沸腾,出现回流.
12:05
升高温度,控制加热蒸馏速度使分馏柱顶温度不超过90℃.蒸至无馏出液滴为止.
温度控制在69.0-83.0℃之间,以防环己醇被蒸出
环己烯-水共沸沸点70.8℃;环己醇-环己烯共沸沸点64.9℃;环己醇-水共沸沸点97.8℃.
12:30
烧瓶内出现白雾,停止加热
粗产品中油层:3.2ml
水层:2.5ml
说明环己醇的脱水反应已经结束
12:40
将量桶中的馏出液倒入分液漏斗中进行分液,静置5min.
分层,
水层在下层,无色
有机层在上层,无色
13:00
分出下层水溶液.
用10ml饱和食盐水洗涤有机层.
除去粗产品中的水分,减少有机物的在水中的溶解度,有利于分层.
13:15
分出水层,将有机层倒入一个干燥并且干净的锥形瓶里,加入1.0g无水氯化钙,盖上盖子,振动后,放置30min
有机物中有明显悬浮干燥剂.
氯化钙还可除去原料环己醇.
有悬浮干燥剂存在说明干燥剂用量足够.每10ml液体产品约加入0.5-1.0g干燥剂.
13:45
安装蒸馏装置.
将滤去干燥剂的粗产品加入蒸馏烧瓶中,加2粒沸石.
热水浴加热,蒸馏收集82-85℃之间的馏分.可以将三角烧瓶放在冷水浴中冷却,以防挥发.
馏分为82.0-83.6℃之间的馏分
产品为无色透明液体,略有香味.
整个装置所用仪器均需提前干燥无水.
锥形瓶空重:
65.5g
瓶+产品共重:
70.8g
产 品 重:
5.30g
14:15
停止蒸馏,拆卸装置.
九、产品产率计算
产率=5.30/7.89 ×100% =67.2%1年前查看全部
- 100℃的水蒸气遇到人体液化成水时,水的温度为什么还是100℃
 mmm000200021年前4
mmm000200021年前4 -
 1313往往 共回答了10个问题
1313往往 共回答了10个问题 |采纳率100%因为水是晶体,晶体在从一种形态转化成另外一种形态的过程中,其温度是不变化的,这是晶体的一个特性.所以水蒸气在液化成水的过程中温度始终是100℃.只不过在液化过程中,水蒸气要大量放热,所以水蒸气遇到人体后很容易把人烫伤.1年前查看全部
- 一定温度下将a%的硝酸钾水溶液分成两等份,一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无
一定温度下将a%的硝酸钾水溶液分成两等份,一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无水晶体,则该温度下硝酸钾的溶解度为()
选项
A、10m克
B、20m克
C、30m克
D、(1000a/100-a)克 晃悠懒猫1年前1
晃悠懒猫1年前1 -
 萧岚 共回答了18个问题
萧岚 共回答了18个问题 |采纳率88.9%一份等温蒸发10克水,得到m克无水晶体; 另一份等温蒸发20克水,得到3m克无水晶体,相当于在饱和溶液中蒸发10克水,析出晶体2m克
2m/10=S/100 S=20m g
选B1年前查看全部
- 铁的熔点是1535度温度是1535度的铁a正在融化b正在凝固C不融化也不凝固D条件不足无
 angex1年前4
angex1年前4 -
 闪亮蓝梅 共回答了19个问题
闪亮蓝梅 共回答了19个问题 |采纳率100%D对.
因为温度刚好等于铁的熔点,可以是铁将要熔化,也可以是铁正在熔化,也可以是刚熔化完毕,也可以是将要凝固,也可以是正在凝固,也可以是刚好凝固完毕.1年前查看全部
- 科技人员昼夜在隧道里实地观察,经过反复观察,反复试验,终于找到了喷射混泥土最佳温度这句话采用了什么修辞
科技人员昼夜在隧道里实地观察,经过反复观察,反复试验,终于找到了喷射混泥土最佳温度这句话采用了什么修辞
快
越快越好, 乡心梦不成1年前1
乡心梦不成1年前1 -
 lihaiyingaa 共回答了17个问题
lihaiyingaa 共回答了17个问题 |采纳率94.1%排比呗,错了不要怪我1年前查看全部
- 几道关于科学的选择题,1、小明用热水配制了大半杯的饱和硝酸钾水溶液,溶液的温度是70摄氏度,一个密度均匀的实心小球恰能悬
几道关于科学的选择题,
1、小明用热水配制了大半杯的饱和硝酸钾水溶液,溶液的温度是70摄氏度,一个密度均匀的实心小球恰能悬浮在溶液中.在室温下放置一段时间后,小球将
a、上浮 b、下沉
c、悬浮 d、无法确定
2、有四个500毫升的瓶子,分别装满海水、纯水、酒精和汽油.其中装的质量最多的是.(海水密度大于纯水密度大于酒精密度大于汽油密度)
a、海水 b、纯水
c、酒精 d、汽油
3、两条长度相等、横截面积不等的同种材料制成的电阻丝,串联在电路中,则粗电阻丝
a、电流强度较大 b、电流强度较小
c、电压较大 d、电压较小 风中曾经的承诺1年前1
风中曾经的承诺1年前1 -
 ethanhua 共回答了21个问题
ethanhua 共回答了21个问题 |采纳率85.7%第一题选B
因为当温度降低,硝酸钾溶解度变小,溶液密度变小,所以浮力小于重力,小球下沉
第二题选A
M=V×P 质量=体积×密度
第三题选D
因为是串联所以电流一样大,电阻越粗,其阻值越小,所以粗电阻串联分压的少1年前查看全部
- 李明和王强利用温差测量某座山的温度,李明在山顶上测得温度为-2℃,王刚在山脚下测得温度为2℃.
李明和王强利用温差测量某座山的温度,李明在山顶上测得温度为-2℃,王刚在山脚下测得温度为2℃.
已知该地区高度每升高100米,气温下降约0.5℃,那么山脚与山顶的温差是多少?这座山的高度是多少?
请祥写步骤,或者说出答案思路. 在镜中飞翔1年前3
在镜中飞翔1年前3 -
 烧头 共回答了18个问题
烧头 共回答了18个问题 |采纳率94.4%2减-2差4度,4除以0.5乘以100等于800米1年前查看全部
- 10度水200克加100度水100克后温度多少
 renqingzhao1年前5
renqingzhao1年前5 -
 nonidie 共回答了25个问题
nonidie 共回答了25个问题 |采纳率92%利用热平衡方程求解,设混合后的温度为t,则
C水m1(t—10度)=C水m2(100度—t) 解得t=40度
注;C水为水的比热容 m1=200克 m2=100克1年前查看全部
- 在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温
在一定温度下,将一包白色无水硫酸铜粉末投入到150g蒸馏水中,充分搅拌,过滤,得到一定质量的蓝色晶体和84g滤液,若此温度下无水硫酸铜的溶解度为40g,则此包无水硫酸铜的质量是多少?
 默儿爱李强1年前3
默儿爱李强1年前3 -
 光看不回帖 共回答了20个问题
光看不回帖 共回答了20个问题 |采纳率90%解题思路:根据饱和溶液中质量分数不变和溶解度计算出剩余饱和溶液中溶质和溶剂的质量,根据硫酸铜晶体组成计算晶体中溶质的质量,两者之和为此包无水硫酸铜的质量.把无水硫酸铜粉末加入150g蒸馏水中,得到一定量的蓝色晶体CuSO4•5H20,剩余溶液仍然是饱和溶液,设剩余溶液中的溶质为xg,
则[40g/100g+40g]=[xg/84g]得:x=24
结晶水的质量=150g-(84g-24g)=90g,设结晶中硫酸铜的质量为yg
CuSO4~5H20
160 90
yg90g
[160/90]=[yg/90g]
y=160,此包无水硫酸铜的质量为=160g+24g=184g.
答:此包无水硫酸铜的质量是184g.点评:
本题考点: 溶液中溶质的质量分数及相关计算.
考点点评: 本题考查质量守恒定律,质量分数的计算,解题时注意守恒思想的运用.1年前查看全部
- 在压强为1.01*105pa,温度为300度时,有1mol某气体A发生如下反应:2A(g)=xB(g)+C(g),当反应
在压强为1.01*105pa,温度为300度时,有1mol某气体A发生如下反应:2A(g)=xB(g)+C(g),当反应达到平衡时,平衡混合气体中含A体积分数为60%,混合气体的总质量为46g,体积为64L.求;
1)平衡后混合气体的平均相对分子质量
2)平衡后已转化的A的物质的量
3)求x的值 Lonely-Dancer1年前1
Lonely-Dancer1年前1 -
 57201747 共回答了15个问题
57201747 共回答了15个问题 |采纳率86.7%1)根据题意,非标准状况下混合气体的温度T非=573 K,体积V非=64 L,转化为标准状况下的体积V标,由PV=nRT得:V标=(T标/T非)×V非=(273/573)×64 L = 30.5 L.则混合气体的物质的量n=(30.5/22.4)mol=1.36 mol,
设平衡时,已转化的A的物质的量为a mol,依题意:
2A(g)= xB(g)+ C(g)
起始/mol 1 0 0
变化/mol a xa/2 a/2
平衡/mol 1-a xa/2 a/2
[(1-a)/1.36]×100%=60%
a=0.184
即平衡后已转化的A的物质的量为0.184 mol.
(2)由(1-a)+xa/2+a/2=1.36,a=0.184,可计算得x=5.1年前查看全部
- 定压的绝热压缩使气体温度升高是否存在焓变,
 11235831年前2
11235831年前2 -
 欧阳逍遥 共回答了18个问题
欧阳逍遥 共回答了18个问题 |采纳率94.4%在工程热力学理论中,定压过程与绝热过程是不同的两种过程,不是一回事,不能混为一谈.绝热压缩或膨胀过程熵不变,即等熵过程,但工质内的焓有变化.定压过程(等压过程)容积随温度变化,有焓变.1年前查看全部
- 温度降低,植物的光合作用为什么减弱?HIV在体内合成DNA的原料?
 idothee1年前3
idothee1年前3 -
 zjnbwhj 共回答了18个问题
zjnbwhj 共回答了18个问题 |采纳率88.9%温度降低使得参与植物光合作用的酶活性降低,从而减弱植物的光合作用.合成DNA的原料是五碳糖,磷酸,碱基(A,T,G,C).1年前查看全部
- 有谁懂医用基础化学有谁比较懂医用化学的啊 我有一些题麻烦帮我解答一下啊 ( )16、一定温度下,稀溶液的蒸汽压下降决定于
有谁懂医用基础化学
有谁比较懂医用化学的啊 我有一些题麻烦帮我解答一下啊
( )16、一定温度下,稀溶液的蒸汽压下降决定于:
A.大气压强 B.溶质的本性 C.溶质的分子数 D.溶液的渗透浓度
( )17.浓度相同的NH4Cl与 NH3溶液按下列哪种比例混合,才能得到pH=9.25的缓冲溶液.(pK(NH3)=4.75)
A.一体积NH4Cl溶液与二体积NH3水溶液 B.二体积NH4Cl溶液与一体积NH3水溶液 C.三体积NH4Cl溶液与一体积NH3水溶液 D.等体积
( )18、某一级反应,当反应物浓度消耗一半时需要12分钟,则36分钟后反应物浓度为原始浓度的
A、1/6 B、1/8 C、1/3 D、1/4
( )19.有碳酸钠0.53g,求n( Na2CO3) 是多少?已知[Mr(Na2CO3)=106].将其溶于400 ml 的水中,配制成溶液,其浓度为多少?
A.n=0.005,c=0.0125mol/L B.n=0.010,c=0.0125 mol/L
C.n=0.005 c=0.025mol/L D.n=0.010,c=0.025mol/L
( )20酸碱质子理论认为:凡是能 (12) 的物质都是酸;凡是能 (13) 的物质都是碱.共轭酸的酸性越强,其共轭碱的碱性就越___(14)___.
(12)A.给出质子 B.接受质子 C.使石蕊变红 D.使酚酞无色
(13)A.给出质子 B.接受质子 C.使石蕊变蓝 D.使酚酞变红
(14)A.越强 B.越弱 C.不变 D.与其无关
( )21在乙炔分子中共含有σ键 (1) 个,π键 (2) 个.NH3分子中的N原子是以_(3)_杂化轨道成键的;H2O分子中的O原子是以_(4)_杂化轨道成键的.
(1) A.5 B.2 C.0 D.3
(2) A.3 B.5 C.2 D.0
(3) A.SP3 B.SP2 C.没有杂化 D.SP3不等性
(4) A.SP3不等性 B.SP2 C.SP3 D.SP
( )22、某电子的运动状态n = __(5)__,l = 3,m = -1,si = +1/2.
(5)A.2 B.3 C.4 D.-1/2
( )23、正常人血液的pH应维持在 (8) 范围,其中最重要的一个缓冲系是 (9) .(8) A.7.35-7.45 B.7.10-7.20 C.7.0-7.40 D.6.35-7.00
(9) A.H2PO4--HPO42- B.H2bO2-HbO2- C.HCO3--CO2(aq)
( )24、在下述分子中CCl4、 CHCl3、C2H4和CH2CCl2,极性分子有 (17) ,含有π键的分子有 (18) .
(17)A.CHCl3和CH2CCl2 B.CH2CCl2 C.CCl4和C2H4 D.CCl4
(18)A.CHCl3 B.CCl4 C.C2H4 D.C2H4和CH2CCl2
( )25、为简要说明σ键和π键 的主要区别,叙述最完整的为
A.σ键是指两个原子的原子轨道沿键轴方向以“头碰头”方式重叠所形成的共价键;而π键是指两个原子轨道垂直于键轴,以“肩并肩”方式重叠所形成的共价健.
B.除A.中所述内容外,σ键重叠程度大,较π键牢固.可单独存在于两原子之间,构成分子的骨架.
C.除B.中所述内容外,π键较σ键活泼,较易断开.
D.σ键和π键 的主要区别只是σ键能独立存在于两原子之间,而π键则不能. 最好看眼神1年前1
最好看眼神1年前1 -
 jornme 共回答了21个问题
jornme 共回答了21个问题 |采纳率95.2%16、D.溶液的渗透浓度
17、D.等体积 pH=pKa,所以是等体积
18、B、1/8 一半一半又一半,得到1/8
19、A.n=0.005,c=0.0125mol/L
20、A.给出质子 是酸 B.接受质子 是碱 B.越弱
21、D.3 σ键 C.2 π键 D.SP3不等性 A.SP3不等性
22、A.2
23、A.7.35-7.45 标准是7.4;C.HCO3--CO2(aq)
24、A.CHCl3和CH2CCl2 不对称就有极性;D.C2H4和CH2CCl2 π键含在双键里面
25、B 具体的区别如下:
σ键可以单独存在
π键一定要与σ键共存
σ键键能较大,由电子云沿轴对称重叠而成,重叠程度大,能绕键轴自由旋转
π键键能较小,是由p电子云从侧面重叠,易断,不能旋转
σ键不易极化,电子云分布比较集中
π键容易极化,电子云分散在对称平面上下,有较大流动性1年前查看全部
- 比热容 物体温度升高时吸收的热量Q吸= ;物体温度降低时
比热容 物体温度升高时吸收的热量Q吸= ;物体温度降低时
比热容
物体温度升高时吸收的热量Q吸= ;物体温度降低时放出的热量Q放= ;式中T1表示物体的 ,T表示物体的 ,M表示物体的 ,如用KG作单位,则比热容就应以 作单位,这样计算出的热量单位是 . liangjing03201年前1
liangjing03201年前1 -
 tianya_2001 共回答了13个问题
tianya_2001 共回答了13个问题 |采纳率92.3%答案:
Q吸=cm(t1-t)
Q放=cm(t-t1)
t1是物体的末温度,t是物体的初温度,m是物体的质量,
J/(kg·℃)
J1年前查看全部
- 质量为10千克的水.温度升高了10℃ 求水吸收的热量Q吸
质量为10千克的水.温度升高了10℃ 求水吸收的热量Q吸
带公式最好! grace07061年前1
grace07061年前1 -
 hxl0806 共回答了18个问题
hxl0806 共回答了18个问题 |采纳率94.4%Q=cmt=4200*10*10=420000焦1年前查看全部
- 1.萝卜的根地上部分是绿色,地下部分是白色,由此可推测,与叶绿素的形成有关是()A.光 B.温度 C.水分
1.萝卜的根地上部分是绿色,地下部分是白色,由此可推测,与叶绿素的形成有关是()A.光 B.温度 C.水分
2.关于生物与环境关系的说法中,最为确切的是()A.蚯蚓能增加土壤肥力是生物对环境的适应 B.生物因素指不同生物之间的相互作用 C.生物不仅能适应一定的环境,而且能影响环境 D.生物对环境的影响是各种非生物因素共同作用的结果 eckx6j1年前1
eckx6j1年前1 -
 刺客198 共回答了22个问题
刺客198 共回答了22个问题 |采纳率86.4%d或c1年前查看全部
- 一个物体也没有用( )来表示;在表示温度时
一个物体也没有用( )来表示;在表示温度时
它是正负温度的( )线;在刻度尺上它是( )在数轴上它是正数和负数的( )点;在计数器上它起( )作用 dajunli1年前1
dajunli1年前1 -
 yunjie1984 共回答了19个问题
yunjie1984 共回答了19个问题 |采纳率100%一个物体也没有用(0)来表示;在表示温度时它是正负温度的(分界)线;在刻度尺上它是(原点),在数轴上它是正数和负数的(分界)点;在计数器上它起(标准点)作用1年前查看全部
- 对于密闭容器中进行的反应:N2+O2=2NO,下列条件中哪些能加快反应速率(假定改变下列条件时温度不变)
对于密闭容器中进行的反应:N2+O2=2NO,下列条件中哪些能加快反应速率(假定改变下列条件时温度不变)
A缩小容器体积使压强增大
B压强不变,充入N2使容器体积增大
C容器体积不变充入氦气使压强增大
D增大容器的体积 feng833525551年前2
feng833525551年前2 -
 clivia0429 共回答了14个问题
clivia0429 共回答了14个问题 |采纳率92.9%A1年前查看全部
- 科学《电阻大小的因素》 不在考虑温度对电阻的影响时,某导体中的电流由小变大,由此可断定此导体的电阻将
科学《电阻大小的因素》 不在考虑温度对电阻的影响时,某导体中的电流由小变大,由此可断定此导体的电阻将
().
A.增大
B.减小
C.不变
D.无法判断 happyman_szcn1年前2
happyman_szcn1年前2 -
 橘子juzi 共回答了14个问题
橘子juzi 共回答了14个问题 |采纳率85.7%不变
电阻大小是由自身物质决定的,你就是不通电它也是那么大.1年前查看全部
- 雨是液态的水,那为什么冻雨的温度可以低于零度,一标准大气压下的水就不能高于一百摄氏度呢?
雨是液态的水,那为什么冻雨的温度可以低于零度,一标准大气压下的水就不能高于一百摄氏度呢?
雨的温度低于零度,就应该凝固成冰了,水的温度高于一百摄氏度(一标准大气压下)就会沸腾变成水蒸气,那为什么水低于零摄氏度不会结冰而高于一百摄氏度不行呢? wangzhi08301年前1
wangzhi08301年前1 -
 七月的熊 共回答了23个问题
七月的熊 共回答了23个问题 |采纳率91.3%所谓的熔点和沸点都是指平衡状态而言,但其实液体的温度既可以略低于熔点,也可以略高于沸点,这种状态属于亚稳态,你可以把它理解为暂时呆住的状态.对水而言,分别叫做过冷水和过热水.
能够形成偏离平衡态的亚稳态,主要原因是在水中形成小气泡或者小冰晶,会形成 气-液 或者 固-液 的界面,这个界面的形成是不容易自然发生的.然而从另外一个方面讲,过冷水或者过热水发生凝固或沸腾的时候,也更加激烈.
冻雨就是过冷水,它的形成主要是由于降温过快,因为它是过冷水,所以当落在固体上开始结冰之后就非常猛烈,很快结冰.
说起高中知识,其实高中就讲过过热水.你记不记得加热水的时候,要在水中加一种叫做沸石的东西,加了沸石之后,气液界面更容易形成,所以水不容易过热.如果出现过热水的话,正如刚才说的,一旦发生沸腾会非常剧烈,这是很危险的.1年前查看全部
- 据说南极最低温度是-88.3摄氏度,最高温度是突尼斯的63摄氏度,但他们出现在什么年份?
 wwingsz1年前1
wwingsz1年前1 -
 windtalker1001 共回答了11个问题
windtalker1001 共回答了11个问题 |采纳率90.9%最高的是出现在索马里,63°C,也是发生在20世纪60年代,但至于发生在何日已不可考.
最低(正式记录)出现在南极洲东方站,-89.2°C,出现在1961年8月24日1年前查看全部
- 电熨斗通电后温度很高,而连接电熨斗的导线却不怎么热,这是因为( )
电熨斗通电后温度很高,而连接电熨斗的导线却不怎么热,这是因为( )
A 导线有绝缘层保护,能隔热
B 通过导线的电流小于通过电熨斗的电流
C 导线散热快,所以温度低
D 导线电阻小,产生的热量也很小 yusuifengpiao1年前3
yusuifengpiao1年前3 -
 6d45361058092557 共回答了12个问题
6d45361058092557 共回答了12个问题 |采纳率83.3%D 导线电阻小,产生的热量也很小
很显然的.1年前查看全部
- 将温度为—8℃的冰块投入0℃的水杯中,过一段时间后冰的质量会
将温度为—8℃的冰块投入0℃的水杯中,过一段时间后冰的质量会
A减少 B不变 C增加 D以上三种都有可能 大大丁小小甲1年前5
大大丁小小甲1年前5 -
 nexttime1202 共回答了9个问题
nexttime1202 共回答了9个问题 |采纳率66.7%选择D.当它得到的热量使它升高的温度正好为8℃时,它的质量不变.当它得到的热量使它升高的温度超过8℃时,它会溶解一部分,质量减少.也有可能水的热量被冰吸收,使水也凝固了,那质量就增加了.1年前查看全部
- 在测定过程中,为什么要使用温度校正值
 anzhongyu87611年前3
anzhongyu87611年前3 -
 快乐鱼茫茫 共回答了23个问题
快乐鱼茫茫 共回答了23个问题 |采纳率91.3%温度会对许多物理性质和化学性质造成影响1年前查看全部
- 简要计算饱和蒸汽管道温降,只考虑压力降所导致的温度降,P=8公斤,温度=160-170℃
 joecy1年前1
joecy1年前1 -
 g0vde 共回答了19个问题
g0vde 共回答了19个问题 |采纳率89.5%蒸汽压力与温度的关系由实验得出,人们测得当压力为7.0kgf/cm2表压时(绝对压为8.0kgf/cm2),此时饱和蒸汽温度为169.61℃,当温度降到143(142.92)℃时,对应的饱和蒸汽压力为3.0kgf/cm2表压.因此不需要计算过程.1年前查看全部
- 图中所示的电路中,不计温度对灯丝电阻的影响,电源电压保持不变.当在ab间接入“6V 6W”的灯泡时,闭合开
 无火无烟1年前1
无火无烟1年前1 -
 xieyuyuan 共回答了15个问题
xieyuyuan 共回答了15个问题 |采纳率93.3%(1)当接入“6V 6W”时正常发光,所以此时“6V 6W”灯泡两端的实际电压为6V;由铭牌及R=U2P可知,两灯泡的额定电压相同,6W灯泡的额定功率大于4W灯泡的额定功率,则6W灯泡的电阻小于4W灯泡的电阻;x0d(2)当接入“6V 4W”灯泡时,因电阻变大,分得的电压变大、大于6V,所以换接的灯可能烧坏;x0d而此时灯泡L分得的电压变小,实际功率变小,所以灯泡L变暗;x0d电路的总电阻变大,根据欧姆定律可知电路中的电流变小,根据P=UI可知电路消耗的总功率变小.故选A.1年前查看全部
- 为什么密度随压强 温度 状态等改变而改变
 gargantua1年前1
gargantua1年前1 -
 avbnovea 共回答了14个问题
avbnovea 共回答了14个问题 |采纳率92.9%想想密度的定义,密度和质量和体积有关,在非相对论情况下,认为质量一般不会变化.那么,一个物体的体积,就有可能受到温度压强等因素的影响了,最简单的一个例子就是气体.压缩气体体积,气体的密度变大.这样的例子太多了.浅层次的解释就是这样,稍微深层次一点的就涉及到分子热运动的问题了,你到大学就知道,固态物质的温度反应了分子做振动动能的大小,温度越高,振幅越大,那么宏观反应就是物体的体积变大了.1年前查看全部
- 请问温度20度,需要提高3个立方的水到80度并保持三个小时.请问总热能是多少,锅炉多大才够(24小时连续).
 ppd811年前1
ppd811年前1 -
 sos3sos3sos 共回答了23个问题
sos3sos3sos 共回答了23个问题 |采纳率95.7%温差60度,水量3吨,总热量:18万大卡.
每小时热量:6万大卡.
锅炉效率50%计算,锅炉出力:12万大卡/小时,140KW.1年前查看全部
- 研究不同的光强、温度对植物光合作用和呼吸作用的影响,实验结果如图所示.下列有关分析正确的是( )
研究不同的光强、温度对植物光合作用和呼吸作用的影响,实验结果如图所示.下列有关分析正确的是( )
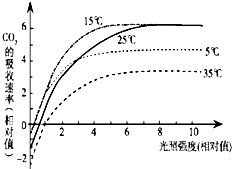 A. 光强小于1时,温度是光合作用的主要限制因素
A. 光强小于1时,温度是光合作用的主要限制因素
B. 光强大于7时,35℃条件下有氧呼吸酶的活性最低
C. 光强大于7时,25℃条件下植物合成有机物的速率最大
D. 光强小于7时,15℃条件下植物产生氧气的速率最大 creicy1年前2
creicy1年前2 -
 8752963 共回答了19个问题
8752963 共回答了19个问题 |采纳率89.5%解题思路:光合速率:光合作用固定二氧化碳的速率.即单位时间单位叶面积的二氧化碳固定(或氧气释放)量.影响光合速率的条件:光照强度、温度和空气中二氧化碳浓度.结合题意,识图作答.光合速率或称光合强度,是指一定量的植物(如一定的叶面积)在单位时间内进行了多少光合作用(如消耗多少二氧化碳、释放多少氧气、积累多少有机物等).光合作用速率受多种环境因素的影响,其中最重要的因素是光照强度、温度和空气中二氧化碳的浓度.由曲线图可知,光照强度、温度和二氧化碳浓度对光合作用的影响是综合性的.因此,只有当光强大于7时,25℃条件下植物合成有机物的速率最大的分析是正确的.因此,选项C符合题意.
故选:C点评:
本题考点: 探究光合作用的条件、原料和产物.
考点点评: 解答此题的关键是理解影响光合速率的条件是:光照强度、温度和空气中二氧化碳浓度.1年前查看全部
- 古代神话传说往往寄寓了人们对美好生活的向往和对可贵精神的褒扬.后羿射日给人们创造了一个温度适宜的居住环境,仓颉造字把人类
古代神话传说往往寄寓了人们对美好生活的向往和对可贵精神的褒扬.后羿射日给人们创造了一个温度适宜的居住环境,仓颉造字把人类带入新的文明里程,精卫填海表现了不畏艰难、奋斗到底的坚强意志,而夸父逐日,即使献出了自己的生命,也要“( ) ”,庇佑后来者以追求光明.
()内填什么啊 玛拉和洛伊的故事1年前1
玛拉和洛伊的故事1年前1 -
 laohu1234567 共回答了22个问题
laohu1234567 共回答了22个问题 |采纳率90.9%也要(战胜大自然的困境),庇佑后来者以追求光明.1年前查看全部
- 为了使温度为32℃的500千克的水沸腾,需要完全燃烧多少千克的无烟煤?
 lillian_cat331年前2
lillian_cat331年前2 -
 jwq43 共回答了18个问题
jwq43 共回答了18个问题 |采纳率88.9%无烟煤的热值为:3.4*10^7J/kg
水吸收的热量就是无烟煤放的热量,于是有等式:
Q吸=Q放
c水m水(t-t0)=m煤q煤
4200*500*(100-32)=m煤*3.4*10^7
解之有:m煤=4.2kg
明白后,1年前查看全部
- 1.甲的比热是乙的一半,甲的质量是乙的2倍,当他们吸收相等的热量后升高的温度之比为( )
1.甲的比热是乙的一半,甲的质量是乙的2倍,当他们吸收相等的热量后升高的温度之比为( )
2.把质量和温度都相同的铁球,铝球,铜球同时投入沸水中,一段时间后,三球的温度变化( )(填相同或不相同)其中吸收热量最多的是( )吸收热量最少的是( )
3.甲乙两金属块质量之比为5:3,吸收了相等热量后,升高温度之比为2:5,他们的比热容之比为( )
4.一块质量为200克的铝块,温度为55摄氏度,放入20摄氏度的水中,使水的温度升高到26摄氏度(不及热量损失)求水的质量(步骤清楚) yglqwerty1年前1
yglqwerty1年前1 -
 人生海海海海人生 共回答了12个问题
人生海海海海人生 共回答了12个问题 |采纳率66.7%Q=cmΔt
1.Q相同,cm相乘相同,所以Δt相同,所以为1:1
2.相同,最后都和水达到平衡.铝的比热容最大,吸热最多;铜的最小,吸热最少.
3.3;21年前查看全部
- 1.在某温度时,一定量的元素A的氢化物AH3在一定体积密闭容器中可完全分解成两种气态单质,此时压强增强了75%,则此反应
1.在某温度时,一定量的元素A的氢化物AH3在一定体积密闭容器中可完全分解成两种气态单质,此时压强增强了75%,则此反应的化学方程式是----------
2.将氢气,氧气,氮气分别放入不同容器中,当温度和密度完全相同时,三种气体压强(p)的大小关系是----------
3.实验测得一氧化碳和氧气混合气体的密度是氢气的14.5倍,可知其中一氧化碳的体积分数为-------------------
4.在20℃时,一钢性容器内部有一个不漏气且可滑动的活塞将容器分割成左右两室,左室冲入氮气,右室冲入氢气和氧气,活塞正好停留在离左端的1/4处,然后点燃氢气和氧气,反应完毕后恢复到原来温度,活塞恰好停在中间,水蒸气的体积可忽略,则反应前后氢气和氧气的体积比可能为------------- sarah_chan1年前1
sarah_chan1年前1 -
 旅游指南 共回答了18个问题
旅游指南 共回答了18个问题 |采纳率94.4%1、设A单质为Ax,则方程式为:2xAH3=2Ax + 3xH2,压强增强了75%即(3x+2)/2x=1.75,解得x=4,即此反应的化学方程式:4AH3=A4 + 6H2
2、温度和密度完全相同时,单位体积内气体质量相同,假设为1的话,氢气,氧气,氮气的物质的量分别为:1/2、1/32、1/28,所以三种气体压强(p)的大小关系为:p(H2)>p(N2)>p(O2).
3、密度是氢气的14.5倍即相对分子质量是2*14.5=29,设一氧化碳的体积分数为x,则:
28x+32(1-x)=29,解得x=75%
4、原来活塞正好停留在离左端的1/4处,说明原来H2、O2总体积是N2的三倍,设氮气为1,则H2、O2总体积是3,反应后活塞恰好停在中间,说明反应后剩余气体体积为1(和氮气一样),所以体积减少2,根据方程式2H2+O2=2H2O可得参加反应氢气体积为2*2/3、氧气体积为2*1/3
当剩余1体积是H2时,反应前氢气和氧气的体积比=7:2;当剩余1体积是O2时,反应前氢气和氧气的体积比=4:51年前查看全部
- 太阳氢聚变启动是隧道效应?最近在看《千亿个太阳》里面对太阳聚变启动的原因归结为隧道效应?认为太阳的温度不足以启动聚变,是
太阳氢聚变启动是隧道效应?
最近在看《千亿个太阳》里面对太阳聚变启动的原因归结为隧道效应?认为太阳的温度不足以启动聚变,是这样的吗?另外,为什么电子不会坠入原子核?所有天体之所以没有坠入一点,是因为互相引力平衡吗? 华盛艺术1年前1
华盛艺术1年前1 -
 唐基柯德 共回答了19个问题
唐基柯德 共回答了19个问题 |采纳率68.4%最近在看《千亿个太阳》里面对太阳聚变启动的原因归结为隧道效应?认为太阳的温度不足以启动聚变,是这样的吗?是这样.另外,为什么电子不会坠入原子核?所有天体之所以没有坠入一点,是因为互相引力平衡吗?电子这种微观世界不了解,只说天体.人造卫星之所以绕地球转,而没有全坠到地球上,是因为它绕地球转的速度够快.同样,地球没有坠到太阳上,也是这个道理.不客气.1年前查看全部
- 只给出一条酶活性和温度关系的函数图像,最高点可以说是最适温度吗(不用说明PH吗)?
 jy30827621年前1
jy30827621年前1 -
 莫失莫忘夏 共回答了14个问题
莫失莫忘夏 共回答了14个问题 |采纳率92.9%最高点可以说是最适温度,那是不考虑PH值的情况下1年前查看全部
- 氮气和氢气以1:1的物质量混合后等分成2份分别冲入装有催化剂的真空密闭容器中在保持温度的条件下,反应相继达到平衡,A容器
氮气和氢气以1:1的物质量混合后等分成2份分别冲入装有催化剂的真空密闭容器中在保持温度的条件下,反应相继达到平衡,A容器中氢气的转化率是60%.B容器中氮气的转化率是10%.问A容器和B容器哪个体积大?
 yangsong121年前2
yangsong121年前2 -
 深色领带 共回答了17个问题
深色领带 共回答了17个问题 |采纳率94.1%A容器中氢气的转化率是60%,氮气的转化率就是20%,比B容器中氮气的转化率大,氮气和氢气的反应是一个体积减小的,则B容器体积大.1年前查看全部
- 一定温度下,在密闭容器中,发生反应:2NO2⇌2NO+O2,经过一段时间后,测得混合气体中NO2浓度为0.06mol/L
一定温度下,在密闭容器中,发生反应:2NO2⇌2NO+O2,经过一段时间后,测得混合气体中NO2浓度为0.06mol/L,O2的浓度为0.12mol/L,且各物质的浓度不再发生变化,求:
(1)NO2的起始浓度?
(2)此时NO2的分解率? zd1001年前1
zd1001年前1 -
 398088586 共回答了17个问题
398088586 共回答了17个问题 |采纳率100%解题思路:一定温度下,在密闭容器中,发生反应:2NO2⇌2NO+O2,经2min时间后,测得混合气中NO2浓度为0.06mol•L-1,O2的浓度为0.12mol•L-1,且各物质的浓度不再发生变化,说明反应达到平衡状态,依据化学平衡三段式列式计算.
(1)浓度c=[n/V]计算得到;
(2)二氧化氮转化率=[消耗量/起始量]×100%.一定温度下,在密闭容器中,发生反应:2NO2⇌2NO+O2,经2min时间后,测得混合气中NO2浓度为0.06mol•L-1,O2的浓度为0.12mol•L-1,且各物质的浓度不再发生变化,说明反应达到平衡状态,依据化学平衡三段式列式计算,设二氧化氮起始量为x;
2NO2⇌2NO+O2
起始量(mol/L) x 0 0
变化量(mol/L) 0.24 0.24 0.12
平衡量(mol/L)x-0.24 0.24 0.12
x-0.24=0.06,解得:x=0.30mol/L
(1)NO2的起始浓度=0.3 mol/L;
答:NO2的起始浓度0.3 mol/L;
(2)二氧化氮转化率=[消耗量/起始量]×100%=[0.24mol/L/0.3mol/L]×100%=80%;
答:此时NO2的转化率80%.点评:
本题考点: 化学平衡的计算.
考点点评: 本题考查了和平衡的计算应用,主要是转化率、反应速率概念的计算应用,掌握基础是关键,题目较简单.1年前查看全部
- 某温度下.A克溶质溶解在A克水中恰好饱和.此溶质在该温度下溶解度是多少
 ok4l1年前5
ok4l1年前5 -
 gzhzh987 共回答了18个问题
gzhzh987 共回答了18个问题 |采纳率88.9%溶解度是100克水中溶解的溶质的质量,既然A克溶质溶解在A克水中恰好饱和,那么100克水中最多能溶解100克溶质,即溶解度为100克1年前查看全部
- 一定温度下,取某物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半.给另一份溶液里加入原溶质的
一定温度下,取某物质的溶液mg,分成等质量的两份,将一份溶液恒温蒸发达饱和时,其质量减轻一半.给另一份溶液里加入原溶质的晶体(该溶质的晶体不含结晶水),当达到饱和时,所加晶体的质量恰好是此份溶液质量的1/8.求此温度下的物质的溶解度.
我们没有学过质量分数,可以使用别的方法吗?
比如用m质/m剂=s/100的解法 jeansmine1年前1
jeansmine1年前1 -
 紫夜V枫叶 共回答了14个问题
紫夜V枫叶 共回答了14个问题 |采纳率92.9%第一份溶液的操作可以理解成把纯水部分都蒸干了,剩下了饱和溶液.这样可知纯水部分质量为M/4.第二部分溶液的操作可以理解成向纯水里加溶质达到饱和.这样可知纯水部分里加质量为M/16的溶质即可饱和.
由此可以算出,饱和时水和溶质的比例为(M/4):(M/16) = 4:1.按照溶解度的定义可以算出溶解度是25g.1年前查看全部
- 太阳表面温度很高,就是钢铁碰到它也会变成汽,这样写好在哪里?
太阳表面温度很高,就是钢铁碰到它也会变成汽,这样写好在哪里?
为什么用“汽”,而不是“气”? lyc01891年前3
lyc01891年前3 -
 xx克 共回答了19个问题
xx克 共回答了19个问题 |采纳率89.5%运用举例子的说明方法形象地写出太阳表面温度很高
用"汽"是水蒸气,物理学泛称一切液体或固体受热变成的气体.而“气”只是单单有气体的意思1年前查看全部
- 氢氧化钙的溶解度为什么会随温度升高而降低?
 右脚枪1年前1
右脚枪1年前1 -
 cs008 共回答了12个问题
cs008 共回答了12个问题 |采纳率91.7%温度升高时 H2O的K值增大,由H2O电离出的H+也增大 由电离平衡可知,当H+的浓度增大时,由同离子效应,OH-的浓度要降低 即由氢氧化钙电离出来的OH-浓度要降低,所以更难溶解1年前查看全部
- 在压缩体积使气体液化时,怎样进行才快些和好些.比如控制温度等?
 亡子1年前2
亡子1年前2 -
 白绫无忧 共回答了20个问题
白绫无忧 共回答了20个问题 |采纳率95%一般都是低温液化的.因为很多气体单纯加压不能液化的,需要温度下降到临界温度以下.空气的主要成分氮气,临界温度是-147℃.加压的同时,使温度降到临界温度以下才能液化.1年前查看全部
- 某一元有机酸分子中的C、H、O的原子个数比为1:2:1,某钠盐含有一定质量的结晶水.当此钠盐加热到一定温度时,因失去结晶
某一元有机酸分子中的C、H、O的原子个数比为1:2:1,某钠盐含有一定质量的结晶水.当此钠盐加热到一定温度时,因失去结晶水,质量减少39.7%,将此含结晶水的钠盐0.57g与适量的硫酸在加热条件下反应,得0.298g Na2SO4.
(1)求此钠盐的式量及其含结晶水的数目.
(2)求此一元有机酸的式量并写出结构简式.答案是(1)136,3(2)60,CH3COOH求解题过程【最好解题过程能规范些= = winson_yu1年前2
winson_yu1年前2 -
 litnew 共回答了16个问题
litnew 共回答了16个问题 |采纳率87.5%设有机酸为CxH2xOx,则钠盐为NaCxH(2x-1)Ox.yH2O.
18y/(18y+22+30x)*100%=39.7%
化简得到:5.427y=5.955x+4.367
试算得到:y=3,x=2
NaC2H3O2.3H2O
C2H3O2H
CH3COOH
根据“此含结晶水的钠盐0.57g与适量的硫酸在加热条件下反应,得0.298g Na2SO4”该条件,可以知道含结晶水的钠盐的相对分子质量为:0.57/(0.298/142*2)=136.1年前查看全部
- 磷自燃是吸热还是放热?那物体温度升高,它的内能增加这句话是错的?放热,那内能不是应该减少么?
 21century1年前4
21century1年前4 -
 ziyun00 共回答了15个问题
ziyun00 共回答了15个问题 |采纳率86.7%开始吸热,一旦燃烧就是放热反应.1年前查看全部
- 想到1道关于温度的问题,在宇宙里,就是真空的状态,没有任何分子或其他什么东西,就是说没有“温度”这个概念了,因为温度的产
想到1道关于温度的问题,
在宇宙里,就是真空的状态,没有任何分子或其他什么东西,就是说没有“温度”这个概念了,因为温度的产生不就是由于分子运动而产生的吗?然后放一支正常的温度计,那么温度计示数是不变呢,还是上升,下降,或者起伏不定,还是有其他情况?
用一个玻璃罩罩住温度计,然后抽完空气,温度计的示数会如何变化? 斌仔_rr1年前4
斌仔_rr1年前4 -
 fjt44 共回答了13个问题
fjt44 共回答了13个问题 |采纳率100%宇宙不是绝对真空,是理想状态下的真空,是存在分子的,所以有温度.但一般温度极低,只有几K.由于气压几乎为零,一般温度计会因内外压力差而损坏.1年前查看全部
- 早上妈妈用热水给小明热奶,若一袋奶220ml,温度为10℃,将奶暖到40℃需要60℃的热水多少千克?
早上妈妈用热水给小明热奶,若一袋奶220ml,温度为10℃,将奶暖到40℃需要60℃的热水多少千克?
密度【奶】=1.05*10³kg/m³ margaret4121年前3
margaret4121年前3 -
 蓝天大海8 共回答了21个问题
蓝天大海8 共回答了21个问题 |采纳率81%m奶=ρV=1.05*10^3*220*10^-6=0.231kg
Q放=Q吸
cm水(to-t)=cm奶(t'-to')
m水(60-40)=0.231*(40-10)
m水=0.3465kg
所以需要60℃的热水0.3465千克
赞同0|评论1年前查看全部
- 水的熔点是0摄氏度,那么在该温度下水可能存在的状态是()a固态b液态c气态d三种状态都有可能
 njfast1年前1
njfast1年前1 -
 梁山198 共回答了20个问题
梁山198 共回答了20个问题 |采纳率90%d 是固.液.气共存态1年前查看全部
- 用活塞式抽气机,在温度不变的情况下,从容积为4L的玻璃瓶中抽气,每抽一次,瓶内气体的压强减小到原来的5/6,那么这台抽气
用活塞式抽气机,在温度不变的情况下,从容积为4L的玻璃瓶中抽气,每抽一次,瓶内气体的压强减小到原来的5/6,那么这台抽气机的气室容积为多少升?
 落雨划痕1年前1
落雨划痕1年前1 -
 amyloveamyhoho 共回答了17个问题
amyloveamyhoho 共回答了17个问题 |采纳率94.1%(4-v)/4=6/5
因为温度不变的情况下PV为一定值1年前查看全部
大家在问
- 1下列有机物发生的反应属于取代反应的是 ( )
- 2(2006•无锡)下列实验的基本操作中,错误的是( )
- 3默写古诗词中字面上含有“鸟”字的诗句
- 4文言文问题,速度解决,快的好的送50财富.速度啊啊啊啊 啊啊啊啊啊啊啊啊啊啊啊啊
- 5有两组人数相等的工人,工作效率比是7:8,工作时间比是12:11,求两组所完成的工作量的比
- 6If it was a scolding idea,we would have impaired our ability
- 7汉语为什么没有时态,或者有的语言一定要有时态.
- 8十五分七×()=()×八分之五=0.1×()=()×25=1
- 9开平碉楼 作文
- 10苯胺上有甲基或有硝基是怎么比较其碱性的大小,吸电子基团与推电子基团对其影响是怎么样的形式?
- 11甲乙两仓库,甲仓比乙仓多存粮10%,如果从甲仓调出20吨到乙仓,则甲乙两仓存粮相等,甲乙两仓原来各
- 12that s her dog 别给我说其他的东东!
- 13Children’sDay is on()1st
- 14帮我的作文取个有文学气息的名字.
- 15与你的伙伴谈成功的方法的英语口语对话
