鲍林的杂化轨道理论是什么?
 zhansuzhen6182022-10-04 11:39:541条回答
zhansuzhen6182022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 北岛大毛利 共回答了16个问题
北岛大毛利 共回答了16个问题 |采纳率93.8%- 电子运动不仅具有粒子性,同时还有波动性.而波又是可以叠加的.所以鲍林认为,碳原子和周围口个氢原子成键时,所使用的轨道不是原来的s轨道或p轨道,而是二者经混杂、叠加而成的“杂化轨道”,这种杂化轨道在能量和方向上...
- 1年前
相关推荐
- 原子得失电子的顺序判断原子得失电子顺序如何判定?是不是的电子的顺序按照Pauling(鲍林)原子能级图,而失电子按照由外
原子得失电子的顺序判断
原子得失电子顺序如何判定?
是不是的电子的顺序按照Pauling(鲍林)原子能级图,而失电子按照由外向内的顺序?
如果是那么Contton(科顿)原子轨道能级图又起到什么作用呢?
那要是忽略这些细节问题,-是不是失电子的顺序就是按4f 4d 4p 4s 3d 3p 3s 2d 2s 1s 的顺序失电子啊 ffdll1年前1
ffdll1年前1 -
 scarlett87 共回答了23个问题
scarlett87 共回答了23个问题 |采纳率91.3%能级图也是一个参考阿,具体还要分析,比如有时候会遇到半满状态,就像IB族元素外的电子排布.能级图只是一个参考,确实是最外的电子亚层先失电子,不过有时候比如3d5 4s2状态,3d比4s靠后,但是这时候再失电子就要失4s层的一个电子达到半满的稳定状态.个人认为能级图只是一个参考,具体问题要自己分析.1年前查看全部
- 鲍林研究电负性的细节问题.书上说,鲍林在研究电负性的时候规定F的电负性为4.0.但是一些电负性表(比如这个:鲍林标度电负
鲍林研究电负性的细节问题.
书上说,鲍林在研究电负性的时候规定F的电负性为4.0.但是一些电负性表(比如这个:鲍林标度电负性表),表中F的电负性为3.8.这是怎么回事?到底F的电负性应该是多少呢?

 向往漂流1年前1
向往漂流1年前1 -
 安妮爱 共回答了18个问题
安妮爱 共回答了18个问题 |采纳率94.4%我是想说……图中F的电负性是3.98啊~
至于Pauling当年研究电负性的时候,最初确实是F是4.0,O是3.5,没有两位小数,这张表格的数据我个人觉得应该是Pauling在之后又做了一些测定,修正和完善了部分数据,得出了这张更精确点的.
事实上,我们看到的很多电负性表格,除了F是4.0的那种注明Pauling电负性的以外,基本都是将很多人的很多版本的电负性数据求平均值.1年前查看全部
- Na和Ca的金属性比较,应该是Na的强吧?在鲍林的电负性表里Na是0.9而Ca是1.0,但是为什么在金属活泼性顺序中Ca
Na和Ca的金属性比较,应该是Na的强吧?在鲍林的电负性表里Na是0.9而Ca是1.0,但是为什么在金属活泼性顺序中Ca要比Na活泼呢?
 nihao122320021年前5
nihao122320021年前5 -
 Kitty_77 共回答了21个问题
Kitty_77 共回答了21个问题 |采纳率95.2%金属活动顺序是一个实验结果 很多与金属性不符合的
比如Sn和Pb 活动顺序Sn在Pb前面
但是根据周期表 Pb的金属性应该比Sn强
Ca与水反应的确比Na要缓慢 但是不是因为活泼性的原因
而是产物Ca(OH)2微溶 覆盖在Ca表面 阻止反应进行1年前查看全部
- 鲍林的杂化轨道理论是什么?
 uncle20081年前1
uncle20081年前1 -
 fangvic 共回答了21个问题
fangvic 共回答了21个问题 |采纳率90.5%价键理论对共价键的本质和特点做了有力的论证,但它把讨论的基础放在共用一对电子形成一个共价键上,在解释许多分子、原子的价键数目及分子空间结构时却遇到了困难.例如C原子的价电子是2s22p2,按电子排布规律,2个s电子是已配对的,只有2个p电子未成对,而许多含碳化合物中C都呈4价而不是2价,可以设想有1个s电子激发到p轨道去了.那么1个s轨道和3个p轨道都有不成对电子,可以形成4个共价键,但s和p的成键方向和能量应该是不同的.而实验证明:CH4分子中,4个C-H共价键是完全等同的,键长为114pm,键角为109.5°.BCl3,BeCl2,PCl3等许多分子也都有类似的情况.为了解释这些矛盾,1928年鲍林(Pauling)提出了杂化轨道概念,丰富和发展了的价键理论.他根据量子力学的观点提出:在同一个原子中,能量相近的不同类型的几个原子轨道在成键时,可以互相叠加重组,成为相同数目、能量相等的新轨道,这种新轨道叫杂化轨道.C原子中1个2s电子激发到2p后,1个2s轨道和3个2p轨道重新组合成4个sp3杂化轨道,它们再和4个H原子形成4个相同的C-H键,C位于正四面体中心,4个H位于四个顶角.
杂化轨道种类很多,如三氯化硼(BCl3)分子中B有sp2杂化轨道,即由1个s轨道和2个p轨道组合成3个sp2杂化轨道,在氯化铍(BeCl2)中有sp杂化轨道,在过渡金属化合物中还有d轨道参与的sp3d和sp3d2杂化轨道等.以上几例都是阐明了共价单键的性质,至于乙烯和乙炔分子中的双键和三键的形成,又提出了σ键和π键的概念.如把两个成键原子核间联线叫键轴,把原子轨道沿键轴方向“头碰头”的方式重叠成键,称为σ键.把原子轨道沿键轴方向“肩并肩”的方式重叠,称为π键.例如在乙烯( )分子中有碳碳双键(C=C),碳原子的激发态中2px,2py和2s形成sp2杂化轨道,这3个轨道能量相等,位于同一平面并互成120℃夹角,另外一个pz轨道未参与杂化,位于与平面垂直的方向上.碳碳双键中的sp2杂化如下所示.
这3个sp2杂化轨道中有2个轨道分别与2个H原子形成σ单键,还有1个sp2轨道则与另一个C的sp2轨道形成头对头的σ键,同时位于垂直方向的pz轨道则以肩并肩的方式形成了π键.也就是说碳碳双键是由一个σ键和一个π键组成,即双键中两个键是不等同的.π键原子轨道的重叠程度小于σ键,π键不稳定,容易断裂,所以含有双键的烯烃很容易发生加成反应,如乙烯(H2C=CH2)和氯(Cl2)反应生成氯乙烯(Cl—CH2—CH2—Cl).
乙炔分子(C2H2)中有碳碳三键(HC≡CH),激发态的C原子中2s和2px轨道形成sp杂化轨道.这两个能量相等的sp杂化轨道在同一直线上,其中之一与H原子形成σ单键,另外一个sp杂化轨道形成C原子之间的σ键,而未参与杂化的py与pz则垂直于x轴并互相垂直,它们以肩并肩的方式与另一个C的py,pz形成π键.即碳碳三键是由一个σ键和两个π键组成.这两个π键不同于σ键,轨道重叠也较少并不稳定,因而容易断开,所以含三键的炔烃也容易发生加成反应1年前查看全部
- 60年代美国化学家鲍林提出了一个经验规则:设含氧酸的化学式为HnROm,其中(m-n)为非羟基氧原子数,鲍林认为含氧酸的
60年代美国化学家鲍林提出了一个经验规则:设含氧酸的化学式为HnROm,其中(m-n)为非羟基氧原子数,鲍林认为含氧酸的强弱与非羟基氧原子数(m-n)的关系见表.
试回答下列问题:m-n 0 1 2 3 含氧酸强度 弱酸 中强 强 很强 实例 HClO H3PO4 HNO3 HClO4
(1)按此规则判断H3AsO4、H2CrO4、HMnO4酸性由弱到强的顺序为______.
(2)H3PO3和H3AsO3的形式一样,但酸性强弱相差很大.已知H3PO3为中强酸,H3AsO3
为弱酸,试推断H3PO3和H3AsO3的分子结构______.
(3)按此规则判断碳酸应属于______酸,与通常认为的碳酸的强度是否一致?______.其可能的原因是______. hengyang681年前0
hengyang681年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 60年代美国化学家鲍林提出一个经验规律:若含氧酸的化学式为HnROm,其中(m-n)为非羟基氧原子数
60年代美国化学家鲍林提出一个经验规律:若含氧酸的化学式为HnROm,其中(m-n)为非羟基氧原子数
(m-n的值越大,酸性越强)
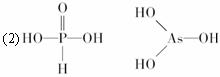
)H3PO3与H3AsO3的分子组成相似,但酸性强弱却相差很大,已知H3PO3为中强酸,H3AsO3为弱酸,试推断H3PO3和H3AsO3的结构式分别为
我也是这么写的,但是我就很纠结一个问题:P在H3PO3中显+3价,按照判断8电子稳定结构的方法(所显价态+最外层电子数=8)来判断,P满足8电子稳定结构,按理说形成3对共价键即可,为什么结构式里有5对共价键?晕了- -||||
图片
 苍野一尾马1年前1
苍野一尾马1年前1 -
 毛超 共回答了16个问题
毛超 共回答了16个问题 |采纳率100%有一个双键可以用配位键来表达1年前查看全部
- 鲍林提出的共振混合体能帮忙解释一下吗?
 雁儿0661年前1
雁儿0661年前1 -
 swllove83 共回答了23个问题
swllove83 共回答了23个问题 |采纳率73.9%电子分布在这种极端形式下“共振”,也就是说介于它们之间.所谓共振,就是说我们不能确定电子会在哪里(因为它们会乱跑),只能说“有一定概率”是这样,也有一定概率是那样,或者介于两者之间的过渡态.1年前查看全部
- 碳酸为什么是弱酸20世纪60年代美国化学家鲍林提出一个经验规则:设含氧酸化学式:HnROm,其中(m-n)为非羟基氧原子
碳酸为什么是弱酸
20世纪60年代美国化学家鲍林提出一个经验规则:设含氧酸化学式:HnROm,其中
(m-n)为非羟基氧原子数.鲍林认为含氧酸酸性与非羟基氧原子数(m-n)有如下关系:
m-n=0为弱酸,实例:HClO m-n=1为中强酸,实例:H3PO4 m-n=2为强酸,实例:HNO3 m-n=3为很强算,实例:HClO4
根据上述规则那么H2CO3应该是中强酸,但事实是碳酸是弱酸,问可能的原因是什么?
今天老师说是溶解度的问题 雷倒我 poolman881年前2
poolman881年前2 -
 shang3210072 共回答了20个问题
shang3210072 共回答了20个问题 |采纳率95%二氧化碳溶解于水以后,绝大多数以水合二氧化碳形式存在,生成碳酸并电离出氢离子的极少.我们平时计算的时候将溶解于水的二氧化碳都当成碳酸了,没有将其与水合二氧化碳相区别,所以会出现这样的偏差.实际上H2CO3应该是中强酸.1年前查看全部
- 鲍林五个规则请高手分五条给出答案~~~非常感谢
 8ll98481年前1
8ll98481年前1 -
 流御 共回答了18个问题
流御 共回答了18个问题 |采纳率88.9%按照晶体结构的局部电中性要求,确定离子晶体中某一离子周围带异号电荷的离子数的规则.20世纪30年代初,L.C.鲍林提出以下五项规则:
第一规则 在每一正离子周围形成一个负离子配位多面体(见离子配位多面体),正、负离子的距离取决于半径和,正离子的配位数取决于正、负离子的半径比.
第二规则(电价规则) 在一个稳定的离子晶体结构中,每一负离子的电价ζ等于或近似等于诸邻接正离子至该负离子的静电键强si的总和,即,称为电价规则.式中正离子 i的静电键强si定义为si=wi/vi,wi和vi分别是正离子 i的电荷数和配位数.例如,氯化钠NaCl中每个Na+与6个Cl-相连,即Na+的配位数为6,Na+的电荷数是1,因此 Na+-Cl-的静电键强是1/6.每个Cl-与6个Na+-Cl-离子键相连,可验证诸键强和(6×1/6)恰等于负离子的电荷数.电价规则主要规定了公用同一配位多面体顶点的多面体数.
第三规则 在配位结构中,公用多面体的棱,特别是公用多面体的面将会降低结构的稳定性.对于高电价和低配位数的正离子,这一效应特别显著.
第四规则 在含有一种以上正离子的晶体中,电价大、配位数低的那些正离子倾向于不公用多面体的点、棱、面等几何元素.
第五规则 晶体中实质不同的组成者的种数一般趋于最小限度.
鲍林规则高度概括了离子晶体中配位多面体及其连接方式的规律,对阐明晶体化学、地球化学领域涉及的复杂离子化合物(如硅铝酸盐等)的结构有重要的指导意义.
70年代,以I.D.布朗为代表的化学家提出的键价法以更广泛的精密实测晶体结构信息为基础,已将鲍林的电价规律发展到定量化的阶段.1年前查看全部
- 1932年美国化学家鲍林首先提出电负性的概念.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的1
1932年美国化学家鲍林首先提出电负性的概念.电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
请仔细分析,回答下列有关问题;元素 H Li Be B C N O F 电负性 2.1 1.0 1.5 2.0 2.5 3.0 3.5 4.0 元素 Na Mg Al Si P S Cl K 电负性 0.9 1.2 1.5 1.7 2.1 2.3 3.0 0.8
(1)预测周期表中电负性最大的元素应为______;估计钙元素的电负性的取值范围:______<X<______.
(2)根据表中的所给数据分析,同主族内的不同元素X的值变化______;简述元素电负性X的大小与元素金属性、非金属性之间的关系______.
(3)经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键.试推断AlBr3中形成的化学键的类型为______,其理由是______. 华丽丽的宝蓝色1年前1
华丽丽的宝蓝色1年前1 -
 xiaobdian 共回答了25个问题
xiaobdian 共回答了25个问题 |采纳率88%解题思路:(1)电负性表示对键合电子的吸引力,电负性越大对键合电子吸引力越大,所以非金属性越强电负性越强,故电负性最强的物质在周期表的右上角(零族元素除外);
由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,非金属性越强电负性越强,故金属性越强电负性越小,钙元素的电负性比K元素大,但小于Li元素的电负性;
(2)由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,故非金属性越强电负性越大,金属性越强电负性越小;
(3)AlCl3中两电负性之差为1.5,Br元素的电负性小于Cl元素电负性,AlBr3中两电负性之差小于1.5.(1)电负性表示对键合电子的吸引力,电负性越大对键合电子吸引力越大,所以非金属性越强电负性越强,故电负性最强的物质在周期表的右上角为F元素;
由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,非金属性越强电负性越强,故金属性越强电负性越小,故钙元素的电负性比K元素大,但小于Li元素的电负性,即0.8<X(Ca)<1,
故答案为:F,0.8、1;
(2)由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,故非金属性越强电负性越大,金属性越强电负性越小,
故答案为:自上而下电负性降低,非金属性越强电负性越大,金属性越强电负性越小;
(3)AlCl3中两电负性之差为1.5,Br元素的电负性小于Cl元素电负性,AlBr3中两电负性之差小于1.5,故AlBr3中化学键为共价键,
故答案为:共价键,AlCl3中两电负性之差为1.5,Br元素的电负性小于Cl元素电负性,AlBr3中两电负性之差小于1.5.点评:
本题考点: 元素电离能、电负性的含义及应用.
考点点评: 考查电负性及与金属性非金属性的关系等,难度中等,清楚主族元素电负性的递变规律是解题关键.1年前查看全部
- 下列叙述不正确的是( )A.“绿色荧光蛋白质”是不可降解的高分子化合物,其水溶液有丁达尔效应B.化学家鲍林提出了氢键理
下列叙述不正确的是( )
A.“绿色荧光蛋白质”是不可降解的高分子化合物,其水溶液有丁达尔效应
B.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础
C.纤维素属于糖类,醋酸纤维、硝化纤维属于酯类
D.将废动植物油脂经反应改性制成“生物柴油”,代替柴油作为内燃机燃料的做法符合“绿色化学”的理念 kjxl20071年前1
kjxl20071年前1 -
 liai_hua 共回答了14个问题
liai_hua 共回答了14个问题 |采纳率85.7%解题思路:A.“绿色荧光蛋白质”是蛋白质;
B.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型;
C.糖类包括单糖、二糖、多糖三类.如葡萄糖属于单糖,蔗糖属于二糖,淀粉和纤维素属于多糖,酸(羧酸或无机含氧酸)与醇起反应生成的一类有机化合物叫做酯;
D.绿色化学要求原料物质中所有的原子完全被利用且全部转入期望的产品中,原子的利用率100%,废动植物油脂经反应改性制成“生物柴油”,可实现变废为宝.A.“绿色荧光蛋白质”是蛋白质,蛋白质能水解,所以是可降解的高分子化合物,故A错误;
B.化学家鲍林提出了氢键理论和蛋白质分子的螺旋结构模型,为DNA分子双螺旋结构模型的提出奠定了基础,故B正确;
C.纤维素属于糖类,醋酸纤维、硝化纤维属于酯类,故C正确;
D.将废动植物油脂经反应改性制成“生物柴油”,代替柴油作为内燃机燃料,实现变废为宝,符合“绿色化学”的理念,故D正确.
故选A.点评:
本题考点: 氨基酸、蛋白质的结构和性质特点;纤维素的性质和用途.
考点点评: 本题考查糖类蛋白质油脂的性质,注意酸(羧酸或无机含氧酸)与醇起反应生成的一类有机化合物叫做酯.1年前查看全部
大家在问
- 1让梦飞翔 作文
- 2当X等于二分之三时,求3(x+5)(x-3)-5(x-2)(x+3)的值,
- 3某些食品包装袋中常放入一小袋生石灰(CaO)做干燥剂,该物质属于 [ ]
- 4公元前770年东周建立,为什么书上说是春秋时代
- 5四边形ABCD的边AB在x轴上,点D在y轴上,AD=BC=4,A(-2,0),C(5,2√3)
- 6解方程36÷3x+(36-36÷3x)÷9=6
- 7请问当有重力做功时Gh=FS么
- 8形容历经坎坷苦难的成语
- 9如图,底下那几行的英文是什么意思?
- 10(2013•牡丹江一模)如图,在四棱锥P-ABCD中,底面ABCD为菱形,其中PA=PD=AD=2,∠BAD=60°,Q
- 11当我们不得不去收起遗像的时候,海鸥们像炸了营似的朝遗像扑过来,这句话把什么比作了什么
- 12金属离子 或 铵根离子一样的 物质 是不不反应
- 131.若函数F(x)=-1/b乘以e的ax次方的图象在X=0处的切线与单位圆(以原点为圆心,1为半径)相离,则点P(a,b
- 14如图,ab,ac相交于点e,且e为cd的中点,∠bac=∠abd,ac=df,ab=af.求证ad平分∠baf.如图,△
- 15CD是线段AB上两点,已知AC:CD:DB=2:3:4,点E,F分别是AC,BD的中点,且EF=10cm,求AB的长
