臭氧对人有什么副作用
 极度燃烧2022-10-04 11:39:541条回答
极度燃烧2022-10-04 11:39:541条回答
已提交,审核后显示!提交回复
共1条回复
 zoey44655429 共回答了16个问题
zoey44655429 共回答了16个问题 |采纳率87.5%- 是一种强氧化剂,由三个氧原子共价组成,对人的作用嘛,少量的对人有一定兴奋作用,太多了对人的组织会造成损害.雷雨后空气中会有少量臭氧,人会感觉空气很清新,很兴奋! 希望能帮到你
- 1年前
相关推荐
- 大气底层臭氧量少的原因是什么
 SSGF1年前2
SSGF1年前2 -
 我贱吗 共回答了14个问题
我贱吗 共回答了14个问题 |采纳率92.9%这个要从臭氧的生成说起,大气中的臭氧生成的常规途径是通过紫外线照射使O2分解得到游离氧,然后O2结合生成O3,也就是臭氧,但是臭氧本身能够吸收排除大量紫外线,所以在大气上层产生臭氧层后,到达地表的紫外线很少,也就无法使低层大气生成臭氧了.近代,由于部分制冷剂(如氟利昂等)使用,导致大气污染和大气高层臭氧空洞,还有空气中一氧化氮等污染物的催化,也导致地表臭氧急剧增加的事件,比如光化学污染等.1年前查看全部
- 氧气和臭氧从组成上看——相同,但是由于构成他们的——不同,因此化学性质不同.快回答!
 quanweixudan1年前4
quanweixudan1年前4 -
 素素子 共回答了18个问题
素素子 共回答了18个问题 |采纳率88.9%含有的元素种类相同,
分子结构不同.1年前查看全部
- 构成物质的微粒有什么 什么 和什么 化学变化中的最小微粒是什么 臭氧 和金刚石的化学方程式分别是什么...
构成物质的微粒有什么 什么 和什么 化学变化中的最小微粒是什么 臭氧 和金刚石的化学方程式分别是什么...
构成物质的微粒有什么 什么 和什么
化学变化中的最小微粒是什么
臭氧 和金刚石的化学方程式分别是什么
3SO7(右上角有一个2-)
中的数字分别表示的意义 867103541年前4
867103541年前4 -
 crazy5880 共回答了18个问题
crazy5880 共回答了18个问题 |采纳率88.9%1离子 原子 分子
2 化学变化最小微粒是分子
3 臭氧 O3 金刚石是C
4 由1个S原子 7个氧原子构成的酸根离子带两个单位的负电荷.1年前查看全部
- 臭氧空洞、酸雨、汽车尾气、工业废气看到这样的景象你有什么感想?150字以上!
臭氧空洞、酸雨、汽车尾气、工业废气看到这样的景象你有什么感想?150字以上!
急用!急用!速回!速回! taoran20001年前1
taoran20001年前1 -
 chzw123456 共回答了15个问题
chzw123456 共回答了15个问题 |采纳率93.3%大气污染及其防治
自然界清新、洁净的空气,使人心旷神怡、精神振奋.但是随着工业的迅速发展和人口急剧增长,大量燃烧煤炭、石油所产生的化学物质以废气和烟尘等形式排放到大气中,超过了大气环境的容许量,给人类的生活、生产和身体健康带来有害影响.
据统计,全世界每年排入大气的污染物约有6亿多吨.污染源主要是以下三方面:
生活污染源:如家庭、商业服务部门等燃煤排放的烟尘和废气.
交通污染源:如汽车、火车、飞机、船舶等排放的废气.
工业污染源:如发电厂、钢铁厂、水泥厂、氮肥厂、烧碱厂及其它各类化工厂排放的废气和粉尘.
主要大气污染物有两大类:
气态污染物(如二氧化硫、硫化氢、一氧化碳、二氧化碳、二氧化氮、氨、氯气等)
颗粒态污染物(如烟、雾、粉尘)
大气污染会对人类和其它生物造成危害.本世纪以来,不断发生的公害,使人们认识到保护大气不受污染的重要性.如1952年12月5~8日英国伦敦大雾乃为烧煤所产生的烟尘和烟雾散发不出去,造成千万人呼吸道感染,4天中死亡达4000多人.1991年日本四日市石油冶炼和工业燃油所排放的工业废气,使大气中的二氧化硫的浓度超过标准5~6倍,致使全市哮喘病发作.
我国政府十分重视环境保护工作,制订了防治大气污染的法规.例如“大气污染防治法”,“大气环境质量标准”等.人类只有一个地球,应该珍惜它.在不断发展生产的同时学会保护大气不受污染,保护地球环境,以使我们生活的大气永远洁净,天空永远蔚蓝.1年前查看全部
- H的右下角有一个小3,和臭氧的写法差不多,就是把O换成H,这种物质叫什么?
 popzlg1年前1
popzlg1年前1 -
 cleo19750721 共回答了14个问题
cleo19750721 共回答了14个问题 |采纳率92.9%三原子氢(H3)
可以看成是一个氢气分子与一个氢离子的加合物,
H3+是科学家在宇宙深处发现的一种物质
H3+离子是由H2结合一个质子(即H+)构成,可视为(H2.H+)-离子络合物
H3分子是由H2结合一个氢原子(H)而形成,和臭氧O3一样,由O2和一个氧原子结合构成,可写为(O2.O),H3分子亦可写为(H2.H),有三中心三电子键.它非常不稳定,存在时间为微秒级,很快转化为氢气.其分子构型为V型.
是一种由三个氢原子构成的不稳定分子.
这种中性的分子可以在低压放电管中制备.1年前查看全部
- 物质的量内容疑难解答为什么氧原子的微粒个数等于2倍的氧气的微粒个数等于3倍的臭氧的微粒个数 @1mol的H2SO4 含有
物质的量内容疑难解答
为什么氧原子的微粒个数等于2倍的氧气的微粒个数等于3倍的臭氧的微粒个数 @1mol的H2SO4 含有几摩尔的O原子 pollux1年前2
pollux1年前2 -
 linliucandy 共回答了24个问题
linliucandy 共回答了24个问题 |采纳率87.5%解析:假设有1molO2,因为每个氧气分子含有两个氧原子,所以每有1mol氧气,便有2mol氧原子.又因为N=nNA(NA指阿伏伽德罗常数),所以氧原子微粒的个数等于氧气微粒个数的二倍.
每一个H2SO4分子含有4个氧原子,所以1mol的H2SO4含有4mol的氧原子.1年前查看全部
- 氧族元素3一定体积的氧气放电后有百分之六十转化为臭氧,放电后所得混合气体对氢气的相对密度为多少?
 opencn1年前1
opencn1年前1 -
 rainbownsdf 共回答了13个问题
rainbownsdf 共回答了13个问题 |采纳率84.6%设有100mol的氧气其中有60mol转化为臭氧,由3O2=2O3知臭氧有40mol所以现在总体积就是80mol所以其混合物的摩尔质量是质量除以摩尔数,就是M=m/n=100*32/80=40而氢气摩尔质量为2,所以相对密度是201年前查看全部
- 呼吸作用的定义是:细胞内的有机物与氧反应.为什么不是“氧气”?难不成有机物还会和臭氧反应?
呼吸作用的定义是:细胞内的有机物与氧反应.为什么不是“氧气”?难不成有机物还会和臭氧反应?
可能是我对“氧”的理解有误,那么“氧”指的是什么? 非典型dd1年前2
非典型dd1年前2 -
 灵清竹 共回答了18个问题
灵清竹 共回答了18个问题 |采纳率94.4%定义中的氧除了氧气外还包括其他具有氧化性,即能接受电子的物质.这类物质统称电子受体.
并且有机物也不是直接与电子受体反应,有机物脱下的电子经过呼吸链的传递,沿途将能量用于合成ATP后才与电子受体反应.
一般生物有氧呼吸作用的电子受体是氧,产物是二氧化碳和水.
反硝化细菌呼吸作用的电子受体是亚硝酸盐,产物是二氧化碳和氮气.1年前查看全部
- 一写出下列物质的符号表达式氯酸钾高锰酸钾过氧化氢硫磺臭氧磷酸二写出下列符号的意义SO4 2- CO
一写出下列物质的符号表达式
氯酸钾
高锰酸钾
过氧化氢
硫磺
臭氧
磷酸
二写出下列符号的意义
SO4 2- CO3 2- 2NO SO2 congjue1年前1
congjue1年前1 -
 sxh2 共回答了21个问题
sxh2 共回答了21个问题 |采纳率81%KClO3(氯酸钾)
KMnO4(高锰酸钾)
H2O2(过氧化氢)
S(硫磺)
O3(臭氧)
H3PO4(磷酸)
符号分别代表,硫酸根,碳酸根,2个一氧化氮分子,二氧化硫分子1年前查看全部
- 地球正面临哪些危机?水,垃圾,雾霾,臭氧空洞,全球变暖,还有呢?
 lvdream1年前1
lvdream1年前1 -
 wangfei2686 共回答了19个问题
wangfei2686 共回答了19个问题 |采纳率89.5%能源危机、外太空威胁(小行星带的行星由于地球的引力有时会像地球运移、彗星轨道与地球运行轨道可能相交)、人口过多、太阳膨胀1年前查看全部
- 求教.A.氧气和液氧 B.氧气和臭氧 C.CO2和CO D.冰和水 E.过氧化氢和水属于单质:属于化合物:属于纯净物:属
求教.
A.氧气和液氧 B.氧气和臭氧 C.CO2和CO D.冰和水 E.过氧化氢和水
属于单质:
属于化合物:
属于纯净物:
属于混合物:
属于氧化物:
均填序号 carriezlove1年前1
carriezlove1年前1 -
 公共dd01 共回答了13个问题
公共dd01 共回答了13个问题 |采纳率84.6%单质:A
化合物:E
纯净物:D
混合物:B
氧化物:C1年前查看全部
- 臭氧的结构式的解释!说明氧原子最外层电子是否达8电子结构!
 yuantianyou1年前2
yuantianyou1年前2 -
 549879277 共回答了19个问题
549879277 共回答了19个问题 |采纳率94.7%三个氧都是以单键结合,并未达到8电子结构,外面形成了一个3电子π键1年前查看全部
- 下列关于人类活动队气候的消极影响的叙述,不正确的有 ①人类食用冰箱、冰柜排放的废气导致“臭氧空洞
下列关于人类活动队气候的消极影响的叙述,不正确的有 ①人类食用冰箱、冰柜排放的废气导致“臭氧空洞
”
②砍伐森林导致全球变暖
③燃烧煤炭、石油导致酸雨危害
④植树种草导致洪涝灾害
A、①②③ B、②③④ C、①③④ D、④
 悟空他姐1年前1
悟空他姐1年前1 -
 cooper1260 共回答了21个问题
cooper1260 共回答了21个问题 |采纳率95.2%A1年前查看全部
- “水立方”是2008年北京奥运会的主游泳馆.为确保“水立方”的水质达到国际泳联最新卫生标准,泳池的水将采用砂滤→臭氧→活
“水立方”是2008年北京奥运会的主游泳馆.为确保“水立方”的水质达到国际泳联最新卫生标准,泳池的水将采用砂滤→臭氧→活性炭等净水工艺,其中砂滤的作用是______,用活性炭净水是利用活性炭的______性.
“鸟巢”是使用钢铁建造的主体育场,为防止钢铁结构受到腐蚀,进行了防锈处理.
根据你所学过的知识谈谈防止钢铁生锈常采用的措施:____________.(答出一点即可) 小结巴33921年前1
小结巴33921年前1 -
 银笛书生 共回答了21个问题
银笛书生 共回答了21个问题 |采纳率81%泳池的水将采用砂滤→臭氧→活性炭等净水工艺,其中砂滤的作用是把不溶于水的物质除去,用活性炭净水是利用活性炭的吸附性.故填:除去杂质;吸附.
在金属表面刷油漆(镀金属、保护表面的洁净和干燥)可以防止金属生锈.故填:刷油漆;镀金属、保护表面的洁净和干燥.1年前查看全部
- 臭氧在雷电过后回反应生成氧气,那么氧气又如何生成臭氧
 闷声驴1年前1
闷声驴1年前1 -
 rr小K 共回答了17个问题
rr小K 共回答了17个问题 |采纳率88.2%好象你说错了吧!氧气在闪电时生成臭氧!1年前查看全部
- 高一化学题:在体积相同的两个密闭容器中分别充满氧气和臭氧.
高一化学题:在体积相同的两个密闭容器中分别充满氧气和臭氧.
当这两个容器的温度和气体密度相等时,下列说法正确的是?A两种气体的压强相等B氧气比臭氧的质量小C两种气体的分子数相等C两种气体氧原子数相等 拜托会的都解释解释啊!谢谢!每个选项分析下.重谢!我现在在预习高一
 倚楼听风Y1年前1
倚楼听风Y1年前1 -
 jasmine521521 共回答了23个问题
jasmine521521 共回答了23个问题 |采纳率82.6%选D.
密度相等体积相等可推出氧气和臭氧的质量相等,排除B.
又因为氧气和臭氧的摩尔质量不等,由n=m/M得它们的物质的量不等,即分子个数不等,排除C.
又因为在等体同温的条件下,压强与物质的量成正比,所以压强不等,排除A.
其实我们可以把两容器装的都看成是氧原子,由两容器所装气体的质量相等,氧原子的质量一定,可得氧原子的个数相等.1年前查看全部
- 检测臭氧时,1PPM等于多少mg?
检测臭氧时,1PPM等于多少mg?
空气中的吗 showbow1231年前3
showbow1231年前3 -
 iqaqs 共回答了14个问题
iqaqs 共回答了14个问题 |采纳率92.9%1ppm=1mg/kg=0.0001%
ppm-
abbr.百万分率,百万分之…(parts per million)
如果是要检测空气中的臭氧,那就是臭氧占空气的比值.1年前查看全部
- 硫 臭氧 反应硫单质与臭氧能发生反应吗 生成什么
 mikychan1年前4
mikychan1年前4 -
 xmyzxx 共回答了28个问题
xmyzxx 共回答了28个问题 |采纳率89.3%可以的,反应很剧烈
生成三氧化硫,而氧气和硫反应只能生成二氧化硫,这是因为氧气的氧化性不强,没有能力直接将硫氧化成+6价,臭氧的氧化性强的多
S+O3==SO3
S+O3+H2O==H2SO41年前查看全部
- 人类的生命之伞——臭氧层在地球上空20至30千米的大气同温层中,聚集着占自然界总量90%的臭氧,这就构成了大气臭氧层。虽
人类的生命之伞——臭氧层
在地球上空20至30千米的大气同温层中,聚集着占自然界总量90%的臭氧,这就构成了大气臭氧层。虽然其中臭氧的质量只占整个大气层的1/1000000,但它却能吸收来自太阳的99%的紫外线,使地球免遭太阳紫外线过强的辐射。正是臭氧层这一“生命之伞”,庇护着人类及地球的所有生灵!
1985年5月,英国科学家首次发现南极上空出现了臭氧层“空洞”,后来英国的“云雨7号”卫星探测出这个空洞的面积大如美国。科学家们还发现,北极、欧洲的上空,臭氧层也在受到侵蚀,形成臭氧稀薄区域。从全球来看,大气中的臭氧含量正在逐年减少。
致使大气中臭氧含量减少的原因很多,而人类生产和生活所产生的CFC类物质进入大气层,则是造成臭氧含量减少、臭氧层被破坏的主要原因。CFC类物质主要是各类气溶胶、制冷剂、除臭剂所释放的氟氯烃,如广泛使用于冰箱、空调器的氟利昂、氟氯甲烷等。这些化合物在大气低空中很稳定,经过漫长的时日,顽强地飘到同温层,经阳光中的紫外线照射,发生光化反应,释放由化学反应能力很强的自由氯原子。而一个自由氯原子就可以借助连锁反应破坏10万个臭氧分子!
臭氧层被破坏的后果是极其严重的。科学家研究表明,大气中臭氧每减少2.5%,就会给世界带来47万个皮肤癌患者。由臭氧层被破坏所带来的地球环境的变化,会造成农作物的大幅度减产。不仅如此,臭氧层被破坏还会使全球气候变暖,雨量增多,加速极地冰川的融化,海平面上升,导致大片海滨地区被淹没。为此,科学家们呼吁世界各国必须加强合作,采取措施,最大限度地避免臭氧层再遭进一步破坏,以保护人类自身。
1.为什么称臭氧层为“生命之伞”?
答:_______________________________________________________________________
_______________________________________________________________________________
2.臭氧层“空洞”在文中指什么?
答:_______________________________________________________________________
_______________________________________________________________________________
3.为什么说CFC类物质是造成臭氧含量减少、臭氧层被破坏的主要原因?请简要回答。
答:_______________________________________________________________________
_______________________________________________________________________________
4.臭氧层被破坏,对人类生存有哪些危害?请简要回答。
答:_______________________________________________________________________
_______________________________________________________________________________
可以只回答第5题
5.本文使用的说明方法有哪几种,谈谈这些的作用 ynhyp1年前2
ynhyp1年前2 -
 在网精灵 共回答了17个问题
在网精灵 共回答了17个问题 |采纳率88.2%1、能吸收来自太阳的99%的紫外线,使地球免遭太阳紫外线过强的辐射。
2、臭氧层受到侵蚀,形成臭氧稀薄区域
3、经阳光中的紫外线照射,发生光化反应,释放由化学反应能力很强的自由氯原子。而一个自由氯原子就可以借助连锁反应破坏10万个臭氧分子!
4、皮肤癌患者 由臭氧层被破坏所带来的地球环境的变化,会造成农作物的大幅度减产 气候变暖,雨量增多,加速极地冰川的融化,海平...1年前查看全部
- 打雷放电时,空气中极少量的氧气会转变为臭氧,这个反应可以表示为氧气 臭氧.下列说法正确的是 [ &
打雷放电时,空气中极少量的氧气会转变为臭氧,这个反应可以表示为氧气  臭氧.下列说法正确的是 [ ]
臭氧.下列说法正确的是 [ ]A.这是物理变化
B.这是分解反应
C.这是化合反应
D.这是化学变化 fang8410201年前1
fang8410201年前1 -
 wei5244360 共回答了21个问题
wei5244360 共回答了21个问题 |采纳率95.2%D1年前查看全部
- 紫外线怎么把氧气转化成臭氧
 鸿翼1年前5
鸿翼1年前5 -
 skyfox_g 共回答了22个问题
skyfox_g 共回答了22个问题 |采纳率90.9%臭氧可以吸收紫外线.
氧气在电子流、质子流、短波辐射的作用下可以转化为臭氧.在雷雨天,空气中的氧在电火花的作用下,可部分转化为臭氧.1年前查看全部
- 求臭氧的Lewis结构式你的意思是?O=O-O可以肯定 O2 是O=O 那么O3是 O=O-O的话 肯定有配位键哪个是配
求臭氧的Lewis结构式
你的意思是?
O=O-O
可以肯定 O2 是O=O
那么O3是 O=O-O的话 肯定有配位键
哪个是配位键? skinwhite1年前1
skinwhite1年前1 -
 方舟xt 共回答了16个问题
方舟xt 共回答了16个问题 |采纳率87.5%臭氧分子结构呈V形
口口口口口口口口口口口口..
口口口口口口口口口口口口O
口口口口口口口口口口口 /..
口口口口口口口口口口 / 口口
口口口口口口口口口:O.口口口.O:
口口口口口口口口口 ..口口口 ..
这三个氧原子采取sp2杂化,中心氧原子1个sp2杂化轨道为孤对电子占据,另外2个未成对电子则分别与两旁氧原子的sp2杂化轨道上未成对电子形成2个(sp2-sp3)希格玛键.中心氧原子未参与杂化的p轨道上的一对电子,与两旁氧原子未参与杂化的p轨道上各1个原子互相平行,彼此重叠形成垂直的三中心四电子大π键(就是中间那四个点).这个π键是离域π键,不固定在两原子之间.1年前查看全部
- 为什么在南极上空出现了臭氧空洞,而不是在人口密集地区的上空呢
 lookwl1年前1
lookwl1年前1 -
 月儿挂天上 共回答了20个问题
月儿挂天上 共回答了20个问题 |采纳率85%经过跟踪、监测,科学家们找到了臭氧空洞的成因:一种大量用作制冷剂、喷雾剂、发泡剂等化工制剂的氟氯烃是导致臭氧减少的“罪魁祸首”.另外,寒冷也是臭氧层变薄的关键,这就是为什么首先在地球南北极最冷地区出现臭氧空洞的原因了.1年前查看全部
- 臭氧和氧气化学性质不同的原因是什么啊?学霸帮帮忙!
 chenxideng1年前6
chenxideng1年前6 -
 悠悠照我心 共回答了1个问题
悠悠照我心 共回答了1个问题 |采纳率电子排布不同亲,对我的回答满意的话,就给个好评吧。如果还有不清楚的地方,可以跟我继续交流哦。分子构成不同说错了也就是成的分子不同吧?感谢你的细致回答,我的问题已经解决了,多谢大家的帮助哦!嗯,构成的分子不同就是分子的构成不同...1年前查看全部
- (2012•厦门二模)碳在氧气或臭氧中燃烧的能量变化如图.下列说法不正确的是( )
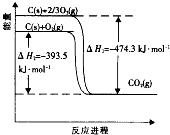 (2012•厦门二模)碳在氧气或臭氧中燃烧的能量变化如图.下列说法不正确的是( )
(2012•厦门二模)碳在氧气或臭氧中燃烧的能量变化如图.下列说法不正确的是( )
A.3O2(g)=2O3(g)△H=+242.4kJ•mol-1
B.氧气比臭氧稳定,大气中臭氧层易被破坏
C.若火电厂用臭氧燃烧煤有利于获得更多的电能
D.断裂l mol O2(g)中的共价键吸收的能量比形成1 molCO2(g)中的共价键放出的能量少 xlifeng1631年前1
xlifeng1631年前1 -
 一只特立独行的波 共回答了19个问题
一只特立独行的波 共回答了19个问题 |采纳率94.7%解题思路:由能量变化图可知①C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1,②C(s)+[2/3]O3(g)=CO2(g)△H=-474.3kJ•mol-1,由盖斯定律将①×3-②×3可得③3O2(g)=2O3(g)△H=+242.4kJ•mol-1,以此解答该题.由能量变化图可知①C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1,②C(s)+[2/3]O3(g)=CO2(g)△H=-474.3kJ•mol-1,由盖斯定律将①×3-②×3可得③3O2(g)=2O3(g)△H=+242.4kJ•mol-1,
A.由以上分析可知3O2(g)=2O3(g)△H=+242.4kJ•mol-1,故A正确;
B.由A可知O2的能量比O3低,物质的能量越低越稳定,故B正确;
C.由热化学方程式可知碳和臭氧反应生成等量的二氧化碳,放出的热量更多,但臭氧对人体健康不利,不能用于工业生成,且生成臭氧需要吸收能量,如以氧气为原料生成臭氧,则放热的热量相等,故C错误;
D.由C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-1可知,断裂l mol O2(g)中的共价键吸收的能量比形成1 molCO2(g)中的共价键放出的能量少,故D正确.
故选C.点评:
本题考点: 反应热和焓变.
考点点评: 本题考查反应热与焓变,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握图象,根据图象书写热化学方程式,为解答该题的关键,难度中等.1年前查看全部
- 英语翻译1.臭氧发生系统:采用世界最先进的非玻璃放电技术产生臭氧,在借鉴国外先进机型的基础上,采用德国安斯罗斯发生腔产生
英语翻译
1.臭氧发生系统:采用世界最先进的非玻璃放电技术产生臭氧,在借鉴国外先进机型的基础上,采用德国安斯罗斯发生腔产生臭氧,使产生的臭氧浓度更加准确,对于发生器的寿命可延长为20万次以上.
2.浓度调节系统:流量检测单元(PLC)及控制程序软件由美国霍尼维尔公司生产,触摸屏操作,可快速,简便的根据治疗需要任意调节浓度(0—80mg/L连续可调),达到时时调节,时时显示,时时获取臭氧的目的.
3.数字显示系统:可使操作者更好的观察与调节浓度,确保准确无误.
4.双取气装置(弹压/自动):采用两种取气方式,可确保操作者在不同情况下快速获取臭氧气体.弹压式;轻压取气阀门,即可获取O3气体,取气后阀门自动关闭,此方式快捷方便,不会造成取气时遗漏气体,以免造成对医务人员呼吸道的刺激等污染.
5.臭氧回收分解装置:使残余的O3气体迅速转化为纯氧气,通过排气口释放,确保工作环境清晰.
6.管路压力调节装置:本仪器对气源的气压无特定要求,只需打开就可,仪器内会自动调节气压,可使医院使用任何纯氧气源.
7.自动待机系统:本仪器的结构为仪器与发生器分离式电源,仪器本身可连续性长时间待机(≥48小时),对发生器无任何耗损,保证了发生器的寿命更长久.
8.散热冷却系统:通过散热装置避免高压管温度升高,影响臭氧浓度的数值准确度,更保证了仪器内部各原器件的寿命 jakenba1年前1
jakenba1年前1 -
 柒匹狼 共回答了15个问题
柒匹狼 共回答了15个问题 |采纳率86.7%1. The ozone generating system: adopting the most advanced technologies to produce the glass discharge ozone in the reference of foreign advanced type, on the basis of adopting Germany Ann, Ross happen cavity, make produce generated ozone concentrations of ozone generator is more accurate, for life can be extended to 20 million times above.
2. Concentration regulation system: flow measuring unit (PLC) and control procedures software by American honeywell Nashville, company produces, touch screen operation is quick, simple, but the treatment need according to arbitrarily regulate concentration (0-80mg/L continuous adjustable), to constantly adjust display, always, always get ozone purpose.
3. Digital display system: can make the operator better observed and adjust concentration, ensure accurate.
4. Double take gas device (leaned/automatic) : to use two kinds of take breath way, can ensure operators in different circumstances quickly get ozone gas. Leaned type; Gently press take gas valve, can obtain O3 gas, take gas valve shut down automatically, this way is fast and convenient, won't cause take when gas omissions gas, lest cause of medical personnel respiratory stimulation such pollution.
5. Ozone recycling decomposition device: make the residual O3 gas rapidly into pure oxygen, through vent release, ensure the working environment is clear.
6. Line pressure adjusting device: this instrument to air pressure without specific requirements, just open it can, the instrument inside will automatically regulate atmospheric pressure, can make the hospital use any pure oxygen source.
7. Automatic standby system: the instrument structure for instruments and generator can be seperated power, the instrument itself continuity long standby (p), 48 hours for generators without any loss, to ensure the generator long life expectancy.
8. Radiator cooling system: through radiator avoid high-pressure tube temperature, influence of ozone concentration numerical accuracy, more guaranteed the instrument of every internal original device of life1年前查看全部
- 今年春天,不同寻常的低温导致北极上空差点形成臭氧洞。臭氧(O 3 )属于 [
今年春天,不同寻常的低温导致北极上空差点形成臭氧洞。臭氧(O 3 )属于 [ ]A.氧气
B.空气污染物
C.有机物
D.稀有气体 切半斤多1年前1
切半斤多1年前1 -
 limi134 共回答了13个问题
limi134 共回答了13个问题 |采纳率92.3%B1年前查看全部
- 酸雨、温室效应、臭氧空洞是人类面临的三大环境问题,下列说法不准确的是( )
酸雨、温室效应、臭氧空洞是人类面临的三大环境问题,下列说法不准确的是( )
A. 使用液化气代替汽油作汽车燃料,可以减少温室效应
B. 逐步使用核能、风能、氢能,可以减少温室效应
C. 使用无氟冰箱等,可以减少臭氧空洞
D. 对燃煤预先采取脱硫措施,可以减少酸雨 井Q1年前1
井Q1年前1 -
 华广 共回答了9个问题
华广 共回答了9个问题 |采纳率88.9%解题思路:A、液化气是石油分馏的产物,燃烧同样会产生温室气体.
B、根据减少温室效应的措施进行分析判断.
C、电冰箱中的制冷剂“氟里昂”等,会使臭氧层形成空洞.
D、酸雨是因为空气中的污染物二氧化硫、氮氧化合物等过多造成的,二氧化硫、氮氧化合物来自于煤等化石燃料的大量使用.A、液化气是石油分馏的产物,它的燃烧同样会产生温室气体,不会减少温室效应,故选项说法错误.
B、逐步使用核能、风能、氢能等新能源,可以减少二氧化碳的排放量,可以减少温室效应,故选项说法正确.
C、电冰箱中的制冷剂“氟里昂”等,对臭氧层有很大的破坏作用,会使臭氧层形成空洞;使用无氟冰箱等,可以减少臭氧空洞,故选项说法正确.
D、二氧化硫、氮氧化合物等排放会形成酸雨,对燃煤预先采取脱硫措施,可减少二氧化硫等气体的排放,可以减少酸雨,故选项说法正确.
故选A.点评:
本题考点: 常用燃料的使用与其对环境的影响;酸雨的产生、危害及防治;资源综合利用和新能源开发.
考点点评: 环境污染与保护是人们关注的热点,也是中考考查的热点之一,了解当今世界常见的环境污染与防治措施即可正确解答本题.1年前查看全部
- 1.1982年,科学家首次发现臭氧减少的现象是在()上空.( ) A A.北极 B B.南极 C
1.1982年,科学家首次发现臭氧减少的现象是在()上空.( ) A A.北极 B B.南极 C
C. stella_z1年前1
stella_z1年前1 -
 leiloveme 共回答了18个问题
leiloveme 共回答了18个问题 |采纳率94.4%A1年前查看全部
- 化学元素分子式请问DDT(滴滴涕)化学式为:C14H9CL5和03(臭氧)发生反应后应该生成什么?PCBs(多氯联苯)E
化学元素分子式
请问DDT(滴滴涕)化学式为:C14H9CL5和03(臭氧)发生反应后应该生成什么?
PCBs(多氯联苯)English:(polychlonnated biphenyl)分子式鄙人不知,
再加点问题:请问多氯联苯同臭氧发生反应生成什么?
以上两组分子式反应后生成的化学元素哪些有害请指出! xila-爱琴海1年前2
xila-爱琴海1年前2 -
 xjbadboy 共回答了9个问题
xjbadboy 共回答了9个问题 |采纳率88.9%中文名称:滴滴涕
英文名称:DDT
中文名称2:1,1,1-三氯-2,2-双(对氯苯基)乙烷
英文名称2:1,1,1-trichloro-2,2-bis(p-chlorophenyl)ethane
CAS No.:50-29-3
分子式:C14H9CI5
分子量:354.48
理化特性
主要成分:乳剂、可湿性粉剂、粉剂和气溶胶.
外观与性状:白色或淡黄色粉末.
熔点(℃):107~109
沸点(℃):260
相对密度(水=1):1.55(25℃)
饱和蒸气压(kPa):2.53×10-8(20℃)
闪点(℃):72~77
溶解性:不溶于水,易溶于丙酮、苯、二氯乙烷.
主要用途:用作农用杀虫剂.
健康危害:急性中毒症状有头痛、眩晕、恶心、呕吐、四肢感觉异常,共济失调;重者体温升高、心动过速、呼吸困难、昏迷、甚至死亡.对皮肤有刺激作用.
环境危害:对环境有危害.
燃爆危险:本品可燃,有毒,具刺激性.
危险特性:遇明火、高热可燃.其粉体与空气可形成爆炸性混合物,当达到一定浓度时,遇火星会发生爆炸.受高热分解放出有毒的气体.
滴滴涕是第一个大量使用的有机合成杀虫剂.早在1874年,齐德勒就已发现,用氯笨和三氯乙醛反应生成一种物质,具有杀虫效力.1936年-1938年,瑞士的缪勒在实验中重复了齐德勒的反应,得到了这种具有杀虫效力的物质,并为之申请了专利.这种物质于1943年正式投入生产,在40年代已为人们广泛使用了.
滴滴涕对害虫有极强的触杀和胃毒作用,对于种种害虫都有很好的效果,用途极广.因此在它出现的30年里,一直是重要的杀虫剂.然而,长期使用中,它也暴露了自己的缺点,最严重的是它不易被生物分解,会残留下来,造成环境污染,于是,自1971年之后,许多国家对之实行封禁政策.
一种主要的有机氯杀虫剂,又称二二三.由德国人蔡德勒在1874年合成,1938年瑞士人马勒首次证明其杀虫作用.1943年开始大量生产,首先在瑞士推广使用.二战期间,曾用以防止煤昆虫,使上百万人免于痢疾和伤寒等传染病造成的死亡,马勒也因此获1948年诺贝尔医学奖.由于滴滴涕对害虫有强力的触杀和胃毒作用,可以用来防止棉铃虫、棉红铃虫等多种农业害虫和蚊、蝇、蚤、虱、臭虫等卫生害虫,效果较好.它是第一个大量使用的有机合成杀虫剂.40-70年代初的三十多年里,滴滴涕一直是一个重要的广泛应用的杀虫剂.后来人们发现其半衰期长达2.5-5年,且脂培性很强,很容易蓄积在动物体脂肪中,造成环境、食品的污染和对人类健康的潜在威胁,从70年代初期先后为许多国家禁用于农业,中国也于1983年停止生产农用滴滴涕.1年前查看全部
- 氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:4Al(s)+3O2(g)=2Al2O3(s)△H
氧气(O2)和臭氧(O3)是氧元素的两种同素异形体,已知热化学方程式:4Al(s)+3O2(g)=2Al2O3(s)△H1,4Al(s)+2O3(g)=2Al2O3(s)△H2 ,3O2(g)=2O3(g)△H3 则( )
A.△H2-△H1=△H3
B.△H1+△H2=△H3
C.△H1-△H2=△H3
D.△H2+△H1+△H3=0 瑞峰19771年前1
瑞峰19771年前1 -
 郑甦鸿 共回答了21个问题
郑甦鸿 共回答了21个问题 |采纳率90.5%解题思路:①4Al(s)+3O2(g)=2Al2O3(s)△H1,②4Al(s)+2O3(g)=2Al2O3(s)△H2 ,根据盖斯定律可知,反应①-②可得3O2(g)=2O3(g),以此来解答.①4Al(s)+3O2(g)=2Al2O3(s)△H1,
②4Al(s)+2O3(g)=2Al2O3(s)△H2 ,
根据盖斯定律可知,反应①-②可得3O2(g)=2O3(g),
所以△H3 =△H1-△H2,
故选C.点评:
本题考点: 用盖斯定律进行有关反应热的计算.
考点点评: 本题考查盖斯定律计算反应热,明确已知反应与目标反应的关系是解答本题的关键,题目较简单.1年前查看全部
- 臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,同时产生O 2 ,则:
臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,同时产生O 2 ,则:
(1)该反应的化学方程式为:______;
(2)该反应中氧化剂的名称为______,还原产物的化学式为______;
(3)若消耗0.1mol氧化剂,反应中转移电子的物质的量为______. xingrou1年前1
xingrou1年前1 -
 senloveJennifer 共回答了9个问题
senloveJennifer 共回答了9个问题 |采纳率77.8%(1)臭氧(O 3 )可以使湿润的淀粉碘化钾试纸变蓝,说明反应过程中有碘单质生成,反应中碘化钾是还原剂,臭氧作氧化剂得电子发生还原反应,所以是碘化钾和臭氧、水反应生成碘、氧气和氢氧化钾,
反应方程式为:2KI+O 3 +H 2 O=2KOH+I 2 +O 2 .
故答案为:2KI+O 3 +H 2 O=2KOH+I 2 +O 2 ;
(2)该反应中臭氧得电子化合价降低,所以臭氧是氧化剂;氧化剂对应的产物是还原产物,所以氢氧化钾是还原产物.
故答案为:臭氧; KOH;
(3)设转移电子的物质的量是x.
2KI+O 3 +H 2 O=2KOH+I 2 +O 2 转移电子
1mol 2mol
0.1mol x
x=0.2mol
故答案为:0.2 mol.1年前查看全部
- 化学上把同种元素组成的不同单质互称为同素异形体,例如氧气和臭氧,下列各组物质互称为同素异形体的是______
化学上把同种元素组成的不同单质互称为同素异形体,例如氧气和臭氧,下列各组物质互称为同素异形体的是______
A.氢气与液氢B.冰与干冰C.红磷与白磷D.______. 柳随风柳五1年前1
柳随风柳五1年前1 -
 抢三分 共回答了18个问题
抢三分 共回答了18个问题 |采纳率88.9%解题思路:根据同素异形体的定义,由同种元素组成的不同单质互称同素异形体,进行判断.A、液氧和氧气都是O2,是同一种单质的不同状态,不是不同单质,故不是互称同素异形体;
B、冰是固态的水,干冰是二氧化碳的固体,二者是由不同种元素组成的化合物,故不符合题意;
C、红磷和白磷都是磷元素组成的单质,属于同素异形体;故符合题意;
D、金刚石和石墨
故选C.点评:
本题考点: 同素异形体和同素异形现象.
考点点评: 本题主要考查学生对概念的理解,一般一个概念的要从两方面理解掌握,一是概念的内涵,即实质;二是概念的外延,即范围.如同素异形体的内涵是“由同种元素组成”,外延是“不同单质”.1年前查看全部
- 下列关于臭氧的叙述中正确的是( )
下列关于臭氧的叙述中正确的是( )
A.臭氧与氧气是氧元素的两种同素异形体,其物理性质相同
B.打雷时、高压电机和复印机工作时均会产生臭氧
C.臭氧能与Ag、Hg等与氧气不易反应的物质发生化学反应
D.臭氧的密度大于空气,故臭氧主要集中在地面 晕1991年前1
晕1991年前1 -
 完美天气99 共回答了15个问题
完美天气99 共回答了15个问题 |采纳率93.3%解题思路:A、O2和O3都是由氧元素组成的性质不同的单质,属于同素异形体,结构不同,性质不同;
B、电弧能使氧气分子分解为氧原子,氧原子不稳定,迅速结合为氧气,部分结合为臭氧;
C、臭氧比氧气更活泼,氧化性更强;
D、从臭氧的形成条件分析.A、O2和O3都是由氧元素组成的性质不同的单质,属于同素异形体,结构不同,物理性质不同,故A错误;
B、电弧能使氧气分子分解为氧原子,氧原子不稳定,迅速结合为氧气,部分结合为臭氧,故B正确;
C、臭氧具有强氧化性,它比氧气的氧化性更强,能将金属银等不活泼金属氧化,故C正确;
D、形成臭氧的主要条件是紫外线,在大气外层受到紫外线直接辐射量最多,所以在外层反而有臭氧比较多,形成的臭氧本身,又特别能吸收过滤紫外线,从而下层到达地面的紫外线就很少,故D错误;
故选BC.点评:
本题考点: 臭氧.
考点点评: 本题考查了臭氧的化学性质,题目难度不大,注意打雷时、高压电机和复印机工作时均会产生臭氧的机理.1年前查看全部
- 为什么臭氧可吸收紫外线而氧气不可以,臭氧是怎样吸收紫外线
 水木残阳1年前1
水木残阳1年前1 -
 513条木鱼 共回答了22个问题
513条木鱼 共回答了22个问题 |采纳率81.8%臭氧主要是紫外线制造出来的.太阳光线中的紫外线分为长波和短波两种,当大气中(含有21%)的氧气分子受到短波紫外线照射时,氧分子会分解成原子状态.氧原子的不稳定性极强,极易与其他物质发生反应.如与氢(H?)反应生成水(H?O),与碳(C)反应生成二氧化碳(C0?).同样的,与氧分子(O?)反应时,就形成了臭氧(O?).臭氧形成后,由于其比重大于氧气,会逐渐的向臭氧层的底层降落,在降落过程中随着温度的变化(上升),臭氧不稳定性愈趋明显,再受到长波紫外线的照射,再度还原为氧.臭氧层就是保持了这种氧气与臭氧相互转换的动态平衡.1年前查看全部
- 臭氧层是怎么形成的?臭氧分子量大,应该下沉阿,为什么反而跑到上面去了?臭氧层是怎么形成的呢?
 南的ww1年前1
南的ww1年前1 -
 起名真难啊啊 共回答了16个问题
起名真难啊啊 共回答了16个问题 |采纳率100%在数亿年以前,地球上的大气中没有臭氧层,地球的表面受到来自太阳的紫外线强烈照射,地面上没有生物存在,仅有少数生物生存在水中,因为水能吸收紫外线,水中绿色植物不断地吸收大气中的二氧化碳,释放出氧气,扩散到空气中,而其中一部分的氧气在大气层的上层,受到紫外线的作用,依下面所示的反应式,氧气变成了臭氧而产生了臭氧层.
O2 + hν→ 2O
O2 + O → O3
即高层大气中的氧气受阳光紫外辐射变成游离的氧原子,有些游离的氧原子又与氧气结合就生成了臭氧,大气中 90%的臭氧是以这种方式形成的.
臭氧层对地球上的生命相当重要,因它能滤除紫外线,地球上生物才能登上陆地,展开另一种灿烂多姿的地表生活1年前查看全部
- (2分)科学家测得单质臭氧(O 3 )的相对分子质量为48,则相同分子数的臭氧与氧气的质量比为 _______,质量相同
(2分)科学家测得单质臭氧(O 3 )的相对分子质量为48,则相同分子数的臭氧与氧气的质量比为 _______,质量相同的臭氧和氧气的分子个数比为 ____________。
 duoqimei1年前0
duoqimei1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 南极上空的臭氧为何大量减少?
 lovesunpassion1年前1
lovesunpassion1年前1 -
 一个普通的芋头 共回答了17个问题
一个普通的芋头 共回答了17个问题 |采纳率94.1%自己说不准确,引用一下~~
对于大气臭氧层破坏的原因,科学家中间有多种见解.但是大多数人认为,人类过多地使用氯氟烃类化学物质(用CFCs表示)是破坏臭氧层的主要原因.氯氟烃是一种人造化学物质,1930年由美国的杜邦公司投入生产.在第二次世界大战后,尤其是进入60年以后,开始大量使用,主要用作气溶胶、制冷剂、发泡剂、化工溶剂等.另外,哈龙类物质(用于灭火器)、氮氧化物也会造成臭氧层的损耗.
如上文说述,在平流层内离地面20-30千米的地方是臭氧的集中层带,在这个臭氧层中存在着氧原子(O)、氧分子(O2)和臭氧(O3)的动态平衡.但是氮氧化物、氯、溴等活性物质及其他活性基团会破坏这个平衡,使其向着臭氧分解的方向转移.而CFCs物质的非同寻常的稳定性使其在大气同温层中很容易聚集起来,其影响将持续一个世纪或更长的时间.在强烈的紫外辐射作用下它们光解出氯原子和溴原子,成为破坏臭氧的催化剂(一个氯原子可以破坏10万个臭氧分子).1年前查看全部
- 由水和氧气在放电条件下生成臭氧和过氧化氢的正、负极电极反应方程式
 zzq_cqy1年前1
zzq_cqy1年前1 -
 棠中铁 共回答了17个问题
棠中铁 共回答了17个问题 |采纳率88.2%2O2+H2O=放电=O3+H2O2
阴极:2O2 +e ===O3 + O-(-1价)
阳极:H2O -e + O- ===H2O21年前查看全部
- O3+NH3=?(臭氧与氨的反应式?)
 kerry_8202121年前4
kerry_8202121年前4 -
 素婉 共回答了21个问题
素婉 共回答了21个问题 |采纳率95.2%7O3+6NH3=6NO2+9H2O1年前查看全部
- 为什么2mol臭氧的摩尔质量与96g氧气的摩尔质量之比为3:2
 welby0051年前2
welby0051年前2 -
 yaoruiling 共回答了17个问题
yaoruiling 共回答了17个问题 |采纳率88.2%摩尔质量是不变的,数值上等于分子量
臭氧分子是O3,氧气分子为O2
所以摩尔质量是48:32=3:2
这个与臭氧、氧气的质量、物质的量都无关.
另外摩尔质量的单位是g/mol1年前查看全部
- 常温常压下,氧气与臭氧的混合物16g中约含有6.02×1023个氧原子
常温常压下,氧气与臭氧的混合物16g中约含有6.02×1023个氧原子
为什么是对的 wersdfasdf1年前1
wersdfasdf1年前1 -
 流窜作案07 共回答了20个问题
流窜作案07 共回答了20个问题 |采纳率95%16克氧与臭氧都是由氧原子构成的,故可以看成是16克的氧原子,即1摩尔的氧原子,也即6.02*10^23个氧原子.1年前查看全部
- 氧气转换为臭氧属于什么变化?
 hualei_231年前1
hualei_231年前1 -
 衰宝 共回答了16个问题
衰宝 共回答了16个问题 |采纳率87.5%化学变化1年前查看全部
- 臭氧浓度有统一的单位吗?
 chen981171年前2
chen981171年前2 -
 85629654 共回答了18个问题
85629654 共回答了18个问题 |采纳率83.3%有的,楼上只说了一种.
臭氧的浓度分在空气中,氧气中和在水中.
一般用PPM,mg/l,g/m3,
臭氧机技术参数使用以上的单位都可以.1年前查看全部
- 汞和银在常温下能与臭氧反应吗
 zhuxiao661年前1
zhuxiao661年前1 -
 ENorton 共回答了25个问题
ENorton 共回答了25个问题 |采纳率96%都可以
Hg生成HgO
Ag生成Ag2O2,不是Ag2O1年前查看全部
- (2011•重庆)臭氧是一种强氧化剂,常用于消毒、灭菌等.
 (2011•重庆)臭氧是一种强氧化剂,常用于消毒、灭菌等.
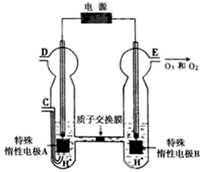
(2011•重庆)臭氧是一种强氧化剂,常用于消毒、灭菌等.
(1)O3与KI溶液反应生成的两种单质是______和______.(填分子式)
(2)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如下表所示.已知:O3的起始浓度为0.0216mol/L.
①pH增大能加速O3分解,表明对O3分解起催化作用的是______.pH
t/min
T/℃3.0 4.0 5.0 6.0 20 301 231 169 58 30 158 108 48 15 50 31 26 15 7
②在30℃、pH=4.0条件下,O3的分解速率为______mol/(L•min);
③据表中的递变规律,推测O3在下列条件下分解速率依次增大的顺序为______.(填字母代号)
a. 40℃、pH=3.0 b. 10℃、pH=4.0 c. 30℃、pH=7.0
(3)O3可由臭氧发生器(原理如图)电解稀硫酸制得.
①图中阴极为______(填“A”或“B”),其电极反应式为______.
②若C处通入O2,则A极的电极反应式为______.
③若C处不通入O2,D、E处分别收集到x L和y L气体(标准状况),则E处收集的气体中O3所占的体积分数为[x−2y/y][x−2y/y](忽略O3的分解). 跟着小孩混1年前1
跟着小孩混1年前1 -
 gz_xiaoliang 共回答了19个问题
gz_xiaoliang 共回答了19个问题 |采纳率84.2%解题思路:(1)O3与KI溶液反应生成的两种单质只能为O2、I2;
(2)①pH增大,则OH-浓度增大;
②根据v=[△c/t]计算;
③根据pH和温度判断达到平衡所用的时间的范围,可判断分解速率;
(3))①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极;
②C处通入O2,O2发生还原反应,在酸性条件下生成水;
③若C处不通入O2,实质为电解水,D处为氢气,体积为x L,E处为氧气、臭氧,体积共为yL,令臭氧的体积为ZL,利用电子转移守恒列放出计算Z的值,再根据体积分数定义计算.(1)O3与KI溶液反应生成的两种单质只能为O2、I2,故答案为:O2;I2;
(2)①pH增大,则OH-浓度增大,pH增大能加速O3分解,表明对O3分解起催化作用的是OH-,故答案为:OH-;
②v=[△c/t]=[0.0108mol/L/108min]=1.00×10-4mol/(L•min),故答案为:1.00×10-4;
③由表中数据可知,40°C、pH=3.0时,所需时间在31min~158min之间;
10°C、pH=4.0时,所需时间>231min;
30°C、pH=7.0时,所需时间<15min,则分解速率依次增大的顺序为b、a、c,
故答案为:b、a、c.
(3))①由图可知,B极生成O2、O3,B极反应氧化反应,电解池阳极发生氧化反应,故A为阴极,电极反应为2H++2e-═H2↑;
故答案为:A;2H++2e-═H2↑;
②C处通入O2,O2发生还原反应,在酸性条件下生成水,电极反应式为O2+4H++4e-=2H2O,故答案为:O2+4H++4e-=2H2O.
③若C处不通入O2,实质为电解水,D处为氢气,体积为x L,E处为氧气、臭氧,体积共为y L,令臭氧的体积为ZL,根据电子转移守恒有
x×2=Z×3×2+(y-Z)×2×2,解得Z=x-2y,所以E处收集的气体中O3所占的体积分数为[x−2y/y],
故答案为:[x−2y/y].点评:
本题考点: 臭氧;反应速率的定量表示方法;化学反应速率的影响因素;电解原理.
考点点评: 本题考查化学反应速率的影响因素的实验探究,原电池与电解池反应原理,题目难度中等,本题注意对表中数据的分析和处理.1年前查看全部
- 标况下22.4升氧气和臭氧组成的混合物中总原子数为什么是2Na至3Na?怎么算?要详解
 人淡如菊_CC1年前1
人淡如菊_CC1年前1 -
 永远娜娜 共回答了18个问题
永远娜娜 共回答了18个问题 |采纳率94.4%用极值法,当22.4升全是O2时是2Na,当22.4升全是臭氧时是3Na,因为是混合物所以是在2Na至3Na1年前查看全部
- 臭氧的化学价和物质类别?物质类别的选项:金属,非金属,稀有气体,金属氧化物,非金属氧化物,酸,碱,盐
 宜宾夏阳1年前6
宜宾夏阳1年前6 -
 夜微凉 共回答了19个问题
夜微凉 共回答了19个问题 |采纳率89.5%臭氧 O3 化学价为0,非金属,
这位同学要加强化学学习啊,别老是上网了额1年前查看全部
大家在问
- 1801.11a/b/g和802.11a/b/g有什么区别
- 2要使430÷囗0的商是两位数,囗里最大填口
- 3某同学把30克质量分数为15%的高猛酸钾容液稀释成质量分数为0.03%的容液,需加水多少千克?
- 4形容幸福的佳句有哪些
- 5感谢有您的教导 作文
- 6某校买来一批图书,放在两个书柜中,其中第一柜的本数占这批图书的58%,如果从第一柜取出32本,放到第二柜中,这时两个书柜
- 7-------mike -----(read)english every day动词的适当形式填空
- 8希望暑假过得有意义一点.所以,希望大家给一些建议帮我列一个暑假计划表让我参考吧...
- 9吞吞吐吐是什么意思
- 101nm=多少A°
- 11把下列方程化成一元二次方程的一般形式,并分别写出它们的二次项系数,一次项系数和长数项;(表格的形式)
- 12企业所得税是怎样计算得来的?具体的公式是怎样的?比如说利润总额是怎样算出来的?
- 13关于“广袤无垠、青草覆盖的原野,寸草不生、青石嶙峋的山峰,深邃的蓝天和凝滞的云团,心头边弥漫着古典边塞诗词的悲壮和苍凉.
- 14解方程组 2x-根号3y=0 根号3x-2y=1
- 15把“人生难得几位知己,虽然无法常聚一起,但在我心中总是有你这位好朋友.”这句话翻译成英文是什么?
