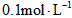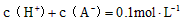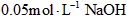在常温常压下,取下列四种气态烃各1mol,分别在足量的氧气中燃烧,消耗氧气最多的是CH4 C3H8 C4H10 C2H6
 ronanlee72022-10-04 11:39:542条回答
ronanlee72022-10-04 11:39:542条回答
已提交,审核后显示!提交回复
共2条回复
 花无缺7758 共回答了23个问题
花无缺7758 共回答了23个问题 |采纳率87%- CH4 ---CO2 + 2H2O -----2O2
C3H8 ----3CO2 +4H2O ----5O2
C4H10 ---4CO2 + 5H2O ----6.5O2
C2H6 ----2CO2 + 3H2O ----3.5O2
消耗氧气最多的是 C4H10 - 1年前
 露冷 共回答了5个问题
露冷 共回答了5个问题 |采纳率- C4H10最多
根据原子数守恒,写出化学方程式即可知道 - 1年前
相关推荐
- 有A、B、C、D四种物质,常温下,A是黑色固体,B、C、D都是无色气体.A和B在不同反应条件下分别化合成C或D,A和C在
有A、B、C、D四种物质,常温下,A是黑色固体,B、C、D都是无色气体.A和B在不同反应条件下分别化合成C或D,A和C在高温下可化合成D.
求A、B、C、D各物质的化学式和这三个反应的化学式? 我糊涂我快乐21年前4
我糊涂我快乐21年前4 -
 henrshandong 共回答了15个问题
henrshandong 共回答了15个问题 |采纳率93.3%A:碳(C)
B:氧气(O2)
C:二氧化碳(CO2)
D:一氧化碳(CO)
A到C:C+O2==CO2(等号上写点燃)
A到D:2C+O2==CO(等号上写点燃)
化合成D:CO2+O2==2CO(等号上写高温)1年前查看全部
- 现有常温下的四份溶液:①0.01mol/L CH3COOH溶液;②pH=2 的HCl溶液;③pH=1
现有常温下的四份溶液:①0.01mol/L CH3COOH溶液;②pH=2 的HCl溶液;③pH=12的氨水;④0.01mol/L的NaOH溶液.下列说法正确的是( )
A.①中水的电离程度最小,③中水的电离程度最大
B.将①④混合,若c(CH3COO-)>c(H+),则混合液一定呈碱性
C.将四份溶液分别稀释到原体积相同倍数后,溶液的pH:③>④,②>①
D.将②③混合,若pH=7,则消耗溶液的体积:②>③ 森浩希1年前1
森浩希1年前1 -
 企盾护航 共回答了12个问题
企盾护航 共回答了12个问题 |采纳率83.3%解题思路:A、酸碱对水的电离起到抑制作用,酸中的氢离子或碱中的氢氧根离子浓度越大,抑制程度越大;
B、将①、④混合体积不同混合后溶液不一定成碱性,中性溶液中也存在c(CH3COO-)>c(H+);
C、稀释相同倍数,弱电解质存在电离平衡;
D、氨水是弱碱,等体积混合时溶液呈碱性,所以盐酸体积大于氨水溶液的体积.A、②③④溶液是强酸、弱碱、强碱,溶液中氢离子和氢氧根离子浓度相同,对水的电离抑制程度相同,①溶液中的氢离子浓度,对水抑制程度小,所以①水的电离程度最小,②③④溶液中水的电离程度大,故A错误;
B、若将①、④等体积混合,醋酸和氢氧化钠恰好反应生成醋酸钠,溶液呈碱性,有c(CH3COO-)>c(H+),若混合后溶液呈中性时存在C(Na+)=c(CH3COO-)>C(OH-)=c(H+),故错误;
C、将四份溶液稀释相同倍数后溶液的pH:氨水存在电离平衡,溶液中氢氧根离子浓度大于氢氧化钠溶液中氢氧根离子,③>④,同浓度醋酸和盐酸稀释相同倍数,醋酸存在电离平衡,醋酸溶液中氢离子浓度小于盐酸溶液中的氢离子浓度,所以溶液pH为①>②,故C错误;
D、②③若等体积混合后溶液呈碱性,若有pH=7,则消耗溶液的体积为②>③,故D正确;
故选D.点评:
本题考点: 弱电解质在水溶液中的电离平衡.
考点点评: 本题考查了弱电解质的电离平衡应用,主要是对水的电离影响,溶液酸碱性的判断,溶液稀释的PH变化,关键是酸碱反应后溶液酸碱性的判断.1年前查看全部
- 密闭容器中混合气体的压强常温时,下列各组气体在同一密闭容器中等物质的量混合后压强最小的是A.H2S和SO2 B.H2和O
密闭容器中混合气体的压强
常温时,下列各组气体在同一密闭容器中等物质的量混合后压强最小的是
A.H2S和SO2 B.H2和O2 C.H2S和O2 D.H2和CI2
原因是什么,像这种判断压强的题要怎么做 真我风采_ss1年前4
真我风采_ss1年前4 -
 yang向东 共回答了17个问题
yang向东 共回答了17个问题 |采纳率76.5%这种题看气体与气体之间是否反应.反应后体积是否变化!变化,哪个变得更小.
A中H2S与SO2反应生成很水和S固体.所以体积减少了.1年前查看全部
- (1)常温下向20l真空容器中通入amol硫化氢和bmol二氧化硫(a,b都是正整数,且a
 潮汐乘风1年前2
潮汐乘风1年前2 -
 朴原1 共回答了22个问题
朴原1 共回答了22个问题 |采纳率90.9%(1)容器中发生的反应为:2H2S+SO2=3S↓+2H2O,
欲使容器内气的密度(ρ=m÷V,容器的体积一定)最大,则要让容器中的气体质量最大(质量与物质的量成正比,即物质的量最大).
两种气体反应,最后剩余的气体为过量的气体,所以只要让剩余的气体的质量(物质的量)最大,容器内气体的密度最大.要让剩余气体的物质的量最大,则让硫化氢气体和二氧化硫气体的物质的量差值最大即可;
所以欲使容器中气体密度最大,则b取最大值5,a取最大值1即可;
此时硫化氢完全反应,剩余的SO2的物质的量为5-0.5=4.5mol(通过方程式计算可知);
所以容器中气体的质量为m=n×M=4.5mol×64g/mol=288g;
所以此时容器中的气体的密度为:ρ=m÷V=288g÷20L=14.4g/L;
综上所述,容器内气体可能达到的最大密度约是14.4g/mol.
(楼上错误的原因是a取了0,0不是正整数)
(2)根据气体状态方程PV=nRT可知:同问同体积时,压强和物质的量成正比,即P1/P2=n1/n2;所以反应前后容器中气体的总物质的量之比为P1/P2=2:1;
根据反应方程式可知若恰好完全反应则无气体剩余,所以剩余的气体为过量的气体;
设反应前H2S的物质的量为x,SO2的物质的量为y.
①若H2S过量;则有:
(x-2y)/(x+y)=1/2,所以x:y=5:1;
②若SO2过量,则有:
(y-0.5x)/(x+y)=1/2,所以x:y=1:2;
综上所述:反应前H2S和SO2的体积比是5:1或1:2.1年前查看全部
- 实验室用Cu与浓HNO3在常温下反应制取NO2气体,同时生成Cu(NO3)2和H2O,试回答:
实验室用Cu与浓HNO3在常温下反应制取NO2气体,同时生成Cu(NO3)2和H2O,试回答:
1.写出铜和硝酸反应的化学方程式.
2.若实验室用足量的浓硝酸制取23克NO2气体,则需要加入铜多少克?
3.反应中同时有多少克HNO3被还原? sddlphoenix1年前4
sddlphoenix1年前4 -
 smartkobe 共回答了22个问题
smartkobe 共回答了22个问题 |采纳率81.8%1.反应方程式为:Cu + 4HNO3 = Cu(NO3)2 + 2NO2 ↑ + 2H2O
2.由关系式:Cu 2NO2
64 92
X g 23g
可得 X=16g
3.此反应中硝酸一部分起还原作用,一部起酸性作用.
被还原硝酸与其还原产物NO2间的关系式:
HNO3 NO2
63 92
Yg 23g
可得 Y = 15.75g
则被还原的硝酸为15.75g1年前查看全部
- 已知常温下,硝酸浓度越稀,其还原产物的价态越低.(本题气体数据均已折算至标准状况)
已知常温下,硝酸浓度越稀,其还原产物的价态越低.(本题气体数据均已折算至标准状况)
(1)实验室欲用70%的浓硝酸(密度1.41g/mL)配制1.0mol/L的稀硝酸(密度1.04g/mL)500mL.求:70%浓硝酸的物质的量浓度______mol/L(保留1位小数,下同),配制时需浓硝酸______mL.
(2)将9.65克某铜锌合金加入到足量的浓硝酸中,得到气体 6.72L(假设不含N2O4),则该合金中铜与锌的物质的量之比为______.
(3)向100mL某浓度的硝酸溶液中加入足量的铁粉,铁粉部分溶解,却无气体产生.向反应后的溶液中加入过量的氢氧化钠溶液,过滤后对滤渣进行洗涤后灼烧得到固体物质4.8g,写出铁与硝酸反应的化学方程式______,该硝酸溶液的物质的量浓度______.
(4)将13克锌加入到200mL 3.6mol/L的硝酸溶液中,锌全部溶解,得到无色气体2.464L(已知常温下N2O3为液体),测得反应后的溶液pH=0(假设反应前后溶液体积无变化).取少量反应后的溶液加入足量的氢氧化钠溶液并加热,无刺激性气味的气体生成.试求该无色气体的组成及其物质的量. 扭曲的小圈儿1年前1
扭曲的小圈儿1年前1 -
 83648364 共回答了19个问题
83648364 共回答了19个问题 |采纳率84.2%解题思路:(1)根据c=[1000ρw/M]计算浓硝酸的浓度,根据稀释定律计算所需浓硝酸的体积;
(2)6.72LNO2的物质的量为0.3mol,设Cu为xmol,Zn为ymol,根据质量9.65g与生成NO2的物质的量0.3mol列式计算;
(3)铁粉部分溶解,说明生成Fe(NO3)2,却无气体产生说明即生成NH4NO3;
(4)由加入NaOH没有刺激性气体产生,得到没有生成NH3,则得到的无色气体为NO、N2,根据原子守恒和得失电子守恒计算物质的量.(1)浓硝酸的物质的量浓度c=[1000ρw/M]=[1000×1.41×70%/63]mol/L=15.7 mol/L,
由稀释定律可得:15.7 mol/L×V浓硝酸 =1.0mol/L×500mL,解得:V浓硝酸 =31.8ml,
故答案为:15.7;31.8;
(2)标准状况下,6.72LNO2的物质的量为[6.72L/22.4L/mol]=0.3mol,设Cu为xmol,Zn为ymol,则
①xmol×64g/mol+ymol×65g/mol=9.65g
②2xmol+2ymol=0.3mol,
①②联立解得:x=0.1,y=0.05,
因此该合金中铜与锌的物质的量之比为0.1mol:0.05mol=2:1,
故答案为:2:1;
(3)铁粉部分溶解,说明生成Fe(NO3)2,却无气体产生说明即生成NH4NO3,所以方程式为10HNO3+4Fe=4Fe(NO3)2+NH4NO3+3H2O,
再加NaOH,Fe(NO3)2都转化成Fe(OH)2,并进一步转化成Fe(OH)3,再灼烧,则生成Fe2O3为4.8g,Fe2O3的物质的量为[4.8g/160g/mol]=.03mol,
所以Fe为0.03mol×2=0.06mol,HNO3为0.06mol×[10/4]=0.15mol,因此该硝酸溶液的物质的量浓度为[0.15mol/0.1L]=1.5mol/L,
故答案为:10HNO3+4Fe=4Fe(NO3)2+NH4NO3+3H2O;1.5mol/L;
(4)13g锌的物质的量为[13g/65g/mol]=0.2mol,2.464L气体共[2.464L/22.4L/mol]=0.11mol,HNO3的物质的量为0.2L×3.6mol/L=0.72mol,测得反应后的溶液pH=0,则剩余H+的物质的量为1mol/L×0.2L=0.2mol,因此有0.72mol-0.2mol=0.52mol硝酸发生了反应,
由加入NaOH没有刺激性气体产生,得到没有生成NH3,NO2为红棕色气体,因此得到的无色气体为NO、N2;
化学方程式为20Zn+52HNO3=20Zn(NO3)2+26H2O+10NO(g)+N2(g),
因此无色气体为NO 0.1mol和N2 0.01mol,
答:无色气体有NO和N2组成,NO 0.1mol,N2 0.01mol.点评:
本题考点: 化学方程式的有关计算;物质的量浓度的相关计算.
考点点评: 本题考查了化学方程式的计算,侧重于化学性质、原子守恒、电荷守恒的应用,题目难度较大,熟悉物质的性质及物质之间的转化是解题的关键.1年前查看全部
- 常温下,pH=5的氯化铵溶液中,c(Cl-)-c(NH4+)=10-5mol/L
 fxhlz1年前1
fxhlz1年前1 -
 rex1216 共回答了15个问题
rex1216 共回答了15个问题 |采纳率100%错误.c(Cl-)-c(NH4+)=10^-5-10^-9 mol/L
电荷守恒:c(NH4+)+c(H+)=c(Cl-)+c(OH-)
移项得到:c(Cl-)-c(NH4+)=c(H+)-c(OH-)
pH=5的氯化铵溶液中c(H+)=10^-5mol/L,c(OH-)=Kw/c(H+)=10^-14/10^-5=10^-9mol/L
c(Cl-)-c(NH4+)=c(H+)-c(OH-)=10^-5-10^-91年前查看全部
- 假如实现了常温下超导,导体没有了电阻,会出现什么现象,请写出几个合理的情景,最好要说明(三个或三个以上)谢谢~
 中散康1年前3
中散康1年前3 -
 better_mam 共回答了15个问题
better_mam 共回答了15个问题 |采纳率80%没有能量损耗不会发热
节省很多电能1年前查看全部
- 常温常压下的33.6L氯气与足量的铝充分反应,转移电子数是多少?解析要清晰!
常温常压下的33.6L氯气与足量的铝充分反应,转移电子数是多少?解析要清晰!
解析要清楚!十万火急! 葬心811年前1
葬心811年前1 -
 181628455 共回答了22个问题
181628455 共回答了22个问题 |采纳率90.9%2Al+3Cl2==2AlCl3 转移电子数
````````3```````````````6(可以通过化合价的升降得出)
``````33.6/22.4````````n(e-)
解得n(e-)=3mol
补充:接替过程中用了气体摩尔体积=22.4L/mol,这是标况下的数据,楼主说的是常温常压,可能有出入,但我看楼主提供的数据33.6很明显是根据22.4来的,所以还是按照标况算,如果不符合可以尝试改为常温常压下的数据)1年前查看全部
- 核聚变真的需要几千万度高温吗?氢弹是靠原子弹的高温引爆的,那么核聚变到目前没有发现有什么办法可以在常温下聚变么?
 光辉岁月19711年前1
光辉岁月19711年前1 -
 rossiwang 共回答了15个问题
rossiwang 共回答了15个问题 |采纳率93.3%没有什么办法,核聚变只有原子核的动能强大到可以克服核子间作用力才有可能发生.这必须由超高温来实现.没有办法常温发生1年前查看全部
- 已知常温下硫酸钡的溶度积Ksp=10-10,求该温度下硫酸钡的溶解度,
已知常温下硫酸钡的溶度积Ksp=10-10,求该温度下硫酸钡的溶解度,
BaSO4(s)=可逆=Ba2+(aq)+SO4^2-(aq)
x x
Ksp=C(Ba2+)*C(SO4^2-)=10^-10 即x2=10^-10
x=10^-5 mol/L
即溶解的硫酸钡浓度为10^-5 mol/L
硫酸钡相对分子质量为 233g/mol
硫酸钡浓度为2.33*10^-3 g/L
1L水等于1000g水
也就是说1000g水中溶解了2.33*10^-3g硫酸钡,100g水中溶解了硫酸钡2.33*10^-4g
为什么要用到相对分子质量乘溶解的硫酸钡浓度,为什么不直接用溶解的硫酸钡浓度, 文刀大少1年前1
文刀大少1年前1 -
 俺来自高庙村 共回答了21个问题
俺来自高庙村 共回答了21个问题 |采纳率95.2%因为溶解度的单位是 g/100g水.
我们根据溶解积可以计算得出,饱和溶液中 BaSO4的物质的量浓度.
然后,根据此物质的量浓度,可以计算出,1L溶液中,所含BaSO4的质量.
接着根据这个计算出溶解度.
如果直接用 10^-5mol/L,那么只能得到饱和BaSO4溶液的物质的量浓度.
不知道这样说你明白吗?
有不理解的地方请追问!1年前查看全部
- 下列物质在常温常压下为液体的是( )
下列物质在常温常压下为液体的是( )
A. 乙醇
B. 异丁烷
C. 乙烯
D. 一氯甲烷 ccq81501年前1
ccq81501年前1 -
 微笑的五月森林 共回答了18个问题
微笑的五月森林 共回答了18个问题 |采纳率77.8%解题思路:常见有机物中常温下为气态有:C原子数≤4烃、新戊烷、一氯甲烷、甲醛等,据此判断.异丁烷、乙烯、一氯甲烷在常温下呈气态,乙醇在常温下呈液态,故选:A;
点评:
本题考点: 乙醇的化学性质.
考点点评: 本题主要考查了物质的状态,抓住物质的状态是解题的关键,需要注意的是新戊烷也是气态.1年前查看全部
- 已知常温下:Ksp[Fe(OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31;Ksp[Zn(O
已知常温下:Ksp[Fe(OH)3]=2.6×10-39;Ksp[Cr(OH)3]=7.0×10-31;Ksp[Zn(OH)2]=1.0×10-17;Ksp[Mg(OH)2]=5.6×10-12.某溶液中有浓度均为0.0l mol/L的Fe3+、Cr3+、Zn2+、Mg2+等离子,加入氢氧化钠溶液,当溶液的pH=6时,下列叙述不正确的是( )
A.Fe3+ 已经沉淀完全
B.Cr3+已经沉淀完全
C.Zn2+ 已经开始沉淀
D.Mg2+还没开始沉淀 奢侈品ノ1年前1
奢侈品ノ1年前1 -
 专业生产pcb 共回答了12个问题
专业生产pcb 共回答了12个问题 |采纳率83.3%解题思路:加入氢氧化钠溶液,当溶液的pH=6时,溶液中氢氧根离子浓度为10-8mmol/L,依据溶液中的氢氧根离子浓度和金属离子浓度计算浓度积和溶度积常数分析比较判断.A、Q(Fe(OH)3)=c(Fe3+)c3(OH-)=0.01×(10-8)3=10-26>Ksp[Fe(OH)3]=2.6×10-39;说明生成氢氧化铁沉淀;依据Ksp[Fe(OH)3])=c(Fe3+)c3(OH-)=2.6×10-39;离子全部沉淀溶液中的铁离子为10-6,计算c(OH-)=
3
2.6×10−39
10−6
=
32.6×10−33
=<10-8,说明Fe3+离子沉淀完全,故A正确;
B、Q(Cr(OH)3)=c(Cr3+)c3(OH-)=0.01×(10-8)3=10-26>Ksp[Cr(OH)3]=2.6×10-39;说明氢氧化铬沉淀;依据Ksp[Cr(OH)3])=c(Cr3+)c3(OH-)=7.0×10-31;离子全部沉淀溶液中的铁离子为10-6,计算c(OH-)=
3
7.1×10−31
10−6
=
37.1×10−25
<10-8;说明Cr3+离子全部沉淀,故B正确;
C、Q(Zn(OH)2)=c(Zn2+)c2(OH-)=0.01×(10-8)2=10-18<Ksp[Zn(OH)2]=1.0×10-17,此时锌离子没有开始沉淀,故C错误;
D、Q(Mg(OH)2)=c(Mg2+)c2(OH-)=0.01×(10-8)2=10-18<Ksp[Mg(OH)2]=5.6×10-12,此时镁离子没有沉淀,故D正确;
故选C.点评:
本题考点: 难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查了沉淀溶解平衡的计算应用,溶度积的分析判断,离子沉淀条件的应用,题目难度较大.1年前查看全部
- 使气体液化的方法有两种.其中居民使用的液化石油气,就是在常温下用压缩体积压缩体积的方法使石油气变为液体储存在钢罐中的.让
使气体液化的方法有两种.其中居民使用的液化石油气,就是在常温下用压缩体积压缩体积的方法使石油气变为液体储存在钢罐中的.让气体液化的另一种方法是降低温度降低温度.
 1m5bacm1年前1
1m5bacm1年前1 -
 xp061282 共回答了24个问题
xp061282 共回答了24个问题 |采纳率91.7%使气体液化的方法有降低温度和压缩体积两种;
液化石油气就是在常温下利用压缩体积的办法使气体液化的,液化可以大大的减少体积,可以节省空间.
故答案为:压缩体积;降低温度.1年前查看全部
- 常温下,下列各组离子在指定环境下能大量共存的是( )
常温下,下列各组离子在指定环境下能大量共存的是( )
A. pH=1的溶液中:Na+、K+、SO32-、MnO4-
B. pH=7的溶液中:Na+、Al3+、Cl-、SO42-
C. pH>12的溶液中:Na+、K+、SO32-、AlO2-
D. pH=0的溶液中:Na+、K+、NO3-、ClO- 大小棋子1年前5
大小棋子1年前5 -
 天宇00082 共回答了21个问题
天宇00082 共回答了21个问题 |采纳率95.2%解题思路:A.pH=1的溶液,显酸性,H+、SO32-反应,H+、SO32-、MnO4-发生氧化还原反应;
B.pH=7的溶液,Al3+转化为沉淀;
C.pH>12的溶液,显碱性;
D.pH=0的溶液,显酸性,H+、ClO-反应.A.pH=1的溶液,显酸性,H+、SO32-反应生成水和气体,H+、SO32-、MnO4-发生氧化还原反应,则不能共存,故A错误;B.pH=7的溶液,Al3+转化为沉淀,则该组离子不能大量共存,故B错误;C.pH>12的溶液,显碱性,该组离...
点评:
本题考点: 离子共存问题.
考点点评: 本题考查离子的共存问题,熟悉题目中的信息及离子之间的反应是解答本题的关键,选项B为解答的难点和易错点,题目难度不大.1年前查看全部
- 常温下, 某一元酸(HA)溶液中 ,下列叙述正确的是 [ ] A.该溶液
常温下, 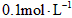 某一元酸(HA)溶液中
某一元酸(HA)溶液中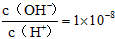 ,下列叙述正确的是[ ]
,下列叙述正确的是[ ]A.该溶液中由水电离出的 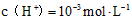
B.该溶液中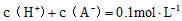
C.该溶液与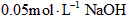 溶液等体积混合后所得溶液中
溶液等体积混合后所得溶液中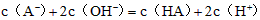
D.向该溶液中加入一定量的水,溶液中离子的浓度均减小 heavenwind1年前1
heavenwind1年前1 -
 zeroleonhart 共回答了17个问题
zeroleonhart 共回答了17个问题 |采纳率88.2%1年前查看全部
- 常温常压下58.5g氯化钠固体含na个氯化钠分子 句话错哪了
 抬头看烟花灿烂1年前2
抬头看烟花灿烂1年前2 -
 d020402061 共回答了13个问题
d020402061 共回答了13个问题 |采纳率84.6%常温常压下58.5g氯化钠固体的物质的量是1mol.但是由于氯化钠固体是离子晶体,是由钠离子和氯离子构成的,没有氯化钠分子.所以常温常压下58.5g氯化钠固体含NA个氯化钠分子是错的.正确的说法是常温常压下58.5g氯化钠固体含NA个钠离子和NA个氯离子.1年前查看全部
- 水是极弱的电解质,常温下测得水中c(H+)=10^-7 mol/l.求常温下水的电离度
 sardonna431年前3
sardonna431年前3 -
 我爱哭泣的百合花 共回答了22个问题
我爱哭泣的百合花 共回答了22个问题 |采纳率86.4%也就是1L水中有10-7mol水发生电离
1L水物质的量为 1000/18 mol
因此根据电离度概念可知 1000/18 mol水中 有10-7 mol水分子发生电离
故电离度为 10-7 除以 1000/18 x100%=1.8x10-7 %1年前查看全部
- (2012•宜春模拟)一般较强酸可制取较弱酸,这是复分解反应的规律之一.已知在常温下测得浓度均为0.1mol/L的下列6
(2012•宜春模拟)一般较强酸可制取较弱酸,这是复分解反应的规律之一.已知在常温下测得浓度均为0.1mol/L的下列6种溶液的pH:
(1)①请根据上述信息判断下列反应不能发生的是______(填编号).溶质 CH3COONa NaHCO3 Na2CO3 NaClO NaCN C6H5ONa pH 8.1 8.8 11.6 10.3 11.1 11.3
A.CH3COOH+NaCN═CH3COONa+HCN
B.CO2+H2O+2NaClO═Na2CO3+2HClO
C.2HCN+Na2CO3-→2NaCN+CO2+H2O
D.Na2CO3+C6H5OH-→NaHCO3+C6H5ONa
E.CO2+H2O+C6H5ONa-→NaHCO3+C6H5OH
②已知HA、H2B是两种弱酸,存在以下关系:H2B(少量)+2A-=B2-+2HA,则A-、B2-、HB-三种阴离子结合H+的难易顺序为______.
(2)一些复分解反应的发生还遵循其他规律.下列变化都属于复分解反应:
①将石灰乳与纯碱溶液混合可制得苛性钠溶液 ②向饱和碳酸氢铵溶液中加入饱和食盐水可获得小苏打固体③蒸发KCl和NaNO3的混合溶液,首先析出NaCl晶体.根据上述反应,总结出复分解反应发生的另一规律为______.
(3)常温下某电解质溶解在水中后,溶液中的c(H+)=10-9mol•L-1,则该电解质可能是______(填序号).
A. CuSO4B. HClC. Na2SD.NaOHE.K2SO4
(4)常温下,将pH=3的盐酸a L分别与下列三种溶液混合,结果溶液均呈中性.
①浓度为1.0×l0-3mol.L-1的氨水b L;
②c(OH -)=1.0×10-3mol.L-l的氨水c L;
③c(OH-)=1.0×10-3mol•L-1的氢氧化钡溶液d L.
则a、b、c、d之间由大到小的关系是:______.
(5)一定温度下,向等体积等物质的量浓度的下列三份溶液:①NaOH、②CH3COOH、③CH3COONa分别加等量水,pH变化最小的是______(填编号).一定温度下,向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,两溶液中阴离子的总物质的量分别为n1和n2,则n1和n2的关系为n1______n2(填“>”、“<”或“=”).
(6)己知常温时Ksp(AgCl)=1.8×10-10mol2•L-2,向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,则c(Ag+)=______,此时所得混合溶液的pH=______. jc07231年前1
jc07231年前1 -
 77cx75 共回答了20个问题
77cx75 共回答了20个问题 |采纳率75%解题思路:(1)①六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,根据强酸生成弱酸的特点判断反应能否进行;
②根据反应H2B(少量)+2A-=B2-+2HA,可知,HA酸性小于H2B,HA酸性最弱,酸性越弱,对应的酸根离子得H+能力越强;
(2)复分解反应中有一种条件是生成难溶物质,由②③可以看出,在饱和溶液中,可生成溶解度更小的物质;
(3)溶液中的c(H+)=10-9mol.L-1,说明溶液呈碱性;
(4)一水合氨为弱电解质,不能完全电离,pH相同时,氨水浓度最大;
(5)CH3COONa为强碱弱酸盐,水解呈碱性,且水解程度较小,加水稀释时,浓度减小同时促进水解,但pH变化不大;向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,NaCN水解程度比大CH3COONa,结合溶液电中性原则分析;
(6)根据溶度积常数计算.(1)①六种盐都为强碱弱酸盐,盐的pH越大,说明对应的酸水解程度越大,则对应的酸越弱,则
A.CH3COOH酸性大于HCN,反应能发生,故A正确;
B.酸性H2CO3>HClO>HCO3-,应生成NaHCO3,反应不能发生,故B错误;
C.酸性H2CO3>HClO>HCN,应生成NaHCO3,不能生成CO2,故C错误;
D.酸性C6H5OH>HCO3-,反应能发生,故D正确;
E.酸性H2CO3>C6H5OH>HCO3-,反应能发生,故E正确,
故答案为:BC;
②据反应H2B(少量)+2A-=B2-+2HA,可知,HA酸性小于H2B,HA酸性最弱,酸性越弱,对应的酸根离子得H+能力越强,没有HB-生成,说明得电子能力A-大于HB-,则得电子能力顺序为A->B2->HB-,故答案为:A->B2->HB-;
(2)各反应均有固体生成,其溶解度更小,故复分解反应能够向生成更难溶的物质的方向进行,
故答案为:由溶解度相对较大的物质向生成溶解度相对较小的物质的方向进行;
(3)溶液中的c(H+)=10-9mol•L-1,说明溶液呈碱性,只有Na2S和NaOH符合,故答案为:CD;
(4)一水合氨为弱电解质,不能完全电离,与盐酸反应至中性时,氨水应稍过量,则b>a,c(OH -)=1.0×10-3mol•L-1的氨水,一水合氨浓度远大于1.0×10-3mol.L-l的氨水,反应至中性时,a>c,氢氧化钡为强碱,与盐酸完全中和时,a=d,则b>a=d>c,
故答案为:b>a=d>c;
(5)CH3COONa为强碱弱酸盐,水解呈碱性,且水解程度较小,加水稀释时,浓度减小同时促进水解,但pH变化不大;向等体积纯水中分别加入等物质的量的CH3COONa和NaCN,NaCN水解程度比大CH3COONa,两种溶液中c(Na+)相等,由于CH3COONa溶液中H+浓度大于NaCN溶液中H+的浓度,则CH3COONa溶液中阴离子浓度较大,
故答案为:③;>;
(6)向50mL 0.018mol•L-1的AgNO3溶液中加入相同体积0.020mol•L-1的盐酸,盐酸过量,反应后的c(Cl-)=[0.02mol/L×0.05L-0.018mol/L×0.05L/0.1L]=0.001mol/L,
则c(Ag+)=
Ksp(AgCl)
c(Cl-)=
1.8×10-10
0.001mol/L=1.8×10-7 mol/L,
c(H+)=[0.02mol/L×0.05L/0.1L]=0.01mol/L,
pH=2,
故答案为:1.8×10-7 mol/L; 2.点评:
本题考点: 酸碱混合时的定性判断及有关ph的计算;弱电解质在水溶液中的电离平衡;难溶电解质的溶解平衡及沉淀转化的本质.
考点点评: 本题考查较为综合,题目难度较大,易错点为(1),注意弱电解质的比较方法以及判断角度.1年前查看全部
- 常温下能使溴的四氯化碳溶液及高锰酸钾溶液褪色的烃类物质是
 理吾直1年前2
理吾直1年前2 -
 vivianyoung 共回答了17个问题
vivianyoung 共回答了17个问题 |采纳率94.1%不饱和烃均可(除去单环类)
另外苯的同系物可以使酸性高锰酸钾溶液退色,其侧链的烃基被氧化成羧基(-COOH),这也是鉴别苯和苯的同系物的一种方法1年前查看全部
- 化学(是否正确)以下说法是否正确?常温下,0.1 mol/L某一元弱酸(HA)溶液中加入一定量的CH3COONa晶体或加
化学(是否正确)
以下说法是否正确?
常温下,0.1 mol/L某一元弱酸(HA)溶液中加入一定量的CH3COONa晶体或加水稀释,溶液的c(OH-)均增大. 罗白菜1年前3
罗白菜1年前3 -
 爱的精灵 共回答了23个问题
爱的精灵 共回答了23个问题 |采纳率87%加入醋酸钠晶体是增大的,CH3COO- + H+ H+ + OH-表面上看加入水后平衡向右移动,OH浓度上升,但是加水稀释的倍数远比平衡移动增加的量大得多,所以应该是减小的1年前查看全部
- 1:常温下,把下列四种X的溶液分别加入四个盛有10mL 2mol`L-1的盐酸的烧杯中,均加入水稀释至50mL.此时,X
1:常温下,把下列四种X的溶液分别加入四个盛有10mL 2mol`L-1的盐酸的烧杯中,均加入水稀释至50mL.此时,X和盐酸缓慢的进行反应,其中反应速率最大的是( )
A.20mL .3mol`L-1 B:20mL.2mol`L-1
C:10mL,4mol`L-1 D:10mL,2mol`L-1 cuo_xiao1年前2
cuo_xiao1年前2 -
 幽兰心 共回答了21个问题
幽兰心 共回答了21个问题 |采纳率90.5%化学反应的速率和温度,浓度,接触面积有关
由于最后都是稀释到50ML常温代表温度一样,接触面积由于都是50ML溶液当然一样
之和浓度有关,又因为最后体积一样,所以我们只需要加入的X的物质的量最大就可以了
A0.06mol
B0.04mol
C0.04mol
D0.02mol
所以最后的溶液中A的浓度最大,所以速率最大
选A1年前查看全部
- 常温下将Vml 0.1mol/L的盐酸和0.06mol/L的Ba(oh)2混合,则溶液的PH等于12.问混合加入的氢氧化
常温下将Vml 0.1mol/L的盐酸和0.06mol/L的Ba(oh)2混合,则溶液的PH等于12.问混合加入的氢氧化钡的体积为
 半丝伴缕1年前3
半丝伴缕1年前3 -
 107320751 共回答了13个问题
107320751 共回答了13个问题 |采纳率76.9%V mL
设混合加入的氢氧化钡的体积为x mL.
1个HCl含有1个H+,H+的物质的量是V*10^-3*0.1=10^-4mol
1个Ba(OH)2含有2个OH-,OH-的物质的量是x*10^-3*0.06*2=1.2*10^-4mol
pH=12,c(OH-)=10^-2 mol/L
H+ +OH-=H2O
1 1
混合后pH=12,所以是碱过量.
(x*1.2*10^-4 - V*10^-4)/(V*10^-3+x*10^-3)=10^-2
x=V mL1年前查看全部
- 常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
其中反应速率最大的是 A.20mL,3 mol·L-1 B.25mL,2 mol·L-1
C.10mL,3 mol·L-1 D.18mL,4 mol·L-1 winging1231年前1
winging1231年前1 -
 洪都拉斯小猪 共回答了15个问题
洪都拉斯小猪 共回答了15个问题 |采纳率86.7%常温下把4种不同体积不同浓度的醋酸溶液分别加入4个盛有10mL2mol/L氢氧化钠溶液中并加水稀释到100ml
D.18mL,4 mol·L-1中所含醋酸最多 所以加水稀释到100ml浓度最大,速率最快1年前查看全部
- 已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料
已知A、B、C、D、E、F、G是初中化学常见的物质,A在常温下是一种无色液体,D是天然气的主要成分,G是一种重要建筑材料的主要成分,E是一种金属氧化物,与A反应能生成一种常见的碱.它们之间的转换关系如图所示:
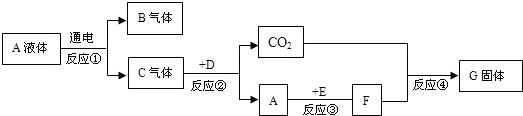
(1)写出下列物质的化学式:A______、D______.
(2)写出反应②的化学方程式CH4+2O2
CO2+2H2O点燃 .CH4+2O2.
CO2+2H2O点燃 .
(3)F在日常生活中用途广泛,请写出其中一点______.
(4)反应③属于______反应(填“化合”、“分解”、“置换”、“复分解”).
(5)B是最清洁的燃料,与其它燃料相比其优点有______. cqycqy1年前1
cqycqy1年前1 -
 leyons 共回答了18个问题
leyons 共回答了18个问题 |采纳率83.3%解题思路:根据题目中的信息:“D是天然气的主要成分”,说明D是甲烷;“G是一种重要建筑材料的主要成分”,说明G是碳酸钙;“E是一种金属氧化物,与A反应能生成一种常见的碱”,而“A在常温下是一种无色液体”,说明E是氧化钙,A为水;那么B和C为氢气和氧气,C和D反应生成二氧化碳和A即水,说明C为氧气,而B为氢气,水和E(氧化钙)反应生成了F,说明F为氢氧化钙,氢氧化钙和二氧化碳反应生成了碳酸钙.代入题目,符合刚才的推断,可以据此答题.根据题目中的信息:“D是天然气的主要成分”,说明D是甲烷;“G是一种重要建筑材料的主要成分”,说明G是碳酸钙;“E是一种金属氧化物,与A反应能生成一种常见的碱”,而“A在常温下是一种无色液体”,说明E是氧化钙,A为水;那么B和C为氢气和氧气,C和D反应生成二氧化碳和A即水,说明C为氧气,而B为氢气,水和E(氧化钙)反应生成了F,说明F为氢氧化钙,氢氧化钙和二氧化碳反应生成了碳酸钙.
(1)“A在常温下是一种无色液体”,又能在通电的条件下分解得两种气体,说明A为水,“D是天然气的主要成分”,说明D为甲烷
(2)A通电能够生成氢气和氧气,C能够和甲烷反应生成二氧化碳和水,所以B是氧气;故化学方程式为CH4+2O2
点燃
.
CO2+2H2O;
(3)F是氢氧化钙,在日常生活中常被用作建筑材料;
(4)反应③是氢氧化钙和水反应生成氢氧化钙的过程,其反应物是两种生成物是一种,该反应符合“多变一”的化合反应特征;
(5)B为氢气在燃烧时产生水,不会污染空气.
故答案为:(1)H2O;CH4;(2)CH4+2O2
点燃
.
CO2+2H2O;(3)做建筑材料;(4)化合;(5)生成物都是水,无污染(热值大;来源广泛).点评:
本题考点: 物质的鉴别、推断;化学式的书写及意义;反应类型的判定;书写化学方程式、文字表达式、电离方程式;氢气的用途和氢能的优缺点.
考点点评: 本题为框图式物质推断题,完成此类题目,关键是找准解题突破口,根据物质的化学特性直接得出结论,然后顺藤摸瓜,利用顺推或逆推或从两边向中间推断,逐步得出其他结论.1年前查看全部
- 镁与氧气在常温下反应么?镁条可以在点燃的条件下与氧气反应在常温下可以么?不是金属燃烧,是说它们常温发生氧化反应
 doom-sol1年前3
doom-sol1年前3 -
 mariaselfheaven 共回答了29个问题
mariaselfheaven 共回答了29个问题 |采纳率89.7%不能,金属燃烧反应通常都需要加热
氧化反应在常温下是可以进行的1年前查看全部
- 常温下的绝缘体在极低温度下可以变成超导体吗?
 wenxo19761年前1
wenxo19761年前1 -
 easonico1 共回答了21个问题
easonico1 共回答了21个问题 |采纳率90.5%当然可以.比如说水银4K左右变成超导体,是世界上发现的第一个
超导体.现在铜氧化物的超导转变温度已经超多100K.另外
MgB2大概39K.2008年后发现的铁基已经达到55K左右、1年前查看全部
- 金刚石在空气中的常温会一点点氧化吗 如果它失掉电子,会捕捉空气中的电子吗
 七翅天使1年前1
七翅天使1年前1 -
 duqixi 共回答了22个问题
duqixi 共回答了22个问题 |采纳率81.8%金刚石是单质碳,它与石墨是同一种成分,是碳的一种同素异形体,碳的化学性质不活泼,很稳定,碳的外层电子有4个,它最多失去4个电子,得到也还是4个,这就决定了它化学性质的稳定.除非外界条件改变,如高温等,否则常温它不会被氧化.如果它失去电子那么碳就显正电性,但在空气中,显正电性的碳具有氧化性,而空气中的其他气体 要么氧化性更强,要么稳定性强,不容易被碳氧化,因此也不容易得到电子.1年前查看全部
- 天空晴朗时,对于0.4-1.4微米的所有波长,在野外利用不同波段的遥感设备观测理想的常温黑体和同等温度的灰体表面,观测到
天空晴朗时,对于0.4-1.4微米的所有波长,在野外利用不同波段的遥感设备观测理想的常温黑体和同等温度的灰体表面,观测到的黑体表面的数值总比灰体的大么?为什么?
 我们记录1年前1
我们记录1年前1 -
 好心要让你听见 共回答了23个问题
好心要让你听见 共回答了23个问题 |采纳率95.7%不一定,不同的物体的发射率不同,定向发射率也不同,尽管黑体的辐射能力更强,但他们的表面状况等都不明确,0.4到1.4微米,有可见光部分以及微波部分,这道题涉及了遥感分析原理与应用书中的三四五章,需要对于各个波段进行区分,可见光—近红外的,热红外的,微波的不同情况,可以提一些定量遥感的知识,北师大科研项目很多都在这方面,主要是李院士太牛了,哈哈
这样的题能体会出对于这个专业的全局的认识,需要好好准备,组织好之后找专业课老师看看吧,我曾经写过,但是笔记找不到了,另外,很快就考试了,调整好心态,北师的遥感专业课没有那么恐怖(比起数据结构),祝你成功1年前查看全部
- 0.6%硫代巴比妥酸溶液短期内能在常温避光条件下存放吗?用于测植物丙二醛的
 君一1年前1
君一1年前1 -
 我很强 共回答了20个问题
我很强 共回答了20个问题 |采纳率85%能1年前查看全部
- 疑问1:常温下铵根离子与氢氧离子能共存吗?疑问2:加热条件下铵根离子与氢氧根离子能共存吗?请把...
疑问1:常温下铵根离子与氢氧离子能共存吗?疑问2:加热条件下铵根离子与氢氧根离子能共存吗?请把...
疑问1:常温下铵根离子与氢氧离子能共存吗?疑问2:加热条件下铵根离子与氢氧根离子能共存吗?请把其中的知识与原理详细的“分条”“分点”解
有些网友说常温下这两种能共存,理由是常温下氨水中存在这两中离子;可有些网友说常温下这两种离子不能共存,理由是常温下生成了难电离的弱电解?到底谁说得对呢?谁能把这里面牵扯到的化学知识详详细细地解说一下,一定要准确严谨! sweetmint1年前5
sweetmint1年前5 -
 szvnym 共回答了21个问题
szvnym 共回答了21个问题 |采纳率85.7%常温下能共存,氨水中就有这两种离子
加热下不共存,因为它们会形成NH3挥发掉1年前查看全部
- abcd四种化合物,常温下,固体a跟b溶液反应生成无色气体c逸出,将c导入...
abcd四种化合物,常温下,固体a跟b溶液反应生成无色气体c逸出,将c导入...
abcd四种化合物,常温下,固体a跟b溶液反应生成无色气体c逸出,将c导入氢氧化钠可生成a,将c氧化后得到d,将d导入水中得到b, zhuyes1年前3
zhuyes1年前3 -
 saner32 共回答了24个问题
saner32 共回答了24个问题 |采纳率87.5%i问题不完整啊,下面是我猜的
a为Na2SO3,b为H2SO4 c 为二氧化硫,d为三氧化硫1年前查看全部
- 常温条件下,核糖核酸与甲基绿作用呈现绿色.为什么错
 andy_sk2281年前2
andy_sk2281年前2 -
 yunasa 共回答了18个问题
yunasa 共回答了18个问题 |采纳率88.9%甲基绿应该亲和DNA,吡罗红才亲和RNA1年前查看全部
- 一氧化碳在常温下跟氧气反应是否能生成CO2
 红蕊1年前1
红蕊1年前1 -
 tpzy82 共回答了24个问题
tpzy82 共回答了24个问题 |采纳率95.8%不反应1年前查看全部
- 常温下,pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol/L的碘酸(
常温下,pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显酸性;0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性.
请回答下列问题:
(1)高碘酸是______(填“强酸”或“弱酸”),理由是______.
(2)0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合所得溶液中IO3-与Na+的浓度关系是______(填“大于”、“小于”或“等于”).
(3)已知高碘酸和硫酸锰在溶液中反应生成高锰酸、碘酸和硫酸,此反应中的还原剂是______(写化学式),该反应的离子方程式为______. mengfan1501年前1
mengfan1501年前1 -
 christy蓝薇 共回答了15个问题
christy蓝薇 共回答了15个问题 |采纳率86.7%解题思路:(1)pH=2的高碘酸溶液与pH=12的NaOH溶液中氢离子浓度和氢氧根离子的浓度相等,氢氧化钠是强碱,讨论高碘酸分别为强酸或弱酸,根据反应后溶液的酸碱性判断;
(2)由0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性,说明碘酸(HIO3)或高锰酸(HMnO4)都是强酸,0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合,两者恰好完全反应,生成碘酸钠,是强酸强碱盐,溶液呈中性,c(H+)=c(OH-),电荷守恒知,c(IO3-)+c(OH-)=c(H+)+c(Na+),所以液中IO3-与Na+的浓度相等;
(3)高碘酸和硫酸锰在溶液中反应生成高锰酸、碘酸和硫酸,根据化合价的变化结合氧化还原反应得失电子数目相等书写离子方程式.(1)pH=2的高碘酸溶液与pH=12的NaOH溶液中氢离子浓度和氢氧根离子的浓度相等,氢氧化钠是强碱,等体积混合时,若溶液呈中性,说明氢离子和氢氧根离子恰好反应,高碘酸是强酸,但实际上混合溶液呈酸性,这说明高碘酸又电离出部分氢离子,所以高碘酸是弱酸,
故答案为:弱酸;pH=2的高碘酸电离出的c(H+)和pH=2的NaOH溶液电离出的c(OH-)相等,且两者体积相等,但所得溶液显酸性,则高碘酸必定是不完全电离,所以高碘酸是弱酸;
(2)由0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得溶液显中性,说明碘酸(HIO3)或高锰酸(HMnO4)都是强酸,0.01mol/L的碘酸(HIO3)溶液与pH=12的NaOH溶液等体积混合,两者恰好完全反应,生成碘酸钠,是强酸强碱盐,溶液呈中性,c(H+)=c(OH-),电荷守恒知,c(IO3-)+c(OH-)=c(H+)+c(Na+),所以液中IO3-与Na+的浓度相等,故答案为:等于;
(3)高碘酸和硫酸锰在溶液中反应生成高锰酸、碘酸和硫酸,反应中Mn元素的化合价升高,则MnSO4为还原剂,在酸性条件下高碘酸和锰离子发生氧化还原反应生成生成高锰酸、碘酸和硫酸,所以离子方程式为2Mn2++5HIO4+3H2O═2MnO4-+5IO3-+11H+,故答案为:MnSO4;2Mn2++5HIO4+3H2O═2MnO4-+5IO3-+11H+.点评:
本题考点: 酸碱混合时的定性判断及有关ph的计算.
考点点评: 本题考查酸碱混合反应以及氧化还原反应,题目难度中等,解答本题时注意判断酸碱溶液中氢离子和氢氧根离子的物质的量关系,根据反应后溶液的酸碱性判断,本题易错点为(2),注意电解质强弱的判断.1年前查看全部
- 常温下,已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得...
常温下,已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得...
常温下,已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液显酸性.0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液显中性.已知高碘酸和硫酸锰在溶液中反应生成高猛酸,碘酸和硫酸,该反应的反应式怎么写 ncrecentl1年前1
ncrecentl1年前1 -
 xudukeren 共回答了13个问题
xudukeren 共回答了13个问题 |采纳率92.3%5H5IO6 + 2 Mn2+ =2MnO4- + 5IO3- + 11H+ +7 H2O
已知pH=2的高碘酸(H5IO6)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液显酸性,可以推出——高碘酸(H5IO6)是弱酸,要书写化学式,不能写成离子形式
0.01mol/L的碘酸(HIO3)或高锰酸(HMnO4)溶液与pH=12的NaOH溶液等体积混合,所得混合溶液显中性,可以推出——碘酸(HIO3)或高锰酸(HMnO4)是强酸,要写成离子形式1年前查看全部
- 现有A~F六种常见的物质,其中A到E为均不含金属元素,F为大理石的主要成分,A、B常温下为液态.且他们互相之间存在如下转
现有A~F六种常见的物质,其中A到E为均不含金属元素,F为大理石的主要成分,A、B常温下为液态.且他们互相之间存在如下转化关系,箭头表转化方向,双箭头表示互相间可以发生转化.请你推断A.F六种物质各是什么物质.
 lg99065201年前4
lg99065201年前4 -
 qiandd 共回答了19个问题
qiandd 共回答了19个问题 |采纳率94.7%筒子好、同北郊的.
你们家作也这个阿、
A水 B过氧化新 C氧气 D二氧化碳 E碳酸(H2CO3) F碳酸钙.
下面的自己应该会了、、本人7班的.1年前查看全部
- 常温和室温各是多少度?这两个温度下,水的电离平衡常数有什么变化和不同?
 xiaotaohua1年前1
xiaotaohua1年前1 -
 suibian1981 共回答了21个问题
suibian1981 共回答了21个问题 |采纳率100%常温 室温
20度 25度
室温 高于 常温
水的电离平衡常数随温度升高而升高
故室温下水的电离平衡常数大1年前查看全部
- CuSO4溶于水时的水溶液为蓝色,那么CuSO4在常温下溶于水是不是不会与水发生反应?
 黄帝1年前1
黄帝1年前1 -
 笑霸天_心问佛 共回答了19个问题
笑霸天_心问佛 共回答了19个问题 |采纳率94.7%先CuSO4在水中全部电离,很少一部分与水发生水解反应,
化学方程式:CuSO4 + 2H2O(可逆) Cu(OH)2 + H2SO4
离子方程式:Cu2+ 2H2O(可逆) Cu(OH)2 +2H+
大部分CuSO4溶于水电离生成Cu2+离子和SO42-离子,所以溶液呈蓝色(即Cu2+颜色)..
只有加CuSO4固体过多,溶液成饱和溶液后,有蓝色晶体析出.
CuSO4+ 5H2O = CuSO4.5H2O1年前查看全部
- 常温下,AI与哪些酸发生钝化现象?
 zxj04091年前2
zxj04091年前2 -
 吃大白兔奶糖 共回答了22个问题
吃大白兔奶糖 共回答了22个问题 |采纳率90.9%浓硫酸、浓硝酸 注意浓1年前查看全部
- 常温下饱和碘化铅溶液和饱和氯化氨溶液的浓度各是多少?
 lrongx1年前1
lrongx1年前1 -
 dd公贼 共回答了14个问题
dd公贼 共回答了14个问题 |采纳率92.9%室温时,碘化铅的容度积(Ksp)为1.7×10的负9次方mol/L负3次,溶液浓度1.19×10^(-3)mol/L.
氯化铵在水中溶解度列表:
0℃:29.4g
10℃:33.3g
20℃:37.2g
30℃:41.4g
40℃:45.8g
50℃:50.4g
60℃:55.2g
70℃:60.2g
80℃:65.6g
90℃:71.3g
100℃:77.3g
常温按20℃,溶解度s=37.2g,饱和溶液中氯化铵的质量分数为27.1%,没有密度不好计算物质的量浓度.1年前查看全部
- 常温下,决定晶体热导和金属电阻的主要因素是什么?如果不是常温,影响晶体热导的因素是什么?影响金属热导的因素是什么?
 tbest1年前2
tbest1年前2 -
 迷惘小伙 共回答了11个问题
迷惘小伙 共回答了11个问题 |采纳率100%晶格畸变程度和晶界密度.间隙原子越多、位错密度越高、晶格畸变程度越大、晶界越多的晶体声子散射越强,电阻越大.1年前查看全部
- 常温常压下一升二氧化碳变成多少克干冰?
常温常压下一升二氧化碳变成多少克干冰?
如题,最好能给出解题过程, wusrula1年前2
wusrula1年前2 -
 没有名字的心 共回答了15个问题
没有名字的心 共回答了15个问题 |采纳率93.3%先把1L转化成标况下的体积:
V/T=K ,V(273k)=1*273/298=0.916L
转换成物质的量;0.916/22.4=0.0409mol
计算成质量:0.0409*44=1.8g1年前查看全部
- 干冰暴露在常温下!干冰暴露在常温下是,它会直接由固态变为气态,这种现象叫( )用干冰( )在舞台上产生淡淡的白雾,是由于
干冰暴露在常温下!
干冰暴露在常温下是,它会直接由固态变为气态,这种现象叫( )
用干冰( )在舞台上产生淡淡的白雾,是由于干冰( ),使周围的空气温度降低,空气中的水蒸气遇冷( )形成( ). dxzll1年前6
dxzll1年前6 -
 wjm333 共回答了22个问题
wjm333 共回答了22个问题 |采纳率100%干冰暴露在常温下是,它会直接由固态变为气态,这种现象叫(升华)
用干冰(放置)在舞台上产生淡淡的白雾,是由于干冰(升华吸热),使周围的空气温度降低,空气中的水蒸气遇冷(凝结)形成(小液滴).1年前查看全部
- (NH4)2CO3+HClO=常温下(NH4)2CO3和足量HClO稀溶液反应的离子方程式
 乱草忌秋风1年前3
乱草忌秋风1年前3 -
 共苦同甘 共回答了19个问题
共苦同甘 共回答了19个问题 |采纳率89.5%CO3(2-)+2HClO===H2O+CO2(g)+2Cl(-)+O2(g)1年前查看全部
- 金刚石1000度可以缓慢变会石墨 那常温下会不会也在超级缓慢进行这种反应?
 蔡寒雨1年前5
蔡寒雨1年前5 -
 inn001 共回答了17个问题
inn001 共回答了17个问题 |采纳率94.1%一百年有一个分子转变
那种速度可以理解为不进行1年前查看全部
- 酸碱混合常温下,将体积V1,PH=a,的某一元强碱与体积为V2,PH=b的某二元强酸混合.若所得溶液的PH=11,且a=
酸碱混合
常温下,将体积V1,PH=a,的某一元强碱与体积为V2,PH=b的某二元强酸混合.
若所得溶液的PH=11,且a=13,b=2,则V1:V2=__:__ liang36267991年前1
liang36267991年前1 -
 yu6112 共回答了19个问题
yu6112 共回答了19个问题 |采纳率89.5%(V1*0.1-V2*0.01)/(V1+V2)=0.001
V1:V2=1:91年前查看全部
- 常温下,固体分为晶体和非晶体.那么晶体与非晶体的最主要区别在哪里?
 hover1511年前5
hover1511年前5 -
 xx才 共回答了17个问题
xx才 共回答了17个问题 |采纳率94.1%晶体:具有固定熔沸点
非晶体:没有固定熔沸点1年前查看全部
- 1.常温下,在含有氢离子、氯离子和三价铁离子的溶液中加入下列离子后,溶液中各种离子仍能大量共存的是
1.常温下,在含有氢离子、氯离子和三价铁离子的溶液中加入下列离子后,溶液中各种离子仍能大量共存的是
A.硝酸根离子 B.CLO离子 C.碳酸氢根离子 D.碘离子
2.在下列化合物中,只有在水溶液中才能导电的电解质是
A.氯化钠 B.酒精 C.硫酸 D.硫酸钾
麻烦给出正确答案和解释. 别封啦prhlt0id1年前4
别封啦prhlt0id1年前4 -
 mrdawei0 共回答了16个问题
mrdawei0 共回答了16个问题 |采纳率93.8%1:
a.正确
b会和cl-发生氧化还原反应、
c会和h+反应生成co2
d会和fe3+发生氧化还原反应到I和fe2+
2:
a熔融状态下也行.
b是非电解质,水溶液中肯定不导电
c正确
d与a一样.
加油咯!1年前查看全部
大家在问
- 1用表示a的小数部分,(a)表示不超过a的最大整数,记f(x)=2x+1分之x+2,则=( )
- 2荔园小学三年级上学期语文期中质量检测试卷的反思怎么写?
- 3(2013•湖北)已知α,β是一元二次方程x2-5x-2=0的两个实数根,则α2+αβ+β2的值为( )
- 4(2013•道里区三模)A′B′是物体AB通过凸透镜成的像,请在图中准确画出凸透镜及凸透镜一侧焦点F的位置.
- 5有一段钢可做成一个底面直径8厘米,高9厘米的圆钢,如果把这段钢做成一个高12厘米圆锥形的零件,它的底面积是多少平方厘米?
- 6David had a cold yesterday.改成否定句.david()()a cold yesterday.
- 7同学们,请安静 让我来帮你吧 请给我看一下你的身份证 翻译英语
- 8(-21x^3+7x^2-14x)÷(-7x)=?
- 9英国化学家戴维1806年,用电解的方法从苏打中得到一种金属,他对新金属作了如下实验:取一小块金属,用小刀切下一小块金属,
- 10许多农民往往直接将农作物秸秆焚烧归田,请你从物质循环的角度分析这种做法的利于弊?
- 11已知f(x)=xe^x,g(x)=-(x+1)^2+a,若存在x1,x2属于R,使得f(x2)≤g(x1)成立,则实数a
- 12带单位名称嘛?
- 13细菌在生态系统的什么流动和什么循环中起到重要的作用?
- 14下列说法错误的是( )A.化学反应的限度可以通过改变条件而改变B.可逆反应达到平衡状态时,就是此条件下该反应所能达到的
- 15硫酸铵中氮氢硫氧元素的原子个数比 :