前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的
 kamiabaji2022-10-04 11:39:541条回答
kamiabaji2022-10-04 11:39:541条回答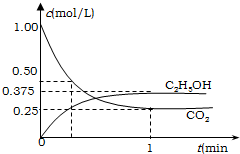 前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.
前些天在北京、西安、南昌等25个大中城市都出现雾霾天气,人类的活动改变了全球的气候.全球气候变暖已经成为全世界人类面临的重大问题.(1)地球上的能源主要源于太阳,绿色植物的光合作用可以大量吸收CO2以减缓温室效应,主要过程可以描述分为下列三步:
Ⅰ、H2O(l)═2H+(aq)+[1/2]O2(g)+2e-△H═+284kJ•mol-1
Ⅱ、CO2(g)+C5H10O4 (s)+2H+(aq)═2C3H6O3+(s)△H═+396kJ•mol-1
Ⅲ、12C3H6O3+(s)+12e-═C6H12O6(s)+6C5H10O4 (s)+3O2(g)△H═-1200kJ•mol-1
写出绿色植物利用水和二氧化碳合成葡萄糖并放出氧气的热化学方程式______.
(2)降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料乙醇.为探究反
应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反
应:CO2(g)+3H2(g)⇌[1/2]CH3CH2OH(g)+[3/2]H2O(l)△H=-683kJ•mol-1.测得CO2和C2H5OH(g)的浓度随时间变化如图所示.
①该反应的平衡常数为
0.375
| ||
| 0.25×0.753 |
0.375
| ||
| 0.25×0.753 |
②关于该反应的下列说法中,正确的是______.
A.△H>0,△S>0B.△H>0,△S<0C.△H<0,△S<0D.△H<0,△S>0
③当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2.则c1______c2的关系(填>、<、=).

已提交,审核后显示!提交回复
共1条回复
 教zz007 共回答了17个问题
教zz007 共回答了17个问题 |采纳率100%- 解题思路:(1)依据盖斯定律和热化学方程式计算得到所需的热化学方程式,利用热化学方程式的加减消去不需要的物质,注意加减时焓变随之变化;
(2)化学平衡常数K=[各个生成物平衡浓度系数次幂之积/各个产物平衡浓度系数次幂之积],据此计算;
(3)根据衡移动的影响知识来回答.(1)依据盖斯定律由题干所给的热化学方程式,结合盖斯定律计算(①+②)×6+③得到绿色植物利用水和二氧化碳合成葡萄糖并放出氧气的热化学方程式,
6CO2(g)+6H2O(g)=C6H12O6(葡萄糖、s)+6O2(g)△H=[(+284KJ/mol)+(+396KJ/mol)]×6+(-1200KJ/mol)=+2880KJ/mol;
则△H=[(+284KJ/mol)+(+396KJ/mol)]×6+(-1200KJ/mol)=+2880KJ/mol,即6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJ•mol-1,故答案为:6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g)△H=+2880 kJ•mol-1;
(2)①根据表中数据,化学平衡常数K=[各个生成物平衡浓度系数次幂之积/各个产物平衡浓度系数次幂之积]=
c(CH3CH2OH)
1
2×c(H2O)
3
2
c(CO2)×c(H2)3=
0.375
1
2
0.25×0.753 (水的浓度是1),故答案为:
0.375
1
2
0.25×0.753;
②根据反应的焓变知道反应是放热的,所以△H<0,产物气体的物质的量小于反应物气体的总物质的量,所以反应的熵变小于零,故选C.
③当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,平衡会正向移动,但是不能完全消耗,所以H2的物质的量浓度增加,故答案为:<.点评:
本题考点: 热化学方程式;焓变和熵变;化学平衡常数的含义;化学平衡的影响因素.
考点点评: 本题涉及热化学中盖斯定律的应用、化学平衡常数表达式的书写、平衡移动的影响因素等知识,注意知识的归纳和梳理是解题的关键,难度中等. - 1年前
相关推荐
- 呜呜~还有20天就开学了,时间过得好快啊~可我作业一个字也没写,前些天都在玩,我决定从今天开始写作业,大家说说我应该怎样
呜呜~还有20天就开学了,时间过得好快啊~可我作业一个字也没写,前些天都在玩,我决定从今天开始写作业,大家说说我应该怎样安排吧~
 feng_8161年前1
feng_8161年前1 -
 绕指银蛇 共回答了26个问题
绕指银蛇 共回答了26个问题 |采纳率100%我也是倒数二十天开始写的 把作业剩下的页数加起来除以二十 知道你每天的目标是多少 最起码做到哪一页 有能力多做几页就几页 减轻之后的负担233我就是这样1年前查看全部
大家在问
- 1句子赏析:1.她不愧是赏月的行家,在她的眼里,月的阴晴圆缺无不各具风韵.2.她牢牢盯着月亮,就像财主
- 2暮霭沉沉楚天阔 后边是什么
- 3哪个给我讲一下就是初一数学有理数和相反数,这些我知道,就是化简不懂,谁讲一下
- 4子曰:由,诲女知之乎!知之为知之,不知为不知,是知也”
- 5口算题...a-b/a+b除以1/b-a*1/a-b
- 6求值:(1)[(−5)4]14-(15)0;(2)[(338)−23•(545)0.5+(0.008)−23÷(0.02
- 7《试卷发下来》为题目,写一篇350字的作文
- 8现只有稀盐酸、浓硫酸和Na2CO3溶液.要用如图所示装置对H2和CO2的混合气体进行分分离和干燥,则:①甲中应
- 9原生木浆与原生浆的区别
- 10六一班办了科技和美术两个兴趣组(每人至少参加一样),已知全班有五分之三参加美术组,十分之七参加科技
- 11明天你去图书馆看书?明天你去儿童公园玩?(用上合适的关联词语,把上面的两句话连成一句话)
- 12如何剪围成八个一圈的小人
- 13已知某池塘养殖着鲤鱼和鲫鱼,为了估计这两种鱼的数量,养殖者从池塘中捕出两种鱼各 只,给每只鱼做上不影响其存活的标记,然后
- 14有些理论上不能反应的反应却实现了比如钠置换钾.氢氟酸和二氧化硅反应.都是因为生成气体离开体系导致反应向正方向进行 那我想
- 15通过复习总结,你认为下列对化学知识概括合理的组合是 (
