56gFe粉投入500g稀HNO3中,两者恰好完全反应放出NO,溶液增重32g,则反应后,溶液中金
 west19852022-10-04 11:39:543条回答
west19852022-10-04 11:39:543条回答
56gFe粉投入500g稀HNO3中,两者恰好完全反应放出NO,溶液增重32g,则反应后,溶液中金
56gFe粉投入500g稀HNO3中,两者恰好完全反应放出NO,溶液增重26g,则反应后,溶液中金属离子是什么并说明理由
说错了 是32g不是26g~
56gFe粉投入500g稀HNO3中,两者恰好完全反应放出NO,溶液增重26g,则反应后,溶液中金属离子是什么并说明理由
说错了 是32g不是26g~

已提交,审核后显示!提交回复
共3条回复
 chupachupa 共回答了18个问题
chupachupa 共回答了18个问题 |采纳率83.3%- 我是按26g算的
首先 写出化学式 Fe+4HNo3==NO+Fe(NO3)3+2H2O
下来铁有56g也就是1mol
由化学式可知出来30g气体也就是NO(1mol)
溶液就+了26g
分析完了
溶液中有 3价铁离子 硝酸根离子 氢离子 氢氧根离子 应该全了
求赞 - 1年前
 种子424讨力 共回答了310个问题
种子424讨力 共回答了310个问题 |采纳率- 56gFe粉是1mol,挥发的NO的质量为56g-26g=30g
即1mol,由于还原得到1molNO,
所以铁失去3mol电子而变成1molFe3+离子,
发生的反应为:Fe+4HNO3=Fe(NO3)3+NO+2H2O,
所以溶液中金属离子是三价铁离子.
不懂的欢迎追问,如有帮助请采纳,谢谢! - 1年前
 夏日冰块 共回答了82个问题
夏日冰块 共回答了82个问题 |采纳率- 先用质量守恒定律算出NO质量是56-26=30g
那么NO就是1mol。再根据电子守恒,1mol的NO生成要得到3mol的电子,Fe 56克也是1mol
所以每个Fe失去3mol电子就是正三价的Fe3+
——————————————————————————————————
如果是32克,那么NO质量是56-32=24克,物质的量是24/30=0.8mol
一... - 1年前
相关推荐
- 某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16浓HNO3,反应过程中产生气体的体积和反应时间
某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16浓HNO3,反应过程中产生气体的体积和反应时间的关系如图所示,最后固体全部溶解,气体体积均在标准状况下测定.假设反应中HNO3的还原产物只有NO和NO2,那么理论上从哪一时刻开始产生NO()
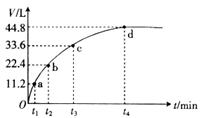
若fe与硝酸反应全部为fe(no3)3则需要硝酸(56g÷56g/mol)×3+44.8l÷22.4l/mol
=5 mol <6.4 (6.4=16×0.4)因此硝酸足量,根据原子守恒n(no)+n(no2)=2,电荷守恒可得 3n(no)+n(no2)=3 ,解得n(no2)=1.5mol 即33.6l.
电荷守恒可得 3n(NO)+n(NO2)=3 ,解得n(NO2)=1.5mol 即33.6L
这句话是什麽意思啊?哪两个离子的电荷守恒? 枳子花1年前1
枳子花1年前1 -
 acwy1984 共回答了13个问题
acwy1984 共回答了13个问题 |采纳率76.9%实际是电子守恒,即得失电子数相等,铁有1摩尔,反应后变成+3价,失去3摩尔电子,HNO3中的N原子得到3摩尔电子,得到n(no)+n(no2)=3 .1年前查看全部
- 高中无机化学的一个图像题某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16mol/L的浓HNO3
高中无机化学的一个图像题
某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16mol/L的浓HNO3,反应过程中产生气体的体积和反应时间的关系如图所示,最后固体全部溶解,气体体积均在标准状况下测定.假设反应中HNO3的还原产物只有NO和NO2,那么理论上从哪一时刻开始产生NO( )
A.t1 B.t2 C.t3 D.t4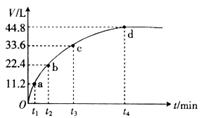
 cyf75105341年前1
cyf75105341年前1 -
 qqfish 共回答了19个问题
qqfish 共回答了19个问题 |采纳率94.7%吧
先是看成铁跟浓硝酸反应生成二价铁离子,然后同时二价铁被较稀的硝酸氧化成三价铁1年前查看全部
- 高中无机化学的一个图像题某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16mol/L的浓HNO3
高中无机化学的一个图像题
某温度下,向一洁净干燥的烧杯中加入56gFe粉,然后加入400 mL 16mol/L的浓HNO3,反应过程中产生气体的体积和反应时间的关系如图所示,最后固体全部溶解,气体体积均在标准状况下测定.假设反应中HNO3的还原产物只有NO和NO2,那么理论上从哪一时刻开始产生NO( )
A.t1 B.t2 C.t3 D.t4
答案有一步看不懂啊,说是Fe与HNO3反应若是全部生成Fe(NO3)3的话,需要HNO3:56g/(56g/mol)·3+44.8L/(22.4mol/L)=5,什么意思?看不懂啊...TAT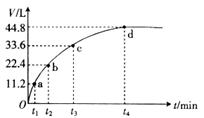
 cyj_lei1年前1
cyj_lei1年前1 -
 hh者一脚踩脸上 共回答了13个问题
hh者一脚踩脸上 共回答了13个问题 |采纳率92.3%Fe与硝酸反应,硝酸里面的N有2个去处
1个是与三价铁结合生成硝酸铁,这个是56g/(56g/mol)*3
另一个是被还原,1份硝酸对应1份气体(N原子守恒),也就是气体的物质的量44.8L/(22.4mol/L)1年前查看全部
大家在问
- 1书山有路的后一句是什么
- 2从哪些看出作者的态度《伤仲永》
- 3为什么浓硫酸有强氧化性,稀硫酸却没有?
- 4伤仲永中的第二段中,一"闻"一"见"一"问",表现了作者对伤仲永什么样的态度?
- 516.My American friend knows my problem because I ( ) my idea
- 6弹性势能与弹力的区别它们有关系吗
- 7检验空气,氧气,二氧化碳,要在瓶内放进什么?
- 8谁知道背英文快的方法,急
- 9什么方法可以背英语更快?背的是文章.
- 10叶绿体中ATP所储存的能量和可以接收的能量分别是( )
- 11请问“学无止境”英文怎么讲?
- 12因式分解:4a的立方-4a的平方b+ab的平方
- 13崂山道士 加点字解释,帮个忙 阴有志归 阴 尚无灯烛 尚俄顷,月明辉室 俄顷 辉分赉诸徒 赉良宵胜乐 胜然不胜酒力矣 胜
- 14在算式A×(B+C)=110+C中,A、B、C是三个互不相等的质数,那么B= ___ .
- 15在X+2Y=Z+2W反应中,若8克和32克Y恰好完全反应,生成18克W,且Z的相对分子质量是44,则Y的相对分子质量是
