1.最外层有2个电子的原子都是金属原子
 mj520312022-10-04 11:39:541条回答
mj520312022-10-04 11:39:541条回答2.非金属元素呈现的最高化合价不超过该元素原子的最外层电子数
如有错最好能说明理由

已提交,审核后显示!提交回复
共1条回复
 独孤碧血箭 共回答了23个问题
独孤碧血箭 共回答了23个问题 |采纳率95.7%- 1X,氦最外层2个电子,是非金属.
2V - 1年前
相关推荐
- 若某元素原子最外层电子数为1,则一定在第一主族对吗?
 j123123us1年前12
j123123us1年前12 -
 弄个名字好难 共回答了17个问题
弄个名字好难 共回答了17个问题 |采纳率100%错误的.因为除了主族元素之外,还有副族元素.你看看可以元素周期表,有个IB族,金Au和银Ag最外层就是一个电子.1年前查看全部
- A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大.已知A与B不在同周期,A与C同主族B原子最外层电子
A、B、C、D、E是元素周期表中的短周期主族元素,且原子序数依次增大.已知A与B不在同周期,A与C同主族B原子最外层电子数是其电子层数的两倍,A、C、E原子最外层电子数之和为6D的氧化物具有两性,下列说法正确的是()
A.A、B只能形成一种化合物.B.离子半径:CE.DD.元素C、D的最高价氧化物对应水化物之间不能发生反应. fgmgupiao1年前2
fgmgupiao1年前2 -
 maggie_1983 共回答了20个问题
maggie_1983 共回答了20个问题 |采纳率95%A:氢
B:碳
C:钠
D:铝
E:硅
所以正确答案是C1年前查看全部
- 某元素的原子最外层只有一个电子,它跟卤素相结合时,可形成的化学键 [ ]
某元素的原子最外层只有一个电子,它跟卤素相结合时,可形成的化学键 [ ]A.一定是共价键
B.一定是离子键
C.可能是共价键,也可能是离子键
D.上述说法都不正确 飘雪8501年前1
飘雪8501年前1 -
 qingshan521 共回答了19个问题
qingshan521 共回答了19个问题 |采纳率84.2%C1年前查看全部
- 电学新手求助,关于电荷与电子!“电荷是指电子所携带的电量,科学实验发现的最小电荷量叫做原电荷”这句话中的电子是指最外层的
电学新手求助,关于电荷与电子!
“电荷是指电子所携带的电量,科学实验发现的最小电荷量叫做原电荷”这句话中的电子是指最外层的电子还是一个电子还是指全部核外电子,我不太理解这句话,感激不尽 justineyuan1年前1
justineyuan1年前1 -
 姚a姚 共回答了16个问题
姚a姚 共回答了16个问题 |采纳率87.5%电子是指核外电子其中的任一个电子,并不是全部.这个问题也困扰过我,如果你不能明白就提出化学微观吧1年前查看全部
- 在国庆典礼上,有一个方阵外层共100人,这个方阵一共有多少人?
 stevaying1年前2
stevaying1年前2 -
 LJSSK 共回答了14个问题
LJSSK 共回答了14个问题 |采纳率100%这样一个方阵需要26*26=676人.1年前查看全部
- abcde为周期表前20元素不是稀有气体原子半径依次减小ae同族a与c b与d 电子层数相差2 ab最外层电子数比为1比
abcde为周期表前20元素
不是稀有气体原子半径依次减小ae同族a与c b与d 电子层数相差2 ab最外层电子数比为1比4 c的最外电子数为次外层的3倍 abcd是什么元素 mm咸猪手1年前1
mm咸猪手1年前1 -
 ee的小路上 共回答了21个问题
ee的小路上 共回答了21个问题 |采纳率95.2%a=K b=Ca c=O d=Be e=H1年前查看全部
- 超氧化钾和臭氧化钾的化学式是什么?钾的最外层为1个那么他的化学价是什么
超氧化钾和臭氧化钾的化学式是什么?钾的最外层为1个那么他的化学价是什么
两个氧为负一价?没错吧 helioslee1年前2
helioslee1年前2 -
 秋水为仙 共回答了17个问题
秋水为仙 共回答了17个问题 |采纳率94.1%超氧化钾 KO2 两个氧原子组合成的显-1价1年前查看全部
- 离子价电子排布记得在网上查时,有说亚铁离子是从最外层开始失电子,那其他过渡金属是不是都是这样?为什么?不是最外层能量不是
离子价电子排布
记得在网上查时,有说亚铁离子是从最外层开始失电子,那其他过渡金属是不是都是这样?为什么?不是最外层能量不是最少的啊. jian606_11171年前1
jian606_11171年前1 -
 oumeng215 共回答了14个问题
oumeng215 共回答了14个问题 |采纳率92.9%不太好讲,要看该能级的电离能,个人见解;亚铁离子从稳定性而言我觉得先失去最外层似乎不是稳定的,但是可这样认为,这样的失去电子可能是因为在溶液中水合导致.若先失去外层电子,水合后的亚铁离子应该能量比水加上亚铁离子低很多.其他的也是类似分析.对于金属离子得失电子我尚未见到什么很有力的证据能说明一定是如何进行的,只能猜测其可能的.最外层的能量不能说“少”只能说是绝对值较小,正常情况下能级是和负的电子所在层的平方呈反比(这只是浅显的说),这对应的能量事实上就是电离能,详细写说明的话就是当电子能量大于这个电离能的情况,电子的能谱变成连续的,将不受到原子核库仑力的束缚.一般来说就是上述规律,但是伴随着电子的屏蔽、钻穿、能级交错,以及相对论效应,上述命题就不是完全正确的了.1年前查看全部
- 植树节时,四年级少先队员在正方形草坪上种的树苗排成了方阵,最外层每边种了10棵树苗,最外层一共种了多少棵?整个方阵一共种
植树节时,四年级少先队员在正方形草坪上种的树苗排成了方阵,最外层每边种了10棵树苗,最外层一共种了多少棵?整个方阵一共种了多少棵树苗?
 跳跳虎1年前4
跳跳虎1年前4 -
 生活精彩26 共回答了22个问题
生活精彩26 共回答了22个问题 |采纳率90.9%解题思路:最外层点数=每边点数×4-4;实心方阵中总点数=每边点数×每边点数;代入数据即可解答.10×4-4=36(棵),
10×10=100(棵),
答:最外层人数有36棵,整个方阵一共有100棵.点评:
本题考点: 方阵问题.
考点点评: 此题考查了方阵问题中:最外层点数=每边点数×4-4;实心方阵中总点数=每边点数×每边点数的灵活应用.1年前查看全部
- 九·阅读课文片段,回答问题蚁团在火舌氏的草丛间越来越迅速的滚动,并不断发出外层蚂蚁被烧焦后的爆裂的声响,但是蚁团却不见缩
九·阅读课文片段,回答问题
蚁团在火舌氏的草丛间越来越迅速的滚动,并不断发出外层蚂蚁被烧焦后的爆裂的声响,但是蚁团却不见缩小,显然,这群外层被灼焦的蚁国英雄们至死也不松动分毫,肝胆俱裂也不放弃自己的岗位.
1·“自己的岗位”是指(?).
2·这段话写出了(?).我对它产生了一种(?)之情. lxlzl1年前1
lxlzl1年前1 -
 oolbjs 共回答了23个问题
oolbjs 共回答了23个问题 |采纳率91.3%1、凝聚成蚁团
2、蚂蚁的团结的精神;敬畏
小朋友,阅读理解最好自己动脑筋哦~不要投机取巧1年前查看全部
- 第三周期元素的原子,其最外层P能级上仅有一个未成对电子,它最高价氧化物对应的水化物的酸根离子是?
第三周期元素的原子,其最外层P能级上仅有一个未成对电子,它最高价氧化物对应的水化物的酸根离子是?
A.RO3-
B.RO5-
C.RO42-
D.RO4- 一粒枸杞1年前1
一粒枸杞1年前1 -
 陌上冷青桑 共回答了17个问题
陌上冷青桑 共回答了17个问题 |采纳率82.4%第三周期的原子外层电子一定先排满3s轨道后再排入3p轨道,没有过渡金属,情况比较简单.
要想使相应氧化物水化物的酸根离子化合价最高,需要最外层电子数尽可能多;仅有一个未成对电子时,其它电子都已成对且对数最多时可以使电子数尽可能多.这样最外层可以有7个电子,最高可以达到+7价.D选项对应的就是+7价.验证:第三周期外层7电子对应的元素是Cl,ClO4^-(高氯酸根)也是存在的,符合题意.所以选D.1年前查看全部
- 原子结构 在足够大的压力下,使形成共价化合物(SiO2 P2O5为例)的原子间距减小后,硅原子和磷原子最外层所有电子会不
原子结构
在足够大的压力下,使形成共价化合物(SiO2 P2O5为例)的原子间距减小后,硅原子和磷原子最外层所有电子会不会受到氧原子的引力,而脱离原子轨道变成导电的自由电子? wang_lewis1年前1
wang_lewis1年前1 -
 rfjx103 共回答了15个问题
rfjx103 共回答了15个问题 |采纳率93.3%共价化合物的电子通常比单质元素稳定.你提到的共价化合物尤其如此.换句话说,要把电子“压”出来,选化合物不如选单质.
其次,即使能把共价化合物的最外层所有电子“压”出来,也不是因为受到氧原子的吸引力.完全是压力的作用.氧原子的作用和这个正好相反,氧是把电子更紧密地吸引在它周围.1年前查看全部
- 化学大神帮忙!一道选择题第三周期元素的原子,其最外层3p亚层上有一个未成对电子,它的最高价氧化物对应的水化物的酸根离子是
化学大神帮忙!一道选择题
第三周期元素的原子,其最外层3p亚层上有一个未成对电子,它的最高价氧化物对应的水化物的酸根离子是( )
A. RO5- B.RO3- C.RO4 2- D.RO4-
应该怎么算丫. wmt20581年前2
wmt20581年前2 -
 睡在添崖 共回答了17个问题
睡在添崖 共回答了17个问题 |采纳率94.1%第3周期,则表示它第1.2层排满.1s22s22p6现在已经有10个电子了,3p有一个未成对电子,那就是说3s满了.不然不会往3p排的.那又加3s2,有12个电子了.
3p亚层有3个空轨道.那么它的3p层可以是3p1,3p3,3p5.这样3种情况.
如果是3p1.那么就是13号元素,铝.铝的最高价氧化物对应的水化物是偏铝酸跟.AlO2-.没有符合的.
如果是3P3,那么就是磷,磷的最高价氧化物对应的水化物是磷酸根,PO4 3-
没有符合的.
如果是3P5,那么就是氯,最高价氧化物对应的水化物是高氯酸,酸根写作ClO4-
D符合.
没有直接算的.只能一个一个去推测排除.1年前查看全部
- 原子失电子时,是先失最外层的轨道电子,还是先失外层能量较低轨道的电子?
原子失电子时,是先失最外层的轨道电子,还是先失外层能量较低轨道的电子?
请以铁为例 轩之月语1年前1
轩之月语1年前1 -
 huge0101 共回答了17个问题
huge0101 共回答了17个问题 |采纳率88.2%先失最外层的.因为最外层能量高,它有远离质子的趋势.就犹如人,能力强就能远离父母,自己去闯荡.还有问题吗?铁或其它粒子都一样1年前查看全部
- 问一道奥数题有一个用圆片摆成的两层中空方阵,外层每边有16个圆片,如果把内层的圆片取出来,在外层再摆一层,变成一个新的中
问一道奥数题
有一个用圆片摆成的两层中空方阵,外层每边有16个圆片,如果把内层的圆片取出来,在外层再摆一层,变成一个新的中空方阵,应再增加多少圆片? 性闻zz1年前1
性闻zz1年前1 -
 kanwo123e 共回答了14个问题
kanwo123e 共回答了14个问题 |采纳率85.7%4*(18-1)-4*(14-1)
=4*(18-14)
=16
应再增加16个圆片1年前查看全部
- a,b,c,d,e是短周期元素,周期表中a与b,b与c相邻,c与e同主族,a与c的最外层电子数之比为2:3,b的最外层电
a,b,c,d,e是短周期元素,周期表中a与b,b与c相邻,c与e同主族,a与c的最外层电子数之比为2:3,b的最外层电子数比c的最外层电子数少一个,常见化合物d2c2与水反应生成c的单质,且溶液使酚酞溶液变红.
1.e的元素符号是:
2.a,b,c的氢化物稳定性顺序为:
b的氢化物和b的最高价氧化物的水化物反应生成z,则z中的化学键类型为:
z的化合物类型为:(填共价化合物或离子化合物)
3.写出d2c2与ac2反应的化学方程式:
d2c2与水反应生成c的单质的离子方程式: 重庆英语9221年前2
重庆英语9221年前2 -
 另类情感 共回答了21个问题
另类情感 共回答了21个问题 |采纳率90.5%a:C,b:N,c:O,d:Na,e,S,z:NH4NO3
1.e的元素符号是:S
2.a,b,c的氢化物稳定性顺序为:H2O>NH3>CH4
b的氢化物和b的最高价氧化物的水化物反应生成z,则z中的化学键类型为:共价键和离子键
z的化合物类型为:离子化合物 (填共价化合物或离子化合物)
3.写出d2c2与ac2反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑
d2c2与水反应生成c的单质的离子方程式:2Na2O2+2H2O=4NaOH+O2↑1年前查看全部
- 原子序数依次增大的ABCDE都是元素周期表中前20号元素,BCD同周期,AD同主族,且A的原子结构中最外层电子数
原子序数依次增大的ABCDE都是元素周期表中前20号元素,BCD同周期,AD同主族,且A的原子结构中最外层电子数
原子序数依次增大的ABCDE都是元素周期表中前20号元素,BCD同周期,AD同主族,且A的原子结构中最外层电子数是电子层数的3倍。E和其他元素既不在同周期也不再同主族,D的最高价氧化物对应的水化物为强酸,且BCD的最高价氧化物对应的水化合物两两混合均能发生反应生成盐和水。则ABCDE分别为哪几种元素_________. 脏ル1年前2
脏ル1年前2 -
 cafe5420 共回答了24个问题
cafe5420 共回答了24个问题 |采纳率87.5%首先,你要把原题写清楚吧 这才能解题
等你1年前查看全部
- 下列说法中正确的是( )A.CO2、NH3、CCl4、N2中,所有原子都满足最外层8电子的稳定结构B.在元素周期表中金
下列说法中正确的是( )
A.CO2、NH3、CCl4、N2中,所有原子都满足最外层8电子的稳定结构
B.在元素周期表中金属和非金属交界处可以找到半导体材料
C.共价化合物可能含离子键
D.第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键 元江镍业1年前1
元江镍业1年前1 -
 永失我心1 共回答了11个问题
永失我心1 共回答了11个问题 |采纳率81.8%解题思路:A.氢原子最多满足最为最外层两电子结构;
B.在金属元素与非金属元素的分界线附近的元素,通常既具有金属性又具有非金属性,可以找到半导体材料;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键;
D.氢和第ⅦA族元素的原子之间形成共价键.A.氢原子最多满足最为最外层两电子结构,故氨气中氢原子没达到8电子稳定结构,故A错误;
B.在金属元素和非金属元素交接区域的元素通常既具有金属性又具有非金属性,可以用来做良好的半导体材料,如硅等,故B正确;
C.含离子键的化合物一定是离子化合物,共价化合物中一定不存在离子键,故C错误;
D.第ⅠA族氢元素和第ⅦA族元素的原子之间形成共价键,故D错误;
故选B.点评:
本题考点: 质子数、中子数、核外电子数及其相互联系;元素周期表的结构及其应用;离子化合物的结构特征与性质;共价键的形成及共价键的主要类型.
考点点评: 本题考查了原子结构、元素周期表应用及化学键类型判断,中等难度.注意氢元素原子结构的特殊性及氢元素在周期表的位置.1年前查看全部
- A B C D E F为原子序数一次增大的五种短周期元素,其中仅含一种金属元素.A和D最外层电子数相同,B C和E 在周
A B C D E F为原子序数一次增大的五种短周期元素,其中仅含一种金属元素.A和D最外层电子数相同,B C和E 在周期表中相邻,且C E同主族,B元素的氢化物与其最高价氧化物水化物化合生成一种盐,B C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的化合物甲和乙(相对分子质量甲小于乙) ABCDEF分别是什么元素?
 只抽三五烟1年前1
只抽三五烟1年前1 -
 妖怪尼尼 共回答了21个问题
妖怪尼尼 共回答了21个问题 |采纳率90.5%abcde分别是氢氮氧纳氯1年前查看全部
- 为了迎接 文化节 ,组织一个正方形的彩灯队伍,最外层每边站20人,整队伍有多少人
 房观最后一个ii1年前1
房观最后一个ii1年前1 -
 爱家窗帘 共回答了23个问题
爱家窗帘 共回答了23个问题 |采纳率95.7%设最外层为n则第n层的人数是19*4 第n-1层为(19-2)*4 最后一层为(3-2)*4 共有人数19*4+17*4+·······+1*4=4001年前查看全部
- 若非金属元素R的原子最外层电子数为N.则R的最高正化合价为______.最低负化合价为_____
 a188811年前1
a188811年前1 -
 常在雨中想着晴 共回答了16个问题
常在雨中想着晴 共回答了16个问题 |采纳率87.5%最高正化合价为+N;最低负化合价为-(8-N).O、F及稀有气体除外1年前查看全部
- 下列有关化学用语表达正确的是( ) A.Cl 的最外层电子排布式: B.聚丙烯的结构简式: CH 2 -CH 2 -C
下列有关化学用语表达正确的是( )
A.Cl  的最外层电子排布式:
的最外层电子排布式:
B.聚丙烯的结构简式: 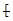 CH 2 -CH 2 -CH 2
CH 2 -CH 2 -CH 2 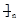
C.CH 2 Br 2 只能表示一种物质 D.NH 3 的电子式: 
 caolie20031年前1
caolie20031年前1 -
 爱的就是这粒米 共回答了19个问题
爱的就是这粒米 共回答了19个问题 |采纳率94.7%1年前查看全部
- 46号元素的原子结构示意图怎么画?26和28元素的最外层电子书是多少?是怎么判断的?
 infernaltang1年前1
infernaltang1年前1 -
 阿波88898 共回答了19个问题
阿波88898 共回答了19个问题 |采纳率84.2%钯+46,2,8,18,18(这个比较诡异)
铁+26,2,8,14,2
镍+28,2,8,16,2
你得学电子亚层,能级排布,就明白了1年前查看全部
- 某校的学生刚好排成一个方阵,最外层的人数是96人,问这个学校共有多少人?翻译成英文怎么说
 敲门1年前1
敲门1年前1 -
 爱上poison 共回答了25个问题
爱上poison 共回答了25个问题 |采纳率96%The students of a school are in just a square formation, the most the outer layer of the number is 96 people, ask how many people in this school?1年前查看全部
- 放上棋子,最外层一共要放多少枚棋子?如果棋盘上放满了棋子,最外层一共要放多少枚棋子?如果棋盘上放满了棋子,这些棋子一共是
放上棋子,最外层一共要放多少枚棋子?如果棋盘上放满了棋子,最外层一共要放多少枚棋子?如果棋盘上放满了棋子,这些棋子一共是多少枚?
打错了,重新来,围棋的棋子是放在围棋棋盘的格点上的,已知围棋棋盘是正方形,最外边每边有19个格点.如果在每一个格点上都放上棋子,最外层一共要放多少枚棋子?如果棋盘上放满了棋子,这些棋子一共是多少枚? 钟青娃1年前1
钟青娃1年前1 -
 横江流逝 共回答了15个问题
横江流逝 共回答了15个问题 |采纳率100%最外层(19-1)*4=72
全部19*19=3611年前查看全部
- 初一科学密度计算题水立方的外层是只有2.4毫米厚的膜结构气枕,像一层皮肤一样保住了整个建筑.该膜每平方米质量为0.24千
初一科学密度计算题
水立方的外层是只有2.4毫米厚的膜结构气枕,像一层皮肤一样保住了整个建筑.该膜每平方米质量为0.24千克,则它的密度是多少? 庞雅1年前1
庞雅1年前1 -
 love_baobao 共回答了19个问题
love_baobao 共回答了19个问题 |采纳率94.7%每平方米这种膜的体积V=1米²×0.0024米=0.0024米³
这种膜的密度=ρ=m/V=0.24千克/0.0024米³=100千克/米³
答:这种膜的密度为100千克/米³.1年前查看全部
- 下列说法中,不正确的是( ) A.原子最外层电子数比次外层电子数多的元素一定位于第二周期 B.从氟到碘,单质与氢气发生
下列说法中,不正确的是( ) A.原子最外层电子数比次外层电子数多的元素一定位于第二周期 B.从氟到碘,单质与氢气发生化合反应越来越难 C. 14 C和 14 N两种核素的质量数相同,中子数也相同 D.离子化合物中可能含有共价键,但共价化合物中一定不含离子健  qiuyannan11年前1
qiuyannan11年前1 -
 文心2004 共回答了18个问题
文心2004 共回答了18个问题 |采纳率100%A、因第一层最多排2个电子,第二层最多排8个电子,第三层最多排布18个电子,且在每层最多容纳的电子数为2n 2 个时,同时符合最外层电子数不超过8个,倒数第二层不超过18个,显然原子最外层电子数比次外层电子数多的元素一定位于第二周期,故A正确;
B、从氟到碘非金属性逐渐减弱,则与氢气发生化合反应越来越难,故B正确;
C、 14 C的中子数为14-6=8, 14 N的中子数14-7=7,中子数不同,故C错误;
D、含有离子键的化合物一定是离子化合物,但离子化合物中可以含有共价键,如NaOH等,故D正确;
故选C.1年前查看全部
- 为什么氢和硼是非金属元素氢的固态不也具有金属的性质么 而且氢只有1个电子 化学反应中也常常显正价啊硼最外层电子数不是3么
为什么氢和硼是非金属元素
氢的固态不也具有金属的性质么 而且氢只有1个电子 化学反应中也常常显正价啊
硼最外层电子数不是3么,根据定义,最外层电子数小于4不都是金属吗,那为什么还把它归在非金属一类? andylakers1年前5
andylakers1年前5 -
 悟空转转转 共回答了26个问题
悟空转转转 共回答了26个问题 |采纳率92.3%“非金属元素的最外层电子数不是大于或等于4.”这个判别方法,是依据化学家门捷列夫[俄]的元素周期表总结出来的.这个规律不是一般规律.也不全面.氢跟硼他们一个只有1层,一个只有2层,他们更容易得到电子形成稳定结构.非金属性为主要性质.所以为非金属!
其实金属和非金属的区别在于:容易得到电子的定义为非金属,容易失去电子的定义为金属!但是有些元素既能得到电子,又能失去电子,这时就要看得电子能力强还是失电子能力强!其实有时候金属和非金属没有明显界限的!1年前查看全部
- 金属活泼顺序与亚层电子有关么?是副族的金属看亚层的不饱和度还是能量高低排序么?那当最外层电子数目和所在层数一样的时候.是
金属活泼顺序与亚层电子有关么?
是副族的金属看亚层的不饱和度还是能量高低排序么?那当最外层电子数目和所在层数一样的时候.是有亚层易失去还是没有亚层?我觉得亚层***核的引力应该更活泼..可是镁比铁活泼..但是镁和铁只差在亚层了.. albertyyp1年前1
albertyyp1年前1 -
 FFFDDD000 共回答了14个问题
FFFDDD000 共回答了14个问题 |采纳率92.9%上高中的时候,初中的知识全忘光了,上大学的时候,高中以前的东西又都丢了……T-T1年前查看全部
- 英语翻译他是第一位研究外层空间的科学家.请坐在那里别动,不要打开书.请别出声,不要开窗.你能想象得出他是多么紧张,可他的
英语翻译
他是第一位研究外层空间的科学家.
请坐在那里别动,不要打开书.
请别出声,不要开窗.
你能想象得出他是多么紧张,可他的朋友都抱有信心.
你能想象得出他是多么兴奋,可他的父母都无所谓. zhu11121年前2
zhu11121年前2 -
 鸿渐于磐 共回答了19个问题
鸿渐于磐 共回答了19个问题 |采纳率100%1.He was the first scientist who studied the outer space.
2.Please sit there still and do not open the book.
3.Please keep silent and do not open the window.
4.You can imagine how nervous he was,but all of his friends had confidence in him.
5.You can imagine how nervous he was,but his parents were all the same to him.(注:all the same to 表示对……无所谓)1年前查看全部
- 元素X的基态原子最外层电子排布为nsn-1npn+2,则X元素的原子序数为( )
元素X的基态原子最外层电子排布为nsn-1npn+2,则X元素的原子序数为( )
A. 9
B. 10
C. 17
D. 18 舒亦纤尘1年前1
舒亦纤尘1年前1 -
 匠人爱芳直 共回答了14个问题
匠人爱芳直 共回答了14个问题 |采纳率85.7%解题思路:根据排布规律可知nsn-1应排满,为2个电子,故n=3,元素X的基态原子最外层电子排布为3s2np5.nsn-1应排满,为2个电子,故n=3,元素X的基态原子最外层电子排布为3s2np5,为Cl元素,故选C.
点评:
本题考点: 原子核外电子排布.
考点点评: 本题考查原子结构与元素的性质,难度不大,注意根据构造原理,先排能量低的再排能量高的.1年前查看全部
- 下列分子所有原子满足最外层为8电子结构的是
下列分子所有原子满足最外层为8电子结构的是
BCl3 CS2 PCl5 LiCl 锌钛白1年前1
锌钛白1年前1 -
 兰心蝶骨nn 共回答了23个问题
兰心蝶骨nn 共回答了23个问题 |采纳率91.3%BCl3不是,因为B3+最外层是2个
CS2不是,C4+最外层2个
PCl5是
LiCl不是,Li+最外层2个1年前查看全部
- 国家游泳中心“水立方”是北京2008年奥运会场馆之一,它的外层膜的展开面积约为260 000平方米,用科学记数法表示是(
国家游泳中心“水立方”是北京2008年奥运会场馆之一,它的外层膜的展开面积约为260 000平方米,用科学记数法表示是()平方米.  lkaede1年前1
lkaede1年前1 -
 凝固冰点 共回答了11个问题
凝固冰点 共回答了11个问题 |采纳率90.9%2.6×10 51年前查看全部
- 有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级中的电子数等于次外层的电子总数,C原子最外层
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级中的电子数等于次外层的电子总数,C原子最外层中有2个不成对的电子.已知C、D、E原子核内的质子数均与中子数相等,且C元素可分别与A、B、D、E生成RC2型化合物,在DC2中,D与C的质量比为7:8,在EC2中,E与C的质量比为1:1.请回答下列问题:
(1)写出A、E两种元素的元素符号:A______、E______.
(2)写出D原子的电子排布式______.
(3)指出E在元素周期表中的位置______.
(4)比较A、B、C三种元素的第一电离能的大小顺序______.
(5)比较D和E元素的电负性的相对大小______. jsnyht1年前1
jsnyht1年前1 -
 gf1097 共回答了20个问题
gf1097 共回答了20个问题 |采纳率80%解题思路:p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,所以次外层为2个电子,则A的核外电子排布为1s22s22p2,应为C元素;
C原子最外层中有两个不成对的电子,且C的原子序数大于A,所以C原子核外电子排布式为1s22s22p4,为O元素,B的原子序数大于A而小于C,所以B是N元素;
B元素可分别与A、C、D、E生成RB2型化合物,在DC2中D与C的质量比为7:8,设D的摩尔质量为M,
:7 M
=7:8,M=28,C、D、E原子核内的质子数均与中子数相等,所以D是Si元素;8 32
在EC2中,E与C的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,
结合元素对应原子的结构、单质以及化合物的性质解答该题.p能级电子数不超过6,A原子最外层p能级的电子数等于次外层的电子数总数,所以次外层为2个电子,则A的核外电子排布为1s22s22p2,应为C元素;
C原子最外层中有两个不成对的电子,且C的原子序数大于A,所以C原子核外电子排布式为1s22s22p4,为O元素,B的原子序数大于A而小于C,所以B是N元素;
B元素可分别与A、C、D、E生成RB2型化合物,在DC2中D与C的质量比为7:8,设D的摩尔质量为M,
7
M:
8
32=7:8,M=28,C、D、E原子核内的质子数均与中子数相等,所以D是Si元素;
在EC2中,E与C的质量比为1:1,则M(E)=2M(O)=2×16=32,所以E为S元素,
(1)通过以上分析知,A是C元素,E是S元素,故答案为:C;S;
(2)D是Si元素,其原子核外有14个电子,根据构造原理知,其原子核外电子排布式为:1s22s22p63s23p2,
故答案为:1s22s22p63s23p2;
(3)E是S元素,其原子核外有3个电子层,最外层有6个电子,元素原子核外电子层数等于其周期数,主族元素的最外层电子数等于其族序数,所以S位于第三周期、第ⅥA族,故答案为:第三周期、第ⅥA族;
(4)A是C元素,B是N元素,C是O元素,同一周期中,元素的第一电离能随着原子序数的增大而呈增大趋势,但第VA族元素第一电离能大于其相邻元素,所以这三种元素的第一电离能从小到大顺序是:C<O<N,故答案为:C<O<N;
(5)D是Si元素,E是S元素,同一周期中,元素的电负性随着原子序数的增大而增大,所以电负性:Si<S,故答案为:Si<S.点评:
本题考点: 位置结构性质的相互关系应用.
考点点评: 本题考查了元素第一电离能大小的判断、电负性大小的判断、核外电子排布式的书写等知识点,正确推断元素是解本题关键,结合元素周期律来分析解答,注意第一电离能大小的规律及异常,为易错点.1年前查看全部
- X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是(
 X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
A.Y的氢化物沸点较高是因为其相对分子质量比较大
B.W的最高价氧化物对应水化物的酸性比Z的强
C.Z的非金属性比Y的强
D.X与Y形成的化合物中既有离子键又有共价键 沉浮小白1年前1
沉浮小白1年前1 -
 yan000000 共回答了11个问题
yan000000 共回答了11个问题 |采纳率100%解题思路:X、Y、Z、W均为短周期元素,由元素的位置可知,X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是内层电子数的3倍,Y原子最外层电子数为6,所以Y为O元素,可推知X为N元素,Z为S元素,W为Cl元素,
A.水分子之间存在氢键,沸点高于硫化氢;
B.同周期随原子序数增大,元素非金属性增强,非金属性越强,最高价含氧酸的酸性越强;
C.同主族自上而下非金属性减弱;
D.X与Y形成的常见化合物属于共价化合物.X、Y、Z、W均为短周期元素,由元素的位置可知,X、Y处于第二周期,Z、W处于第三周期,Y原子的最外层电子数是内层电子数的3倍,Y原子最外层电子数为6,所以Y为O元素,可推知X为N元素,Z为S元素,W为Cl元素,
A.水分子之间存在氢键,沸点高于硫化氢,故A错误;
B.非金属性W>Z,故最高价氧化物对应水化物的酸性W>Z,故B正确;
C.同主族自上而下非金属性减弱,非金属性Y>Z,故C错误;
D.X与Y形成的常见化合物属于共价化合物,不含离子键,故D错误,
故选B.点评:
本题考点: 元素周期律和元素周期表的综合应用.
考点点评: 本题考查结构性质位置关系应用,侧重对元素周期表与元素周期律的考查,难度不大,注意掌握元素周期律,理解同主族、同周期元素性质的递变规律.1年前查看全部
- 小东用棋子摆成一个实心方阵,最外层共有36枚棋子,这个方阵里一共有
小东用棋子摆成一个实心方阵,最外层共有36枚棋子,这个方阵里一共有
小东用棋子摆成一个实心方阵,最外层共有36枚棋子,这个方阵里一共有多少枚棋子? baozai0020281年前4
baozai0020281年前4 -
 knowy 共回答了19个问题
knowy 共回答了19个问题 |采纳率94.7%先求出正方形的每边上有多少个棋子
36-4=32
(外层减去四个角上的4个棋子)
32÷4=8
(外层每边上除了角上的棋子数量)
8+2=10
(加上角上的2个得到外层上每条边上的棋子数量,说明是1个10×10的方阵)
10×10=100
共有100个棋子1年前查看全部
- 某元素最外层电子数是总电子数四分之一是哪个原子
 ycj11171年前2
ycj11171年前2 -
 hlt4300 共回答了23个问题
hlt4300 共回答了23个问题 |采纳率91.3%2 8 8 6为24号元素 铬 CR1年前查看全部
- X,Y,Z,W组成的化学式X,Y,Z,W四种元素的原子最外层电子数依次为1,6,2,4,则下列各组化学式都正确的是( )
X,Y,Z,W组成的化学式
X,Y,Z,W四种元素的原子最外层电子数依次为1,6,2,4,则下列各组化学式都正确的是( )
A.WY2,X2Z,X2WY4 B.WX4,X2Y,ZWY3 C.ZY,ZW2,XYW2 D.WZ2,Y2X,Z(XY)2 浪花打湿裤脚1年前3
浪花打湿裤脚1年前3 -
 yuzhang20022008 共回答了24个问题
yuzhang20022008 共回答了24个问题 |采纳率95.8%B
可以把X Y Z W看成H O Mg C再代入就好判断了1年前查看全部
- 共价化合物中,共价键的计算它等于0.5*各原子最外层单电子之和?如H2O2 它的共价键数目就应该是0.5*(1+6+6+
共价化合物中,共价键的计算
它等于0.5*各原子最外层单电子之和?
如H2O2 它的共价键数目就应该是0.5*(1+6+6+1)=7? 开心果_0011年前2
开心果_0011年前2 -
 用户伊莲 共回答了22个问题
用户伊莲 共回答了22个问题 |采纳率90.9%单电子指的就是原子最外层的未成对电子.这句话的意思就是对于一个共价化合物,其共价键的数目就是形成该化合物的所有原子自身未成对电子之和的一半;或者换句话说,就是参与形成共价键的电子数的一半.(当然也有例外)...1年前查看全部
- 硬币能否溶解于王水是否需要打磨掉最外层的漆?
 威风长刀小钢炮1年前4
威风长刀小钢炮1年前4 -
 娘娘娘娘 共回答了21个问题
娘娘娘娘 共回答了21个问题 |采纳率90.5%硬币都能溶解于王水;【人民币硬币总共发行了4套…不同时期不同面值有不同合金成分,1角硬币 铝镁合金 1角硬币 不锈钢 5角硬币 钢芯镀铜合金 1元硬币 钢芯镀镍;以上金属材料都是可以溶解于王水的.】1年前查看全部
- 离子正电荷数和电子最多相差多大比如 一个离子 正电荷数为X 两个电子层 内层2个电子 最外层8个电子 当为阳离子时 X=
离子正电荷数和电子最多相差多大
比如 一个离子 正电荷数为X 两个电子层 内层2个电子 最外层8个电子 当为阳离子时 X=() 当为阴离子时 X=() 括号中的数字不止一个 oO小猪Oo乖乖1年前1
oO小猪Oo乖乖1年前1 -
 小乱来 共回答了26个问题
小乱来 共回答了26个问题 |采纳率88.5%一个离子 正电荷数为X 两个电子层 内层2个电子 最外层8个电子 当为阳离子时 X=(11,12,13) 当为阴离子时 X=(7,8,9)
最多相差31年前查看全部
- 电子数的定义,和次外层电子数,的定义,电子数是不是核电荷数
 x745362131年前1
x745362131年前1 -
 weigaoa 共回答了14个问题
weigaoa 共回答了14个问题 |采纳率78.6%电子数多少是根据核内的质子数来说的 因为要电荷平衡 所以也是核电荷数 因为核电荷是正的 和原子外电子负的相平所以等于核电荷数 次外层电子数不超过18个1年前查看全部
- 某元素原子的最外电子层上有6个电子,次外层上有2个电子
某元素原子的最外电子层上有6个电子,次外层上有2个电子
该元素是——该元素跟核内只有1个质子的元素结合形成的化合物是——(填“离子””共价“)化合物 cuizhihua5211年前2
cuizhihua5211年前2 -
 184064 共回答了21个问题
184064 共回答了21个问题 |采纳率81%氧 共价化合物 和2氧化但1年前查看全部
- 街心雕像,四周用花盆摆成了一个四层长方形方坛,一直最外层每边有40盆花,共共摆了多少盆花?
 光华西门1年前1
光华西门1年前1 -
 人过30 共回答了23个问题
人过30 共回答了23个问题 |采纳率95.7%一共
4x(40+34)x4/2
=8x74
=592(盆)1年前查看全部
- 最外层为三的元素,一定位于第三主族,为什么
 peiwenpeng1年前3
peiwenpeng1年前3 -
 looking4murong 共回答了21个问题
looking4murong 共回答了21个问题 |采纳率95.2%一定位于第三主族
副族元素电子回填1年前查看全部
- 57.希望有人帮忙)最外层有5个电子,次外层有8个电子的元素位于周期表中
57.希望有人帮忙)最外层有5个电子,次外层有8个电子的元素位于周期表中
最外层有5个电子,次外层有8个电子的元素位于周期表中 ()
A.第一周期
B.第二周期
C.第三周期
D.第四周期
希望人有帮忙,解析..越详细越好.急. 让我笑1年前2
让我笑1年前2 -
 wgi123 共回答了22个问题
wgi123 共回答了22个问题 |采纳率100%第三或者第四周期元素都有可能,但需要具体分析
第三周期 2 8 5 P
第四周期 按照题意 应该有 2 8 8 5
但是显然该元素不能稳定存在,因为其次外层轨道还能继续填充电子,
第四周期元素次外层8电子稳定必须满足最外层电子数不大于2,而此处为5,故而应舍弃.
只能选C1年前查看全部
- 碳元素原子最外层4个电子,易得还是失电子
 jenny1801年前3
jenny1801年前3 -
 玫瑰的王子 共回答了22个问题
玫瑰的王子 共回答了22个问题 |采纳率90.9%既不易得电子,也不易失电子,所以碳的单质很稳定1年前查看全部
- 电子层排列规律笔记上记的:“最外层最多放8个电子”可是 Ca 2 8 8 2 这样的排布第三层为什么不可以是"9”呢?第
电子层排列规律
笔记上记的:“最外层最多放8个电子”可是 Ca 2 8 8 2 这样的排布第三层为什么不可以是"9”呢?第三层不是最外层啊...难道不能是 Ca 2 8 9 1 honlang5051年前1
honlang5051年前1 -
 爱你我学不会 共回答了21个问题
爱你我学不会 共回答了21个问题 |采纳率100%原子轨道分为s,p,d,f 轨道,s 层只能放2个电子,p层只能放6个电子.钙的电子排布应该是:1s2 1p2 2s2 2p6 3s2 3p6 4s2,字母前面的数字代表第几层轨道,字母后面的数字代表在这个轨道上的电子数.在第三层,轨道排布为3s2 3p6 ,那就是8个电子咯.1年前查看全部
- 电晕现象用高绝缘物体隔离会好吗一个高压升压器(200v升4万v)的,由于高压外层非常靠近一个接地的的铁壳,请问在他们之间
电晕现象用高绝缘物体隔离会好吗
一个高压升压器(200v升4万v)的,由于高压外层非常靠近一个接地的的铁壳,请问在他们之间加一个高绝缘的板能起到防止电晕现象吗? guirong1年前2
guirong1年前2 -
 彼岸_灯火 共回答了15个问题
彼岸_灯火 共回答了15个问题 |采纳率86.7%可以的!产生电晕的条件是金属材料,和导体,才会放电,而且还有远近,要跟椐你的电压来算的话,按最大的功率算,你的正极要离负极只少也要有250(MM)的距离才可以不放电,从而接地线一定要接好,1年前查看全部
大家在问
- 1已知正项数列{an}的前n项的乘积等于Tn=(14)n2−6n(n∈N*),bn=log2an,则数列{bn}的前n项和
- 2当在电场中某点放入电量为q的正试探电荷时,测得该点的场强为E,若在同一点放入电量q′=2q的负试探电荷时,测得该点的场强
- 3浓氨水加氢氧化钠制氨气和浓硝酸与铜制NO2可否用启普发生器?
- 4按要求写英语作文,介绍我和我的好朋友.
- 5平面镜成像的大小决定于( )A.平面镜的大小B.物体离平面镜的距离C.物体本身的大小D.与以上三种因素都有关系
- 6用5、3、8三张数字卡片按要求摆放.(1)从三张卡片中选一张、两张或者三张,可以摆出多少个不同的自然数
- 7请你对青少年的娱乐和休闲提两条合理化建议
- 8最近有什么电影用英语怎么说?
- 9仿照下面诗句的内容和格式,清再继续写一节诗句.
- 10(2014•岚山区模拟)5÷9的商用小数表示是______,保留三位小数约是______.
- 11b分之a=七分之四,a-b=12,a等于?
- 12二乙二醇丁醚(BDG),在含F水中有一定量BDG,致使COD含量超高,请问有什么化学方法可以降低水中COD的含量
- 13早上8;15分,钟面上的时针和分针所夹的角度是?
- 14数学题如下(写清楚算式和过程,要正确)
- 15质量是5kg的物体浸在水中,受到的水的浮力是40N,则该物体会


