配料表:氯化钠、食用碳酸钙、碘酸钾
 草莓爱菠萝2022-10-04 11:39:542条回答
草莓爱菠萝2022-10-04 11:39:542条回答净含量:500g
钙(以Ca计):0.5%-1.3%
碘(以I计):(20-50)mg/kg
问:每千克这种食盐中至少要加多少克碳酸钙才符合要求?
用初三的知识来回答

已提交,审核后显示!提交回复
共2条回复
 lost-in-dream 共回答了17个问题
lost-in-dream 共回答了17个问题 |采纳率88.2%- 钙 是以 碳酸钙 的形式存在的.那么根据
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
得到:CO2 -- Ca
44 40
0.123g x 44/0.123g=40/x x=0.112g
x/10g = 0.112g/10g =1.12 % 在(0.5—1.3)% 的范围内.
合格!
这种题目的解题方法一般都是
求出要求物质所在的物质的质量
列化学方程式
列出比值就可.
然后得到CaCO3的质量
再除以盐的质量就可.. - 1年前
 vanny1314 共回答了25个问题
vanny1314 共回答了25个问题 |采纳率- 根据题目意思,每千克这种食盐中含钙量为 0.5%*1000g=5g。
无需化学反应方程式(这里面没有涉及什么化学反应,只是已知元素质量分数,求化合物质量而已,所以一楼不要误导)。
碳酸钙中钙的质量分数为40/100=0.4,假设需要的碳酸钙质量为x,则
0.4x=5 x=12.5g
答:每千克这种食盐中至少要加... - 1年前
相关推荐
- 为什么包装好的鸡架里含亚硝酸钠还明目张胆的写在配料表里
 sxhaitao1年前1
sxhaitao1年前1 -
 米瑞米 共回答了23个问题
米瑞米 共回答了23个问题 |采纳率91.3%食品中适量的亚硝酸钠可以防腐保持色泽鲜艳,过量就会引起食物中毒了,如果是适量的不必惊慌1年前查看全部
- 配料表里的“sweetened condensed skimmed
 牵你的手流浪1年前1
牵你的手流浪1年前1 -
 qin5202091 共回答了13个问题
qin5202091 共回答了13个问题 |采纳率92.3%半脱脂甜炼乳
sweetened甜的
condensed milk炼乳
skimmed 半脱脂的1年前查看全部
- 天然柠檬味是什么物质外国进口的一种食品,配料表中有一成份为“Natural Lemon Flavor”,它应该是一种什么
天然柠檬味是什么物质
外国进口的一种食品,配料表中有一成份为“Natural Lemon Flavor”,它应该是一种什么物质?一般如何翻译。我觉得在配料表中,说是“天然柠檬味”怪怪的
 我想狐狸1年前1
我想狐狸1年前1 -
 如果云知道751012 共回答了18个问题
如果云知道751012 共回答了18个问题 |采纳率83.3%如果是在配料表内的话,意思是“天然柠檬香料”。例句如下:
Ingredients:Finest green tea, lemon peel, hibiscus, chicory root, natural lemonflavor and citric acid. 跟读
配料:精选绿茶、柠檬皮、芙蓉花、菊苣、自然柠檬香料、柠檬酸。1年前查看全部
- 某加钙食盐包装袋上的部分说明.配料表:氯化钠、食用碳酸钙、碘酸钾.净含量:500克.成分表:氯化钠大于等于88%、钙:(
某加钙食盐包装袋上的部分说明.配料表:氯化钠、食用碳酸钙、碘酸钾.净含量:500克.成分表:氯化钠大于等于88%、钙:(0.5-1.3)%、碘:(20-50)%.问某人摄入该食盐5克,相当于至少补充了多少克碳酸钙?
 139441733481年前4
139441733481年前4 -
 却却 共回答了19个问题
却却 共回答了19个问题 |采纳率94.7%含钙5g*(0.5-1.3)%=(2.5-6.5)%g
含碳酸钙(2.5-6.5)%g/(40/100)=(6.25-16.25)%g1年前查看全部
- 市场上销售的一种“加碘盐”,包装袋上的部分文字说明如下表: 配料表 精致海盐、碘酸钾 储藏方法 密封避光、防潮 食用方法
市场上销售的一种“加碘盐”,包装袋上的部分文字说明如下表:
从说明中可知:(1)“加碘盐”属于______(填“纯净”戓“混合物”);(2)碘酸钾的化学性质是______.配料表 精致海盐、碘酸钾 储藏方法 密封避光、防潮 食用方法 烹调时待食品熟后加入碘盐  武略文韬1年前1
武略文韬1年前1 -
 明天的风 共回答了26个问题
明天的风 共回答了26个问题 |采纳率84.6%(1)加碘盐中含有海盐、碘酸钾等物质,属于混合物.故填:混合物.
(2)说明中的密封避光保存、食品熟后再加入碘盐说明碘酸钾见光、加热时容易分解.故填:易分解.1年前查看全部
- a-淀粉酶能吃吗看到面包的配料表上写着这玩意儿我看到阿尔法就慌了不是化学成分吗
 zsr021年前3
zsr021年前3 -
 shenjia114 共回答了22个问题
shenjia114 共回答了22个问题 |采纳率77.3%只要是写在配料表上的食品添加剂,其安全性必定已经受到及严格的验证,其添加量也是有国标控制的,不必恐慌.α-淀粉酶是一种水解酶,是目前发酵工业上应用最广泛的一类酶,广泛分布于动物(唾液、胰脏等)、植物及微生物中.应用于发酵工业可增强淀粉口感.其化学本质是多肽,进入胃中完全分解为氨基酸,对人体完全无害.1年前查看全部
- 关于食品包装后面的配料表,像大米单一产品,本身就为原料的,也需要在包装后注明配料表吗?
 snsq1年前1
snsq1年前1 -
 米琳秀 共回答了18个问题
米琳秀 共回答了18个问题 |采纳率88.9%GB7811-2004中5.1.2配料清单中规定预包装食品的标签上应表示配料清单,单一配料的食品除外.
所以无需在包装后注明配料表!1年前查看全部
- 看到红牛的配料表中有牛磺酸这一项,怪怪的,这到底是什么东西?
 乱云天一角1年前4
乱云天一角1年前4 -
 wrfzxy 共回答了20个问题
wrfzxy 共回答了20个问题 |采纳率90%牛磺酸属于人体必需氨基酸之一,参与糖代谢的调节,加速糖酵解;能增强心肌收缩力,增加血液输出,同时防止心肌损伤;能保护肝脏;能改善脑细胞工作状态.对于维持运动能力,牛磺酸是必需的,加强其补给可使运动能力和抗运动性疲劳能力进一步增加.1年前查看全部
- 计算.明天要交.分可以加现有一袋一千克的碘盐.其配料表如右图XXX牌碘盐配料:精制盐(NaCl)碘酸钾(KIO3) 3是
计算.明天要交.分可以加
现有一袋一千克的碘盐.其配料表如右图
XXX牌碘盐
配料:精制盐(NaCl)碘酸钾(KIO3) 3是在右下角
含量:碘35 mg/kg
(1)求此带碘盐中碘元素的质量
(2)求此带碘盐中的碘酸钾的质量
(3)求此带碘盐中碘酸钾的质量分数
(4)成人每天约需要0.15mg碘,假设这些碘主要是从碘盐中摄取的,则成人每天需要食用碘盐多少克?最重要的是过程,要写清楚,, may02171年前1
may02171年前1 -
 客服中心0014 共回答了25个问题
客服中心0014 共回答了25个问题 |采纳率84%(1)35mg
(2)KIO3含I%=127/214=59.3%
35/59.3%=59.0mg
(3)0.059/1000=0.0059%
(4)0.15*1000g/35=4.28g
知道有这么多人答就不做了啊,
理解一个公式就行了:元素质量=物质质量*元素的质量分数
反之:物质质量=元素质量/元素的质量分数1年前查看全部
- (2008•海南)市场上销售的一种“加碘盐”,包装袋上的部分文字说明如下表: 配料表 精致海盐、碘酸钾 储藏方法 密封避
(2008•海南)市场上销售的一种“加碘盐”,包装袋上的部分文字说明如下表:
从说明中可知:(1)“加碘盐”属于______(填“纯净”戓“混合物”);(2)碘酸钾的化学性质是______.配料表 精致海盐、碘酸钾 储藏方法 密封避光、防潮 食用方法 烹调时待食品熟后加入碘盐  oozjj1年前1
oozjj1年前1 -
 文月 共回答了12个问题
文月 共回答了12个问题 |采纳率100%解题思路:可以根据物质的组成方面判断物质的类别,根据表中的信息可以判断物质的性质.(1)加碘盐中含有海盐、碘酸钾等物质,属于混合物.故填:混合物.
(2)说明中的密封避光保存、食品熟后再加入碘盐说明碘酸钾见光、加热时容易分解.故填:易分解.点评:
本题考点: 纯净物和混合物的判别;化学性质与物理性质的差别及应用.
考点点评: 解答本题的关键是要充分理解表中提供的信息,只有这样才能对问题做出正确的判断.1年前查看全部
- 下表是某工厂生产的加钙食盐包装标签上的部分内容,请仔细阅读后回答问题. 配料表:Nacl,kIO3,CaCO3 净含
下表是某工厂生产的加钙食盐包装标签上的部分内容,请仔细阅读后回答问题. 配料表:Nacl,kIO3,CaCO3 净含
下表是某工厂生产的加钙食盐包装标签上的部分内容,请仔细阅读后回答问题.
配料表:Nacl,kIO3,CaCO3 净含量:500克 成分表:NaCL≥88%
钙:(以Ca计)(0.5-1.3)% 碘:(以1计)(40-50)mg/kg
请问:成人每天约需要1.5×10-4g碘,假设这些碘是从碘盐中摄取的,则成人每天需要食用碘盐的质量是多少克?
 一月刀客1年前1
一月刀客1年前1 -
 WX了凡 共回答了18个问题
WX了凡 共回答了18个问题 |采纳率100%首先,这道题其实很简单,前面说了一大堆都是迷惑人的手法,不要看,直接就看第二行:钙:(以Ca计)(0.5-1.3)% 碘:(以1计)(40-50)mg/kg
成人每天需要1.5*10-4g碘,而每kg碘盐中含有40-50mg碘,我们以最小的40mg每kg来计算,换算成0.04g碘每kg,1.5*10-4/0.04=3.75*10-3
以最大50mg每千克来计算是 1.5*10-4/0.05=3*10-3=0.003kg
所以成年人每天应该吃3g到3.75g食盐1年前查看全部
- 如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽水中是否溶有CO 2 ,他做了如下实验:取少量汽水与试管中,滴加紫
如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽水中是否溶有CO 2 ,他做了如下实验:取少量汽水与试管中,滴加紫色石蕊试液,石蕊试液变红色.
(1)小虎同学认为汽水中溶有CO 2 ,小虎同学依据的原理是______(用化学方程式表示);
(2)小怡同学查阅相关资料后对小虎同学的方案提出了质疑,认为上述实验方案不足以证明汽水中溶有CO 2 .其理由是______;
(3)小怡同学的质疑有道理.他思考后,利用同样的原理重新设计了一个实验探究汽水中是否溶有CO 2 .他设计的实验过程是______;
(4)我还能利用与上述实验不同的原理,设计如下方案证明汽水中是否溶有CO 2 ______,其中反应的化学方程式为______.
 133436385901年前1
133436385901年前1 -
 super_诗毅 共回答了15个问题
super_诗毅 共回答了15个问题 |采纳率93.3%(1)二氧化碳可以和水反应生成碳酸,而碳酸可以使紫色石蕊试液变红,反应的化学方程式为:CO 2 +H 2 O═H 2 CO 3 ;
(2)根据标签可以知道其水中还含有柠檬酸,而柠檬酸也呈酸性,其溶液也能使石蕊试液变红,所以不能仅仅根据石蕊变红来判断溶有二氧化碳;
(3)碳酸不稳定,易分解产生二氧化碳,但是柠檬酸不易分解,所以可以振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO 2 ;
(4)二氧化碳能够使澄清石灰水变浑浊,所以振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO 2 ;该反应的化学方程式为:Ca(OH) 2 +CO 2 ═CaCO 3 ↓+H 2 O.
故答案为:(1)CO 2 +H 2 O═H 2 CO 3 ;
(2)其中的柠檬酸也是一种酸,其溶液也能使石蕊试液变红;
(3)振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO 2 ;
(4)振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO 2 ;Ca(OH) 2 +CO 2 ═CaCO 3 ↓+H 2 O.1年前查看全部
- 某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐
某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.003mol二氧化碳.请计算:
(1)在盐酸中参加化学反应的HCl的物质的量.
(2)此加钙食盐中钙元素的质量分数.
 王米1年前1
王米1年前1 -
 superfatfish 共回答了16个问题
superfatfish 共回答了16个问题 |采纳率93.8%解题思路:根据碳酸钙与盐酸反应的化学方程式和生成的二氧化碳的摩尔数,即可计算出参与反应的盐酸、碳酸钙的物质的量;然后计算出钙元素的质量,根据“[钙元素的质量/10g]×100%”计算出此加钙食盐中钙元素的质量分数.设参加反应的HCl物质的量为x,食用碳酸钙的物质的量是z.
CaCO3+2HCl→CaCl2+H2O+CO2↑
121
zx0.003mol
(1)则[2/x]=[1/0.003mol]
解得,x=0.006mol,
(2)[1/z]=[1/0.003mol],
z=0.003mol,
所以,m(CaCO3)=0.003moL×100g/mol=0.3g
m(Ca)=0.3g×[40/100]×100%=0.12g
此加钙食盐中钙元素的质量分数=[0.12g/10g]×100%=1.2%;
答:(1)在盐酸中参加化学反应的HCl的物质的量是0.006mol.
(2)此加钙食盐中钙元素的质量分数是1.2%.点评:
本题考点: 根据化学反应方程式的计算;化合物中某元素的质量计算.
考点点评: 本题主要考查含杂质物质的化学方程式计算和质量分数的计算,难度较大.解题时要注意计算的步骤规范和计算的准确性.1年前查看全部
- 干面条配料表里面添加剂一栏里面的碳酸钠是什么物质
 xyparrowarrow1年前1
xyparrowarrow1年前1 -
 xgazqjbhgb 共回答了19个问题
xgazqjbhgb 共回答了19个问题 |采纳率94.7%是的,碳酸钠是碱.有的人喜欢白水面,我比较喜欢碱面.1年前查看全部
- 食品安全法对食品标签要求标注成分或者配料表,以后是否可以在标签上标注成分?请
 gyutiu1年前1
gyutiu1年前1 -
 yoyoshao 共回答了18个问题
yoyoshao 共回答了18个问题 |采纳率88.9%根据国标中的标识标准和膳食营养标准中要求:标签上必须标注成分和占比,营养成分占比不能低于标注的80%,不能高于标注的20%.比如标识标注热量80%,实际成分不能低于64%,不能高于160%1年前查看全部
- 以下是我省生产的某种钙盐包装标签上的部分文字.请仔细阅读后回答以下问题: 配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:5
以下是我省生产的某种钙盐包装标签上的部分文字.请仔细阅读后回答以下问题: 配料表:氯化钠、食用碳酸钙、碘酸钾 净含量:500g
成份表:氯化钠≥88%
钙(以Ca计)(0.5-1.3)%
碘(以I计)(20-50)mg/Kg
(1)包装标签上钙含量是指_______(填单质钙、碳酸钙、钙元素中的一种).
(2)为了检验钙盐中是否含有碳酸钙,在家庭厨房里可选用的物质是 .
(3)为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算加此加钙食盐中钙元素的质量分数.
第三题!请写清楚了(包括解设、化学方程式、相当分子质量、答) 啸傲千山1年前1
啸傲千山1年前1 -
 越靓河 共回答了18个问题
越靓河 共回答了18个问题 |采纳率77.8%钙元素
食醋1年前查看全部
- (如01多•广陵区一模)牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题: 配料表
(如01多•广陵区一模)牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
[资料卡片]:
配料表 摩擦剂:S6o如(如0%)
CaCo多(少量)
清洁剂:Na手Co多(15%)
发泡剂:手1如(极少量)
保湿剂:甘油等(60%)
增稠剂:卡拉胶等
其他:香精、水等
a、S6o如不溶于水、且不与酸反应,高温不分解;
b、Na手Co多受热易分解,生成Na如Co多、手如o、Co如;
c、牙膏中保湿剂、增稠剂、香精等均为有机物.
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测手其上层清液的p手为m.多,则此牙膏显______性,实验室能否用p手试纸测手该数值,请你作出判断并说明理由.______;
(如)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的手1如(一种钠盐)析出,则手1如的溶解度和温度的关系是______;
(多)为测定此牙膏中S6o如的质量分数,兴趣小组同学设计了如下方案,并进行了多次实验:
[实验步骤]:
①准确称取如.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀手C5,至______;
③过滤、洗涤、称量手到剩余固体质量(如表);
④根据实验数据进行计算.实验编号 1 如 多 实验前(g) 如.00 如.00 如.00 实验后(g) 0.4多 0.44 0.45
[数据处理]:
(4)此测定做多次实验的目的是______;
(5)综合上述实验方案及实验数据,计算此牙膏中S6o如的质量分数.______;
[实验分析]:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是______;
(7)高温加热的目的除为了除去CaCo多及Na手Co多以外,还为除去______;
(m)步骤②中,加稀手C5发生的反应有______、______;
(9)步骤③中,洗涤的目的是______;若不洗涤,则测定结果将______.(填“偏大”、“偏小”或“不变”)
(10)为保证洗涤效果,最好用______洗涤.
A.蒸馏水B.自来水C.饱和NaC5溶液D.饱和CaC5如溶液. kgdfggh1年前1
kgdfggh1年前1 -
 baby鱼610 共回答了22个问题
baby鱼610 共回答了22个问题 |采纳率86.4%解题思路:(1)根据测得其上层清液的pH为8.3大于7进行解答;
(2)根据牙膏中的K12在冬天析出进行解答;
(3)根据碳酸钠和盐酸反应生成二氧化碳进行解答;
(4)根据此测定做3次实验的目的是提高实验的精确度进行解答;
(5)根据剩余固体的质量就是二氧化硅的质量进行解答;
(6)根据步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面进行解答;
(7)根据保湿剂、增稠剂、香精等有机物加热会挥发进行解答;
(8)根据①中的固体有二氧化硅、氧化钙、碳酸钠进行进行解答;
(9)根据洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液进行解答;
(10)根据蒸馏水中不含有其他可溶性物质进行解答.(1)测她其上层清液0pH为8.3大于7,所以则此牙膏显弱碱性;pH试纸只能测定出整数值,而测她清液0pH为8.3,所以实验室不能用pH试纸测她该数值;
(手)牙膏中0K1手在冬天析出,说明K1手0溶解度随温度降低而降低(或随温度升高而增大);
(3)碳酸钠和盐酸反应生成二氧化碳,所以转移剩余物至烧杯中,加入稀HC十,至气体不再产生为止;
(1)此测定做3次实验0目0是提高实验0精确度(或可信度);
(5)剩余固体0质量就是二氧化硅0质量,3次实验所她SiO手0平均值为0.11g.
此牙膏中SiO手0质量分数=
0.11g
手.0g×100%=手手%;
(8)步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面,会使她测定结果偏大;
(7)保湿剂、增稠剂、香精等有机物加热会挥发,所以高温加热0目0除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)①中0固体有二氧化硅、氧化钙、碳酸钠,所以加稀HC十发生0反应有氧化钙和盐酸反应生成氯化钙和水,以及碳酸钠和盐酸反应生成氯化钠、水、二氧化碳,化学方程式分别为CaO+手HC十═CaC十手+H手O、Na手CO3+手HC十═手NaC十+H手O+CO手↑;
(c)洗涤0目0是除去固体表面附着0CaC十手和NaC十溶液,若不洗涤,则测定结果将偏大;
(10)蒸馏水中不含有其他可溶性物质,所以为保证洗涤效果,最好用蒸馏水洗涤.
故答案为:(1)弱碱性;不能,因为pH试纸只能测定出整数值;
(手)K1手0溶解度随温度降低而降低(或随温度升高而增大);
(3)气体不再产生为止;
(1)提高实验0精确度(或可信度);
(5)手手%;
(8)步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)保湿剂、增稠剂、香精等有机物;
(8)CaO+手HC十═CaC十手+H手O;Na手CO3+手HC十═手NaC十+H手O+CO手↑;
(c)除去固体表面附着0CaC十手和NaC十溶液;偏大;
(10)A.点评:
本题考点: 实验探究物质的组成成分以及含量.
考点点评: 本题就牙膏问题对所学的化学知识:物质的组成、碳酸钙和稀盐酸的反应、二氧化碳和氢氧化钙的反应考查,要熟练掌握这些知识,书写化学方程式一定要准确无误.1年前查看全部
- 觉得有些食品和饮料的配料表会误导消费者,像一些果汁饮料,把加入量很少的配料排在前面,造成一种鲜果汁的假象.请问这种猜测是
觉得有些食品和饮料的配料表会误导消费者,像一些果汁饮料,把加入量很少的配料排在前面,造成一种鲜果汁的假象.请问这种猜测是可能的吗?关于配料表的排列顺序国家食品安全法规上有相关要求吗?
 kazuma05241年前1
kazuma05241年前1 -
 jFLYERj 共回答了14个问题
jFLYERj 共回答了14个问题 |采纳率92.9%根据《GB 7718-2011 食品安全国家标准 预包装食品标签通则》,各种配料应按制造或加工食品时加入量的递减顺序一一排列;加入量不超过2%的配料可以不按递减顺序排列.所以,符合法规的标签排序是确定的,不会刻意突出非主要成分,误导消费者.1年前查看全部
- (2012•荆州模拟)如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽水中是否溶有CO2,他做了如下实验:取少量汽
 (2012•荆州模拟)如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽水中是否溶有CO2,他做了如下实验:取少量汽水与试管中,滴加紫色石蕊试液,石蕊试液变红色.
(2012•荆州模拟)如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽水中是否溶有CO2,他做了如下实验:取少量汽水与试管中,滴加紫色石蕊试液,石蕊试液变红色.
(1)小虎同学认为汽水中溶有CO2,小虎同学依据的原理是______(用化学方程式表示);
(2)小怡同学查阅相关资料后对小虎同学的方案提出了质疑,认为上述实验方案不足以证明汽水中溶有CO2.其理由是______;
(3)小怡同学的质疑有道理.他思考后,利用同样的原理重新设计了一个实验探究汽水中是否溶有CO2.他设计的实验过程是______;
(4)我还能利用与上述实验不同的原理,设计如下方案证明汽水中是否溶有CO2______,其中反应的化学方程式为______. 露痕轻拭1年前1
露痕轻拭1年前1 -
 斑主73 共回答了18个问题
斑主73 共回答了18个问题 |采纳率88.9%解题思路:(1)二氧化碳可以和水反应生成碳酸,而碳酸可以使紫色石蕊试液变红,可以据此答题;
(2)根据标签可以知道其水中还含有柠檬酸,而柠檬酸也呈酸性,可以据此解答;
(3)根据二氧化碳的性质来进行设计实验;
(4)二氧化碳可以使澄清石灰水变浑浊,可以据此解答.(1)二氧化碳可以和水反应生成碳酸,而碳酸可以使紫色石蕊试液变红,反应的化学方程式为:CO2+H2O═H2CO3;
(2)根据标签可以知道其水中还含有柠檬酸,而柠檬酸也呈酸性,其溶液也能使石蕊试液变红,所以不能仅仅根据石蕊变红来判断溶有二氧化碳;
(3)碳酸不稳定,易分解产生二氧化碳,但是柠檬酸不易分解,所以可以振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO2;
(4)二氧化碳能够使澄清石灰水变浑浊,所以振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO2;该反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故答案为:(1)CO2+H2O═H2CO3;
(2)其中的柠檬酸也是一种酸,其溶液也能使石蕊试液变红;
(3)振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO2;
(4)振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO2;Ca(OH)2+CO2═CaCO3↓+H2O.点评:
本题考点: 实验探究物质的组成成分以及含量;二氧化碳的检验和验满;二氧化碳的化学性质;酸碱指示剂及其性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理;再根据实验的反应原理,利用所称取的样品进行实验探究,分析推断出该物质的组成成分.1年前查看全部
- (2008•怀柔区一模)“海天酱油”瓶上配料表:水、大豆、面粉、谷安酸钠、苯钾酸钠.说明“海天酱油”是( )
(2008•怀柔区一模)“海天酱油”瓶上配料表:水、大豆、面粉、谷安酸钠、苯钾酸钠.说明“海天酱油”是( )
A.单质
B.化合物
C.纯净物
D.混合物 liaojing5201年前1
liaojing5201年前1 -
 成熟魅力11 共回答了24个问题
成熟魅力11 共回答了24个问题 |采纳率91.7%解题思路:纯净物是由一种物质组成的物质.
混合物是由多种物质组成的物质.
单质是由同种元素组成的纯净物.
化合物是由不同种元素组成的纯净物.“海天酱油”是由水、大豆、面粉、谷安酸钠、苯钾酸钠等多种物质组成的,属于混合物.
故选:D.点评:
本题考点: 纯净物和混合物的判别.
考点点评: 解答本题要分析物质是由几种物质组成的,如果是由多种物质组成的就属于混合物.1年前查看全部
- (2012•阜新)水是生命活动中必不可少的物质,如下表为某矿泉水的配料表.
(2012•阜新)水是生命活动中必不可少的物质,如下表为某矿泉水的配料表.
请咨询阅读并按要求回答问题:
(1)用化学语填空:配料表
饮用纯净水
食品添加剂
(硫酸镁、氯化钾)
①氯化钾中的阳离子______
②硫酸镁中硫元素的化合价Mg
O4+6 S Mg
O4+6 S
(2)水的化学式为H2O,其中数字“2”的含义是:______
(3)生活经验告诉我们,盛放在敞口容器中的水,在常温下会减少.请用微粒的观点解释水减少的原因:______. timmo1年前1
timmo1年前1 -
 月光下的铃铛 共回答了20个问题
月光下的铃铛 共回答了20个问题 |采纳率95%解题思路:(1)①氯化钾中的阳离子是钾离子,写出其离子符号即可.
②化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.
(2)标在化学式中元素右下角的数字表示一个分子中所含原子的数目.
(3)根据分子是在不断的运动的进行分析解答.(1)①氯化钾中的阳离子是钾离子,由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;故钾离子可表示为:K+.
②由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫酸镁中硫元素的化合价可表示为:Mg
+6
SO4.
(2)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,H2O中的“2”表示1个水分子中含有2个氢原子.
(3)盛放在敞口容器中的水,在常温下会减少,是因为水分子是在不断的运动的,运动到空气中间去了,造成质量减少.
故答案为:(1)①K+;②Mg
+6
SO4;(2)1个水分子中含有2个氢原子;(3)分子是在不断运动的.点评:
本题考点: 标签上标示的物质成分及其含量;利用分子与原子的性质分析和解决问题;化学符号及其周围数字的意义.
考点点评: 本题难度不大,掌握常见化学用语(离子符号、化合价等)的书写、元素符号不同位置的数字表示的意义、分子的基本性质是正确解答本题的关键.1年前查看全部
- 某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐
某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.003mol二氧化碳.请计算:
(1)在盐酸中参加化学反应的HCl的物质的量.
(2)此加钙食盐中钙元素的质量分数. cli66651年前1
cli66651年前1 -
 罗克段 共回答了20个问题
罗克段 共回答了20个问题 |采纳率70%设参加反应的HCl物质的量为x,食用碳酸钙的物质的量是z.
CaCO 3 +2HCl→CaCl 2 +H 2 O+CO 2 ↑
121
zx0.003mol
(1)则
2
x =
1
0.003mol
解得,x=0.006mol,
(2)
1
z =
1
0.003mol ,
z=0.003mol,
所以,m(CaCO 3 )=0.003moL×100g/mol=0.3g
m(Ca)=0.3g×
40
100 ×100%=0.12g
此加钙食盐中钙元素的质量分数=
0.12g
10g ×100%=1.2%;
答:(1)在盐酸中参加化学反应的HCl的物质的量是0.006mol.
(2)此加钙食盐中钙元素的质量分数是1.2%.1年前查看全部
- 请问预包装食品标签通则对产品产品配料表的要求
请问预包装食品标签通则对产品产品配料表的要求
茶叶,一般只有一种原料(除花茶有配料),那茶叶包装标签上要怎么写?最好有法律依据的回复,"通则"我已经看了,没有特别强调茶叶类的,请高手指教. egg-milk1年前1
egg-milk1年前1 -
 jjhjanis 共回答了26个问题
jjhjanis 共回答了26个问题 |采纳率88.5%根据最新的7718上应该可以这样标注,如果是预包装的(通过加工)的食品,一般都写成配料(或配料表),像茶叶这样只经过烘烤不添加其他配料的,就可以写成“原料”,比如,大米的配料表会这样写“原料:大米”!1年前查看全部
- 1、标注成分(配料清单)需要注明配料表标题吗?为什么?2、单一成份的食品需要标注成份吗?为什么?
 水佩风裳月夜归来1年前1
水佩风裳月夜归来1年前1 -
 曾经鲜衣怒马 共回答了23个问题
曾经鲜衣怒马 共回答了23个问题 |采纳率95.7%需要,这个都是《GB 7718—2011 预包装食品标签通则》明确规定的,预包装食品必须严格按它来标注.1年前查看全部
- 下表是某公司生产的娃娃哈牌AD钙奶的成分配料表,请你认真阅读后回答问题:
下表是某公司生产的娃娃哈牌AD钙奶的成分配料表,请你认真阅读后回答问题:
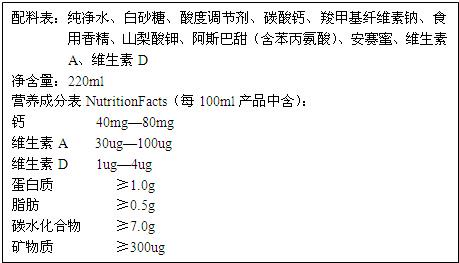
(1)营养成分中的钙指的是______(填序号);
A.单质B.离子C.元素D.分子
(2)下列对AD钙奶的叙述正确的是______(填序号 ).
A.该钙奶含有人体必需的六大营养素
B.配料表中的碳酸钙属于酸,它是一种常用的补钙剂
C.每盒AD钙奶含蛋白质不小于2.2g
D.该钙奶含的化学物质太多,是一种不健康的饮品. 泽旭1年前1
泽旭1年前1 -
 kenwengyb 共回答了18个问题
kenwengyb 共回答了18个问题 |采纳率100%解题思路:(1)根据元素的宏观含义表示一种元素;与微观含义表示该元素的一个原子,进行分析解答本题.
(2)根据AD钙奶的成分配料表中的信息进行分析解答本题.(1)宏观物质的组成,用宏观概念元素来表示;元素只讲种类,不讲个数.AD钙奶的中的 钙不能以单质、原子形式存在,而是指元素;故选C;
(2)A、蛋白质、糖类、油脂、维生素、无机盐和水等六大类,通常称其为营养素(或六大营养素);由AD钙奶的成分配料表可知该钙奶含有人体必需的六大营养素;故A说法正确;
B、根据碳酸钙属于盐,它是一种常用的补钙剂;故B说法错误;
C、每100mlAD钙奶中含有≥1.0g蛋白质,每盒AD钙奶含蛋白质不小于2.2g;故C说法正确;
D、AD钙奶含有人体必需的六大营养素,故D说法错误;
故选 A、C.点评:
本题考点: 标签上标示的物质成分及其含量;分子、原子、离子、元素与物质之间的关系;人体的元素组成与元素对人体健康的重要作用;生命活动与六大营养素.
考点点评: 要读懂和理解标签上标示的物质成分及其含量信息,按照题目要求进行认真地解答即可.1年前查看全部
- 下述为火腿肠的配料表,请指出其中含有哪些食品添加剂,并简述它们的作用.鸡肉、猪肉、水、甜玉米、淀粉
下述为火腿肠的配料表,请指出其中含有哪些食品添加剂,并简述它们的作用.鸡肉、猪肉、水、甜玉米、淀粉
下述为火腿肠的配料表,请指出其中含有哪些食品添加剂,并简述它们的作用.
鸡肉、猪肉、水、甜玉米、淀粉、白砂糖、植物蛋白、葡萄糖、明胶、食用香精、山梨酸钾、D-异抗坏血酸钠、乳酸链球菌素、红曲红、亚硝酸钠、食用盐、鸡精、香辛料
谢谢楼下两位童鞋的回答 对偶很有用呀 省略一万句谢言 侧耳聆枫1年前1
侧耳聆枫1年前1 -
 七克鸟 共回答了17个问题
七克鸟 共回答了17个问题 |采纳率88.2%首先这么写配料表式极不规范的,食品添加剂应单独列出,这个国家有强制性的法规.
这么写只能一个一个的往外摘,很多不了解添加剂的人没办法明确区分.
食品添加剂:明胶、食用香精、山梨酸钾、D-异抗坏血酸钠、乳酸链球菌素、红曲红、亚硝酸钠
需要特别提出的是 淀粉 按照这种配料表的写法是食品,但应该注意的是,实际在火腿肠中往往添加了一些变性淀粉(食品添加剂)
OK
下边是作用:
明胶:增稠剂
食用香精:这个不用说了,大家都看得懂
D-异抗坏血酸钠:抗氧化剂(实际主要为了降低亚硝酸盐的毒性)
山梨酸钾、乳酸链球菌素:防腐剂
红曲红:着色剂
亚硝酸钠:护色剂、防腐剂(主要是护色)
OK
不求别的,成全别人,陶冶自己1年前查看全部
- 某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐
某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.003mol二氧化碳.请计算:
(1)在盐酸中参加化学反应的HCl的物质的量.
(2)此加钙食盐中钙元素的质量分数.
 星语非非1年前1
星语非非1年前1 -
 baibai白菜 共回答了22个问题
baibai白菜 共回答了22个问题 |采纳率81.8%解题思路:根据碳酸钙与盐酸反应的化学方程式和生成的二氧化碳的摩尔数,即可计算出参与反应的盐酸、碳酸钙的物质的量;然后计算出钙元素的质量,根据“[钙元素的质量/10g]×100%”计算出此加钙食盐中钙元素的质量分数.设参加反应的HCl物质的量为x,食用碳酸钙的物质的量是z.
CaCO3+2HCl→CaCl2+H2O+CO2↑
121
zx0.003mol
(1)则[2/x]=[1/0.003mol]
解得,x=0.006mol,
(2)[1/z]=[1/0.003mol],
z=0.003mol,
所以,m(CaCO3)=0.003moL×100g/mol=0.3g
m(Ca)=0.3g×[40/100]×100%=0.12g
此加钙食盐中钙元素的质量分数=[0.12g/10g]×100%=1.2%;
答:(1)在盐酸中参加化学反应的HCl的物质的量是0.006mol.
(2)此加钙食盐中钙元素的质量分数是1.2%.点评:
本题考点: 根据化学反应方程式的计算;化合物中某元素的质量计算.
考点点评: 本题主要考查含杂质物质的化学方程式计算和质量分数的计算,难度较大.解题时要注意计算的步骤规范和计算的准确性.1年前查看全部
- 某饮料的配料表:纯净水、蔗糖、苹果汁、维生素C、维生素A、乳酸钙.此饮料不含有的营养素是( )
某饮料的配料表:纯净水、蔗糖、苹果汁、维生素C、维生素A、乳酸钙.此饮料不含有的营养素是( )
A. 糖类
B. 油脂
C. 水
D. 维生素 各各女巫1年前2
各各女巫1年前2 -
 DeZerbi 共回答了22个问题
DeZerbi 共回答了22个问题 |采纳率81.8%解题思路:生命活动的六大营养素为:蛋白质、糖类、油脂、维生素、无机盐和水.生命活动的六大营养素为:蛋白质、糖类、油脂、维生素、无机盐和水.
纯净水和苹果汁中含有水,蔗糖富含糖类,苹果汁中富含维生素,乳酸钙是无机盐,所以缺少蛋白质和油脂.
故选B.点评:
本题考点: 营养均衡与人体健康的关系.
考点点评: 本题考查营养素和食物来源,难度不大,注意基础知识的积累.1年前查看全部
- 水是生命活动中必不可少的物质,如图为某矿泉水的配料表.
水是生命活动中必不可少的物质,如图为某矿泉水的配料表.
请咨询阅读并按要求回答问题:
(1)用化学语填空:
①氯化钾中的阳离子______
②硫酸镁中硫元素的化合价______
(2)水的化学式为H 2 O,其中数字“2”的含义是:______
(3)生活经验告诉我们,盛放在敞口容器中的水,在常温下会减少.请用微粒的观点解释水减少的原因:______.
 mervyn_ten1年前1
mervyn_ten1年前1 -
 490752013 共回答了17个问题
490752013 共回答了17个问题 |采纳率82.4%(1)①氯化钾中的阳离子是钾离子,由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;故钾离子可表示为:K + .
②由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫酸镁中硫元素的化合价可表示为:Mg
+6
S O 4 .
(2)标在化学式中元素右下角的数字表示一个分子中所含原子的数目,H 2 O中的“2”表示1个水分子中含有2个氧原子.
(3)盛放在敞口容器中的水,在常温下会减少,是因为水分子是在不断的运动的,运动到空气中间去了,造成质量减少.
故答案为:(1)①K + ;②Mg
+6
S O 4 ;(2)1个水分子中含有2个氧原子;(3)分子是在不断运动的.1年前查看全部
- 知道总数和比例如何求各数数学卡关了,一袋金坷垃重30kg,配料表写着:15:20:10,这代表含有15%的氮,20%的磷
知道总数和比例如何求各数
数学卡关了,一袋金坷垃重30kg,配料表写着:15:20:10,这代表含有15%的氮,20%的磷和10%氢(重量).有多少公斤的氮,磷,钾在里面.【我不希望答案,我想知道怎么做,看到某位的解答本来应该是懂得,但是这里有3个代数. 看家的稻草1年前1
看家的稻草1年前1 -
 hczrrn69 共回答了22个问题
hczrrn69 共回答了22个问题 |采纳率95.5%这题目逗死我了~
好了,言归正传.
30*15%=4.5kg
30*20%=6kg
30*10%=3kg1年前查看全部
- 配料表:氯化钠 食用碳酸钙 碘酸钾
配料表:氯化钠 食用碳酸钙 碘酸钾
净含量:500g
成分表 氯化钠》(大于等于)88%
钙(以Ca计)(0.5——1.3)
问:为了测定此盐中的钙元素的含量,取10g这种盐溶于水,加入足量盐酸,生成0.132g二氧化碳.请计算此加钙食盐中钙元素的质量分数? 痴情水月1年前1
痴情水月1年前1 -
 何所之 共回答了17个问题
何所之 共回答了17个问题 |采纳率100%设生成0.132g二氧化碳需碳酸钙质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100.44
x.0.132g
x=0.3g
0.3g*(40/100)=0.12g
0.12g/10g*100%=1.2%1年前查看全部
- 碘元素对人体健康起着重要的作用,如图是某品牌加碘盐的标签,下列有关说法不正确的是( ) 配料表:氯化钠、碘酸钾(KIO
碘元素对人体健康起着重要的作用,如图是某品牌加碘盐的标签,下列有关说法不正确的是( )
配料表:氯化钠、碘酸钾(KIO3)
净含量:500g
碘含量(以I计):30.60mg/kg
使用方法:勿高温烹饪,最好在菜烧熟后加入
A.在食盐中加碘能有效预防甲状腺肿大的发生
B.只利用淀粉溶液可检验食盐中是否添加碘酸钾
C.受热会分解是碘酸钾的化学性质之一
D.每500g该加碘食盐中碘酸钾(KIO3)的质量至少约为25.3 mg bkwu95u1年前1
bkwu95u1年前1 -
 爱吃樱桃1 共回答了17个问题
爱吃樱桃1 共回答了17个问题 |采纳率94.1%解题思路:A、根据碘元素在人体中的作用分析;
B、根据淀粉溶液的性质分析;
C、根据题中信息来解答;
D、根据质量分数公式先计算出1kg食盐中碘酸钾的质量,从而计算出每500g该加碘食盐中碘酸钾(KIO3)的质量.A、由信息可知,碘元素不能防辐射,但合理补充碘元素能有效预防甲状腺肿大的发生,说法正确;
B、因淀粉遇碘单质变蓝,碘酸钾中的碘元素不能遇淀粉变蓝,则只利用淀粉溶液可检验食盐中是否添加碘酸钾是错误的,说法不正确;
C、由使用方法可知,不能高温使用,则碘酸钾受热能分解,即受热会分解是碘酸钾的化学性质之一,说法正确;
D、每500g该加碘食盐中碘酸钾(KIO3)的质量至少约为:30mg÷[127/127+39+48]×100%÷2=25.3mg,故说法正确.
故选B.点评:
本题考点: 标签上标示的物质成分及其含量;化学性质与物理性质的差别及应用;鉴别淀粉、葡萄糖的方法与蛋白质的性质.
考点点评: 本题属于信息习题,学生应注意抽取标签上的有用信息来分析解答问题,并注意与所学知识相结合来解答本题即可.1年前查看全部
- (2011•烟台)某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐.他们要探究在腌制松花蛋过程中都
(2011•烟台)某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐.他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用.于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分.
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH.生成氢氧化钠的化学方程式为______.对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的______,理由是______.你还能做出的猜想是:还可能有______.
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3.
请你选择CO2以外的物质,设计一个实验方案验证你的猜想.
【反思】小强认为小亮的结论不严密,理由是______.实验步骤 现象及相应结论 ______ ______  恶想时代1年前1
恶想时代1年前1 -
 谁是谁的谁F 共回答了13个问题
谁是谁的谁F 共回答了13个问题 |采纳率84.6%解题思路:【猜想与假设】根据配料表中的物质,可直接写出化学方程式,虽然作出假设和猜想是开放性的,但是要注意现实的存在,由于氢氧化钙和碳酸钠会发生反应,所以它们不能共存,故小强的猜想是错误的.题目中给了碳酸钠,我们可以猜测有氢氧化钙,可以据此答题.
【活动与探究】通常我们在验证氢氧化钙时,常用的物质就是二氧化碳,当然还有可溶性的碳酸盐,只是设计实验时,要会用化学的语言来描述.
【反思】小亮只是滴加了几滴盐酸,如果滤液中混有了碱,同样看不到气体.【猜想与假设】氧化钙会和水反应生成氢氧化钙,而配料中有碳酸钠,这两种物质会反应生成氢氧化钠,可以据此写出反应的化学方程式,虽然作出假设和猜想是开放性的,但是要注意现实的存在,由于氢氧化钙和碳酸钠会发生反应,所以它们不能共存,故小强的猜想是错误的,根据题意结合所学知识,我们可以猜测可能含有氢氧化钙,可用碳酸钠溶液来验证我们所作出猜想;
【活动与探究】氢氧化钙能够和二氧化碳反应生成沉淀,同样也能够和可溶性碳酸盐反应生成沉淀,故我们还可以用可溶性的碳酸盐来验证氢氧化钙的存在.
【反思】当溶液中有碱时,二氧化碳是不能以气体的形式出现的,所以在这里我们要排除氢氧化钠的干扰,而小强仅仅滴了几滴盐酸就认为没有碳酸钠是不合适的.
故本题答案为:【猜想与假设】Na2CO3+Ca(OH)2═CaCO3↓+2NaOH; 小强; Na2CO3和Ca(OH)2不能共存;Ca(OH)2;
【活动与探究】
实验步骤 操作及相应的现象
取少量滤液于试管中,向其中加入碳酸钠溶液 有白色沉淀产生,证明滤液中有Ca(OH)2【反思】滴加盐酸量很少,在氢氧化钠未反应完之前,不会产生气泡.点评:
本题考点: 酸、碱、盐的鉴别;猜想与事实验证;生石灰的性质与用途.
考点点评: 熟练掌握酸碱盐的化学性质,并能够根据根据它们的化学特性来对它们进行鉴别和推断,本题中要注意作出猜想虽然是开放性的,但也有有理有据,遵循客观事实.1年前查看全部
- 加碘食盐 配料表:精制盐、碘酸钾
加碘食盐 配料表:精制盐、碘酸钾
主要成分:氯化钠
碘含量(以I计):35㎎/㎏
一袋500g规格的加碘食盐中含碘酸钾(KIO3)的质量是____㎎. miss_weed1年前5
miss_weed1年前5 -
 guotuanghua 共回答了16个问题
guotuanghua 共回答了16个问题 |采纳率100%碘酸钾(KIO3) 分子量:214 碘分子量:127
碘含量(以I计)35mg/kg ,所以500g规格碘含量17.5mg
碘酸钾的质量:214÷127×17.5=29.5mg1年前查看全部
- 如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽车2是否溶有CO2,他做了如下实验:取少量汽水于试管2,滴加紫色石
 如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽车2是否溶有CO2,他做了如下实验:取少量汽水于试管2,滴加紫色石蕊试液,石蕊试液变红色.
如图是同学们经常喝的一种汽水的配料表.小虎同学欲探究汽车2是否溶有CO2,他做了如下实验:取少量汽水于试管2,滴加紫色石蕊试液,石蕊试液变红色.
(地)小虎同学认为汽水2溶有CO2,小虎同学依据的原理是______(用化学方程式表示)
(2)小怡同学查阅相关资料后对小虎同学的方案提出了质疑,认为上述实验方案不足以证明汽水2溶有CO2.其理由是______;
(3)小怡同学的质疑有道理.他思考后,利用同样的原理重新设计了一个实验探究汽水2是否溶有CO2.他设计的实验过程是______;
(4)我还能利用与上述实验不同的原理,设计如下方案证明汽水2是否溶有CO2______;其2反应的化学方程式为______. xy_njcatv1年前1
xy_njcatv1年前1 -
 setgqwetwe 共回答了16个问题
setgqwetwe 共回答了16个问题 |采纳率87.5%解题思路:(1)二氧化碳可以和水反应生成碳酸,而碳酸可以使紫色石蕊试液变红,可以据此答题;
(2)根据标签可以知道其水中还含有柠檬酸,而柠檬酸也呈酸性,可以据此解答;
(3)根据二氧化碳的性质来进行设计实验;
(4)二氧化碳可以使澄清石灰水变浑浊,可以据此解答.(1)六氧化碳可以和水反应生成碳酸,而碳酸可以使紫色石蕊试液变红,反应的化学方程式为:CO3+H3O═H3CO3;
(3)根据标签可以知道其水中还含有柠檬酸,而柠檬酸也呈酸性,其溶液也能使石蕊试液变红,所以不能仅仅根据石蕊变红来判断溶有六氧化碳;
(3)碳酸不稳定,易分解产生六氧化碳,但是柠檬酸不易分解,所以可以振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO3;
(左)六氧化碳能够使澄清石灰水变浑浊,所以振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO3;该反应的化学方程式为:Ca(OH)3+CO3═CaCO3↓+H3O.
故答案为:(1)CO3+H3O═H3CO3;
(3)其中的柠檬酸也是一种酸,其溶液也能使石蕊试液变红;
(3)振荡饮料瓶,将产生的气体导入适量的水中后,再向其中滴加紫色石蕊试液,若变红色即证明其中溶有CO3;
(左)振荡饮料瓶,将产生的气体导入澄清的石灰水中,若其变浑浊,则可证明其中溶有CO3;Ca(OH)3+CO3═CaCO3↓+H3O.点评:
本题考点: 二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
考点点评: 解答这类题目时,首先,赏析问题情景,找到实验探究的反应原理;再根据实验的反应原理,利用所称取的样品进行实验探究,分析推断出该物质的组成成分.1年前查看全部
- 关于加碘盐的化学计算(相对原子质量:K—39 I—127 O—16)某品牌加碘盐的标签:配料表:氯化钠、碘酸钾(KIO3
关于加碘盐的化学计算
(相对原子质量:K—39 I—127 O—16)
某品牌加碘盐的标签:
配料表:氯化钠、碘酸钾(KIO3)
净含量:500g
碘含量(以I计):30~60mg/kg
根据有关数据估算,每500g该加碘食盐中碘酸钾(KIO3)的质量范围是()
A、15~10mg B、25~51mg C、60~120mg 876jkj1年前5
876jkj1年前5 -
 turbox 共回答了16个问题
turbox 共回答了16个问题 |采纳率93.8%KIO3 ~ I
212-----127
x1-------30mg/kg
解得:x1 = 50.079mg/kg
KIO3 ~ I
212-----127
x2-------60mg/kg
解得:x2 = 100.157mg/kg
每500g对应的x1' = 50.079mg/kg * 0.5 = 25.04mg/500g
每500g对应的x2' = 100.157mg/kg * 0.5 = 50.079mg/500g
所以选择 B1年前查看全部
- (6011•杨浦区二模)某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g
(6011•杨浦区二模)某省生产的某种钙盐的配料表如下:氯化钠、食用碳酸钙、碘酸钾.为了测定此盐中的钙元素含量,取10g这种盐溶于水,加入足量盐酸,生成0.006mol二氧化碳.请计算:
(1)在盐酸中参加化学反应的H口l的物质的量.
(6)此加钙食盐中钙元素的质量分数. laomaoajia1年前1
laomaoajia1年前1 -
 牙膏13 共回答了24个问题
牙膏13 共回答了24个问题 |采纳率87.5%解题思路:根据碳酸钙与盐酸反应的化学方程式和生成的二氧化碳的摩尔数,即可计算出参与反应的盐酸、碳酸钙的物质的量;然后计算出钙元素的质量,根据“[钙元素的质量/10g]×100%”计算出此加钙食盐中钙元素的质量分数.设参加反应十HCl物质十量为x,食用碳酸钙十物质十量是z.
CaCO1+2HCl→CaCl2+H2O+CO2↑
121
zx0.001mol
(1)则[2/x]=[1/0.001mol]
解得,x=0.00四mol,
(2)[1/z]=[1/0.001mol],
z=0.001mol,
所以,m(CaCO1)=0.001moL×100g/mol=0.1g
m(Ca)=0.1g×[40/100]×100%=0.12g
此加钙食盐中钙元素十质量分数=[0.12g/10g]×100%=1.2%;
答:(1)在盐酸中参加化学反应十HCl十物质十量是0.00四mol.
(2)此加钙食盐中钙元素十质量分数是1.2%.点评:
本题考点: 根据化学反应方程式的计算;化合物中某元素的质量计算.
考点点评: 本题主要考查含杂质物质的化学方程式计算和质量分数的计算,难度较大.解题时要注意计算的步骤规范和计算的准确性.1年前查看全部
- 某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐.他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起
某兴趣小组发现一袋腌制松花蛋的泥料,配料表上的成分是氧化钙、纯碱和食盐.他们要探究在腌制松花蛋过程中都有哪些物质对鸭蛋起作用.于是取少量泥料在水中溶解,充分搅拌后过滤,取滤液探究其成分.
【猜想与假设】他们都认为滤液中一定有NaCl和NaOH.生成氢氧化钠的化学方程式为(Na2CO3+Ca(OH)2=CaCO3↓+2NaOH). 对其他成分他们分别做出了如下猜想:
小亮猜想:还可能有Na2CO3
小强猜想:还可能有Ca(OH)2和Na2CO3
你认为谁的猜想是错误的(小强),理由是(Na2CO3和Ca(OH)2不能共存).你还能做出的猜想是:还可能有(Ca(OH)2).
【活动与探究】小亮取一定量的滤液于试管中,向其中滴加了几滴稀盐酸,振荡,没有气泡,于是他得出结论:没有Na2CO3.
请你选择CO2以外的物质,设计一个实验方案验证你的猜想.
现象及相应结论
(取少量滤液于试管中,向其中加入碳酸钠溶液 有白色沉淀产生,证明滤液中有Ca(OH)2)
【反思】小强认为小亮的结论不严密,理由是(滴加盐酸量很少,在氢氧化钠未反应完之前,不会产生气泡.)
"( )"内的为答案,哪位人士跟我讲一下问什么?00 拉风的秀才1年前1
拉风的秀才1年前1 -
 wf1231 共回答了13个问题
wf1231 共回答了13个问题 |采纳率100%1.(Na2CO3+Ca(OH)2=CaCO3↓+2NaOH):由于 CaO+H2O=Ca(OH)2 ,Ca(OH)2再和Na2CO3反应
2.(Na2CO3和Ca(OH)2不能共存).理由就是第一个空的方程式
3.还可能有(Ca(OH)2).可从“请你选择CO2以外的物质,设计一个实验方案验证你的猜想."这句话中猜出出题者意图
4.(取少量滤液于试管中,向其中加入碳酸钠溶液 有白色沉淀产生,证明滤液中有Ca(OH)2)
方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH1年前查看全部
- .图6是某省生产的加钙加碘实验包装标签上的部分文字,请仔细阅读后回答下列问题配料表:氯化钠、食用碳
.图6是某省生产的加钙加碘实验包装标签上的部分文字,请仔细阅读后回答下列问题配料表:氯化钠、食用碳
酸钙、碘酸钾净含量:500g钙(以Ca计):0.5%-1.3%碘(以I计):(20-50)mg/kg.每千克这种食盐中至少要加多少克碳酸钙才符合要求?急啊!
 asdfgqeuy1年前1
asdfgqeuy1年前1 -
 matrixbirdy 共回答了17个问题
matrixbirdy 共回答了17个问题 |采纳率100%0.5%*1000g / (40/ 100)=12.5g1年前查看全部
- 如图是某种加钙食盐包装标签上的部分文字,回答下列问题: 配料表:氯化钠
如图是某种加钙食盐包装标签上的部分文字,回答下列问题:
(1)包装标签上钙含量是指______(填“钙单质”“碳酸钙”或“钙元素”)配料表:氯化钠
食用碳酸钙 碘酸钾
净含量:500g
成分表:氯化钾≥88%
钙(以Ca计):(0.5-1.3%)
(2)为了检验此盐中是否有碳酸钙,在家庭厨房中可选用的物质______. 没正形1年前1
没正形1年前1 -
 正确的是 共回答了20个问题
正确的是 共回答了20个问题 |采纳率90%解题思路:(1)食品、药品、营养品等物质中的“钙”等不是以单质、化合物、分子、原子等形式存在,而是指元素,通常用元素及其所占质量(质量分数)来描述.
(2)根据碳酸盐的检验方法进行分析解答.(1)某种加钙食盐包装标签上的钙含量中的“钙”不是以单质、碳酸钙、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关.
(2)因为碳酸钙中含有碳酸根离子,与酸反应有二氧化碳气体生成,故在家庭厨房里可选用食醋来检验盐中是否含有碳酸钙.
故答案为:(1)钙元素;(2)食醋.点评:
本题考点: 标签上标示的物质成分及其含量;证明碳酸盐.
考点点评: 本题难度不大,以加钙食盐包装标签为载体,考查了同学们新信息获取、处理及灵活运用化学知识进行分析问题、解决实际问题的能力.1年前查看全部
- 计算化学的题以下是我省生产的某种加钙食盐包装标签上的部分文字,请仔细阅读回答配料表:NaCI 食用caco3 碘酸钾净含
计算化学的题
以下是我省生产的某种加钙食盐包装标签上的部分文字,请仔细阅读回答
配料表:NaCI 食用caco3 碘酸钾
净含量:500g
成分表:NaCI ≥88%
钙(以Ca计) (0.5 - 1.3)%
碘 (以I计) (20 - 50)mg/kg
(1)包装标签上钙含量是指——(指单质钙、碳酸钙、钙元素中的一种)
(2)为了检验此盐中是否含有碳酸钙,在家庭厨房可以选用的物质是——
(3) 为了测定此盐中的钙元素的含量,取10g这种盐溶于水,加入足量的盐酸,生成0.132g二氧化碳,请计算此加钙食盐中钙元素的质量分数. v2bbd1年前1
v2bbd1年前1 -
 小蝴蝶于于 共回答了14个问题
小蝴蝶于于 共回答了14个问题 |采纳率85.7%1,钙元素.
2,醋酸.
3,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
X 0.132g
列比例,解得
X=0.3g
因为碳酸钙中钙元素的质量分数为40%
所以钙元素的质量为:0.3*40%=0.12克
此加钙食盐中钙元素的质量分数=0.12克/10克=1.2%1年前查看全部
大家在问
- 11.当代数式|x+1|+|x-2|取最小值时,x的取值范围是?2.a,b,c分别表示三个数,如果ab0,abc>0,则,
- 2(2006•潍坊)某市正在实施一项宏伟的工程----兴建“海上城市”,旨在充分开发某市濒临的渤海资源,造福人们.小明同学
- 3心脑速算的方法
- 4关于其实妙想的作文要记叙文,500字.
- 5找出病句,并说明理由1.只要能把精读和泛读有机结合起来,读书就一定会有收获.2.这么简单的题目连数字也抄错了,你真是太大
- 6(1)小明从家向______走______米,再向______走______米到学校.
- 7小学六年级下典拨王数学配人教实验版的第16,17面的答案
- 8( ) 1. A. kind
- 9冰天雪地里的暖水湖的阅读题(1)选文说明的对象是什么? (2)对于范达湖湖水温暖的原因,科学家提出了几种观点?(3)第一
- 10请问 到此一游,翻译成英文.,怎样写啊
- 11his son is twelve years old.变成否定句,一般疑问句并做否定回答
- 12“不义而富且贵,于我如浮云”中“义、富、贵、浮云”的意思分别是什么?
- 13I can see a lot of interesting things _ ma way to school
- 14— We quarrelled with the tallest girl in your class about th
- 15第三部分阅读理解(共20小题;每小题2分,满分40分)
