六 一小包糖分给几个小朋友,如果毎人分3块,则余3块;如果每人分5块,则少一块.那么小朋友有多少人
 熟读唐诗三百首2022-10-04 11:39:541条回答
熟读唐诗三百首2022-10-04 11:39:541条回答糖有多少块?

已提交,审核后显示!提交回复
共1条回复
 爱上微笑的感觉 共回答了16个问题
爱上微笑的感觉 共回答了16个问题 |采纳率87.5%- 小朋友:﹙3+1﹚÷﹙5-3﹚=2人
糖:2×5-1=9 - 1年前
相关推荐
- 食品的包装袋内常放入一小包干燥剂,其主要成分为生石灰吗?
 尤一人1年前1
尤一人1年前1 -
 佳吖_mm 共回答了24个问题
佳吖_mm 共回答了24个问题 |采纳率91.7%一般有三种:
1.生石灰干燥剂
生石灰干燥剂的主要成分为氧化钙,其吸水能力是通过化学反应来实现的,因此吸水具有不可逆性.不管外界环境湿度高低,它能保持大于自重35%的吸湿能力,更适合于低温度保存,具有极好的干燥吸湿效果,而且价格 较低.可广泛用于食品、服装、茶叶、皮革、制鞋、电器等行业.
2.硅胶干燥剂
此干燥剂是透湿性小袋包装的不同品种的硅胶,主要原料硅胶是一种高微孔结构的含水二氧化硅,无毒、无味、无嗅,化学性质稳定,具强烈的吸湿性能.因而广泛用于仪器、仪表、设备器械、皮革、箱包、鞋类、纺织品、食品、药品等的贮存和运输中控制环境的相对湿度,防止物品受潮,霉变和锈蚀.
3.蒙脱石干燥剂
此干燥剂采用纯天然原料膨润土,绿色环保,无毒无味,对人体无损害.它在室温及一般湿度下吸附性能良好,具有吸附活性,静态减湿和异味去除等功效.不仅吸附速度快,吸附能力高且无毒、无味、无接触腐蚀性、无环境污染,尤其应用于食品包装,对人体无害.适用范围:广泛应用于不能采用油封、气相封存的产品中,诸如:光学仪器、电子产品、医学保健、食品包装及军工产品和民用产品的干燥空气封存.
食品中的干燥剂一般是无毒、无味、无接触腐蚀性、无环境污染;而实验室的干燥剂如浓硫酸,碱石灰等等就太危险了,但是它们也有优点,例如吸水极快,效率高,价格便宜等.1年前查看全部
- 为了防止月饼变质,常在月饼的内包装中放入一小包防腐剂,其主要成分是铁粉,铁粉的作用是________________.
为了防止月饼变质,常在月饼的内包装中放入一小包防腐剂,其主要成分是铁粉,铁粉的作用是________________.
“百炼成钢”(将反复烧红的生铁在空气中不断捶打,转化为钢)所涉及的一个化学方程式是_________________________.
 蓝山游牧1年前4
蓝山游牧1年前4 -
 8234ed 共回答了12个问题
8234ed 共回答了12个问题 |采纳率83.3%1、Fe为双吸剂(水和氧气)
2、生铁中碳的含量较高,所以在高温下,通过捶打以及与空气中的氧气接触,使碳与氧气反应生成二氧化碳(C+O2=CO2 ,条件为高温或点燃)从而使碳的含量降低,使生铁变为钢.1年前查看全部
- 在一杯温开水中加入一大勺糖和一小包酵母,进行搅拌.将这个杯子中的液体倒入透明的矿泉水瓶中,将一个小气球挤瘪套在瓶口,将瓶
在一杯温开水中加入一大勺糖和一小包酵母,进行搅拌.将这个杯子中的液体倒入透明的矿泉水瓶中,将一个小气球挤瘪套在瓶口,将瓶子放在教室内的窗台上
(1)观察瓶中会不会冒出气泡,气球会胀大吗?
(2)使气球胀大的气体是什么气体?
(3)这种现象叫什么现象? PrinceAnn1年前1
PrinceAnn1年前1 -
 佛是一滴泪 共回答了25个问题
佛是一滴泪 共回答了25个问题 |采纳率72%(1)观察到瓶中液体出现的现象是有气泡产生,这是酵母菌分解糖产生的气体.酵母菌进行发酵,分解糖产生酒精和二氧化碳,产生大量的二氧化碳气体,能使小气球会膨胀起来.
(2)酵母菌进行发酵,分解糖产生酒精和二氧化碳,因此,使气球胀大的气体是二氧化碳.
(3)发酵就是有机物在一定温度下被酵母或其他菌类分解成某些产物的过程.酵母菌在有氧气时,葡萄糖被彻底分解为二氧化碳、水、大量能量,用于制作蒸馒头、面包.没有氧的情况下,葡萄糖的分解不彻底,产物是酒精、二氧化碳和少量能量,用于酿酒.因此,这种现象叫发酵.
故答案为:
(1)产生气泡;小气球会膨胀起来;
(2)二氧化碳;
(3)发酵.1年前查看全部
- (4分)食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,上面的部分文字如图如示。请仔细阅读,回答下列问题:
(4分)食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,上面的部分文字如图如示。请仔细阅读,回答下列问题:
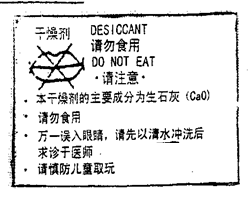
(1)这包干燥剂吸收水分的反应的化学方程式是 。
(2)“请勿食用”是因为干燥剂吸水后具有 性。
(3)如果误食入口,应该 冲洗。 44737361年前1
44737361年前1 -
 我Candy 共回答了19个问题
我Candy 共回答了19个问题 |采纳率73.7%(1)CaO+H 2 O=Ca(OH) 2 ;(2)腐蚀性;(3)水或食醋冲洗
(1)这包干燥剂吸收水分的反应方程式是:CaO+H 2 O=Ca(OH) 2 ;
(2)因为干燥剂的主要成份是生石灰,吸收水分后生成氢氧化钙,氢氧化钙有强碱性,对皮肤、织物、器皿等物质有腐蚀作用;
(3)①因为用水冲洗可以降低氧化钙的浓度,以达到没有腐蚀性的目的;
②因为CaO溶于水后生成氢氧化钙,氢氧化钙可以与食醋反应生成醋酸钙,醋酸钙是没有腐蚀性的,食醋也是无毒的,所以应该用食醋洗.1年前查看全部
- (2009•大港区模拟)在盛有温开水的瓶中加入一大勺糖和一小包酵母菌,摇匀后,将一个挤瘪的小气球套在瓶口处.将瓶子放在2
 (2009•大港区模拟)在盛有温开水的瓶中加入一大勺糖和一小包酵母菌,摇匀后,将一个挤瘪的小气球套在瓶口处.将瓶子放在25℃的条件下,一段时间后,瓶口的小气球鼓了起来(如图所示),对此现象最好的解释是( )
(2009•大港区模拟)在盛有温开水的瓶中加入一大勺糖和一小包酵母菌,摇匀后,将一个挤瘪的小气球套在瓶口处.将瓶子放在25℃的条件下,一段时间后,瓶口的小气球鼓了起来(如图所示),对此现象最好的解释是( )
A.酵母菌属于真菌
B.酵母菌不能进行光合作用
C.酵母菌能把糖转化为酒精并产生二氧化碳
D.瓶中的糖为酵母菌提供了营养,产生了氧气 zhu888991年前1
zhu888991年前1 -
 peggyzhao2002 共回答了20个问题
peggyzhao2002 共回答了20个问题 |采纳率95%1年前查看全部
- (2003•宿迁)(1)某绢纺厂需用0.5%的烧碱溶液洗去绢丝上的油污,现有一小包烧碱固体,要将其配成该溶液,需要进行如
 (2003•宿迁)(1)某绢纺厂需用0.5%的烧碱溶液洗去绢丝上的油污,现有一小包烧碱固体,要将其配成该溶液,需要进行如下操作:
(2003•宿迁)(1)某绢纺厂需用0.5%的烧碱溶液洗去绢丝上的油污,现有一小包烧碱固体,要将其配成该溶液,需要进行如下操作:
①称量.其正确的操作步骤依次为______(填序号)
a、调节天平平衡;
b、向右盘先加大砝码,后加上小砝码;
c、向左盘已知质量的烧杯中加入烧碱;
d、移动游码至天平平衡;
e、读数并记录质量为4.5克
②通过计算量取______毫升的水.该步骤操作所需的主要仪器有______
③溶解.其中玻璃棒的主要作用是______以及便于热量散发.
(2)在点燃可燃性气体之前,必须要______以防爆炸.某校化学兴趣小组根据爆炸原理,利用废旧眼药水瓶,对点燃可燃性气体装置进行了如右图设计,点燃时就可有效地防止爆炸.其原因是(至少写一条)______. niucha1234561年前1
niucha1234561年前1 -
 qingsuyiye 共回答了23个问题
qingsuyiye 共回答了23个问题 |采纳率82.6%解题思路:(1)①根据称量药品的方法和步骤考虑;②用4.5g除以0.5%计算出总溶液质量,再减去溶质的质量算出水的质量,再算出水的体积,根据量取水的方法考虑用到的仪器;③根据溶解时玻璃棒的仪器考虑;(2)本考点是防范爆炸的措施,任何可燃性气体如果不纯都有引起爆炸的危险.本题中设计的防止爆炸的方案比较好,即使气体不纯,由于水槽中有水,也可以防止爆炸的发生.(1)①称量药品的方法:先调节天平平衡,在左盘放上药品,向右盘上加砝码,先加质量大的砝码,再加质量小的砝码,最后移动游码,读出数值进行记录;
②根据溶液质量=[溶质质量/溶质质量分数],所以溶液质量=[4.5克/0.5%]=900克,需要水质量为900克-4.5克=895.5克,即895.5mL,量水的主要仪器是量筒和胶头滴管;
③溶解时玻璃棒的作用是搅拌,加速氢氧化钠溶解;
(2)可燃性气体在使用之前都要检查气体的纯度,如果不纯容易引起爆炸.本题中设计的实验方案比较好,如果气体不纯可以防止爆炸.因为气体燃烧是在眼药水瓶口处,如果不纯,因为水槽中有水,火焰也不会进入制取装置,并且水可以灭火.故答案为:验纯;降低温度到着火点以下;防止火焰进入发生装置.
故答案为:(1)①a、c、b、d、e;②895.5;量筒和胶头滴管;③搅拌,加速溶解;(2)验纯;降低温度到着火点以下;防止火焰进入发生装置.点评:
本题考点: 一定溶质质量分数的溶液的配制;氢气、一氧化碳、甲烷等可燃气体的验纯.
考点点评: 本题属于对实验设计的评价题,此类题型考查了学生对不同实验设计的理解能力,并发散学生的思维,使学生能从不同方面对实验设计进行评价.1年前查看全部
- 一些食品的包装袋内常放有一小包干燥剂,干燥剂袋上的部分文字如图模,请仔细阅读并回答下列问题: 干燥剂DESICCANT
一些食品的包装袋内常放有一小包干燥剂,干燥剂袋上的部分文字如图模,请仔细阅读并回答下列问题:
(1)“请勿食用”是因为干燥剂食用后,对人体有______作用.干燥剂DESICCANT 
请勿食用
DO NOT EAT
请注意:
本干燥剂的主要成分为生石灰(CaO)
请勿食用
万一误入眼睛,请先以清水冲洗后求诊于医师
谨防儿童取玩
(2)写出干燥剂的主要成分吸水过程中,发生反应的化学方程式:______. gjzw35561年前1
gjzw35561年前1 -
 airman025 共回答了22个问题
airman025 共回答了22个问题 |采纳率90.9%此干燥剂的成分为生石灰,可与水反应生成氢氧化钙,同时放出大量的热,氢氧化钙具有腐蚀性,所以本题答案为:灼伤与腐蚀,CaO+H 2 0=Ca(OH) 2 .1年前查看全部
- 铁粉为什么属于“双吸剂”“双吸剂”:食品袋内的一小包物质可以吸收氧气和水分.
 wenshikui1年前1
wenshikui1年前1 -
 绿水江南 共回答了18个问题
绿水江南 共回答了18个问题 |采纳率83.3%我想是利用铁生锈
Fe中一般都含C
就可以构成原电池
电极反应:正极(C):2H2O+O2+4e=4OH-
负极(Fe):Fe-2e=Fe2+
总反应:2Fe+O2+2H2O=2Fe(OH)2
然后再氧化:
4Fe(OH)2+O2+2H2O=4Fe(OH)31年前查看全部
- 在包装中放入一小包防腐剂,其主要成分是铁粉,铁粉的作用是什么?这种铁粉可以在实验室里用CO还原Fe2O3粉末而得到,进行
在包装中放入一小包防腐剂,其主要成分是铁粉,铁粉的作用是什么?这种铁粉可以在实验室里用CO还原Fe2O3粉末而得到,进行该实验前应先做什么,以确保安全?
 em2jkm0i1年前1
em2jkm0i1年前1 -
 l888y999h888 共回答了14个问题
l888y999h888 共回答了14个问题 |采纳率92.9%铁粉是防潮剂不是防腐剂……铁粉与H2O反应得到Fe2O3.xH2O.保证食品不受潮.
还原反应需要高温,注意安全.且CO有毒,注意通风.
3CO+Fe2O3=高温=2Fe+3CO21年前查看全部
- 旺旺食品公司在“旺旺雪饼”的包装袋内都放有一小包干燥剂,上面的部分文字见如图.请看图回答下列问题:
 旺旺食品公司在“旺旺雪饼”的包装袋内都放有一小包干燥剂,上面的部分文字见如图.请看图回答下列问题:
旺旺食品公司在“旺旺雪饼”的包装袋内都放有一小包干燥剂,上面的部分文字见如图.请看图回答下列问题:
(1)写出这包干燥剂吸收水分时发生反应的化学方程式:______.
(2)从物质性质的角度上看,这包干燥剂不能食用的原因是什么?______. wxl_pds1年前1
wxl_pds1年前1 -
 叶落zhi秋 共回答了14个问题
叶落zhi秋 共回答了14个问题 |采纳率100%解题思路:根据标签内容可知此干燥剂为生石灰,可与水反应生成氢氧化钙,氢氧化钙具有腐蚀性.(1)这包干燥剂吸收水分是氧化钙和水反应生成氢氧化钙,该反应的方程式为:CaO+H2O=Ca(OH)2;
(2)因为干燥剂的主要成份是生石灰,吸收水分后生成氢氧化钙,氢氧化钙属于强碱,有腐蚀作用.
故答案为:(1)CaO+H2O=Ca(OH)2;
(2)氢氧化钙属于强碱,有腐蚀作用.点评:
本题考点: 生石灰的性质与用途.
考点点评: 本题主要考查学生对氧化钙和氢氧化钙的性质的认识,了解一些常见的干燥剂.注重基础知识的考查.1年前查看全部
- 回到学校,他取出从家里带来的一小包纯碱样品进行实验:准确称取5.5 g样品放入烧杯中,在滴加盐酸至刚好完全反应(忽略CO
回到学校,他取出从家里带来的一小包纯碱样品进行实验:准确称取5.5 g样品放入烧杯中,在滴加盐酸至刚好完全反应(忽略CO2溶于水),共用去稀盐酸25 g,得溶液质量为28.3 g(杂质溶于水且与盐酸不反应).求:(计算结果精确到0.1%)
(1)生成CO2的质量是
第一题为什们不能用25/2*(1+35.5)=X/16*2+12,设CO2质量为Xg 蔚深蓝1年前1
蔚深蓝1年前1 -
 luocongcc 共回答了19个问题
luocongcc 共回答了19个问题 |采纳率73.7%稀盐酸25g,稀盐酸是HCL融于水的产物阿,不是25gHCL,所以不能这么算1年前查看全部
- 一道关于物体密度的物理题!现有如下器材:贴有刻度的平底均匀试管一支,黄沙一小包,水一杯.请利用这些器材,根据阿基米德原理
一道关于物体密度的物理题!
现有如下器材:贴有刻度的平底均匀试管一支,黄沙一小包,水一杯.请利用这些器材,根据阿基米德原理,测定液体的密度.
1、制定探究方案
2、设计试验数据记录表格,列出待液体密度的计算式 popp011年前1
popp011年前1 -
 soho营销网 共回答了19个问题
soho营销网 共回答了19个问题 |采纳率84.2%1、将试管放入水杯,使垂直漂浮,记录试管上地水刻度.x0
2、试管内倒入黄沙适量,试管垂直漂浮,记录试管上的刻度.x1
3、将水倒掉,倒入液体,将有黄沙试管放入液体漂浮,记录刻度.x2
则:x1*1000=x2*p
p=x1/x2*1000 (kg/m3)
注意,一定要记录好刻度.1年前查看全部
- 在化学实验课上,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种物质的混合物,请你和同学们一起探
在化学实验课上,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种物质的混合物,请你和同学们一起探究黑色粉末的成分.
(提出假设)假设①黑色粉末是炭粉;假设②黑色粉末是______;假设③黑色粉末是______.
(设计实验)同学们对实验做了如下设想和分析,取少量黑色粉末于烧杯中,加入过量的稀硫酸,充分搅拌后,静置.请你完成下表:
(实验验证)通过实验并对实验现象进行分析,确定了黑色粉末是炭粉和氧化铜的混合物.实验中可能出现的现象 结论 ______ 假设①成立 ______ 假设②成立 ______ 假设③成立
(拓展思维)为了进一步探究炭粉和氧化铜的性质,同学们又利用这种混合物补充做了如下实验:将此混合物隔绝空气加热到高温,待反应停止后冷却到室温,得到剩余固体X,再将X加入到过量的稀硫酸中,充分搅拌后,静置.
(1)若静置后溶液呈无色,则溶液中含有的溶质是______;
(2)若静置后溶液呈蓝色,则溶液中含有的溶质是______,剩余固体X中一定含有______. love晓雅1年前1
love晓雅1年前1 -
 Dennis1998 共回答了18个问题
Dennis1998 共回答了18个问题 |采纳率94.4%(提出假设)根据题意,可以做出三种假设,即第一种可能是只有炭粉,第二中可能是只有氧化铜,第三种可能是氧化铜与炭粉的混合物;
(设计实验)炭粉不会与稀硫酸反应,氧化铜会与稀硫酸反应生成硫酸铜溶液,硫酸铜溶液显蓝色,根据结论可以推测反应现象:
(拓展思维)炭粉与氧化铜在隔绝空气加热的条件下会发生反应即C+2CuO
高温
.
2Cu+CO 2 ↑,题意中有告诉我们,炭粉完全反应,所以最终的固体有两种可能,一种可能是只有铜,另一种可能是铜和氧化铜的混合物,当只有铜时,铜和硫酸不反应,溶液为无色,当X是铜和氧化铜的混合物时,溶液为蓝色;
故答案为:(提出假设)②氧化铜;③炭和氧化铜的混合物.
(设计实验)
实验中可能出现的现象 结论
①溶液为无色,有黑色不溶物 假设1成立
②溶液为蓝色 假设2成立
③溶液为蓝色,有黑色不溶物 假设3成立 (拓展思维)
(1)H 2 SO 4 ;
(2)CuSO 4 ,Cu和CuO.1年前查看全部
- (2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:
(2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:①Ca(HCO3)2
CaCO3+CO2↑+H2O ②2NaHCO3△ .
Na2CO3+CO2↑+H2O ),将生成的CO2全部通入足量的石灰水中产生bg CaCO3沉淀;芳芳在小明加热、冷却后的试管中又加入足量的稀盐酸,再将生成的气体全部通入足量的石灰水,结果产生cg CaCO3沉淀.那么下列关系一定正确的是( )△ .
A. a=c
B. a<b+c
C. b<c
D. a<b 放纵灵魂1年前1
放纵灵魂1年前1 -
 NANAYUEYUE 共回答了21个问题
NANAYUEYUE 共回答了21个问题 |采纳率95.2%解题思路:混合物中碳元素通过两条途径分别转化到碳酸钙沉淀中,其中一条途径是通过加热分解出的二氧化碳与氢氧化钙反应而转移到碳酸钙中,另一途径则是把分解后碳酸钙与碳酸钠中的碳转变为二氧化碳后再与氢氧化钙反应而转移到碳酸钙中;根据题意,两条途径所转移碳元素的质量相等,因此两个途径所得到的碳酸钙也相等;而固体混合物中碳元素的质量分数大于碳酸钙中碳元素质量分数,因此也得到最终所得碳酸钙的总质量大于原固体混合物的质量.根据①Ca(HCO3)2
△
.
CaCO3+CO2↑+H2O,碳酸氢钙中碳元素平均转移到生成的碳酸钙和二氧化碳中; ②2NaHCO3
△
.
Na2CO3+CO2↑+H2O 碳酸氢钠中的碳元素也平均转移到碳酸钠和二氧化碳中;由此可判断受热分解后所得二氧化碳气体中碳元素质量与剩余固体中碳元素质量相等;所以加热分解所得气体二氧化碳的质量等于剩余固体与盐酸反应放出二氧化碳气体的质量,可判断b=c;
根据化学变化前后元素质量不变,小明和芳芳所得碳酸钙的总和(b+c)g中碳元素全部来自于固体混合物中所有碳元素,即(b+c)g碳酸钙中所含的碳元素质量等于ag的NaHCO3和Ca(HCO3)2的固体混合物中所含的碳元素的质量;而碳酸钙中碳元素的质量分数=[12/100]×100%=12%,碳酸氢钠中碳元素质量分数=[12/84]×100%≈14%,碳酸氢钙中碳元素的质量分数=[24/162]×100%≈15%,由此可知碳酸钙中碳元素的质量分数小于NaHCO3和Ca(HCO3)2的固体混合物中碳元素的质量分数,因此当两者碳元素质量相等时,两者的质量关系为:a<b+c;
由于b=c,而NaHCO3和Ca(HCO3)2的固体混合物中碳元素的质量分数在14%~15%之间,而碳酸钙中碳元素质量分数为12%,可得a>b=c,因此a=c、a<b的判断都不正确;
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 根据化学变化前后元素质量不变,解答本题时需要关注转化过程中碳元素质量不变这一特殊情况,抓住变化中碳元素的质量关系就抓住了问题的关键.1年前查看全部
- (2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:
(2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:①Ca(HCO3)2
CaCO3+CO2↑+H2O ②2NaHCO3△ .
Na2CO3+CO2↑+H2O ),将生成的CO2全部通入足量的石灰水中产生bg CaCO3沉淀;芳芳在小明加热、冷却后的试管中又加入足量的稀盐酸,再将生成的气体全部通入足量的石灰水,结果产生cg CaCO3沉淀.那么下列关系一定正确的是( )△ .
A.a=c
B.a<b+c
C.b<c
D.a<b 挟狗看夕阳1年前1
挟狗看夕阳1年前1 -
 三万英尺的天空 共回答了16个问题
三万英尺的天空 共回答了16个问题 |采纳率93.8%解题思路:混合物中碳元素通过两条途径分别转化到碳酸钙沉淀中,其中一条途径是通过加热分解出的二氧化碳与氢氧化钙反应而转移到碳酸钙中,另一途径则是把分解后碳酸钙与碳酸钠中的碳转变为二氧化碳后再与氢氧化钙反应而转移到碳酸钙中;根据题意,两条途径所转移碳元素的质量相等,因此两个途径所得到的碳酸钙也相等;而固体混合物中碳元素的质量分数大于碳酸钙中碳元素质量分数,因此也得到最终所得碳酸钙的总质量大于原固体混合物的质量.根据①Ca(HCO3)2
△
.
CaCO3+CO2↑+H2O,碳酸氢钙中碳元素平均转移到生成的碳酸钙和二氧化碳中; ②2NaHCO3
△
.
Na2CO3+CO2↑+H2O 碳酸氢钠中的碳元素也平均转移到碳酸钠和二氧化碳中;由此可判断受热分解后所得二氧化碳气体中碳元素质量与剩余固体中碳元素质量相等;所以加热分解所得气体二氧化碳的质量等于剩余固体与盐酸反应放出二氧化碳气体的质量,可判断b=c;
根据化学变化前后元素质量不变,小明和芳芳所得碳酸钙的总和(b+c)g中碳元素全部来自于固体混合物中所有碳元素,即(b+c)g碳酸钙中所含的碳元素质量等于ag的NaHCO3和Ca(HCO3)2的固体混合物中所含的碳元素的质量;而碳酸钙中碳元素的质量分数=[12/100]×100%=12%,碳酸氢钠中碳元素质量分数=[12/84]×100%≈14%,碳酸氢钙中碳元素的质量分数=[24/162]×100%≈15%,由此可知碳酸钙中碳元素的质量分数小于NaHCO3和Ca(HCO3)2的固体混合物中碳元素的质量分数,因此当两者碳元素质量相等时,两者的质量关系为:a<b+c;
由于b=c,而NaHCO3和Ca(HCO3)2的固体混合物中碳元素的质量分数在14%~15%之间,而碳酸钙中碳元素质量分数为12%,可得a>b=c,因此a=c、a<b的判断都不正确;
故选B.点评:
本题考点: 质量守恒定律及其应用.
考点点评: 根据化学变化前后元素质量不变,解答本题时需要关注转化过程中碳元素质量不变这一特殊情况,抓住变化中碳元素的质量关系就抓住了问题的关键.1年前查看全部
- 检验水的存在在密封的袋装食品袋内,常用一小包干燥剂,一般是硅胶内加入少量的氯化钴,如果拆开后食品袋后发现硅胶全部变成红色
检验水的存在
在密封的袋装食品袋内,常用一小包干燥剂,一般是硅胶内加入少量的氯化钴,如果拆开后食品袋后发现硅胶全部变成红色,则说明:()
A、食品袋内有较多水分 B、食品袋内没有任何水分
C、食品一定变质无法使用 C、以上各种去情况都有可能
答案是? duchunlei1年前2
duchunlei1年前2 -
 1someday 共回答了16个问题
1someday 共回答了16个问题 |采纳率87.5%在化学工业(级别)中,用氯化亚钴试纸检验(空气中)水的存在.将此种试纸从干燥的瓶中取出(蓝色),放入被检空气中.如变为紫红即为有水. 无水1年前查看全部
- 现已研究成功在食品中放入一小包铁粉来代替CaO作干燥剂效果更好.用铁粉代替CaO粉末的优点是:
 一梦二十年1年前1
一梦二十年1年前1 -
 若不是因为爱着你 共回答了25个问题
若不是因为爱着你 共回答了25个问题 |采纳率84%铁粉不但可以吸收空气中的水蒸气 防止食物变潮 还能吸收空气中的氧气 生成三氧化二铁 防止食物腐烂1年前查看全部
- 淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
“请勿使用”等字样.为了提高自己的实验探究能力,淑平决定对这包干燥剂展开实验.
(1)她将这包干燥剂全部倒入一定量的水中,充分搅拌后,触摸杯壁,感觉有点热,将其过滤,得到白色沉淀物和滤液.
(2)联系到空气中成分和氧化钙的性质,她对白色沉淀物的组成提出了一下假设:
假设1:是氧化钙和碳酸钙的混合物
假设2:是氢氧化钙和碳酸钙的混合物
假设3:只有碳酸钙
假设4:只有氢氧化钙
其中假设______不合理,用化学方程式说明原因.
取少量沉淀物放入试管中,有气泡产生,由此可否定假设_________
为了得到最后结论,再取少量沉淀物放在另一支试管,加入水后震荡静置后,滴入酚酞试液,呈红色,说明只有假设________成立.
“请勿使用”是因为该干燥剂吸水后有_______性且放热
该干燥剂吸水后会变质,变质后物质可能是碳酸钙,写出氧化钙变质后生成碳酸钙的最后一步化学方程式.
 澜玉1年前1
澜玉1年前1 -
 Xelibei 共回答了19个问题
Xelibei 共回答了19个问题 |采纳率94.7%其中假设___3___不合理,用化学方程式说明原因. CaO+H20=ca(oH)2
由此可否定假设____1___
为了得到最后结论,再取少量沉淀物放在另一支试管,加入水后震荡静置后,滴入酚酞试液,呈红色,说明只有假设___4_____成立.(碱使酚酞变红)
“请勿使用”是因为该干燥剂吸水后有_腐蚀_性且放热
ca(oH)2+CO2=CaCO3 ↓+H2O
我自己做的题,不知道是不是全对.1年前查看全部
- 旺旺仙贝、雪饼大包的一包几个,仙贝、雪饼都是两个一小包的那种.
 就到附近快速1年前1
就到附近快速1年前1 -
 tongguozheng 共回答了20个问题
tongguozheng 共回答了20个问题 |采纳率90%旺旺雪饼 520g的应该是32个 16个一层 一共两层
旺旺仙贝 520g的应该是80个 20个一排 一共四排1年前查看全部
- 现有如下器材:贴有刻度的平底均匀试管一支,黄沙一小包,水一杯,待测液体一杯.请利用这些器材,根据阿基米德原理,测定液体密
现有如下器材:贴有刻度的平底均匀试管一支,黄沙一小包,水一杯,待测液体一杯.请利用这些器材,根据阿基米德原理,测定液体密度
 欧阳絮絮1年前2
欧阳絮絮1年前2 -
 蒜泥黄瓜 共回答了16个问题
蒜泥黄瓜 共回答了16个问题 |采纳率87.5%(1)制定探究方案
1、平底均匀试管中放入合适的黄沙,(目的是使其在液体中直立)
2、放入水中记下与水面相平位置的刻度L水;
3、放入代测液体中记下与代测液面相平位置的刻度L液;
4、利用浮力相等:ρ水*S*L水=ρ液*S*L液.即可求出液体密度.
(2)设计实验数据记录表格,列出代测液体密度的计算式
………L水…L液…ρ液
第1次
第2次
第3次
平均
表达式:ρ液=ρ水*L水/L液1年前查看全部
- 某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是两者的混合物,让他们通过实验探
某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是两者的混合物,让他们通过实验探究来确定。某同学探究过程如下:
(1)[提出假设]假设1:黑色粉末是炭粉;假设2:________ ;假设3:________。
(2)[设计实验方案]他对实验做了如下设想和分析:取少量黑色粉末于烧杯中,加入过量的稀硫酸(稀硫酸与氧化铜反应生成含铜化合物和一种无色液体,且溶液呈蓝色,与炭不反应),充分反应后过滤。则实验中可能出现的现象与对应结论如下表,请你完成下表。
(3)请写出稀硫酸与氧化铜反应的化学方程式:__________________。  zqdldavid1年前1
zqdldavid1年前1 -
 大师傅感13 共回答了18个问题
大师傅感13 共回答了18个问题 |采纳率88.9%1年前查看全部
- 一小包纸巾的长,宽,高分别是7厘米,5厘米,3厘米.用一大张塑料将10包纸巾包起来至少需要多大面积 方程解和
一小包纸巾的长,宽,高分别是7厘米,5厘米,3厘米.用一大张塑料将10包纸巾包起来至少需要多大面积 方程解和
单位1是?和关系式 道格拉斯bear1年前1
道格拉斯bear1年前1 -
 寄托者 共回答了17个问题
寄托者 共回答了17个问题 |采纳率94.1%1、如果纸巾堆放中存在空隙,必然不是最少面积,因为体积缩小,面积就可相应缩小.2、堆放后的最大面积就是各包纸巾的面积和,而最小面积,就是依靠相互合并消除面积,因此可以把长方纸巾的最大一面相互依靠,就能消除最多面积从而的到最少面积.3、最大面积是7*5,10包堆放后高为3*10=30,所以最小面积可依靠7*5*30的长方体求得,=(35+210+150)*2=790.1年前查看全部
- 商场搞促销.买二盒2升装的牛奶送一小包350毫升的牛奶,小丁丁学校买10盒牛奶,他们一共可得到多少牛奶?
 sandy789_20001年前1
sandy789_20001年前1 -
 hnlyzzh 共回答了19个问题
hnlyzzh 共回答了19个问题 |采纳率84.2%10盒送5小包,10盒+5包=151年前查看全部
- 包装袋内常放入一小包生石灰干燥剂,试回答下列问题:
包装袋内常放入一小包生石灰干燥剂,试回答下列问题:
这包干燥剂吸水的过程中,发生反应的化学方程式是:__________________________ __;此干燥剂露置在空气中最终会变成 . 魏晨的YY女王1年前2
魏晨的YY女王1年前2 -
 xprebirth 共回答了18个问题
xprebirth 共回答了18个问题 |采纳率88.9%CaO+H2O=Ca(OH)2
CaCO3
反应是Ca(OH)2+CO2=CaCO3↓+H2O1年前查看全部
- 怎样 用天平称量一小包食盐的质量
 pennyaemi1年前1
pennyaemi1年前1 -
 禾水2007 共回答了19个问题
禾水2007 共回答了19个问题 |采纳率94.7%一小包达到天平的感量了吗?如果到 了,可以直接测量.
如果不到,可以用天平称出10袋的总质量,然后用总质量除以10就是一袋小包食盐的质量.1年前查看全部
- (2009•郑州)晓松在参观一个容积为5×103m3粮仓时,想知道这粮仓能装多少质量的稻谷.于是他取一小包稻谷作样品,进
 (2009•郑州)晓松在参观一个容积为5×103m3粮仓时,想知道这粮仓能装多少质量的稻谷.于是他取一小包稻谷作样品,进行了以下实验:
(2009•郑州)晓松在参观一个容积为5×103m3粮仓时,想知道这粮仓能装多少质量的稻谷.于是他取一小包稻谷作样品,进行了以下实验:
(1)调节天平平衡时,发现天平的指针偏向分度标尺的右侧.此时,应将平衡螺母向______调(选填“左”或“右”),直至天平平衡.
(2)取适量稻谷倒入左盘,在右盘中加减砝码,并移动称量标尺上的______,使天平重新平衡.所用的砝码和游码的位置如如图所示,则稻谷质量为______g.将这些稻谷倒入量筒中压实,测出它的体积为40cm3.
(3)稻谷的密度为______g/cm3,这个粮仓大约能装______kg的稻谷. rbz431年前1
rbz431年前1 -
 qq过河 共回答了24个问题
qq过河 共回答了24个问题 |采纳率83.3%(1)调节天平平衡时,发现天平的指针偏向分度标尺的右侧,应向左调节平衡螺母;
故答案为:左.
(2)用天平称量物体质量时,先由大到小加砝码,最后靠拨动游码使横梁平衡;物体质量m=20g+20g+5g+3g=48g;
故答案为:游码、48.
(3)稻谷样品的体积V=40cm3,稻谷的密度ρ=[m/V]=
48g
40cm3=1.2g/cm3=1.2×103kg/m3,
粮仓中稻谷的总质量M=ρV总=1.2×103kg/m3×5×103m3=6×106kg.
故答案为:1.2、6×106.1年前查看全部
- 食品的包装袋内常放入一小包干燥剂,其主要成分为生石灰,干燥袋上都有“请勿食用”字样.
食品的包装袋内常放入一小包干燥剂,其主要成分为生石灰,干燥袋上都有“请勿食用”字样.
(1)“请勿食用”是因为干燥剂食用后,对人体有______ 作用.
(2)写出干燥剂的主要成分吸水过程中发生反应的化学方程式______. polaris4255281年前1
polaris4255281年前1 -
 流宇星辰 共回答了16个问题
流宇星辰 共回答了16个问题 |采纳率93.8%解题思路:(1)根据题意可知该干燥剂为生石灰,能与水反应生成氢氧化钙,氢氧化钙具有腐蚀性,据此进行分析解答即可.
(2)氧化钙与水反应生成氢氧化钙,写出反应的化学方程式即可.(1)根据题意,该干燥剂的成分为生石灰,可与水反应生成氢氧化钙,同时放出大量的热,氢氧化钙具有腐蚀性,故不能食用.
(2)氧化钙与水反应生成氢氧化钙,反应的化学方程式为:CaO+H2O=Ca(OH)2.
故答案为:(1)腐蚀;(2)CaO+H2O=Ca(OH)2.点评:
本题考点: 酸碱盐的应用;书写化学方程式、文字表达式、电离方程式.
考点点评: 生石灰是常用的干燥剂,也是化学考查的热点,掌握生石灰的性质、氢氧化钙的性质并能灵活运用是正确解答本题的关键.1年前查看全部
- (2006•石家庄)为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的
(2006•石家庄)为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的是( )
A.炭粉
B.铁粉
C.氯化钙
D.生石灰 lzlily1年前1
lzlily1年前1 -
 雅典神 共回答了20个问题
雅典神 共回答了20个问题 |采纳率80%解题思路:能用作食品抗氧化剂的物质需具备易和氧气反应的性质.A、碳粉需在点燃的条件下与氧气反应,不能用作食品抗氧化剂,故A错误;
B、铁粉在常温下就可以与氧气反应,可以用作食品抗氧化剂,故B正确;
C、氯化钙与氧气不反应,不能用作食品抗氧化剂,故C错误;
D、生石灰与氧气不反应,不能用作食品抗氧化剂,故D错误,
故选B.点评:
本题考点: 金属的化学性质.
考点点评: 此题以实际应用的形式考查了金属铁与氧气的反应,完成此题,可以依据铁生锈的条件作为解题的依据.1年前查看全部
- 一道关于化学题某食品公司在“XX饼干”的包装袋内放入一小包干燥剂,它的主要成分是生石灰.(1)干燥剂包装袋上标明“请勿食
一道关于化学题
某食品公司在“XX饼干”的包装袋内放入一小包干燥剂,它的主要成分是生石灰.
(1)干燥剂包装袋上标明“请勿食用”,其原因是——------------.
(2)若误食入口,应立即用-----------冲洗. bh1121wang1年前2
bh1121wang1年前2 -
 止心浊 共回答了18个问题
止心浊 共回答了18个问题 |采纳率94.4%(1)生石灰有腐蚀性
(2)醋1年前查看全部
- “××雪饼”的包装袋内有一小包干燥剂,干燥剂袋上的说明如图所示,这些说明表达的内容不包括( )
 “××雪饼”的包装袋内有一小包干燥剂,干燥剂袋上的说明如图所示,这些说明表达的内容不包括( )
“××雪饼”的包装袋内有一小包干燥剂,干燥剂袋上的说明如图所示,这些说明表达的内容不包括( )
A.物质的组成
B.物质的性质
C.物质的用途
D.物质的制取 chhyjb1年前1
chhyjb1年前1 -
 凡尘清影 共回答了14个问题
凡尘清影 共回答了14个问题 |采纳率78.6%解题思路:根据“××雪饼”包装袋内干燥剂袋上的说明书,生石灰的化学式为CaO,能作干燥剂,据此进行分析判断.A、由“××雪饼”包装袋内干燥剂袋上的说明书,生石灰的化学式为CaO,由此可确定生石灰的组成,故选项错误.
B、由“××雪饼”包装袋内干燥剂袋上的说明书,生石灰能用作干燥剂,说明生石灰能与水反应或具有吸水性,表达的内容包括的性质,故选项错误.
C、由“××雪饼”包装袋内干燥剂袋上的说明书,生石灰能用作干燥剂,表达的内容包括生石灰的用途,故选项错误.
D、由“××雪饼”包装袋内干燥剂袋上的说明书,表达的内容不包括生石灰的制取,故选项正确.
故选:D.点评:
本题考点: 标签上标示的物质成分及其含量;化学性质与物理性质的差别及应用.
考点点评: 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的含义、物质的性质与用途等进行分析问题、解决问题的能力.1年前查看全部
- (2009•宝鸡)某些食品包装袋内有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂
(2009•宝鸡)某些食品包装袋内有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”.下列物质属于“双吸剂”的是( )
A.铁粉
B.炭粉
C.氯化钙
D.生石灰 yy781年前1
yy781年前1 -
 我的小媳妇捏 共回答了9个问题
我的小媳妇捏 共回答了9个问题 |采纳率66.7%铁能和水、氧气反应生成铁锈,可以用作“双吸剂”;氯化钙和氧化钙只能吸收水,不能和氧气反应,不能用作“双吸剂”.
故选:A.1年前查看全部
- 1.一小包纸巾的长、宽、高分别是7厘米、5厘米、3厘米.如果,用一大张塑料纸将这10包纸巾包起来,至少需要多大面积的塑料
1.一小包纸巾的长、宽、高分别是7厘米、5厘米、3厘米.如果,用一大张塑料纸将这10包纸巾包起来,至少需要多大面积的塑料纸?
2.把一个棱长为20厘米的正方体分成2个相同的长方体,每个长方体的表面积是多少?
3.小明有15张邮票,是小芳邮票的4分之3.
(1)小芳有多少张邮票?
(2)小丽的邮票张数是小芳的5分之3,小丽有多少张邮票?
4.东方小学五(2)班每周的课程表上共有30节课,其中语文课占5分之1,数学课占6分之1,音乐课占15分之1,体育课占10分之1,语文课、数学课、音乐课、体育课每周分别有多少节?
长是5厘米,宽是7厘米,高是3厘米.那个后面是:如图 heren051年前1
heren051年前1 -
 帅帅西 共回答了26个问题
帅帅西 共回答了26个问题 |采纳率88.5%①70*5*3或50*7*3或30*7*5
②10*20*20
③①15除以4分之3
②20*5分之3
④语30*5分之1
数30*6分之1
音30*15分之1
体30*10分之1
答案自己算哦1年前查看全部
- 小明要测量一小包盐的质量.首先,他将托盘天平放在水平台面上,游码移至“0”刻度线处;然后,他将盐从纸包中倒入左盘,在右盘
小明要测量一小包盐的质量.首先,他将托盘天平放在水平台面上,游码移至“0”刻度线处;然后,他将盐从纸包中倒入左盘,在右盘中加砝码,直至横梁平衡;最后,他读出测量数值.小明在测量过程中有两处明显的错误,请你给他指出来.
 xczvjsdfoiuasiod1年前2
xczvjsdfoiuasiod1年前2 -
 ee谈人生 共回答了17个问题
ee谈人生 共回答了17个问题 |采纳率100%解题思路:从天平的正确使用和注意事项进行解答:
(1)天平的正确使用:
把天平放在水平台上,游码移到标尺左端的零刻度;
调节天平的平衡螺母使天平的横梁平衡;
物体放在天平的左盘,砝码放在天平的右盘,使天平的横梁重新平衡;
物体的质量等于砝码的质量加游码对应的刻度值.
(2)天平使用的注意事项:
不要超过天平的测量范围;
不要把化学药品和潮湿的物体直接放在天平盘上;
要用镊子夹取砝码,不能用手拿砝码;
砝码要及时放回砝码盒,要轻拿轻放.小明在测量过程中有两处明显的错误:
①把天平放在水平台上,游码移到标尺左端的零刻度;要调节天平的平衡螺母使天平的横梁平衡;而小明没有调节天平的平衡螺母使天平的横梁平衡,就测量了;
②化学药品直接放在托盘中,化学药品会腐蚀托盘.所以不允许把化学药品直接放在托盘中.点评:
本题考点: 天平的使用.
考点点评: 此题主要考查的是学生对天平的基本调节、读数的理解和掌握,基础性题目.1年前查看全部
- (2004•珠海)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种的混合
(2004•珠海)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,这种黑色粉末可能是氧化铜、炭粉或者是这两种的混合物,让他们通过实验探究来确定.某同学探究过程如下:
(1)提出假设:假设1:黑色粉末是炭粉;实验中可能出现的现象 结论 ① 假设1成立 ② 假设2成立 ③ 假设3成立
假设2:______;
假设3:______.
(2)设计实验方案:他对实验做了如下设想和分析:
取少量黑色粉末于烧杯中,并加入过量的稀硫酸.则实验中可能出现的现象与对应结论如上表,请你完成上表.
(3)进行实验:通过实验及分析,确定该黑色物质为炭粉和氧化铜的混合物.
(4)拓展:为了进一步探究炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验:将此黑色粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置.请你回答:
①烧杯中______(填“有”或“无”)不溶物;
②若静置后溶液呈无色,则该溶液中溶质是______(写化学式);
③若静置后溶液呈蓝色,该反应的化学方程式为______. Sinter_Lee1年前1
Sinter_Lee1年前1 -
 efengjoe 共回答了21个问题
efengjoe 共回答了21个问题 |采纳率85.7%解题思路:根据炭粉、氧化铜、硫酸铜的物理化学性质作答.硫酸铜溶液显蓝色,炭粉、氧化铜均为黑色,木炭有还原性,可以还原氧化铜.(1)根据题意,可以做出三种假设,即第一种可能是只有炭粉,第二中可能是只有氧化铜,第三种可能是氧化铜与炭粉的混合物;
故答案为:黑色粉末是氧化铜,黑色粉末是氧化铜和炭粉的混合物
(2)炭粉不会与稀硫酸反应,氧化铜会与稀硫酸反应生成硫酸铜溶液,硫酸铜溶液显蓝色,故答案为:
实验中可能出现的现象 结论
①溶液为无色,有黑色不溶物 假设1成立
②溶液为蓝色 假设2成立
③溶液为蓝色,有黑色不溶物 假设3成立(4)炭粉与氧化铜在隔绝空气加热的条件下会发生反应即C+2CuO═2Cu+CO2↑,题意中有告诉我们,炭粉完全反应,所以最终的固体有两种可能,一种可能是只有铜,另一种可能是铜和氧化铜的混合物,
故答案为:有;H2SO4CuO+H2SO4═CuSO4+H2O.点评:
本题考点: 缺失标签的药品成分的探究;猜想与事实验证;酸的化学性质;碳的化学性质;反应现象和本质的联系;书写化学方程式、文字表达式、电离方程式.
考点点评: 此题属于混合物的推断题,做此类题的关键是理清思路.1年前查看全部
- (2008•崇明县二模)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,某同学通过实验及分析,确定该黑色物质为炭粉
(2008•崇明县二模)某校进行化学实验考查时,教师给了同学们一小包黑色粉末,某同学通过实验及分析,确定该黑色物质为炭粉和氧化铜的混合物.为了进一步探究炭粉和氧化铜的性质,他又利用这种混合物补充做了如下实验:将此黑色粉末隔绝空气加热(若碳完全反应),待冷却到室温后,取剩余固体于烧杯中,再加入过量稀硫酸,反应完全后,静置.请你回答:
(1)烧杯中 ______(填“有”或“无”)不溶物;
(2)若静置后溶液呈无色,则该溶液中溶质是 ______(写化学式);
(3)若静置后溶液呈蓝色,该反应的化学方程式为:______. 留下淡淡1年前1
留下淡淡1年前1 -
 过马路的蛋 共回答了26个问题
过马路的蛋 共回答了26个问题 |采纳率100%解题思路:炭和氧化铜在加热的条件下反应生成铜和二氧化碳,在本题中已知炭完全反应,氧化铜则可能有剩余,向剩余固体中加入过量稀硫酸后,其中的铜与稀硫酸不反应,所以烧杯中一定有不溶物,如果剩余固体中有氧化铜,氧化铜会与稀硫酸反应生成蓝色硫酸铜溶液.在解答这种探究题的时候,要对可能出现的结果根据现象逐一分析.(1)因为炭和氧化铜在加热的条件下反应生成铜和二氧化碳,铜和稀硫酸不反应,故不溶于稀硫酸,所以烧杯中一定有不溶物铜.答案:有
(2)若静置后溶液呈无色,说明没有生成硫酸铜,那么溶液中的溶质只有H2SO4,答案:H2SO4
(3)若静置后溶液呈蓝色,说明有氧化铜和硫酸反应生成了硫酸铜,答案:CuO+H2SO4═CuSO4+H2O点评:
本题考点: 实验探究物质的性质或变化规律.
考点点评: 对于实验结果的可能性要全面考虑,提高对实验结果的分析能力.1年前查看全部
- (2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:
(2006•扬州)有一小包质量为ag的NaHCO3和Ca(HCO3)2的固体混合物,小明将该包固体充分加热(仅发生反应:①Ca(HCO3)2
CaCO3+CO2↑+H2O ②2NaHCO3△ .
Na2CO3+CO2↑+H2O ),将生成的CO2全部通入足量的石灰水中产生bg CaCO3沉淀;芳芳在小明加热、冷却后的试管中又加入足量的稀盐酸,再将生成的气体全部通入足量的石灰水,结果产生cg CaCO3沉淀.那么下列关系一定正确的是( )△ .
A. a=c
B. a<b+c
C. b<c
D. a<b 夜半低语时1年前2
夜半低语时1年前2 -
 穿拖鞋跑大街 共回答了26个问题
穿拖鞋跑大街 共回答了26个问题 |采纳率80.8%解题思路:混合物中碳元素通过两条途径分别转化到碳酸钙沉淀中,其中一条途径是通过加热分解出的二氧化碳与氢氧化钙反应而转移到碳酸钙中,另一途径则是把分解后碳酸钙与碳酸钠中的碳转变为二氧化碳后再与氢氧化钙反应而转移到碳酸钙中;根据题意,两条途径所转移碳元素的质量相等,因此两个途径所得到的碳酸钙也相等;而固体混合物中碳元素的质量分数大于碳酸钙中碳元素质量分数,因此也得到最终所得碳酸钙的总质量大于原固体混合物的质量.根据①Ca(HCO3)2 △. CaCO3+CO2↑+H2O,碳酸氢钙中碳元素平均转移到生成的碳酸钙和二氧化碳中; ②2NaHCO3△. Na2CO3+CO2↑+H2O 碳酸氢钠中的碳元素也...
点评:
本题考点: 质量守恒定律及其应用.
考点点评: 根据化学变化前后元素质量不变,解答本题时需要关注转化过程中碳元素质量不变这一特殊情况,抓住变化中碳元素的质量关系就抓住了问题的关键.1年前查看全部
- (2005•南通)食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”,下列物质可以作“双吸剂
(2005•南通)食品包装袋内常有一小包物质,用来吸收氧气和水分,以防止食品腐败,常称“双吸剂”,下列物质可以作“双吸剂”的是( )
A.炭粉
B.铁粉
C.氯化钙
D.生石灰 小猪妮妮1年前1
小猪妮妮1年前1 -
 kcufer 共回答了13个问题
kcufer 共回答了13个问题 |采纳率84.6%解题思路:可以根据物质的性质方面进行分析、判断,从而得出正确的结论.在通常情况下铁能和空气中的氧气和水反应生成铁锈,从而除去氧气和水蒸气.可以用作双吸剂.观察选项,故选B.
点评:
本题考点: 食品干燥剂、保鲜剂和真空包装的成分探究.
考点点评: 解答本题的关键是要充分理解物质的性质,只有掌握了物质的性质,才能确定物质的用途.1年前查看全部
- (1)月饼包装袋中有一包还原铁粉,是“双吸剂”,吸收的物质是______;“旺旺”雪饼包装袋中有一小包干燥剂,主要成分是
(1)月饼包装袋中有一包还原铁粉,是“双吸剂”,吸收的物质是______;“旺旺”雪饼包装袋中有一小包干燥剂,主要成分是生石灰,吸收水的原因(用化学方程式表示)______.

(2)用“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,则右图所示的化学反应方程式为:2H2O2
”表示氧原子,则右图所示的化学反应方程式为:2H2O2
2H2O+O2↑催化剂 .2H2O2.根据右图,你能得出的结论是(写一条):______.
2H2O+O2↑催化剂 . 蓝天宝石11年前1
蓝天宝石11年前1 -
 岸岸M 共回答了21个问题
岸岸M 共回答了21个问题 |采纳率85.7%解题思路:(1)可从月饼变质的条件,以及铁生锈的条件来分析,生石灰具有吸水性,常用作食品干燥剂,
(2)由化学反应的微观模拟示意图可知:化学变化前后原子的种类和个数都不发生变化.(1)物质在有氧气和水存在的条件下发生反应而变质,防腐剂的作用是除去氧气和水,铁粉恰好可以与氧气和水发生化学反应而生锈,防止月饼因氧化而变质并且能吸水防潮;生石灰具有吸水性,常用作食品干燥剂,化学方程...
点评:
本题考点: 食品干燥剂、保鲜剂和真空包装的成分探究;生石灰的性质与用途;微粒观点及模型图的应用;质量守恒定律及其应用.
考点点评: 本题考查了食品保鲜剂的研究,完成此题,可以依据已有的知识进行;通过给出微粒的模型,考查学生的观察能力和对基本概念的理解与运用能力;通过分子、原子、离子、元素与物质之间的关系处理问题.1年前查看全部
- 一小包糖分给几个小朋友,如果每人分3块,则余3块;如果每人分5块,则少7块,请问:有多少小朋友?
 玫瑰xx1年前1
玫瑰xx1年前1 -
 yac420 共回答了21个问题
yac420 共回答了21个问题 |采纳率85.7%设小朋友为X
糖为Y
Y=3X+3
Y=5X-1
解得X=2
所以有2个小朋友1年前查看全部
- 发酵现象 为什么了?发酵现象 在一杯温开水中加入一大勺糖和一小包酵母,进行搅拌.将这个杯子中的液体倒入透明的玻璃瓶或矿泉
发酵现象 为什么了?
发酵现象
在一杯温开水中加入一大勺糖和一小包酵母,进行搅拌.将这个杯子中的液体倒入透明的玻璃瓶或矿泉水瓶内,再往瓶内加一些温开水.将一个小气球挤瘪后套在瓶口.将瓶子放在教室内窗台上,每天观察瓶中的情况,看看瓶中的液体会不会冒出气泡,气球会不会胀大.
你所观察到的现象就是发酵. zztshy1年前3
zztshy1年前3 -
 andyzhang209 共回答了14个问题
andyzhang209 共回答了14个问题 |采纳率78.6%酵母菌利用加入的糖进行增殖.酵母菌以糖分为养料,进行有氧呼吸,吸收6mol氧气,放出6mol水,6mol二氧化碳,现象是冒出气泡,瓶子膨胀;氧气耗尽后,进行无氧呼吸,同样可以释放二氧化碳,使瓶子膨胀.1年前查看全部
- 为了防止食品受潮,可在包装袋种放一小包生石灰做干燥剂,生石灰起干燥作用时,发生的反应方程式为?
 许多橙子1年前2
许多橙子1年前2 -
 脸角的眼泪还未干 共回答了24个问题
脸角的眼泪还未干 共回答了24个问题 |采纳率91.7%CaO+H2O=Ca(OH)21年前查看全部
- 李阿姨织了180双袜子,分装成2大盒与6小包.已知1大盒可比一小包多装10双袜子.每大盒装多少双?(算术解)
 pahnysb1年前1
pahnysb1年前1 -
 哈克龙 共回答了11个问题
哈克龙 共回答了11个问题 |采纳率81.8%设一小包装x双,一大盒装x+10双 则:
2(x+10)+6x=180
解得:x=20 所以每大盒装20+10=30双1年前查看全部
- 一小包速溶咖啡,用285可开水可泡成浓度为5%的饮料,设这包速溶咖啡有x克,则可列出方程________________
一小包速溶咖啡,用285可开水可泡成浓度为5%的饮料,设这包速溶咖啡有x克,则可列出方程_________________
 8a4538cc9d096fbc1年前1
8a4538cc9d096fbc1年前1 -
 hyper2008 共回答了17个问题
hyper2008 共回答了17个问题 |采纳率100%5%×(285+x)=x1年前查看全部
- 猫医生给兔子一包70克的药粉,告诉他每天吃5克,不多也不少,如果分成5克每天一小包,兔妈妈想用天平分成5
猫医生给兔子一包70克的药粉,告诉他每天吃5克,不多也不少,如果分成5克每天一小包,兔妈妈想用天平分成5
克1小包的药粉.可是只有20可得砝码.怎么分出5克的药粉 akong1131年前1
akong1131年前1 -
 andison0206 共回答了16个问题
andison0206 共回答了16个问题 |采纳率93.8%用20克分走三次.一共60克~70剩下10克.用天平对半分分成5克和5克.然后拿5克作为砝码、一份份分呗1年前查看全部
- 生活中许多富脂糕点的包装盒内都装有一小包黑色的还原铁粉 长时间放置的糕点 包装盒内的还原铁粉往往
生活中许多富脂糕点的包装盒内都装有一小包黑色的还原铁粉 长时间放置的糕点 包装盒内的还原铁粉往往
变成红棕色(主要成分是Fe2O3)下列说法中正确的是
A 还原铁粉变成红棕色 发生了氧化反应
B 富脂食品长时间放置易被氧化
C Fe2O3是还原产物
D 如果放入Fe2(SO4)3也可以起到同样的作用 dalynana131年前1
dalynana131年前1 -
 linlilhs00 共回答了14个问题
linlilhs00 共回答了14个问题 |采纳率85.7%AB
还原铁粉是作为脱氧剂使用的.因为富含脂肪的食品容易氧化生成过氧化物,导致食物变质,所以在包装中加入脱氧剂,减少食品存储环境中的氧含量.脱氧剂脱氧是靠还原铁粉的氧化反应消耗包装中的氧气而起作用.1年前查看全部
- 8.有一小包质量为ag的NaHC03和Ca(HC03)2的固体混合物,小明将该包固体充分加热(仅发生反应:①Ca(HC0
8.有一小包质量为ag的NaHC03和Ca(HC03)2的固体混合物,小明将该包固体充分加热(仅发生反应:①Ca(HC03)2 △ CaC03+C02↑+H20②2NaHC03 △ Na2C03+C02↑+H2O),将生成的C02全部通入足量的石灰水中产生bgCaC03沉淀;芳芳在小明加热、冷却后的试管中又加入足量的稀盐酸,再将生成的气体全部通入足量的石灰水,结果产生cgCaC03沉淀.那么下列关系一定正确的是( )
A.a=c B.a 风雩1年前1
风雩1年前1 -
 艾草凄凄 共回答了15个问题
艾草凄凄 共回答了15个问题 |采纳率100%根据碳元素的转移来进行比较和简单计算,答案选择B
1)2NaHCO3==Na2CO3+H2O+CO2;CO2+Ca(OH)2==CaCO3+H2O
168 106 44 44 100
Ca(HCO3)2==CaCO3+H2O+CO2;CO2+Ca(OH)2==CaCO3+H2O
162 100 44 44 100
(168+162)大于(100+100),所以有a大于b
2)Na2CO3+2HCl==2NaCl+H2O+CO2;CO2+Ca(OH)2==CaCO3+H2O
106 44 44 100
CaCO3+2HCl==CaCl2+H2O+CO2;CO2+Ca(OH)2==CaCO3+H2O
100 44 44 100
根据C元素的转移,可知前后两次生成CO2的质量相同,则两次生成CaCO3沉淀的质量也相同,即b==C;(168+162)小于2*(100+100),答案选择B
芳芳往试管中加入稀盐酸,就是将盐酸加入到碳酸钠和碳酸钙的混合物中,充分反应生成二氧化碳1年前查看全部
- 食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,其上面的部分文字见图,请仔细阅读,回答问题:
食品公司通常在“XX雪饼”的包装袋内放入一小包干燥剂,其上面的部分文字见图,请仔细阅读,回答问题:

(1)写出这包干燥剂吸收水分的反应的化学方程式.
(2)“请勿食用”是因为干燥剂吸水后具有什么样的性质? 戏王之王KEN1年前1
戏王之王KEN1年前1 -
 xinzimin 共回答了23个问题
xinzimin 共回答了23个问题 |采纳率82.6%解题思路:根据标签内容可知此干燥剂为生石灰,可与水反应生成氢氧化钙,氢氧化钙具有腐蚀性.(1)这包干燥剂吸收水分是氧化钙和水反应生成氢氧化钙,该反应的方程式为:CaO+H2O=Ca(OH)2;
(2)因为干燥剂的主要成份是生石灰,吸收水分后生成氢氧化钙,氢氧化钙属于强碱,对皮肤、织物、器皿等物质有腐蚀作用.
故答案为:(1)CaO+H2O=Ca(OH)2;
(2)氢氧化钙属于强碱,对皮肤、织物、器皿等物质有腐蚀作用.点评:
本题考点: 生石灰的性质与用途;常见碱的特性和用途;标签上标示的物质成分及其含量.
考点点评: 本题主要考查学生对氧化钙和氢氧化钙的性质的认识,了解一些常见的干燥剂.注重基础知识的考查.1年前查看全部
- 为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的是( )
为延长食品保质期,在月饼、蛋糕等食品包装袋内常放有一小包食品抗氧化剂,下列物质可以用作食品抗氧化剂的是( )
A. 炭粉
B. 铁粉
C. 氯化钙
D. 生石灰 彷煌1年前1
彷煌1年前1 -
 小妖祖儿 共回答了21个问题
小妖祖儿 共回答了21个问题 |采纳率90.5%解题思路:能用作食品抗氧化剂的物质需具备易和氧气反应的性质.A、碳粉需在点燃的条件下与氧气反应,不能用作食品抗氧化剂,故A错误;
B、铁粉在常温下就可以与氧气反应,可以用作食品抗氧化剂,故B正确;
C、氯化钙与氧气不反应,不能用作食品抗氧化剂,故C错误;
D、生石灰与氧气不反应,不能用作食品抗氧化剂,故D错误,
故选B.点评:
本题考点: 金属的化学性质.
考点点评: 此题以实际应用的形式考查了金属铁与氧气的反应,完成此题,可以依据铁生锈的条件作为解题的依据.1年前查看全部
- 淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
淑平同学在我市某食品厂生产的盒装饼干中,发现盒内有一小包东西,其上标有“干燥剂”主要成分生石灰,
“请勿使用”等字样.为了提高自己的实验探究能力,淑平决定对这包干燥剂展开实验.
(1)她将这包干燥剂全部倒入一定量的水中,充分搅拌后,触摸杯壁,感觉有点热,将其过滤,得到白色沉淀物和滤液.
(2)联系到空气中成分和氧化钙的性质,她对白色沉淀物的组成提出了一下假设:
假设1:是氧化钙和碳酸钙的混合物
假设2:是氢氧化钙和碳酸钙的混合物
假设3:只有碳酸钙
假设4:只有氢氧化钙
其中假设______不合理,用化学方程式说明原因.
为什么是假设一不正确呢?解析一下
 睫毛上的钻石1年前1
睫毛上的钻石1年前1 -
 chriswu1979 共回答了17个问题
chriswu1979 共回答了17个问题 |采纳率88.2%是氯化钙和其他混合物1年前查看全部
大家在问
- 1名人名言的意思 我们可以由读书搜集知识,但必须利用思考把糠和麦子分开
- 2仔细品读下列句子,然后选择正确的词语填在横线处。
- 3论友谊 西塞罗 答案检举 ---西塞罗文章:我以为,友谊的基础是美德。别人相信你有美德,所以才与你建立友谊。你若放弃了美
- 4作文 :写给2021年自己的一封信,或写给2049年祖国的一封信
- 5请问下,我像用气球弄成一个桃心形状的,我的意思是:把很多气球绑在一起,弄成一个桃心状的.
- 6(2010•番禺区一模)翔翔在家探究鸡蛋受到的浮力大小与哪些因素有关,如图7所示.请仔细观察图示并回答下列问题:
- 710点15分—8点30分=
- 8雨给大地万物带来了勃勃生机,雨让他们勇敢地笑了,于是大地有了希望。面对春雨这种润物无声的奉献精神,文学小组的同学纷纷发言
- 9'非P'形式的命题是什么?P:6是12或24的约数
- 10已知一个数的七分之六是十分之九,这个数的七分之一是多少
- 11Go a_____ the road,and you'll find the bookshop.
- 12碘盐溶入水中,加入KI的淀粉溶液,再加入酸性试剂 为什么会变蓝色?
- 13The boy in a white T-shirt is my friend(对The boy in a white
- 14如果我存一万块钱一年的定期在银行,利率是3.25,那么一年后我一共可以拿到多少利息?怎么算?
- 15解方程:根号2X-4X=4根号2如题 谢谢了


