若制取18.8g硝酸铜,至少需要消耗10%的稀硝酸多少克?
 hexiansheng2022-10-04 11:39:543条回答
hexiansheng2022-10-04 11:39:543条回答
已提交,审核后显示!提交回复
共3条回复
 tomcatfire 共回答了18个问题
tomcatfire 共回答了18个问题 |采纳率83.3%- 3Cu+8HNO3=3Cu(NO3)2+2NO+4H2O
----------504--------564
-----------X*10%----18.8
X=168克
至少需要消耗10%的稀硝酸168克 - 1年前
 will123456 共回答了1个问题
will123456 共回答了1个问题 |采纳率- 不清楚
- 1年前
 2cqkg 共回答了1个问题
2cqkg 共回答了1个问题 |采纳率- 这么稀,反应么……
- 1年前
相关推荐
- 实验室用下图装置制取少量溴苯,试填写下列空白。
实验室用下图装置制取少量溴苯,试填写下列空白。
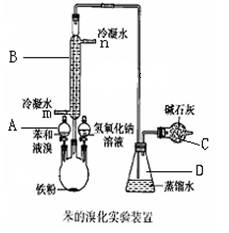
(1).写出仪器A的名称 ;B的名称 ;
(2).请你写出实验室制取溴苯的化学方程式 ___ ;
(3).长导管的下口为什么不插入锥形瓶的液面下
(4).反应完毕后,向烧瓶A中滴加NaOH 溶液的作用是:
(5).冷凝水的进水口是(填m或n) ,,图中干燥管C的作用是 爱情的契约1年前1
爱情的契约1年前1 -
 wwwindy 共回答了8个问题
wwwindy 共回答了8个问题 |采纳率87.5%1年前查看全部
- 氯酸钾能否代替过氧化氢制取氧气?主要理由是什么?
 bbswang1年前2
bbswang1年前2 -
 忘了忘了你 共回答了15个问题
忘了忘了你 共回答了15个问题 |采纳率86.7%不能
理由:过氧化氢制氧用的是固液反应不加热装置,前者要用固固反应加热装置才能制氧1年前查看全部
- 有下列几种反应类型:①消去②加聚③水解④加成⑤还原⑥氧化,用丙醛制取1,2一丙二醇,按正确的合成路线依次发生的反应所属类
有下列几种反应类型:①消去②加聚③水解④加成⑤还原⑥氧化,用丙醛制取1,2一丙二醇,按正确的合成路线依次发生的反应所属类型应是( ) A.⑤①④③ B.⑥④③① C.①②③⑤ D.⑤③④①  异维之心1年前1
异维之心1年前1 -
 127fl 共回答了14个问题
127fl 共回答了14个问题 |采纳率85.7%用丙醛制取1,2一丙二醇,官能团发生变化,官能团数目变化,1,2一丙二醇有2个羟基,且处于相邻的碳原子上,
所以应先制备丙烯,先加氢还原为丙醇,在浓硫酸加热条件下发生消去反应,得丙烯;
再与溴加成,制得1,2一二溴丙烷,再在碱的水溶液条件下水解,得1,2一丙二醇.
故合成路线依次发生的反应所属类型顺序为⑤①④③,
故选A.1年前查看全部
- 如图所示的装置是实验室常用来制取和收集气体的装置.
如图所示的装置是实验室常用来制取和收集气体的装置.

(1)写出仪器a和b的名称:a______,b______;如果选择实验装置A和F组合,用氯酸钾和二氧化锰来制取氧气,反应的方程式为2KClO3
2KCl+3O2↑MnO2 .△ 2KClO3,加热时试管口为什么应略向下倾斜______.
2KCl+3O2↑MnO2 .△
(2)某同学打算用大理石和稀盐酸制取二氧化碳,他选择了装置B和E连接,当稀盐酸和大理石都加入装置B一段时间后,他用燃着的火柴在E的瓶口试验,火柴仍然燃烧,你认为原因可能是______.
(3)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应生成氢氧化钠和氧气.用该反应来制取一瓶氧气,应选择的实验装置是______(填字母编号).反应方程式为______. DLSS0011年前1
DLSS0011年前1 -
 北极的星星草 共回答了28个问题
北极的星星草 共回答了28个问题 |采纳率92.9%解题思路:(1)据常用仪器回答;并据氯酸钾分解的反应原理书写方程式,加热时试管口下倾是为了防止冷凝水倒流引起试管炸裂;
(2)根据装置特点分析原因;
(3)据反应物状态和反应条件选择发生装置,据气体的密度和性质选择收集装置,据反应原理书写方程式.(1)标号仪器分别是酒精灯和集气瓶;用氯酸钾和二氧化锰来制取氧气,反应的方程式为2KClO3
MnO2
.
△2KCl+3O2↑;加热时试管口下倾是为了防止冷凝水倒流引起试管炸裂;
(2)观察装置可知:B装置中的长颈漏斗下端未伸入液面以下,会导致生成的二氧化碳从长颈漏斗逸出;
(3)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应生成氢氧化钠和氧气,该反应不需加热,属于固液常温型,故选发生装置C,氧气密度比空气大且不易溶于水,可用向上排空气法或排水法收集,根据反应原理,方程式是:2Na2O2+2H2O=4NaOH+O2↑;
故答案为:
(1)酒精灯;集气瓶;2KClO3
MnO2
.
△2KCl+3O2↑;防止冷凝水倒流使试管破裂;
(2)CO2已经从长颈漏斗上口逸出到空气中;
(3)C和E(或C和F);2Na2O2+2H2O=4NaOH+O2↑.点评:
本题考点: 常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;二氧化碳的实验室制法;书写化学方程式、文字表达式、电离方程式.
考点点评: 据反应物状态和反应条件选择发生装置,据气体的密度和性质选择收集装置,据反应原理书写方程式,并能据装置特点分析相关问题.1年前查看全部
- 以铁为基本原料两步制取氢氧化铁方程式
 俺是潢川人1年前2
俺是潢川人1年前2 -
 3rdsfiu 共回答了16个问题
3rdsfiu 共回答了16个问题 |采纳率100%2Fe+3Cl2=点燃==2FeCl3
FeCl3+3NaOH===Fe(OH)3+3NaCl1年前查看全部
- 、从实验室用氯酸钾于二氧化锰制取氧气后的残渣中(假定反应充分)回收氯化钾和二氧化锰.
 zjx21cn1年前4
zjx21cn1年前4 -
 小鱼蛮儿 共回答了16个问题
小鱼蛮儿 共回答了16个问题 |采纳率93.8%加水后,用过滤纸过滤氯化钾和二氧化锰,把过滤纸上的水分蒸发掉,就可以得到干燥的氯化钾和二氧化锰.1年前查看全部
- (2014•普陀区一模)工业上常利用反应 3Cl2+6KOH(热)→KClO3+5KCl+3H2O制取KClO
(2014•普陀区一模)工业上常利用反应 3Cl2+6KOH(热)→KClO3+5KCl+3H2O制取KClO3(混有KClO).实验室模拟上述制备:在含溶质14mol的KOH(aq,热)中通入一定量Cl2,充分反应后,测得溶液中n(Cl-)=11mol;将此溶液低温蒸干,得到的固体中KClO3的物质的量可能为( )
A.2.20
B.2.33
C.2.00
D.0.50 叮叮ling1年前1
叮叮ling1年前1 -
 x521779 共回答了18个问题
x521779 共回答了18个问题 |采纳率88.9%解题思路:在氧化还原反应中转移电子数相等,且各元素的原子个数相等,假设反应后溶液中的溶质是氢氧化钾和氯酸钾结合得失电子守恒计算氯酸钾的物质的量,假设反应后溶液中的溶质是氯酸钾和次氯酸钾,根据钾离子守恒和得失电子守恒计算氯酸钾的物质的量.假设反应后溶液中的溶质是氢氧化钾和氯酸钾,根据转移电子守恒得氯酸钾的物质的量=
11mol×(1−0)
5−0=2.2mol;
假设反应后溶液中的溶质是次氯酸钾和氯酸钾,
设氯酸钾的物质的量为x,次氯酸钾的物质的量为y,
根据转移电子守恒和钾离子守恒得方程式组
5x+y×1=11×1
x+y+11=14,
所以得
x=2
y=1,
实际上溶液中含有氯酸钾和次氯酸钾,所以得到的氯酸钾的物质的量可能为2.00mol,
故选C.点评:
本题考点: 化学方程式的有关计算.
考点点评: 本题考查了物质的量的有关计算,根据溶液中的溶质及转移电子守恒和钾原子守恒来分析解答即可,难度中等.1年前查看全部
- 用氯酸钾制取氧气,当看到_____向倒立在水槽中的集气瓶_____时,说明集气瓶充满氧气.这种收集气体的方法叫____法
用氯酸钾制取氧气,当看到_____向倒立在水槽中的集气瓶_____时,说明集气瓶充满氧气.这种收集气体的方法叫____法.其条件是这种气体必须_____.
点燃氢气前,必须_____.
某同学把一只点燃的蜡烛伸进盛有氧气的集气瓶里,燃烧停止后,冷却,可观察到瓶壁上_____,由此说明蜡烛中一定含有_____元素.
还有一题.
用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收满,这是利用了氧气的___、_____性质. 御风荷1年前1
御风荷1年前1 -
 bagizo 共回答了16个问题
bagizo 共回答了16个问题 |采纳率100%用氯酸钾制取氧气,当看到__大气泡___向倒立在水槽中的集气瓶_冒出____时,说明集气瓶充满氧气.这种收集气体的方法叫___排水_法.其条件是这种气体必须___不溶于水的__.
点燃氢气前,必须____验纯_.
某同学把一只点燃的蜡烛伸进盛有氧气的集气瓶里,燃烧停止后,冷却,可观察到瓶壁上__有水珠生成___,由此说明蜡烛中一定含有___H__元素.
用向上排空气法收集氧气,并用带火星的木条放在集气瓶口检验氧气是否收满,这是利用了氧气的__密度比空气大_、__有助燃性___性质.
我补充了1年前查看全部
- 某中学化学研究性学习小组利用以下装置制取并探究氨气的性质
某中学化学研究性学习小组利用以下装置制取并探究氨气的性质
[A中发生反应的化学方程式:2NH 4 Cl+Ca(OH) 2 2NH 3 ↑+2H 2 O+CaCl 2 ] 。
2NH 3 ↑+2H 2 O+CaCl 2 ] 。 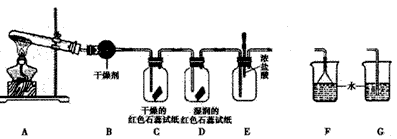
【实验探究】
(1)A中的反应___(填“是”或“不是”)氧化还原反应。
(2)A装置还可用于制取____气体(只填一种)。
(3)若有10.7 g NH 4 Cl固体,最多可制取NH 3 (标准状况)的体积是____L(NH 4 Cl 的摩尔质量为53.5
g·mol -1 )。
(4)实验室收集氨气的方法是___。
(5)C、D装置中颜色会发生变化的是___(填“C”或“D”)。
(6)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___。
(7)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是____(填“F”或“G”)。
【知识拓展】
(8)生石灰与水反应生成Ca(OH) 2 并放出热量[化学方程式为CaO+H 2 O==Ca(OH) 2 ]。实验室利用此原理,往生石灰中滴加浓氨水,可以快速制取氨气。你认为生石灰可用下列 ___物质代替(填序号)。
A.碱石灰(NaOH与CaO的固体混合物)
B.NaOH固体
C.硫酸溶液
D.石灰石(CaCO 3 )
【知识应用】
(9) 2010年11月9日晚,我省宁德市一冷冻厂发生氨气泄漏事件,500多居民深夜大转移。假如你在现场,你会采用什么自救方法? 二三加人1年前1
二三加人1年前1 -
 机构的士的 共回答了13个问题
机构的士的 共回答了13个问题 |采纳率92.3%(1)不是
(2) O 2 (或氧气,其他合理答案即可)
(3)4. 48
(4)向下排空气法
(5)D
(6)有白烟生成
(7)F
(8)A B
(9)
①用湿毛巾捂住口鼻,并迅速撤离。
②低头弯腰,往低处跑,迅速撤离。
③逆风奔跑,迅速撤离。
④戴上防毒面具,迅速撤离。1年前查看全部
- 求高中化学的制取乙醇和乙醛的方法和方程式
 海里的蚂蚁1年前1
海里的蚂蚁1年前1 -
 sclzl 共回答了23个问题
sclzl 共回答了23个问题 |采纳率95.7%醇一般是由卤代烃水解来的,CH3CH2Br+NaOH====(条件水,加热)CH3CH2OH+NaBr
乙醛由乙烯氧化 2CH3CH2OH+O2====(Cu做催化剂,加热)2CH3CHO+2H2O1年前查看全部
- 室温下,用铁片与1mol•L-1稀硫酸反应制取氢气时,改用下列措施不能使氢气生成速率加快的是( )
室温下,用铁片与1mol•L-1稀硫酸反应制取氢气时,改用下列措施不能使氢气生成速率加快的是( )
A.改用热的稀硫酸
B.改用98%的浓硫酸
C.改用铁粉
D.改用2 mol•L-1硫酸 yoat1年前1
yoat1年前1 -
 荔枝后援1号 共回答了21个问题
荔枝后援1号 共回答了21个问题 |采纳率90.5%解题思路:增大反应速率可增大浓度、升高温度或增大固体的表面积,注意不能用浓硫酸,也可形成原电池反应,以此解答.A.改用热的稀硫酸,温度升高,活化分子的百分数增大,反应速率增大,故A不选;
B.改用98%的浓硫酸,铁在室温下与浓硫酸发生钝化反应,不能加快生成氢气的反应速率,故B选;
C.改用铁粉,固体表面积增大,反应速率增大,故C不选;
D.改用2 mol•L-1硫酸,浓度增大,且不影响硫酸的性质,反应速率增大,故D不选.
故选B.点评:
本题考点: 化学反应速率的影响因素.
考点点评: 本题考查化学反应速率的影响因素,为高考高频考点,侧重于学生的分析能力的考查,注意浓硫酸与铁发生钝化反应的性质,为易错点.1年前查看全部
- 氮气是制备含氮化合物的一种重要物质。工业上可在碱性溶液中,通过电解的方法实现由N 2 制取NH 3 ,反应的化学方程式为
氮气是制备含氮化合物的一种重要物质。工业上可在碱性溶液中,通过电解的方法实现由N 2 制取NH 3 ,反应的化学方程式为:2N 2 +6H 2 O
 4NH 3 +3O 2 。计算生产34t NH 3 所需N 2 的质量。
4NH 3 +3O 2 。计算生产34t NH 3 所需N 2 的质量。 yxl9061年前1
yxl9061年前1 -
 红鱼游来了 共回答了17个问题
红鱼游来了 共回答了17个问题 |采纳率94.1%28t
1年前查看全部
- 铜和氧气 稀硫酸制取硫酸铜的化学方程式拜托了各位
铜和氧气 稀硫酸制取硫酸铜的化学方程式拜托了各位
还有离子方程式 谢桥女1年前1
谢桥女1年前1 -
 就是来黑你的 共回答了17个问题
就是来黑你的 共回答了17个问题 |采纳率94.1%楼上错了.不能合起来写 应该是2Cu+O2=2CuO(条件是△) CuO+H2SO4=CuSO4+H2O1年前查看全部
- 老师说可以用电解醋酸钠来制取甲烷,我想问怎么制取,写出电极反应式?
 njtantan1年前1
njtantan1年前1 -
 2007nowhereman 共回答了24个问题
2007nowhereman 共回答了24个问题 |采纳率83.3%以前的课本有醋酸钠与氢氢化钠(固体)在加热下生成CH4,机理是脱羧反应.电解好象看到过.但具体怎么反应想不起来.C2H6好象也可以电解出来 .1年前查看全部
- 元素周期表的13原子怎么读?二氧化猛制取氧气的化学方程式
 fei天堆堆猪1年前2
fei天堆堆猪1年前2 -
 娃哈哈ql685 共回答了15个问题
娃哈哈ql685 共回答了15个问题 |采纳率86.7%是铝吗? 读“吕”
二氧化锰可以和氯酸钾加热制氧气
2KCLO3(二氧化锰催化加热)=2KCL+3O2
望采纳~~1年前查看全部
- 制取二氧化碳是能否用生石灰做干燥剂
 ckinlove19851年前1
ckinlove19851年前1 -
 彼得文 共回答了20个问题
彼得文 共回答了20个问题 |采纳率85%不能,碱性氧化物和酸性氧化物会反应1年前查看全部
- 过氧化氢制取氧气 有几种发生装置
 小创ABC1年前0
小创ABC1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 如果要制取508g漂白粉,一共需含杂质20%的石灰石多少克
 hypertan1年前1
hypertan1年前1 -
 google999 共回答了15个问题
google999 共回答了15个问题 |采纳率100%漂白粉是Ca(ClO)2 石灰石是CaCO3
CaCO3=CaO+CO2
CaO+H2O=Ca(OH)2
2Ca(OH)2+2Cl2=CaCl2+Ca(ClO)2+2H2O
二份CaCO3制取二份CaO制取二份Ca(OH)2制取一份Ca(ClO)2
二份CaCO3制取一份Ca(ClO)2
CaCO3式量为100 Ca(ClO)2式量为143
100*2/(80%m)=143/508
m=888.11克1年前查看全部
- 用高锰酸钾制取氧气的化学方式
 viyes1年前0
viyes1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 生石灰放入水中的化学方程式( ) 实验室制取氢气的方法(
生石灰放入水中的化学方程式( ) 实验室制取氢气的方法(
生石灰放入水中的化学方程式( ) 实验室制取氢气的方法( ) spirit_ll1年前1
spirit_ll1年前1 -
 真的喝高了 共回答了19个问题
真的喝高了 共回答了19个问题 |采纳率84.2%CaO + H2O = Ca(OH)2
2HCl +Zn = H2(向上箭头)+ZnCl21年前查看全部
- 用淀粉为原料制取B(B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B).
用淀粉为原料制取B(B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B).
若有含淀粉40%的植物果实1kg,经反应制得184kg的B,则淀粉的转化率为____.(提示:转化率=已反应的量/原有的量*100%) chenrui211年前2
chenrui211年前2 -
 AliciaForget 共回答了17个问题
AliciaForget 共回答了17个问题 |采纳率94.1%B是乙醇
[C6H10O5]n+nH2O=nC6H12O6 含淀粉40%的植物果实1kg,生成葡萄糖4000/9kg
C6H12O6=2C2H5OH+2CO2 葡萄糖4000/9kg理论生成乙醇227.16kg,实际生成184kg,则淀粉的转化率为81%1年前查看全部
- 制取氢氧化铁时为什么必须使用饱和氯化铁溶液而不能用稀氯化铁溶液?
 guoliang88581年前3
guoliang88581年前3 -
 深水绯蓝 共回答了17个问题
深水绯蓝 共回答了17个问题 |采纳率88.2%制氢氧化铁胶体利用的是氯化铁水解反应.
氯化铁水解反应:
FeCl3+3H2O=Fe(OH)3+3HCl,这是一个可逆反应
选用饱和溶液的目的是增加铁离子的浓度,有利于平衡向右移动
这样更有利于氢氧化铁胶体的制备1年前查看全部
- 实验室制取二氧化碳不能使用稀硫酸的原因是
 小胖雪爱大头飞1年前1
小胖雪爱大头飞1年前1 -
 rilson 共回答了19个问题
rilson 共回答了19个问题 |采纳率78.9%硫酸钙是微溶于水的,多了之后会阻碍反应进行1年前查看全部
- 加热氯酸钾制取氧气安全吗?
 魔力BEIBEI1年前3
魔力BEIBEI1年前3 -
 shiyang211 共回答了17个问题
shiyang211 共回答了17个问题 |采纳率82.4%安全是肯定安全啦,不然实验室还敢用吗?
缺点是:要加热、加催化剂等,步骤太多太复杂,生成的氧气是热的,冷却后气压减小,可能会使空气进入,从而影响精确的实验计算!1年前查看全部
- 以锌.稀硫酸.氧化铜制取铜的方案最简单的是
 捻花郎1年前1
捻花郎1年前1 -
 kemior 共回答了16个问题
kemior 共回答了16个问题 |采纳率87.5%CuO+H2SO4=CuSO4+H2O
Zn+CuSO4=ZnSO4+Cu1年前查看全部
- 实验室怎样制取CO方程式
 范冰冰的苹果1年前2
范冰冰的苹果1年前2 -
 wgy528 共回答了12个问题
wgy528 共回答了12个问题 |采纳率83.3%实验室一般使用浓硫酸在加热条件下催化草酸分解并用氢氧化钠除掉二氧化碳制得一氧化碳,具体反应如下:
1.COOH・COOH===Δ===CO2↑+CO↑+H2O(H2SO4催化)
2.2NaOH+CO2======Na2CO3+H2O1年前查看全部
- 高温制取水煤气方法为C+H2O=CO+CO2,ΔH
 enjoyalone1年前1
enjoyalone1年前1 -
 adidas777 共回答了18个问题
adidas777 共回答了18个问题 |采纳率100%这个反应方程式应该是C(s)+H2O(g)===CO(g)+H(g)ΔH1年前查看全部
- 为什么大理石和稀盐酸制取二氧化碳,碳酸氢钠受热分解产生的二氧化碳不会对自然环境造成污染
 yuanyongpeng1年前1
yuanyongpeng1年前1 -
 ohnosos 共回答了20个问题
ohnosos 共回答了20个问题 |采纳率70%毕竟是产生少量的1年前查看全部
- 制取氢氧化钠的三个离子方程式
 gloryren1年前0
gloryren1年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 浓硫酸与碳酸钠制取co2体现浓硫酸的什么性质
 玉堂金马何须道1年前2
玉堂金马何须道1年前2 -
 hzw6932 共回答了19个问题
hzw6932 共回答了19个问题 |采纳率84.2%体现了硫酸的酸性
H2SO4+NA2CO3=NA2SO4+H2O+CO21年前查看全部
- 2.某兴趣小组用氯酸钾和二氧化锰的化合物加热制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适
2.某兴趣小组用氯酸钾和二氧化锰的化合物加热制取氧气,试管中固体的质量随时间变化的数据见下表.制取结束后,将剩余固体用适量水充分溶解后,过滤,回收二氧化锰固体,并得到氯化钾溶液100g.

(1)共制得氧气 g.
(2)计算生成氯化钾的质量. 在镜中飞翔1年前1
在镜中飞翔1年前1 -
 晓曦cc 共回答了13个问题
晓曦cc 共回答了13个问题 |采纳率100%1) 28.0-18.4=9.6g
2KClO3 = 2KCl + 3O2
149 96
x 9.6
x=14.9g1年前查看全部
- 制取蒸馏水为何要弃去开始馏出的部分液体?
 VV淡定纯情1年前3
VV淡定纯情1年前3 -
 披qq的小胖 共回答了18个问题
披qq的小胖 共回答了18个问题 |采纳率88.9%开始馏出的部分液体既含有沸点低于水的沸点的物质,又含有蒸馏器具中残留的少量杂质,所以应当弃去.1年前查看全部
- 实验室利用大理石与100克稀盐酸刚好反应制取二氧化碳,如果制取二氧化碳4.4克,求:(见下面的补充)
实验室利用大理石与100克稀盐酸刚好反应制取二氧化碳,如果制取二氧化碳4.4克,求:(见下面的补充)
(1)需用含碳酸钙质量分数为96%的大理石多少克?(2)稀盐酸的质量分数是多少? gaozai11年前1
gaozai11年前1 -
 yamaziyi 共回答了24个问题
yamaziyi 共回答了24个问题 |采纳率79.2%CaCO3+2HCl=CaCl2+H2O+CO2(气体箭号)
100 73 44
0.96x y 4.4g
100 44
一一一= 一一
0.96x 4.4g
x=10.4g
73 44
一一一=一一一
y 4.4g
y=7.3g
(HCl)%=7.3g/100g=7.3%1年前查看全部
- 复分解反应存在这样一个规律:较强酸可制取较弱酸.盐类的水解也是复分解反应,弱酸强碱盐对应的弱酸越弱,其盐越容易发生水解.
复分解反应存在这样一个规律:较强酸可制取较弱酸.盐类的水解也是复分解反应,弱酸强碱盐对应的弱酸越弱,其盐越容易发生水解.
A.CO2+H2O+2NaClO===Na2CO3+2HClO
B.CO2+H2O+NaClO===NaHCO3+HClO
弱酸的酸性由强到弱的顺序为CH3COOH、H2CO3、HClO、HCN、C6H5OH、HCO(注意:Na2CO3对应的弱酸为HCO,NaHCO3对应的弱酸为H2CO3A反应若生成HClO,则可与Na2CO3起反应生成NaClO和NaHCO3,A不能发生,B能发生
为什么A不能反映呢?我根本看不懂答案,明明强酸制弱酸,HClO不是可以制HCO(即Na2CO3)吗? leo_hu1年前3
leo_hu1年前3 -
 shastef 共回答了21个问题
shastef 共回答了21个问题 |采纳率90.5%CO2 + H2O就是H2CO3.H2CO3是二元酸,其一级电离:H2CO3 = H+ + HCO3-
与NaClO反应时,其实只有其一级电离出来的H+与ClO-发生反应,所以是得到NaHCO3与HClO
这里体现的强制弱,是“H2CO3”制“HClO".1年前查看全部
- 用氢氧化铜制取氧化铜 的化学方程式
 猫猫月盈1年前3
猫猫月盈1年前3 -
 ma1jie 共回答了10个问题
ma1jie 共回答了10个问题 |采纳率90%2Cu(OH)2=(等号上面写"加热")2Cu+2H2O1年前查看全部
- 过氧化氢制取氧气时是吸热还是放热!
 几百哈达1年前3
几百哈达1年前3 -
 xiahaibin 共回答了18个问题
xiahaibin 共回答了18个问题 |采纳率100%楼上那两个人在那扯淡,
过氧化氢的分解是放热的反应,在做实验室,可以看到有大量水变成水蒸气凝结,
证明是放热的,
换一种思路,过氧化氢的氧是-1价,不是最低价,成键键能比水中O-H键能高,故为放热反应1年前查看全部
- 制取二氧化碳时 怎么检查气体发生装置的气密性
 wx_8002061年前3
wx_8002061年前3 -
 lianshangxinyuan 共回答了22个问题
lianshangxinyuan 共回答了22个问题 |采纳率86.4%实验室用:CaCO3和HCL制CO2试验装置.用长颈漏斗插入液面内的气体发生装置,紧闭导气管出口,从漏斗中加水.如果液面稳定后水面下降,则表明漏气;若水面不下降,则表明不漏气.1年前查看全部
- 制取漂白粉 原料氢氧化钙是否拆开?漂白粉失效的反应中次氯酸钙是否拆开
 蚩蚩211年前4
蚩蚩211年前4 -
 暖暖的青 共回答了11个问题
暖暖的青 共回答了11个问题 |采纳率90.9%不拆,原料是石灰乳不是溶液不拆
次氯酸钙也不拆1年前查看全部
- 下列实验目的可以达到的是:1、浓硫酸与溴化钠共热制取溴化氢2、饱和碳酸钠溶液出去二氧化碳的氯化氢含大量Al3+的溶液中:
下列实验目的可以达到的是:
1、浓硫酸与溴化钠共热制取溴化氢
2、饱和碳酸钠溶液出去二氧化碳的氯化氢
含大量Al3+的溶液中:硝酸根、钠离子、氯离子、次酸根离子为什么不能大量共存?
下列各组有机物只用一种试剂无法鉴别的是:
A、乙醇、甲苯、硝基苯
B、苯、苯酚、己烯
C、苯、甲苯、环己烷
D、甲酸、乙醛、乙酸
这几个问题,希望能一个个细的解答,很细很细~ ╃浪漫已nn╃1年前1
╃浪漫已nn╃1年前1 -
 泰兰德 共回答了21个问题
泰兰德 共回答了21个问题 |采纳率90.5%1、浓硫酸与溴化钠共热制取溴化氢
溴会被氧化成单质.
如果是稀硫酸,这个反应可以看作是一个可逆反应,根据 勒夏特列原理,生成物中溴化氢因为遇热而溢出,反应向正向移动.
2、饱和碳酸钠溶液除去二氧化碳中氯化氢
二氧化碳能与碳酸钠反应生成碳酸氢钠.
4.A用水,将水慢慢倒入烧杯中,乙醇互溶,甲苯会在上层,硝基苯在下层,(有界面,可以根据体积来判断)
B苯和溴水发生萃取,分层,上层为红棕色苯层,苯酚和浓溴水反应生成白色不溶于水的三溴苯酚沉淀,己烯和溴水反应,分层后退色(加成)
C Cu(OH)2
甲酸,Cu(OH)2溶解,得到蓝色甲酸铜溶液,加热煮沸后,还能产生红色沉淀Cu2O,即甲酸中存在醛基,可以被Cu(OH)2氧化.
乙酸,Cu(OH)2溶解,得到蓝色的乙酸铜溶液,但是加热煮沸,没有其它变化
乙醛,Cu(OH)2不能溶解,但是加热煮沸后,出现红色沉淀Cu2O1年前查看全部
- 氨是重要的化工原料,实验室制取氨气的化学方程式为?这套卷子是?
 zzq5841年前1
zzq5841年前1 -
 fba365 共回答了15个问题
fba365 共回答了15个问题 |采纳率73.3%氯气 制取原理——强氧化剂氧化含氧化合物 制取方程式——MnO2 4HCl(浓)MnCl2 Cl2↑ 2H2O 装置——分液漏斗,圆底烧瓶,加热 检验——能使湿润的蓝色石蕊试纸先变红后褪色; 除杂质——先通入饱和食盐水(除HCl),再通入浓H2SO4(除水蒸气) 收集——排饱和食盐水法或向上排气法 尾气回收——Cl2 2NaOH=== NaCl NaClO H2O1年前查看全部
- 实验室制取二氧化碳一般有五步实验操作:请排列顺序
实验室制取二氧化碳一般有五步实验操作:请排列顺序
检查装置的气密性
按要求组装好仪器
向长颈漏斗中注入吸盐酸
向锥形瓶中加入大理石块
检查气体是否集满
收集二氧化碳 歪木瓜1年前1
歪木瓜1年前1 -
 穿越麦田 共回答了17个问题
穿越麦田 共回答了17个问题 |采纳率88.2%按要求组装好仪器
检查装置的气密性
向锥形瓶中加入大理石块
向长颈漏斗中注入吸盐酸
收集二氧化碳
检查气体是否集满1年前查看全部
- 制取乙酸乙酯时生成物H2O中的氧来自于—------(填结构式)
 zjxsluo1年前3
zjxsluo1年前3 -
 bearbeargz 共回答了13个问题
bearbeargz 共回答了13个问题 |采纳率100%CH3COOH + CH3CH2OH < =浓H2SO4 加热=> CH3COOC2H5 + H2O
有机酸:酸脱羟基醇脱氢.所以制取乙酸乙酯时生成物H2O中的氧来自于-乙酸-.
无机酸:醇脱羟基酸脱氢.1年前查看全部
- 加热MnO2和KCLO3的混合物制取氧气图像 为什么刚开始是直线?
加热MnO2和KCLO3的混合物制取氧气图像 为什么刚开始是直线?
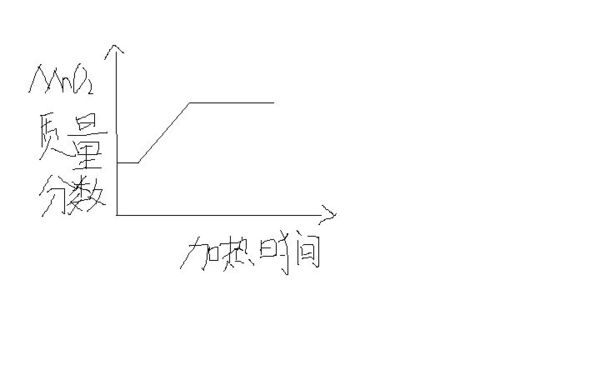
为什么刚开始是直线? aifeidexuan1211年前1
aifeidexuan1211年前1 -
 飞狼best 共回答了18个问题
飞狼best 共回答了18个问题 |采纳率94.4%刚开始时,加热时间短,温度没有达到反应所需的最低温度1年前查看全部
- 怎么样用排水集气法制取氧气?这个“排水”我不太懂,就是集气瓶装满水盖上玻璃片后倒立在水中,然后把导管口从集气瓶的贴着水底
怎么样用排水集气法制取氧气?
这个“排水”我不太懂,就是集气瓶装满水盖上玻璃片后倒立在水中,然后把导管口从集气瓶的贴着水底的瓶口插进去,就是这一步骤不太懂,是把集气瓶掀开一个小口让导管插进去吗,但是水槽里的其他水也会相继进到集气瓶里,这怎么排出去呢,我知道酒精灯加热高猛酸钾的生成物是锰酸钾、二氧化锰、氧气 kk乐乐1年前1
kk乐乐1年前1 -
 路的那边 共回答了20个问题
路的那边 共回答了20个问题 |采纳率80%排水法收集气体,首先将集气瓶充满水,只要把水中的集气瓶拿高一点,就可以将导气管伸入集气瓶内收集气体了.【不懂再问】1年前查看全部
- 工业制取HCl的程序框图
 wolfsky19831年前0
wolfsky19831年前0 -
 共回答了个问题
共回答了个问题 |采纳率
- 写出制取硫酸亚铁的4种方法(原理不能重复)
 cwka1年前1
cwka1年前1 -
 袁小痴 共回答了23个问题
袁小痴 共回答了23个问题 |采纳率91.3%1.直接反应:
Fe+H2SO4=FeSO4+H2↑
2.铜和氧气反应再硫酸反应,铁置换
2Cu+O2=加热=2CuO
CuO+H2SO4=CuSO4+H2O
Fe+CuSO4=FeSO4+Cu
3.铁和氧气反应,再和硫酸反应,用铜还原
3Fe+2O2=点燃=Fe3O4
Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O
Cu+Fe2(SO4)3=2FeSO4+CuSO4
4.铜和硫酸反应,铁置换
Cu+2H2SO4(浓)=加热=CuSO4+SO2↑+2H2O
Fe+CuSO4=FeSO4+Cu1年前查看全部
- 下图是用绿色粉末A制取红色金属H的两种流程,其中白色固体Fe(Cao)是一种常见的建筑材料,固体乙是目前用途最广,产量最
下图是用绿色粉末A制取红色金属H的两种流程,其中白色固体Fe(Cao)是一种常见的建筑材料,固体乙是目前用途最广,产量最高的金属.
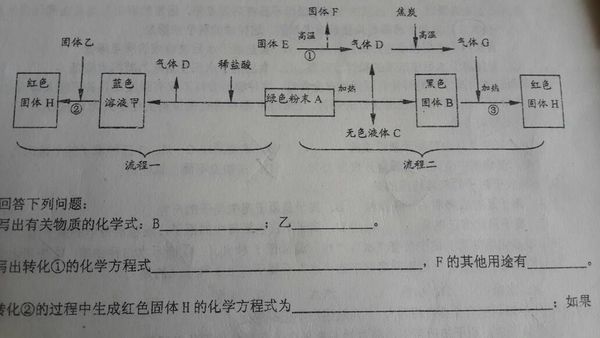
 想长翅膀的猪1年前2
想长翅膀的猪1年前2 -
 tttjuan 共回答了19个问题
tttjuan 共回答了19个问题 |采纳率100%1、固体乙是目前用途最广,产量最高的金属.可判断乙=Fe.
2、由绿色粉末A及红色固体H,可判断是碱式碳酸铜:A=Cu2(OH)2CO3
3、Cu2(OH)2CO3+盐酸可知:分解出二氧化碳气体,故知道D=CO2,蓝色液体是CuCl2
4、CuCl2+乙(Fe)置换出来纯铜Cu,故知道H=Cu.
5、白色固体(Cao)是一种常见的建筑材料可知,固体E=CaCO3,碳酸钙.
6、碳酸钙加热生成氧化钙和二氧化碳,故知道固体F=CaO、气体D=CO2.
7、CO2+焦炭=CO一氧化碳,煤气反应,故知道气体G=CO.
8、绿色粉末A碱式碳酸铜加热,生成CuO+H2O+气体D(CO2):Cu2(OH)2CO3CO+CuO+H2O+CO2,知道黑色固体B=CuO.1年前查看全部
- 实验室制取硝基苯,应选用浓硫酸,浓硝酸在55℃到60℃条件下生成.回答1.2小问
 爱娇-无尘1年前1
爱娇-无尘1年前1 -
 懂得了11 共回答了24个问题
懂得了11 共回答了24个问题 |采纳率95.8%选b 优点温度易控制1年前查看全部
- 实验探究是学习化学的重要方法.某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,
实验探究是学习化学的重要方法.某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,
某化学兴趣小组利用饱和的澄清石灰水和碳酸钠溶液制取NaOH,反应后将浑浊的液体过滤,得到无色澄清的滤液,为了确定滤液的成分,进行下列的实验探究.
(1)[提出问题] 探究滤液中(除氢氧化钠和水外)是否还有其他物质.
(2)[猜想]①王晓认为滤液中可能含有氢氧化钙;
②李娜认为滤液中可能含有________(填物质的名称,下同).
(3)[设计方案并实验]为了验证王晓的猜想,应该选用的试剂是______.为了验证李娜的猜想,应选用的试剂是______,可观察到的现象是________________,该反应的化学方程式为______________________ zdz0121年前1
zdz0121年前1 -
 406812597 共回答了10个问题
406812597 共回答了10个问题 |采纳率100%①王晓认为滤液中可能含有氢氧化钙;
②李娜认为滤液中可能含有__碳酸钠__(填物质的名称,下同).问题补充:
(3)[设计方案并实验]为了验证王晓的猜想,应该选用的试剂是__碳酸钠溶液_.为了验证李娜的猜想,应选用的试剂是_氯化钙溶液_,可观察到的现象是__有白色沉淀生成____,该反应的化学方程式为___CaCl2+Na2CO3==CaCO3↓+2NaCl___1年前查看全部
大家在问
- 1一道专四真题,希望大虾解答!( ) I'll marry him all the same.A.was he rich
- 2the vicar went up into the clock tower to see what was going
- 3任选1.2.3.4.5.6.7.8.9中的一个,乘以9再乘以123456789,有何规律
- 4帮忙写一篇高三的英语作文,快,按下面内容,写100词的文章:2009.12.7 哥本哈根会议在丹麦首都召开了;会议上各国
- 5动词+宾语+不定式结构中既可以动词用被动语态,也可以在不定式中用被动语态.谁能举个例子讲解一下?
- 6关于高一化学问题神马的.要解析~~
- 7用3种科学方法鉴定从海水中出来的水是淡水
- 8图书馆有故事书m本,比科技书的2倍多n本,科技书有多少本.正确的算式是( )
- 9Are the books in your backpack?
- 10初二物理 要解析.并解释当弹簧超过弹性限度时A选项如何成立?
- 11如图7,连接实物图,并在电路图上标出电路方向
- 12一次比赛,一二三等奖若干名,获一二等奖占获奖人数的2/5,二三等奖占获奖人数的9/10,二等奖占获奖人几分
- 13请问这是定语从句还是同位语从句?谢谢
- 14三个数成等差数列,他们的和是9,积是15,求这三个数
- 15关于篮球规则的英语怎么说(全)大神们帮帮忙

